Вступить в сообщество
Членство в сообществе бесплатное.
Получайте актуальные информирующие рассылки с новостями, проводимыми вебинарами и исследованиями в области кардиологии и смежных областей.
Формулировка диагноза
При формулировании диагноза необходимо максимально полно отразить наличие ФР, ПОМ, диагностированные сердечно-сосудистые или почечные заболевания, сердечно-сосудистый риск. Степень повышения АД обязательно указывается у пациентов с впервые диагностированой АГ, если пациент принимает антигипертензивную терапию, то в диагнозе указывается наличие контроля АД (контролируемая/неконтролируемая АГ). Необходимо также указать стадии заболевания.
Необходимо указать целевой уровень АД для данного пациента.
При отсутствии диагностированных сердечно-сосудистых или почечных заболеваний термин «гипертоническая болезнь» в силу своей высокой прогностической значимости закономерно занимает первую позицию в структуре диагноза.
При наличии диагностированных сердечно-сосудистых или почечных заболеваний, сопровождающихся высокой степенью нарушения функции или протекающих в острой форме, например, острый коронарный синдром, «гипертоническая болезнь» в структуре диагноза сердечно-сосудистой патологии может занимать не первую позицию.
При вторичных формах АГ, «артериальная гипертензия», занимает не первое место в структуре диагноза.
Примеры диагностических заключений.
- ГБ I стадии. Степень АГ 1. Гиперлипидемия. Риск 2 (средний). Целевое АД <130/<80 мм рт. ст.
- ГБ II стадии. Неконтролируемая АГ. Нарушенная гликемия натощак. Гиперлипидемия. ГЛЖ. Риск 3 (высокий) Целевое АД <130/<80 мм рт. ст.
- ГБ II стадии. Неконтролируемая АГ. Гиперлипидемия. Ожирение II степени. Нарушение толерантности к глюкозе. ГЛЖ. Альбуминурия высокой степени. Риск 4 (очень высокий). Целевое АД 130-139/<80 мм рт. ст.
- ИБС. Стенокардия напряжения III ФК. Постинфарктный кардиосклероз (2010г). ГБ III стадии. Неконтролируемая АГ. Риск 4 (очень высокий). Целевое АД <130/<80 мм рт. ст.
- ГБ III стадии. Контролируемая АГ. Ожирение I степени. Сахарный диабет 2-го типа, целевой уровень гликированного гемоглобина ≤7,5%. ХБП С4 стадии, альбуминурия А2. Риск 4 (очень высокий). Целевое АД 130–139/< мм рт. ст.
Обращаем ваше внимание! Эта статья не является призывом к самолечению. Она написана и опубликована для повышения уровня знаний читателя о своём здоровье и понимания схемы лечения, прописанной врачом. Если вы обнаружили у себя схожие симптомы, обязательно обратитесь за помощью к доктору. Помните: самолечение может вам навредить.
Артериальная гипертензия у взрослых
Версия: Клинические рекомендации РФ 2018-2020 (Россия)
Категории МКБ:
Вторичная гипертензия (I15), Гипертензивная [гипертоническая] болезнь с преимущественным поражением сердца и почек (I13), Гипертензивная [гипертоническая] болезнь с преимущественным поражением почек (I12), Гипертензивная болезнь сердца [гипертоническая болезнь сердца с преимущественным поражением сердца] (I11), Эссенциальная [первичная] гипертензия (I10)
Разделы медицины:
Кардиология
Общая информация
Краткое описание
Российское кардиологическое общество
Клинические рекомендации
Артериальная гипертензия у взрослых
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: I10/ I11/ I12/ I13/ I15
Возрастная группа: взрослые
Год утверждения: 2020
Определение заболевания или состояния (группы заболеваний, состояний)
Артериальная гипертензия (АГ) — синдром повышения систолического АД (далее — САД) ≥140 мм рт. ст. и/или диастолического АД (далее — ДАД) ≥90 мм рт. ст.
Гипертоническая болезнь (далее — ГБ) — хронически протекающее заболевание, основным проявлением которого является повышение АД, не связанное с выявлением явных причин, приводящих к развитию вторичных форм АГ (симптоматические АГ). Термин «гипертоническая болезнь», предложенный Г. Ф. Лангом в 1948 г., соответствует терминам «эссенциальная гипертензия» и «артериальная гипертензия», используемым за рубежом. ГБ преобладает среди всех форм АГ, ее распространенность превышает 90%.
Вторичная (симптоматическая) АГ — АГ, обусловленная известной причиной, которую можно устранить с помощью соответствующего вмешательства.
Гипертонический криз — cостояние, вызванное значительным повышением АД, ассоциирующееся с острым поражением органов-мишеней, нередко жизнеугрожающим, требующее немедленных квалифицированных действий, направленных на снижение АД, обычно с помощью внутривенной терапии
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
Болезни, характеризующиеся повышенным кровяным давлением (I10, I11, I12, I13, I15):
I10 — Эссенциальная [первичная] гипертензия:
Высокое кровяное давление;
Гипертензия (артериальная) (доброкачественная) (эссенциальная) (злокачественная) (первичная) (системная).
I11 — Гипертензивная болезнь сердца [гипертоническая болезнь сердца с преимущественным поражением сердца];
I11.0 — Гипертензивная [гипертоническая] болезнь с преимущественным поражением сердца с (застойной) сердечной недостаточностью:
Гипертензивная [гипертоническая] сердечная недостаточность.
I11.9 — Гипертензивная [гипертоническая] болезнь с преимущественным поражением сердца без (застойной) сердечной недостаточности:
Гипертензивная болезнь сердца без дополнительных уточнений (БДУ).
I12 — Гипертензивная [гипертоническая] болезнь с преимущественным поражением почек:
Артериосклероз почек
Артериосклеротический нефрит (хронический) (интерстициальный);
Гипертензивная нефропатия;
Нефросклероз.
I12.0 — Гипертензивная [гипертоническая] болезнь с преимущественным поражением почек с почечной недостаточностью:
Гипертоническая почечная недостаточность.
I12.9 — Гипертензивная [гипертоническая] болезнь с преимущественным поражением почек без почечной недостаточности:
Почечная форма гипертонической болезни БДУ.
I13 — Гипертензивная [гипертоническая] болезнь с преимущественным поражением сердца и почек.
I13.0 — Гипертензивная [гипертоническая] болезнь с преимущественным поражением сердца и почек с (застойной) сердечной недостаточностью.
I13.1 — Гипертензивная [гипертоническая] болезнь с преимущественным поражением почек с почечной недостаточностью.
I13.2 — Гипертензивная [гипертоническая] болезнь с преимущественным поражением сердца и почек с (застойной) сердечной недостаточностью и почечной недостаточностью.
I13.9 — Гипертензивная [гипертоническая] болезнь с преимущественным поражением сердца и почек неуточненная.
I15 — Вторичная гипертензия.
I15.0 — Реноваскулярная гипертензия.
I15.1 — Гипертензия вторичная по отношению к другим поражениям почек.
I15.2 — Гипертензия вторичная по отношению к эндокринным нарушениям.
I15.8 — Другая вторичная гипертензия.
I15.9 — Вторичная гипертензия неуточненная.
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация заболевания или состояния (группы заболеваний, состояний)
АГ классифицируют по степени, которая определяется уровнем АД у нелеченных пациентов; стадии, которая определяется наличием сахарного диабета (СД), поражения органов-мишеней (ПОМ) и ассоциированных клинических состояний (АКС); категории риска развития сердечно-сосудистых осложнений, которая учитывает уровень АД, сопутствующие факторы риска (ФР), наличие СД, ПОМ, АКС.
Классификация уровней АД у лиц старше 18 лет представлена в таблице П2, Приложение Г1. Категорию АД определяют по результатам его трехкратного измерения в положении пациента сидя. Используют средние значения САД и ДАД, определенных при двух последних измерениях. Изолированная систолическая гипертензия классифицируется на степени 1, 2 или 3 в зависимости от значения САД. Если значения САД и ДАД попадают в разные категории, то степень АГ оценивается по более высокой категории.
Выделение 3 стадий АГ (Таблица П1, Приложение Г3) основано на наличии поражения органов-мишеней (ПОМ), ассоциированных клинических состояний, сахарного диабета и хронической болезни почек. Стадия АГ не зависит от уровня АД.
Выделяются 3 стадии гипертонической болезни.
Стадия I — отсутствие ПОМ и АКС, возможное наличие факторов риска
Факторы СС риска у пациентов с АГ:
— Пол (мужчины > женщин);
— Возраст ≥55 лет у мужчин, ≥65 лет у женщин;
— Курение (в настоящем или прошлом; курение в прошлом следует рассматривать как фактор риска при отказе от курения в течение последнего года);
— Дислипидемия (принимается во внимание каждый из представленных показателей липидного обмена): ОХС >4,9 ммоль/л и/или ХС ЛПНП >3,0 ммоль/л и/или ХС ЛПВП у мужчин — <1,0 ммоль/л (40 мг/дл), у женщин — <1,2 ммоль/л (46 мг/дл) и/или триглицериды >1,7 ммоль/л;
— Мочевая кислота (≥360 мкмоль/л у женщин, ≥420 мкмоль/л у мужчин);
— Нарушение гликемии натощак: глюкоза плазмы натощак 5,6–6,9 ммоль/л;
— Нарушение толерантности к глюкозе;
— Избыточная масса тела (ИМТ 25-29,9 кг/м2) или ожирение (ИМТ ≥ 30 кг/м2);
— Семейный анамнез развития ССЗ в молодом возрасте (< 55 лет для мужчин и <65 лет для женщин);
— Развитие АГ в молодом возрасте у родителей или в семье;
— Ранняя менопауза;
— Малоподвижный образ жизни;
— Психологические и социально-экономические факторы;
— Частота сердечных сокращений в покое >80 ударов в минуту.
Стадия II подразумевает наличие бессимптомного поражения органов-мишеней, связанного с АГ и/или ХБП С3 (СКФ 30–59 мл/мин), и/или СД без поражения органов-мишеней и предполагает отсутствие АКС.
• Артериальная жесткость:
Пульсовое давление (ПД) (у пожилых пациентов) ≥60 мм рт. ст.
Каротидно-феморальная СПВ >10 м/с
• Электрокардиографические (ЭКГ) признаки ГЛЖ на (индекс Соколова–Лайона > 35 мм, или амплитуда зубца R в отведении aVL ≥11 мм, корнельское произведение >2440 мм x мс или корнельский вольтажный индекс >28 мм для мужчин и >20 мм для женщин);
• Эхокардиографические признаки ГЛЖ (индекс массы ЛЖ (масса ЛЖ, г/рост, м) формула ASE для пациентов с избыточной массой тела и ожирением: для мужчин >50 г/м2,7, для женщин >47 г/м2,7; индексация на площадь поверхности тела (масса ЛЖ/рост, м2) для пациентов с нормальной массой тела: >115 г/м2(мужчины) и > 95 г/м2 (женщины);
• Альбуминурия 30–300 мг/24 ч или отношения альбумин-креатинин 30–300 мг/г или 3,4-34 мг/ммоль (предпочтительно в утренней порции мочи);
• ХБП С3 стадии с СКФ >30–59 мл/мин/1,73 м2;
• Лодыжечно-плечевой индекс <0,9;
• Выраженная ретинопатия: наличие кровоизлияний, экссудатов или отека соска зрительного нерва.
Стадия III определяется наличием АКС, в том числе ХБП С4–С5 стадии, и/или СД с поражением органов-мишеней.
СД (рассматривается как дополнительное состояние, усугубляющее риск) [31]: глюкоза плазмы натощак ≥7,0 ммоль/л при двух последовательных измерениях и/или HbA1c ≥6,5%, и/или глюкоза плазмы после нагрузки или при случайном определении ≥11,1 ммоль/л.
Стадии АГ имеют уточняющий характер по поражениям органов-мишеней и сопутствующей патологии.
На основании уровня АД, наличия ФР, ПОМ, АКС, СД выделяют 4 категории риска СС осложнений: низкий (риск 1), умеренный (риск 2), высокий (риск 3) и очень высокий (риск 4) (Приложение Г2, таблица П12). Наиболее значимым является определение категории риска у пациентов с гипертонической болезнью I и II стадий.
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний, состояний)
Предрасполагающие факторы Этиология АГ остается не до конца выясненной, но выявлен ряд факторов, тесно и независимо связанных с повышением АД:
• возраст — увеличение возраста ассоциировано с повышением частоты АГ и уровня АД (прежде всего систолического) [10];
• избыточная масса тела и ожирение способствуют повышению АД;
• наследственная предрасположенность — повышение АД встречается приблизительно в 2 раза чаще среди лиц, у которых один или оба родителя имели АГ. Эпидемиологические исследования показали, что около 30% вариаций АД в различных популяциях обусловлены генетическими факторами [11].
• избыточное потребление натрия (>5 г/день) [12];
• злоупотребление алкоголем;
• гиподинамия.
Стойкое и длительное повышение АД обусловлено изменением соотношения трех гемодинамических показателей:
• повышением общего периферического сосудистого сопротивления (ОПСС);
• увеличением сердечного выброса (минутного объема);
• увеличением объема циркулирующей крови (ОЦК).
Наиболее важными патогенетическими звеньями формирования и прогрессирования эссенциальной АГ (ГБ) являются [13-16]:
• активация симпатоадреналовой системы (САС) (реализуется преимущественно через альфа- и бета-адренорецепторы);
• активация ренин-ангиотензин-альдостероновой системы (РААС); в т.ч. повышение продукции минералокортикоидов (альдостерона и др.), инициируемое, в частности, гиперактивацией почечной РААС;
• нарушение мембранного транспорта катионов (Nа+, Са2+, К+);
• увеличение реабсорбции натрия в почках;
• дисфункция эндотелия с преобладанием продукции вазоконстрикторных субстанций (тканевого ангиотензина-II, эндотелина) и снижением выработки депрессорных соединений (брадикинина, NО, простациклина и др.);
• структурные изменения сосудистой стенки артерий мышечного (резистивного) и эластического типа, в том числе вследствие низкоинтенсивного неинфекционного воспаления;
• нарушение микроциркуляции (снижение плотности капилляров);
• нарушение барорецепторного звена системы центральной регуляции уровня АД;
• повышение жесткости крупных сосудов.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний, состояний)
Распространенность АГ среди взрослого населения составляет 30–45% [17]. Распространенность АГ не зависит от уровня дохода и одинакова в странах с низким, средним и высоким уровнями дохода [17]. В российской популяции среди мужчин в возрасте 25–65 лет распространенность АГ несколько выше (в некоторых регионах она достигает 47%), тогда как среди женщин распространенность АГ — около 40% [18]. Распространенность АГ увеличивается с возрастом, достигая 60% и выше у лиц старше 60 лет [17]. Поскольку наблюдаемое увеличение продолжительности жизни сопровождается постарением населения и, соответственно, увеличением количества малоподвижных пациентов с избыточной массой тела, прогнозируется, что распространенность АГ будет расти во всем мире. Согласно прогнозу, к 2025 году число пациентов АГ увеличится на 15–20% и достигнет почти 1,5 миллиардов [19].
АГ является ведущим фактором риска развития сердечно-сосудистых (СС) (инфаркт миокарда, инсульт, ишемическая болезнь сердца (ИБС), хроническая сердечная недостаточность), цереброваскулярных (ишемический или геморрагический инсульт, транзиторная ишемическая атака) и почечных (хроническая болезнь почек (ХБП)) заболеваний [20–22].
Взаимосвязь артериального давления с риском развития сердечно-сосудистых, цереброваскулярных и почечных осложнений
Повышенное АД является основным фактором развития преждевременной смерти и причиной почти 10 миллионов смертей и более чем 200 миллионов случаев инвалидности в мире [20–22]. Уровень САД ≥140 мм рт. ст. ассоциируется с повышением риска смертности и инвалидности в 70% случаев, при этом наибольшее число смертей в течение года, связанных с уровнем САД, возникают вследствие ИБС, ишемических и геморрагических инсультов [21].Между уровнем АД и риском сердечно-сосудистых заболеваний (ССЗ) существует прямая связь. Эта связь начинается с относительно низких значений — 110–115 мм рт. ст. для САД и 70–75 мм рт. ст. для ДАД [22].
Повышенные уровни АД, измеренные в медицинском учреждении или вне его, имеют прямую и независимую связь с частотой развития большинства СС событий (геморрагического инсульта, ишемического инсульта, инфаркта миокарда, внезапной смерти, сердечной недостаточности и заболеваний периферических артерий), а также терминальной почечной недостаточности [23]. Все больше данных свидетельствуют о тесной связи АГ с увеличением частоты развития фибрилляции предсердий [24], а также когнитивной дисфункции и деменции. Повышение АД в среднем возрасте ассоциируется с развитием когнитивных нарушений и деменции в пожилом возрасте, а интенсивная терапия артериальной гипертензии с достижением целевых цифр АД уменьшает риски развития умеренных когнитивных нарушений и возможной деменции [25, 26].
Прямая связь между повышенным уровнем АД и риском СС событий продемонстрирована для всех возрастных [27] и этнических групп [28]. У пациентов старше 50 лет САД является более сильным предиктором событий, чем ДАД [27, 29]. Высокое ДАД ассоциируется с увеличением риска СС событий и чаще является повышенным у более молодых (<50 лет) пациентов. ДАД имеет тенденцию к понижению во второй половине жизни вследствие увеличения артериальной жесткости, тогда как САД, как фактор риска, приобретает в этот период еще большее значение [29]. У пациентов среднего возраста и пожилых повышение пульсового давления (ПД) (которое представляет собой разницу между САД и ДАД) оказывает дополнительное негативное влияние на прогноз [20, 30].
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний, состояний)
В большинстве случаев АД повышается бессимптомно, и АГ обнаруживают лишь в ходе объективного исследования пациента. В тех случаях, когда жалобы есть, они неспецифичны (головная боль, головокружение, сердцебиение и т.д.). При симптоматической гипертонии жалобы обусловлены основным заболеванием:
Синдром обструктивного апноэ во сне: храп, головная боль по утрам, сонливость в дневное время, нарушение памяти, внимания, неполноценный ночной сон;
Первичный гиперальдостеронизм: мышечная слабость, полиурия, полидипсия, запоры;
Феохромоцитома: пароксизмальная АГ, головная боль, профузная потливость, сердцебиение, лабильное повышение АД, ортостатическая гипотония;
Синдром Иценко–Кушинга: лунообразное лицо, плетора, жировой горбик, гирсутизм, центральное ожирение, атрофия кожи, багровые стрии, синяки, нарушения углеводного обмена;
Заболевания щитовидной железы: симптомы тиреотоксикоза или гипотиреоза;
Коарктация аорты: головная боль, холодные конечности, боль в ногах при физических нагрузках, носовые кровотечения.
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний), медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза:
Диагноз АГ на основании СМАД устанавливается в соответствии с пороговыми значениями, указанными в таблице П9, Приложение Г2 [32]. Мониторинг АД в домашних условиях рекомендуется при недоступности метода СМАД или из-за предпочтений пациента. При этом диагноз АГ устанавливается в соответствии с пороговыми значениями, указанными в таблице П9, Приложение Г2 [32].
В случае если диагноз важен для экспертизы трудоспособности или определения годности к военной службе, а также годности к профессиональной деятельности, необходима объективизация с помощью постановки СМАД.
Диагностика АГ включает следующие этапы:
• выяснение жалоб и сбор анамнеза;
• повторные измерения АД;
• объективное обследование;
• лабораторно-инструментальные методы исследования: рутинные на первом этапе и сложные — на втором этапе обследования (по показаниям);
• исключение вторичных (симптоматических) АГ при необходимости;
• оценка общего сердечно-сосудистого риска.
• Всем пациентам при измерении уровня АД в медицинском учреждении рекомендуется классифицировать его на оптимальное, нормальное, высокое нормальное артериальное давление или артериальную гипертензию 1–3-й степени [21, 22].
ЕОК/ЕОАГ нет (УУР С, УУД 5)
Комментарий. Повышение АД, измеренного в медицинском учреждении выше 140 и/или 90 мм рт. ст. (таблица П2, Приложение Г1) на двух разных визитах, за исключением тяжелой АГ (АГ 3-й степени, особенно у пациентов высокого риска) и/или повышения АД при измерении вне медицинского учреждения (по данным СМАД и/или ДМАД) при условии экономической и логистической целесообразности [32–37] (таблица П7, Приложение Г2).
У всех пациентов с впервые диагностированным гипертоническим кризом, необходимо выявить причину повышения АД, в т.ч. симптоматическую АГ.
У всех пациентов при выявлении повышения АД в медицинском учреждении необходимо два измерения АД на двух разных визитах для постановки диагноза АГ (таблица П2, Приложение Г1) [21;32].
На каждом визите должно быть проведено не менее двух измерений АД с интервалом в 1-2 мин и еще одно дополнительное измерение при разнице между первыми двумя более 10 мм рт. ст. Уровень АД — это среднее из последних двух измерений.
- Проведение методов измерения АД вне медицинского учреждения (СМАД и ДМАД) рекомендуется в отдельных клинических ситуациях: при выявлении гипертонии белого халата и маскированной АГ с целью оценки эффективности лечения и выявлении возможных побочных эффектов [21, 32, 38].
ЕОК/ЕОАГ IA (УУР C, УДД 5)
- Рекомендуется при установлении диагноза учитывать возможность вторичной (симптоматической) формы АГ и проводить диагностические мероприятия, направленные на ее исключение при наличии следующих признаков [39, 138, 220] (таблица П3, Приложение Г2):
o АГ 2-й степени у пациентов моложе 40 лет или любое повышение АД у детей
o Внезапное острое развитие АГ у пациентов с ранее документированной стойкой нормотонией
o Резистентная АГ
o АГ 3-й степени или гипертонический криз
o Признаки значительных изменений в органах-мишенях
o Клинические или лабораторные признаки, позволяющие подозревать эндокринные причины АГ или ХБП
o Клинические симптомы СОАС
o Симптомы, позволяющие заподозрить феохромоцитому, или семейный анамнез данной опухоли
ЕОК/ЕОАГ нет (УУР A, УДД 1)
Комментарии. Вторичные АГ выявляются у 5–10% пациентов с АГ [39]. Для диагностики вторичных форм АГ важно детальное обследование пациента, начиная с рутинных методов: опроса, осмотра, лабораторной диагностики, до выполнения сложных инструментальных методов (Таблица П3, Приложение Г2).
Принципы формулировки диагноза при АГ
• Необходимо указать стадию гипертонической болезни (Таблица П1, Приложение Г3).
• Степень повышения АД (степень АГ (Таблица 2, Приложение Г1) обязательно указывается у пациентов с впервые диагностированной АГ. Если пациент принимает антигипертензивную терапию, то в диагнозе указывается наличие контроля АД (контролируемая/неконтролируемая АГ).
• При формулировании диагноза максимально полно должны быть отражены ФР, ПОМ, ССЗ, ХБП и категория сердечно-сосудистого риска (таблицы П1 и П2, Приложение Г3).
• Указание целевого уровня АД для данного пациента
Примеры формулировки диагноза:
1. ГБ I стадии. Степень АГ 1. Гиперлипидемия. Риск 2 (средний). Целевое АД <130/<80 мм рт. ст.
2. ГБ II стадии. Неконтролируемая АГ. Нарушенная гликемия натощак. Гиперлипидемия. ГЛЖ. Риск 3 (высокий) Целевое АД <130/<80 мм рт. ст.
3. ГБ II стадии. Неконтролируемая АГ. Гиперлипидемия. Ожирение II степени. Нарушение толерантности к глюкозе. ГЛЖ. Альбуминурия высокой степени. Риск 4 (очень высокий). Целевое АД 130-139/<80 мм рт. ст.
4. ИБС. Стенокардия напряжения III ФК. Постинфарктный кардиосклероз (2010г). ГБ III стадии. Неконтролируемая АГ. Риск 4 (очень высокий). Целевое АД <130/<80 мм рт. ст.
5. ГБ III стадии. Контролируемая АГ. Ожирение I степени. Сахарный диабет 2-го типа, целевой уровень гликированного гемоглобина ≤7,5%. ХБП С4 стадии, альбуминурия А2. Риск 4 (очень высокий). Целевое АД 130–139/< мм рт. ст.
Принципы измерения АД
- Скрининг АГ путем измерения АД в медицинском учреждении и регистрация полученных цифр АД в медицинской документации рекомендован всем пациентам с 18 лет [33, 40] (Таблица П1, Приложение Г2).
ЕОК/ЕОАГ IВ (УУР А, УДД 1)
- Для определения степени и стабильности повышения уровня АД рекомендовано проводить измерения АД в медицинском учреждении (таблица П2, Приложение Г1) у всех пациентов с повышением АД [33, 40, 42].
EОК/ЕОАГ IВ (УУР А, УДД 1)
Комментарии. Клиническое измерение АД имеет наибольшую доказательную базу для диагностики АГ и оценки эффективности антигипертензивной терапии (АГТ). Точность измерения АД и, соответственно, диагностика АГ, определение ее степени тяжести зависят от соблюдения правил по измерению АД (Таблица П1, Приложение Г1).
- Рекомендуется проводить измерения АД в медицинском учреждении на обеих руках, по крайней мере, во время первого визита пациента для выявления возможного поражения артерий (в первую очередь атеросклеротического), ассоциированного с более высоким СС риском [41].
EОК/ЕОАГ IА (УУР А, УДД 2)
Комментарии. При разнице показателей АД на правой и левой руке более 15 мм рт. ст. вероятно атеросклеротическое поражение сосудов. При выявленной разнице показателей между правой и левой руками в дальнейшем рекомендуется проводить измерения на руке с более высоким АД.
- Определение АД, измеренного вне медицинского учреждения (СМАД или ДМАД) для постановки диагноза или контроля эффективности АГТ рекомендуется в ряде клинических ситуаций, указанных в таблице П7, Приложение Г2 [40, 42–46].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
Комментарии. Преимущества и недостатки каждого метода измерения АД суммированы в таблице П8, Приложение Г2. Диагностические критерии АГ по данным СМАД приведены в таблице П9, Приложение Г2. Результаты СМАД и ДМАД могут помочь в диагностике АГ, но не заменяют повторные измерения АД в лечебном учреждении. Следует обратить внимание, что критерии диагностики АГ по результатам клинического измерения АД, СМАД и ДМАД (таблица П2, приложение Г1 и таблица П9 приложение Г2).
Оценка сердечно-сосудистого риска
- Базовый скрининг на наличие ПОМ рекомендовано проводить у всех пациентов с АГ. Расширенное обследование рекомендовано в том случае, когда выявление ПОМ повлияет на выбор терапевтической тактики [21, 22].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. Для выявления поражения сердца всем пациентам целесообразно проводить регистрацию электрокардиограммы (ЭКГ) с расчетом индексов гипертрофии ЛЖ, в случае расширенного обследования — ЭхоКГ с определением индекса массы миокарда левого желудочка. Для выявления поражения почек у всех оценивают протеинурию/альбуминурию, концентрационную функцию и мочевой осадок; при расширенном обследовании выполняется УЗИ почек и допплерография почечных артерий. Для выявления поражения сосудов рекомендовано выполнение фундоскопии, расчет пульсового давления (ПД) у пожилых, оценка лодыжочно-плечевого индекса (ЛПИ), скорость пульсовой волны (СПВ) и обследования для выявления атеросклеротических бляшек в брахиоцефальных, почечных и подвздошно-бедренных сосудах при расширенном обследовании (таблицы П4 и П5, приложение Г2).
- Всем пациентам с АГ рекомендуется оценка общего сердечно-сосудистого риска (ССР) — выявление ФР, ПОМ и АКС, СД, ХБП, которые влияют на прогноз (таблица П10, Приложение Г2). Для оценки степени риска развития ССО рекомендуется обследование с целью оценки состояния органов-мишеней в соответствии с действующими клиническими рекомендациями [47].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. Величина АД является важнейшим, но не единственным фактором, определяющим тяжесть АГ, прогноз пациента и тактику лечения. Большое значение имеет оценка общего ССР, степень которого зависит от величины АД, наличия или отсутствия сопутствующих ФР, субклинического поражения органов-мишеней и наличия АКС и СД. Повышенный уровень АД, наличие ФР и ПОМ взаимно усиливают влияние друг на друга, что приводит к увеличению степени ССР, превышающего сумму отдельных его компонентов. Комплексный подход к оценке сердечно-сосудистого риска приведен в таблице П10 приложения Г2.
Оценка риска по шкале SCORE (Таблица П11, Приложение Г2) является одним из вариантов алгоритма оценки суммарного сердечно-сосудистого риска у пациентов с ГБ I–II стадии, т.е. не имеющих установленных ССЗ, ХБП и СД.
Пациенты с ГБ III стадии, имеющие документированное ССЗ атеросклеротического генеза (под атеросклеротическим ССЗ подразумевают ишемическую болезнь сердца, ишемический инсульт или транзиторное нарушение мозгового кровообращения, ишемию нижних конечностей), включая бессимптомный атеросклероз при визуализации, СД 1-го или 2-го типа, очень высокие значения по отдельным факторам риска (в том числе АГ 3-й степени) или ХБП 3–5-й стадий по умолчанию относятся к категории высокого или очень высокого риска по глобальной шкале 10-летнего риска сердечно-сосудистых осложнений (Таблица П12, Приложение Г2). Внутри категории очень высокого риска введена категория экстремального риска. К экстремальному риску следует относить:
сочетание клинически значимого сердечно-сосудистого заболевания, вызванного атеросклерозом, с СД 2 типа и/или СГХС;
сердечно-сосудистое осложнение у пациента с атеросклеротически сердечно-сосудистым заболеванием, несмотря на оптимальную гиполипидемическую терапию и/или достигнутый уровень ХС ЛНП ≤1,5 ммоль/л;
2 и более сердечно-сосудистых осложнения в течение 2 лет.
Акцент на значимость выявления поражения ФР и органов-мишеней для корректной оценки сердечно-сосудистого риска — одна из ключевых особенностей современных рекомендаций. Бессимптомное ПОМ может существенно увеличивать риск у пациентов с АГ. Наибольшая польза от детальной оценки ПОМ может наблюдаться у пациентов среднего возраста, у молодых пациентов с АГ 1-й степени, пациентов с высоким нормальным АД. Необходимо подчеркнуть важность оценки функции почек по показателям скорости клубочковой фильтрации (СКФ), альбуминурии и количественной оценки гипертрофии левого желудочка (ГЛЖ). Основная цель выявления ПОМ — правильное определение категории риска [48]. Первостепенное значение оценка ПОМ имеет у больных с низким и умеренным риском, меньшее значение — при высоком и очень высоком риске. Характер органного поражения не играет решающей роли в выборе режима антигипертензивной терапии, но регресс ПОМ — суррогатный маркер среднесрочной эффективности АГТ [49].
Для выявления ПОМ целесообразно использовать дополнительные методы исследования (таблица П5, приложение Г2): сердца (ЭхоКГ с определением индекса массы миокарда левого желудочка), почек (количественное определение альбуминурии/протеинурии, определение скорости клубочковой фильтрации), сосудов (наличие атеросклеротических бляшек в брахиоцефальных, почечных и подвздошно-бедренных сосудах, определение лодыжечно-плечевого индекса (ЛПИ), каротидно-феморальной скорости пульсовой волны (СПВ).
Наличие ПОМ способствует дальнейшему прогрессированию ССЗ, что существенно увеличивает риск смерти у таких пациентов по сравнению с пациентами, у которых имеются только ФР (Таблица П2, Приложение Г3). Риск возрастает с увеличением числа органных поражений, ассоциированных с АГ. Уровень СС риска у ряда пациентов может быть выше, чем он определен по стандартной системе стратификации (Таблица П1, Приложение Г3):
— при малоподвижном образе жизни у пациентов с центральным ожирением (увеличение относительного риска, ассоциированного с ожирением, более выражено у молодых, чем у пожилых пациентов);
— у лиц с низким социальным статусом;
— у пациентов с повышенным уровнем аполипопротеина В, липопротеина (а) и уровня С-реактивного белка, определенного высокочувствительным методом.
Как в общей популяции, так и у пациентов АГ необходимо учитывать факторы, повышающие СС риск (таблица П13, Приложение Г2). Такие модифицирующие факторы приобретают особое значение у пациентов, относящихся к категории умеренного риска. Наличие модифицирующих факторов может привести к изменению категории риска на более высокую и, соответственно, повлиять на решение о старте и выборе терапии.
- Пациентам с АГ, которые не соответствуют категориям высокого или очень высокого риска при оценке по глобальной шкале 10-летнего СС риска (Таблица П12, Приложение Г2), рекомендуется проводить оценку СС риска по шкале SCORE (Приложение Г) [49, 50].
ЕОК/ЕОАГ IВ (УУР С, УДД 4)
Комментарии. Пациенты с АГ с диагностированным ССЗ, включая бессимптомные атеросклеротические бляшки со стенозом ≥50%, выявленные при визуализации, сахарным диабетом 1-го и 2-го типа, значимо повышенным единственным фактором риска (в том числе — с АГ 3-й степени) или хронической болезнью почек (ХБП, стадии 3–5) автоматически относятся к категориям очень высокого (риск СС смертности ≥10%) или высокого (СС смертность 5–10%) 10-летнего СС риска.
Жалобы и анамнез
Многие пациенты с повышенным АД могут не иметь никаких жалоб. Симптомы (головные боли, одышка, боль в груди, кровотечение из носа, субъективное головокружение, отеки, расстройство зрения, ощущение жара, потливость, приливы), встречающиеся при АГ неспецифичны и могут наблюдаться при других заболеваниях.
При наличии перечисленных симптомов у любого пациента необходимо в процессе его обследования учитывать возможность диагностированной АГ.
- Рекомендуется собирать полный медицинский и семейный анамнез для оценки семейной предрасположенности к АГ и ССЗ [51, 52].
ЕОК/ЕОАГ нет (УУР С, УДД 4)
Комментарии. Сбор анамнеза включает сбор сведений о наличии ФР, субклинических симптомов ПОМ, наличии в анамнезе ССЗ, ЦВБ, ХБП и вторичных форм АГ, образе жизни, предшествующем опыте лечения АГ (таблица П3, Приложение Г1).
Физикальное обследование
- Всем пациентам с АГ рекомендуется определение антропометрических данных для выявления избыточной массы тела/ожирения, оценка неврологического статуса и когнитивной функции, исследование глазного дна для выявления гипертонической ретинопатии, пальпация и аускультация сердца и сонных артерий, пальпация и аускультация периферических артерий для выявления патологических шумов, сравнение АД между руками хотя бы однократно [21].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. Объективное исследование пациента с АГ направлено на выявление ФР, признаков вторичных форм АГ и ПОМ. В таблице П3, Приложение Г2 суммированы основные положения и требования к клиническому обследованию пациента.
- Всем пациентам с АГ рекомендуется пальпировать пульс в покое для измерения его частоты и ритмичности с целью выявления аритмий [21; 32; 43].
ЕОК/ЕОАГ IС (УУР В, УДД 2)
Лабораторная диагностика
Для установления диагноза АГ лабораторная диагностика не требуется, однако, она необходима с целью исключения вторичных форм АГ, выявления ПОМ, оценки СС риска, и сопутствующей патологии, влияющей на эффективность лечения и качество жизни пациента.
- Всем пациентам с АГ с целью исключения вторичной гипертензии рекомендуется проведение общего (клинического) анализа крови (гемоглобин/гематокрит, лейкоциты, тромбоциты) [21, 22].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
- Для выявления предиабета, СД и оценки сердечно-сосудистого риска всем пациентам с АГ рекомендуется исследование уровня глюкозы в венозной крови [53,54,55,56,57, 302].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. При значениях глюкозы ≥ 6,1 ммоль/Л следует повторно определить ее уровень во всех случаях, кроме несомненной гипергликемии с острой метаболической декомпенсацией или очевидными симптомами. В качестве теста, подтверждающего гипергликемию, может быть определение гликированного гемоглобина (НвА1с). Диагноз СД устанавливают на основании двух цифр, находящихся в диабетическом диапазоне: дважды определенный HbA1c или однократное определение HbA1c и однократное определение уровня глюкозы крови. Значения перечисленных параметров оценки гликемии выше нормальных, но ниже диабетических, указывают на наличие предиабета. Пероральный глюкозотолерантный тест (ПГТТ) проводится в сомнительных случаях для уточнения диагноза СД, а также для выявления предиабета. Гликированный гемоглобин (НвА1с) может быть использован для диагностики СД и предиабета, если метод его определения сертифицирован в соответствии с National Glycohemoglobin Standartization Program (NGSP), или International Federation of Clinical Chemists (IFCC) и стандартизованного в соответствии с референсными значениями, принятыми в Diabetes Control and Complications Trial (DCCT). При наличии СД рекомендуется стратификация пациента в категорию высокого или очень высокого сердечно-сосудистого риска.
- Всем пациентам с АГ для выявления нарушения функции почки оценки сердечно-сосудистого риска рекомендуются исследование уровня креатинина в сыворотке крови и расчет скорости клубочковой фильтрации (СКФ) в мл/мин/1,73м2 по формуле Chronic Kidney Disease Epidemiology (CKD-EPI) [58] в специальных калькуляторах (Таблица П3, Приложение Г3) [21, 22, 58].
ЕОК/ЕОАГ IВ (УУР B, УДД 2)
Комментарии. Выполняется у всех пациентов с АГ для выявления ХБП в связи с тем, что снижение СКФ <60 мл/мин/1,73м2 является значимым прогностическим фактором при АГ [60] и в связи с наличием доказанной связи между даже незначительным снижением СКФ и повышением сердечно-сосудистой смертности [61, 62]. Формула CKD-EPI включает те же 4 переменные, что и формула MDRD. Формула CKD-EPI дает меньше погрешностей, чем формула MDRD, особенно при СКФ≥60 мл/мин/1,73 м2, и характеризуется несколько меньшим разбросом данных и бόльшей точностью. Значительная часть (но не все) исследований в Северной Америке, Европе показали, что формула CKD-EPI дает более точные результаты, чем формула MDRD, особенно при высокой СКФ [63]. Меньшая погрешность формулы CKD-EPIпо сравнению с формулой MDRD отражает более высокую рСКФ в большей части возрастного диапазона и значений креатинина, особенно у лиц молодого возраста, женщин и представителей европеоидной расы [64].
- Всем пациентам с АГ для выявления заболеваний почек и оценки СС риска рекомендуется проводить общий (клинический) анализ мочи с микроскопическим исследованием осадка мочи, количественной оценкой альбуминурии или отношения альбумин/креатинин (оптимально) [64, 65].
ЕОК/ЕОАГ IВ (УУР В, УДД 2)
Комментарии. Выполняется у всех пациентов с АГ в связи с тем, что повреждение почек является значимым прогностическим фактором при АГ, наличием доказанной связи между выявлением альбуминурии и повышением середечно-сосудистой смертности [60, 61, 64, 66]. Суточная экскреция альбумина с мочой ≥30 мг/сут ассоциирована с повышенным риском осложнений ХБП [64]. В мета-анализе Консорциума по прогнозу ХБП обнаружены ассоциации между СЭА ≥30 мг/сут при исследовании тест-полосками, с риском общей смертности и смертности от ССЗ, почечной недостаточности прогрессирования ХБП в общей популяции и в популяциях с повышенным риском развития ССЗ. Соотношение альбумин/креатинин в моче (предпочтительно в утренней порции) 30–300 мг/г; 3,4–34 мг/ммоль является маркером повреждения почек [64].
- Всем пациентам с АГ для стратификации риска и выявления нарушений липидного обмена рекомендуется исследование уровня общего холестерина (ОХС), холестерина липопротеинов высокой плотности (ХС-ЛВП), холестерина липопротеинов низкой плотности (ХС-ЛНП) (прямое измерение или расчетно) и триглицеридов (ТГ) в крови [21, 67, 68].
ЕОК/ЕОАГ нет (УУР В, УДД 2)
Комментарии. Выполняется у всех пациентов с АГ для стратификации риска [67, 68], а также в связи с высокой распространенностью дислипидемии в популяции пациентов с АГ и положительным эффектом коррекции дислипидемии на СС риск у пациентов с АГ [21, 22].
- Всем пациентам с АГ для выявления электролитных нарушений и дифференциального диагноза с вторичной АГ рекомендуется исследование уровня калия и натрия в крови [21, 22].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. Выполняется у всех пациентов с АГ для выявления электролитных нарушений в связи с доказанной взаимосвязью между уровнем калия и натрия сыворотки крови и уровнем АД [69, 70].
- Всем пациентам с АГ для выявления гиперурикемии рекомендуется исследование уровня мочевой кислоты в крови [71].
ЕОК/ЕОАГ нет (УУР А, УДД 2)
Комментарии. Выполняется у всех пациентов с АГ в связи с тем, что уровень мочевой кислоты является значимым прогностическим фактором при АГ, а также наличием доказанной связи между гиперурикемией и повышением сердечно-сосудистой смертности [71-73].
Инструментальная диагностика
Проведение инструментальных методов диагностики является необходимым для исключения вторичных форм АГ, выявления поражения органов-мишеней, оценки сердечно-сосудистого риска, и сопутствующей патологии, влияющей на эффективность лечения и качество жизни пациента.
- Всем пациентам с АГ для выявления ГЛЖ и определения СС риска рекомендуется проведение 12-канальной ЭКГ [21, 22, 78, 297].
ЕОК/ЕОАГ IВ (УУР В, УДД 1)
Комментарии. Выполняется у всех пациентов с АГ для выявления гипертрофии левого желудочка (ГЛЖ) и определения сердечно-сосудистого риска [74–84]. ГЛЖ характеризуют индекс Соколова–Лайона (SV1+RV5-6 >35 мм); амплитуда зубца R в Корнельский показатель (RaVL+SV3) >20 мм для женщин, (RAVL+SV3) >28 мм для мужчин; Корнельское произведение (RAVL+SV5) мм х QRS мс> 2440 мм х мс [21, 22]. Несмотря на то, что ЭКГ является менее чувствительным методом диагностики ГЛЖ по сравнению с ЭхоКГ [80, 82, 84], она незаменима для документирования сердечного ритма, ЧСС и выявления аритмий.
- Пациентам с АГ при наличии изменений на ЭКГ или симптомов/признаков дисфункции левого желудочка рекомендуется проведение ЭхоКГ для выявления степени ГЛЖ [21, 22, 81].
ЕОК/ЕОАГ IВ (УУР B, УДД 2)
Комментарии. В таблице П6 (Приложение Г2) приведены эхокардиографические критерии для диагностики изменений левых отделов сердца [85].
- Пациентам с АГ в сочетании с ЦВБ или признаками атеросклеротического поражения сосудов других локализаций, при указании в анамнезе на преходящую слабость в конечностях с одной стороны или онемение половины тела, а также мужчинам старше 40 лет, женщинам старше 50 лет и пациентам с высоким общим сердечно-сосудистым риском (Таблица П12, Приложение Г2) рекомендуется дуплексное сканирование брахиоцефальных артерий для выявления атеросклеротических бляшек/стенозов внутренних сонных артерий [21, 298].
ЕОК/ЕОАГ IВ (УУР В, УДД 1)
Комментарии. О наличии бляшки говорит толщина комплекса интима-медиа (КИМ)>1,5 мм или локальное увеличение толщины на 0,5 мм или на 50%, по сравнению со значением КИМ в прилежащих участках сонной артерии [21].
- Рекомендуется определение ЛПИ в целях уточнения категории риска пациентам с симптомами значимого атеросклероза артерий нижних конечностей или пациентам умеренного риска, у которых положительные результаты данного исследованияприведут к изменению категории риска [86, 87].
ЕОК/ЕОАГ IIbВ (УУР B, УДД 2)
- Всем пациентам с нарушением функции почек, альбуминурией и при подозрении на вторичную АГ рекомендуется проведение УЗИ (ультразвукового исследования) почек и дуплексного сканирования артерий почек с целью оценки размеров, структуры, а также наличия врожденных аномалий почек или стеноза почечных артерий [60, 61, 64].
ЕОК/ЕОАГ IIaC (УУР В, УДД 1)
- Пациентам с АГ 2–3-й степеней, всем пациентам с сахарным диабетом и АГ рекомендуется проводить исследование глазного дна врачом-офтальмологом (геморрагии, экссудаты, отек соска зрительного нерва) для выявления гипертонической ретинопатии [21, 89].
ЕОК/ЕОАГ IС (УУР С, УДД 4)
Комментарии. Гипертоническая ретинопатия, выявленная с помощью фундоскопии (осмотра глазного дна), имеет высокую прогностическую значимость при АГ [88–90]. Обнаружение кровоизлияний в сетчатку, микроаневризм, твердых экссудатов, папиллоэдемы указывает на тяжелую гипертоническую ретинопатию и значимо коррелирует с плохим прогнозом. Изменения, характерные для ранних стадий ретинопатии, не имеют существенного прогностического значения и характеризуются низкой воспроизводимостью. Фундоскопия также показана, если диагноз важен для экспертизы трудоспособности или определения годности к военной службе.
- Пациентам с АГ при наличии неврологических симптомов и/или когнитивных нарушений рекомендуется выполнение КТ или МРТ головного мозга для исключения инфарктов мозга, микрокровоизлияний и повреждений белого вещества и других патологических образований [21, 91, 92].
ЕОК/ЕОАГ IIаВ (УУР А, УДД 1)
Комментарии. Гиперинтенсивные очаги в белом веществе головного мозга и бессимптомные инфаркты ассоциированы с прогрессированием когнитивной дисфункции и повышением риска инсульта в связи с дегенеративной и сосудистой деменцией.
Иные диагностические исследования
Иные диагностические исследования в рамках диагностики АГ не предусмотрены, возможно расширение диагностических исследований по решению врача в зависимости от клинической ситуации и состояния пациента.
- Когнитивные нарушения у пожилых пациентов частично ассоциированы с АГ, в связи с чем у пожилых пациентов с анамнезом, позволяющим предположить ранний когнитивный дефицит, рекомендована оценка когнитивной функции с использованием теста MMSE (MiniMentalStateExamination) [93, 94].
ЕОК/ЕОАГ нет (УУР A, УДД 1)
Лечение
Лечение, включая медикаментозную и немедикаментозную терапию, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Решение о тактике лечения рекомендуется принимать в зависимости от исходного уровня АД и общего сердечно-сосудистого риска. Показания к АГТ суммированы в таблице П1, Приложение Г4.
- Всем пациентам с АГ 1-й степени рекомендуется проводить мероприятия по изменению (оздоровлению) образа жизни с целью нормализации АД и коррекции факторов риска [21, 95, 96].
ЕОК/ЕОАГ IIаB (УУР B, УДД 1)
Комментарии. Подробный подход к изменению образа жизни с целью снижения СС риска представлен в разделе «Немедикаментозное лечение АГ».
Показания к антигипертензивной терапии
(Таблица П2, Приложение Г4)
- Пациентам с АГ 2-й или 3-й степени при любом уровне СС риска рекомендуется незамедлительное начало антигипертензивной лекарственной терапии для снижения риска развития сердечно-сосудистых осложнений, СС смерти одновременно с рекомендациями по изменению образа жизни [59, 110].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Пациентам с АГ 1-й степени, относящимся к категориям низкого/умеренного риска без признаков ПОМ (оценка риска по шкале SCORE (Таблица П11, Приложение Г2) рекомендуется начинать антигипертензивную лекарственную терапию в том случае, если у них сохраняется повышенное АД, несмотря на мероприятия по изменению образа жизни в течение 3 месяцев [21, 22, 97].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Пациентам с АГ 1-й степени, относящимся к категории высокого риска (оценка риска по шкале SCORE (Приложение Г3) при неосложненной АГ или при наличии ПОМ, рекомендуется незамедлительное начало антигипертензивной лекарственной терапии одновременно с рекомендациями по изменению образа жизни [21, 22, 97].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Пациентам с высоким нормальным АД (130–139/85–89 мм рт. ст.) рекомендуется начало АГТ при очень высоком уровне СС риска вследствие наличия ССЗ (особенно ИБС) (Таблица П12, Приложение Г2) [21, 22, 99].
ЕОК/ЕОАГ IIbA (УУР А, УДД 1)
- Пожилым пациентам с АГ (даже в возрасте >80 лет), находящимся в удовлетворительном физическом состоянии, рекомендуется изменение образа жизни и АГТ при уровне САД ≥160 мм рт. ст. [21, 22, 100]. Пожилым пациентам (>65 лет, но не >80 лет), находящимся в удовлетворительном физическом состоянии (без синдрома старческой астении), если их САД соответствует показателям АГ 1-й степени (140–159 мм рт. ст.), рекомендуются изменение образа жизни и АГТ при хорошей переносимости [21, 22, 100, 101, 102, 235].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Рекомендуется рассмотреть возможность назначения АГТ пожилым пациентам с синдромом старческой астении при удовлетворительной переносимости [100, 101, 235].
ЕОК/ЕОАГ IIbB (УУР A, УДД 1)
- У пациентов старше 80 лет не рекомендуется отменять антигипертензивную лекарственную терапию, при условии, что эта терапия хорошо переносится, не сопровождается ортостатической гипотонией, развитием/усугублением гериатрических синдромов и снижением функционального статуса в связи с доказанными преимуществами в отношении СС смертности [21, 22, 101, 103, 104].
ЕОК/ЕОАГ IIIA (УУР А, УДД 1)
Целевые уровни артериального давления
- Всем пациентам с АГ, получающим лечение, независимо от возраста и степени риска, рекомендуется в качестве первого целевого уровня снижать АД до значений <140/90 мм рт. ст., а при условии хорошей переносимости — до целевого уровня 130/80 мм рт. ст. или ниже, в связи с доказанными преимуществами в плане снижения риска сердечно-сосудистых осложнений [59, 105, 107].
ЕОК/ЕОАГ IA (УУР A, УДД 1)
- Пациентам моложе 65 лет и без ХБП, получающих антигипертензивную терапию, рекомендуется снижать САД до значений 120–130 мм рт. ст., в связи с доказанным влиянием вмешательства на СС риск [59, 103, 106, 107, 108].
ЕОК/ЕОАГ IA (УУР A, УДД 1)
- Пациентам 65 лет и старше без старческой астении, получающим антигипертензивную терапию, вне зависимости от уровня СС риска и наличия ССЗ рекомендуется снижать САД до целевых значений 130–139 мм рт. ст., при условии хорошей переносимости. [59, 103, 107, 108].
ЕОК/ЕОАГ IA (УУР A, УДД 1)
Комментарии. Всем пациентам в возрасте ≥65 лет, получающим антигипертензивную терапию, при каждом визите к врачу рекомендуется проводить оценку возможных нежелательных явлений.
- Всем пациентам с АГ вне зависимости от возраста, уровня риска и наличия сопутствующих заболеваний рекомендуется снижать ДАД до целевых значений 70–79 мм рт. ст. (таблица П3, Приложение Г4) [107, 109, 110].
ЕОК/ЕОАГ IIaB (УУР B, УДД 2)
Комментарии. Следует учитывать, что нижняя граница безопасности установлена в связи с результатами исследований, проведенных преимущественно в группах пациентов высокого и очень высокого риска (пожилые с коморбидностью, установленными ССЗ, в том числе — лица с ИБС, заболеванием периферических артерий. Таким образом, в общей популяции пациентов с АГ, верятно, нет необходимости в коррекции лечения при уровне САД <120 мм рт. ст. и ДАД <70 мм рт. ст. при его хорошей переносимости.
Немедикаментозное лечение АГ
Мероприятия по изменению образа жизни рекомендуются всем пациентам с АГ. Немедикаментозные методы лечения АГ способствуют снижению АД, уменьшают потребность в антигипертензивных препаратах (АГП) и повышают их эффективность, позволяют осуществлять коррекцию ФР, проводить первичную профилактику АГ у пациентов с высоким нормальным АД и имеющих ФР [114, 115].
- Всем пациентам с АГ для улучшения контроля заболевания рекомендуется ограничение употребления соли до <5 г в сутки [116–119].
ЕОК/ЕОАГ IA (УУР A, УДД 1)
Комментарии. Избыточное потребление соли может играть существенную неблагоприятную роль в развитии рефрактерной АГ. Стандартное потребление соли во многих странах составляет от 9 до 12 г/сутки (80% потребляемой соли приходится на так называемую «скрытую соль»), уменьшение ее потребления до 5 г/сутки у пациентов АГ ведет к снижению САД на 4–5 мм рт. ст. Влияние ограничения натрия более выражено у пациентов пожилого и старческого возраста, у пациентов с СД, МС и ХБП.
- Всем пациентам с АГ для улучшения контроля заболевания рекомендуется ограничить употребления алкоголя (менее 14 единиц в неделю для мужчин, менее 8 единиц в неделю для женщин*) и избегать хронического злоупотребления алкоголем [21, 22, 120].
ЕОК/ЕОАГ IA (УУР A, УДД 1)
Комментарии. Одной единицей употребления алкоголя следует считать 10 мл или 8 г чистого спирта, что соответствует 125 мл вина или 250 мл пива.
- Всем пациентам с АГ для улучшения метаболических показателей рекомендуется увеличить употребление овощей, свежих фруктов, рыбы, орехов и ненасыщенных жирных кислот (оливковое масло), молочных продуктов низкой жирности, уменьшить употребление мяса [121].
ЕОК/ЕОАГ IA (УУР А, УДД 1)
Комментарии. Необходимо увеличение потребления растительной пищи, содержания в рационе калия, кальция (в овощах, фруктах, зерновых) и магния (в молочных продуктах), а также уменьшение потребления жиров животного происхождения. Пациентам с АГ следует рекомендовать употребление рыбы не реже двух раз в неделю и 300–400 г в сутки свежих овощей и фруктов.
- Всем пациентам с АГ рекомендуется контролировать массу тела для предупреждения развития ожирения (индекс массы тела (ИМТ) ≥30 кг/м2 или окружность талии >102 см у мужчин и >88 см у женщин) и достижение ИМТ в пределах 20–25 кг/м2; окружности талии <94 см у мужчин и <80 см у женщин с целью снижения АД и уменьшения СС риска [122–124].
ЕОК/ЕОАГ IA (УУР А, УДД 1)
Комментарии. У лиц с ожирением уменьшение массы тела на 5–10% от исходной приводит к достоверному снижению риска развития ССО.
- Всем пациентам с АГ в связи с доказанным положительным эффектом на уровень СС смертности рекомендуются регулярные аэробные физические упражнения (не менее 30 минут динамических упражнений умеренной интенсивности 5–7 дней в неделю) [125, 126].
ЕОК/ЕОАГ IA (УУР А, УДД 2)
Комментарии. Пациентам с АГ следует рекомендовать умеренные аэробные нагрузки (ходьба, скандинавская ходьба, езда на велосипеде, плавание, фитнес). Влияние изометрической силовой нагрузки на уровень АД и СС риск до конца не ясно.
- Всем пациентам с АГ в связи с доказанным негативным эффектом курения на уровень смертности рекомендуются прекращение курения, психологическая поддержка и выполнение программ по прекращению курения [127–129].
ЕОК/ЕОАГ IB (УУР А, УДД 2)
Медикаментозная терапия АГ
Общие принципы медикаментозной терапии
Основой антигипертензивной терапии для снижения АД и уменьшения числа СС событий являются 5 классов антигипертензивных препаратов: ингибиторы АПФ (ИАПФ), блокаторы рецепторов ангиотензина-II (БРА), бета-адреноблокаторы (ББ), блокаторы кальциевых каналов (АК) и диуретики (тиазидные — гидрохлортиазид, и тиазидоподобные — хлорталидон и индапамид).
Противопоказания к назначению основных антигипертензивных препаратов суммированы в таблице П4, Приложение Г4.
- Всем пациентам с АГ (кроме пациентов низкого риска с АД<150/90 мм рт. ст., пациентов ≥80 лет, пациентов с синдромом старческой астении) в качестве стартовой терапии рекомендована комбинация антигипертензивных препаратов, предпочтительно фиксированная, для улучшения приверженности к терапии. Предпочтительные комбинации должны включать блокатор ренин-ангиотензиновой системы (РААС) (ингибитор АПФ или БРА) и дигидропиридиновый АК или диуретик (Приложение Б2) [130–134].
ЕОК/ЕОАГ IA (УУР А, УДД 1)
Комментарии. Многочисленными РКИ показано, что монотерапия эффективно снижает АД лишь у ограниченного числа пациентов АГ, большинству пациентов для контроля АД требуется комбинация как минимум из двух препаратов. Метаанализ более 40 исследований показал, что комбинация двух препаратов из любых двух классов антигипертензивных средств усиливает степень снижения АД намного сильнее, чем повышение дозы одного препарата. Еще одно преимущество комбинированной терапии — возможность физиологического и фармакологического синергизма между препаратами разных классов, что может не только лежать в основе более выраженного снижения АД и лучшей переносимости. Комбинированная терапия позволяет также подавить контррегуляторные механизмы повышения АД. Все преимущества комбинированной терапии присущи только рациональным комбинациям АГП. К ним относятся: ИАПФ + диуретик; БРА + диуретик; ИАПФ + АК; БРА + АК, дигидропиридиновый АК + ББ, АК + диуретик, ББ + диуретик. На практике могут быть использованы и другие комбинации пяти основных классов антигипертензивных средств при наличии индивидуальных показаний. При наличии клинической целесообразности, с учетом особенностей клинического течения заболевания, коморбидной патологии, переносимости лечения и профиля побочных эффектов, а также при наличии предпочтений пациента, связанных с его личным позитивным или негативным опытом, и, соответственно с учетом ожидаемой приверженности к лечению врач имеет право назначать любой антигипертензивный препарат, который зарегистрирован для лечения АГ в РФ, как в монотерапии, так и в комбинации. При этом отклонение от стандартных схем терапии требует соответствующего объяснения в истории болезни.
К запрещенным комбинациям относится комбинация двух блокаторов РААС.
Фиксированные комбинации повышают приверженность к лечению. Однако такие лекарственные формы не входят в формуляры многих учреждений и в списки жизненно важных лекарственных препаратов, что делает сложным их назначение пациентам в стационаре и льготным категориям пациентов, поэтому если у пациента достигнут целевой уровень АД в пределах установленных значений и наблюдается хорошая приверженность к лечению, то нет необходимости его перевода со свободной на фиксированные комбинации. Свободные комбинации могут быть использованы также по организационным соображениям, в частности с целью обеспечения доступности препаратов для пациента.
Шаги АГТ предполагают возможность или использования более высоких дозировок в комбинации, или сразу переход на 3-компонентную схему лечения. Оба подхода допустимы на этапе 2-компонентной схемы, но они должны обеспечить достижение целевого АД в течение 3 месяцев с шагом титрации дозы приблизительно 4 недели.
Следует подчеркнуть, что в реальной практике на 1 шаге терапии необходимо назначать препараты в оптимальных терапевтических дозах, которые могут обеспечить достижение целевого АД в указанные сроки. В этом случае при недостижении целевого АД рациональным будет переход на следующий шаг. До перехода на 4-компонентную схему необходимо использование трех препаратов в максимальных дозах при хорошей переносимости.
У 15–20% пациентов контроль АД может быть не достигнут при использовании 3 препаратов. В этом случае используется комбинация из 4 и более АГП. Однако в случаях резистентной АГ при добавлении каждого нового препарата необходимо контролировать их эффективность, и неэффективные АГП следует отменять, а не сохранять в рамках постепенного усиления многокомпонентной АГТ.
К рекомендуемым комбинациям трех антигипертензивных препаратов относятся: ИАПФ + АК + диуретик; БРА + АК + диуретик.
По показаниям, при наличии особых условий можно использовать и другие комбинации: ИАПФ + дигидропиридиновый АК + ББ; БРА + дигидропиридиновый АК + ББ; ИАПФ + диуретик + ББ; БРА + диуретик + ББ; дигидропиридиновый АК + диуретик + ББ.
Целевые уровни АД являются рекомендованными для достижения в каждой подгруппе пациентов, но важнейшим принципом их достижения является соблюдение безопасности и сохранения качества жизни пациента. Поэтому скорость достижения целевых значений и степень снижения АД может быть скорректирована у конкретного пациента в зависимости от конкретной клинической ситуации. При этом плохая переносимость снижения АД может быть основанием для более медленной титрации доз и числа назначаемых препаратов, равно как и при хорошей переносимости АД, может быть снижено до более низких значений, чем рекомендовано в среднем. Недостижение целевого АД в указанные сроки не является ошибочным, если это продиктовано клинической необходимостью. Если врач считает, что препятствием к достижению целевого АД является плохая приверженность пациента, это должно находить отражение в медицинской документации и должны быть предприняты и зафиксированы меры по повышению приверженности. В этих случаях недостижение целевого уровня не должно считаться дефектом оказания помощи.
- Пациентам, не достигшим целевого АД на фоне двойной комбинированной терапии, рекомендуется тройная комбинация, как правило, блокатора РААС с АК и тиазидовым/тиазидоподобным диуретиком, предпочтительно в форме фиксированной комбинации [135, 136].
ЕОК/ЕОАГ IА (УУР В, УДД 1)
- Пациентам с АГ, не достигшим целевого АД на фоне тройной комбинированной терапии, рекомендуется добавление спиронолактона (подробнее в разделе 3.6.11.) [106, 137, 138, 169].
ЕОК/ЕОАГ IB (УУР А, УДД 1)
Комментарии. При непереносимости спиронолактона рекомендуется назначение других диуретиков (эплеренона, хлорталидона, петлевых диуретиков, в т.ч в более высоких дозах), ББ, альфа-адреноблокаторов или препаратов центрального действия. [139].
- Всем пациентам с АГ не рекомендуется назначение комбинации двух блокаторов РААС вследствие повышенного риска развития гиперкалиемии, гипотензии и ухудшения функции почек [21, 139, 145, 146].
ЕОК/ЕОАГ IIIА (УУР A, УДД 1)
Основные классы препаратов для лечения артериальной гипертензии
Ингибиторы ангиотензинпревращающего фермента и антагонисты рецепторов ангиотензина II
ИАПФ и БРА — среди наиболее часто используемых классов антигипертензивных препаратов, обладающие сходной эффективностью в отношении сердечно-сосудистых осложнений и смертности по сравнению как друг с другом, так и с другими классами АГТ [59, 140–142]. БРА по сравнению с другими классами характеризуются более низкой частотой отмены из-за побочных эффектов, сопоставимой с плацебо [143, 144].
ИАПФ и БРА снижают альбуминурию в большей степени, чем другие антигипертензивные препараты, и эффективно замедляют прогрессирование диабетической и недиабетической ХБП [99]. По данным метаанализов, блокаторы РААС — единственные из всех антигипертензивных препаратов доказанно снижают риск терминальной ХБП.
ИАПФ и БРА эффективно предотвращают или приводят к обратному развитию ПОМ (ГЛЖ, ремоделирование мелких артерий) на фоне соответствующего снижения АД [140]. Оба препарата снижают риск пароксизмов ФП, что может быть обусловлено улучшением функции ЛЖ и более эффективным регрессом структурных изменений ЛЖ [140]. ИАПФ и БРА показаны пациентам с перенесенным ИМ, ХСНнФВ.
ИАПФ ассоциированы с умеренным повышением риска ангионевротического отека, особенно у представителей негроидной расы. У таких пациентов следует отдавать предпочтение БРА.
Для всех пациентов с АГ в связи с наличием абсолютных противопоказаний не рекомендуется назначение ИАПФ и БРА при беременности, высокой гиперкалиемии (≥5,5 ммоль/л), двухстороннем стенозе почечных артерий, стенозе почечной артерии единственной почки, у беременных и кормящих женщин и ангионевротическом отеке в анамнезе.
Блокаторы кальциевых каналов
Все АК метаболически нейтральны и не оказывают отрицательного действия на углеводный, липидный и пуриновый обмен. Помимо антигипертензивного, они оказывают антиангинальное и органопротективное действие, тормозят агрегацию тромбоцитов. В целом их влияние на СС риск схоже с другими классами антигипертензивных препаратов [59, 140]. При этом АК обладают большим эффектом в отношении профилактики инсультов, чем этого можно было ожидать только от антигипертензивного эффекта, однако они менее эффективны в отношении профилактики СНнФВ [59, 140].
Не рекомендуется (абсолютное противопоказание) назначение недигидропиридиновых АК при атриовентрикулярной блокаде 2–3-й степени, ХСН снизкой ФВ ЛЖ. Для дигидропиридиновых АК абсолютных противопоказаний нет.
Диуретики тиазидные и тиазидоподобные
Диуретики оказывают выраженный антигипертензивный эффект и остаются краеугольным камнем антигипертензивной терапии. Их эффективность в предотвращении всех вариантов СС осложнений и смертности подтверждена в РКИ и метаанализах [147]. Диуретики более эффективно предотвращают СН, чем другие классы препаратов [140]. В настоящее время ведутся дискуссии о том, следует ли предпочесть тиазидоподобные диуретики классическим тиазидным диуретикам, хотя их превосходство не было подтверждено в РКИ с прямым сравнением. Недавний метаанализ плацебо-контролируемых РКИ показал сходные эффекты трех типов диуретиков на СС исходы [147]. Таким образом, в отсутствие прямых сравнительных исследований и с учетом того, что гидрохлортиазид является компонентом многих фиксированных комбинаций, можно рекомендовать равноценное использование тиазидов, хлорталидона и индапамида.
И тиазидные, и тиазидоподобные диуретики снижают уровень сывороточного калия и имеют менее благоприятный профиль безопасности, чем блокаторы РААС [147, 148]. Они также могут способствовать повышению инсулинорезистентности и риска развития СД. Недавно проведенные исследования показали, что снизить негативное влияние тиазидов на метаболизм глюкозы можно добавлением калийсберегающего диуретика [149]. И тиазидные, и тиазидоподобные диуретики характеризуются снижением антигипертензивной эффективности при СКФ менее 45 мл/мин, а при СКФ менее 30 мл/мин препараты становятся неэффективными. В этом случае в качестве альтернативы следует использовать петлевые диуретики.
- У пациентов, не достигших целевого АД при приеме моно- или комбинированной АГТ, не включавшей диуретики, рекомендуется назначение низких доз тиазидных или тиазидоподобных диуретиков в составе комбинированной терапии с БРА, ИАПФ и АК для усиления АГЭ и достижения целевого АД [150–152].
ЕОК/ЕОАГ IB (УУР А, УДД 1)
Комментарии. Подагра и бессимптомная гиперурикемия являются абсолютным противопоказанием к назначению гидрохлортиазида и хлорталидона и относительным противопоказанием для индапамида.
Антагонисты минералокортикоидных рецепторов
АГЭ антагонистов минералокортикоидных рецепторов (АМКР) (спиронолактон, эплеренон) связан с тем, что они, имея стероидную структуру, конкурентно по отношению к альдостерону, связываются с его рецепторами, блокируя биологические эффекты альдостерона.
Cпиронолактон оказывает положительный эффект при сердечной недостаточности и резистентной АГ. Эплеренон также продемонстрировал положительный эффект при сердечной недостаточности и резистентной АГ и может использоваться как альтернатива спиронолактону. Для лечения АГ используются низкие суточные дозы АМКР (25–50 мг). Не рекомендуется (абсолютное противопоказание) назначение антагонистов альдостероновых рецепторов при нарушении функции почек с СКФ<30 мл/мин/1,73 м2 из-за повышения риска гиперкалиемии и ухудшения функции почек.
Бета-адреноблокаторы. АГЭ ББ обусловлена их способностью блокировать β1- и β2-адренорецепторы и уменьшать адренергическое влияние на сердце (снижение частоты и силы сердечных сокращений), а также снижать секрецию ренина (блокада β1-рецепторов юкстагломерулярного аппарата).
- ББ рекомендованы в качестве антигипертензивной терапии при наличии особых клинических ситуаций: например, стенокардии, перенесенного инфаркта миокарда, сердечной недостаточности [21, 22].
ЕОК ЕОАГ IA (УУР С, УДД 5)
Комментарии. ББ — один из пяти основных классов АГП. Предпочтительными ситуациями для их назначения являются симптомная стенокардия напряжения, перенесенный ИМ, ХСН с низкой фракцией выброса, ФП, аневризма аорты, контроль ЧСС, а также лечение АГ у женщин детородного возраста, особенно планирующих беременность. ББ — гетерогенный класс препаратов. В отдельных исследованиях продемонстрированы неодинаковые эффекты классических и вазодилатирующих ББ в отношении центрального АД, артериальной ригидности, риска развития СД, исходов при ХСН. РКИ по сопоставлению эффективности ББ с разными свойствами у пациентов с АГ не проводились. У физически активных пациентов и при наличии у них МС, НТГ рекомендованы ББ с вазодилатирующим эффектом, не оказывающие отрицательного влияния на инсулинорезистетность.
В многоцентровых исследованиях была показана несколько меньшая эффективность ББ по предупреждению инсульта в сравнении с другими АГП [153]. Однако все эти данные были получены при анализе исследований, где применялся атенолол. В отношении небиволола, карведилола и высокоселективных ББ (бисопролол и метопролол замедленного высвобождения) нет данных по влиянию на жесткие конечные точки [147].
Абсолютное противопоказание для назначения ББ — синоатриальная, атриовентрикулярная блокада 2–3-й степени, синдром слабости синусового узла и бронхиальная астма.
Другие (дополнительные) классы антигипертензивных препаратов
В целом антигипертензивные препараты, не относящиеся к пяти основным классам (например, препараты центрального действия, альфа-адреноблокаторы), не рекомендуются для рутинного применения при АГ, но остаются препаратами резерва, например, для применения при резистентной гипертензии при неэффективности остальных препаратов [21].
Агонисты имидазолиновых рецепторов (моксонидин) стимулируют имидазолиновые рецепторы, расположенные в вентролатеральном отделе продолговатого мозга. В отличие от других классов АГП, для моксонидина не проводились РКИ с использованием жестких конечных точек. С учетом результатов исследования ALMAZ [154], показавшего, что моксонидин повышает чувствительность тканей к инсулину у пациентов с избыточной массой тела, мягкой АГ и инсулинорезистентностью и нарушением углеводного обмена, назначение моксонидина возможно при ведении пациентов с АГ, ожирением и инсулинорезистентностью. Несмотря на отсутствие в рекомендациях данного класса препаратов среди основных, нет оснований для отмены такой терапии пациентам, которые уже получают данную группу препаратов при условии их хорошей эффективности и переносимости.
- Моксонидин для лечения АГ рекомендуется пациентам с МС или ожирением в комбинации с ИАПФ, БРА, АК и диуретиками при недостаточной эффективности классических комбинаций [154–156].
ЕОК/ЕОАГ нет (УУР B, УДД 3)
Комментарии. Не рекомендовано (абсолютное противопоказание) назначение агонистов имидазолиновых рецепторов при синдроме слабости синусового узла, синоатриальной, атриовентрикулярной блокаде 2–3-й степени, выраженной брадикардии с ЧСС менее 50 в минуту, ХСН (III–IV ФК).
Альфа-адреноблокаторы. Альфа-адреноблокаторы улучшают углеводный и липидный обмены, повышают чувствительность тканей к инсулину, улучшают почечную гемодинамику. Ввиду того, что эти препараты вызывают постуральную гипотензию, их с осторожностью применяют у пациентов с диабетической нейропатией и у пациентов старше 65 лет. Предпочтительным показанием для этого класса препаратов является наличие у пациентов с АГ доброкачественной гиперплазии предстательной железы.
- Альфа-адероноблокаторы рекомендуются при резистентной АГ (подробнее в разделе 3.6.11.), в качестве четвертого препарата к комбинации ИАПФ/БРА, АК, диуретика (при непереносимости спиронолактона**) [137].
ЕОК/ЕОАГ нет (УУР B, УДД 2)
Аппаратное лечение артериальной гипертензии
- Денервация почечных артерий (ренальная денервация) не рекомендована для лечения артериальной гипертензии в рутинной практике, пока не будет доступно больше данных относительно их эффективности и безопасности [157, 158].
ЕОК/ЕОАГ нет (УУР С, УДД 5)
Комментарии. Денервация почечных артерий может выполнятьсядля предотвращения эффектов симпатической нервной системы в отношении почечного сосудистого сопротивления, высвобождения ренина и реабсорбции натрия [159]. Для лечения пациентов с резистентной АГ были предложены минимально инвазивные методы катетерной денервации почек с помощью радиочастотной стимуляции, ультразвука или периваскулярной инъекции нейротоксичных веществ, например, этилового спирта [160]. Однако клинические данные относительно антигипертензивной эффективности ренальной денервации неоднозначны и требуют дальнейшего изучения.
Лечение артериальной гипертензии в отдельных клинических ситуациях
Артериальная гипертензия и сахарный диабет
- Пациентам с АГ в сочетании с СД рекомендуется начинать антигипертензивную терапию при значениях АД, измеренного в медицинском учреждении ≥140/90 мм рт. ст. [107, 157, 158]
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Пациентам с АГ в сочетании с СД, получающим АГП, в связи с доказанными преимуществами в снижении СС риска рекомендуется:
— в качестве целевого уровня снижать САД у пациентов моложе 65 лет до значений 130 мм рт. ст. и ниже при хорошей переносимости, но не ниже 120 мм рт. ст. [107, 157, 159]
ЕОК/ЕОАГ IА (УУР А, УДД 1)
— у пожилых пациентов (≥65 лет) с СД целевой уровень САД составляет 130–139 мм рт. ст. [107, 157, 160]
ЕОК/ЕОАГ IА (УУР А, УДД 1)
— целевой уровень ДАД у всех пациентов с АГ и СД составляет <80 мм рт. ст., но не ниже 70 мм рт. ст. [21, 22].
ЕОК/ЕОАГ IС (УУР С, УДД 5)
- Всем пациентам с АГ и СД рекомендуется начинать лечение с комбинации блокатора РААС с АК или тиазидным/тиазидоподобным диуретиком в связи с наилучшим влиянием этих комбинаций на частоту достижения целевого АД и снижение СС риска, а также нефропротективным потенциалом блокаторов РААС [106–107, 165].
ЕОК/ЕОАГ IА (УУР А, УДД 2)
Комментарии. Сочетание СД и АГ заслуживает особого внимания, поскольку оба заболевания существенно увеличивают риск развития микро- и макрососудистых поражений, включая диабетическую нефропатию, инсульт, ИБС, ИМ, ХСН, атеросклероз периферических артерий, и способствуют увеличению СС смертности. При лечении пациентов АГ с СД необходимо контролировать все имеющиеся у пациента ФР, включая дислипидемию (назначение гиполипидемической терапии). Развитие диабетической нефропатии сопровождается очень высоким риском развития ССО, при этом необходимы контроль АД и уменьшение протеинурии до минимально возможных значений.
Артериальная гипертензия и хроническая болезнь почек
- Пациентам с ХБП рекомендуется начинать лечение (изменение образа жизни и лекарственную терапию) вне зависимости от наличия сахарного диабета при уровне АД, измеренного в медицинском учреждении, ≥140/90 мм рт. ст. (Приложение Б3) [165, 166].
ЕОК/ЕОАГIА (УУР С, УДД 4)
- Пациентам с диабетической и недиабетической ХБП рекомендуется снижать САД до значений 130–139 мм рт. ст. в связи с доказанными преимуществами в снижении риска сердечно-сосудистых событий [168].
ЕОК/ЕОАГ IА (УУР С, УДД 4)
Комментарии. Следует назначать индивидуализированную терапию в зависимости от ее переносимости и влияния на функцию почек и уровень электролитов
- Блокаторы РААС рекомендуются в качестве компонента терапевтической стратегии при наличии альбуминурии высокой степени или протеинурии, как более эффективные препараты для уменьшения выраженности альбуминурии [167, 168].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Всем пациентам с АГ и ХБП в качестве начальной терапии рекомендуется комбинация блокатора РААС с АК или диуретиком в связи с наилучшим влиянием данных комбинаций на частоту достижения целевого АД и снижение СС риска [165].
ЕОК/ЕОАГ IА (УУР А, УДД 2)
Комментарии. АГ является важнейшим фактором риска развития и прогрессирования хронической болезни почек (ХБП) любой этиологии; адекватный контроль АД замедляет ее развитие. В свою очередь, ХБП является важным независимым фактором риска развития и прогрессирования ССЗ, в том числе фатальных. У пациентов, получающих почечную заместительную терапию гемодиализом, АГ существенно влияет на выживаемость. Для ведения таких пациентов крайне важно точное и правильное измерение АД, однако АД до сеанса гемодиализа может не отражать средний уровень АД, так как большие колебания натрия и воды в организме способствуют большей вариабельности АД. Доказано, что АД, измеренное методом ДМАД, более информативно, чем показатели АД перед сеансом гемодиализа.
У пациентов с терминальной стадией ХБП, находящихся на диализе, снижение САД и ДАД сопровождается уменьшением частоты СС осложнений и общей смертности. Пациентам, находящимся на гемодиализе, можно назначать все АГП, при этом их дозы зависят от стабильности гемодинамики и способности конкретного препарата проходить через диализные мембраны. Петлевые диуретики — препараты выбора среди диуретиков при терминальной ХБП.
При использовании АМКР, особенно в комбинации с блокатором РААС, необходим более тщательный контроль функции почек и уровня калия (опасность гиперкалиемии).
Артериальная гипертензия и ишемическая болезнь сердца
Пациентам с АГ в сочетании с ИБС рекомендуется:
- Пациентам моложе 65 лет, без ХБП, получающим антигипертензивную терапию, в связи с доказанными преимуществами в снижении риска СС событий рекомендуется снижать САД до целевого уровня ≤130 мм рт. ст. при хорошей переносимости, но не <120 мм рт. ст. (Приложение Б4) [157, 170].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- У пожилых пациентов (≥65 лет) и/или с наличием ХБП рекомендовано снижать САД до целевых значений 130–139 мм рт. ст. [157, 170].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Снижать ДАД до целевых значений <80 мм рт. ст., но не <70 мм рт. ст. [299]
ЕОК/ЕОАГ IА (УУР А, УДД 3)
- Пациентам с АГ с перенесенным инфарктом миокарда рекомендуется назначение ББ и блокаторов РААС в качестве составной части терапии для снижения риска СС смертности [171].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Пациентам с АГ и симптомами стенокардии рекомендуется назначение ББ и/или АК. [171].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
Артериальная гипертензия, гипертрофия левого желудочка и сердечная недостаточность
- Пациентам с АГ в сочетании с сердечной недостаточностью (СН) (с низкой или сохраненной фракцией выброса) рекомендуется назначение АГТ при уровне АД ≥140/90 мм рт. ст. в связи с доказанными преимуществами в отношении снижения СС смертности [172].
ЕОК/ЕОАГ IIaB (УУР C, УДД 5)
Комментарии. У пациентов с АГ и СН с сохранной функцией левого желудочка при назначении АГТ возможно использование всех основных лекарственных средств, поскольку ни один из препаратов не продемонстрировал свое превосходство над другими в отношении улучшения СС исходов [21, 22].
- Пациентам с АГ в сочетании с СН со сниженной ФВ в качестве АГТ рекомендуется использовать ИАПФ или БРА, а также ББ, диуретиков и/или АМКР при необходимости [171, 173] (Приложение Б5).
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- При недостаточном контроле АД пациентам с СН и АГ рекомендуется рассмотреть возможность добавления к терапии дигидропиридиновых АК для достижения целевого АД [21, 22].
ЕОК/ЕОАГ IIbC (УУР C, УДД 5)
- Пациентам с АГ и СН с сохраненной ФВ рекомендуется руководствоваться теми же пороговыми и целевыми значениями АД, что и при сниженной ФВ [174–176].
ЕОК/ЕОАГ IIaB (УУР С, УДД 5)
- Всем пациентам с ГЛЖ рекомендуется назначение блокаторов РААС в комбинации с АК или диуретиком в связи с доказанным влиянием на процессы ремоделирования ЛЖ [177].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- У пациентов с АГ и ГЛЖ моложе 65 лет и при отсутствии ХБП рекомендуется снижать САД до значений 120–130 мм рт. ст. в связи с доказанными преимуществами в отношении снижения СС исходов и смертности [107, 178–180].
ЕОК/ЕОАГ IIaB (УУР А, УДД 1)
Артериальная гипертензия, фибрилляция предсердий и другие аритмии
Ведение пациентов с АГ в сочетании с фибрилляцией предсердий проводится в соответствии с действующими клиническими рекомендациями.
- Всех пациентов с ФП рекомендуется обследовать для исключения АГ [181].
ЕОК/ЕОАГ IC (УУР C, УДД 5)
- Пациентам с АГ и ФП при необходимости контроля ЧСС в качестве компонента АГТ рекомендуется назначать ББ или недигидропиридиновые АК (Приложение Б6) [181].
ЕОК/ЕОАГ IIaB (УУР C, УДД 5)
Комментарии. Индивидуальный выбор доз ББ или недигидропиридиновых АК препаратов должен быть ориентирован на целевые значения ЧСС не выше 110 в минуту в состоянии покоя [182].
- Пациентам с АГ в сочетании с ФП при числе баллов по шкале CHA2DS2-Vasc ≥2 для мужчин и ≥3 для женщин рекомендуется проводить профилактику инсульта с помощью пероральных антикоагулянтов (шкала предсталена в Таблице 4, Приложение Г3) [183].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Назначение пероральных антикоагулянтов рекомендовано пациентам с ФП, имеющим 1 балл по шкале CHA2DS2-VASc, учитывая индивидуальные особенности и предпочтения пациента [182,184].
ЕОК/ЕОАГ IIaB (УУР C, УДД 5)
Комментарии. Развитие ФП у пациентов АГ ухудшает прогноз заболевания, значимо повышает риск развития инсульта (кардиоэмболического генеза) и сердечной недостаточности. АГ — самое распространенное сопутствующее заболевание у пациентов с ФП. В отсутствие противопоказаний пациенты ФП должны получать пероральные антикоагулянты для профилактики инсульта и других эмболий. Адекватный контроль АГ у пациентов, получающих антикоагулянты, способствует снижению частоты кровотечений. Оральные антикоагулянты следует применять с осторожностью у пациентов со значительно повышенным АД (САД ≥180 мм рт. ст. и/или ДАД ≥100 мм рт. ст.), при этом необходимо применить срочные меры для достижения контроля АД; целью является снижение САД как минимум <140 мм рт. ст., ДАД <90 мм рт. ст. Целесообразно оценить возможность снижения САД до <130 мм рт. ст. [181, 185].
Артериальная гипертензия и цереброваскулярная болезнь
- Пациентам с внутримозговой гематомой и САД < 200 мм рт. ст. не рекомендуется незамедлительное снижение АД для профилактики осложнений (в том числе гипоперфузии головного мозга или увеличения размеров очага поражения) [186-192].
ЕОК/ЕОАГ IIIA (УУР A, УДД 2)
- Пациентам с внутримозговой гематомой при САД ≥220 мм рт. ст. рекомендовано осторожное снижение АД до уровня <180 мм рт. ст. с помощью в/в терапии для профилактики осложнений (в том числе гипоперфузии головного мозга или увеличения размеров очага поражения) [191, 192].
ЕОК/ЕОАГ IIaB (УУР С, УДД 5)
- Пациентам c острым ишемическим инсультом рутинное снижение АД не рекомендуется для профилактики осложнений (в том числе гипоперфузии головного мозга) [190-195].
ЕОК/ЕОАГ IIIA (УУР A, УДД 1)
- Пациентам с острым ишемическим инсультом, которым планируется проведение внутривенной тромболитической терапии, АД рекомендуется осторожно снизить и поддерживать на <180/105 мм рт. ст. в течение как минимум 24 часов после тромболизиса в связи с доказанными преимуществами в отношении прогноза неврологического восстановления [193, 196, 197].
ЕОК/ЕОАГ IIaB (УУР С, УДД 3)
- Пациентам с САД ≥ 220 и/или ДАД ≥120 мм рт. ст., которым не проводился тромболизис, рекомендуется рассмотреть возможность целесообразности лекарственной терапии с целью снижения АД на 15% в течение первых суток после инсульта принимается на основании оценки клинической ситуации [21, 22, 193].
ЕОК/ЕОАГ IIbC (УУР C, УДД 5)
- Пациентам с АГ, перенесшим острое цереброваскулярное нарушение, с целью сокращения риска повторного острого нарушения мозгового кровообращения (ОНМК) назначение АГТ рекомендовано сразу после транзиторной ишемической атаки (ТИА) и через несколько дней после ишемического инсульта [185, 198, 199].
ЕОК/ЕОАГ IА (УУР С, УДД 4)
- Всем пациентам с АГ после ишемического инсульта или ТИА моложе 65 лет и без ХБП рекомендуется снижать САД до целевых значений 120–130 мм рт. ст. в связи с доказанными преимуществами в отношении снижения СС смертности [108, 185, 199, 200].
ЕОК/ЕОАГ IIaB (УУР B, УДД 2)
- АГТ, направленная на снижение риска инсульта и рекомендованная всем пациентам с ЦВБ, включает блокатор РААС в сочетании с АК или тиазидоподобным диуретиком [108, 153, 198].
ЕОК/ЕОАГ IA (УУР А, УДД 1)
Комментарии. У пациентов АГ с ЦВБ (дисциркуляторная энцефалопатия II–III степени и/или ТИА/инсульт в анамнезе, гемодинамически значимый стеноз магистральных брахиоцефальных артерий) не следует резко снижать АД, так как у части пациентов может быть плохая индивидуальная переносимость более низких уровней АД вследствие нарушения ауторегуляции сосудов головного мозга. У этих пациентов целесообразно применение этапной (ступенчатой) схемы снижения АД.
Артериальная гипертензия у пациентов с заболеванием периферических артерий
- Пациентам с АГ в сочетании с периферическим атеросклерозом, учитывая высокий риск инфаркта миокарда, инсульта, сердечной недостаточности и сердечно-сосудистой смерти, рекомендуется назначение АГТ с достижением целевого АД <140/90 мм рт. ст. [21, 22, 107, 171, 201–203].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Всем пациентам с АГ в сочетании с атеросклерозом периферических артерий в качестве начальной терапии рекомендуется назначать комбинацию блокатора РААС и АК или диуретика [21, 22, 201, 202].
ЕОК/ЕОАГ IIaВ (УУР А, УДД 1)
- Пациентам с атеросклерозом сонных артерий рекомендуется назначать АК и блокаторы РААС, так как препараты данных групп более эффективно замедляют прогрессирование атеросклероза, чем диуретики и ББ [21, 22, 201–205].
ЕОК/ЕОАГ нет (УУР А, УДД 1)
Комментарии. На основании данных РКИ установлено, что контроль АГ замедляет прогрессирование атеросклероза сонных артерий. АК, ИАПФ и их комбинация в этом случае более эффективны, чем диуретики и ББ [204, 205]. Следует учитывать, что пациенты с каротидным атеросклерозом имеют высокий риск атероэмболического инсульта и СС осложнений, в связи с чем АГТ должна сочетаться с назначением статинов и антитромбоцитарных препаратов. Снижение АД у пациентов с двусторонним стенозом сонных артерий следует проводить осторожно, начиная с монотерапии и тщательно отслеживая побочные эффекты [21, 22].
- У пациентов с периферическим атеросклерозом рекомендуется рассмотреть возможность назначения ББ в качестве АГТ, особенно при наличии показаний к их применению для снижения выраженности симптоматики [21, 22].
ЕОК/ЕОАГ IIbC (УУР С, УДД 5)
Артериальная гипертензия у пациентов с заболеваниями легких
- Пациентам с АГ в сочетании с бронхиальной астмой (БА) и/или ХОБЛ с целью достижения целевого уровня АД в качестве стартовой АГТ не рекомедовано назначение ББ, рекомендуется назначение блокаторов РААС и АК [206–211].
ЕОК/ЕОАГ нет (УУР B, УДД 1)
Комментарии. Сочетание АГ с ХОБЛ и/или бронхиальной астмой обуславливает особенности проведения АГТ.
Пациентам с БА и/или ХОБЛ назначение петлевых и тиазидных диуретиков требует осторожности, в связи с высокой вероятностью развития гипокалиемии при их совместном применении с β2-агонистами и особенно — системными стероидами.
ББ могут стать причиной развития бронхоспазма, особенно неселективные, в связи с чем не должны рутинно назначаться пациентам с ХОБЛ и противопоказаны пациентам с БА. Ряд исследований, проведенных у ограниченного числа пациентов, показали, что применение небольших доз высокоселективных ББ не ухудшает и может даже несколько улучшать бронхиальную проходимость [210].
Применение АК у пациентов с ХОБЛ и/или БА безопасно и даже способствует снижению гиперреактивности бронхов и повышению бронходилатирующего эффекта β2-агонистов. Таким образом, наравне с изменением образа жизни (в первую очередь — отказом от курения) в качестве стартовой АГТ предопочтительно использование блокаторов РААС и АК. При недостижении целевого АД или наличии сопутствующих заболеваний с соответствующими показаниями можно рассмотреть добавление/назначение тиазидных или тиазидоподобных диуретиков и высокоселективных ББ [21, 22].
Пациенты с АГ с бронхообструктивной патологией часто применяют бронхолитические и глюкокортикостероидные (ГКС) препараты. Системное и длительное применение ГКС способствует повышению АД. При применении ингаляционных ГКС подобные эффекты незначительны.
Артериальная гипертензия и синдром обструктивного апноэ сна
- Для улучшения контроля АГ у пациентов с синдромом обструктивного апноэ во время сна (СОАС) рекомендуется применение CPAP (“сипап”) — терапии (от англ. Constant Positive Airway Pressure), заключающейся в создании непрерывного положительного давления в дыхательных путях аппаратным методом) [21].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. СОАС характеризуется периодическим спадением верхних дыхательных путей на уровне глотки и прекращением легочной вентиляции при сохраняющихся дыхательных усилиях во время сна с последовательным снижением насыщения кислородом крови, грубой фрагментацией сна и выраженной дневной сонливостью. При СОАС, особенно тяжелой степени (индекс апноэ/гипопноэ >30), происходит активация СНС, что приводит к повышению или недостаточному снижению АД в ночные часы, развитию эндотелиальной дисфункции, оксидативного стресса и увеличению риска развития ССО. На наличие СОАС должны быть обследованы пациенты с АГ с ожирением, резистентностью к АГТ, у которых по результатам СМАД имеется недостаточное снижение или повышение АД в ночные часы. Признаками, позволяющими заподозрить СОАС, являются: беспокойный, «неосвежающий» сон; учащенное ночное мочеиспускание; дневная сонливость; разбитость, утренние головные боли; хроническая усталость; снижение памяти и внимания; громкий, прерывистый храп; остановки дыхания во сне; увеличение массы тела и снижение потенции.
Для скрининга СОАС можно использовать опросник шкалы сонливости по Эпфорт (Epworth Sleepiness Scale) (Таблица П5, Приложение Г3), компьютерную пульсоксиметрию.
Для постановки диагноза и оценки степени тяжести СОАС проводится респираторное или кардиореспираторное мониторирование. Золотой стандарт выявления СОАС — полисомнографическое исследование.
Лечение пациентов с СОАС включает снижение веса у пациентов с ожирением, отказ от курения, приема транквилизаторов и снотворных препаратов, а также проведение мероприятий, направленных на обеспечение свободного носового дыхания. Основной метод лечения пациентов с СОАС — CPAP терапия (создание постоянного положительного давления воздуха в дыхательных путях — Continuous Positive Airways Pressure). При CPAP терапии поток нагнетаемого под давлением воздуха предотвращает спадение верхних дыхательных путей. Для СРАР терапии применяются аппараты с индивидуальными режимами вентиляции, обеспечивающими максимально эффективное их использование [212].
Артериальная гипертензия в периоперационном периоде
- При впервые выявленной АГ перед плановым хирургическим вмешательством рекомендуется провести обследование в объеме, предусмотренном п. 2 данных рекомендаций, с целью выявления ПОМ и оценки CC риска [21].
ЕОК/ЕОАГ IС (УУР C, УДД 5)
- Всем пациентам с АГ рекомендуется избегать существенных колебаний АД (более 10%) в периоперационном периоде [21, 213, 214].
ЕОК/ЕОАГ IС (УУР B, УДД 2)
Комментарии. Можно не откладывать некардиохирургическое вмешательство у пациентов с АГ 1–2-й степени (САД<180 мм рт. ст. и ДАД <110 мм рт. ст.) [21].
- Пациентам с АГ, длительно получающим ББ, рекомендуется продолжить терапию в периоперационном периоде для контроля АД. [215, 216].
ЕОК/ЕОАГ IВ (УУР А, УДД 3)
- Резкая отмена ББ или препаратов центрального действия (например, клонидина) потенциально опасна и не рекомендуется [217, 218].
ЕОК/ЕОАГ IIIВ (УУР С, УДД 4)
- Пациентам с АГ перед некардиохирургическим вмешательством для снижения риска интраоперационной гипотензии рекомендуется временная отмена блокаторов РААС [21].
ЕОК/ЕОАГ IIaC (УУР С, УДД 5)
Резистентная артериальная гипертензия
Резистентная к терапии АГ (т.е. резистентная АГ) устанавливается на основании следующих критериев:
— соблюдение мероприятий по изменению образа жизни и лечение с использованием оптимальных (или максимальных переносимых) доз трех и более лекарственных препаратов, включая ингибитор АПФ или БРА, АК и диуретик не приводит к снижению САД и ДАД до значений <140 мм рт. ст. и/или <90 мм рт. ст. соответственно;
— неадекватность контроля АД подтверждена с помощью СМАД и/или ДМАД;
— подтверждена приверженность пациента к лечению
— исключены причины псевдорезистентности и причины вторичной АГ.
Прежде чем диагностировать резистентную АГ, необходимо исключить причины псевдорезистентности:
— низкая приверженность к назначенной терапии является частой причиной псевдорезистентности, она выявляется у ≤50% пациентов, которых обследовали с помощью методов прямого мониторинга контроля приема препаратов, этот показатель прямо зависит от количества назначенных таблеток [219].
— феномен «белого халата» (при котором АД, измеренное в медицинском учреждении, повышено, но по данным СМАД или ДМАД уровень АД контролируется) встречается нередко, в связи с чем рекомендуется подтвердить наличие АГ с помощью СМАД или ДМАД до установления диагноза резистентной АГ.
— нарушение правил измерения АД в медицинском учреждении, включая использование манжеты меньшего размера, может привести к ложному выявлению повышенного АД.
— выраженный кальциноз плечевой артерии, особенно у пожилых пациентов.
— клиническая инертность, приводящая к назначению нерациональных комбинаций и неадекватных доз АГП.
Другие причины резистентной гипертензии:
— образ жизни, включая ожирение или быструю прибавку веса, чрезмерное употребление алкоголя или поваренной соли.
— применение вазопрессоров или веществ, способствующих задержке натрия, препаратов, назначенных по поводу сопутствующих заболеваний, растительных препаратов, употребление наркотиков (кокаин и т.п.) или анаболических стероидов
— СОАС
— выраженное ПОМ, особенно ХБП или жесткость крупных артерий [21, 22].
Истинная резистентная АГ встречается, не более чем в 10% случаев среди всей популяции пациентов АГ, однако в отдельных группах пациентов, например, с ХБП, ее распространенность может доходить до 30% [21,220]. Истинная резистентная АГ часто наблюдается у пациентов с ожирением, метаболическим синлромом, СД, СОАС, множественным ПОМ, при вторичных формах АГ. Тяжелое ПОМ (выраженная ГЛЖ, снижение функции почек, атеросклеротическое поражение артерий) способствует развитию резистентности к лечению.
- Всем пациентам с резистентной АГ рекомендовано усиление мероприятий по изменению образа жизни, особенно ограничение употребления соли с целью достижения целевого уровня АД [221].
ЕОК/ЕОАГ IВ (УУР В, УДД 2)
- Всем пациентам с резистентной АГ рекомендовано добавление к проводимой терапии спиронолактона** в дозах 25-50 мг/сут для достижения целевого уровня АД [137, 222, 223].
ЕОК/ЕОАГ IВ (УУР А, УДД 1)
Комментарии. При непереносимости спиронолактона рекомендовано добавление других диуретиков, включающих эплеренон, более высокие дозы тиазидных/тиазидоподобных диуретиков, или петлевые диуретики, или добавление бисопролола или доксазозина. Применение спиронолактона, эплеренона противопоказано пациентам с СКФ ≤ 30 мл/мин и концентрацией калия в плазме ≥ 5 ммоль/л из-за риска гиперкалиемии. Петлевые диуретики следует использовать вместо тиазидных/тиазидоподобных при СКФ <30 мл/мин.
Артериальная гипертензия «белого халата»
- Пациентам с АГ «белого халата» рекомендуется проводить мероприятия по изменению образа жизни, направленные на уменьшение СС риска [21, 22].
ЕОК/ЕОАГ IС (УУР А, УДД3)
- Всем пациентам с АГ «белого халата» рекомендуется проводить регулярные обследования (не менее 1 раза в 2 года) с периодическим мониторированием АД, вне медицинского учреждения [21, 22, 224–230].
ЕОК/ЕОАГ IС (УУР B, УДД 2)
Комментарии. АГ «белого халата» диагностируется при выявлении повышенного АД, измеренного в медицинском учреждении и нормальных показателей АД, измеренного вне медицинского учреждения. АГ «белого халата» может иметь место у многих людей с повышением клинического АД, особенно с АГ 1-й степени, а также у очень пожилых пациентов (>50%) [21, 22]. По сравнению со здоровыми лицами АГ «белого халата» ассоциируется с более высокой распространенностью метаболических факторов риска и ПОМ. Она также ассоциирована с более высоким риском развития сахарного диабета типа 2 и устойчивой АГ, а также с повышенным сердечно-сосудистым риском [227–230]. Различают «эффект белого халата», являющийся дополнительным прессорным ответом (реакцией) у пациента с АГ на измерение АД (реакция тревоги), чаще наблюдаемый в условиях медицинской организации.
- Для пациентов с АГ «белого халата» рекомендуется рассмотреть возможность медикаментозной антигипертензивной терапии при наличии признаков ПОМ или высоком/очень высоком СС риске (раздел 2.3, Таблица П11, Приложение Г2 и Таблица П12, Приложение Г2) [21, 22].
ЕОК/ЕОАГ IIbC (УУР C, УДД 5)
Комментарии. Для остальных пациентов с АГ «белого халата» рутинная медикаментозная терапия не рекомендована [21, 22].
«Маскированная» артериальная гипертензия
«Маскированная» гипертензия (МГ) (скрытая гипертензия) диагностируется у пациентов с нормальными показателями АД, измеренного в медицинском учреждении, но с повышенными значениями АД, измеренного вне медицинского учреждения. У таких пациентов метаболические факторы риска и ПОМ, встречается чаще, чем у пациентов с истинной нормотензией [37, 228–231]. Проблему представляет диагностика «маскированной» АГ, поскольку большинство скрининговых программ основано на использовании показателей АД, измеренного в медицинском учреждении, которое является нормальным. «Маскированная» АГ чаще встречается у молодых пациентов, чем у пожилых, а также у тех, чьи показатели клинического АД находятся в пределах значений высокого нормального АД (130–139/80–89 мм рт. ст.). Она редко встречается у лиц с показателями клинического АД <130/80 мм рт. ст. «Маскированная» АГ ассоциируется с повышением риска прогрессирования заболевания до стойкой АГ, повышенной частотой развития СД типа 2 и наличием ПОМ [21, 22]. Уровень отдаленного риска развития фатальных и нефатальных СС событий приближается к значению этого показателя у пациентов с устойчивой АГ [37, 38, 98, 232–233].
- Всем пациентам с «маскированной» АГ рекомендуются мероприятия по изменению образа жизни с целью уменьшения СС риска [21, 22].
ЕОК/ЕОАГ IС (УУР C, УДД 5)
- Всем пациентам с «маскированной» АГ рекомендуется регулярное наблюдение, включающее периодическое мониторирование показателей АД, измеренного вне медицинского учреждения [21, 22, 230, 232].
ЕОК/ЕОАГ IС (УУР C, УДД 4)
- Всем пациентам с «маскированной» АГ рекомендуется проведение антигипертензивной медикаментозной терапии, учитывая прогностическое значение высоких значений АД, измеренного вне медицинского учреждения [38, 228, 232].
ЕОК/ЕОАГ IIaC (УУР А, УДД 2)
- Пациентам с неконтролируемой «маскированной» АГ (не достигнут контроль АД, измеренного вне медицинского учреждения), получающим медикаментозное лечение, рекомендуется усиление АГТ с целью снижения СС риска [230, 232].
ЕОК/ЕОАГ IIaC (УУР А, УДД 2)
Артериальная гипертензия у молодых пациентов (<50 лет)
АГ у молодых пациентов характеризуется более высокой частотой повышения ДАД и изолированной диастолической АГ [97]. При обследовании пациентов этой возрастной группы, особенно при наличии тяжелой АГ, следует учитывать, что вероятность обнаружения вторичной гипертензии, может достигать 10% [21].
- Всем пациентам моложе 50 лет при наличии АГ 2 и 3 степени, а также АГ 1 степени в сочетании с множественными ФР, ПОМ, СД, сердечно-сосудистыми, цереброваскулярными или почечные заболеваниями следует назначать АГТ одновременно с рекомендациями по изменению образа жизни в соответствии с общими принципами[21].
ЕОК/ЕОАГ нет (УУР С, УДД 5)
Комментарии.В связи с тем, что ранее назначение АГТ может предотвратить более тяжелую АГ и развитие ПОМ в будущем, молодым пациентам с АГ 1 степени при отсутствии ФР, ПОМ и ССЗ можно обсуждать назначение АГТ наравне с изменениями образа жизни [21]. При этом целевой уровень АД составляет 120-130/70-79 мм рт. ст. (см. раздел 3.2). В случае, если принимается решение о немедикаментозной коррекции АД или пациент отказывается принимать АГТ, необходимо дать подробные рекомендации по изменению образа жизни и длительно наблюдать пациента, так как со временем АД неизбежно будет расти [21].
Артериальная гипертензия у пожилых пациентов (≥65 лет)
- У пациентов 65 лет и старше с АГ, обратившихся за медицинской помощью в учреждения амбулаторного или стационарного типа, рекомендуется проводить скрининг синдрома старческой астении с использованием опросника «Возраст не помеха» (Приложение Г3, таблица П6), поскольку выявление старческой астении может влиять на тактику АГТ и уровень целевого АД [9].
ЕОК/ЕОАГ нет (УУР А, УДД 1)
- Пациентам >65 лет с АГ рекомендуется назначение антигипертензивной терапии с использованием любого из основных классов АГП [238, 239].
ЕОК/ЕОАГ нет (УУР В, УДД 1)
Комментарии. Пациенты старше 65 лет должны получать АГТ в соответствии с общим алгоритмом, приведенном в Приложении Б2. У пациентов очень пожилого возраста (>80 лет) может быть целесообразно начинать лечение с монотерапии. У всех пожилых пациентов комбинированную терапию следует начинать с минимальных доз препаратов. При отсутствии дополнительных показаний следует избегать назначения петлевых диуретиков и альфа-адреноблокаторов, так как они увеличивают риск падений [240, 241]. При лечении пожилых пациентов целевое АД составляет 130-139/70-79 мм рт. ст. при переносимости [21].
До назначения и в процессе приема АГТ необходим тщательный мониторинг функции почек для выявления ее возможного ухудшения вследствие АД-обусловленного снижения почечной перфузии. Всех пациентов 65 лет и старше, особенно старше 80 лет, и пациентов со старческой астенией необходимо тщательно наблюдать на предмет возможного развития ортостатической гипотензии (при необходимости — использовать СМАД) и мониторировать переносимость и развитие возможных побочных эффектов [21]. Не рекомендуется отмена медикаментозной АГТ на основании возраста, даже при достижении 80 лет, при условии, что лечение хорошо переносится.
При лечении пациентов 65 лет и старше необходимо учитывать методические рекомендации МР 103 «Фармакотерапия у пациентов пожилого и старческого возраста».
Изолированная систолическая артериальная гипертензия
Изолированная систолическая АГ: повышение САД ≥140 мм рт. ст. при ДАД <90 мм рт. ст.
Наиболее распространена у пожилых пациентов (до 29,4%), может встречаться и у пациентов молодого (1,8% среди пациентов 18–39 лет) и среднего возраста (6% среди пациентов 40–60 лет) [242, 243]. В основе развития ИСАГ лежат артериолосклероз и повышение артериальной ригидности, эндотелиальная дисфункция, провоспалительная активность, кальцификация эластина. Наблюдается у пожилых, пациентов с СД, ХБП, остеопорозом с кальцификацией сосудов [244]. ИСАГ независимо ассоциирована с риском неблагоприятных СС исходов и смертности [245, 246].
Пороговым значением САД для начала АГТ является ≥140 мм рт. ст. Лечение пациентов с ИСАГ проводят в соответствии с алгоритмом антигипертензивной терапии, при этом необходимо ориентироваться на уровень САД, а нормальное значение ДАД не должно препятствовать назначению оптимального лечения для достижения целевого САД [21, 31].
Помимо истинной ИСАГ, у некоторых молодых здоровых людей, чаще у мужчин, может выявляться ложная ИСАГ 1-й степени, сопровождающаяся нормальными показателями центрального САД за счет чрезмерной амплификации периферического САД [247]. Показано, что у молодых пациентов с ИСАГ сердечно-сосудистый риск аналогичен риску пациентов с высоким нормальным АД, причем, риск развития ИСАГ ассоциирован с курением [248].
На основании имеющихся данных молодым пациентам с изолированной систолической АГ 1-й степени следует рекомендовать мероприятия по изменению образа жизни (особенно прекращение курения); необходимость назначения АГТ на настоящий момент не доказана; показано длительное наблюдение, поскольку у многих из них в дальнейшем возможно развитие стойкой АГ [21].
Артериальная гипертензия при беременности и лактации
Выделяют следующие клинические варианты АГ при беременности [21]:
— АГ, развившаяся до беременности (хроническая АГ — ХАГ) — АГ, определяемая до беременности или проявившаяся до 20 нед. беременности и персистирующая более 6 недель после родов. АГ, диагностированная после 20-й недели гестации и не исчезнувшая в течение 6 недель после родов, также классифицируется как существовавшая ранее АГ, но уже ретроспективно;
— Гестационная артериальная гипертензия (ГАГ) — состояние, индуцированное беременностью и проявляющееся повышением АД ≥140/90 мм рт. ст. впервые после 20 нед., со спонтанной нормализацией АД в течение 6 нед. после родов АД;
— Преэклампсия (ПЭ) — гестационная АГ с протеинурией >300 мг/сут или альбумин/креатинин в разовой порции мочи >30 мг/ммоль, в ряде случаев с проявлениями полиорганной недостаточности.
— ХАГ, осложненная преэклампсией.
- Беременным женщинам, имеющим ФР, ПОМ, СД или поражение почек, рекомендуется проведение СМАД для подтверждения АГ [43, 228].
ЕОК/ЕОАГ нет (УУР B, УДД 1)
- Женщинам с гестационной АГ, преэклампсией или хронической АГ, сопровождающейся субклиническим ПОМ, рекомендуется начинать лекарственную терапию при САД ≥140 мм рт. ст. или ДАД ≥90 мм рт. ст. с целью снижения СС риска [21, 22].
ЕОК/ЕОАГ IС (УУР C, УДД 5)
- Беременным женщинам с повышением АД без наличия признаков ПОМ, преэклампсии и АКС с целью снижения СС риска начало лекарственной терапии рекомендуется при САД ≥150 мм рт. ст. или ДАД ≥95 мм рт. ст. [21, 22].
ЕОК/ЕОАГ IС (УУР C, УДД 5)
Комментарии. Цель лечения беременных с АГ — предупредить развитие осложнений, обусловленных высоким уровнем АД, обеспечить сохранение беременности, нормальное развитие плода и успешные роды. Целевой уровень АД для беременных <140/90 мм рт. ст. Следует не допускать развития эпизодов гипотонии, чтобы не ухудшить плацентарный кровоток.
- Беременных женщин с САД ≥ 170 и ДАД ≥ 110 мм рт. ст. рекомендуется срочно госпитализировать и расценивать данное состояние как гипертонический криз [21, 22].
ЕОК/ЕОАГ IС (УУР C, УДД 5)
Комментарии. Главное правило при лечении гипертонического криза (ГК)у беременных — контролируемое снижение САД до <160 И ДАД до <105 мм рт. ст. Для пероральной терапии следует использовать метилдопу или нифедипин замедленного высвобождения. Для лечения преэклампсии с отеком легких препаратом выбора является нитроглицерин, длительность его применения не должна составлять более 4 часов, из-за отрицательного воздействия на плод и риска развития отека мозга у матери. Применение диуретиков не показано, т.к. при преэклампсии уменьшается объем циркулирующей крови. Для предотвращения эклампсии и лечения судорог рекомендовано в/в введение сульфата магния.
- Женщинам с высоким риском преэклампсии с целью ее профилактики рекомендуется назначать малые дозы (150 мг) аспирина с 12-й недели беременности и до 36-й недели, при условии низкого риска желудочно-кишечных кровотечений [236].
ЕОК IA (УУР В, УДД 2)
Комментарии. Высокий риск преэклампсии отмечается у женщин с АГ во время предыдущей беременности, ХБП, аутоиммунными заболеваниями (системной красной волчанкой или антифосфолипидным синдромом), СД 1-го или 2-го типа, хронической АГ; к умеренному — первая беременность, возраст ≥40 лет, интервал между беременностями более 10 лет, ИМТ ≥35 кг/ м2 на первом визите, семейный анамнез преэклампсии и многоплодная беременность.
- Беременным женщинам с АГ в качестве АГТ с целью контроля уровня АД рекомендуется назначение лекарственных препаратов с замедленным высвобождением лекарственного вещества (метилдопа**) [237, 250].
ЕОК/ЕОАГ IB (УУР А, УДД 2)
- Беременным женщинам с АГ в качестве АГТ с целью контроля уровня АД рекомендуется назначение лекарственных препаратов с замедленным высвобождением лекарственного вещества (нифедипин**) [237, 250].
ЕОК/ЕОАГ IC (УУР А, УДД 2)
Комментарии
. Резервными препаратами для плановой АГТ у беременных женщин с АГ являются верапамил и бисопролол. АГТ должна быть продолжена в течение 12 недель после родов, особенно у женщин с ПЭ и при рождении недоношенных детей. Можно использовать любые классы АГП, согласно алгоритму АГТ, с рациональным выбором препаратов при лактации и учитывая то, что метилдопа не рекомендована к назначению в связи с повышением риска послеродовой депрессии.
- Не рекомендовано назначение ИАПФ, БРА и прямых ингибиторов ренина при беременности в связи с риском развития врожденных уродств и гибели плода [237, 250, 251].
ЕОК/ЕОАГ IIIC (УУР C, УДД 5)
- Женщинам с АГ в репродуктивном возрасте с риском наступления незапланированной беременности не рекомендуется назначение блокаторов РААС в связи с риском развития врожденных уродств и гибели плода [21, 22, 237, 251].
ЕОК/ЕОАГ IIIC (УУР C, УДД 4)
Препараты для оральной контрацепции и заместительной гормональной терапии и артериальная гипертензия
- Не рекомендуется применять оральные контрацептивы (ОК) женщинам с неконтролируемой АГ [252, 253].
ЕОК/ЕОАГ нет (УУР B, УДД 3)
Комментарии. Комбинированные пероральные контрацептивные препараты, содержащие эстрогены и прогестины, могут приводить к повышению АД и развитию АГ приблизительно у 5% пациенток [254, 255]. При назначении оральных контрацептивов (ОК) следует оценивать риски и преимущества, наличие сопутствующих факторов СС риска (особенно курения) у конкретной пациентки. Необходимо тщательно контролировать уровень АД [256, 257]. Отмена ОК может улучшить контроль АД у женщин с АГ [252]. Прием ОК женщинами с АГ диктует необходимость их тщательного выбора и начала приема после сопоставления риска и пользы индивидуально у каждой пациентки.
Заместительная гормональная терапия не противопоказана женщинам с АГ при условии контроля АД с помощью АГП [21]. Не рекомендуется назначение гормональной заместительной терапии и селективных модуляторов рецепторов к эстрогенам с целью первичной или вторичной профилактики ССЗ.
Артериальная гипертензия и эректильная дисфункция
- Всем пациентам с АГ и наличием эректильной дисфункции (ЭД) для коррекции эндотелиальной дисфункции рекомендовано назначение ингибиторов фосфодиэстеразы-5, даже тем из них, которые получают несколько АГП (за исключением альфа-адреноблокаторов и нитратов в связи с опасностью ортостатической гипотонии) [258, 259].
ЕОК/ЕОАГ нет (УУР B, УДД 2)
Комментарии.ЭД у мужчин с АГ встречается чаще, чем у лиц с нормальным АД. ЭД считается независимым ФР сердечно-сосудистых событий и смертности, ассоциированным с ПОМ. Сбор анамнеза у пациентов АГ должен включать оценку половой функции. Изменение (оздоровление) образа жизни может уменьшить степень ЭД. Современные препараты (БРА, ИАПФ, АК и вазодилатирующие ББ) не влияют на эректильную функцию. Адекватный контроль АГ способствует ее улучшению.
Артериальная гипертензия и противоопухолевая терапия
АГ является наиболее частым сопутствующим ССЗ по данным онкологических регистров, при этом повышение АД выявляется более чем у трети пациентов [260]. Это может быть связано с высокой распространенностью АГ в той возрастной категории, в которой наиболее часто встречаются и онкологические заболевания. Однако это также обусловлено прессорным эффектом двух групп широко используемых противоопухолевых препаратов: ингибиторов фактора роста эндотелия сосудов (бевацизумаб, сорафениб, сунитиниб и пазопаниб) и ингибиторов протеасом (карфизомиб [261]).
Повышение АД выявлялось у большого числа пациентов (≤30%), получающих терапию вышеописанными противоопухолевыми препаратами. Этот эффект часто наблюдается в течение первого месяца после начала лечения.
- Рекомендовано контролировать офисное АД еженедельно в течение первого цикла терапии ингибиторами фактора роста эндотелия сосудов (бевацизумаб, сорафениб, сунитиниб и пазопаниб) или ингибиторами протеасом (карфизомиб) у пациентов со злокачественными новообразованиями и каждые 2–3 нед. в дальнейшем [262]. После завершения первого цикла лечения, при условии стабильных значений АД, его следует измерять во время рутинных посещений врача или с помощью ДМАД.
ЕОК/ЕОАГ нет (УУР С, УДД 5)
- В случае развития АГ (≥140/90 мм рт. ст.) или повышения ДАД на ≥20 мм рт. ст. по сравнению с исходным уровнем на фоне терапии ингибиторами фактора роста эндотелия сосудов (бевацизумаб, сорафениб, сунитиниб и пазопаниб) или ингибиторами протеасом (карфизомиб) у пациентов рекомендовано начать или оптимизировать антигипертензивную терапию. Предпочтительными являются блокаторы РААС и дигидропиридиновые АК[263, 264].
ЕОК/ЕОАГ нет (УУР С, УДД 5)
Комментарии
: Хотя противоопухолевая терапия имеет очевидный приоритет, следует рассмотреть возможность ее прерывания в случаях чрезмерно высоких показателей АД, несмотря на многокомпонентную терапию, при наличии симптомов, обусловленных АГ, или при развитии ССС, требующего немедленного снижения АД [263, 264].
Коррекция сопутствующих факторов сердечно-сосудистого риска
- Пациентам с АГ и очень высоким или экстремальным СС риском рекомендовано назначение статинов для достижения целевого ХС-ЛНП ≤1,4 ммоль/л или его снижение на ≥50% от исходного [265–267].
ЕОК/ЕОАГ IВ (УУР А, УДД 1)
- Пациентам с АГ и высоким СС риском рекомендовано назначение статинов для достижения целевого ХС-ЛНП ≤1,8 ммоль/л или его снижение на ≥50% от исходного [266, 267].
ЕОК/ЕОАГ IВ (УУР А, УДД 1)
Комментарии. У пациентов с низким риском можно рассмотреть назначение статинов для достижения целевого ХС-ЛНП ≤3,0 ммоль/л. У пациентов с умеренным риском можно рассмотреть назначение статинов для достижения целевого ХС-ЛНП ≤2,6 ммоль/л.
- Пациентам с АГ с целью вторичной профилактики СС событий рекомендуется назначение ацетилсалициловой кислоты в низких дозах [268].
ЕОК/ЕОАГ IА (УУР А, УДД 1)
- Пациентам с АГ не рекомендуется назначение ацетилсалициловой кислоты с целью первичной профилактики при отсутствии ССЗ в связи с недоказанными преимуществами данного вмешательства в отношении снижения СС риска [268].
ЕОК/ЕОАГ IIIA (УУР A, УДД 1)
Неотложные состояния при артериальной гипертензии: гипертонический криз
Гипертонический криз (ГК) — cостояние, при котором значительное повышение АД (до 3 степени) ассоциируется с острым поражением органов-мишеней, нередко жизнеугрожающим, требующее немедленных квалифицированных действий, направленных на снижение АД, обычно с помощью внутривенной терапии [269]. При определении тяжести поражения органов скорость и степень повышения АД могут быть так же важны, как и абсолютный уровень АД [270]. Можно выделить следующие типичные проявления гипертонических кризов:
— Пациенты со злокачественной АГ: тяжелая АГ (чаще 3-й степени) ассоциируется с изменениями на глазном дне (кровоизлияния и/или отек соска зрительного нерва), микроангиопатией и диссеминированным внутрисусосудистым свертыванием. Может приводить к энцефалопатии (примерно в 15% случаев) [271], ОСН, острому ухудшению функции почек [272–275].
— Пациенты с тяжелой АГ, ассоциированной с другими клиническими состояниями, требующими неотложного снижения АД: расслоение аорты, острая ишемия миокарда, ОСН
— Пациенты с внезапным повышением АД на фоне феохромоцитомы, ассоциированным с ПОМ
— Беременные с тяжелой АГ или преэклампсией.
Ранее использовавшийся термин «неосложненный гипертонический криз», описывавший пациентов со значительным повышением АД, но без признаков острых изменений в органах-мишенях [276], в настоящее время не рекомендован к использованию. В данной группе пациентов снижение АД обычно может проводиться в амбулаторных условиях, чаще всего путем назначения пероральной терапии в соответствии со стандартным алгоритмом, представленным выше. У этих пациентов необходимо проводить строгий контроль цифр АД до достижения целевых значений.
- Лечение пациентов с ГК рекомендуется проводить в отделении неотложной кардиологии или палате интенсивной терапии [22].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. При наличии инсульта целесообразна безотлагательная госпитализация в палату интенсивной терапии неврологического отделения или нейрореанимацию сосудистого центра.
- Осмотр врачом-терапевтом или врачом-кардиологом рекомендуется проводить не позднее 10 минут от момента поступления в стационар [22].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
- ЭКГ рекомендуется проводить при ГК не позднее 15 минут от момента поступления в стационар [22].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. Рутинное обследование при всех возможных вариантах криза включает фундоскопию, ЭКГ, общий анализ крови, определение фибриногена, креатинина, рСКФ, электролитов, ЛДГ, гаптоглобин, оценку альбуминурии и микроскопию осадка мочи, тест на беременность у женщин детородного возраста. Специфическое обследование по показаниям может включать определение тропонина, МВ-КФК, НУП, рентгенографию органов грудной клетки, ЭХО-КГ, КТ-ангиографию аорты и ее ветвей, КТ или МРТ головного мозга, УЗИ почек, исследование мочи на наркотики (метамфетамины, кокаин) [269].
- При ГК терапию антигипертензивными лекарственными препаратами внутривенно рекомендуется проводить не позднее 15 минут от момента поступления в стационар [22, 278].
ЕОК/ЕОАГ нет (УУР A, УДД 1)
Комментарии. При лечении гипертонического криза для своевременной коррекции терапии в соответствии с изменениями АД оптимальным представляется в/в назначение препарата с коротким периодом полувыведения. Быстрое неконтролируемое снижение АД не рекомендовано, так как может привести к осложнениям [277].
У пациентов со злокачественной АГ можно рассмотреть осторожное пероральное назначение иАПФ, БРА или ББ, так как почечная ишемия приводит к активации РААС. Лечение следует начинать с очень низких доз в условиях стационара, поскольку такие пациенты могут быть очень чувствительны к данным препаратам.
Для лечения ГК используются следующие парентеральные препараты:
— Вазодилататоры:
o нитроглицерин (предпочтителен при ОКС и острой левожелудочковой недостаточности);
o нитропруссид натрия (является препаратом выбора при острой гипертонической энцефалопатии).
— ИАПФ: эналаприлат (предпочтителен при острой левожелудочковой недостаточности);
— ББ (метопролол предпочтителен при расслаивающей аневризме аорты и ОКС);
— диуретики (фуросемид при острой левожелудочковой недостаточности);
— альфа-адреноблокаторы (урапидил);
— нейролептики (дроперидол).
- В остром периоде инсульта вопрос о необходимости снижения АД и его оптимальной величине рекомендуется решать совместно с врачом-неврологом, индивидуально для каждого пациента [22].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. Пациенты с инсультом требуют особого подхода, т.к. избыточное и/или быстрое снижение АД может привести к нарастанию ишемии головного мозга.
- В большинстве других случаев врачам рекомендуется обеспечить быстрое, но не более чем на 25% от исходных значений, снижение АД за первые 2 часа от момента поступления в стационар [22].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. Рекомендуются следующие сроки и выраженность снижения АД [270, 278]:
— У пациентов со злокачественной АГ с или без почечной недостаточности среднее давление должно быть снижено на 20–25% от исходного в течение нескольких часов
— У пациентов с гипертонической энцефалопатией рекомендовано немедленное снижение среднего АД на 20–25% от исходного
— У пациентов с ОКС рекомендовано немедленное снижение САД ниже 140 мм рт. ст.
— У пациентов с кардиогенным отеком легких рекомендовано немедленное снижение САД ниже 140 мм рт. ст.
— У пациентов с расслоением аорты рекомендовано немедленное снижение САД ниже 120 мм рт. ст. и ЧСС ниже 60 уд/мин.
— У пациенток с эклампсией и тяжелой преэклампсией или HELLP-синдромом рекомендовано немедленное снижение САД ниже 160 мм рт. ст. и ДАД ниже 105 мм рт. ст.
Пациенты с ГК являются группой высокого риска [279, 280] и должны быть скринированы на наличие вторичной АГ. Выписка из стационара осуществляется при достижении безопасного стабильного уровня АД на фоне перорального приема препаратов. Наблюдение в амбулаторных условиях следует проводить хотя бы раз в месяц до достижения целевого АД. Далее рекомендуется длительное регулярное наблюдение специалистом.
Медицинская реабилитация
Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
- Для всех пациентов с АГ рекомендована разработка индивидуального плана реабилитационных мероприятий, включающий в себя рекомендации по достижению целевого АД, самоконтролю АД, повышению приверженности к лечению, питанию, физической активности, контролю веса [287].
ЕОК/ЕОАГ нет (УУР B, УДД 2)
- С целью снижения риска сердечно-сосудистых осложнений всем пациентам с АГ рекомендованы, по крайней мере, 150 мин (2 часа 30 мин) в неделю аэробной физической активности умеренной интенсивности или 75 мин (1 час 15 мин) в неделю аэробной физической активности высокой интенсивности [281, 300-301].
ЕОК/ЕОАГ нет (УУР B, УДД 1)
Комментарии. Умеренная физическая нагрузка — это такая нагрузка, которую можно выдержать в течение 1 часа, а интенсивная физическая нагрузка та, при которой через 30 минут появляется усталость [281]. Во время проведения физических нагрузок обязателен контроль АД.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Динамическое наблюдение — чрезвычайно важная составляющая медицинской помощи пациентам с АГ, задачами которого являются: поддержание целевых уровней АД, контроль выполнения врачебных рекомендаций по коррекции ФР, контроль за соблюдением режима приема АГП, оценка состояния органов-мишеней.
При стабильном течении АГ приемлемой альтернативой визитам в медицинское учреждение могут быть ДМАД [292, 294–296].
Все рекомендации, даваемые пациенту, должны быть ясными, четкими и соответствовать его интеллектуальному уровню.
С целью обеспечить осознанное участие пациента в лечебно-профилактическом процессе и повысить эффективность лечения целесообразно для ряда пациентов, для которых устных рекомендаций недостаточно, продублировать их в письменном виде.
- Всем пациентам с высоким нормальным АД (130–139/85–89 мм рт. ст.) рекомендуется изменение образа жизни [21, 22, 98].
ЕОК/ЕОАГ IА (УУР C, УДД 5)
- Рекомендуется всем пациентам с АГ в рамках диспансерного наблюдения проводить оценку факторов риска и ПОМ не реже, чем 1 раз в год [21].
ЕОК/ЕОАГ нет (УУР 5, УДД С)
Комментарии. У пациентов с высоким нормальным АД или АГ «белого халата» нередко выявляются дополнительные факторы риска, ПОМ, а также высокий риск развития устойчивой АГ [282–286], поэтому даже при отсутствии лечения пациентов необходимо регулярно наблюдать (по крайней мере, ежегодно) для оценки клинического АД, АД, измеренного вне медицинского учреждения и СС риска. При ежегодных визитах следует обращать внимание на рекомендации по изменению образа жизни, которые являются методом адекватной терапии таких пациентов.
- Всем пациентам с АГ, которым была назначена АГТ, рекомендуется проводить плановые визиты к врачу для оценки переносимости, эффективности и безопасности лечения, а также контроля выполнения врачебных рекомендаций [21, 289, 290].
ЕОК/ЕОАГ нет (УУР B, УДД 1)
Комментарии. Визиты проводятся с интервалом в 3–4 недели до достижения целевого уровня АД (при отсутствии других причин более частых визитов). Целевое АД должно быть достигнуто в течение 3 месяцев.
- Всем пациентам с АГ, принимающим АГТ, при ее недостаточной эффективности рекомендуется производить замену ранее назначенного АГП или присоединять другой АГП. При отсутствии эффективного снижения АД на фоне 2-компонентной терапии рекомендуется присоединение третьего препарата (одним из трех препаратов, как правило, должен быть диуретик) с обязательным последующим контролем эффективности, безопасности и переносимости комбинированной терапии [21].
ЕОК/ЕОАГ нет (УУР C, УДД 5)
Комментарии. Целевые уровни АД являются рекомендованными для достижения в каждой подгруппе пациентов, но важнейшим принципом их достижения является соблюдение безопасности и сохранения качества жизни пациента. Поэтому скорость достижения целевых значений и степень снижения АД могут быть скорректированы у конкретного пациента в зависимости от конкретной клинической ситуации. При этом плохая переносимость снижения АД может быть основанием для более медленной титрации доз и числа назначаемых препаратов, равно как и при хорошей переносимости АД может быть снижено до более низких значений, чем рекомендовано в среднем. Недостижение целевого АД в указанные сроки не является ошибочным, если это продиктовано клинической необходимостью. Если врач считает, что препятствием к достижению целевого АД является плохая приверженность пациента, это должно находить отражение в медицинской документации и должны быть предприняты и зафиксированы меры по повышению приверженности. В этих случаях недостижение целевого уровня не должно считаться дефектом оказания помощи.
- Пациентам с высоким и очень высоким сердечно-сосудистым риском (таблица П10, Приложение Г2 и таблица П12, Приложение Г2), а также для пациентов, получающих только немедикаментозное лечение, и для лиц с низкой приверженностью к лечению после достижения целевого уровня АД на фоне проводимой терапии последующие визиты к врачу рекомендуется проводить не реже, чем один раз в 3 месяца; визиты для пациентов со средним и низким риском, которые регулярно измеряют АД дома, рекомендуется проводить с интервалом в 4–6 месяцев [288].
ЕОК/ЕОАГ нет (УУР С, УДД 2)
- Пациентам с АГ для повышения приверженности к проводимой АГТ рекомендуется проведение ДМАД и ведение дневников с указанием доз принимаемых препаратов и уровня АД [21, 289, 290].
ЕОК/ЕОАГ нет (УУР B, УДД 1)
- Пациентам с АГ для повышения эффективности и приверженности к проводимой АГТ рекомендуется проведение телемониторинга показателей системной гемодинамики с телеметрической передачей результатов измерения АД непосредственно в лечебное учреждение для оперативной обработки информации и оперативного принятия решения [291–293].
ЕОК/ЕОАГ нет (УУР В, УДД 1)
- Рекомендуется при динамическом наблюдении особое внимание уделять показателям АД в ночные часы (особенно у пациентов с метаболическим синдромом (МС), сахарным диабетом (СД), синдромом обструктивного апноэ во время сна (СОАС), хронической болезнью почек (ХБП) 3–5-й ст.) и ранние утренние часы с целью снижения риска таких осложнений, как ИМ, инсульт [21, 34, 35].
ЕОК/ЕОАГ нет (УУР В, УДД 2)
Информация
Источники и литература
-
Клинические рекомендации Российского кардиологического общества
- 1. Rosenberg WM, Gray JA et al. Evidence based medicine: what it is and what it isn’t. BMJ 1996, January; 312 (7023): 71–72. 2. Федеральный закон от 21.11.2011 № 323-ФЗ (ред. от 03.04.2017) «Об основах охраны здоровья граждан в Российской Федерации». 3. Эпидемиологический словарь, 4-е издание. Под ред. Джона М. Ласта для Международной эпидемиологической ассоциации. М., 2009. 316 с.
4. Федеральное агентство по техническому регулированию и метрологии. Национальный стандарт Российской Федерации. ГОСТР 52379-2005. Надлежащая клиническая практика. Москва, 2005 5. Федеральный закон от 12.04.2010 № 61-ФЗ (ред. от 03.07.2016) «Об обращении лекарственных средств».
6. Jansen RW, Lipsitz LA. Postprandial hypotension: epidemiology, pathophysiology, and clinical management. Ann Int Med 1995;122(4):286–295. 7. Малая медицинская энциклопедия. М.: Медицинская энциклопедия, 1991—96 гг. [Электронный ресурс]. Режим доступа:http://dic.academic.ru/dic.nsf/enc_medicine/28878/Синдром 8. Андреева Н. С., Реброва О. Ю., Зорин Н. А. и др. Системы оценки достоверности научных доказательств и убедительности рекомендаций: сравнительная характеристика и перспективы унификации. Медицинские технологии. Оценка и выбор. 2012. №. 4. С. 10–24.
9. Общероссийская общественная организация «Российская ассоциация геронтологов и гериатров». Клинические рекомендации «Старческая астения». 2018. 10. Rapsomaniki E et al. Blood pressure and incidence of twelve cardiovascular diseases: lifetime risks, healthy life-years lost, and age-specific associations in 1• 25 million people. The Lancet 383.9932 (2014):1899–1911. 11. Ehret GB, Caulfield MJ. Genes for blood pressure: an opportunity to understand hypertension. Eur Heart J 2013;34:951–961. 12. Elliott P, Stamler J, Nichols R, et al. Intersalt revisited: further analyses of 24 hour sodium excretion and blood . pressure within and across populations. Intersalt Cooperative Research Group. . BMJ 1996;312:1249–1253. 13. Кушаковский М. С. Эссенциальная гипертензия (гипертоническая болезнь). Причины, механизмы, клиника, лечение. СПб., 2002. 14. Ланг Г. Ф. Гипертоническая болезнь. М.: Медгиз, 1950. 459 с. 15. Постнов Ю. В., Орлов С. Н. Первичная гипертензия как патология клеточных мембран. М.: Медицина, 1987. 192 с. 16. Мясников А. Л. Гипертоническая болезнь. М.: Медгиз, 1954. 17. Распространенность факторов риска неинфекционных заболеваний в российской популяции в 2012–2013 гг. Результаты исследования ЭССЕ-РФ. Кардиоваскулярная терапия и профилактика 2014; 13(6):4–11. 18. Бойцов С. А., Баланова Ю. А., Шальнова С. А., Деев А. Д. и др. Артериальная гипертония среди лиц 25–64 лет: распространенность, осведомленность, лечение и контроль. По материалам исследования ЭССЕ. Кардиоваскулярная терапия и профилактика. 2014;4:4-14.do1.org/10.15829/1728-8800-2014-4-4-14. 19. Kearney PM, Whelton M, Reynolds K, et al. Global burden of hypertension: analysis of worldwide data. Lancet 2005;365:217–223. 20. Franklin SS, Lopez VA, Wong ND, et al. Single versus combined blood pressure components and risk for cardiovascular disease: the Framingham Heart Study. Circulation 2009;119:243–250. 21. Williams B, Mancia G, Spiering W et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension. JHypertens 2018;36(10):1953–2041.
22. Чазова И. Е., Жернакова Ю. В. [от имени экспертов]. Клинические рекомендации. Диагностика и лечение артериальной гипертонии. Системные гипертензии. 2019;16 (1):6–31. 23. Lewington S, Clarke R, Qizilbash N et al. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002;360:1903–1913. 24. Lip GYH, Coca A, Kahan T, et al. Hypertension and cardiac arrhythmias: executive summary of a consensus document from the European Heart Rhythm Association (EHRA) and ESC Council on Hypertension, endorsed by the Heart Rhythm Society (HRS), Asia-Pacific Heart Rhythm Society (APHRS), and Sociedad Latinoamericana de Estimulacion Cardiaca y Electrofisiologia (SOLEACE). Eur Heart J Cardiovasc Pharmacother 2017;3:235–250. 25. Gottesman RF, Albert MS, Alonso A, et al. Associations between midlife vascular risk factors and 25-year incident dementia in the Atherosclerosis Risk in Communities (ARIC) cohort. JAMA Neurol 2017;74:1246–1254. 26. Rovio SP, Pahkala K, Nevalainen J et al. Cardiovascular risk factors from childhood and midlife cognitive performance: the Young Finns study. J Am Coll Cardiol 2017;69:2279–2289. 27. Vishram JK, Borglykke A, Andreasen AH, et al, MORGAM Project. Impact of age on the importance of systolic and diastolic blood pressures for stroke risk: the MOnica, Risk, Genetics, Archiving, and Monograph (MORGAM) project. Hypertension 2012;60:1117–1123. 28. Brown DW, Giles WH, Greenlund KJ. Blood pressure parameters and risk of fatal stroke, NHANES II mortality study. Am J Hypertens 2007;20:338–341. 29. Franklin SS, Khan SA, Wong ND, et al. Is pulse pressure useful in predicting risk for coronary heart disease? The Framingham heart study. Circulation 1999;100:354–360. 30. Domanski M, Mitchell G, Pfeffer M, Neaton JD, Norman J, Svendsen K, Grimm R, Cohen J, Stamler J, MRFIT Research Group. Pulse pressure and cardiovascular disease-related mortality: follow-up study of the Multiple Risk Factor Intervention Trial (MRFIT). JAMA 2002;287:2677–2683. 31. Кобалава Ж. Д., Конради А. О., Недогода С. В. и др. Меморандум экспертов Российского кардиологического общества по рекомендациям Европейского общества кардиологов/Европейского общества по артериальной гипертензии по лечению артериальной гипертензии 2018 г. Российский кардиологический журнал. 2018;(12):131–42. 32. Lewington S, Clarke R, Qizilbash N, et al. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002; 360:1903–1913.
33. Reino-Gonzalez S. et al. How in-office and ambulatory BP monitoring compare: A systematic review and meta-analysis. – 2017. 34. Kollias A., Ntineri A., Stergiou G. S. Association of night-time home blood pressure with night-time ambulatory blood pressure and target-organ damage: a systematic review and meta-analysis //Journal of hypertension. – 2017. – Т. 35. – №. 3. – С. 442-452. 35. Fagard RH, Celis H, Thijs L, et al. Daytime and night-time blood pressure as predictors of death and cause-specific cardiovascular events in hypertension. Hypertension 2008; 51:55–61. 36. Ward AM, Takahashi O, Stevens R, Heneghan C. Home measurement of blood pressure and cardiovascular disease: systematic review and meta-analysis of prospective studies. J Hypertens 2012; 30:449–456. 37. Mancia G, Facchetti R, Bombelli M, et al. Long-term risk of mortality associated with selective and combined elevation in office, home and ambulatory blood pressure. Hypertension 2006; 47:846–853. 38. Fagard RH, Cornelissen VA. Incidence of cardiovascular events in white-coat, masked and sustained hypertension vs. true normotension: a meta-analysis. J Hypertens 2007; 25:2193–219. 39. Rimoldi SF, Scherrer U, Messerli FH. Secondary arterial hypertension: when, who, and how to screen? Eur Heart J 2014;35:1245–1254. 40. Albasri A. et al. A comparison of blood pressure in community pharmacies with ambulatory, home and general practitioner office readings: systematic review and meta-analysis //Journal of hypertension. – 2017. – Т. 35. – №. 10. – С. 1919. 41. Clark CE, Taylor RS, Shore AC, et al. Association of a difference in systolic blood pressure between arms with vascular disease and mortality: a systematic review and meta-analysis. Lancet 2012;379:905–914. 42. Sega R, Facchetti R, Bombelli M, et al.Prognostic value of ambulatory and home blood pressures compared with office blood pressure in the general population: follow-up results from the Pressioni Arteriose Monitorate e Loro Associazioni (PAMELA) study. Circulation 2005;111:1777–1783. 43. Shi Y. et al. Resting heart rate and the risk of hypertension and heart failure: a dose–response meta-analysis of prospective studies //Journal of hypertension. – 2018. – Т. 36. – №. 5. – С. 995-1004. 44. Salles GF, Reboldi G, Fagard RH, et al. Prognostic effect of the nocturnal blood pressure fall in hypertensive patients: the Ambulatory Blood pressure Collaboration in patients with Hypertension (ABC-H) meta-analysis. Hypertension 2016;67:693–700.
45. Ward AM, Takahashi O, Stevens R, Heneghan C. Home measurement of blood pressure and cardiovascular disease: systematic review and meta-analysis of prospective studies. J Hypertens 2012;30:449–56. 46. Tucker KL, Sheppard JP, Stevens R et al. Self-monitoring of blood pressure in hypertension: a systematic review and individual patient data meta-analysis. PLoS Med 2017;14:e1002389. 47. Parati G, Stergiou G, O’Brien E, et al, European Society of Hypertension Working Group on Blood Pressure Monitoring and Cardiovascular Variability. European Society of Hypertension practice guidelines for ambulatory blood pressure monitoring. J Hypertens 2014;32:1359–1366. 48. Sehestedt T, Jeppesen J, Hansen TW, et al. Risk prediction is improved by adding markers of subclinical organ damage to SCORE. Eur Heart J 2010;31:883–891. 49. Volpe M, Battistoni A, Tocci G, et al. Cardiovascular risk assessment beyond systemic coronary risk estimation: a role for organ damage markers. J Hypertens 2012;30:1056–1064. 50. Conroy, R. M., et al. Estimation of ten-year risk of fatal cardiovascular disease in Europe: the SCORE project. European heart journal 24.11 (2003): 987–1003. 51. Hunt SC, Williams RR, Barlow GK. A comparison of positive family history definitions for defining risk of future disease. J Chronic Dis 1986; 39:809–821. 52. Friedman GD, Selby JV, Quesenberry CP Jr, et al Precursors of essential hypertension: body weight, alcohol and salt use and parental history of hypertension. Prev Med 1988;17:387–402. 53. Дедов И. И. и др. Алгоритмы специализированной медицинской помощи больным сахарным диабетом. Сахарный диабет 1S (2019). 54. Cosentino F, Grant P, Aboyans V et al. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD: The Task Force for diabetes, pre-diabetes, and cardiovascular diseases of the European Society of Cardiology (ESC) and the European Association for the Study of Diabetes (EASD). Eur Heart J 2019, published online on 31 August 2019. 55. Emerging Risk Factors Collaboration. Diabetes mellitus, fasting blood glucose concentration, and risk of vascular disease: a collaborative meta-analysis of 102 prospective studies. The Lancet 375.9733 (2010): 2215–2222. 56. Wilson PW, Cupples CF, Kannel WB. Is hyperglycemia associated with cardiovascular disease? The Framingham Study. Amer. Heart J 1991;121:586–90. 57. Izzo R, de Simone G, Trimarco V. et al. Hypertensive target organ damage predicts incident diabetes mellitus. EurHeartJ. epub 27 June 2013. 58. Matsushita K. et al. Comparison of risk prediction using the CKD-EPI equation and the MDRD study equation for estimated glomerular filtration rate //Jama. – 2012. – Т. 307. – №. 18. – С. 1941-1951.
59. Ettehad D, Emdin CA, Kiran A, et al. Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis. Lancet 2016;387:957–967. 60. De Haan M. W. et al. Renovascular disease in patients with hypertension: detection with duplex ultrasound //Journal of human hypertension. – 2002. – Т. 16. – №. 7. – С. 501. 61. Mahmoodi, Bakhtawar K., et al. Associations of kidney disease measures with mortality and end-stage renal disease in individuals with and without hypertension: a meta-analysis. The Lancet 380.9854 (2012):1649–1661. 62. Van Der Velde M. et al. Lower estimated glomerular filtration rate and higher albuminuria are associated with all-cause and cardiovascular mortality. A collaborative meta-analysis of high-risk population cohorts. Kidney international 79.12 (2011): 1341–1352. 63. Earley A, Miskulin D, Lamb EJ et al. Estimating equations for glomerular filtration rate in the era of creatinine standardization: a systematic review. Ann Intern Med 2012; 156: 785–795. 64. Zachrisson K. et al. Duplex ultrasound for identifying renal artery stenosis: direct criteria re-evaluated //Acta Radiologica. – 2017. – Т. 58. – №. 2. – С. 176-182. 65. Matsushita K. et al. Kidney measures beyond traditional risk factors for cardiovascular prediction: A collaborative meta-analysis //The lancet. Diabetes & endocrinology. – 2015. – Т. 3. – №. 7. – С. 514. 66. Gerstein HC, Mann JF, Yi Q, Zinman B, et al. HOPE Study Investigators. Albuminuria and risk of cardiovascular events, death, and heart failure in diabetic and nondiabetic individuals. JAMA 2001;286:421–426. 67. Boekholdt SM et al. Association of LDL cholesterol, non–HDL cholesterol, and apolipoprotein B levels with risk of cardiovascular events among patients treated with statins: a meta-analysis //Jama. — 2012. — Т. 307. — №. 12. — С. 1302-1309. 68. Guo X. et al. Prehypertension: a meta-analysis of the epidemiology, risk factors, and predictors of progression //Texas heart institute journal. – 2011. – Т. 38. – №. 6. – С. 643. 69. Geleijnse JM, Kok FJ, Grobbee DE. Blood pressure response to changes in sodium and potassium intake: a metaregression analysis of randomised trials. Journal of human hypertension 17.7(2003):471. 70. Macdonald JE, Struthers AD. hat is the optimal serum potassium level in cardiovascular patients? Journal of the American College of Cardiology 43.2 (2004):155–161. 71. Wang J. et al. Hyperuricemia and risk of incident hypertension: a systematic review and meta-analysis of observational studies //PloS one. – 2014. – Т. 9. – №. 12. – С. e114259. 72. Grayson PC et al. Hyperuricemia and incident hypertension: a systematic review and meta‐analysis.. Arthritis care & research 63.1 (2011):102–110.
73. Palmer TM et al. Association of plasma uric acid with ischaemic heart disease and blood pressure: mendelian randomisation analysis of two large cohorts. Bmj 347 (2013): f4262. 74. Schillaci, G., Battista, F., & Pucci, G. (2012). A review of the role of electrocardiography in the diagnosis of left ventricular hypertrophy in hypertension. Journal of electrocardiology, 45(6), 617–623. 75. Kahn S, Frishman WH, Weissman S et al. Left ventricular hypertrophy on electrocardiogram: prognostic implications from a 10-year cohort study of older subjects: a report from the Bronx Longitudinal Aging Study. J Am Geriatr Soc 1996;44:524–529. 76. Lonn E, Mathew J, Pogue J et al. Relationship of electrocardiographic left ventricular hypertrophy to mortality and cardiovascular morbidity in high-risk patients. Eur J Cardiovasc Prevent Rehab. 2003;10:420–428. 77. Bacharova L, Schocken D, Estes EH, Strauss D. The role of ECG in the diagnosis of left ventricular hypertrophy. Curr Cardiol Rev 2014;10:257–261. 78. Lehtonen AO, Puukka P, Varis J et al. Prevalence and prognosis of ECG abnormalities in normotensive and hypertensive individuals. J Hypertens 2016;34:959–966.
- 1. Rosenberg WM, Gray JA et al. Evidence based medicine: what it is and what it isn’t. BMJ 1996, January; 312 (7023): 71–72. 2. Федеральный закон от 21.11.2011 № 323-ФЗ (ред. от 03.04.2017) «Об основах охраны здоровья граждан в Российской Федерации». 3. Эпидемиологический словарь, 4-е издание. Под ред. Джона М. Ласта для Международной эпидемиологической ассоциации. М., 2009. 316 с.
Информация
Список сокращений
АГ — артериальная гипертензия
АГП — антигипертензивные препараты
АГТ — антигипертензивная лекарственная терапия
АГЭ — антигипертензивный эффект
АД — артериальное давление
АИР — агонисты имидазолиновых рецепторов
АК — антагонисты кальция (блокаторы кальциевых каналов)
АКС — ассоциированное клиническое состояние
АЛТ — аланинаминотрансфераза
АМКР — антагонисты минералокортикоидных рецепторов
АПФ — ангиотензинпревращающий фермент
АСТ — аспартатаминотрансфераза
БА — бронхиальная астма
ББ — бета-адреноблокатор
БРА — блокатор рецепторов ангиотензина
БСК — болезни системы кровообращения
ГБ — гипертоническая болезнь
ГК — гипертонический криз
ГКС — глюкокортикостероиды
ГЛЖ — гипертрофия левого желудочка
ДАД — диастолическое артериальное давление
ДМАД — домашнее мониторирование артериального давления
ЕОК/ЕОАГ — Европейское общество кардиологов/Европейское общество артериальной гипертонии
ИААГ — изолированная амбулаторная артериальная гипертензия
ИАПФ — ингибитор ангиотензинпревращающего фермента
ИБС — ишемическая болезнь сердца
ИММЛЖ — индекс массы миокарда левого желудочка
ИМТ — индекс массы тела
ИСАГ — изолированная систолическая артериальная гипертензия
КТ — компьютерная томография
ЛЖ — левый желудочек
ЛП — левое предсердие
ЛПИ — лодыжечно-плечевой индекс
МРТ — магнитно-резонансная томография
МС — метаболический синдром
НТГ — нарушенная толерантность к глюкозе
ОК — оральные контрацептивы
ОКС — острый коронарный синдром
ОПСС — общее периферическое сосудистое сопротивление
ОХС — общий холестерин
ОЦК — объем циркулирующей крови
ПД — пульсовое давление
ПОМ — поражение органов-мишеней
РААС — ренин-ангиотензин-альдостероновая система
РКИ — рандомизированные клинические исследования
РФ — Российская Федерация
САД — систолическое артериальное давление
САС — симпато-адреналовая система
СД — сахарный диабет
СКФ — скорость клубочковой фильтрации
СМАД — суточное мониторирование артериального давления
СНС — симпатическая нервная система
СОАС — синдром обструктивного апноэ во время сна
СПВ — скорость пульсовой волны
СС — сердечно-сосудистый
ССЗ — сердечно-сосудистые заболевания
ССО — сердечно-сосудистые осложнения
ТГ — триглицериды
ТИА — транзиторная ишемическая атака
УДД — уровень достоверности доказательств
УЗИ — ультразвуковое исследование
УУР — уровень убедительности рекомендаций
ФВ — фракция выброса
ФК — функциональный класс
ФП — фибрилляция предсердий
ФР — фактор риска
ХБП — хроническая болезнь почек
ХОБЛ — хроническая обструктивная болезнь легких
ХПН — хроническая почечная недостаточность
ХС ЛВП — холестерин липопротеинов высокой плотности
ХС ЛНП — холестерин липопротеинов низкой плотности
ХСН — хроническая сердечная недостаточность
ЦАД — центральное артериальное давление
ЦВБ — цереброваскулярная болезнь
ЧСС — частота сердечных сокращений
ЭД — эректильная дисфункция
ЭКГ — электрокардиограмма
ЭхоКГ — эхокардиография
CKD-EPI — ChronicKidneyDiseaseEpidemiology Collaboration
ESC/ESH — European society of cardiology/European society of hypertension
MDRD — Modification of Diet in Renal Disease
SCORE — Systemic coronary risk evaluation
Термины и определения
Артериальная гипертензия (АГ) — синдром повышения клинического артериального давления (АД) при гипертонической болезни и симптоматических АГ выше пороговых значений, определенных в результате эпидемиологических и рандомизированных контролируемых исследований, продемонстрировавших связь с повышением сердечно-сосудистого риска и целесообразность и пользу лечения, направленного на снижение АД ниже этих уровней АД.
АГ у молодых — повышение АД выше пороговых значений у лиц моложе 50 лет
Высокое нормальное АД — давление в диапазоне систолического АД (САД) от 130 до 139 мм рт. ст. и/или диастолического АД (ДАД) от 85 до 89 мм рт. ст.
Гипертония белого халата — форма АГ, при которой повышение АД ≥140 и/или ≥90 мм рт. ст. отмечается только на приеме у врача, а при измерении АД методом домашнего мониторирования АД (ДМАД) и/или суточного мониторирования АД (СМАД) показатели АД — в пределах нормальных значений. Доказательная медицина — надлежащее, последовательное и осмысленное использование современных наилучших доказательств (результатов клинических исследований) в сочетании с индивидуальным клиническим опытом и c учетом ценностей и предпочтений пациента в процессе принятия решений о состоянии здоровья и лечении пациента [1].
Заболевание — состояние, возникающее в связи с воздействием патогенных факторов, нарушение деятельности организма, работоспособности, способности адаптироваться к изменяющимся условиям внешней и внутренней среды при одновременном изменении защитно-компенсаторных и защитно-приспособительных реакций и механизмов организма [2].
Изолированная систолическая АГ–повышение САД ≥140 мм рт. ст. при уровне ДАД <90 мм рт. ст.
Исход — любой возможный результат, возникающий от воздействия причинного фактора, профилактического или терапевтического вмешательства, все установленные изменения состояния здоровья, возникающие как следствие вмешательства [3].
Клиническое исследование — любое исследование, проводимое с участием человека в качестве субъекта для выявления или подтверждения клинических и/или фармакологических эффектов исследуемых продуктов и/или выявления нежелательных реакций на исследуемые продукты, и/или изучения их всасывания, распределения, метаболизма и выведения с целью оценить их безопасность и/или эффективность [4].
Конфликт интересов — ситуация, при которой у медицинского или фармацевтического работника при осуществлении ими профессиональной деятельности возникает личная заинтересованность в получении лично либо через представителя компании материальной выгоды или иного преимущества, которое влияет или может повлиять на надлежащее исполнение ими профессиональных обязанностей вследствие противоречия между личной заинтересованностью медицинского работника или фармацевтического работника и интересами пациента [2].
Лекарственные препараты — лекарственные средства в виде лекарственных форм, применяемые для профилактики, диагностики, лечения заболевания, реабилитации, для сохранения, предотвращения или прерывания беременности [5].
Маскированная (скрытая) АГ — форма гипертонии, особенностью которой являются нормальные показатели клинического АД (<140/90 мм рт. ст.) и повышенные — по данным СМАД и/или ДМАД.
Медицинское вмешательство — выполняемые медицинским работником и иным работником, имеющим право на осуществление медицинской деятельности, по отношению к пациенту, затрагивающие физическое или психическое состояние человека и имеющие профилактическую, диагностическую, лечебную, реабилитационную или исследовательскую направленность виды медицинских обследований и (или) медицинских манипуляций, а также искусственное прерывание беременности [2].
Изменение образа жизни — мероприятия, направленные на нормализацию веса и характера питания, двигательной активности, целью которых является снижение сердечно-сосудистого риска.
Оптимальное АД — САД менее 120 ммрт. ст. и/или ДАД менее 80 мм рт. ст.
Очень пожилые пациенты — пациенты в возрасте ≥ 80 лет. Пациент — физическое лицо, которому оказывается медицинская помощь или которое обратилось за оказанием медицинской помощи независимо от наличия у него заболевания и от его состояния [2].
Нормальное АД — давление в диапазоне САД 120–129 мм рт. ст. и/или ДАД 80–84 мм рт. ст.
Пожилые пациенты — пациенты, которым от 65 лет до 79 лет.
Постпрандиальная гипотензия — снижение систолического АД более, чем на 20 мм рт. ст. в течение двух часов после приема пищи при нахождении в положении лежа или сидя [6].
Постуральная гипотензия — снижение САД на 20 мм рт. ст. и более и/или ДАД — на 10 мм рт. ст. и более в первые 3 мин при переходе из горизонтального в вертикальное положение.
Псевдорезистентная АГ — случаи резистентной АГ, в которых не могут быть исключены причины плохого контроля АД: эффект «белого халата», плохая приверженность к лечению, неправильно подобранная терапия, неправильное измерениеАД, выраженная кальцификация артерий, регулярный прием препаратов, повышающих АД, факторы образа жизни, наличие синдрома обструктивного апноэ во время сна.
Пульсовое давление — разница между САД и ДАД.
Рабочая группа по разработке/актуализации клинических рекомендаций — коллектив специалистов, работающих совместно и согласованно в целях разработки/актуализации клинических рекомендаций и несущих общую ответственность за результаты данной работы.
Резистентная АГ — диагностируется в случаях, когда назначение трех антигипертензивных препаратов (включая диуретик) в оптимальных или максимально переносимых дозах не приводит к достижению целевого АД ниже 140 и/или 90 мм рт. ст. у приверженных к лечению пациентов. При этом отсутствие контроля АД подтверждено измерением АД вне медицинского учреждения (СМАД или ДМАД), а вторичные причины АГ исключены.
Синдром — устойчивая совокупность ряда симптомов с единым патогенезом [7].
Состояние — изменения организма, возникающие в связи с воздействием патогенных и (или) физиологических факторов и требующие оказания медицинской помощи [2].
Уровень достоверности доказательств — степень уверенности в том, что полученный эффект от применения медицинского вмешательства является истинным [8].
Уровень убедительности рекомендаций — степень уверенности в достоверности эффекта вмешательства и в том, что следование рекомендациям принесет больше пользы, чем вреда в конкретной ситуации [8].
Фиксированная комбинация лекарственных препаратов — сочетание двух и более разных классов препаратов в одной таблетке.
Хроническая болезнь почек — наднозологическое понятие, объединяющее всех пациентов с признаками повреждения почек и/или снижением функции, оцениваемой по величине скорости клубочковой фильтрации, которые сохраняются в течение 3 и более месяцев.
Хроническая алкогольная интоксикация — комплекс физиологических, поведенческих и когнитивных явлений, при которых употребление алкогольных напитков начинает занимать более важное место в системе ценностей человека, чем другие формы поведения, которые ранее были более важными для него.
Синдром старческой астении — гериатрическийсиндром, характеризующийся возраст-ассоциированным снижением физиологического резерва и функций многих систем организма, приводящий к повышенной уязвимости организма пожилого человека к воздействию эндо- и экзогенных факторов и высокому риску развития неблагоприятных исходов для здоровья, потери автономности и смерти [9].
Целевой уровень АД — уровень АД, различный для разных групп пациентов с АГ, достижение которого в процессе лечения позволяет добиться наиболее благоприятного соотношения польза (снижение сердечно-сосудистого (СС) риска) — риск (неблагоприятные эффекты).
Организация оказания медицинской помощи
Показания для плановой госпитализации:
- неясность диагноза и необходимость в специальных методах исследования (использование диагностических процедур, проведение которых невозможно или нецелесообразно в условиях поликлиники) для уточнения причины повышения АД (исключение симптоматических АГ);
- трудности в подборе медикаментозной терапии (сочетанная патология, частые гипертонические кризы);
- рефрактерная АГ.
Показания для экстренной госпитализации:
- гипертонический криз, не купирующийся на догоспитальном этапе;
- гипертонический криз при феохромоцитоме;
- гипертонический криз с выраженными явлениями гипертонической энцефалопатии;
- осложнения АГ, требующие интенсивной терапии: инсульт, ОКС, субарахноидальное кровоизлияние, острые нарушения зрения, отек легких, расслоение аорты, почечная недостаточность, эклампсия.
Показания к выписке пациента из стационара:
- установленный диагноз симптоматической АГ или ГБ с использованием специальных методов исследования при уточнении причины повышения АД;
- подобранная медикаментозная терапия при сочетанной патологии и/или частых гипертонических кризах с достижением целевого уровня АД или снижение АД на 25–30% от исходных значений на момент выписки из стационара;
- купированный гипертонический криз, отсутствие осложнений, требующих интенсивной терапии, стабилизация уровня АД.
Иные организационные технологии
При анализе работы медицинской организации с пациентами с АГ целесообразно анализировать следующие показатели:
- процент пациентов, достигших целевого АД менее 140/90 мм рт. ст. и 130/80 мм рт. ст. через 3, 6 и 12 месяцев наблюдения;
- процент пациентов, получающих комбинированную антигипертензивную терапию.
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Снижение АД, достижение и удержание его на целевом уровне является ключевым фактором, влияющим на прогноз и улучшающим сердечно-сосудистые исходы у пациентов с АГ.
Другими важными целями при лечении АГ являются:
— максимальное снижение риска развития ССО и смерти;
— коррекция всех модифицируемых ФР (курение, дислипидемия, гипергликемия, ожирение);
— предупреждение, замедление темпа прогрессирования и/или уменьшение ПОМ;
— лечение сопутствующих заболеваний (ИБС, ХСН, СД, ФП, ХБП).
Критерии оценки качества медицинской помощи
| № | Критерий качества |
EОК Класс и уровень |
Да/ нет |
| 1 | Установлен диагноз АГ согласно рекомендациям. Зафиксировано повышение офисного (клинического) АД выше 140 и/или 90 мм рт. ст. на повторных визитах, либо на основании СМАД (среднее за 24 часа ≥130 мм и/или ≥80 мм рт. ст.) | IA | Да/нет |
| 2 | Выполнен общий анализ крови | — | Да/нет |
| 3 | Выполнен биохимический анализ крови (креатинин, расчетная скорость клубочковой фильтрации, глюкоза, калий, натрий, мочевая кислота, ОХ, ЛПНП, ТГ, ЛПВП) | IB | Да/нет |
| 4 | Выполнен общий анализ мочи | IB | Да/нет |
| 5 | Выполнена качественная оценка протеинурии тест-полоской или количественное определение альбуминурии | IB | Да/нет |
| 6 | Выполнена ЭКГ в 12 отведениях | IB | Да/нет |
| 7 | Даны рекомендации по модификации образа жизни (ограничение потребления натрия, увеличение физической активности, снижение избыточной массы тела, отказ от курения, ограничение потребления алкоголя) | IA | Да/нет |
| 8 | Поставлен клинический диагноз с указанием стадии заболевания, степени повышения АД (при отсутствии терапии), категории риска, наличия ПОМ и АКС | — | Да/нет |
| 9 | У пациентов с АГ 1-й степени, относящимся к категориям низкого/среднего риска, начата антигипертензивная лекарственная терапия одним из препаратов рекомендованных классов после 3-го месяца модификации образа жизни | IA | Да/нет |
| 10 | Лицам с АГ второй степени и выше назначена комбинированная двухкомпонентная антигипертензивная терапия сразу после постановки диагноза и проведена ее интенсификация для достижения целевого АД. | IA | Да/нет |
| 11 | Достигнут целевой уровень САД<140 мм рт. ст. и ДАД < 90 мм рт. ст. через 3 месяца от начала лечения. При недостижении целевого АД приведено объяснение необходимости индивидуального уровня АД и скорости его снижения (плохая переносимость, побочные эффекты лекарственной терапии, низкая приверженность пациента к лечению, включая невыполнения рекомендаций врача, необходимость ревизии поставленного диагноза для исключения симптоматической АГ, наличие сопутствующей патологии или лекарственной терапии, затрудняющей контроль АД) | IA | Да/нет |
| 12 | Пациент взят под диспансерное наблюдение | — | Да/нет |
Типичными дефектами при оказании медицинской помощи пациентам с АГ являются:
при сборе анамнеза:
• не уточнены характер начала заболевания, продолжительность, особенности течения заболевания;
• отсутствуют сведения об эффективности ранее проводимой терапии, о возможном приеме пациентами других, помимо антигипертензивных, лекарственных препаратов: глюкокортикоидных гормонов, цитостатиков, нестероидных противовоспалительных препаратов, оральных контрацептивов и др.
• отсутствуют сведения о наличии менопаузы у женщин, характере питания, статусе курения, семейном анамнезе ранних сердечно-сосудистых заболеваний, осложнений АГ;
• отсутствие сведений о наличии предшествующих госпитализаций.
при обследовании пациентов:
• неполное физическое, лабораторное и инструментальное обследование, что приводит к недооценке возможности наличия симптоматической АГ, неверной оценке ПОМ и СС риска;
• отсутствие развернутого клинического диагноза, с указанием стадии гипертонической болезни, степени повышения АД (степени АГ при впервые выявленной АГ), с максимально полным отражением ФР, ПОМ, ССЗ, ХБП и категории сердечно-сосудистого риска;
• необоснованное и неверное установление стадии ГБ и степени АГ, категории риска;
• отсутствие сведений о наличии у пациента ПОМ, сопутствующих заболеваний и факторов риска;
при проведении лечения:
• измерение АД на высоте эффекта АГТ;
• назначение нерациональных комбинаций АГП, в неверном режиме и отсутствие интенсификации антигипертензивной терапии;
• недооценка наличия сопутствующей патологии, влияющей на выбор антигипертензивной терапии;
при обеспечении преемственности:
• отсутствие назначения повторных визитов для контроля АД;
• несвоевременная постановка на диспансерный учет;
• нерегулярность диспансерных осмотров.
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Президиум рабочей группы:
- Кобалава Ж. Д.
- Конради А. О.
- Недогода С. В.
- Шляхто Е. В.
Другие члены рабочей группы:
- Арутюнов Г. П.,
- Баранова Е. И.,
- Барбараш О. Л.,
- Бойцов С. А.,
- Вавилова Т. В.,
- Виллевальде С. В.,
- Галявич А. С.,
- Глезер М. Г.,
- Гринева Е. Н.,
- Гринштейн Ю. И.,
- Драпкина О. М.,
- Жернакова Ю. В.,
- Звартау Н. Э.,
- Кисляк О. А.,
- Козиолова Н. А.,
- Космачева Е. Д.,
- Котовская Ю. В.,
- Либис Р. А.,
- Лопатин Ю. М.,
- Небиридзе Д. В.,
- Недошивин А. О.
- Остроумова О. Д.,
- Ощепкова Е. В.,
- Ратова Л. Г.,
- Скибицкий В. В.,
- Ткачева О. Н.,
- Чазова И. Е,
- Чесникова А. И.,
- Чумакова Г. А.,
- Шальнова С. А.,
- Шестакова М. В.,
- Якушин С. С.,
- Янишевский С. Н.
Члены Рабочей группы подтвердили отсутствие финансовой поддержки/конфликта интересов. В случае сообщения о наличии конфликта интересов член(ы) рабочей группы был(и) исключен(ы) из обсуждения разделов, связанных с областью конфликта интересов.
Приложение А2. Методология разработки клинических рекомендаций
Представленные Рекомендации разработаны на основе Рекомендаций РМОАГ 2019 г. по диагностике и лечению артериальной гипертензии и Рекомендаций по лечению артериальной гипертензии Европейского общества кардиологов 2018 года [28, 29].
В Рекомендациях, основанных на результатах крупнейших эпидемиологических, рандомизированных клинических исследований и метаанализов, обобщены и изложены основные принципы лечения пациентов с АГ в целом и в особых клинических ситуациях. Основная цель Рекомендаций — облегчить принятие решения при выборе оптимальной стратегии лечения конкретного пациента с АГ. Тем не менее окончательное решение о лечении должно быть принято с учетом индивидуальных особенностей механизмов развития и течения заболевания (например, солечувствительность, вторичный гиперальдостеронизм, индивидуальная чувствительность к АГП).
Целевая аудитория данных клинических рекомендаций:
1. Врач-кардиолог.
2. Врач-терапевт.
3. Врач общей практики.
4. Врач-эндокринолог.
5. Врач-невролог
Вследствие того, что члены Российского кардиологического общества входят в состав Европейского общества кардиологов и также являются его членами, все рекомендации Европейского общества кардиологов (ЕОК) формируются с участием российских экспертов, которые являются соавторами европейских рекомендаций. Таким образом, существующие рекомендации ЕОК отражают общее мнение ведущих российских и европейских кардиологов. В связи с этим формирование Национальных рекомендаций проводилось на основе рекомендаций ЕОК, с учетом национальной специфики, особенностей обследования, лечения, учитывающие доступность медицинской помощи. По этой причине в тексте настоящих клинических рекомендаций, одновременно использованы две шкалы оценки достоверности доказательств тезисов рекомендаций: уровни достоверности доказательств ЕОК с УУР и УДД. Добавлены классы рекомендаций ЕОК, позволяющие оценить необходимость выполнения тезиса рекомендаций (Таблицы 1, 2, 3, 4,5 ).
Таблица 1/А2 — Шкала оценки классов рекомендаций Европейского общества кардиологов (ЕОК).
Таблица 2/А2 — Шкала оценки уровней достоверности доказательств Европейского общества кардиологов (ЕОК).
Таблица 3/А2 — Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
Уровни достоверности доказательств (УДД) Приказ Министерства здравоохранения Российской Федерации от 28.02.2019 № 103н «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации» |
|
| 1 | Систематический обзор рандомизированных клинических исследований с применением метаанализа |
| 2 | Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа |
| 3 | Нерандомизированные сравнительные исследования, в том числе когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая или серии случаев, исследование «случай–контроль» |
| 5 | Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 4/А2. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Таблица 5/А2. Шкала оценки уровней убедительности рекомендаций(УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
Уровень убедительности рекомендации (УРР), Приказ Министерства здравоохранения Российской Федерации от 28.02.2019 № 103н «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации» (Зарегистрирован 08.05.2019 № 54588) |
|
| А | Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
| В | Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными). |
| С | Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными). |
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию — не реже чем один раз в три года или при появлении новой информации о тактике ведения пациентов с данным заболеванием. Решение об обновлении принимает МЗ РФ на основе предложений, представленных медицинскими некоммерческими профессиональными организациями. Сформированные предложения должны учитывать результаты комплексной оценки лекарственных препаратов, медицинских изделий, а также результаты клинической апробации.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов инструкции по применению лекарственного препарата
1. Приказ Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. № 918н «Об утверждении Порядка оказания медицинской помощи больным с сердечно-сосудистыми заболеваниями».
2. Стандарт медицинской помощи больным эссенциальной первичной артериальной гипертензией (при оказании специализированной помощи), утвержден приказом Министерства здравоохранения и социального развития Российской Федерации от 13 июня 2007г. № 419.
3. Приказ Министерства здравоохранения Российской Федерации от 15 июля 2016 г. № 520н «Об утверждении критериев оценки качества медицинской помощи»
4. Приказ Министерства здравоохранения Российской Федерации от 28.02.2019 № 103н «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации» (Зарегистрирован 08.05.2019 № 54588)
Приложение Б. Алгоритмы действий врача
Приложение Б2. Алгоритм лечения АГ I–II стадий
Этот алгоритм подходит для большинства пациентов с ПОМ, а также может быть использован при лечении пациентов с цереброваскулярной болезнью, СД или заболеваниями периферических артерий.
Приложение Б3. Стратегия лекарственной терапии при сочетании АГ и ХБП
1У пациентов с ХБП, получающих антигипертензивную терапию, особенно ИАПФ или БРА, можно ожидать повышения уровня креатинина. Значительное повышение уровня креатинина на фоне назначения блокаторов РААС требует обследования пациента для исключения реноваскулярного заболевания.
2Диуретик — тиазидный или тиазидоподобный диуретик. Оценить целесообразность назначения петлевых диуретиков у пациентов с отеками.
3Риск гиперкалиемии при назначении спиронолактона, особенно при исходной СКФ <45 мл/мин/1,73 м2 и уровне калия 4,5 ммоль/л.
Приложение Б4. Стратегия лекарственной терапии при сочетании АГ и ИБС
Приложение Б5. Стратегия лекарственной терапии при сочетании АГ и ХСН со сниженной ФВ левого желудочка
Приложение Б6. Стратегия лекарственной терапии при сочетании АГ и ФП
Оральные антикоагулянты должны быть назначены по показаниям в соответствии с оценкой риска по CHA2DS2Vasc при отсутствии противопоказаний.
Приложение В. Информация для пациентов
Гипертоническая болезнь — заболевание, основным симптомом которого является повышение артериального давления выше 140/90 мм рт. ст., что приводит к поражению мозга, сердца, почек.
Только 50% людей̆ с повышенным артериальным давлением знают, что больны, из них систематически лечатся далеко не все. Нелеченная гипертоническая болезнь опасна осложнениями, главные из которых — инсульт, инфаркт миокарда, сердечная недостаточность, почечная недостаточность.
Главным фактором снижения риска смерти, инсульта и инфаркта миокарда является контроль АД и поддержание его на уровне как минимум <140/90 мм рт. ст., поэтому важен самоконтроль АД в домашних условиях с использованием сертифицированных аппаратов для измерения АД.
При этом необходимо выполнение следующих правил:
• перед измерением АД необходимы минимум 5 мин отдыха в положении сидя;
• сидеть во время измерения АД нужно с полной опорой стоп на пол, не перекрещивая и не поджимая ноги, положив руку на стол так, чтобы наложенная на плечо манжета была на уровне сердца, спина и рука с манжетой должны быть расслаблены;
• необходимо выполнять минимум 2 последовательных измерения АД утром и вечером ежедневно, хотя бы за 7 дней до планового визита к врачу или после изменения терапии; следует записывать результаты измерений в дневник самоконтроля;
• минимум за 30 мин до измерения АД не следует курить и употреблять кофеинсодержащие напитки;
• во время измерения АД одежда не должна плотно охватывать плечо, создавая складки и дополнительную компрессию.
Пациент и члены его семьи должны владеть методикой измерения АД, уметь вести дневник АД с записью цифр.
Если пациент получает антигипертензивные препараты, он должен быть осведомлен об ожидаемом эффекте, изменениях самочувствия и качестве жизни в ходе терапии, возможных побочных эффектах и способах их устранения.
Пациент должен знать об имеющихся у него и членов его семьи сердечно-сосудистых факторах риска — это курение, избыточная масса тела, психоэмоциональный стресс, малоподвижный образ жизни, повышенный уровень холестерина. Влияние указанных факторов риска может быть снижено. Особенно важна коррекция изменяемых факторов риска при наличии у пациента и членов его семьи некорригируемых факторов риска, к которым относятся: наличие в семейном анамнезе ранних мозговых инсультов, инфарктов ммммиокарда, сахарного диабета; мужской пол; пожилой возраст; физиологическая или хирургическая менопауза у женщин.
Коррекцию факторов риска требуется проводить не только пациенту, но и членам его семьи. Она осуществляется путем реализации программ семейной первичной профилактики и воспитания, составленных врачом.
• индекс массы тела (Кетле) = масса тела в килограммах/(рост в м2)
15–19,9 кг/м2 — недостаточная масса тела;
20–24,9 кг/м2 — нормальная масса тела (целевой уровень);
25–29,9 кг/м2- избыточная масса тела;
30–39,9 кг/м2 — ожирение;
40 кг/м2 — выраженное ожирение.
• индекс талия/бедра (ИТБ): ИТБ = ОТ/ОБ, где ОТ (окружность талии) — наименьшая окружность, измеренная над пупком; ОБ (окружность бедер) — наибольшая окружность, измеренная на уровне ягодиц.
0,8–0,9 — промежуточный тип распределения жировой ткани,
< 0,8 — гиноидный (бедренно-ягодичный),
>0,9 — андроидный (абдоминальный);
• Интерпретация уровня холестерина плазмы:
— целевой уровень ХС ЛНП для пациентов с очень высоким риском < 1,8 ммоль/л или его снижение не менее чем на 50% от исходного уровня, если он находился в диапазоне 1,8-3,5 ммоль/л (70–135 мг/дл)
— целевой уровень ХС ЛНП для пациентов с высоким риском < 2,6 ммоль/л или его снижение не менее чем на 50% от исходного уровня, если он находился в диапазоне 2,6–5,2 ммоль/л (100–200 мг/дл)
— целевой уровень ХС ЛНП для пациентов с низким и умеренным риском по шкале SCORE <3 ммоль/л
— ЛПВП >1,2 ммоль/л (у женщин), >1,0 ммоль/л (у мужчин),
— триглицеридов < 1,7 ммоль/л
• уровень глюкозы в плазме натощак не выше 6,1 ммоль/л;
• уровень мочевой кислоты сыворотки крови<420 мкмоль/л (у мужчин), < 360 мкмоль/л (у женщин).
Советы пациенту и его семье:
• Достаточным считается сон не менее 7 часов в сутки.
• Масса тела должна приближаться к идеальной (ИМТ менее 25 кг/м2). Для этого суточная калорийность пищи в зависимости от массы тела и характера работы должна составлять от 1500 до 2000 ккал. Потребление белка — 1 г/кг массы тела в сутки, углеводов — до 50г/сут, жиров — до 80 г/сут. Желательно вести дневник питания. Пациенту настоятельно рекомендуется избегать жирных, сладких блюд, отдавать предпочтение овощам, фруктам, злаковым и хлебу грубого помола.
• Потребление соли надо ограничить до 5 г/сут. Рекомендовано не подсаливать пищу, заменять соль другими веществами, улучшающими вкус пищи (соусы, небольшие количества перца, уксуса и др.) В соли содержится натрий, который приводит к задержке воды в организме, и как следствие, повышению артериального давления. Так же влияет большое содержание натрия в колбасах, консервах, солениях и копченых мясных продуктах.
• Следует увеличить потребление калия (его много в свежих фруктах, овощах, кураге, печеном картофеле). Соотношение К+/Nа+сдвигается в сторону К+ при преимущественно вегетарианской диете.
• Необходимо прекратить или ограничить курение.
• Потребление алкоголя следует ограничить до 30 мл/сут в пересчете на абсолютный этанол. Крепкие спиртные напитки лучше заменить красными сухими винами.
• При гиподинамии (сидячая работа > 5 ч/сут, физическая активность < 10 ч/нед) — регулярные физические тренировки не менее 4 раз в неделю продолжительностью 30–45 минут. Предпочтительны индивидуально приемлемые для пациента нагрузки: пешие прогулки, теннис, езда на велосипеде, ходьба на лыжах, работа в саду, плавание. При физической нагрузке число сердечных сокращений должно увеличиваться не более чем на 20–30 в 1 мин.
• Психоэмоциональный стресс на производстве и в быту контролируется правильным образом жизни. Следует ограничить продолжительность рабочего дня и домашних нагрузок, избегать ночных смен, командировок.
• Женщинам, больным гипертонической болезнью, надо отказаться от приема пероральных контрацептивов.
• Юношам, занимающимся спортом, нельзя злоупотреблять пищевыми добавками для наращивания мышечной массы и исключить прием анаболических стероидов.
Приложение Г1. Правила измерения АД, классификация уровней АД и основная информация, которая должна быть получена при сборе анамнеза
Таблица П1/Г1. Правила измерения АД
Измерение артериального давления в кабинете врача
АД — артериальное давление, САД — систолическое артериальное давление; ДАД — диастолическое артериальное давление.
Таблица П2/Г1. Классификация АД, измеренного в медицинском учреждении, и определение степеней гипертензии
САД — систолическое артериальное давление; ДАД — диастолическое артериальное давление.
Таблица П3/Г1. Основная информация, которая должна быть получена при сборе анамнеза
Приложение Г2. Принципы диагностики и оценки сердечно-сосудистого риска
Таблица П1/Г2. Скрининг и диагностика артериальной гипертензии
Таблица П2/Г2. Частые причины вторичных гипертензий
| Причина | Распространенность среди пациентов АГ | Возможные симптомы и признаки | Обследование |
| Синдром обструктивного апноэ во время сна | 5–10% | Храп; ожирение (но может встречаться при отсутствии ожирения); сонливость днем | Шкала Эпворта и полисомнография |
| Ренопаренхиматозные заболевания | 2–10% | Бессимптомное течение; сахарный диабет; гематурия, протеинурия, никтурия; анемия, образование почек при поликистозе у взрослых | Креатинин и электролиты плазмы, СКФ; анализ мочи на кровь и белок, отношение альбумин/креатинин мочи; ультразвуковое исследование почек |
| Реноваскулярные заболевания | |||
| Атеросклероз почечных артерий | 1–10% | Пожилые; диффузный атеросклероз (особенно периферических артерий); диабет; курение; рецидивирующий отек легких; шум в проекции почечных артерий. | Дуплексное сканирование почечных артерий или КТ-ангиография или МР-ангиография |
| Фибромускулярная дисплазия почечных артерий | Молодые; чаще у женщин; шум в проекции почечных артерия | ||
| Эндокринные причины | |||
| Первичный альдостеронизм | 5–15% |
Спонтанная или индуцированная диуретиками гипокалиемия, гипертензия в сочетании с надпочечниковой инсиденталомой, или синдромом сонного апноэ или семейным анамнезом гипертензии в раннем возрасте (до 40 лет), семейным анамнезом первичного гиперальдостеронизма (родственники 1-й линии родства) |
Ренин, альдостерон плазмы (исследование проводят на нормокалиемии и через 6 недель после отмены верошпирона); трактуют результаты с учетом антигипертензивой терапии, которую получает пациент |
| Феохромоцитома | <1% | Периодические симптомы: эпизоды повышения АД, головная боль, потливость, сердцебиения и бледность; лабильное АД; подъемы АД могут быть спровоцированы приемом препаратов (ББ, метоклопрамида, симпатомиметиков, опиоидов, трициклических антидепрессантов) | Метанефрины в плазме или суточной моче |
| Синдром Кушинга | <1% | Лунообразное лицо, центральное ожирение, атрофия кожи, стрии, диабет, длительный прием стероидов | Проба с 1 мг дексаметазона, и/или кортизол слюны в 23:00–00:00, и/или суточная экскреция свободного кортизола с мочой — исключить прием глюкокортикоидов! |
| Заболевания щитовидной железы (гипер- или гипотиреоз) | 1–2% | Признаки и симптомы гипер- или гипотиреоза | Оценка функции щитовидной железы (ТТГ, Т4, Т3) |
| Гиперапаратиреоз | <1% | Гиперкальциемия, гипофосфатемия | Паратгормон, уровень кальция |
| Акромегалия | Увеличение акральных частей тела, укрупнение и огрубление черт лица, потливость | Инсулиноподобный фактор роста (ИФР-1) сыворотки крови | |
| Другие причины | |||
| Коарктация аорты | <1% | Обычно выявляется у детей или подростков; разница АД (≥20/10 мм рт. ст.) между верхними и нижними конечностями и/или между правой и левой рукой и задержка радиально-феморальной пульсации; низкий ЛПИ; систолический шум в межлопаточной области; узурация ребер при рентгенографии | Эхокардиография |
Таблица П3/Г2. Основные требования к физическому обследованию
| Антропометрические показатели |
| Определение веса и роста с помощью калиброванных приборов, расчет ИМТ |
| Окружность талии |
| Признаки ПОМ |
| Неврологическое обследование и оценка когнитивного статуса |
| Фундоскопия для выявления гипертонической ретинопатии |
| Пальпация и аускультация сердца, сонных и почечных артерий |
| Пальпация периферических артерий |
| Определение АД на обеих руках (как минимум однократно) |
| Вторичные гипертензии |
| Осмотр кожных покровов: признаки нейрофиброматоза (феохромоцитома) |
| Пальпация почек для исключения их увеличения при поликистозе |
| Аускультация сердца и почечных артерий для выявления шумов, являющихся признаком коарктации аорты или реноваскулярной гипертензии |
| Сравнение пульсации на радиальных и бедренных артериях для выявления задержки пульсовой волны при коарктации аорты |
|
Признаки синдрома Кушинга (сочетание 2 или более симптомов): центральное ожирение, проксимальная мышечная слабость, подкожные кровоизлияния, широкие и глубокие стрии, необъяснимый остеопороз, гипокалиемия, вновь начавшийся СД, аменорея, инсиденталома надпочечника |
|
Признаки акромегалии увеличение акральных частей тела, укрупнение и огрубление черт лица, потливость |
|
Признаки заболеваний щитовидной железы (синдром гипотиреоза): склонность к брадикардии; плохая переносимость холода (зябкость); нарушения стула по типу запора; диффузная алопеция, раннее поседение волос, дистрофии ногтевых пластин (важен факт появления в недавнем анамнезе, возможен неудачный опыт лечения у дерматолога); нарушения менструальной функции у женщин (по типу олиго-, опсо-, аменореи), анамнез бесплодия, невынашивания беременности) |
|
Признаки заболеваний щитовидной железы (синдром тиреотоксикоза): • склонность к тахикардии (нарушения ритма в анамнезе — фибрилляция и трепетание предсердий, суправентрикулярные тахикардии, частые наджелудочковые и желудочковые экстрасистолии); • плохая переносимость тепла; • потливость, кожа влажная, горячая • потеря массы тела • диарея; • нарушения менструальной функции у женщин (по типу олиго-, опсо-, аменореи), анамнез бесплодия, невынашивания беременности); • глазные симптомы: Грефе — отставание верхнего века от края роговицы при движении глазного яблока вниз. Кохера — отставание движения глазного яблока от такового верхнего века при взгляде вверх, в связи с чем обнаруживается участок склеры между верхним веком и радужкой. Краузе — усиленный блеск глаз. Дальримпля — широкое раскрытие глазных щелей — «удивленный взгляд». Розенбаха — мелкое и быстрое дрожание опущенных или слегка сомкнутых век. Штельвага — редкие и неполные мигательные движения всочетании с ретракцией верхнего века. Мебиуса — нарушение конвергенции. Меланодермия в области век (симптом Еллинека) • эндокринная офтальмопатия — выраженный экзофтальм, нередко имеющий несимметричный характер, диплопия при взгляде в одну из сторон или вверх, слезотечение, ощущение песка в глазах, отечность век. • тремор пальцев вытянутых рук, иногда всего тела (симптом телеграфного столба). |
|
Признаки гиперпаратиреоза: • нефролитиаз, • вторичный остеопороз, • мышечная слабость, • боли в мышцах. |
Таблица П4/Г2. Рутинное обследование пациентов с АГ
| Гемоглобин и/или гематокрит |
| Глюкоза и гликозилированный гемоглобин |
| Липиды крови: ОХС, ХС ЛНП, ХС ЛВП |
| Триглицериды |
| Калий, натрий |
| Мочевая кислота |
| Креатинин и расчетная СКФ |
| Показатели функции печени |
| Анализ мочи: микроскопия осадка, качественная оценка протеинурии тест-полоской, отношение альбумин–креатинин в разовой порции мочи (оптимально) |
| ЭКГ в 12 отведениях |
Таблица П5/Г2.Обследование для выявления поражения органов-мишеней
| Показание и интерпретация | |
| Первичные тесты для выявления ПОМ | |
| ЭКГ в 12 отведениях | Скрининг для выявления ГЛЖ и других возможных аномалий, а также для документирования сердечного ритма и выявления аритмий |
| Отношение альбумин–креатинин в разовой порции мочи | Для выявления альбуминурии, что указывает на возможное поражение почек |
| Креатинин и расчетная СКФ | Для выявления поражения почек |
| Фундоскопия | Для выявления гипертонической ретинопатии, особенно у больных АГ 2-й или 3-й степеней |
| Детальное обследование для выявления ПОМ | |
| Эхокардиография | Для оценки структуры и функции сердца, если эта информация может повлиять на выбор тактики лечения |
| УЗИ сонных артерий | Для выявления наличия атеросклеротических бляшек или стенозов сонных артерий, особенно у пациентов с ЦВБ или признаками поражения сосудов других локализаций |
| Ультразвуковое и допплеровское исследование брюшной полости |
– Для оценки размеров и структуры почек (например, рубцовые изменения) и исключения обструктивного поражения мочевыводящих путей как причины ХБП и АГ – Оценить состояние брюшной аорты, исключить аневризму и поражение сосудов – Обследовать надпочечники для исключения аденомы или феохромоцитомы (для тщательного обследования предпочтительно выполнить КТ или МРТ); – Допплеровское исследование почечных артерий для исключения реноваскулярных заболеваний, особенно при выявлении асимметрии размеров почек |
| СПВ | Показатель аортальной жесткости и артериосклероза |
| ЛПИ | Скрининг для выявления атеросклероза нижних конечностей |
| Оценка когнитивных функций | Для оценки когнитивных функций у больных с признаками их нарушений |
| Визуализация головного мозга | Для оценки наличия ишемического или геморрагического повреждения головного мозга, особенно у пациентов с ЦВБ в анамнезе или признаками ухудшения когнитивных функций |
Сокращения: АГ — артериальная гипертензия, ГЛЖ — гипертрофия левого желудочка, КТ — компьютерная томография, ЛПИ — лодыжечно-плечевой индекс, МВП — мочевыводящие пути, МРТ — магнитно-резонансная томография, ПООГ — поражение органов-мишеней, опосредованное гипертензией, СКФ — скорость клубочковой фильтрации, СПВ — скорость пульсовой волны, ХБП — хроническая болезнь почек, ЦВБ — цереброваскулярная болезнь, ЭКГ — электрокардиограмма.
Таблица П6/Г2. Эхокардиографические критерии гипертрофии левого желудочка, концентрического ремоделирования, размеров полости левого желудочка и дилатации левого предсердия
ГЛЖ — гипертрофия левого желудочка, ЛЖ — левый желудочек, ЛП — левое предсердие, ОТС — относительная толщина стенок, ПТТ — площадь поверхности тела.
Таблица П7/Г2. Клинические показания для домашнего (ДМАД) и суточного мониторирования АД (СМАД)
СМАД — суточное мониторирование АД; ДМАД — домашнее мониторирование АД
Таблица П8/Г2. Сравнение методов суточного и домашнего мониторирования артериального давления
| СМАД | ДМАД |
|
Преимущества: Позволяет идентифицировать гипертензию «белого халата» и маскированную гипертензию Более существенная прогностическая значимость Ночные измерения Измерения проводятся в условиях реальной жизни Дополнительное прогностическое значение разных фенотипов АД Большой объем информации на основании одного исследования, включая краткосрочную вариабельность АД |
Преимущества: Позволяет идентифицировать гипертензию «белого халата» и маскированную гипертензию Дешевизна и широкая доступность Измерения в домашних условиях, которые предоставляют больший комфорт, чем кабинет врача Вовлечение пациента в процесс измерения АД Легко выполнимо, может быть использовано в течение длительного периода времени для оценки вариабельности АД от дня ко дню |
|
Недостатки: Дороговизна и иногда ограниченная доступность Может доставлять дискомфорт |
Недостатки: Возможно только статичное измерение АД Возможны ошибки измерений Отсутствие ночных измерений |
АД — артериальное давление, СМАД — суточное мониторирование артериального давления, ДМАД — домашнее мониторирование артериального давления.
Таблица П9/Г2. Определение артериальной гипертензии в зависимости от метода измерения АД: измеренного в медицинском учреждении, СМАД или ДМАД
Таблица П10/Г2. Этапы оценки сердечно-сосудистого риска
| Этапы обследования | Необходимые процедуры |
| Клиническая оценка | Выявление пациентов высокого и очень высокого риска на основании документированных ССЗ, СД, ХБП 3–5-й стадий, чрезмерного повышения отдельных факторов риска, семейной гиперхолестеринемии или высокого риска по SCORE |
| Оценка 10-летнего риска по шкале SCORE | Проводить оценку риска по SCORE рекомендовано у бессимптомных лиц старше 40 лет, без анамнеза ССЗ, СД, ХБП, семейной гиперхолестирнемии или повышения ХС-ЛНП >4,9 ммоль/л (>190 мг/дл) |
| Оценка факторов, изменяющих риск | У отдельных пациентов низкого или умеренного риска целесообразно оценвать дополнительные факторы, которые могут повлиять на стратификацию по риску и выбор тактики лечения: повышение аполипопротеина В, липопротеина (а) или С-реактивного белка, семейный анамнез ранних атеросклеротических ССЗ, выявление атеросклеротической бляшки |
| Стратификация риска сердечно-сосудистых осложнений у пациентов с АГ | На основании уровня АД, наличия ФР, ПОМ, АКС, ХБП 3–5-й стадий, СД |
АГ — артериальная гипертензия, АД — артериальное давление, АКС — ассоциированное клиническое состояние, ПОМ — поражение органов-мишеней, СД — сахарный диабет, ССЗ — сердечно-сосудистое заболевание, ХБП — хроническая болезнь почек, ХС-ЛНП — холестерин липопротеинов низкой плотности, ФР — факторы риска.
Приложение Г3. Шкала SCORE
Название на русском языке: Шкала SCORE
Оригинальное название (если есть): SCORE scale (Systematic COronary Risk Evaluation)
Источник (официальный сайт разработчиков, публикация с валидацией): http://www.heartscore.org/ru_RU
Тип (подчеркнуть):
— шкала оценки
— индекс
— вопросник
— другое (уточнить):
Назначение: клинический инструмент для оценки риска смертельного сердечно-сосудистого заболевания в течение 10 лет. Настоящая шкала разработана для стран с высоким уровнем смертности от ССЗ (включая Россию) на основании следующих факторов: возраст, пол, курение, уровень систолического АД и ОХС. Уровень ХС ЛВП не учитывается. Общая оценка риска с помощью SCORE рекомендуется у бессимптомных взрослых старше 40 лет, без ССЗ, СД, ХБП или СГХС.
Содержание (шаблон):
Ключ (интерпретация): Уровень суммарного СС риск по шкале SCORE: менее 1% — низкий. от 1 до 4% — средний или умеренно повышенный. от 5% до 9% — высокий. >10% — очень высокий.
Пояснения: нет
Таблица П12/Г2. Шкала глобальной оценки 10-летнего сердечно-сосудистого риска
1 ИБС: стенокардия напряжения 3-4 ФК, нестабильная стенокардия, перенесенный инфаркт миокарда, ишемический инсульт, ЧКВ, операция КШ, ангиопластика сонных артерий или артерий нижних конечностей, каротидная эндартерэктомия, подвздошно-бедренное, бедренно-подколенное шунтирование.
2 Инфаркт миокарда, нестабильная стенокардия, перемежающаяся хромота, транзиторная ишемическая атака/ишемический инсульт.
3 Назначение статинов в максимально переносимых дозах в сочетании с эзетимибом.
АГ — артериальная гипертензия, ХБП — хроническая болезнь почек, СКФ — скорость клубочковой фильтрации, ТИА — транзиторная ишемическая атака, CCЗ — сердечно-сосудистые заболевания, АСБ – атеросклеротическая бляшка, СГХС – семейная гиперхолестеринемия, ФР – фактор риска.
Таблица П13/Г2. Модифицирующие факторы, способствующие увеличению сердечно-сосудистого риска
Приложение Г3.1. Классификация стадий и стратификация риска при АГ
Таблица П1/Г3. Классификация стадий АГ в зависимости от уровней артериального давления, наличия факторов СС риска, поражения органов, обусловленного гипертензией, и наличия сопутствующих заболеваний
Таблица П2/Г3. Факторы, определяющие сердечно-сосудистый риск и стадию заболевания у пациентов с АГ
а — факторы риска, учтенные в шкале SCORE, b — Протеинурия и снижение СКФ являются независимыми факторами риска.
Таблица П3/Г3. Расчет СКФ по формуле CKD-EpidemiologyCollaboration 2009*
Калькулятор СКФ: https://www.kidney.org/professionals/KDOQI/gfr_calculator
Таблица П4/Г3. CHA2DS2-VASс. Шкала оценки риска тромбоэмболических осложнений у пациентов с фибрилляцией/трепетанием предсердий
Название на русском языке: CHA2DS2-VASс. Шкала оценки риска тромбоэмболических осложнений у пациентов с фибрилляцией/трепетанием предсердий
Оригинальное название (если есть): CHA2DS2-VASс
Источник (официальный сайт разработчиков, публикация с валидацией): Olesen, Jonas Bjerring, et al. Validation of risk stratification schemes for predicting stroke and thromboembolism in patients with atrial fibrillation: nationwide cohort study. Bmj 342 (2011): d124.
Тип (подчеркнуть):
— шкала оценки
— индекс
— вопросник
— другое (уточнить):
Назначение: клинический инструмент для прогнозирования риска ишемического инсульта и системного тромбоэмболизма при фибрилляции предсердий
Содержание (шаблон):
Ключ (интерпретация):
Пояснения: нет
Таблица П5/Г3. Шкала сонливости Эпворта (Epworth)
Название на русском языке: Шкала сонливости Эпворта
Оригинальное название (если есть): Epworth Sleepiness Scale
Источник (официальный сайт разработчиков, публикация с валидацией): https://epworthsleepinessscale.com/about-the-ess/
Тип (подчеркнуть):
— шкала оценки
— индекс
— вопросник
— другое (уточнить):
Назначение: серия вопросов, которые используют для изучения воздействия сна на дневной образ жизни.
Насколько вероятно то, что вы можете задремать или уснуть в ситуациях, описанных ниже, по сравнению с ощущением обычной усталости?
Речь идет об обычном вашем состоянии в последнее время. Даже если вы не были в подобных ситуациях в последнее время, то постарайтесь представить себе, как бы эти ситуации повлияли на вас. Используйте эту шкалу и выбирете наиболее подходящее число для каждой ситуации.
0 — никогда бы не заснул/не задремал
1 — очень небольшая вероятность заснуть или задремать
2 — вероятно, засну или задремлю
3 — большая вероятность заснуть или задремать
Ключ (интерпретация):
1 — 6 баллов: Нормальный сон
7 — 8 баллов: Умеренная сонливость
9 — 24 баллов: Аномальная (возможно, патологическая) сонливость
Пояснения: нет
Таблица П6/Г3. Опросник «Возраст не помеха»
Название на русском языке: Возраст не помеха
Оригинальное название (если есть):
Источник (официальный сайт разработчиков, публикация с валидацией): Общероссийская общественная организация «Российская ассоциация геронтологов и гериатров «Клинические рекомендации «Старческая астения» 2018 г.
Тип (подчеркнуть):
— шкала оценки
— индекс
— вопросник
— другое (уточнить):
Назначение: серия вопросов, которые используют для изучения воздействия сна на дневной образ жизни.
Содержание (шаблон):
Ключ (интерпретация):
за каждый положительный ответ начисляется 1 балл.
3 балла и более — высокая вероятность синдрома старческой астении, необходима консультация гериатра
1–2 балла — вероятен синдром старческой астении (преастения)
0 баллов — нет ССА
Пояснения: * имеется в виду непреднамеренное снижение веса. Если пациент похудел намеренно — за счет соблюдения специальной диеты или регулярной физической активности, балл не засчитывается.
Приложение Г4. принципы антигипертензивной терапии и диспансерное наблюдение больных с АГ
Таблица П1/Г4. Начало антигипертензивной терапии (изменение образа жизни и лекарственные препараты) при различных значениях АД, измеренного в медицинском учреждении
Таблица П2/Г4. Показания к началу антигипертензивной терапии в зависимости от возраста и сопутствующих заболеваний
Таблица П3/Г4. Целевые значения АД, измеренного в медицинском учреждении, в зависимости от возраста и сопутствующих заболеваний.
аОтносится к пациентам с инсультом в анамнезе, а не к показателям АД в остром периоде инсульта.
bЦелевые значения могут меняться у пожилых пациентов с синдромом старческой астении.
Таблица П4/Г4. Противопоказания к назначению отдельных классов антигипертензивных препаратов
Таблица П5/Г4. Алгоритм диспансерного наблюдения больных АГ с контролируемым артериальным давлением на фоне приема антигипертензивных лекарственных препаратов [292]
| Заболевание, состояние | Регулярность профилактических посещений | Рекомендуемые вмешательства и методы исследования во время профилактических посещений |
| АГ 1-й степени без ПОМ, ССЗ, ЦВБ и ХБП |
Не менее 1 раза в год при контроле АД на уровне целевых значений. При стабильном течении возможно наблюдение в отделении/кабинете медицинской профилактики При рефрактерной АГ I-II степени пациент наблюдается у врача-кардиолога; при отсутствии возможности наблюдения у врача-кардиолога — у врача-терапевта/участкового врача. |
— сбор жалоб и анамнеза, активный опрос на наличие, характер и выраженность боли в грудной клетке и одышки при физической нагрузке, эпизодов кратковременной слабости в конечностях, онемения половины лица или конечностей, об объеме диуреза — уточнение факта и характера приема антигипертензивных препаратов — уточнение факта приема гиполипидемических, антиагрегантных и гипогликемических препаратов при наличии показаний — опрос и краткое консультирование по поводу курения, характера питания, физической активности — измерение АД при каждом посещении — анализ данных ДМАД — общий осмотр и объективное обследование, включая пальпацию периферических сосудов и аускультацию подключичных, сонных, почечных и бедренных артерий, измерение индекса массы тела и окружности талии при каждом посещении — глюкоза плазмы крови натощак не реже 1 раза в год (допускается экспресс-метод) — общий холестерин не реже 1 раза в год (допускается экспресс-метод) — оценкасуммарного сердечно-сосудистого риска по шкале SCORE — холестерин липопротеинов низкой плотности, холестерин липопротеинов высокой плотности, триглицериды в сыворотке при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года — калий и натрий сыворотки при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года — креатинин сыворотки (с расчетом СКФ) при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года — анализ мочи на микроальбуминурию при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года
— ЭКГ в 12 отведениях с расчетом индекса Соколова-Лайона и Корнельского показателя не реже 1 раза в год — ЭхоКГ с определением ИММЛЖ и диастолической функции при взятии под диспансерное наблюдение, в последующем по показаниям, но не менее 1 раза в 2 года при отсутствии достижения целевых значений АД и наличии признаков прогрессирования гипертрофии левого желудочка по данным расчета индекса Соколова–Лайона и Корнелльского показателя — дуплексное сканирование сонных артерий у мужчин старше 40 лет, женщин старше 50 лет при ИМТ>30 кг/м2 и более и общем холестерине >5 ммоль/л и более при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раз в 3 года с целью определения ТИМ и наличия атеросклеротических бляшек* — измерение скорости пульсовой волны на каротидно-феморальном участке артериального русла при взятии под диспансерное наблюдение, в последующем по показаниям, но не реже 1 раза в 3 года при отсутствии достижения целевых значений АД* — корректировка терапии (при необходимости) — объяснение пациенту и/или обеспечение его памяткой по алгоритму неотложных действий при жизнеугрожающем состоянии, вероятность развития которого у пациента наиболее высокая |
| АГ 2–3-й степени с ПОМ, но без ССЗ, ЦВБ и ХБП | Не менее 2 раз в год |
— сбор жалоб и анамнеза, активный опрос на наличие, характер и выраженность боли в грудной клетке и одышки при физической нагрузке, эпизодов кратковременной слабости в конечностях, онемения половины лица или конечностей, об объеме диуреза — уточнение факта и характера приема антигипертензивных препаратов — уточнение факта приема гиполипидемических, антиагрегантных и гипогликемических препаратов при наличии показаний — опрос и краткое консультирование по поводу курения, характера питания, физической активности — измерение АД при каждом посещении — анализ данных ДМАД — общий осмотр и объективное обследование, включая пальпацию периферических сосудов и аускультацию подключичных, сонных, почечных и бедренных артерий, измерение индекса массы тела и окружности талии при каждом посещении — гемоглобин и/или гематокрит при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года — глюкоза плазмы натощак не реже 1 раза в год (допускается экспресс-метод) — общий холестерин не реже 1 раза в год (допускается экспресс-метод) — холестерин липопротеинов низкой плотности, холестерин липопротеинов высокой плотности, триглицериды в сыворотке при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года — калий и натрий сыворотки при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года — мочевая кислота сыворотки при взятии под диспансерное наблюдение, далее по показаниям — креатинин сыворотки (с расчетом СКФ) при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года — анализ мочи на микроальбуминурию при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года — ЭКГ в 12 отведениях с расчетом индекса Соколова–Лайона и Корнелльского показателя не реже 1 раза в год — ЭхоКГ с определением ИММЛЖ и диастолической функции при взятии под диспансерное наблюдение, в последующем по показаниям, но не реже 1 раза в год при отсутствии достижения целевых значений АД и наличии признаков прогрессирования гипертрофии левого желудочка по данным расчета индекса Соколова–Лайона и Корнельского показателя — дуплексное сканирование сонных артерий у мужчин старше 40 лет, женщин старше 50 лет при ИМТ>30 кг/м2 и более и общем холестерине >5 ммоль/л и более при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года с целью определения ТИМ и наличия атеросклеротических бляшек* — УЗИ почек и дуплексное сканирование почечных артерий при наличии обоснованного подозрения на их патологию* — лодыжечно-плечевой индекс при наличии обоснованного подозрения на стеноз сосудов нижних конечностей* — консультация окулиста на предмет наличия кровоизлияний или экссудата на глазном дне, отека соска зрительного нерва при взятии под ДН и по показаниям — оценка суммарного сердечно-сосудистого риска по таблице величины риска при АГ и по шкале SCORE (при интерпретации уровня риска приоритет отдается более высокому показателю) — корректировка терапии (при необходимости) — объяснение пациенту и/или обеспечение его памяткой по алгоритму неотложных действий при жизнеугрожающем состоянии, вероятность развития которого у пациента наиболее высокая |
| АГ 1–3-й степени с ССЗ, ЦВБ и ХБП | Не менее 2 раз в год |
— сбор жалоб и анамнеза, активный опрос на наличие, характер и выраженность боли в грудной клетке и одышки при физической нагрузке, эпизодов кратковременной слабости в конечностях, онемения половины лица или конечностей, об объеме диуреза — уточнение факта приема антигипертензивных препаратов — уточнение факта приема гиполипидемических, антиагрегантных и гипогликемических препаратов при наличии показаний — опрос и краткое консультирование по поводу курения, характера питания, физической активности — измерение АД при каждом посещении — анализ данных ДМАД — уточнение характера гипотензивной терапии и терапии по поводу других ССЗ, ЦВБ и ХБП — общий осмотр и объективное обследование, включая пальпацию периферических сосудов и аускультацию подключичных, сонных, почечных и бедренных артерий, измерение индекса массы тела и окружности талии при каждом посещении — гемоглобин и/или гематокрит при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года — глюкоза плазмы натощак не реже 1 раза в год (допускается экспресс-метод) — общий холестерин не реже 1 раза в год (допускается экспресс-метод) — холестерин липопротеинов низкой плотности, холестерин липопротеинов высокой плотности, триглицериды в сыворотке при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года — калий и натрий сыворотки при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в год -мочевая кислота сыворотки при взятии под диспансерное наблюдение, далее по показаниям — креатинин сыворотки (с расчетом СКФ) при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в год — анализ мочи с микроскопией осадка и определением белка в моче не реже 1 раза в год — анализ на микроальбуминурию при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в год — ЭКГ в 12 отведениях с расчетом индекса Соколова–Лайона и Корнелльского показателя не реже 2 раз в год — ЭхоКГ с определением ИММЛЖ и диастолической функции при взятии под диспансерное наблюдение, в последующем по показаниям, но не менее 1 раза в год при отсутствии достижения целевых значений АД и наличии признаков прогрессирования гипертрофии левого желудочка при расчете индекса Соколова–Лайона и Корнелльского показателя — дуплексное сканирование сонных артерий у мужчин старше 40 лет, женщин старше 50 лет не реже 1 раза в 2 года с целью определения ТИМ и наличия атеросклеротических бляшек* -УЗИ почек при взятии под диспансерное наблюдение, далее по показаниям при наличии обоснованного подозрения на развитие или прогрессирование ХБП* — дуплексное сканирование почечных артерий при наличии обоснованного подозрения на их патологию* — лодыжечно-плечевой индекс при наличии обоснованного подозрения на стеноз сосудов нижних конечностей* — дуплексное сканирование подвздошных и бедренных артерий при наличии обоснованного подозрения на их патологию* — консультация окулиста на предмет наличия кровоизлияний или экссудата на глазном дне, отека соска зрительного нерва при взятии под ДН и по показаниям — оценка суммарного сердечно-сосудистого риска по таблице величины риска при АГ и по шкале SCORE (при интерпретации уровня риска приоритет отдается более высокому показателю) — корректировка терапии (при необходимости) -объяснение пациенту и/или обеспечение его памяткой по алгоритму неотложных действий при жизнеугрожающем состоянии, вероятность развития которого у пациента наиболее высокая |
Приложение Г5. Иные
Таблица П1/Г5. Распространенность и типичные причины вторичных гипертензий в различных возрастных группах
| Возрастная группа | Частота (%) | Типичные причины |
| Дети (<12 лет) | 70–85 |
Ренопаренхиматозные заболевания Коарктация аорты Моногенные заболевания |
| Подростки (12–18 лет) | 10-15 |
Ренопаренхиматозные заболевания Коарктация аорты Моногенные заболевания |
| Молодые (19–40 лет) | 5-10 |
Ренопаренхиматозные заболевания Фибромускулярная дисплазия Недиагностированные моногенные заболевания |
| Средний возраст (41–65 лет) | 5-15 |
Первичный альдостеронизм Обструктивное ночное апноэ Синдром Кушинга Феохромоцитома Ренопаренхиматозные заболевания Атеросклероз почечных артерий |
| Пожилые(>65 лет) | 5-10 |
Атеросклероз почечных артерий Ренопаренхиматозные заболевания Заболевания щитовидной железы |
Таблица П2/Г5. Редкие генетические причины вторичных артериальных гипертензий
АРП активность ренина плазмы, КАП концентрация альдостерона плазмы, КРП концентрация ренина плазмы.
Таблица П3/Г5. Лекарственные препараты и другие субстанции, приводящие к повышению артериального давления
| Препарат/субстанция | |
| Оральные контрацептивы | Особенно с содержанием эстрогенов; вызывают АГ у 5% женщин, обычно легкую, но возможна и тяжелая |
| Препараты для снижения веса | Например, фенилпропаноламин и сибутрамин |
| Назальные противоотечные препараты | Например, фенилэфрина гидрохлорид и нафазолина гидрохлорид |
| Стимуляторы | Амфетамины, кокаин, экстази; обычно вызывают острый подъем АД, а не хроническую АГ |
| Лакрица | Хроническое избыточное употребление лакрицы приводит к проявлениям, похожим на гиперальдостеронизм за счет стимуляции минералокортикоидных рецепторов и угнетения метаболизма кортизола |
| Иммуносупрессанты | Например, циклоспорин А (такролимус оказывает меньшее действие на АД, а рапамицин практически его не имеет) и стероиды (например, кортикостероиды и гидрокортизон) |
| Нестероидные противовоспалительные препараты | |
| Антиангиогенные противоопухолевые препараты | Например, ингибиторы эндотелиального сосудистого фактора роста (бевацизумаб), ингибиторы тирозинкиназы (сунитиниб) и сорафениб |
| Другие препараты и субстанции, способные повышать АД | Анаболические стероиды, эритропоэтин, растительные препараты (эфедра и марихуана) |
Таблица П4/Г5. Мероприятия, которые могут повысить приверженность пациентов с артериальной гипертензией к лекарственной терапии
| На уровне врача |
| Предоставление пациенту информации о рисках при АГ и преимуществах терапии, согласование стратегии лечения, направленной на поддержание нормального АД с использованием рекомендаций по изменению образа жизни и назначения фиксированных комбинаций; использование информационных материалов, программ обучения, консультирование с помощью компьютерных технологий |
| Получение обратной связи в отношении соблюдения рекомендаций и наличия улучшения |
| Оценка и разрешение индивидуальных проблем, препятствующих высокой приверженности к лечению |
| Сотрудничество с другими медицинскими сотрудниками |
| На уровне пациента |
| Самоконтроль АД (в том числе телемониторирование) |
| Групповые занятия и тренинги |
| Рекомендации в сочетании с мотивационными стратегиями |
| Использование систем напоминания |
| Получение поддержки семьи и общества |
| Обеспечение лекарственными препаратами на рабочем месте |
| На уровне лекарственной терапии |
| Упрощение схем приема препарата, предпочтение — фиксированным комбинациям и стратегии «одной таблетки» |
| Упаковки с системой напоминаний |
| На уровне системы здравоохранения |
| Поддержка развития систем мониторирования (телефонные контакты, посещения на дому, телемониторинг результатов домашнего контроля АД) |
| Финансовая поддержка системы взаимодействия между различными представителями системы здравоохранения (например, фармацевты и медицинские сестры) |
| Система компенсации стратегии «одной таблетки» |
| Развитие национальных баз данных, включая данные о назначении лекарственных препаратов, доступных для врачей и фармацевтов |
| Доступность препаратов |
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
|
|
Российское медицинское общество по артериальной гипертонии |
|
|
Всероссийское научное общество кардиологов |
Диагностика и лечение артериальной гипертензии
Российские рекомендации (четвертый пересмотр)
Москва 2010
Глубокоуважаемые коллеги!
За 2 года, прошедшие с выхода третьего пересмотра российских национальных рекомендаций по диагностике и лечению артериальной гипертензии, были опубликованы важные результаты новых исследований, посвященных антигипертензивной терапии. Часть из них укрепили позиции, на которых базировались рекомендации 2008 года. В то же время появилась необходимость пересмотреть некоторые из ранее существовавших представлений и добавить новые. Рекомендации дают необходимую врачу практического здравоохранения информацию о современных подходах к диагностике, формулировке диагноза и эффективного лечения пациентов с артериальной гипертонией. Часть информации носит характер руководства, которое поможет не только врачу общей практики, но и клиницисту разобраться в непростой задаче лечения больного с артериальной гипертонией и создать наиболее эффективную схему лечения. Российское медицинское общество по артериальной гипертонии и Всероссийское научное общество кардиологов надеются, что внедрение обновленных рекомендаций повысит профессиональный уровень врачей, улучшит качество оказания медицинской помощи населению и внесет весомый вклад в реализацию национальных программ по борьбе с артериальной гипертонией.
|
Президент РМОАГ, |
Президент ВНОК, |
|
|
|
Список сокращений:
АГ – артериальная гипертензия
АГП – антигипертензивные препараты
АГТ – антигипертензивная терапия
АД – артериальное давление
АК – антагонисты кальция
АКС – ассоциированные клинические состояния
АКТГ – адренокортикотропный гормон
АО – абдоминальное ожирение
АПФ – ангиотензинпревращающий фермент
АРП – активность ренина в плазме крови
АII – ангиотензин II
БА – бронхиальная астма
β-АБ – β-адреноблокатор
БРА – блокатор рецепторов АТ1
ВНОК – Всероссийское научное общество кардиологов
ГБ – гипертоническая болезнь
ГК – гипертонический криз
ГКС – глюкокортикостероиды
ГЛЖ – гипертрофия левого желудочка
ДАД – диастолическое артериальное давление
ДЛП – дислипидемия
ЕОГ – Европейское общество по артериальной гипертонии
ЕОК – Европейское общество кардиологов
ИААГ – изолированная амбулаторная АГ
ИАПФ – ингибитор ангиотензинпревращающего фермента
ИБС – ишемическая болезнь сердца
ИКАГ – изолированная клиническая артериальная гипертензия
ИМ – инфаркт миокарда
ИММЛЖ – индекс массы миокарда левого желудочка
ИМТ – индекс массы тела
ИСАГ – изолированная систолическая артериальная гипертензия
КТ – компьютерная томография
ЛЖ – левый желудочек
МАУ – микроальбуминурия
МИ – мозговой инсульт
ММЛЖ – масса миокарда левого желудочка
МРА – магнитно-резонансная ангиография
МРТ – магнитно-резонансная томография
МС – метаболический синдром
МЭН – множественная эндокринная неоплазия
НТГ – нарушенная толерантность к глюкозе
ОЖ – образ жизни
ОКС – острый коронарный синдром
ОТ – окружность талии
ОХС – общий холестерин
ПОМ – поражение органов-мишеней
РААС – ренин-ангиотензин-альдостероновая система
РЛЖ – радиус левого желудочка
РМОАГ – Российское медицинское общество по артериальной гипертонии
РФ – Российская Федерация
САД – систолическое артериальное давление
СД – сахарный диабет
СЗ – сопутствующие заболевания
СКАД – самоконтроль артериального давления
СКФ – скорость клубочковой фильтрации
СМАД – суточное мониторирование артериального давления
СОАС – синдром обструктивного апноэ во время сна
ССЗ – сердечно-сосудистые заболевания
ССО – сердечно-сосудистые осложнения
ТГ – триглицериды
ТД – тиазидные диуретики
ТЗСЛЖ – толщина задней стенки левого желудочка
ТИА – транзиторная ишемическая атака
ТИМ – толщина интима-медиа
УЗИ – ультразвуковое исследование
ФК – функциональный класс
ФР – фактор риска
ХОБЛ – хроническая обструктивная болезнь легких
ХПН – хроническая почечная недостаточность
ХС ЛПВП – холестерин липопротеидов высокой плотности
ХС ЛПНП – холестерин липопротеидов низкой плотности
ХСН – хроническая сердечная недостаточность
ЦВБ – цереброваскулярные болезни
ЭКГ – электрокардиограмма
ЭхоКГ – эхокардиография
MDRD – Modification of Diet in Renal Disease
SCORE – Systemic Coronary Risk Evaluation
1. Введение
Несмотря на усилия ученых, врачей и органов управления здравоохранением, артериальная гипертензия (АГ) в Российской Федерации (РФ) остается одной из наиболее значимых медико-социальных проблем.
Это обусловлено как широким распространением данного заболевания (около
40% взрослого населения РФ имеет повышенный уровень артериального давления (АД)), так и тем, что АГ является важнейшим фактором риска основных сердечно-сосудистых заболеваний (ССЗ) – инфаркта миокарда (ИМ) и мозгового инсульта (МИ), главным образом определяющих высокую смертность в нашей стране. По материалам обследования, проведенного в рамках целевой Федеральной программы «Профилактика и лечение АГ в Российской Федерации», распространенность АГ среди населения в 2009 г. составила 40,8% (у мужчин 36,6%, у женщин 42,9%). Осведомленность больных АГ о наличии заболевания составляет 83,9–87,1%. Принимают антигипертензивные препараты (АГП) 69,5% больных АГ, из них эффективно лечатся 27,3%, а контролируют АД на целевом уровне 23,2% пациентов [1].
Всероссийское научное общество кардиологов (ВНОК) в 2001 г. опубликовало первую версию Российских рекомендаций по профилактике, диагностике и лечению АГ, в 2004 г. вышла их вторая версия, а в 2008 г. – третья. С этого времени были получены новые данные, требующие пересмотра рекомендаций. В связи с этим по инициативе Российского медицинского общества по АГ (РМОАГ) и ВНОК разработаны данные рекомендации по диагностике и лечению АГ.
В основу настоящего документа легли рекомендации по лечению АГ Европейского общества по артериальной гипертонии (ЕОГ) и Европейского общества кардиологов (ЕОК) 2007 г. и 2009 г. [2, 3] и результаты крупных российских исследований по проблеме АГ. Так же как и в предшествующих версиях рекомендаций, величина АД рассматривается как один из элементов системы стратификации общего (суммарного) сердечно-сосудистого риска. При оценке общего сердечно-сосудистого риска учитывается большое количество переменных, но величина АД является определяющей в силу своей высокой прогностической значимости. При этом уровень АД является наиболее регулируемой переменной в системе стратификации. Как показывает опыт, эффективность действий врача при лечении каждого конкретного пациента и достижение успехов по контролю АД среди населения страны в целом в значительной степени зависят от согласованности действий и терапевтов, и кардиологов, что обеспечивается единым диагностическим и лечебным подходом. Именно эта задача рассматривалась в качестве основной при подготовке рекомендаций.
2. Определение
Под термином «артериальная гипертензия» подразумевают синдром повышения АД при гипертонической болезни (ГБ) и симптоматических АГ.
Термин «гипертоническая болезнь», предложенный Г.Ф.Лангом в 1948 г., соответствует употребляемому в других странах понятию «эссенциальная гипертензия».
Под ГБ принято понимать хронически протекающее заболевание, основным проявлением которого является АГ, не связанная с наличием патологических процессов, при которых повышение АД обусловлено известными, в современных условиях часто устраняемыми причинами (симптоматические АГ). В силу того что ГБ – гетерогенное заболевание, имеющее довольно отчетливые клинико-патогенетические варианты с существенно различающимися на начальных этапах механизмами развития, в научной литературе вместо термина «гипертоническая болезнь» часто используется понятие «артериальная гипертензия».
3. Классификация АГ
3.1. Определение степени повышения АД
Классификация уровней АД у лиц старше 18 лет представлена в таблице 1. Если значения систолического АД (САД) и диастолического АД (ДАД) попадают в разные категории, то степень тяжести АГ оценивается по более высокой категории. Наиболее точно степень АГ может быть определена только у пациентов с впервые диагностированной АГ и у больных, не принимающих АГП. Результаты суточного мониторирования АД (СМАД) и самостоятельных измерений АД больными на дому могут помочь в диагностике АГ, но не заменяют повторные измерения АД в лечебном учреждении. Критерии диагностики АГ по результатам СМАД, измерений АД, сделанных врачом и самим пациентом в домашних условиях, различны. О наличии АГ при оценке результатов СМАД свидетельствует среднесуточное АД ≥130/80 мм рт. ст., при самостоятельном измерении пациентом в домашних условиях АД ≥135/85 мм рт. ст. и при измерении медицинским работником АД ≥140/90 мм рт. ст. (таблица 2).
| Категория АД | Систолическое АД | Диастолическое АД | |
|---|---|---|---|
|
Оптимальное |
<120 |
и |
<80 |
|
Нормальное |
120–129 |
и/или |
80–84 |
|
Высокое нормальное |
130–139 |
и/или |
85–89 |
|
АГ 1-й степени |
140–159 |
и/или |
90–99 |
|
АГ 2-й степени |
160–179 |
и/или |
100–109 |
|
АГ 3-й степени |
≥180 |
и/или |
≥110 |
|
Изолированная систолическая АГ* |
≥140 |
и |
<90 |
|
* ИСАГ должна классифицироваться на 1, 2, 3 степень согласно уровню систолического АД. |
| Показатель | Систолическое АД | Диастолическое АД | |
|---|---|---|---|
|
Клиническое или офисное АД |
140 |
и/или |
90 |
|
СМАД: среднесуточное АД |
125–130 |
и/или |
80 |
|
Дневное АД |
130–135 |
и/или |
85 |
|
Ночное АД |
120 |
и/или |
70 |
|
Домашнее АД |
130–135 |
и/или |
85 |
Следует иметь в виду, что критерии повышенного АД в значительной мере являются условными, поскольку между уровнем АД и риском ССЗ существует прямая связь, начиная с величины 115/75 мм рт. ст. Однако использование классификации уровня АД упрощает диагностику и лечение АГ в повседневной практике.
3.2. Факторы, влияющие на прогноз, и оценка общего (суммарного) сердечно-сосудистого риска
Величина АД является важнейшим, но далеко не единственным фактором, определяющим тяжесть АГ, ее прогноз и тактику лечения. Большое значение имеет оценка общего сердечно-сосудистого риска, степень которого зависит от величины АД, а также наличия или отсутствия сопутствующих факторов риска (ФР), поражения органов-мишеней (ПОМ) и ассоциированных клинических состояний (АКС) (таблица 3).
| *Факторы риска* | *Поражение органов мишеней* |
|---|---|
|
ГЛЖ
Сосуды
Почки
|
|
Сахарный диабет |
Ассоциированные клинические состояния |
|
ЦВБ
Заболевания сердца
Заболевания почек
Заболевания периферических артерий
Гипертоническая ретинопатия
|
|
Метаболический синдром |
|
|
Основной критерий – АО (ОТ>94 см для мужчин и >80 см для женщин)
|
|
|
*При диагностике МС используются критерии, указанные в данной таблице в подразделе «Метаболический синдром». |
По сравнению с предыдущими рекомендациями изменились критерии диагностики метаболического синдрома (МС) [4]. Значения общего холестерина (ОХС), холестерина липопротеидов низкой плотности (ХС ЛПНП), холестерина липопротеидов высокой плотности (ХС ЛПВП) и триглицеридов (ТГ) для диагностики дислипидемии (ДЛП) соответствуют Российским рекомендациям по диагностике и коррекции нарушений липидного обмена [5].
В диагностике поражения сосудов по-прежнему используются такие критерии, как величина скорости пульсовой волны на участке между сонной и бедренной артериями более 12 м/с и лодыжечно-плечевой индекс менее 0,9, а при оценке поражения почек уменьшение скорости клубочковой фильтрации (СКФ) <60 мл/мин/1,73 м2 (MDRD формула*) или клиренс креатинина ниже 60 мл/мин (формула Кокрофта-Гаулта**).

В зависимости от степени повышения АД, наличия ФР, ПОМ и АКС все больные АГ могут быть отнесены к одной из четырех групп риска: низкого, среднего, высокого и очень высокого дополнительного риска (таблица 4). Термин «дополнительный риск» используется, чтобы подчеркнуть, что риск сердечно-сосудистых осложнений (ССО) и смерти от них у пациентов с АГ всегда больше, чем средний риск в популяции. Эта система стратификации риска, учитывающая собственно ФР, ПОМ, сахарный диабет (СД), МС и АКС, разработана на основании результатов Фрамингемского исследования (Фрамингемская модель). Она достаточно проста, удобна в использовании и имеет большое значение при выборе тактики лечения больных (стартовая терапия АГ, определение целевого уровня АД и конечных целей лечения, необходимость назначения комбинированной терапии, потребность в статинах и других негипотензивных препаратах), которая зависит от начального уровня общего сердечно-сосудистого риска. По этой системе стратификации риск ССО определяется врачом после завершения полного обследования пациента.
|
ФР, ПОМ и СЗ |
АД, мм рт. ст. |
||
|
АГ 1-й степени 140–159/90–99 |
АГ 2-й степени 160–179/100–109 |
АГ 3-й степени ≥180/110 |
|
|
Нет ФР |
Низкий дополнительный риск |
Средний дополнительный риск |
Высокий дополнительный риск |
|
1–2 ФР |
Средний дополнительный риск |
Средний дополнительный риск |
Очень высокий дополнительный риск |
|
≥3 ФР, ПОМ, МС или СД |
Высокий дополнительный риск |
Высокий дополнительный риск |
Очень высокий дополнительный риск |
|
АКС |
Очень высокий дополнительный риск |
Очень высокий дополнительный риск |
Очень высокий дополнительный риск |
|
*Точность определения общего сердечно-сосудистого риска напрямую зависит от того, насколько полно проведено клинико-инструментальное и биохимическое обследование больного. Без данных УЗИ сердца и сосудов для диагностики ГЛЖ и утолщения стенки (или наличия бляшки) сонных артерий до 50% больных АГ могут быть ошибочно отнесены к категории низкого или среднего риска вместо высокого или очень высокого. |
Экспресс-оценка уровня риска может проводиться не только врачом, но и медицинской сестрой с использованием европейской системы стратификации SCORE, которая имеет такую же градацию величин риска, как и Фрамингемская модель, – низкий, средний, высокий и очень высокий. Но надо иметь в виду, что по Фрамингемской одели» оценивается риск ССЗ и смерти, а по модели SCORE оценивается только риск сердечно-сосудистой смерти в течение 10 лет у больных, не имеющих доказанной ишемической болезни сердца (ИБС). По Фрамингемской модели низкому риску соответствует вероятность развития ССО и смерти от них в течение ближайших 10 лет менее 15%, среднему риску – 15–20%, высокому – 20–30% и очень высокому риску – более 30%. При оценке величины риска по модели SCORE учитываются пол, возраст, статус курения, величина АД и ОХС. Для РФ по системе SCORE низкому риску соответствует вероятность смерти в течение ближайших 10 лет менее 1%, среднему риску – 1–4%, высокому – 5–9% и очень высокому риску – 10% и более. Особого внимания требуют пациенты, имеющие высокий и очень высокий риск развития ССО как по Фрамингемской модели, так по системе SCORE (таблица 5). Систему стратификации риска SCORE у больных, имеющих высоковероятные ПОМ и АКС, целесообразно использовать как предварительную с последующим уточнением величины риска по методу стратификации, основанному на Фрамингемской модели после проведения дополнительного обследования.
|
3.3. Формулировка диагноза
При формулировании диагноза по возможности максимально полно должны быть отражены ФР, ПОМ, АКС, сердечно-сосудистый риск. Степень повышения АД обязательно указывается у пациентов с впервые диагностированной АГ, у остальных больных пишется достигнутая степень АГ. Если больной находился в стационаре, то в диагнозе указывается степень АГ на момент поступления. Необходимо также указать стадию заболевания, чему в России по-прежнему придают большое значение. Согласно трехстадийной классификации ГБ, ГБ I стадии предполагает отсутствие ПОМ, ГБ II стадии – присутствие изменений со стороны одного или нескольких органов-мишеней. Диагноз ГБ III стадии устанавливается при наличии АКС.
При отсутствии АКС термин «гипертоническая болезнь» в силу своей высокой прогностической значимости закономерно занимает первую позицию в структуре диагноза. При наличии АКС, сопровождающихся высокой степенью нарушения функции или протекающих в острой форме (например, острый коронарный синдром), «гипертоническая болезнь» в структуре диагноза сердечно-сосудистой патологии может занимать не первую позицию. При вторичных формах АГ, «артериальная гипертензия», как правило, занимает не первое место в структуре диагноза.
Примеры диагностических заключений:
-
ГБ I стадии. Степень АГ 2. Дислипидемия. Риск 2 (средний).
-
ГБ II стадии. Достигнутая степень АГ 3. ДЛП. ГЛЖ. Риск 4 (очень высокий).
-
ГБ III стадии. Степень АГ 2. ИБС. Стенокардия напряжения II ФК. Риск 4 (очень высокий).
-
ГБ II стадии. Достигнутая степень АГ 2. Атеросклероз аорты, сонных артерий. Риск 3 (высокий).
-
ГБ III стадии. Достигнутая степень АГ 1. Облитерирующий атеросклероз сосудов нижних конечностей. Перемежающаяся хромота. Риск 4 (очень высокий).
-
ГБ I стадии. Степень АГ 1. СД типа 2. Риск 3 (высокий).
-
ИБС. Стенокардия напряжения III ФК. Постинфарктный (крупноочаговый) и атеросклеротический кардиосклероз. ГБ III стадии. Достигнутая степень АГ 1. Риск 4 (очень высокий).
-
ГБ II стадии. Степень АГ 3. Дислипидемия. ГЛЖ. Ожирение II степени. Нарушение толерантности к глюкозе. Риск 4 (очень высокий).
-
Феохромоцитома правого надпочечника. Степень АГ 3. ГЛЖ. Риск 4 (очень высокий).
4. Диагностика
Обследование пациентов с АГ проводится в соответствии со следующими задачами:
-
определение стабильности повышения АД и степени тяжести АГ (таблица 1);
-
исключение вторичной (симптоматической) АГ или идентификация ее формы;
-
оценка общего сердечно-сосудистого риска:
-
выявление других ФР ССЗ, диагностика ПОМ и АКС, которые могут повлиять на прогноз и эффективность лечения;
-
Диагностика АГ и последующее обследование включают следующие этапы:
-
повторные измерения АД;
-
выяснение жалоб и сбор анамнеза;
-
физикальное обследование;
-
лабораторно-инструментальные методы исследования: более простые на I этапе и более сложные на II этапе обследования.
4.1. Правила измерения АД
4.1.1. Способы измерения АД
Измерение АД проводит врач или медицинская сестра в амбулаторных условиях или стационаре (клиническое АД). Кроме того, АД также может регистрировать сам пациент или родственники в домашних условиях – самоконтроль АД (СКАД). Суточное мониторирование АД проводят медицинские работники амбулаторно или в условиях стационара. Клиническое измерение АД имеет наибольшую доказательную базу для обоснования классификации уровней АД, прогноза рисков, оценки эффективности терапии. Точность измерения АД и, соответственно, гарантия правильной диагностики АГ, определения ее степени тяжести зависят от соблюдения правил по его измерению.
Для измерения АД имеет значение соблюдение следующих условий.
4.1.2. Положение больного
Сидя в удобной позе; рука на столе и находится на уровне сердца; манжета накладывается на плечо, нижний край ее на 2 см выше локтевого сгиба.
4.1.3. Условия измерения АД
-
Исключается употребление кофе и крепкого чая в течение 1 ч перед исследованием;
-
Рекомендуется не курить в течение 30 мин до измерения АД;
-
Отменяется прием симпатомиметиков, включая назальные и глазные капли;
-
АД измеряется в покое после 5-минутного отдыха; в случае если процедуре измерения АД предшествовала значительная физическая или эмоциональная нагрузка, период отдыха следует продлить до 15–30 мин.
4.1.4. Оснащение
-
Размер манжеты должен соответствовать размеру руки: резиновая раздуваемая часть манжеты должна охватывать не менее 80% окружности плеча; для взрослых лиц применяется манжета шириной 12–13 см и длиной
30–35 см (средний размер); но необходимо иметь в наличии большую и маленькую манжету для полных и худых рук соответственно. -
Столбик ртути или стрелка тонометра перед началом измерения должны находиться на нулевой отметке.
4.1.5. Кратность измерения
-
Для оценки уровня АД на каждой руке следует выполнить не менее двух измерений с интервалом не менее 1 мин; при разнице АД≥5 мм рт. ст. производят одно дополнительное измерение; за конечное (регистрируемое) значение принимается минимальное из трех измерений.
-
Для диагностики АГ при небольшом повышении АД повторное измерение (2–3 раза) проводят через несколько месяцев.
-
При выраженном повышении АД и наличии ПОМ, высоком и очень высоком риске ССО повторные измерения АД проводят через несколько дней.
4.1.6. Техника измерения
-
Быстро накачать воздух в манжету до уровня давления, на 20 мм рт. ст. превышающего САД (по исчезновению пульса).
-
АД измеряют с точностью до 2 мм рт. ст.
-
Снижать давление в манжете со скоростью примерно 2 мм рт. ст. в 1 секунду.
-
Уровень давления, при котором появляется 1-й тон, соответствует САД (1 фаза тонов Короткова).
-
Уровень давления, при котором происходит исчезновение тонов (5 фаза тонов Короткова) соответствует ДАД; у детей, подростков и молодых людей сразу после физической нагрузки, у беременных и при некоторых патологических состояниях у взрослых, когда невозможно определить 5 фазу, следует попытаться определить 4 фазу тонов Короткова, которая характеризуется значительным ослаблением тонов.
-
Если тоны очень слабы, то следует поднять руку и выполнить несколько сжимающих движений кистью, затем измерение повторить, при этом не следует сильно сдавливать артерию мембраной фонендоскопа.
-
При первичном осмотре пациента следует измерить давление на обеих руках; в дальнейшем измерения проводят на той руке, на которой АД выше.
-
У больных старше 65 лет, при наличии СД и у лиц, получающих антигипертензивную терапию (АГТ), следует также произвести измерение АД через 2 мин пребывания в положении стоя.
-
Целесообразно измерять АД на ногах, особенно у больных моложе 30 лет; измерение проводится с помощью широкой манжеты (той же, что и у лиц с ожирением); фонендоскоп располагается в подколенной ямке; для выявления окклюзирующих поражений артерий и оценки лодыжечно-плечевого индекса измеряют САД с помощью манжеты, расположенной на лодыжке, и/или ультразвуковым методом.
-
Частота сердечных сокращений подсчитывается по пульсу на лучевой артерии (минимум за 30 секунд) после второго измерения АД в положении сидя.
4.1.7. Измерение АД в домашних условиях
Показатели АД, полученные в домашних условиях, могут стать ценным дополнением к клиническому АД при диагностике АГ и контроле за эффективностью лечения, но предполагают применение других нормативов. Принято считать, что величина АД 140/90 ммрт. ст., измеренная на приеме у врача, соответствует АД примерно 130–135/85 мм рт. ст. при измерении дома. Оптимальная величина АД при самоконтроле составляет 130/80 мм рт. ст. Для СКАД могут быть использованы традиционные тонометры со стрелочными манометрами, но в последние годы предпочтение отдается автоматическим и полуавтоматическим приборам для домашнего применения, прошедшим строгие клинические испытания для подтверждения точности измерений. Следует с осторожностью трактовать результаты, полученные с помощью большинства имеющихся в настоящее время приборов, которые измеряют АД на запястье; необходимо также иметь в виду, что приборы, измеряющие АД в артериях пальцев кисти, отличает низкая точность получаемых при этом значений АД.
Величины АД, полученные при СКАД, позволяют точнее судить о прогнозе ССО. Проведение его показано при подозрении на изолированную клиническую АГ (ИКАГ) и изолированную амбулаторную АГ (ИААГ), при необходимости длительного контроля АД на фоне медикаментозного лечения, при АГ, резистентной к лечению. СКАД может применяться при диагностике и лечении АГ у беременных, пациентов с СД, пожилых лиц.
СКАД обладает следующими достоинствами:
-
дает дополнительную информацию об эффективности АГТ;
-
улучшает приверженность пациентов к лечению;
-
измерение проводится под контролем пациента, поэтому, в отличие от СМАД, полученные цифры АД вызывают меньше сомнений по поводу надежности работы аппарата и условий измерения АД.
СКАД не может быть рекомендован в следующих ситуациях:
-
измерение вызывает беспокойство у пациента;
-
пациент склонен использовать полученные результаты для самостоятельной коррекции терапии.
Вместе с тем необходимо учитывать, что СКАД не может дать информацию об уровнях АД в течение «повседневной« дневной активности, особенно у работающей части населения, и в ночные часы.
4.1.8. Суточное мониторирование АД
Клиническое АД является основным методом определения величины АД и стратификации риска, но СМАД имеет ряд определенных достоинств:
-
дает информацию об АД в течение «повседневной» дневной активности и ночные часы;
-
позволяет уточнить прогноз ССО;
-
более тесно связано с изменениями в органах-мишенях исходно и наблюдаемой их динамикой в процессе лечения;
-
более точно оценивает антигипертензивный эффект терапии, так как позволяет уменьшить эффект «белого халата» и плацебо.
СМАД предоставляет важную информацию о состоянии механизмов сердечно-сосудистой регуляции, в частности позволяет определять суточный ритм АД, ночную гипотензию и гипертензию, динамику АД во времени и равномерность антигипертензивного эффекта препаратов.
Ситуации, в которых выполнение СМАД наиболее целесообразно:
-
повышенная лабильность АД при повторных измерениях, визитах или по данным самоконтроля;
-
высокие значения клинического АД у пациентов с малым числом ФР и отсутствием характерных для АГ изменений органов-мишеней;
-
нормальные значения клинического АД у пациентов с большим числом ФР и/или наличием характерных для АГ изменений органов-мишеней;
-
большие отличия в величине АД на приеме и по данным самоконтроля;
-
резистентность к АГТ;
-
эпизоды гипотензии, особенно у пожилых пациентов и больных СД;
-
АГ у беременных и подозрение на преэклампсию.
Для проведения СМАД могут быть рекомендованы только аппараты, успешно прошедшие строгие клинические испытания по международным протоколам для подтверждения точности измерений. При интерпретации данных СМАД основное внимание должно быть уделено средним значениям АД за день, ночь и сутки (и их соотношениям). Остальные показатели представляют несомненный интерес, но требуют дальнейшего накопления доказательной базы.
4.1.9. Изолированная клиническая АГ
У некоторых лиц при измерении АД медицинским персоналом регистрируемые величины АД соответствуют АГ, тогда как показатели СМАД или АД, измеренного в домашних условиях, остаются в пределах нормальных величин, т.е. имеет место АГ «белого халата», или что более предпочтительно «изолированная клиническая АГ». ИКАГ выявляется примерно у 15% лиц в общей популяции. У этих лиц риск ССО меньше, чем у больных АГ. Однако по сравнению с нормотониками у этой категории лиц чаще наблюдаются органные и метаболические изменения. Достаточно часто ИКАГ со временем трансформируется в обычную АГ. Предвидеть возможность выявления АГ в каждом конкретном случае сложно, однако чаще ИКАГ наблюдается при АГ 1 степени у женщин, пожилых, некурящих лиц, недавно выявленой АГ и небольшом числе измерений АД в амбулаторных и клинических условиях.
Диагностику ИКАГ проводят на основании данных СКАД и СМАД. При этом наблюдается повышение клинического АД при повторных измерениях (как минимум трижды), тогда как показатели СКАД (среднее значение АД за 7 дней измерения) и СМАД находятся в пределах нормы (таблица 1). Диагностика ИКАГ, по данным СКАД и СМАД, может не совпадать, причем особенно часто это наблюдается у работающих пациентов. В этих случаях необходимо ориентироваться на данные СМАД. Установление данного диагноза требует проведения исследования для уточнения наличия ФР и ПОМ. У всех пациентов с ИКАГ необходимо использовать немедикаментозные методы лечения АГ. При наличии высокого и очень высокого риска ССО рекомендуется начать АГТ.
4.1.10. Изолированная амбулаторная АГ
Обратным феноменом для ИКАГ является «изолированная амбулаторная АГ» (ИААГ) или «маскированная» АГ, когда при измерении АД в медицинском учреждении выявляются нормальные величины АД, но результаты СКАД и/или СМАД указывают на наличие АГ. Информация об ИААГ пока весьма ограничена, но известно, что она выявляется примерно у 12–15% лиц в общей популяции. У этих пациентов по сравнению с нормотониками чаще выявляются ФР, ПОМ, а риск ССО практически такой же, как у пациентов с АГ.
4.1.11. Центральное АД
В артериальном русле наблюдаются сложные гемодинамические явления, приводящие к появлению так называемых «отраженных» пульсовых волн преимущественно от резистивных сосудов, и их суммации с основной (прямой) пульсовой волной, возникающей при выбросе крови из сердца. Суммация прямой и отраженных волн в фазу систолы приводит к формированию феномена «аугментации» (усиления) САД. Сумма прямой и отраженных волн отличается на разных сосудах, в результате АД (в первую очередь САД) отличается в различных магистральных сосудах и не совпадает с измеренным на плече. Так, хорошо известен факт, что в норме САД на нижних конечностях превосходит САД, измеренное на плече, на 5–20%. Большое прогностическое значение имеет АД в восходящей или центральной части аорты или «центральное» АД. В последние годы появились специальные методики (например, апланационная тонометрия лучевой или сонной артерии), которые позволяют исходя из количественной сфигмограммы и АД, измеренного на плече, рассчитывать центральное АД. Исследования показали, что это расчетное центральное АД в аорте может оказаться ценным при оценке эффективности проводимой терапии и, по-видимому, позволит выявить дополнительную группу пациентов с «псевдогипертонией», у которых имеет место нормальное центральное давление, но повышенное АД на плече из-за аномально высокой суммы прямой и отраженной волн давления в верхних конечностях. У пожилых больных большой вклад в повышение АД в плечевой артерии относительно АД в аорте вносит повышение жесткости ее стенки. Эти факты, несомненно, необходимо учитывать, но доказательная база в отношении преимуществ расчетного центрального давления перед традиционным АД, измеряемым на плече, требует проведения дальнейших полномасштабных исследований.
4.2. Методы обследования
После выявления АГ следует обследовать пациента на предмет исключения симптоматических АГ, определить степень и стадию АГ, а также риск ССО.
4.2.1. Сбор анамнеза
Тщательно собранный анамнез обеспечивает возможность получения важной информации о сопутствующих ФР, признаках ПОМ, АКС и вторичных формах АГ. В таблице 6 представлены сведения, которые необходимо выяснить у пациента при беседе с ним.
|
|
Примечание. См. здесь и далее: ТИА – транзиторная ишемическая атака. |
4.2.2. Физикальное исследование
Физикальное обследование больного АГ, направлено на выявление ФР, признаков вторичного характера АГ и органных поражений. Измеряют рост, массу тела с вычислением индекса массы тела (ИМТ) в кг/м2 и окружность талии (ОТ). Данные физикального обследования, указывающие на вторичный характер АГ, и органные поражения представлены в таблице 7.
|
Признаки вторичной АГ:
Признаки ПОМ и АКС:
Показатели висцерального ожирения:
|
|
Примечание. См. здесь и далее: ХСН – хроническая сердечная недостаточность. |
4.2.3. Лабораторные и инструментальные методы исследования
При обследовании больного АГ необходимо идти от простых методов исследования к более сложным. На первом этапе выполняют рутинные исследования, обязательные у каждого больного для диагностики АГ. Если на этом этапе у врача отсутствуют основания подозревать вторичный характер АГ и полученных данных достаточно для четкого определения группы риска пациента и, соответственно, тактики лечения, то на этом обследование может быть закончено. На втором этапе рекомендуются дополнительные исследования для уточнения формы вторичной АГ, оценки ФР, ПОМ и АКС. Профильные специалисты по показаниям проводят углубленное обследование пациента, когда требуется подтвердить вторичный характер АГ и тщательно оценить состояние больных при осложненном течении АГ (таблица 8).
|
Обязательные исследования:
Исследования, рекомендуемые дополнительно:
Углубленное исследование:
|
|
Примечание. См. здесь и далее: УЗИ – ультразвуковое сканирование; КТ – компьютерная томография; МРТ – магнитно-резонансная томография; МРА – магнитно-резонансная ангиография. |
4.2.4. Исследование состояния органов-мишеней
Обследование с целью выявления ПОМ чрезвычайно важно, так как оно позволяет не только определить риск развития ССО, но и проследить за состоянием больных в динамике, оценить эффективность и безопасность АГТ. Для выявления ПОМ используют дополнительные методы исследования сердца, магистральных артерий, почек, головного мозга. Выполнение этих исследований показано в тех случаях, когда они могут повлиять на оценку уровня риска и тактику ведения пациента.
Сердце – для оценки состояния сердца выполняются ЭКГ и ЭхоКГ. ЭКГ по критериям индекса Соколова-Лайона (SV1+RV5–6>38 мм) и Корнельского произведения ((RAVL+SV5) мм × QRS мс >2440 мм × мс) позволяет выявить ГЛЖ. Более чувствительным и специфичным методом оценки поражения сердца при АГ является расчет ИММЛЖ с помощью ЭхоКГ*. Верхнее значение нормы для этого показателя составляет 124 г/м2 для мужчин и 109 г/м2 для женщин. По соотношению толщины задней стенки левого желудочка (ТЗСЛЖ) и его радиуса (РЛЖ), а также с учетом величины ИММЛЖ можно определить тип ремоделирования ЛЖ. При ТЗСЛЖ/РЛЖ >0,42 и увеличении ИММЛЖ имеет место концентрическая ГЛЖ, при ТЗСЛЖ/РЛЖ <0,42 и увеличении ИММЛЖ – эксцентрическая ГЛЖ, в случае же ТЗСЛЖ/РЛЖ >0,42 и нормальном ИММЛЖ – концентрическое ремоделирование. Прогностически наименее благоприятной является концентрическая ГЛЖ. ЭхоКГ позволяет также оценить диастолическую и систолическую функции ЛЖ.
*Масса миокарда ЛЖ (г) = 1,04 × [(ТМЖП, см + ТЗС, см + КДР, см)3 – (КДР, см)3] – 13,6 [6].
ИММЛЖ = ММЛЖ/площадь поверхности тела
Площадь поверхности тела = масса тела0,425 (кг) × рост0,725 (см) × 0,007184 (г/м2).
Сосуды. Для диагностики поражения магистральных артериальных сосудов при АГ проводят УЗИ общей сонной артерии, что позволяет выявить признаки ремоделирования (гипертрофии) ее стенки по увеличению ТИМ>0,9 мм. ТИМ>1,3 мм, или локальное утолщение на 0,5 мм или на 50% относительно соседних участков в области бифуркации или внутренней сонной артерии, расценивается как признак ее атеросклеротического поражения.
С помощью допплерографии на сосудах лодыжки и плеча или измерения на них АД можно рассчитать лодыжечно-плечевой индекс. Снижение его величины менее 0,9 свидетельствует об облитерирующем поражении артерий нижних конечностей и может расцениваться как косвенный признак выраженного атеросклероза.
Существует высокая степень корреляции между вероятностью развития ССО и жесткостью крупных (эластических) артерий, оцениваемой по величине скорости распространения пульсовой волны на участке между сонной и бедренной артериями. Наибольшая вероятность осложнений наблюдается при повышении скорости пульсовой волны более 12 м/с.
Почки. Для диагностики патологии почек и уточнения их функционального состояния исследуют уровень креатинина в сыворотке крови и экскрецию белка с мочой. Обязательно рассчитывают клиренс креатинина по формуле Кокрофта-Гаулта и СКФ по MDRD-формуле. Клиренс креатинина ниже 60 мл/мин, или СКФ <60 мл/мин/1,73 м2, свидетельствует о начальных изменениях функции почек даже при нормальном уровне креатинина в крови. Исследование мочи на наличие альбумина с помощью тест-полосок проводят всем пациентам. При отрицательном результате рекомендуется использование специальных методов для выявления МАУ (30–300 мг/сут). МАУ подтверждает наличие у пациента нефропатии, которая является важным предиктором ССО. Показано определение концентрации мочевой кислоты в крови, так как гиперурикемия часто наблюдается при нелеченой АГ, особенно в рамках МС, и может коррелировать с наличием нефроангиосклероза.
Исследование сосудов глазного дна целесообразно у молодых пациентов и больных с тяжелой АГ, так как небольшие изменения сосудов сетчатки часто являются неспецифичными и присутствуют без связи с АГ. Выраженные изменения – кровоизлияния, экссудаты и отек соска зрительного нерва – у больных с тяжелой АГ ассоциируются с повышенным сердечно-сосудистым риском.
Головной мозг. Проведение КТ или МРТ позволяет уточнить наличие, характер и локализацию патологических изменений, выявить зоны лейкоареоза и бессимптомно перенесенные МИ. Эти методы относятся к дорогостоящим и не являются повсеместно доступными, но их высокая информативность служит основанием для широкого использования в клинической практике. У пожилых пациентов с АГ часто необходимо проведение специальных тестов с использованием опросников для раннего выявления нарушения когнитивных функций.
4.2.5. Генетический анализ у больных АГ
У больных АГ часто прослеживается отягощенный семейный анамнез по ССЗ, что является основанием предполагать ее наследственный характер. ГБ имеет многофакторную этиологию и относится к полигенным заболеваниям. В ряде исследований показано повышение уровня экспрессии и наличие «неблагоприятных» вариантов полиморфизма генов, кодирующих прессорные системы регуляции АД, такие как ангиотензинпревращающий фермент (АПФ), ангиотензиноген, рецепторы к ангиотензину II (А II) и др. Роль этих генетических факторов в патогенезе ГБ нуждается в дальнейшем изучении. Генетическая предрасположенность к АГ может оказывать влияние на эффективность и переносимость АГТ. В клинической практике важно обнаружить или исключить редкие, моногенные формы наследственной АГ. К ним относятся, в частности, синдром Лиддля, патология амилоидчувствительных эпителиальных натриевых каналов, синдром кажущейся избыточности минералокортикоидной активности и гиперальдостеронизм, корригируемый глюкокортикоидами. Генетическое исследование и выявление мутантного гена позволяют в таких случаях выявить причину АГ и в ряде случаев провести патогенетическую терапию.
5. Тактика ведения больных АГ
5.1. Цели терапии
Основная цель лечения больных АГ состоит в максимальном снижении риска развития ССО и смерти от них. Для достижения этой цели требуется не только снижение АД до целевого уровня, но и коррекция всех модифицируемых ФР (курение, ДЛП, гипергликемия, ожирение), предупреждение, замедление темпа прогрессирования и/или уменьшение поражения органов-мишеней, а также лечение ассоциированных и сопутствующих заболеваний (ИБС, СД и др.).
При лечении больных АГ величина АД должна быть менее 140/90 мм рт. ст., что является ее целевым уровнем. При хорошей переносимости назначенной терапии целесообразно снижение АД до более низких значений. У пациентов с высоким и очень высоким риском ССО необходимо снизить АД до 140/90 мм рт. ст. и менее в течение 4 нед. В дальнейшем, при условии хорошей переносимости рекомендуется снижение АД до 130–139/80–89 мм рт. ст. При проведении АГТ следует иметь в виду, что бывает трудно достичь уровня САД<140 мм рт. ст. у пациентов с СД, ПОМ, у пожилых больных и уже имеющих ССО. Достижение более низкого целевого уровня АД возможно только при хорошей переносимости и может занимать больше времени, чем его снижение до величины менее 140/90 мм. рт. ст. При плохой переносимости снижения АД рекомендуется его снижение в несколько этапов. На каждом этапе АД снижается на 10–15% от исходного уровня за 2–4 нед с последующим перерывом для адаптации пациента к более низким величинам АД. Следующий этап снижения АД и, соответственно, усиление АГТ в виде увеличения доз и/или количества принимаемых препаратов возможен только при условии хорошей переносимости уже достигнутых величин АД. Если переход на следующий этап вызывает ухудшение состояния пациента, целесообразно вернуться на предыдущий уровень еще на некоторое время. Таким образом, снижение АД до целевого уровня происходит в несколько этапов, число которых индивидуально и зависит как от исходного уровня АД, так и от переносимости АГТ. Использование этапной схемы снижения АД с учетом индивидуальной переносимости, особенно у пациентов с высоким и очень высоким риском ССО, позволяет достичь целевого уровня АД и избежать эпизодов гипотонии, с которыми связано увеличение риска развития ИМ и МИ. При достижении целевого уровня АД необходимо учитывать нижнюю границу снижения САД до 110–115 мм рт. ст. и ДАД до 70–75 мм рт. ст., а также следить за тем, чтобы в процессе лечения не происходило увеличения пульсового АД у пожилых пациентов, что возникает главным образом за счет снижения ДАД.
5.2. Общие принципы ведения больных
После оценки сердечно-сосудистого риска вырабатывается индивидуальная тактика ведения пациента. Важнейшими ее аспектами являются решения о целе-
сообразности и выборе медикаментозной терапии. При определении показаний к АГТ следует учитывать степень сердечно-сосудистого риска и величину АД. Степень сердечно-сосудистого риска служит основным показанием для назначения АГП (таблица 9).
|
ФР, ПОМ и СЗ |
Артериальное давление, мм рт. ст. |
||
|
АГ 1-й степени 140–159/90–99 |
АГ 2-й степени 160–179/100–109 |
АГ 3-й степени ≥180/110 |
|
|
Нет ФР |
Изменение ОЖ на несколько месяцев, при отсутствии контроля АД начать лекарственную терапию |
Изменение ОЖ на несколько недель, при отсутствии контроля АД начать лекарственную терапию |
Изменение ОЖ + немедленно начать лекарственную терапию |
|
1–2 ФР |
Изменение ОЖ на несколько недель, при отсутствии контроля АД начать лекарственную терапию |
Изменение ОЖ на несколько недель, при отсутствии контроля АД начать лекарственную терапию |
Изменение ОЖ + немедленно начать лекарственную терапию |
|
≥3 ФР, ПОМ, МС или СД |
Изменение ОЖ + немедленно начать лекарственную терапию |
Изменение ОЖ + немедленно начать лекарственную терапию |
Изменение ОЖ + немедленно начать лекарственную терапию |
|
АКС |
Изменение ОЖ + немедленно начать лекарственную терапию |
Изменение ОЖ + немедленно начать лекарственную терапию |
Изменение ОЖ + немедленно начать лекарственную терапию |
|
Примечание. См. здесь и далее: ОЖ – образ жизни. |
Рекомендации по изменению ОЖ следует давать всем пациентам, имеющим АГ (или высокое нормальное АД в сочетании хотя бы с одним фактором риска), и этому должно уделяться особое внимание. У лиц с высоким и очень высоким суммарным сердечно-сосудистым риском независимо от уровня АД АГТ назначают немедленно. При среднем риске у больных АГ 1-2-й степени рекомендуется изменение ОЖ с оценкой состояния больного через несколько недель и началом медикаментозного лечения в случае сохранения АГ. При низком риске у лиц с АГ 1-й степени рекомендуется изменение ОЖ с оценкой состояния больного через несколько месяцев и началом медикаментозного лечения в случае безуспешности предпринимаемых усилий в отношении нормализации АД (АД≥140/90 мм рт. ст.). Таким образом, лечение АГ необходимо начинать при величине АД 140/90 мм рт. ст., так как нет убедительных доказательств эффективности АГТ при АД<140/90 мм рт. ст. Лицам с высоким нормальным АД обязательно рекомендуют изменение ОЖ, а решение о начале лекарственной терапии принимают индивидуально. Наиболее вероятно ее назначение в случае наличия у больного АКС или ПОМ, особенно в комбинации с другими ФР. У лиц с высоким нормальным АД, имеющих только ФР, предписывается изменение ОЖ.
5.3. Мероприятия по изменению образа жизни
Мероприятия по изменению ОЖ рекомендуют всем больным, в том числе получающим медикаментозную терапию. Они позволяют:
-
снизить АД;
-
уменьшить потребность в АГП и повысить их эффективность;
-
благоприятно повлиять на имеющиеся ФР;
-
осуществить первичную профилактику ГБ у больных с высоким нормальным АД и у имеющих ФР.
Немедикаментозные методы включают в себя:
-
отказ от курения;
-
нормализацию массы тела (ИМТ <25 кг/м2);
-
потребление алкогольных напитков менее 30 г/сут алкоголя для мужчин и 20 г/сут для женщин;
-
увеличение физической нагрузки – регулярная аэробная (динамическая) физическая нагрузка по
30–40 мин не менее 4 раз в неделю; -
снижение потребления поваренной соли до 5 г/сут;
-
изменение режима питания с увеличением потребления растительной пищи, увеличением в рационе калия, кальция (содержатся в овощах, фруктах, зерновых) и магния (содержится в молочных продуктах), а также уменьшением потребления животных жиров.
5.4. Медикаментозная терапия
У всех больных АГ необходимо добиваться постепенного снижения АД до целевых уровней. Особенно осторожно следует снижать АД у пожилых и больных, перенесших ИМ и МИ. Количество назначаемых препаратов зависит от исходного уровня АД и сопутствующих заболеваний. Например, при АГ 1 степени и отсутствии ССО возможно достижение целевого АД на фоне монотерапии примерно у 50% больных. При АГ 2 и 3 степени, наличии ПОМ, АКС, СД и МС в большинстве случаев может потребоваться комбинация из 2 или 3 препаратов. В настоящее время возможно использование 2-х стратегий стартовой терапии АГ: монотерапии и низкодозовой комбинированной терапии с последующим увеличением количества и/или доз лекарственного средства при необходимости (схема 1). Монотерапия на старте лечения может быть выбрана для пациентов с низким или средним риском. Комбинацию 2 препаратов в низких дозах назначают больным с высоким или очень высоким риском ССО (схема 1). Монотерапия базируется на поиске оптимального для больного препарата; переход на комбинированную терапию целесообразен только в случае отсутствия эффекта последней. Низкодозовая комбинированная терапия на старте лечения предусматривает подбор эффективной комбинации препаратов с различными механизмами действия.
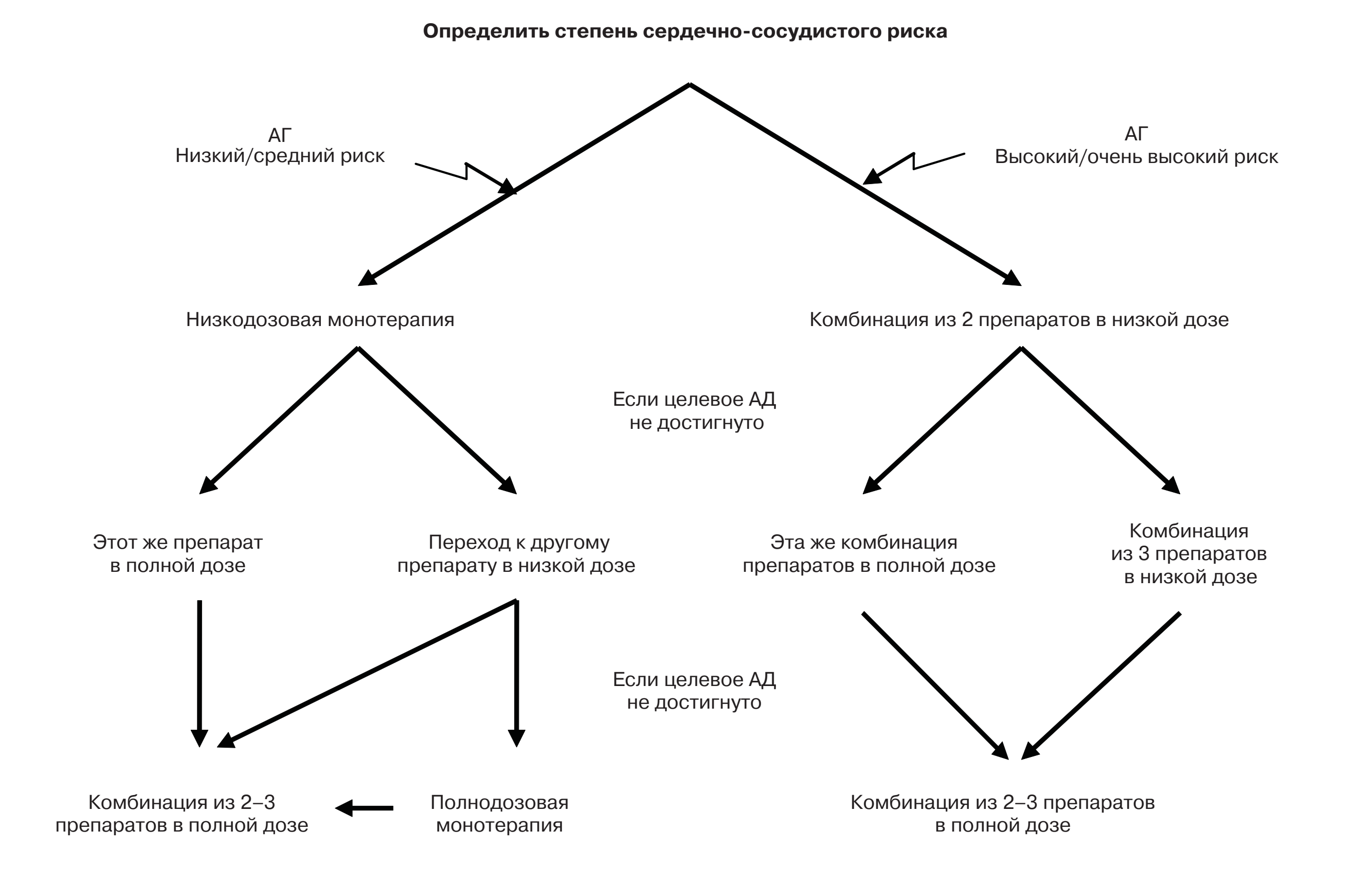
Схема 1. Выбор стартовой терапии для достижения целевого уровня АД
Каждый из этих подходов имеет свои преимущества и недостатки. Преимущество низкодозовой монотерапии состоит в том, что в случае удачного подбора лекарства больной не будет принимать еще один препарат. Однако стратегия монотерапии требует от врача кропотливого поиска оптимального для больного антигипертензивного средства с частой сменой лекарств и их дозировок, что лишает врача и больного уверенности в успехе и в конечном итоге ведет к снижению приверженности пациентов к лечению. Это особенно актуально для больных АГ 1 и 2 степени, большинство из которых не испытывают дискомфорта от повышения АД и не мотивированы к лечению.
При комбинированной терапии в большинстве случаев назначение препаратов с различными механизмами действия позволяет, с одной стороны, добиться целевого АД, а с другой – минимизировать количество побочных эффектов. Комбинированная терапия позволяет также подавить контррегуляторные механизмы повышения АД. Применение фиксированных комбинаций АГП в одной таблетке повышает приверженность больных к лечению. Недостатком комбинированной терапии является то, что иногда больным приходится принимать лекарство, в котором нет необходимости. Пациентам с АД≥160/100 мм рт. ст., имеющим высокий и очень высокий риск ССО, полнодозовая комбинированная терапия может быть назначена на старте лечения. У 15–20% пациентов контроль АД не может быть достигнут при использовании
2 препаратов. В этом случае используется комбинация из 3 лекарственных средств и более.
Для длительной АГТ необходимо использовать препараты пролонгированного действия, обеспечивающие 24-часовой контроль АД при однократном приеме. Преимущества таких препаратов – в большей приверженности больных к лечению, меньшей вариабельности АД и, как следствие, более стабильном контроле АД. В перспективе такой подход к терапии АГ должен эффективнее снижать риск развитие ССО и предупреждать ПОМ.
5.4.1. Выбор антигипертензивного препарата
В настоящее время для лечения АГ рекомендованы 5 основных классов АГП: ингибиторы ангиотензин-превращающего фермента (ИАПФ), блокаторы рецепторов AT1 (БРА), антагонисты кальция (АК), β-адреноблокаторы (β-АБ), диуретики (таблица 10, 11). В качестве дополнительных классов АГП для комбинированной терапии могут использоваться α-АБ, агонисты имидазолиновых рецепторов и прямые ингибиторы ренина.
| *ИАПФ* | *БРА* | *β-АБ* | *АК (дигидропиридиновые)* |
|---|---|---|---|
|
|
|
|
|
АК (верапамил/дилтиазем) |
Диуретики тиазидные |
Диуретики (антагонисты альдостерона) |
Диуретики петлевые |
|
|
|
|
| Класс препаратов | Абсолютные противопоказания | Относительные противопоказания |
|---|---|---|
|
Тиазидные диуретики |
подагра |
МС, НТГ, ДЛП, беременность |
|
β-АБ |
атриовентрикулярная блокада 2–3 степени БА |
заболевания периферических артерий, МС, НТГ, спортсмены и физически активные пациенты, ХОБЛ |
|
АК дигидропиридиновые |
тахиаритмии, ХСН |
|
|
АК недигидропиридиновые |
атриовентрикулярная блокада 2–3 степени, ХСН |
|
|
ИАПФ |
беременность, гиперкалиемия, двусторонний стеноз почечных артерий, ангионевротический отек |
|
|
БРА |
беременность, гиперкалиемия, двусторонний стеноз почечных артерий |
|
|
Диуретики антагонисты альдостерона |
гиперкалиемия, ХПН |
|
|
Примечание. См. здесь и далее: БА – бронхиальная астма; ХОБЛ – хроническая обструктивная болезнь легких. |
На выбор препарата оказывают влияние многие факторы, наиболее важными из которых являются:
-
наличие у больного ФР;
-
ПОМ;
-
АКС, поражения почек, МС, СД;
-
сопутствующие заболевания, при которых необходимо назначение или ограничение применения АГП различных классов;
-
предыдущие индивидуальные реакции больного на препараты различных классов;
-
вероятность взаимодействия с лекарствами, которые пациенту назначены по другим поводам;
-
социально-экономические факторы, включая стоимость лечения.
При выборе АГП необходимо в первую очередь оценить эффективность, вероятность развития побочных эффектов и преимущества лекарственного средства в определенной клинической ситуации (таблица 12). Стоимость препарата не должна быть основным решающим фактором.
|
Поражение органов-мишеней |
|
|
ГЛЖ |
БРА, ИАПФ, АК |
|
Бессимптомный атеросклероз |
АК, ИАПФ |
|
МАУ |
ИАПФ, БРА |
|
Поражение почек |
ИАПФ, БРА |
|
Ассоциированные клинические состояния |
|
|
Предшествующий МИ |
Любые АГП |
|
Предшествующий ИМ |
β-АБ, ИАПФ, БРА |
|
ИБС |
β-АБ, АК, ИАПФ, БРА |
|
ХСН |
ТД, β-АБ, ИАПФ, БРА, антагонисты альдостерона |
|
Мерцательная аритмия пароксизмальная |
ИАПФ, БРА |
|
Мерцательная аритмия постоянная |
β-АБ, недигидропиридиновые АК |
|
Почечная недостаточность/протеинурия |
ИАПФ, БРА, петлевые диуретики |
|
Заболевания периферических артерий |
АК |
|
Особые клинические ситуации |
|
|
Пожилые |
БРА, АК, ТД |
|
ИСАГ |
АК, ТД |
|
МС |
БРА, ИАПФ, АК |
|
СД |
БРА, ИАПФ |
|
Беременность |
АК, метилдопа, β-АБ |
|
Примечание. ТД – тиазидный диуретик; АК – дигидропиридиновый АК. |
Результатами многоцентровых рандомизированных исследований доказано, что ни один из основных классов АГП не имеет существенного преимущества как в плане снижения АД, так и эффективности снижения риска ССО и смерти от них. Уменьшение риска ССЗ и ССО на фоне АГТ больше зависит от величины, на которую снижается АД, чем от используемого класса АГП, и невозможно точно предсказать, какой АГП будет максимально эффективен у конкретного пациента. При назначении любого из основных классов АГП есть свои за и против (таблица 10–12), поэтому универсальное ранжирование АГП является ненужным и скорее всего опасным. В каждой конкретной клинической ситуации необходимо учитывать особенности действия различных классов АГП, обнаруженные при проведении рандомизированных исследований. Но очень часто даже представители одного класса имеют особые свойства, которые делают их назначение более обоснованным. Выбор того или иного АГП, особенно на старте лечения, должен основываться на результатах больших клинических исследований, в которых доказана высокая эффективность и безопасность применения именно этого препарата у пациентов в подобной клинической ситуации.
Ингибиторы АПФ
Для замедления темпа прогрессирования ПОМ и возможности регресса их патологических изменений хорошо зарекомендовали себя ИАПФ. Они доказали свою эффективность в плане уменьшения выраженности ГЛЖ, включая ее фиброзный компонент, а также значимого уменьшения выраженности МАУ и протеинурии и предотвращения снижения функции почек. Наиболее выраженное антигипертензивное действие ИАПФ оказывают на пациентов с повышенной активностью ренин-ангиотензин-альдостероновой системы (РААС). Но ИАПФ не могут полностью подавить избыточную активность РААС, так как до 70–80% АII синтезируется в органах и тканях без участиям АПФ с помощью других ферментов (химаза, катепсин и др.), а при лечении ИАПФ синтез АII может переключаться с АПФ-зависимого пути на химазный. Это объясняет возможность «ускользания» антигипертензивного эффекта при лечении ИАПФ, особенно на фоне высокосолевой диеты, и служит обоснованием для применения препаратов, подавляющих активность АII независимо от пути его образования. Помимо того, ИАПФ влияют на деградацию брадикинина, что, с одной стороны, усиливает их антигипертензивную эффективность, а с другой – часто приводит к развитию таких характерных побочных эффектов, как сухой кашель и ангионевротический отек. Из важных особенностей ИАПФ, в частности рамиприла, следует отметить его способность снижать вероятность развития ССО при высоком и очень высоком сердечнососудистом риске не только у больных АГ, но также у лиц с высоким нормальным и даже нормальным АД [7]. Эффективное предотвращение развития повторного МИ и снижение риска ССО и смерти от них при наличии ИБС доказано для периндоприла [8, 9]. Назначать эналаприл в виде монотерапии не рекомендуется из-за необходимости принимать его 2 раза в сутки. Однако лечение фиксированной комбинацией эналаприла (20 мг) с гидрохлоротиазидом (12,5 мг) характеризовалось стабильным антигипертензивным эффектом в течение всех суток при однократном приеме, по данным СМАД, и метаболической нейтральностью [10, 11].
Блокаторы рецепторов АТ1
В действии АII на сосуды различают два механизма – прессорный и депрессорный. Первый опосредуется влиянием АII на рецепторы 1-го типа и приводит к вазоконстрикции, задержке натрия и жидкости, увеличению симпатической активности, снижению тонуса блуждающего нерва, клеточной пролиферации и положительному инотропному эффекту. Депрессорное действие АII реализуется через стимуляцию рецепторов 2-го типа, что приводит к вазодилятации, особенно выраженной в сосудах головного мозга и почек, натрийуретическому действию, антипролиферативному эффекту, активации кининогена, высвобождениюоксида азота и простагландина I2. В основе антигипертензивного действия и других фармакологических эффектов блокаторов рецепторов АТ1 лежат прямой механизм и два косвенных. Первый связан с ослаблением эффектов АII в условиях селективной блокады АТ1-рецепторов. Второй обусловлен реактивной гиперактивацией РААС в условиях блокады АТ1-рецепторов и дополнительной стимуляцией АТ2- рецепторов. На антигипертензивную эффективность БРА не оказывают влияние активность РААС, пол и возраст пациента. У БРА нет «ускользания» антигипертензивного эффекта, так как их действие не зависит от пути образования АII. Для БРА доказано положительное влияние на состояние органов-мишеней и снижение риска развития всех ССО. Помимо того, для БРА характерна наиболее высокая приверженность пациентов лечению за счет высокой эффективности и наилучшей среди всех классов АГП переносимости лечения. За последние годы показания к применению БРА существенно расширились. К ранее имевшимся показаниям (диабетическая нефропатия, протеинурия/МАУ, ХСН, ГЛЖ, мерцательная аритмия пароксизмальная, кашель при приеме ИАПФ и т.д.) добавились такие позиции как ИБС, недиабетическая нефропатия, дисфункция ЛЖ, пожилые. У пациентов с высоким и очень высоким риском развития ССО показано назначение телмисартана даже при высоком нормальном АД. Среди всех БРА только для телмисартана доказана способность снижать частоту развития всех ССО при отличной переносимости лечения [12].
Антагонисты кальция
Эффективность АК в качестве антигипертензивных средств обусловлена замедлением тока Са через α1— и α2-адренергические пути и кальциевые каналы периферических сосудов, уменьшением чувствительности артериальных сосудов к эндогенным влияниям норадреналина, вазопрессина, гистамина, серотонина, ацетилхолина, что приводит к снижению общего периферического сосудистого сопротивления и АД. АК делят на 3 подгруппы в зависимости от химической структуры: 1) дигидропиридины (нифедипин, амлодипин, фелодипин и др.), 2) фенилалкиламины (верапамил) и 3) бензодипины (дилтиазем). Имеются значительные различия в способности АК влиять на миокард, сосудистую стенку и проводящую систему сердца. Дигидропиридины оказывают выраженное селективное действие на мускулатуру сосудов, приводя к расширению периферических артерий, не влияют на проводящую систему сердца и практически не вызывают снижения сократительной функции миокарда. Для недигидропиридиновых АК (верапамил и дилтиазем) характерно отрицательное ино- и дромотропное действие. Все АК метаболически нейтральны и не оказывают отрицательного действия на углеводный, липидный и пуриновый обмен. Помимо антигипертензивного они оказывают антиангинальное и органопротективное действие, тормозят агрегацию тромбоцитов, достоверно уменьшают риск развития МИ и являются препаратами первого выбора у пациентов с ИСАГ.
Тиазидные диуретики
ТД оказывают выраженный антигипертензивный эффект, сопоставимый с ИАПФ, БРА, АК и β-АБ. Эффективность лечения ТД в отношении снижения АД и уменьшения сердечно-сосудистой смертности доказана в многочисленных контролируемых сравнительных рандомизированных исследованиях, а также результатами метаанализов. Лечение высокими дозами ТД (гидрохлоротиазид 50–100 мг/сут) способно ухудшать показатели углеводного, липидного, пуринового обмена и снижать величину калия в плазме крови [13, 14]. Однако эти изменения не выражены и не оказывают значимого влияния на снижение риска ССО. Использование низких доз ТД (12,5–25 мг гидрохлоротизида в сутки) в больших рандомизированных клинических исследованиях не сопровождалось ростом числа новых случаев СД и повышением величины ОХС по сравнению с плацебо [15]. Поэтому клиническое значение возможного отрицательного влияния ТД на метаболические показатели, скорее всего, невелико. Однако не следует назначать гидрохлоротиазид в дозе 25 мг в сутки и более в виде монотерапии. Эффективность и безопасность низких доз тиазидных диуретиков, особенно в составе комбинированной терапии с БРА или ИАПФ, не ставятся под сомнение. Лечение гидрохлоротиазидом (6,25–12,5 мг) в сочетании с ИАПФ или БРА не ухудшает метаболические показатели и может назначаться даже больным СД. Единственным абсолютным противопоказанием к назначению ТД является подагра.
β-адреноблокаторы
Для β-АБ и ТД доказана высокая эффективность в снижении риска ССО при лечении больных АГ. Формально перечень показаний к назначению β-АБ изменился незначительно. В настоящее время показаниями для их назначения у больных АГ служат стабильная стенокардия, перенесенный ИМ, ХСН, тахиаритмия, глаукома и беременность. Но существенной проблемой при лечении β-АБ является их неблагоприятное метаболическое действие (ДЛП, НТГ), поэтому их не рекомендуется назначать лицам с МС и высоким риском развития СД, особенно в сочетании с ТД. Кроме того, в многоцентровых исследованиях была показана достоверно меньшая эффективность β-АБ по предупреждению МИ в сравнении с другими АГП [16, 17]. Однако все эти данные были получены при анализе исследований, в которых главным образом применяли атенолол, и поэтому указанные ограничения не распространяются на β-АБ, имеющие дополнительные свойства (небиволол и карведилол), а также высокоселективные β-АБ (бисопролол и метопролола сукцинат замедленного высвобождения).
Выбор АГП в зависимости от АКС и особых клинических ситуаций рассмотрен в разделе 7.
5.4.2. Комбинированная терапия АГ
Помимо монотерапии при лечении АГ используются комбинации из 2, 3 и более антигипертензивных препаратов. Комбинированная терапия имеет много преимуществ: усиление антигипертензивного эффекта за счет разнонаправленного действия препаратов на патогенетические механизмы развития АГ, что увеличивает число пациентов со стабильным снижением АД; уменьшение частоты возникновения побочных эффектов, как за счет меньших доз комбинируемых АГП, так и за счет взаимной нейтрализации этих эффектов; обеспечение наиболее эффективной органопротекции и уменьшение риска и числа ССО [18-20]. Однако необходимо помнить, что комбинированная терапия – это прием как минимум 2 лекарственных препаратов, кратность назначения которых может быть различной. Следовательно, применение препаратов в виде комбинированной терапии должно отвечать следующим условиям: препараты должны иметь взаимодополняющее действие; должно достигаться улучшение результата при их совместном применении; препараты должны иметь близкие фармакодинамические и фармакокинетические показатели, что особенно важно для фиксированных комбинаций.
Комбинации двух антигипертензивных препаратов делят на рациональные (эффективные), возможные и нерациональные (таблица 13) [11]. Все преимущества комбинированной терапии присущи только рациональным комбинациям АГП. К ним относятся: ИАПФ + диуретик; БРА + диуретик; ИАПФ + АК; БРА + АК; дигидропиридиновый АК + β-АБ; АК + диуретик; β-АБ + диуретик (схема 2). При выборе комбинации β-АБ с диуретиком необходимо использовать сочетание небиволола, бисопролола, метопролола сукцината замедленного высвобождения или карведилола с гидрохлоротиазидом в дозе не более 6,25 мг в сутки или индапамидом и избегать назначения этой комбинации у больных с МС и СД. Основные показания к назначению рациональных комбинаций АГП представлены в таблице 14, 15 [11]. Для комбинированной терапии АГ могут использоваться как нефиксированные, так и фиксированные комбинации препаратов. Однако предпочтение должно отдаваться фиксированным комбинациям АГП, содержащим 2 препарата в одной таблетке. Отказаться от назначения фиксированной комбинации АГП можно только при абсолютной невозможности ее использования, так как фиксированная комбинация АГП:
-
всегда будет рациональной;
-
является самой эффективной стратегией достижения и поддержания целевого уровня АД;
-
обеспечивает лучшее органопротективное действие и уменьшение риска ССО;
-
позволяет сократить количество принимаемых таблеток, что существенно повышает приверженность пациентов лечению.
| ИАПФ | БРА | ТД | β-АБ | АКд | АКнд | |
|---|---|---|---|---|---|---|
|
ИАПФ |
Н |
В |
Р |
В |
Р |
Р |
|
БРА |
В |
Н |
Р |
В |
Р |
Р |
|
ТД |
Р |
Р |
Н |
Р |
Р |
Р |
|
β-АБ |
В |
В |
Р |
Н |
Р |
Н |
|
АКд |
Р |
Р |
Р |
Р |
Н |
В |
|
АКнд |
Р |
Р |
Р |
Н |
В |
Н |
|
Р – рациональная комбинация; В – возможная комбинация; Н – нерациональная комбинация, АКд – АК дигидропиридиновый; АКнд – АК недигидропиридиновый |
| ИАПФ + ТД | ИАПФ + АК | БРА + ТД | БРА + АК | АК + ТД | АК + β-АБ | ТД + β-АБ |
|---|---|---|---|---|---|---|
|
|
|
|
|
|
|
|
Примечание. АК – дигидропиридиновый АК. |
|
Поражение органов-мишеней |
|
|
ГЛЖ |
БРА/ИАПФ с ТД или АК |
|
Бессимптомный атеросклероз |
БРА/ИАПФ с АК |
|
МАУ |
БРА/ИАПФ с ТД |
|
Поражение почек |
БРА/ИАПФ с ТД |
|
Ассоциированные клинические состояния |
|
|
Предшествующий МИ |
Любые рациональные комбинации АГП |
|
Предшествующий ИМ |
β-АБ/АК с БРА/ИАПФ, β-АБ с АК |
|
ИБС |
β-АБ или АК с БРА или ИАПФ |
|
ХСН |
БРА/ИАПФ с β-АБ и ТД |
|
Почечная недостаточность/протеинурия |
БРА/ИАПФ с петлевым диуретиком |
|
Заболевания периферических артерий |
АК с БРА/ИАПФ |
|
Особые клинические ситуации |
|
|
Пожилые |
БРА/ИАПФ с АК/ТД |
|
ИСАГ |
АК с ТД, АК или ТД с БРА/ИАПФ |
|
МС |
БРА/ИАПФ с АК/ТД |
|
СД |
БРА/ИАПФ с АК/ТД |
|
Беременность |
Метилдопа с АК/β-АБ |
|
Примечание. АК – дигидропиридиновый АК. |
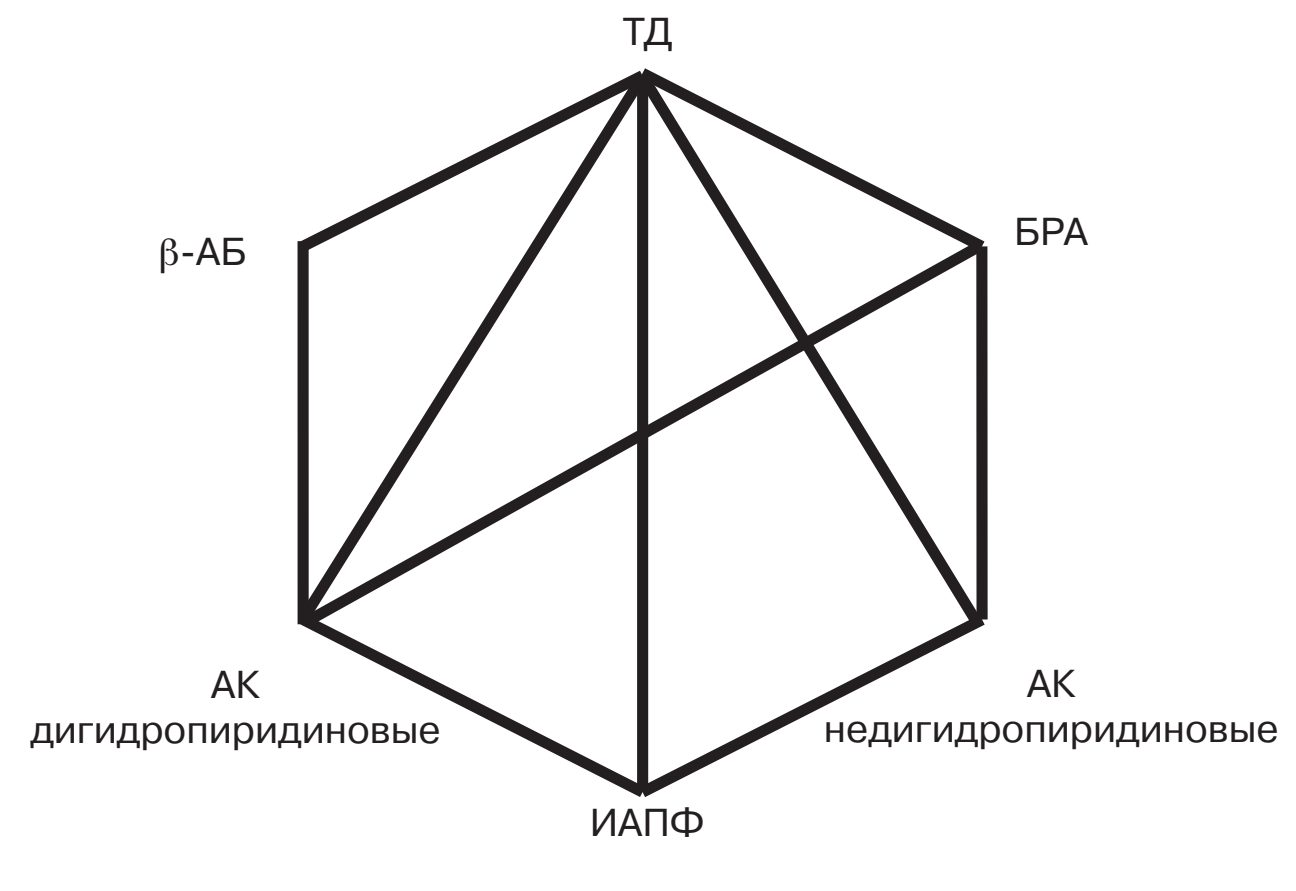
Схема 2. Рациональные комбинации антигипертензивных препаратов
Назначение фиксированной комбинации двух АГП может быть первым шагом лечения у пациентов с высоким сердечно-сосудистым риском или следовать сразу за монотерапией.
К возможным комбинациям АГП относятся сочетание дигидропиридинового и недигидропиридинового АК, ИАПФ + β-АБ, БРА + β-АБ, ИАПФ + БРА, прямого ингибитора ренина или α-адреноблокатора со всеми основными классами АГП. Применение этих комбинаций в виде двухкомпонентной АГТ в настоящее время не является абсолютно рекомендованным, но и не запрещено. Однако сделать выбор в пользу такого сочетания лекарственных средств допустимо только при полной уверенности в невозможности использования рациональных комбинаций. На практике больным АГ, имеющим ИБС и/или ХСН, одновременно назначают ИАПФ и β-АБ. Однако, как правило, в таких ситуациях назначение β-АБ происходит главным образом из-за наличия ИБС или ХСН, т.е. по самостоятельному показанию.
К комбинациям нерациональным, при использовании которых не происходит потенцирования антигипертензивного эффекта препаратов и/или усиливаются побочные эффекты при их совместном применении, относятся: сочетания разных лекарственных средств, относящихся к одному классу АГП, β-АБ + недигидропиридиновый АК, ИАПФ + калийсберегающий диуретик, β-АБ + препарат центрального действия.
Вопрос комбинирования 3 препаратов и более еще недостаточно изучен, поскольку нет результатов рандомизированных контролируемых клинических исследований, изучавших тройную комбинацию АГП. Таким образом, АГП в данных комбинациях объединены вместе на теоретической основе. Однако у многих пациентов, в том числе у больных с рефрактерной АГ, только с помощью 3- и более компонентной АГТ можно достичь целевого уровня АД [20]. К рекомендуемым комбинациям трех АГП относятся: ИАПФ + дигидропиридиновый АК + β-АБ; БРА + дигидропиридиновый АК + β-АБ; ИАПФ + АК + диуретик; БРА + АК + диуретик; ИАПФ + диуретик + β-АБ; БРА + диуретик + β-АБ; дигидропиридиновый АК + диуретик + β-АБ.
5.4.3. Сопутствующая терапия для коррекции имеющихся ФР
Необходимость назначения статинов для достижения целевых уровней ОХС<4,5 ммоль/л (175 мг/дл) и ХС ЛПНП<2,5 ммоль/л (100 мг/дл) должна быть рассмотрена у больных АГ при наличии ССЗ, а также у пациентов с высоким и очень высоким риском ССО [5].
Применение аспирина в низких дозах (75–150 мг в сутки) рекомендуется при наличии перенесенного ИМ, МИ или ТИА, если нет угрозы кровотечения [21]. Низкая доза аспирина также показана пациентам старше 50 лет с умеренным повышением уровня сывороточного креатинина или с очень высоким риском ССО даже при отсутствии других ССЗ. Доказано, что польза от снижения риска ССО при использовании аспирина превышает риск развития кровотечения. Для минимизации риска геморрагического МИ лечение аспирином может быть начато только после достижения величины АД <140/90 мм рт. ст.
Эффективный гликемический контроль очень важен у больных АГ и СД. Его можно достигнуть соблюдением диеты и/или медикаментозной терапии. Необходимо стремиться поддерживать уровень глюкозы в плазме крови натощак менее 6 ммоль/л (108 мг/дл) и гликированного гемоглобина менее 6,5%
6. Динамическое наблюдение
Достижение и поддержание целевых уровней АД требуют длительного врачебного наблюдения с регулярным контролем выполнения пациентом рекомендаций по изменению образа жизни и соблюдению режима приема назначенных антигипертензивных средств, а также коррекции терапии в зависимости от эффективности, безопасности и переносимости лечения. При динамическом наблюдении решающее значение имеют установление личного контакта между врачом и больным, обучение пациентов в школах для больных АГ, повышающее приверженность больного к лечению.
-
При назначении АГТ плановые визиты больного к врачу для оценки переносимости, эффективности и безопасности лечения, а также контроля выполнения полученных рекомендаций проводятся с интервалом 3–4 нед до достижения целевого уровня АД.
-
При недостаточной эффективности АГТ может быть произведена замена ранее назначенного препарата или присоединение к нему еще одного антигипертензивного средства.
-
При отсутствии эффективного снижения АД на фоне 2-компонентной терапии возможно присоединение третьего препарата (одним из трех препаратов, как правило, должен быть диуретик) с обязательным последующим контролем эффективности, безопасности и переносимости комбинированной терапии.
-
После достижения целевого уровня АД на фоне проводимой терапии последующие визиты для пациентов со средним и низким риском, которые регулярно измеряют АД дома, планируются с интервалом в 6 месяцев. Для больных с высоким и очень высоким риском, пациентов, получающих только немедикаментозное лечение, и лиц с низкой приверженностью к лечению интервалы между визитами не должны превышать 3 месяцев.
-
На всех плановых визитах необходимо контролировать выполнение пациентами рекомендаций по лечению. Поскольку состояние органов-мишеней изменяется медленно, контрольное обследование пациента для уточнения их состояния нецелесообразно проводить чаще 1 раза в год.
-
При «резистентной» АГ (АД>140/90 мм рт. ст. во время лечения тремя препаратами, один из которых диуретик, в субмаксимальных или максимальных дозах) необходимо убедиться в отсутствии объективных причин резистентности к терапии (п. 7.11). В случае истиной рефрактерности следует направить больного на дополнительное обследование.
-
Лечение пациента с АГ проводится постоянно или, по сути дела, у большинства больных пожизненно, так как его отмена сопровождается повышением АД. При стойкой нормализации АД в течение 1 года и соблюдении мер по изменению ОЖ у пациентов с низким и средним риском возможно постепенное уменьшение количества и/или снижение доз принимаемых АГП. Снижение дозы и/или уменьшение числа используемых медикаментов требуют увеличения частоты визитов к врачу и проведения самоконтроля АД дома, для того, чтобы убедиться в отсутствии повторных повышений АД.
7. Особенности лечения АГ у отдельных групп больных
7.1. АГ у лиц пожилого возраста
Результаты рандомизированных исследований свидетельствуют о том, что АГТ снижает риск ССЗ и смертности у пожилых больных с систоло-диастолической АГ и ИСАГ [23, 24].
Принципы лечения пожилых больных АГ такие же, как и для общей популяции. Лечение следует начинать с изменения ОЖ. Ограничение потребления поваренной соли и уменьшение массы тела у этой категории больных оказывают существенный антигипертензивный эффект. Для лечения ИСАГ в пожилом возрасте наиболее эффективны ТД и дигидропиридиновые АК, что доказано по результатам завершенных крупномасштабных исследований. Для медикаментозной терапии у пожилых больных с систолодиастолической АГ препаратами первого выбора являются ТД, дигидропиридиновые АК и БРА [24].
Начальная доза АГП у некоторых пожилых пациентов может быть снижена, вместе с тем у большинства больных этой категории требуется назначение стандартных доз для достижения целевого АД. У пожилых пациентов требуется особая осторожность при назначении и титровании дозы АГП из-за большего риска развития побочных эффектов. При этом особое внимание следует обратить на возможность развития ортостатической гипотонии и измерять АД также в положении стоя.
Целевой уровень АД при систоло-диастолической АГ должен быть 130–139/80–89 мм рт. ст., и для его достижения часто требуется комбинация 2-х и более АГП. При ИСАГ целевой уровень САД должен быть менее 150 мм рт. ст. Оптимальный уровень ДАД у пожилых больных точно не определен, но по результатам анализа ряда исследований снижение ДАД<70 мм рт. ст. и особенно <60 мм рт. ст. сопровождается ухудшением прогноза. У большинства пожилых пациентов имеются другие ФР, ПОМ и АКС, что необходимо учитывать при выборе АГП первого ряда. У пациентов старше 80 лет АГТ индапамидом с возможным добавлением периндоприла достоверно уменьшает риск развития ССО и общую смертность [23]. Поэтому необходимость проведения эффективной АГТ у пациентов любого возраста не вызывает сомнений.
7.2. АГ и МС
Наличие МС в 3–6 раз повышает риск развития СД типа 2 и АГ, ассоциируется с большей частотой встречаемости ПОМ, увеличивает риск ССО и смерти от них. Основой лечения пациента с МС являются немедикаментозные мероприятия, направленные на формирование здорового ОЖ и уменьшение массы тела. Обязательной является коррекция имеющихся нарушений углеводного, липидного и пуринового обмена. Пациентам с МС в случае повышения АД≥140/90 мм рт. ст. необходимо назначить АГП и проводить терапию, направленную на устранение абдоминального ожирения, инсулинорезистентности, гипергликемии, ДЛТ.
Препаратами первого выбора для лечения АГ у больных с МС являются ИАПФ и БРА, для которых доказана метаболическая нейтральность и органопротективное действие. БРА, активирующие PPAR-гаммарецепторы (peroxisome proliferative activated-gamma reseptor), например телмисартан, обладают дополнительными свойствами: уменьшают инсулинорезистентность, оказывают положительное влияние на углеводный, липидный обмен и функцию эндотелия. При недостаточной эффективности монотерапии для достижения целевого уровня АД к ним целесообразно присоединять АК или агонисты имидазолиновых рецепторов. Доказано, что эти комбинации хорошо снижают АД, благоприятно воздействуют на органы-мишени и снижают риск развития СД.
Без наличия отчетливых показаний больным с АГ и МС не следует назначать β-АБ, поскольку многие из них негативно влияют на чувствительность к инсулину, углеводный и липидный обмен. Исключением являются небиволол, бисопролол, метопролола сукцинат замедленного высвобождения и карведилол, которые могут быть рекомендованы для лечения пациентов с АГ и МС в составе комбинированной терапии. Тиазидные или петлевые диуретики также могут быть назначены пациентам с АГ и МС в составе комбинированной терапии с ИАПФ или БРА. Пациентам с АГ при наличии метаболических нарушений следует избегать комбинации β-АБ и диуретика, так как оба препарата неблагоприятно влияют на липидный, углеводный и пуриновый обмен.
7.3. АГ и СД
Сочетание СД и АГ заслуживает особого внимания, поскольку оба заболевания существенно увеличивают риск развития микро- и макрососудистых поражений, включая диабетическую нефропатию, МИ, ИБС, ИМ, ХСН, периферических сосудистых заболеваний и способствуют увеличению сердечно-сосудистой смертности.
Мероприятия по изменению ОЖ, особенно соблюдение низкокалорийной диеты, увеличение физической активности и ограничение потребления поваренной соли, должны быть максимально использованы, так как важную роль в прогрессировании СД типа 2 играет ожирение. Уменьшение массы тела у пациентов с АГ и СД помогает дополнительно снизить АД и увеличить чувствительность тканей к инсулину. Препаратами первого выбора являются ИАПФ или БРА, так как для них доказан наилучший ренопротективный эффект. В качестве комбинированной терапии к ним целесообразно присоединять АК, ТД в низких дозах, высокоселективные β-АБ (бисопролол и метопролола сукцинат замедленного высвобождения) или β-АБ с дополнительными свойствами (небиволол и карведилол).
Доказана также эффективность комбинированной терапии периндоприлом с индапамидом у больных с СД типа 2 в плане снижения риска ССО и смерти от них [25]. Учитывая больший риск возникновения ортостатической гипотонии необходимо дополнительно измерять АД в положении стоя. При лечении больных АГ и СД необходимо контролировать все имеющиеся у пациента ФР, включая ДЛТ. Наличие диабетической нефропатии у больных АГ связано с очень высоким риском развития ССО. При развитии нефропатии необходим строгий контроль АД на уровне ниже 130/80 мм рт. ст. и уменьшение протеинурии до минимально возможных значений. Наиболее эффективным классом АГП для профилактики или лечения диабетической нефропатии в настоящее время являются БРА и ИАПФ.
7.4. АГ и ЦВБ
Снижение АД высокоэффективно как в первичной, так и вторичной профилактике МИ ишемического и геморрагического типов. Если роль снижения АД не вызывает сомнений, то для уточнения способности различных классов АГП снижать риск цереброваскулярных осложнений требуется проведение дальнейших исследований. Поэтому для контроля АД в настоящее время могут использоваться все классы АГП и их рациональные комбинации. Однако не следует применять АГП, вызывающие ортостатическую гипотонию. Особенно осторожно следует снижать АД у больных с гемодинамически значимым атеросклерозом сонных артерий.
У больных, перенесших ТИА или МИ, следует использовать этапную схему снижения АД, учитывая индивидуальную переносимость и избегая эпизодов гипотонии. Особый контроль АД необходим в ночные часы.
В настоящее время нет убедительных данных о пользе снижения АД в остром периоде МИ. АГТ в этом случае начинается после стабилизации состояния пациента через несколько дней от начала МИ. В популяционных исследованиях доказана взаимосвязь уровня АД и риска развития когнитивной дисфункции и/или деменции, а также то, что АГТ может отсрочить их появление.
7.5. АГ и ИБС
Контроль АД у больных ИБС имеет важное значение, поскольку риск развития коронарных событий в значительной мере зависит от величины АД. b-АБ, ИАПФ или БРА у больных с перенесенным ИМ снижают риск развития повторного ИМ и смерти. Благоприятный эффект может быть связан как со специфическими свойствами этих препаратов, так и вследствие контроля за АД [8, 12, 26].
У больных с хронической ИБС антигипертензивное лечение с помощью разных классов препаратов оказывает благоприятное влияние на течение заболевания. Использование комбинаций ИАПФ с АК, включая фиксированные, способствует оптимальной кардио-, васкулопротекции и оказывает антиангинальное (антиишемическое) действие.
7.6. АГ и ХСН
Диастолическая дисфункция ЛЖ часто выявляется у больных АГ, особенно имеющих ГЛЖ, что ухудшает прогноз. В настоящее время нет доказательств преимущества какого-либо класса АГП у пациентов с диастолической дисфункцией ЛЖ. При сохранной систолической функции ЛЖ и наличии диастолической дисфункции ЛЖ рекомендованы БРА и ИАПФ.
У больных с застойной ХСН, преимущественно систолической, в анамнезе часто встречается АГ, хотя повышение АД при снижении сократительной функции миокарда ЛЖ бывает относительно редко. В качестве начальной терапии АГ при наличии застойной ХСН рекомендованы петлевые и тиазидные диуретики, ИАПФ, БРА, β-АБ и антагонисты альдостерона. АК дигидропиридинового ряда могут быть назначены в случае недостаточного антигипертензивного эффекта или при наличии стенокардии. Недигидропиридиновые АК не используют из-за возможности ухудшения сократительной способности миокарда и усиления симптомов ХСН.
7.7. АГ при поражении почек
АГ является решающим фактором прогрессирования ХПН любой этиологии, поэтому адекватный контроль АД замедляет ее развитие. Особое внимание следует уделять нефропротекции при диабетической нефропатии. Необходимо добиваться жесткого контроля АД <130/80 мм рт. ст. и уменьшения протеинурии или МАУ до величин, близких к нормальным.
При наличии протеинурии или МАУ препаратами выбора являются ИАПФ или БРА с внепочечным путем элиминации. В некоторых случаях возможно назначение комбинации ИАПФ с БРА. Для достижения целевого уровня АД при поражении почек часто требуется комбинированная терапия, включающая диуретик (при нарушении азотовыделительной функции почек – петлевой диуретик) и/или АК. У больных с поражением почек, особенно при СД, с учетом повышенного риска развития ССО часто показана комплексная терапия – АГП, статины, антиагреганты и др.
7.8. АГ у женщин
Эффективность АГТ и польза от ее применения одинаковы у мужчин и женщин. У женщин с АГ применение оральных контрацептивов, содержащих даже низкую дозу эстрогена, противопоказано из-за увеличения риска развития ИМ и МИ. Необходимо использовать только прогестеронсодержащие препараты, хотя доказательная база пока тоже недостаточна.
АГ и связанные с ней осложнения до настоящего времени остаются одной из основных причин заболеваемости и смертности матери, плода и новорожденного. Критерий диагностики АГ в период беременности – АД ≥140/90 мм рт. ст. Необходимо подтвердить повышение АД как минимум двумя измерениями. Классификация АГ в период беременности включает в себя: 1) хроническую АГ, диагностируемую до беременности или до 20 нед беременности; 2) гестационную АГ, развивающуюся после 20 нед беременности, не сопровождается протеинурией; 3) преэклампсию/эклампсию – возникает после 20 нед беременности и определяется по наличию АГ и протеинурии; 4) преэклампсию/эклампсию на фоне хронической АГ. Степени повышения АД в период беременности: умеренная (140–149/90–109 мм рт. ст.) и тяжелая (≥160/110 мм рт. ст.). АД ≥160/110 мм рт. ст. ассоциировано с ростом частоты геморрагического МИ у беременных [27].
Цель лечения беременных с АГ – предупредить развитие осложнений, обусловленных высоким уровнем АД, обеспечить сохранение беременности, нормальное развитие плода и успешные роды. Для беременных целевой уровень АД <140/90 мм рт. ст., но следует избегать эпизодов гипотонии, чтобы не нарушить плацентарный кровоток. У женщин с хронической АГ без ПОМ, АКС критерием начала АГТ считается АД ≥150/95 мм рт. ст. Женщины, у которых АД хорошо контролировалось до беременности, могут принимать те же препараты, за исключением ИАПФ и БРА.
Практически все АГП проникают через плаценту и потенциально способны оказывать нежелательное влияние на плод, новорожденного и/или дальнейшее развитие ребенка. Поэтому спектр АГП, используемых при беременности, ограничен. Препаратами 1-й линии являются метилдопа, дигидропиридиновые АК (нифедипин) и кардиоселективные β-АБ. В качестве дополнительных препаратов для комбинированной терапии возможно назначение диуретиков при хронической АГ (гидрохлоротиазид), клонидина при рефрактерной к терапии АГ [28] и a-АБ при феохромоцитоме [29]. Противопоказано назначение ИАПФ, БРА, препаратов раувольфии, дилтиазема и спиронолактона [30-32]. Следует воздержаться от использования малоизученных при беременности АГП, таких как индапамид и агонисты имидазолиновых рецепторов.
САД ≥170 и ДАД ≥110 мм рт. ст. у беременной женщины расценивается как неотложное состояние, требующее госпитализации. Для пероральной терапии следует использовать нифедипин или метилдопу. При неэффективности возможно кратковременное применение нитропруссида, гидралазина или клонидина. Для лечения преэклампсии с отеком легких препаратом выбора является нитроглицерин. Его применение возможно не более 4 ч из-за отрицательного воздействия на плод и риска развития отека мозга у матери. Применение диуретиков не оправдано, так как при преэклампсии уменьшается объем циркулирующей крови.
7.9. АГ в сочетании с патологией легких
Принимая во внимание высокую распространенность АГ и обструктивных заболеваний легких в популяции (в основном, это БА и ХОБЛ) и частое их сочетание у одного пациента, при назначении АГТ необходимо учитывать наличие сопутствующей бронхообструктивной патологии у пациента. Основное внимание при этом уделяется сочетанию ХОБЛ и ССЗ [33]. Среди пациентов с БА распространенность АГ также на 36% выше, чем у пациентов без респираторной патологии [34]. Назначать петлевые и тиазидные диуретики этим пациентам нужно с аккуратностью, так как вероятность развития гипокалиемии может усиливаться при назначении β2-агонистов и, особенно, системных стероидов [35]. β-АБ могут стать причиной развития бронхоспазма, особенно при использовании неселективных препаратов, поэтому не должны рутинно назначаться пациентам с обструктивной патологией легких [36]. При этом в ряде исследований, проведенных на ограниченном числе больных, показано, что применение небольших доз высокоселективных β-АБ (бисопролол, небиволол, метопролола сукцинат замедленного высвобождения) допустимо у пациентов как с ХОБЛ, так и с БА [37] под контролем показателей функции внешнего дыхания.
При назначении ИАПФ у пациентов как с бронхообструктивной патологией, так и без таковой отмечается возникновение кашля с частотой до 10–25%, что существенно снижает приверженность этих больных лечению [12, 36]. Существуют данные, что у части пациентов, в основном с БА, применение ИАПФ может приводить к развитию бронхоспазма из-за накопления бронхоирритантов (брадикинина и субстанции Р) [38]. БРА, в отличие от ИАПФ, не вызывают кашель и накопление бронхоирритантов [39]. Применение АК у пациентов с бронхообструктивной патологией безопасно и даже может привести к снижению гиперреактивности бронхов, повысить бронходилатирующий эффект β2-агонистов. Нифедипин снижает бронхоконстрикторный эффект гистамина и холодного воздуха [40]. В настоящее время БРА и АК являются предпочтительным вариантом АГТ у пациентов с БА и ХОБЛ.
Важным элементом лечения пациентов с сочетанием АГ и бронхообструктивной патологии является применение бронхолитических препаратов и глюкокортикостероидов (ГКС) для лечения ХОБЛ и БА. Системное применение ГКС часто повышает АД, однако при использовании невысоких доз ингаляционных ГКС подобные эффекты незначимы [41]. Использовать метилксантины необходимо с большой осторожностью из-за малого терапевтического диапазона и большого количества побочных эффектов [41]. При применении короткодействующих бронхолитических препаратов при ХОБЛ целесообразно комбинирование различных классов бронхолитиков (м-холинолитиков и β2-агонистов) для уменьшения дозы и побочных эффектов каждого из них. Применение пролонгированного м-холинолитика тиотропия бромида при ХОБЛ не вызывает кардиоваскулярных побочных эффектов и снижает смертность от ССО [42, 43]. β2-агонисты (короткодействующие и пролонгированные) совместно с ТД необходимо применять с осторожностью из-за возможного развития гипокалиемии.
7.10. АГ и синдром обструктивного апноэ во время сна
Синдром обструктивного апноэ во время сна (СОАС) – это состояние, характеризующееся периодическим спаданием верхних дыхательных путей на уровне глотки и прекращением легочной вентиляции при сохраняющихся дыхательных усилиях во время сна с последовательным снижением насыщения кислородом крови, грубой фрагментацией сна и избыточной дневной сонливостью. Наличие СОАС оказывает прямое отрицательное воздействие на сердечно-сосудистую систему, вызывая вазопрессорный эффект, эндотелиальную дисфункцию и оксидативный стресс, что ведет к еще большему повышению АД у пациентов с АГ и увеличивает риск развития ССО. Данный синдром часто сопутствует МС, и в настоящее время сочетание этих состояний принято обозначать как синдром Z. Ожирение – основной фактор риска развития СОАС, имеющийся у 50% тучных людей.
На наличие СОАС должны быть обследованы пациенты с АГ и ожирением, с резистентностью к АГТ, имеющие недостаточное снижение или повышение АД в ночное время по результатам СМАД. Признаками, позволяющими заподозрить СОАС, являются: беспокойный, неосвежающий сон; учащенное ночное мочеиспускание, дневная сонливость, разбитость, головные боли по утрам, хроническая усталость, снижение памяти и внимания, громкий, прерывистый храп, остановки дыхания во сне, нарастание массы тела и снижение потенции. Для первичной диагностики СОАС можно использовать опросник «Epworth Sleepiness Scale». Информацию, достаточную для постановки диагноза и установления степени тяжести СОАС, позволяет получить кардиореспираторное мониторирование. Однако «золотым стандартом» остается полисомнографическое исследование. Для оценки степени тяжести СОАС рассчитывают индекс апноэ/гипопноэ за 1 ч ночного сна. Легкое течение – от 5 до 15 приступов; течение средней тяжести – от 15 до 30 приступов и тяжелое течение – более 30 приступов в 1 ч.
Лечение больных с СОАС включает в себя уменьшение массы тела у больных с ожирением, отказ от курения, отказ от приема транквилизаторов и снотворных препаратов, мероприятия, направленные на обеспечение свободного носового дыхания, а также позиционное лечение (создание правильного положения головы по отношению к туловищу). Основной метод лечения больных с СОАС – создание постоянного положительного давления воздуха в дыхательных путях – CPAP (Continuous Positive Airways Pressure). При CPAP-терапии под давлением нагнетаемого воздуха расширяются и в дальнейшем не спадаются верхние дыхательные пути.
7.11. Рефрактерная АГ
Рефрактерной или резистентной к лечению считают АГ, при которой назначенное лечение – изменение ОЖ и рациональная комбинированная АГТ с применением адекватных доз не менее 3 препаратов, включая диуретики, не приводит к достаточному снижению АД и достижению его целевого уровня. В таких случаях показано детальное обследование органов-мишеней, так как при рефрактерной АГ в них часто наблюдаются выраженные изменения. Необходимо исключить вторичные формы АГ, которые служат причиной рефрактерности к антигипертензивному лечению. Неадекватные дозы АГП и их нерациональные комбинации также могут привести к недостаточному снижению АД. Рефрактерность АГ может быть связана с псевдогипертензией, например «гипертонией белого халата», или использованием несоответствующей по размеру манжеты. Основные причины рефрактерной к лечению АГ представлены в таблице 16. Тщательный анализ всех возможных причин рефрактерной АГ способствует рациональному выбору АГТ. Для контроля АД при рефрактерной АГ может потребоваться назначение более 3 АГП, хотя в настоящее время нет специальных исследований эффективности такой терапии. Однако доказано, что включение в комбинацию спиронолактона обеспечивает значительное дополнительное снижение АД.
|
7.12. Злокачественная АГ
Злокачественная АГ встречается редко. При злокачественной АГ наблюдается крайне высокое АД (>180/120 мм рт. ст.) с развитием тяжелых изменений сосудистой стенки (фибриноидный некроз), что приводит к кровоизлияниям и/или отеку соска зрительного нерва, ишемии тканей и нарушению функции различных органов. Переход АГ в злокачественную форму возможен при всех ее формах, однако чаще это происходит у пациентов с вторичной или тяжелой АГ. В развитии злокачественной АГ принимают участие различные нейрогормональные системы, активация их деятельности вызывает увеличение натрийуреза, гиповолемию, а также повреждает эндотелий и вызывает пролиферацию гладкомышечных клеток сосудов. Все эти изменения сопровождаются дальнейшим выбросом в кровяное русло вазоконстрикторов и еще большим повышением АД. Синдрому злокачественной АГ обычно сопутствуют симптомы со стороны центральной нервной системы, прогрессирование ХПН, ухудшение зрения, уменьшение массы тела, изменения реологических свойств крови, вплоть до развития синдрома диссеминированного внутрисосудистого свертывания или гемолитической анемии. Эффективное и своевременное лечение приводит к улучшению прогноза, тогда как при его отсутствии 50% пациентов умирают в течение первого года.
Наличие злокачественной АГ оценивается как тяжелое неотложное состояние и требует снижения ДАД до 100–110 мм рт. ст. в течение 24 ч. Пациентам со злокачественной АГ показано лечение комбинацией из 3 и более АГП. Следует помнить о возможности избыточного выведения из организма натрия, особенно при интенсивном назначении диуретиков, что сопровождается дальнейшей активацией РААС и повышением АД. Больной со злокачественной АГ должен быть еще раз тщательно обследован на предмет наличия вторичной АГ.
8. Диагностика и лечение вторичных форм АГ
Установить причину АГ удается лишь у небольшой части пациентов – у 5–10% взрослых лиц, страдающих АГ. Скрининг больных с целью выявления вторичных форм АГ основывается на изучении анамнеза заболевания, физикальном обследовании и инструментально-лабораторных методах исследования. Наличие вторичной формы АГ можно предположить при тяжелой и/или быстро прогрессирующей АГ, резистентной к проводимой терапии. В этих случаях необходимо проводить целенаправленное обследование для уточнения этиологии АГ.
8.1. АГ, связанная с патологией почек
Патология почек – наиболее частая причина вторичной АГ. УЗИ почек – неинвазивный метод, помогающий определить размер, форму, соотношение коркового и мозгового вещества почек, наличие обструкции в мочевыводящих путях и объемных образований в почках. Метод позволяет диагностировать поликистоз почек, опухоли почек и судить о возможных структурных изменениях в чашечно-лоханочной системе. В настоящее время УЗИ позволяет реже использовать внутривенную урографию с введением контрастного вещества, способного оказать нефротоксическое действие.
Микроскопия мочевого осадка в общем анализе мочи помогает обнаружить эритроциты, лейкоциты, цилиндры, клетки эпителия. О патологии почек свидетельствует протеинурия. Определение относительной плотности мочи и концентрации креатинина в сыворотке крови позволяет судить о функциональном состоянии почек. Эти исследования являются скрининговыми и должны проводиться всем больным АГ. При наличии патологических изменений показано более детальное обследование: количественные и специальные методы исследования мочи, в том числе бактериологическое – посев мочи с количественной оценкой степени бактериурии, радиологические методы – ренография с раздельным исследованием функции обеих почек. Важное диагностическое значение имеют КТ и МРТ почек. По показаниям выполняется биопсия почки.
8.2. АГ при поражении почечных артерий
Вазоренальная или реноваскулярная АГ – вторая по распространенности форма вторичной АГ, которая вызвана одно- или двусторонним стенозирующим поражением почечных артерий. Наиболее частой причиной вазоренальной АГ, особенно в пожилом возрасте, является атеросклероз почечных артерий (~75% случаев). Фибромышечная дисплазия чаще поражает лиц молодого возраста и является второй по частоте причиной реноваскулярной АГ (25%). Внезапное развитие или ухудшение течения АГ, резистентность к медикаментозной терапии – клинические проявления, позволяющие предположить наличие вазоренальной АГ. При стенозе почечных артерий примерно у 40% больных возможен систолический шум над брюшным отделом аорты, отмечается прогрессирующее снижение функции почек.
Важное диагностическое значение имеют инструментальные методы оценки асимметрии размеров, формы и функции почек, в частности УЗИ. Разница в размере почек, превышающая 1,5 см, – характерный признак вазоренальной АГ, однако указанную асимметрию можно обнаружить только у 60–70% больных. Дуплексное сканирование с цветовым допплеровским картированием почечных артерий позволяет выявить стенозы почечных артерий, особенно локализованные в устье сосуда. Чувствительность и специфичность метода во многом определяются опытом исследователя. С диагностической целью используются радиоизотопные методы исследования, позволяющие обнаружить асимметрию ренограмм, указывающую на стеноз почечных артерий. Информативным методом диагностики вазоренальной АГ является МРА; по некоторым данным, чувствительность этого метода превышает 95%. Высокоинформативный и чувствительный метод – спиральная КТ. При признаках, позволяющих заподозрить стеноз почечных артерий, подтвердить диагноз можно методом брюшной ангиографии. Это исследование – «золотой стандарт» для диагностики стеноза почечных артерий. Ангиография противопоказана при непереносимости рентгеноконтрастных препаратов и прогрессирующей ХПН. Катетеризация почечных вен с исследованием соотношения активности ренина в плазме (АРП) крови с обеих сторон и в нижней полой вене не является в достаточной мере чувствительным и специфичным методом, и не может быть рекомендована для скрининга, но позволяет оценить функциональную значимость стеноза почечной артерии.
Основные методы лечения: медикаментозная терапия, ангиопластика и стентирование пораженных почечных артерий, традиционное хирургическое лечение. Длительная медикаментозная терапия при доказанном функционально значимом стенозе почечных артерий не может считаться оправданной. В состав антигипертензивной комбинированной терапии включают АК, диуретики, а также препараты, блокирующие РААС, под контролем величины креатинина и калия в сыворотке крови. Применение их противопоказано при двустороннем гемодинамически значимом стенозе почечных артерий или стенозе почечной артерии единственной почки. При атеросклеротической этиологии вазоренальной АГ присоединяют гиполипидемическую терапию, применяют в небольших дозах аспирин.
8.3. Феохромоцитома
Феохромоцитома – опухоль, секретирующая катехоламины, в 90% случаев развивается из хромаффинных клеток мозгового слоя надпочечников, реже – из экстраадреналовой хромаффинной ткани в симпатических ганглиях и параганглиях различной локализации. Частота выявления феохромоцитом среди больных АГ составляет 0,1–0,8%. Более чем в 80% случаев феохромоцитома – доброкачественная опухоль. Диаметр опухолей достигает от 1 до 15 см. В 7–10% случаев феохромоцитомы могут быть составной частью наследственных синдромов, среди них синдром множественной эндокринной неоплазии (МЭН) типа 2А, реже – типа 2Б, болезнь Хиппеля-Линдау, болезнь Реклингхаузена в сочетании с кожным нейрофиброматозом. При подозрении на наследственную форму заболевания рекомендовано проведение генетического исследования. Выделяют различные варианты клинического течения феохромоцитом: кризовое – в 40–50% случаев, постоянная (стабильная) АГ без ГК – в 30–50% случаев. Нормальный уровень АД выявляется у 13% больных. Наиболее характерные проявления ГК: внезапное быстрое повышение АД до высокого уровня, учащенное сердцебиение, бледность кожных покровов, потливость, чувство беспокойства, страха. Показанием для обязательного обследования с целью возможного выявления феохромоцитомы являются следующие симптомы: кризовое течение АГ, гипертонический криз, провоцируемые приемом некоторых лекарств, наркозом, физической нагрузкой или другими факторами, стабильная АГ, рефрактерная к проводимой АГТ, пароксизмальная тахикардия, наличие семейных наследственных синдромов (МЭН типа 2А или 2Б), а также ближайшее родство с этими больными, инциденталома, выявленная при КТ или МРТ. Лабораторные методы диагностики включают: определение общей концентрации метанефринов (метанефрина и норметанефрина) в плазме крови и конъюгированных метанефринов в моче (чувствительность метода 98%), определение свободных катехоламинов в плазме крови – менее надежный метод, обладает низкой специфичностью, определение концентрации катехоламинов или их метаболитов в моче, собранной за сутки или за 3 ч после начала криза, – метод малоспецифичен, возможны ложноположительные результаты при приеме некоторых препаратов и пищевых продуктов. В сомнительных случаях для подтверждения гормональной активности опухоли проводятся фармакологические пробы, направленные на стимуляцию или супрессию секреции катехоламинов; пробы могут давать ложноположительные и ложноотрицательные результаты, сопряжены с осложнениями и применяются редко. Методы топической диагностики: УЗИ позволяет выявить опухоли, если их диаметр превышает 2 см; высокочувствительные методы – КТ и МРТ. Метод радиоизотопного сканирования с использованием метайодобензилгуанидина (123-I MIBG или 131-I MIBG) позволяет подтвердить функциональную активность феохромоцитом, выявленных в надпочечниках методами КТ или МРТ, диагностировать опухоли из хромаффинной ткани вненадпочечниковой локализации, а также метастазы злокачественных феохромоцитом.
Хирургическое удаление феохромоцитом – единственный радикальный метод лечения этого заболевания. Перед операцией для коррекции АД применяются α-АБ, по показаниям в дальнейшем к ним могут быть присоединены β-АБ. Монотерапия β-АБ без достаточной блокады α-адренорецепторов может привести к резкому повышению АД.
8.4. Первичный альдостеронизм
При первичном гиперальдостеронизме (синдром Конна) АГ развивается на фоне гиперпродукции альдостерона аденомой коры надпочечников. Распространенность этого заболевания составляет 1–11%. У большинства больных наблюдается умеренная и тяжелая АГ, резистентная к медикаментозной терапии. Характерными клиническими проявлениями являются: мышечная слабость, парестезии, судороги, никтурия. У части пациентов течение заболевания может быть малосимптомным. Сходные клинические проявления наблюдаются и при неопухолевых формах гиперальдостеронизма: в 70% случаев наблюдается двусторонняя гиперплазия коры надпочечников, реже – односторонняя гиперплазия коры надпочечников (идиопатический гиперальдостеронизм), а также семейная форма гиперальдостеронизма I типа (гиперальдостеронизм, корригируемый глюкокортикоидами). В редких случаях (не более 1%) причиной первичного альдостеронизма может быть злокачественная опухоль. У большинства (~80%) больных с аденомой или гиперплазией коры надпочечников избыточная секреция альдостерона сопровождается гипокалиемией – калий в плазме крови <3,6 ммоль/л. Поэтому для скрининга больных с первичным альдостеронизмом используют определение содержания калия в плазме крови, а также наличие гипокалиемических изменений, по данным ЭКГ. Категории пациентов с высоким риском наличия первичного альдостеронизма (с относительно высокой его распространенностью) подлежат обследованию (скрининг) для возможного выявления этого заболевания. Скрининг проводят при АГ 2–3 степени, при АГ, рефрактерной к проводимой АГТ, при наличии гипокалиемии (спонтанной или индуцированной диуретиками), при сочетании АГ и выявленной, по данным КТ или МРТ, инциденталоме, при семейном анамнезе АГ или цереброваскулярных осложнений в возрасте до 40 лет, у родственников 1 степени родства пациентов с первичным альдостеронизмом и АГ. Для уточнения функционального состояния надпочечников исследуют концентрацию альдостерона и АРП. Предварительно (не менее чем за 4 недели) отменяют лекарственные препараты, влияющие на эти показатели, в первую очередь – β-АБ, ИАПФ, БРА, диуретики, спиронолактон. Для обеспечения контроля АД при высоком его уровне допускается прием препаратов с минимальным воздействием на РААС: верапамила, α-АБ. Для аденомы (альдостеромы) и гиперплазии коры надпочечников характерна повышенная секреция альдостерона (>150 пг/мл) и низкая АРП, которая не превышает 1 нг/мл/ч после стимулирующего воздействия ходьбы (1–2-часовой) или фуросемида. Для скрининга низкоренинового гиперальдостеронизма анализируют также соотношение концентрации альдостерона к АРП; величина данного коэффициента зависит от единиц измерения, нижней границы определения АРП; при низком уровне АРП имеет место повышенная вероятность ложноположительных результатов. После скрининга больных с низкорениновой формой гиперальдостеронизма проводят дополнительные нагрузочные тесты для дифференциальной диагностики альдостеромы и гиперплазии коры надпочечников, поскольку тактика лечения этих форм АГ различна: больные с альдостеромой успешно лечатся хирургически, а больным с двусторонней гиперплазией коры надпочечников показано медикаментозное лечение. С целью дифференциальной диагностики применяют тест с 4-часовой ходьбой и другие нагрузочные пробы, направленные на стимуляцию или подавление показателей РААС (с каптоприлом, натриевой нагрузкой, физиологическим раствором, флюдрокортизоном). Выбор нагрузочной пробы зависит от состояния пациента (величины АД), а также опыта и предпочтений врача. Проба с дексаметазоном позволяет выявить больных с семейной формой гиперальдостеронизма I типа. Диагноз этого заболевания подтверждается при генетическом исследовании – выявлении химерного гена, патогномоничного для данного моногенного заболевания. Генетическое тестирование показано пациентам с проявлениями низкоренинового гиперальдостеронизма в молодом возрасте (до 20 лет), а также с отягощенным семейным анамнезом по низкорениновому гиперальдостеронизму или нарушениям мозгового кровообращения в молодом возрасте (до 40 лет).
Для визуализации изменений в надпочечниках и уточнения стороны локализации опухоли выполняют КТ или МРТ. О гормональной активности выявленных в надпочечниках структурных изменений можно судить по результатам проведения флебографии надпочечников и раздельной катетеризации вен надпочечников с определением концентрации альдостерона в крови, оттекающей от правого и левого надпочечников. Функциональное состояние надпочечников можно оценить также при радионуклидной визуализации с помощью меченого холестерина. Решение о тактике лечения принимается только после сопоставления структурных изменений надпочечников и их функциональной активности.
Хирургическое удаление альдостером (открытая адреналэктомия или эндоскопическая техника) у 50–70% больных приводит к нормализации или значительному снижению АД. До хирургического удаления альдостером, а также у пациентов с двусторонней гиперплазией коры надпочечников применяют спиронолактон, при недостаточном антигипертензивном эффекте возможно присоединение АК. У больных с семейной формой гиперальдостеронизма I типа проводят терапию ГКС (дексаметазон).
8.5. Синдром и болезнь Иценко-Кушинга
Синдром патологического гиперкортицизма – редкая причина АГ, встречается в 0,1% в общей популяции. Объединяет состояния, обусловленные гиперсекрецией глюкокортикоидов: болезнь Иценко-Кушинга, синдром Иценко-Кушинга и АКТГ – эктопированный синдром. АГ диагностируется при всех формах гиперкортицизма в 75–90% случаев. Диагноз заболевания при гиперсекреции ГКС устанавливается на основании клинической картины заболевания (характерный внешний вид больного – диспластическое ожирение, трофические изменения кожи, нарушение углеводного обмена, изменение костной системы) и дополнительных лабораторных исследований. Для выявления гиперкортицизма исследуют суточную экскрецию свободного кортизола с мочой, экскрецию суммарных 17-оксикортикостероидов в суточной моче, суточный ритм секреции кортизола и адренокортикотропного гормона АКТГ. Для дифференциальной диагностики опухоли (кортикостеромы) или гиперплазии коры надпочечников (опухоли гипофиза) решающее значение имеют функциональные пробы с дексаметазоном, АКТГ и др.
Для уточнения диагноза и выявления этиологии заболевания применяют методы топической диагностики: исследуют состояние гипофиза и надпочечников – КТ или МРТ, а также проводят рентгенологическое исследование органов грудной клетки с целью обнаружения опухоли и ее возможных метастазов; при злокачественных опухолях органов грудной клетки может иметь место АКТГ-эктопированный синдром. Методы лечения гиперкортицизма – в зависимости от установленной этиологии: хирургической, лучевой и медикаментозной. Для лечения АГ применяют ИАПФ, БРА, АК, диуретики и α-АБ, часто в комбинации.
8.6. Коарктация аорты
Коарктация аорты – врожденное органическое сужение аорты, чаще в зоне перешейка и дуги, относится к редким формам АГ. Для диагностики большое значение имеет повышенное АД на верхних конечностях при наличии нормального или пониженного АД на нижних. Пульсация на артериях нижних конечностей ослаблена, тогда как на лучевой артерии пульс не изменен. Выслушивается систолический шум над всей поверхностью сердца, а также в межлопаточном пространстве. Диагноз подтверждается при ЭхоКГ, ангиографии, МРТ. Лечение хирургическое.
8.7. Лекарственная форма АГ
Клекарственным средствам, способным повысить АД относятся: ГКС и нестероидные противовоспалительные препараты, гормональные противозачаточные средства, симпатомиметики, кокаин, эритропоэтин, циклоспорин, лакрица. При опросе пациентов необходимо тщательно выяснять, какие препараты принимались ранее и в настоящее время.
9.Неотложные состояния
Гипертонический криз (ГК) – это остро возникшее выраженное повышение АД, сопровождающееся клиническими симптомами, требующее немедленного контролируемого его снижения с целью предупреждения или ограничения поражения органов-мишеней.
ГК подразделяют на две большие группы – осложненные (жизнеугрожающие) и неосложненные (нежизнеугрожающие) ГК. В большинстве случаев ГК развивается при систолическом АД >180 мм рт. ст. и/или диастолическом АД >120 мм рт. ст., однако возможно развитие данного неотложного состояния и при менее выраженном повышении АД. У всех больных с ГК требуется быстрое снижение АД.
9.1. Осложненный ГК
Осложненный ГК сопровождается жизнеугрожающими осложнениями, появлением или усугублением ПОМ и требует снижения АД начиная с первых минут, в течение нескольких минут или часов при помощи парентерально вводимых препаратов. ГК считается осложненным, в следующих случаях:
-
гипертоническая энцефалопатия;
-
МИ;
-
ОКС;
-
острая ЛЖ-недостаточность;
-
расслаивающая аневризма аорты;
-
ГК при феохромоцитоме;
-
пре-эклампсия беременных;
-
тяжелая АГ, ассоциированная с субарахноидальным кровоизлиянием или травмой головного мозга;
-
АГ у послеоперационных больных и при угрозе кровотечения;
-
ГК на фоне приема амфетаминов, кокаина и др.
Лечение пациентов с осложненным ГК проводят в отделении неотложной кардиологии или палате интенсивной терапии кардиологического или терапевтического отделения. При наличии МИ целесообразна госпитализация в палату интенсивной терапии неврологического отделения или нейрореанимацию. АД следует снижать постепенно, во избежание ухудшения кровоснабжения головного мозга, сердца и почек, как правило, не более чем на 25% за первые 1–2 ч. Наиболее быстрое снижение АД необходимо при расслаивающей аневризме аорты (на 25% от исходного за 5–10 мин, оптимальное время достижения целевого уровня САД 100–110 мм рт. ст. составляет не более 20 мин), а также при выраженной острой ЛЖ-недостаточности (отек легких). Пациенты с МИ, ЦВБ требуют особого подхода, так как избыточное и/или быстрое снижение АД приводит к нарастанию ишемии головного мозга. В остром периоде МИ вопрос о необходимости снижения АД и его оптимальной величине решается совместно с неврологом индивидуально для каждого пациента.
Используются следующие парентеральные препараты для лечения ГК:
-
Вазодилататоры:
-
эналаприлат (предпочтителен при острой недостаточности ЛЖ);
-
нитроглицерин (при ОКС и острой недостаточности ЛЖ);
-
нитропруссид натрия (является препаратом выбора при гипертонической энцефалопатии, однако следует иметь в виду, что он может повышать внутричерепное давление).
-
-
β-АБ (метопролол, эсмолол предпочтительны при расслаивающей аневризме аорты и ОКС);
-
Антиадренергические средства (фентоламин при подозрении на феохромоцитому);
-
Диуретики (фуросемид при острой недостаточности ЛЖ);
-
Нейролептики (дроперидол);
-
Ганглиоблокаторы (пентамин).
9.2. Неосложненный ГК
Несмотря на выраженную клиническую симптоматику, неосложненный ГК не сопровождается острым клинически значимым нарушением функции органов-мишеней (п. 9.1). При неосложненном ГК возможно как внутривенное, так и пероральное либо сублингвальное применение АГП (в зависимости от выраженности повышения АД и клинической симптоматики). Лечение необходимо начинать немедленно, скорость снижения АД не должна превышать 25% за первые 2 ч, с последующим достижением целевого АД в течение нескольких часов (не более 24–48 ч) от начала терапии. Используют препараты с относительно быстрым и коротким действием перорально либо сублингвально: нифедипин, каптоприл, клонидин, пропранолол, празозин. Лечение больного с неосложненным ГК может осуществляться амбулаторно. При впервые выявленном неосложненном ГК у больных с неясным генезом АГ, при некупирующемся ГК, частых повторных кризах показана госпитализация в кардиологическое или терапевтическое отделение стационара.
10. Показания к госпитализации
Показаниями к госпитализации больных АГ служат:
-
неясность диагноза и необходимость в специальных, чаще инвазивных, методах исследований для уточнения формы АГ;
-
трудности в подборе медикаментозной терапии – частые ГК, рефрактерная АГ.
Показания к экстренной госпитализации:
-
ГК, не купирующийся на догоспитальном этапе;
-
ГК с выраженными проявлениями гипертонической энцефалопатии;
-
осложнения АГ, требующие интенсивной терапии и постоянного врачебного наблюдения: ОКС, отек легких, МИ, субарахноидальное кровоизлияние, остро возникшие нарушения зрения и др.;
-
злокачественная АГ.
11. Партнерские отношения с пациентами
Неотъемлемой частью мероприятий по длительной профилактике ССО у больных АГ должно стать повышение образовательного уровня пациентов. Если даже предположить, что для каждого конкретного больного АГ врач разработает оптимальную программу медикаментозного и немедикаментозного лечения, то провести ее в жизнь будет весьма сложно при наличии его низкой мотивации к лечению. Врачу необходимо информировать больного АГ о факторах и заболеваниях, сопутствующих АГ, риске развития осложнений и рассказать о пользе медикаментозного и немедикаментозного лечения АГ. Все применяемые методы лечения и профилактики должны быть обсуждены и согласованы с больным. В начале лечения необходимо выяснить, каким методам немедикаментозной профилактики отдает предпочтение больной, и затем максимально их использовать. При выборе препарата для лекарственной терапии нужно учесть образ жизни пациента и постараться выбирать препараты, принимаемые 1 раз в сутки. Желательно рекомендовать пациенту проводить самоконтроль АД дома. Все рекомендации, даваемые пациенту, должны быть ясными, четкими и соответствовать его интеллектуальному уровню. Для большинства пациентов устных рекомендаций недостаточно, поэтому лучше продублировать их в письменном виде. Такие меры должны обеспечить осознанное участие больного в лечебно-профилактическом процессе и повысить эффективность лечения.
12. Заключение
Представленные рекомендации являются итогом работы большого числа научных работников, врачей, организаторов здравоохранения. Они основаны на опыте как наших зарубежных коллег, так и отечественных ученых.
В сжатой форме представлены современные взгляды на диагностику и лечение АГ. Этот документ призван служить ориентиром в потоке информации по проблеме АГ. Безусловно, личный опыт врача имеет очень большое значение при принятии решения в отношении конкретного больного, однако это решение не должно противоречить накопленному международному и российскому опыту, отраженному в настоящих рекомендациях.
Эти рекомендации Российского медицинского общества по АГ (РМОАГ) и ВНОК изданы только для личного использования врачами. Коммерческое использование не разрешено. Никакая часть рекомендаций не может быть воспроизведена в любой форме без письменного разрешения РМОАГ. Разрешение может быть получено после представления письменного запроса ответственному секретарю РМОАГ (rshonline@hotmail.com).
Литература
-
Шальнова С., Кукушкин С., Маношкина Е., Тимофеева Т. Артериальная гипертензия и приверженность терапии. Врач. 2009; 12:39-42.
-
ESH-ESC Guidelines committee. 2007 guidelines for the management of arterial hypertension. J Hypertens 2007; 25: 1105–87.
-
Reappraisal of European guidelines on hypertension management: a European society of hypertension task force document. J Hypertens 2009; 27: 2121–58.
-
Диагностика и лечение метаболического синдрома. Российские рекомендации. Москва 2009 г. Кардиоваскул. тер. и профилак. 2009; 6 (Прил. 2).
-
Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза Российские рекомендации. Кардиоваскул. тер. и профилак. 2009; 6 (Прил. 3).
-
Devereux R, Reicheck N. Echocardiographic determinstion of left ventricular mass in man: anatomic validation of the method. Circulation 1977; 55: 613–18.
-
Yusuf S, Sleight P, Pogue J et al. Effects of an angiotensin-convertingenzyme inhibitor, ramipril, on cardiovascular events in high-risk patients. The heart outcomes prevention evaluation study investigators. N Engl J Med 2000; 342: 145–53.
-
The European trial on reduction of cardiac events with perindopril in stable coronary artery disease investigators. On reduction of cardiac events with perindopril in stable coronary artery disease investigators. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomised, double-blind, placebo-controlled, multicentre trial (the EUROPA study). Lancet 2003; 362: 782–88.
-
PROGRESS collaborative study group. Randomised trial of perindopril based blood pressure-lowering regimen among 6108 individuals with previous stroke or transient ischaemic attack. Lancet 2001; 358: 1033–41.
-
Чазова И.Е., Ратова Л.Г., исследователи «Клип-Аккорд». КЛИП-АККОРД: 4 года и 7796 пациентов – возможности полнодозовой комбинированной терапии артериальной гипертонии. Систем. гипертенз. 2008; 1: 4–9.
-
Чазова И.Е., Ратова Л.Г.. Комбинированная терапия у пациентов с артериальной гипертонией. Системные гипертензии 2010; 2: 6–10.
-
ONTARGET Investigators, Yusuf S, Teo K, Pogue J et al. Telmisartan, ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008; 358: 1547–59.
-
Veterans administration cooperative study group on antihypertensive agents. Effects of treatment on morbidity in hypertension. Results in patients with diastolic blood pressures averaging 115 through 129 mm Hg. JAMA 1967; 202: 1028–34.
-
Psaty B, Smith N, Siscovick D et al. Health outcomes associated with antihypertensive therapies used as first-line agents: a systematic review and meta-analysis. JAMA 1997; 277: 739–45.
-
Psaty B, Lumley T, Furberg C. Health outcomes associated with various antihypertensive therapies used as first-line agents. JAMA 2003; 289: 2534–44.
-
Lindholm LH, Carlberg B, Samuelsson O. Should beta blockers remain first choice in the treatment of primary hypertension? A meta-analysis. Lancet 2005; 366: 1545–53.
-
Wiysonge C, Bradley H, Mayosi B, et al. Beta blockers for hypertension. Cochrane Database Rev 2007; 1: CD002003.
-
Hansson L, Zanchetti A, Carruthers S et al. Effects of intensive blood-pressure lowering and low-dose aspirin in patients with hypertension: principal results of the hypertension optimal treatment (HOT) randomised trial. Lancet 1998; 351: 1755–62.
-
Чазова И.Е., Мартынюк Т.В., Колос И.П. Первые результаты Российской программы СТРАТЕГИЯ у пациентов с артериальной гипертензией: оценка эффективности Нолипрела при недостаточном контроле артериального давления. Cons. med. 2007; 9(5): 5–10.
-
Чазова И.Е., Беленков Ю.Н., Ратова Л.Г. и др. От идеи к клинической практике. Первые результаты российского национального исследования оптимального снижения артериального давления (РОСА). Систем. гипертенз.
2004; 2: 18–23. -
Antithrombotic Trialists’ Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ 2002; 324:71–86.
-
Ryden L, Standl E, Bartnik M et al. Task force on diabetes and cardiovascular diseases of the European society of cardiology (ESC); European association for the study of diabetes (EASD). Guidelines on diabetes, pre-diabetes, and cardiovascular diseases: executive summary. Eur Heart J 2007; 28: 88–136.
-
Beckett N, Peters R, Fletcher A et al; the HYVET Study Group. Treatment of hypertension in patients 80 years of age or older. N Engl J Med 2008; 358: 1887–98.
-
Lithell H, Hansson L, Skoog I et al., SCOPE Study Group. The study on cognition and prognosis in the elderly (SCOPE). Principal results of a randomised double-blind intervention trial. J Hypertens 2003; 21: 875–86.
-
Patel A; ADVANCE Collaborative Group, MacMahon S, Chalmers J et al. Effects of a fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomised controlled trial. Lancet 2007; 370: 829–40.
-
Fox K, Ferrari R, Yusuf S, Borer J. Should angiotensin-converting enzyme-inhibitors be used to improve outcome in patients with coronary artery disease and ‘preserved’ left ventricular function? Eur Heart J 2006; 27: 2154–57.
-
Martin J, Thigpen B, Moore R et al. Stroke and severe preeclampsia and eclampsia: a paradigm shift focusing on systolic blood pressure. Obstet Gynecol 2005; 105: 246–54.
-
Podymow Т, August Ph. Update on the Use of Antihypertensive Drugs in Pregnancy. Hypertension 2008; 51: 960–69.
-
Grodski S, Jung C, Kertes P et al. Phaeochromocytoma in pregnancy. Intern Med J 2006; 36: 604–6.
-
Hanssens M, Keirse M, Vankelecom F, Van Assche F. Fetal and neonatal effects of treatment with angiotensin-converting enzyme inhibitors in pregnancy. Obstet Gyn 1991; 78: 128–35.
-
Briggs G, Freeman R, Yaffe S. Drugs in Pregnacy and lactation. Seventh Edition. A Reference Guide to Fetal and Neonatal Risk. Lippincott Williams&Wilkins 2005.
-
Groves T, Corenblum B. Spironolactone therapy during human pregnancy. Am J Obstet Gyn 1995; 172: 1655–56.
-
Asthma and COPD (Second Edition) Basic Mechanisms and Clinical Management. Ed. P.J. Barnes Academic Press, Elsevier Ltd. 2009; 584–85.
-
Dogra S, Ardern C, Baker J. The relationship between age of asthma onset and cardiovascular disease in Canadians. J Asthma 2007; 44: 849–54.
-
Asthma. Ed by F. Chung. Eur Respir Mon. 2003; 8: 295.
-
Dart R, Gollub S, Lazar J et al. Treatment of systemic hypertension in patients with pulmonary disease. Chest 2003; 123: 222–43.
-
Salpeter S, Ormiston T, Salpeter E. Cardioselective beta-blockers for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2005; 19: CD003566.
-
Lunde H, Hedner T, Samuelsson O et al. Dyspnoea, asthma, and bronchospasm in relation to treatment with angiotensin converting enzyme inhibitors. BMJ 1994; 308: 18–21.
-
Benz J, Oshrain C, Henry D et al. Valsartan, a new angiotensin II receptor antagonist: a double-blind study comparing the incidence of cough with lisinopril and hydrochlorothiazide. J Clin Pharmacol 1997; 37: 101–7.
-
Barnes PJ. Clinical studies with calcium antagonists in asthma. Br J Clin Pharmacol 1985; 20 (Suppl. 2): S289–98.
-
The Global Strategy for Asthma Management and Prevention (updated 2009) www.ginasthma.org.
-
The Global Strategy for Diagnosis, Management and Prevention of COPD (updated 2009), the Executive Summary (updated 2009), www.goldcopd.org.
-
Celli B, Decramer M, Leimer I et al. Cardiovascular safety of tiotropium in patients with COPD. Chest 2010; 137: 20–30.
Авторы (рабочая группа по подготовке рекомендаций)
И.Е.Чазова, председатель (Москва), Л.Г.Ратова, секретарь (Москва), С.А.Бойцов (Москва), Д.В.Небиеридзе (Москва)
Комитет экспертов:
Карпов Ю.А., председатель (Москва), Белоусов Ю.Б. (Москва), Волкова Э.Г. (Челябинск), Галявич А.С. (Казань), Гринштейн Ю.И. (Красноярск), Ерегин С.Я. (Ярославль), Зыков К.А. (Москва), Карпов Р.С. (Томск), Кисляк О.А. (Москва), Кобалава Ж.Д. (Москва), Кухарчук В.В. (Москва), Литвин А.Ю. (Москва), Лопатин Ю.М. (Волгоград), Мартынов А.И. (Москва), Медведева И.В. (Тюмень), Милягин В.А. (Смоленск), Мычка В.Б. (Москва), Недбайкин А.М. (Брянск), Недогода С.В. (Волгоград), Никитин Ю.П. (Новосибирск), Оганов Р.Г. (Москва), Остроумова О.Д. (Москва), Ощепкова Е.В. (Москва), Перепеч Н.Б. (Санкт-Петербург), Подзолков В.И. (Москва), Поздняков Ю.М. (Московская область), Рогоза А.Н. (Москва), Симонова Г.И. (Новосибирск), Скворцова В.И. (Москва), Скибицкий В.В. (Краснодар), Терещенко С.Н. (Москва), Ткачева О.Н. (Москва), Туев А.В. (Пермь), Тюрина Т.В. (Ленинградская область), Фомин В.В. (Москва), Чихладзе Н.М. (Москва), Чумакова Г.А. (Барнаул), Шалаев С.В. (Тюмень), Шальнова С.А. (Москва), Шестакова М.В. (Москва), Якушин С.С. (Рязань)
Выпуск российских национальных рекомендаций по диагностике и лечению артериальной гипертензии поддержан научными грантами компаний:
АстраЗенека
Берингер Ингельхайм
КРКА
Лаборатории Сервье МСД Фармасьютикалс Никомед
Новартис Фарма












































