→
хлорированная — прилагательное, именительный п., жен. p., ед. ч.
→
хлорированная — прилагательное, именительный п., жен. p., ед. ч.
↳
хлорированная — причастие, именительный п., жен. p., прош. вр., страд, ед. ч.
Часть речи: инфинитив — хлорировать
Часть речи: прилагательное
Положительная степень:
Часть речи: глагол
Часть речи: деепричастие
Часть речи: причастие
Действительное причастие:
Страдательное причастие:
Часть речи: кр. причастие
Страдательное причастие:
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Смотреть что такое ХЛОРИРОВАННЫЙ в других словарях:
ХЛОРИРОВАННЫЙ
хлорированный прил. Из прич. по знач. сов. глаг.: хлорировать (2).
ХЛОРИРОВАННЫЙ
хлорированный
прил., кол-во синонимов: 2
• обеззараженный (11)
• хлорсодержащий (2)
Словарь синонимов ASIS.В.Н. Тришин.2013.
.
Синонимы:
обеззараженный… смотреть
ХЛОРИРОВАННЫЙ
1) Орфографическая запись слова: хлорированный2) Ударение в слове: хлор`ированный3) Деление слова на слоги (перенос слова): хлорированный4) Фонетическа… смотреть
ХЛОРИРОВАННЫЙ
-ая, -ое.1.прич. страд. прош. от хлорировать.
2. в знач. прил.
Обработанный хлором, насыщенный хлором.Хлорированная вода.Синонимы: обеззараженный
ХЛОРИРОВАННЫЙ
страд. прич., прош. вр.спец.Краткая форма: хлорированот глагола: хлорироватьхлорований
ХЛОРИРОВАННЫЙ
1) прич. от хлорировать2) прил. cloradoхлорированная вода — agua clorada
ХЛОРИРОВАННЫЙ
прич.; кр.ф. хлори/рован, хлори/рована, -вано, -ваны
Синонимы: обеззараженный
ХЛОРИРОВАННЫЙ
хлор’ированный; кратк. форма -ан, -анаСинонимы: обеззараженный
ХЛОРИРОВАННЫЙ
хлори́рованный, -ан, -ана, -ано, -аныСинонимы: обеззараженный
ХЛОРИРОВАННЫЙ
ХЛОРИРОВАННЫЙ хлорированная, хлорированное; хлорирован, хлорирована, хлорировано (спец.). Прич. страд. прош. вр. от хлорировать.
ХЛОРИРОВАННЫЙ
-ая, -ое1. прич. от хлорировать;2. хлорланған;- хлорированная вода хлорланған су
ХЛОРИРОВАННЫЙ
прил.
clorurato
Итальяно-русский словарь.2003.
Синонимы:
обеззараженный
ХЛОРИРОВАННЫЙ
хлорированный
хлорнок кардашуда
хлорированный
хлорнокшуда
Как правильно пишется слово «хлорированный»
хлори́рованный
хлори́рованный; кр. ф. -ан, -ана
Источник: Орфографический
академический ресурс «Академос» Института русского языка им. В.В. Виноградова РАН (словарная база
2020)
Делаем Карту слов лучше вместе
Привет! Меня зовут Лампобот, я компьютерная программа, которая помогает делать
Карту слов. Я отлично
умею считать, но пока плохо понимаю, как устроен ваш мир. Помоги мне разобраться!
Спасибо! Я стал чуточку лучше понимать мир эмоций.
Вопрос: фуражир — это что-то нейтральное, положительное или отрицательное?
Синонимы к слову «хлорированный»
Предложения со словом «хлорированный»
- Внутри запах хлорированной воды ощущался куда сильнее, здесь не чувствовался морской бриз и не было подводных течений, которые подталкивали бы её к финишу.
- Хлор полностью не испаряется и, соединяясь с органическими веществами, находившимися в воде, образует хлорированные углеводороды, в том числе диоксины, которые являются особо опасными ядами.
- Конечно, содержание его в водопроводной воде не столь велико, но не стоит забывать, что человек выпивает ежедневно в среднем два литра хлорированной воды.
- (все предложения)
Отправить комментарий
Дополнительно
Смотрите также
ХЛОРИ́РОВАННЫЙ, —ая, —ое. 1. Прич. страд. прош. от хлорировать.
Все значения слова «хлорированный»
-
Внутри запах хлорированной воды ощущался куда сильнее, здесь не чувствовался морской бриз и не было подводных течений, которые подталкивали бы её к финишу.
-
Хлор полностью не испаряется и, соединяясь с органическими веществами, находившимися в воде, образует хлорированные углеводороды, в том числе диоксины, которые являются особо опасными ядами.
-
Конечно, содержание его в водопроводной воде не столь велико, но не стоит забывать, что человек выпивает ежедневно в среднем два литра хлорированной воды.
- (все предложения)
- обеззараженный
- опреснённый
- озонированный
- подкислённый
- фильтрованный
- (ещё синонимы…)
Морфологический разбор «хлорированный»
На чтение 4 мин. Опубликовано 28.10.2021
В данной статье мы рассмотрим слово «хлорированный». В зависимости от контекста, оно может быть именем прилагательным или причастием. Ниже мы подробно разберём каждый из этих случаев, дадим морфологический разбор слова и укажем его возможные синтаксические роли.
Если вы хотите разобрать другое слово, то укажите его в форме поиска.
«Хлорированный» (имя прилагательное)
Морфологический разбор имени прилагательного
- I Часть речи: имя прилагательное;
- IIНачальная форма: хлорированный — единственное число, мужской род, именительный падеж;
- IIIМорфологические признаки:
- А. Постоянные признаки:
- Разряд по значению: относительное
- Б. Непостоянные признаки:
-
- мужской род, единственное число, полная форма, положительная степень
- именительный или винительный падеж
- IV Синтаксическая роль:
1) хлорированный – мужской род, единственное число, полная форма, положительная степень, именительный падеж
определение
именная часть сказуемого
2) хлорированный – мужской род, единственное число, полная форма, положительная степень, винительный падеж
Склонение имени прилагательного по падежам
| Падеж | Мужской род | Средний род | Женский род | Множественное число |
|---|---|---|---|---|
| Именительный падеж | Какой?хлорированный | Какое?хлорированное | Какая?хлорированная | Какие?хлорированные |
| Родительный падеж | Какого?хлорированного | Какого?хлорированного | Какой?хлорированной | Каких?хлорированных |
| Дательный падеж | Какому?хлорированному | Какому?хлорированному | Какой?хлорированной | Каким?хлорированным |
| Винительный падеж | Какого? Какой?хлорированного, хлорированный | Какого? Какое?хлорированное | Какую?хлорированную | Каких? Какие?хлорированные, хлорированных |
| Творительный падеж | Каким?хлорированным | Каким?хлорированным | Какой?хлорированною, хлорированной | Какими?хлорированными |
| Предложный падеж | О каком?хлорированном | О каком?хлорированном | О какой?хлорированной | О каких?хлорированных |
«Хлорированный» (причастие)
Значение слова «хлорировать» по словарю С. И. Ожегова
- Обеззаразить (-аживать) с помощью хлора
- Обработать (-батывать) хлором
Морфологический разбор причастия
- I Часть речи: причастие;
- IIНачальная форма: хлорировать;
- IIIМорфологические признаки:
- А. Постоянные признаки:
- страдательное
- невозвратное
- переходное
- прошедшее время
- несовершенный вид
- Б. Непостоянные признаки:
-
- мужской род, единственное число, полная форма
- именительный или винительный падеж
- IV Синтаксическая роль:
Разобрать другое слово
Введите слово для разбора:Найти
Относительными называются прилагательные, которые обозначают:
- из чего сделан предмет: деревянный стул (стул из дерева), стеклянная ваза (ваза из стекла), малиновое варенье (варенье из малины), бетонная стена (стена из бетона);
- для кого или чего предназначен предмет: детский магазин (магазин для детей), садоводческий фестиваль (фестиваль для садоводов), вязальные спицы (спицы для вязания);
- отношение предмета ко времени: осеннее похолодание (похолодание осенью), вечернее чаепитие (чаепитие вечером);
- отношение предмета к месту: горный хребет (хребет гор), лесной цветок (цветок леса);
- отношение предмета к области деятельности: футбольный журнал (журнал про футбол).
Относительные прилагательные не имеют антонимов и синонимов, степеней сравнения и кратких форм.
Отвечают на вопросы «какой?», «какая?», «какое?», «какие?».
Полные прилагательные отвечают на вопросы «какой?», «какая?», «какое?», «какие?» и могут склоняться по родам, числам и падежам.
Качественные и относительные прилагательные: отвечает на вопросы «какой?», «какая?», «какое?», «какие?»
Притяжательные прилагательные: отвечает на вопросы «чей?», «чья?», «чьё?», «чьи?»
Качественные и относительные прилагательные: отвечает на вопросы «какого?», «какой?», «какое?», «какую?», «каких?», «какие?»
Притяжательные прилагательные: отвечает на вопросы «чьего?», «чей?», «чьё?», «чью?», «чьих?», «чьи?»
Причастия несовершенного вида образуются от глаголов несовершенного вида и обозначают действие, которое ещё не завершено.
Несовершенного вида могут быть действительные и страдательные причастия прошедшего и настоящего времени:
| Действительное | Страдательное | |
|---|---|---|
| Прошедшее время | сотрудник, работавший допоздна — сотрудник, который (что делал?) работал допоздна | взрыв, виденный издалека — взрыв, который (что делали?) видели издалека |
| Настоящее время | сотрудник, работающий допоздна — сотрудник, который (что делает?) работает допоздна | взрыв, видимый издалека — взрыв, который (что делают?) видят издалека |
Невозвратные причастия образуются от невозвратных глаголов (без постфикса -ся (-сь)). Могут быть:
- переходными и непереходными: мама, одевающая дочку (перех.); собака, идущая на поводке (неперех.);
- действительными и страдательными: дети, гуляющие в парке (действ.); обед, приготовленный бабушкой (страд.).
Переходные причастия образуются от переходных глаголов, обозначают, что действие направлено на другой объект.
Могут сочетаться с существительными и местоимениями в винительном падеже (вопросы «кого?», «что?») без предлога.
Страдательные причастия обозначают признак предмета, над которым совершил действие кто-то другой.
Могут быть:
- прошедшего и настоящего времени: мороженое, купленное мамой (прош. вр.); звук, слышимый издалека (наст. вр.);
- совершенного (только в прошедшем времени) и несовершенного вида: чемодан, собранный в поездку (сов.); чемодан, собираемый в поездку (несов.);
- полными и краткими: посуда (какая?), вымытая дочкой (полн.); посуда (какова?) вымыта дочкой (крат.).
Страдательные причастия образуются только от переходных глаголов.
Полные причастия отвечают на вопросы «какой?», «какая?», «какое?», «какие?», бывают страдательными и действительными:
- действительные: папа (какой?), объясняющий задачу; бабушка (какая?), читавшая газету; дети (какие?), играющие в догонялки;
- страдательные: клубника (какая?), выращенная на грядке; трава (какая?), скошенная газонокосилкой; девочки (какие?), одетые нарядно; звук (какой?) слышимый издалека.
Морфемный разбор слова:
Однокоренные слова к слову:
Молекула хлора как пишется
Полезное
Смотреть что такое «хлор» в других словарях:
хлор — хлор, а … Русское словесное ударение
хлор — хлор, а … Русский орфографический словарь
хлор — хлор/ … Морфемно-орфографический словарь
ХЛОР — (греч. chloros зеленовато желтый). Химически простое, газообразное тело, зеленовато желтого цвета, острого, раздражающего запаха, имеющее способность обесцвечивать растительные вещества. Словарь иностранных слов, вошедших в состав русского языка … Словарь иностранных слов русского языка
ХЛОР — (символ С1), широко распространенный неметаллический элемент, один из ГАЛОГЕНОВ (элементы седьмой группы периодической таблицы), впервые открытый в 1774 г. Он входит в состав поваренной соли (NaCl). Хлор представляет собой зеленовато желтый… … Научно-технический энциклопедический словарь
ХЛОР — ХЛОР, С12, хим. элемент, порядковый номер 17, атомный вес 35,457. Находясь в VІI группе III периода, атомы хлора имеют 7 наружных электронов, благодаря чему X. ведет себя как типичный одновалентный металлоид. X. разделен на изотопы с атомными… … Большая медицинская энциклопедия
Хлор — обычно получают электролизом хлоридов щелочных металлов, в частности, хлорида натрия. Хлор зеленовато желтый удушливый, вызывающий коррозию газ, который в 2,5 раза плотнее воздуха, малорастворимый в воде и легко сжижаемый. Обычно транспортируется … Официальная терминология
Хлор — (Chlorum), Cl, химический элемент VII группы периодической системы, атомный номер 17, атомная масса 35,453; относится к галогенам; жёлто зелёный газ, tкип 33,97°C. Используется в производстве поливинилхлорида, хлоропренового каучука,… … Иллюстрированный энциклопедический словарь
ХЛОР — ХЛОР, хлора, мн. нет, муж. (от греч. chloros зеленый) (хим.). Химический элемент, удушливый газ, употр. в технике, в санитарии как обеззараживающее и в военном деле как отравляющее вещество. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
Хлор. — хлор. Начальная часть сложных слов, вносящая значения сл.: хлор, хлористый (хлорорганический, хлорацетон, хлорбензол, хлорметан и т.п.). Толковый словарь Ефремовой. Т. Ф. Ефремова. 2000 … Современный толковый словарь русского языка Ефремовой
Источник
Молекула хлора как пишется
Хлор ( χλωρός — зелёный) — элемент главной подгруппы седьмой группы, третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 17. Обозначается символом Cl (лат. Chlorum). Химически активный неметалл. Входит в группу галогенов (первоначально название «галоген» использовал немецкий химик Швейгер для хлора [дословно «галоген» переводится как солерод], но оно не прижилось, и впоследствии стало общим для VII группы элементов, в которую входит и хлор).
Простое вещество хлор (CAS-номер: 7782-50-5) при нормальных условиях — ядовитый газ желтовато-зелёного цвета, с резким запахом. Молекула хлора двухатомная (формула Cl2).
Впервые хлор был получен в 1772 г. Шееле, описавшим его выделение при взаимодействии пиролюзита с соляной кислотой в своём трактате о пиролюзите:
Шееле отметил запах хлора, схожий с запахом царской водки, его способность взаимодействовать с золотом и киноварью, а также его отбеливающие свойства.
Однако Шееле, в соответствии с господствовавшей в химии того времени теории флогистона, предположил, что хлор представляет собой дефлогистированную соляную кислоту, то есть оксид соляной кислоты. Бертолле и Лавуазье предположили, что хлор является оксидом элемента мурия, однако попытки его выделения оставались безуспешными вплоть до работ Дэви, которому электролизом удалось разложить поваренную соль на натрий и хлор.
Распространение в природе
Изотопный состав
В природе встречаются 2 стабильных изотопа хлора: с массовым числом 35 и 37. Доли их содержания соответственно равны 75,78 % и 24,22 %.
| Изотоп | Относительная масса, а.е.м. | Период полураспада | Тип распада | Ядерный спин |
|---|---|---|---|---|
| 35 Cl | 34.968852721 | Стабилен | — | 3/2 |
| 36 Cl | 35.9683069 | 301000 лет | β-распад в 36 Ar | 0 |
| 37 Cl | 36.96590262 | Стабилен | — | 3/2 |
| 38 Cl | 37.9680106 | 37,2 минуты | β-распад в 38 Ar | 2 |
| 39 Cl | 38.968009 | 55,6 минуты | β-распад в 39 Ar | 3/2 |
| 40 Cl | 39.97042 | 1,38 минуты | β-распад в 40 Ar | 2 |
| 41 Cl | 40.9707 | 34 c | β-распад в 41 Ar | |
| 42 Cl | 41.9732 | 46,8 c | β-распад в 42 Ar | |
| 43 Cl | 42.9742 | 3,3 c | β-распад в 43 Ar |
Физические и физико-химические свойства
При нормальных условиях хлор — жёлто-зелёный газ с удушающим запахом. Некоторые его физические свойства представлены в таблице.
Некоторые физические свойства хлора
1400°С
| Свойство | Значение |
|---|---|
| Температура кипения | −34 °C |
| Температура плавления | −101 °C |
| Температура разложения (диссоциации на атомы) |
|
| Плотность (газ, н.у.) | 3,214 г/л |
| Сродство к электрону атома | 3,65 эВ |
| Первая энергия ионизации | 12,97 эВ |
| Теплоемкость (298 К, газ) | 34,94 (Дж/моль·K) |
| Критическая температура | 144 °C |
| Критическое давление | 76 атм |
| Стандартная энтальпия образования (298 К, газ) | 0 (кДж/моль) |
| Стандартная энтропия образования (298 К, газ) | 222,9 (Дж/моль·K) |
| Энтальпия плавления | 6,406 (кДж/моль) |
| Энтальпия кипения | 20,41 (кДж/моль) |
При охлаждении хлор превращается в жидкость при температуре около 239 К, а затем ниже 113 К кристаллизуется в орторомбическую решётку с пространственной группой Cmca и параметрами a=6,29 Å b=4,50 Å, c=8,21 Å. Ниже 100 К орторомбическая модификация кристаллического хлора переходит в тетрагональную, имеющую пространственную группу P42/ncm и параметры решётки a=8,56 Å и c=6,12 Å.
Растворимость
| Растворитель | Растворимость г/100 г |
|---|---|
| Бензол | Растворим |
| Вода (0 °C) | 1,48 |
| Вода (20 °C) | 0,96 |
| Вода (25 °C) | 0,65 |
| Вода (40 °C) | 0,46 |
| Вода (60 °C) | 0,38 |
| Вода (80 °C) | 0,22 |
| Тетрахлорметан (0 °C) | 31,4 |
| Тетрахлорметан (19 °C) | 17,61 |
| Тетрахлорметан (40 °C) | 11 |
| Хлороформ | Хорошо растворим |
| TiCl4, SiCl4, SnCl4 | Растворим |
Порог восприятия запаха в воздухе равен 0,003 (мг/л).
В реестре CAS — номер 7782-50-5.
По электропроводности жидкий хлор занимает место среди самых сильных изоляторов: он проводит ток почти в миллиард раз хуже, чем дистиллированная вода, и в 10 22 раз хуже серебра. Скорость звука в хлоре примерно в полтора раза меньше, чем в воздухе.
Химические свойства
Строение электронной оболочки
| Валентность | Возможные степени окисления |
Электронное состояние валентного уровня |
Пример соединений |
|---|---|---|---|
| I | +1, −1 | 3s 2 3p 5 | NaCl, NaClO |
| III | +3 | 3s 2 3p 4 3d 1 | NaClO2 |
| V | +5 | 3s 2 3p 3 3d 2 | NaClO3 |
| VII | +7 | 3s 1 3p 3 3d 3 | NaClO4 |
Также известны соединения хлора, в которых атом хлора формально проявляет валентность 4 и 6, например ClO2 и Cl2O6. Однако, эти соединения являются радикалами, то есть у них есть один неспаренный электрон.
Взаимодействие с металлами
Хлор непосредственно реагирует почти со всеми металлами (с некоторыми только в присутствии влаги или при нагревании):
Взаимодействие с неметаллами
На свету или при нагревании активно реагирует (иногда со взрывом) с водородом по радикальному механизму. Смеси хлора с водородом, содержащие от 5,8 до 88,3 % водорода, взрываются при облучении с образованием хлороводорода. Смесь хлора с водородом в небольших концентрациях горит бесцветным или желто-зелёным пламенем. Максимальная температура водородно-хлорного пламени 2200 °C.:
С кислородом хлор образует оксиды в которых он проявляет степень окисления от +1 до +7: Cl2O, ClO2, Cl2O6, Cl2O7. Они имеют резкий запах, термически и фотохимически нестабильны, склонны к взрывному распаду.
При реакции с фтором, образуется не хлорид, а фторид:
Другие свойства
Хлор вытесняет бром и иод из их соединений с водородом и металлами:
При растворении в воде или щелочах, хлор дисмутирует, образуя хлорноватистую (а при нагревании хлорную) и соляную кислоты, либо их соли:
Действие хлора на аммиак можно получить трёххлористый азот:
Окислительные свойства хлора
Хлор очень сильный окислитель.
Реакции с органическими веществами
Присоединяется к ненасыщенным соединениям по кратным связям:
Ароматические соединения замещают атом водорода на хлор в присутствии катализаторов (например, AlCl3 или FeCl3):
Хлор способы получения хлора
Промышленные методы
Первоначально промышленный способ получения хлора основывался на методе Шееле, то есть реакции пиролюзита с соляной кислотой:
В 1867 году Диконом был разработан метод получения хлора каталитическим окислением хлороводорода кислородом воздуха. Процесс Дикона в настоящее время используется при рекуперации хлора из хлороводорода, являющегося побочным продуктом при промышленном хлорировании органических соединений.
Сегодня хлор в промышленных масштабах получают вместе с гидроксидом натрия и водородом путём электролиза раствора поваренной соли:
Так как параллельно электролизу хлорида натрия проходит процесс электролиз воды, то суммарное уравнение можно выразить следующим образом:
1,80 NaCl + 0,50 H2O → 1,00 Cl2↑ + 1,10 NaOH + 0,03 H2↑
Применяется три варианта электрохимического метода получения хлора. Два из них электролиз с твердым катодом: диафрагменный и мембранный методы, третий — электролиз с жидким ртутным катодом (ртутный метод производства). В ряду электрохимических методов производства самым легким и удобным способом является электролиз с ртутным катодом, но этот метод наносит значительный вред окружающей среде в результате испарения и утечек металлической ртути.
Диафрагменный метод с твердым катодом
Полость электролизера разделена пористой асбестовой перегородкой — диафрагмой — на катодное и анодное пространство, где соответственно размещены катод и анод электролизёра. Поэтому такой электролизёр часто называют диафрагменным, а метод получения — диафрагменным электролизом. В анодное пространство диафрагменного электролизера непрерывно поступает поток насыщенного анолита (раствора NaCl). В результате электрохимического процесса на аноде за счёт разложения галита выделяется хлор, а на катоде за счёт разложения воды — водород. При этом прикатодная зона обогащается гидроксидом натрия.
Мембранный метод с твердым катодом
Мембранный метод по сути, аналогичен диафрагменному, но анодное и катодное пространства разделены катионообменной полимерной мембраной. Мембранный метод производства эффективнее, чем диафрагменный, но сложнее в применении.
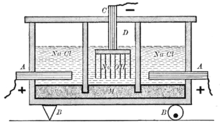
Ртутный метод с жидким катодом
Процесс проводят в электролитической ванне, которая состоит из электролизера, разлагателя и ртутного насоса, объединённых между собой коммуникациями. В электролитической ванне под действием ртутного насоса циркулирует ртуть, проходя через электролизёр и разлагатель. Катодом электролизера служит поток ртути. Аноды — графитовые или малоизнашивающиеся. Вместе с ртутью через электролизер непрерывно течет поток анолита — раствора хлорида натрия. В результате электрохимического разложения хлорида на аноде образуются молекулы хлора, а на катоде выделившийся натрий растворяется в ртути образуя амальгаму.
Лабораторные методы
В лабораториях для получения хлора обычно используют процессы, основанные на окислении хлороводорода сильными окислителями (например, оксидом марганца (IV), перманганатом калия, дихроматом калия):
Хранение хлора
Производимый хлор хранится в специальных «танках» или закачивается в стальные баллоны высокого давления. Баллоны с жидким хлором под давлением имеют специальную окраску — болотный цвет. Следует отметить что при длительной эксплуатации баллонов с хлором в них накапливается чрезвычайно взрывчатый треххлористый азот, и поэтому время от времени баллоны с хлором должны проходить плановую промывку и очистку от хлорида азота.
Стандарты качества хлора
Согласно ГОСТ 6718-93 «Хлор жидкий. Технические условия» производятся следующие сорта хлора
| Наименование показателя ГОСТ 6718-93 | Высший сорт | Первый сорт |
|---|---|---|
| Объемная доля хлора, не менее, % | 99,8 | 99,6 |
| Массовая доля воды, не более, % | 0,01 | 0,04 |
| Массовая доля треххлористого азота, не более, % | 0,002 | 0,004 |
| Массовая доля нелетучего остатка, не более, % | 0,015 | 0,10 |
Применение
Хлор применяют во многих отраслях промышленности, науки и бытовых нужд:
Многие развитые страны стремятся ограничить использование хлора в быту, в том числе потому, что при сжигании хлорсодержащего мусора образуется значительное количество диоксинов.
Биологическая роль хлора
Хлор относится к важнейшим биогенным элементам и входит в состав всех живых организмов.
Человек потребляет 5-10 г NaCl в сутки. Минимальная потребность человека в хлоре составляет около 800 мг в сутки. Младенец получает необходимое количество хлора через молоко матери, в котором содержится 11 ммоль/л хлора. NaCl необходим для выработки в желудке соляной кислоты, которая способствует пищеварению и уничтожению болезнетворных бактерий. В настоящее время участие хлора в возникновении отдельных заболеваний у человека изучено недостаточно хорошо, главным образом из-за малого количества исследований. Достаточно сказать, что не разработаны даже рекомендации по норме суточного потребления хлора. Мышечная ткань человека содержит 0,20-0,52 % хлора, костная — 0,09 %; в крови — 2,89 г/л. В организме среднего человека (масса тела 70 кг) 95 г хлора. Ежедневно с пищей человек получает 3-6 г хлора, что с избытком покрывает потребность в этом элементе.
Ионы хлора жизненно необходимы растениям. Хлор участвует в энергетическом обмене у растений, активируя окислительное фосфорилирование. Он необходим для образования кислорода в процессе фотосинтеза изолированными хлоропластами, стимулирует вспомогательные процессы фотосинтеза, прежде всего те из них, которые связаны с аккумулированием энергии. Хлор положительно влияет на поглощение корнями кислорода, соединений калия, кальция, магния. Чрезмерная концентрация ионов хлора в растениях может иметь и отрицательную сторону, например, снижать содержание хлорофилла, уменьшать активность фотосинтеза, задерживать рост и развитие растений.
Но существуют растения, которые в процессе эволюции либо приспособились к засолению почв, либо в борьбе за пространство заняли пустующие солончаки на которых нет конкуренции. Растения произрастающие на засоленных почвах называются — галофиты, они накапливают хлориды в течение вегетационного сезона, а потом избавляются от излишков посредством листопада или выделяют хлориды на поверхность листьев и веток и получают двойную выгоду притеняя поверхнисти от солнечного света. В России галофиты произрастают на соляных куполах, выходах соляных отложений и засоленных понижениях вокруг соляных озёр Баскунчак, Эльтон.
Среди микроорганизмов, так же известны галофилы — галобактерии — которые обитают в сильносоленых водах или почвах.
Особенности работы и меры предосторожности
Хлор — токсичный удушливый газ, при попадании в лёгкие вызывает ожог лёгочной ткани, удушье. Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе около 0,006 мг/л (т.е. в два раза выше порога восприятия запаха хлора). Хлор был одним из первых химических отравляющих веществ, использованных Германией в Первую мировую войну. При работе с хлором следует пользоваться защитной спецодеждой, противогазом, перчатками. На короткое время защитить органы дыхания от попадания в них хлора можно тряпичной повязкой, смоченной раствором сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3.
ПДК хлора в атмосферном воздухе следующие: среднесуточная — 0,03 мг/м³; максимально разовая — 0,1 мг/м³; в рабочих помещениях промышленного предприятия — 1 мг/м³.
Источник
Молекула хлора как пишется
Хлор / Chlorum (Cl), 17
3,214 г/л;
(жид. при −35 °C) 1,557;
(тв. при −105 °C) 1,9 г/см³
172,2 K ( Ошибка выражения: неопознанный символ пунктуации « »°C)
238,6 K ( Ошибка выражения: неопознанный символ пунктуации « »°C)
Простое вещество хлор (CAS-номер: 7782-50-5) при нормальных условиях — ядовитый газ желтовато-зелёного цвета тяжелее воздуха, с резким запахом. Молекула хлора двухатомная (формула Cl2).
Содержание
История открытия хлора
Соединение с водородом — газообразный хлороводород — было впервые получено Джозефом Пристли в 1772 г. Хлор был получен в 1774 г. шведским химиком Карлом Вильгельмом Шееле, описавшим его выделение при взаимодействии пиролюзита с соляной кислотой в своём трактате о пиролюзите:
Шееле отметил запах хлора, схожий с запахом царской водки, его способность взаимодействовать с золотом и киноварью, а также его отбеливающие свойства. Однако Шееле, в соответствии с господствовавшей в химии того времени теории флогистона, предположил, что хлор представляет собой дефлогистированную муриевую (соляную) кислоту. Бертолле и Лавуазье в рамках кислородной теории кислот обосновали, что новое вещество должно быть оксидом гипотетического элемента мурия. Однако попытки его выделения оставались безуспешными вплоть до работ Дэви, которому электролизом удалось разложить поваренную соль на натрий и хлор, доказав элементарную природу последнего.
Распространение в природе
В природе встречаются два изотопа хлора 35 Cl и 37 Cl. В земной коре хлор самый распространённый галоген. Хлор очень активен — он непосредственно соединяется почти со всеми элементами периодической системы. Поэтому в природе он встречается только в виде соединений в составе минералов: галита NaCl, сильвина KCl, сильвинита KCl · NaCl, бишофита MgCl2 · 6Н2О, карналлита KCl · MgCl2 · 6Н2O, каинита KCl · MgSO4 · 3Н2О. Самые большие запасы хлора содержатся в составе солей вод морей и океанов (содержание в морской воде 19 г/л [4] ). На долю хлора приходится 0,025 % от общего числа атомов земной коры; кларковое число хлора — 0,017 %. Человеческий организм содержит 0,25 % ионов хлора по массе. В организме человека и животных хлор содержится в основном в межклеточных жидкостях (в том числе в крови) и играет важную роль в регуляции осмотических процессов, а также в процессах, связанных с работой нервных клеток.
Изотопный состав
| Изотоп | Относительная масса, а.е.м. | Период полураспада | Тип распада | Ядерный спин | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 35 Cl | 34,968852721 | Стабилен | — | 3/2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 36 Cl | 35,9683069 | 301000 лет | β-распад в править] Физические и химические свойства
При нормальных условиях хлор — жёлто-зелёный газ с удушающим запахом. Некоторые его физические свойства представлены в таблице. 1400 °C
Газообразный хлор относительно легко сжижается. Начиная с давления в 0,8 МПа (8 атмосфер), хлор будет жидким уже при комнатной температуре. При охлаждении до температуры в −34 °C хлор тоже становится жидким при нормальном атмосферном давлении. Жидкий хлор — жёлто-зелёная жидкость, обладающая очень высоким коррозионным действием (за счёт высокой концентрации молекул). Повышая давление, можно добиться существования жидкого хлора вплоть до температуры в +144 °C (критической температуры) при критическом давлении в 7,6 МПа. Растворимость
Степень диссоциации молекулы хлора Cl2 → 2Cl при 1000 К равна 2,07·10 −4 %, а при 2500 К 0,909 %. Порог восприятия запаха в воздухе равен 0,003 (мг/л). По электропроводности жидкий хлор занимает место среди самых сильных изоляторов: он проводит ток почти в миллиард раз хуже, чем дистиллированная вода, и в 10 22 раз хуже серебра. Скорость звука в хлоре примерно в полтора раза меньше, чем в воздухе. Химические свойстваСтроение электронной оболочки
Также известны соединения хлора, в которых атом хлора формально проявляет валентность 4 и 6, например ClO2 и Cl2O6. Однако, эти соединения являются радикалами, то есть у них есть один неспаренный электрон. Взаимодействие с металламиХлор непосредственно реагирует почти со всеми металлами (с некоторыми только в присутствии влаги или при нагревании): Взаимодействие с неметалламиНа свету или при нагревании активно реагирует (иногда со взрывом) с водородом по радикальному механизму. Смеси хлора с водородом, содержащие от 5,8 до 88,3 % водорода, взрываются при облучении с образованием хлороводорода. Смесь хлора с водородом в небольших концентрациях горит бесцветным или желто-зелёным пламенем. Максимальная температура водородно-хлорного пламени 2200 °C.: С кислородом хлор образует оксиды в которых он проявляет степень окисления от +1 до +7: Cl2O, ClO2, Cl2O6, Cl2O7. Они имеют резкий запах, термически и фотохимически нестабильны, склонны к взрывному распаду. При реакции с фтором, образуется не хлорид, а фторид: Другие свойстваХлор вытесняет бром и иод из их соединений с водородом и металлами: При растворении в воде или щелочах, хлор дисмутирует, образуя хлорноватистую (а при нагревании хлорноватую) и соляную кислоты, либо их соли: Действием хлора на аммиак можно получить трихлорид азота: Окислительные свойства хлораХлор — очень сильный окислитель: Раствор хлора в воде используется для отбеливания тканей и бумаги. Реакции с органическими веществами Присоединяется к ненасыщенным соединениям по кратным связям: Ароматические соединения замещают атом водорода на хлор в присутствии катализаторов (например, AlCl3 или FeCl3): Способы полученияХимические методыХимические методы получения хлора малоэффективны и затратны. На сегодняшний день имеют в основном историческое значение. Может быть получен при взаимодействии перманганата калия с соляной кислотой: Метод ШеелеПервоначально промышленный способ получения хлора основывался на методе Шееле, то есть реакции пиролюзита с соляной кислотой: Метод ДиконаВ 1867 году Диконом был разработан метод получения хлора каталитическим окислением хлороводорода кислородом воздуха. Процесс Дикона в настоящее время используется при рекуперации хлора из хлороводорода, являющегося побочным продуктом при промышленном хлорировании органических соединений. Электрохимические методыСегодня хлор в промышленных масштабах получают вместе с гидроксидом натрия и водородом путём электролиза раствора поваренной соли, основные процессы которого можно представить суммарной формулой: Применяется три варианта электрохимического метода получения хлора. Два из них электролиз с твердым катодом: диафрагменный и мембранный методы, третий — электролиз с жидким ртутным катодом (ртутный метод производства). Качество хлора, получаемого электрохимическим методами, отличается мало:
Диафрагменный методНаиболее простым, из электрохимических методов, в плане организации процесса и конструкционных материалов для электролизера, является диафрагменный метод получения хлора. Раствор соли в диафрагменном электролизере непрерывно подается в анодное пространство и протекает через, как правило, насаженную на стальную катодную сетку асбестовую диафрагму, в которую, иногда, добавляют небольшое количество полимерных волокон. Насасывание диафрагмы производится путем прокачивания через электролизер пульпы из асбестовых волокон, которые, застревая в сетке катода образуют слой асбеста, играющий роль диафрагмы. Во многих конструкциях электролизеров катод полностью погружен под слой анолита (электролита из анодного пространства), а выделяющийся на катодной сетке водород отводится из под катода при помощи газоотводных труб, не проникая через диафрагму в анодное пространство благодаря противотоку. Анод: В качестве анода в диафрагменных электролизерах может использоваться графитовый или угольный электроды. На сегодня их в основном заменили титановые аноды с окисно-рутениево-титановым покрытием (аноды ОРТА) или другие малорасходуемые. Поваренная соль, сульфат натрия и другие примеси при повышении их концентрации в растворе выше их предела растворимости выпадают в осадок. Раствор едкой щёлочи декантируют от осадка и передают в качестве готового продукта на склад или продолжают стадию упаривания для получения твёрдого продукта, с последующим плавлением, чешуированием или грануляцией. Обратную, то есть кристаллизовавшуюся в осадок поваренную соль возвращают назад в процесс, приготавливая из неё так называемый обратный рассол. От неё, во избежание накапливания примесей в растворах, перед приготовлением обратного рассола отделяют примеси. Убыль анолита восполняют добавкой свежего рассола, получаемого подземным выщелачиванием соляных пластов галита, бишофита и других минералов содержащих хлорид натрия, а также растворением их в специальных емкостях на месте производства. Свежий рассол перед смешиванием его с обратным рассолом очищают от механических взвесей и значительной части ионов кальция и магния. Полученный хлор отделяется от паров воды, компримируется и подаётся либо на производство хлорсодержащих продуктов, либо на сжижение. Благодаря относительной простоте и дешевизне диафрагменный метод получения хлора до сих пор широко используется в промышленности. Мембранный методМембранный метод производства хлора наиболее энергоэффективен, однако сложен в организации и эксплуатации. С точки зрения электрохимических процессов мембранный метод подобен диафрагменному, но анодное и катодное пространства полностью разделены непроницаемой для анионов катионообменной мембраной. Поэтому в мембранном электролизере, в отличие от диафрагменного, не один поток, а два. В анодное пространство поступает, как и в диафрагменном методе, поток раствора соли. А в катодное — деионизированная вода. Из катодного пространства вытекает поток обедненного анолита, содержащего так же примеси гипохлорит- и хлорат-ионов и выходит хлор, а из анодного — щелока и водород, практически не содержащие примесей и близкие к товарной концентрации, что уменьшает затраты энергии на их упаривание и очистку. Однако, питающий раствор соли (как свежий так и оборотный) и вода предварительно максимально очищается от любых примесей. Такая тщательная очистка определяется высокой стоимость полимерных катионообменных мембран и их уязвимость к примесям в питающем растворе. Кроме того, ограниченная геометрическая форма а также низкая механическая прочность и термическая стойкость ионообменных мембран во многом определяют сравнительно сложные конструкции установок мембранного электролиза. По той же причине мембранные установки требуют наиболее сложных систем автоматического контроля и управления. Ртутный метод с жидким катодомВ ряду электрохимических методов получения хлора ртутный метод позволяет получать самый чистый хлор. Установка для ртутного электролиза состоит из электролизёра, разлагателя амальгамы и ртутного насоса, объединённых между собой ртутепроводящими коммуникациями. Катодом электролизёра служит поток ртути, прокачеваемой насосом. Аноды — графитовые, угольные или малоизнашивающиеся (ОРТА, ТДМА или другие). Вместе с ртутью через электролизёр непрерывно течёт поток питающего раствора поваренной соли. На аноде происходит окисление ионов хлора из электролита, и выделяется хлор: Хлор и анолит отводится из электролизёра. Анолит, выходящий из электролизера, донасыщают свежим галитом, извлекают из него примеси, внесённые с ним, а также вымываемые из анодов и конструкционных материалов, и возвращают на электролиз. Перед донасыщением из анолита извлекают растворённый в нём хлор. Растущие требования к экологической безопасности производств и дороговизна металлической ртути ведут к постепенному вытеснению ртутного метода методами получения хлора с твердым катодом. Лабораторные методыВвиду доступности хлора в лабораторной практике обычно используется сжиженный хлор в баллонах. Для получения хлора в небольших количествах обычно используются процессы, основанные на окислении хлороводорода сильными окислителями (например, оксидом марганца (IV), перманганатом калия, дихроматом калия, диоксид свинца, бертолетова соль и т. п.), обычно использовался диоксид марганца или перманганат калия: При невозможности использования баллонов могут быть использованы небольшие электролизеры с обычным или вентильным электродом для получения хлора. Хранение хлораПроизводимый хлор хранится в специальных «танках» или закачивается в стальные баллоны высокого давления. Баллоны с жидким хлором под давлением имеют специальную окраску — защитный цвет. Следует отметить, что при длительной эксплуатации баллонов с хлором в них накапливается чрезвычайно взрывчатый трихлорид азота, и поэтому время от времени баллоны с хлором должны проходить плановую промывку и очистку от хлорида азота. Стандарты качества хлораСогласно ГОСТ 6718-93 «Хлор жидкий. Технические условия» производятся следующие сорта хлора
ПрименениеХлор применяют во многих отраслях промышленности, науки и бытовых нужд: Многие развитые страны стремятся ограничить использование хлора в быту, в том числе потому, что при сжигании хлорсодержащего мусора образуется значительное количество диоксинов. Биологическая рольХлор относится к важнейшим биогенным элементам и входит в состав всех живых организмов в виде соединений. У животных и человека, ионы хлора участвуют в поддержании осмотического равновесия, хлорид-ион имеет оптимальный радиус для проникновения через мембрану клеток. Именно этим объясняется его совместное участие с ионами натрия и калия в создании постоянного осмотического давления и регуляции водно-солевого обмена. Под воздействием ГАМК (нейромедиатор) ионы хлора оказывают тормозящий эффект на нейроны путём снижения потенциала действия. В желудке ионы хлора создают благоприятную среду для действия протеолитических ферментов желудочного сока. Хлорные каналы представлены во многих типах клеток, митохондриальных мембранах и скелетных мышцах. Эти каналы выполняют важные функции в регуляции объёма жидкости, трансэпителиальном транспорте ионов и стабилизации мембранных потенциалов, участвуют в поддержании рН клеток. Хлор накапливается в висцеральной ткани, коже и скелетных мышцах. Всасывается хлор, в основном, в толстом кишечнике. Всасывание и экскреция хлора тесно связаны с ионами натрия и бикарбонатами, в меньшей степени с минералокортикоидами и активностью Na + /K + — АТФ-азы. В клетках аккумулируется 10-15 % всего хлора, из этого количества от 1/3 до 1/2 — в эритроцитах. Около 85 % хлора находятся во внеклеточном пространстве. Хлор выводится из организма в основном с мочой (90-95 %), калом (4-8 %) и через кожу (до 2 %). Экскреция хлора связана с ионами натрия и калия, и реципрокно с HCO3 − (кислотно-щелочной баланс). Человек потребляет 5-10 г NaCl в сутки. Минимальная потребность человека в хлоре составляет около 800 мг в сутки. Младенец получает необходимое количество хлора через молоко матери, в котором содержится 11 ммоль/л хлора. NaCl необходим для выработки в желудке соляной кислоты, которая способствует пищеварению и уничтожению болезнетворных бактерий. В настоящее время участие хлора в возникновении отдельных заболеваний у человека изучено недостаточно хорошо, главным образом из-за малого количества исследований. Достаточно сказать, что не разработаны даже рекомендации по норме суточного потребления хлора. Мышечная ткань человека содержит 0,20-0,52 % хлора, костная — 0,09 %; в крови — 2,89 г/л. В организме среднего человека (масса тела 70 кг) 95 г хлора. Ежедневно с пищей человек получает 3-6 г хлора, что с избытком покрывает потребность в этом элементе. Ионы хлора жизненно необходимы растениям. Хлор участвует в энергетическом обмене у растений, активируя окислительное фосфорилирование. Он необходим для образования кислорода в процессе фотосинтеза изолированными хлоропластами, стимулирует вспомогательные процессы фотосинтеза, прежде всего те из них, которые связаны с аккумулированием энергии. Хлор положительно влияет на поглощение корнями кислорода, соединений калия, кальция, магния. Чрезмерная концентрация ионов хлора в растениях может иметь и отрицательную сторону, например, снижать содержание хлорофилла, уменьшать активность фотосинтеза, задерживать рост и развитие растений. Но существуют растения, которые в процессе эволюции либо приспособились к засолению почв, либо в борьбе за пространство заняли пустующие солончаки на которых нет конкуренции. Растения произрастающие на засоленных почвах называются — галофиты, они накапливают хлориды в течение вегетационного сезона, а потом избавляются от излишков посредством листопада или выделяют хлориды на поверхность листьев и веток и получают двойную выгоду притеняя поверхности от солнечного света. Среди микроорганизмов, так же известны галофилы — галобактерии — которые обитают в сильносоленых водах или почвах. Особенности работы и меры предосторожностиХлор — токсичный удушливый газ, при попадании в лёгкие вызывает ожог лёгочной ткани, удушье. Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе около 0,006 мг/л (т.е. в два раза выше порога восприятия запаха хлора). Хлор был одним из первых химических отравляющих веществ, использованных Германией в Первую мировую войну. При работе с хлором следует пользоваться защитной спецодеждой, противогазом, перчатками. На короткое время защитить органы дыхания от попадания в них хлора можно тряпичной повязкой, смоченной раствором сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3. ПДК хлора в атмосферном воздухе следующие: среднесуточная — 0,03 мг/м³; максимально разовая — 0,1 мг/м³; в рабочих помещениях промышленного предприятия — 1 мг/м³. Источник Теперь вы знаете какие однокоренные слова подходят к слову Молекула хлора как пишется, а так же какой у него корень, приставка, суффикс и окончание. Вы можете дополнить список однокоренных слов к слову «Молекула хлора как пишется», предложив свой вариант в комментариях ниже, а также выразить свое несогласие проведенным с морфемным разбором. Какие вы еще знаете однокоренные слова к слову Молекула хлора как пишется: |
ПРОИЗНОШЕНИЕ СЛОВА ХЛОРИРОВАННЫЙ
ЧТО ОЗНАЧАЕТ СЛОВО ХЛОРИРОВАННЫЙ
Значение слова хлорированный в словаре русский языка
ХЛОРИРОВАННЫЙ прилагательное см. хлорировать.
СЛОВА, РИФМУЮЩИЕСЯ СО СЛОВОМ ХЛОРИРОВАННЫЙ
ПЕРЕВОД СЛОВА ХЛОРИРОВАННЫЙ
Посмотрите перевод слова хлорированный на 25 языков с помощью нашего многоязыкового переводчика c русский языка.
Переводы слова хлорированный с русский языка на другие языки, представленные в этом разделе, были выполнены с помощью автоматического перевода, в котором главным элементом перевода является слово «хлорированный» на русский языке.
Переводчик с русский языка на китайский язык
氯化
1,325 миллионов дикторов
Переводчик с русский языка на испанский язык
clorada
570 миллионов дикторов
Переводчик с русский языка на английский язык
chlorinated
510 миллионов дикторов
Переводчик с русский языка на хинди язык
क्लोरीनयुक्त
380 миллионов дикторов
Переводчик с русский языка на арабский язык
المكلورة
280 миллионов дикторов
Переводчик с русский языка на португальский язык
clorada
270 миллионов дикторов
Переводчик с русский языка на бенгальский язык
ক্লোরিনযুক্ত
260 миллионов дикторов
Переводчик с русский языка на французский язык
chloré
220 миллионов дикторов
Переводчик с русский языка на малайский язык
berklorin
190 миллионов дикторов
Переводчик с русский языка на немецкий язык
chlorierte
180 миллионов дикторов
Переводчик с русский языка на японский язык
塩素化
130 миллионов дикторов
Переводчик с русский языка на корейский язык
염화
85 миллионов дикторов
Переводчик с русский языка на яванский язык
chlorinated
85 миллионов дикторов
Переводчик с русский языка на вьетнамский язык
clo
80 миллионов дикторов
Переводчик с русский языка на тамильский язык
குளோரின்
75 миллионов дикторов
Переводчик с русский языка на маратхи язык
क्लोरिनेटेड
75 миллионов дикторов
Переводчик с русский языка на турецкий язык
klorlu
70 миллионов дикторов
Переводчик с русский языка на итальянский язык
clorurati
65 миллионов дикторов
Переводчик с русский языка на польский язык
chlorowana
50 миллионов дикторов
Переводчик с русский языка на украинский язык
хлорований
40 миллионов дикторов
Переводчик с русский языка на румынский язык
clorurat
30 миллионов дикторов
Переводчик с русский языка на греческий язык
χλωριωμένα
15 миллионов дикторов
Переводчик с русский языка на африкаанс язык
gechlorineerde
14 миллионов дикторов
Переводчик с русский языка на шведский язык
klorerad
10 миллионов дикторов
Переводчик с русский языка на норвежский язык
klor
5 миллионов дикторов
ТЕНДЕНЦИИ ИСПОЛЬЗОВАНИЯ ТЕРМИНА «ХЛОРИРОВАННЫЙ»

На показанной выше карте показана частотность использования термина «хлорированный» в разных странах.
Примеры использования в литературе на русский языке, цитаты и новости о слове хлорированный
КНИГИ НА РУССКИЙ ЯЗЫКЕ, ИМЕЮЩЕЕ ОТНОШЕНИЕ К СЛОВУ «ХЛОРИРОВАННЫЙ»
Поиск случаев использования слова хлорированный в следующих библиографических источниках. Книги, относящиеся к слову хлорированный, и краткие выдержки из этих книг для получения представления о контексте использования этого слова в литературе на русский языке.
1
Химия лигнина — Страница 337
ёё видная ‘6 ‘ф [88 данные гидролиза хлорированных лигнинов (в %) (по данным Зона [33]) . Таблица 3 Содержание хлора Содержание МВТОКС’НЛОВ м п __ Тип щелочной репарат лигиниа обработки до щелоч- после до …
2
Справочник для инженеров и мастеров по производству …
Следующей операцией является нейтрализация, состоящая в переработке хлорированного ^ензола с кальцинированной содой для удаления растворенных в нем хлористого водорода и хлористого желеаа. Из нейтрализаторов …
Ушаков Н. Н., Лебедев И. В., 2013
3
Труды — Объемы 13-14 — Страница 103
Указанная особенность действия хлорорганических соединений более наглядно может быть показана на примере фракций хлорированного парафина. ФРАКЦИИ ХЛОРИРОВАННОГО ПАРАФИНА Хлорированный парафин …
Институт нефти (Академия наук СССР), 1959
4
Средства и способы защиты организма от повреждающих …
поглотителя, г/кг Промышленный Хлорированный 3,57 1,20 13,9 активный уголь Хлорированный 4,70 41,0 СКТ Жгутовое Хлорированное 8,24 2,13 18,0 активированное Хлорированное 8,28 3,24 73,0 углеродное Хлорированное 8 …
Анна Морозова, Евгений Конопля, 2014
5
Краткая химическая энциклопедия — Страница 710
Хлорированный Н выпускается в промышленном насштабе под маркой «а л л о п р е н» (Англия); содержит 65%хлора, плотн. —-— 1,6 г/смз, мол. в. не менее 5000, т. разлож. 18 200°, уд. объемное электрич. сопротивление 510 2 …
6
Большой энциклопедический словарь медицинских терминов: …
… кислота] египерхлоргидрия хлордан хлорированный углеводород, стойкий и жирорастворимый инсектицид; при всасывании через кожу приводит к тяжёлым отравлениям хлордиазепоксид»»‘НН производное бензодиазепина; …
Эрнст Галимович Улумбеков, 2013
7
Хлорированные диоксиний: биологические и медицинские …
Изомерический структурный аналог 2,3,7,8-ТХДЦ 3,4, 3′ ,4′-тетрахлоразобензол является слабым мутагеном в тесте Эймса, но менее хлорированный гомолог, 4,4′-дихлоразобензол, и 4,4′-дихлоразоксибензол значительно …
8
Органические вещеста — Страница 257
Чаше всего тяжелые и даже смертельные отравления X. Д. наблюдались при применении их в смеси с хлорированными нафталинами. Описаны, однако, поражения кожи с типичными хлоракне на руках, шее, лице, ушах при …
Николай Васильевич Лазарев, 1963
9
Справочник химика. Сырье и продукты промышленности …
Кислоты . . . . х. х. х. отл. отл. о. 1. отл. 0. х. х. ЩеЛочн . . . . о. к. 0. х х. отл. отл. отл. отл. о. к. отл. Растворители: алифатическше , п. п. отл. п. 0. х. уд. отл. 0. к. И. ароматические о. п. 0. п. х. о. п. п. ул. 0. к. п. о. п. хлорированные . 0. п.
10
Trudy konferentsii — Том 3 — Страница 236
поставили перед собой задачу установить сравнительную активность хлорированного парафина среди других синтезированных добавок и определить противоизносные свойства отдельных фракций хлорированного парафина.
Всесоюзная конференция по трению и износу в машинах.3д,Москов,1958, 1960
НОВОСТИ, В КОТОРЫХ ВСТРЕЧАЕТСЯ ТЕРМИН «ХЛОРИРОВАННЫЙ»
Здесь показано, как национальная и международная пресса использует термин хлорированный в контексте приведенных ниже новостных статей.
Этот город самый сложный
Это дыра в стене, из которой веет хлорированный ветер. Очень красиво, тонко даже. Но если распутывать цепочку ассоциаций, которые этот проект … «Коммерсантъ, Окт 15»
Компактная установка позволит получить топливо из отходов
Биофильтр задерживает запахи, а хлорированный фильтр устраняет патогенные микроорганизмы в производимых удобрениях. Установки TevaGas … «Великая Эпоха, Окт 15»
Капитан дальнего плавания: обзор Sony Xperia M4 Aqua
Производитель и вовсе не советует брать его не только на морской берег, но и в хлорированный бассейн. Капитан дальнего плавания: обзор Sony … «Gagadget.com | нескучный сайт о технике, Авг 15»
Адаптация «Пластилин»
«Опилки» и «Хлорированный запах общежитий» были возрождены несколько лет назад для специального тура «Адаптации» с баянистом Виталием … «KM.RU, Апр 13»
А после тренировки – сразу в море! Совмещает приятное с …
Причем куда более полезная, чем хлорированный бассейн. Насчет работы и отдыха у меня случился в отеле еще один забавный диалог – с Игорем … «Советский спорт, Янв 12»
Жить надо живо!
… поступления на медицинский факультет Новосибирского университета понял, что не готов всю жизнь чувствовать хлорированный запах больницы. «Центр Азии, Авг 11»
Как спасти купальник от хлора? Есть народные средства?
Бассейн хлорированный, хоть и слабо, но все же цвет становится блеклым. … устойчивость к хлорированной и вторированной воде, более плотная и … «Woman.ru — интернет для женщин, Апр 10»
Полимерные трубы для теплоснабжения : основные виды …
Совсем иное – хлорированный поливинилхлорид (ХПВХ). Трубы из него имеют приемлемые для горячего водоснабжения и отопления характеристики. «Plastinfo, Авг 08»
































 — основной процесс
— основной процесс 
 Катод:
Катод:  — основной процесс
— основной процесс 






