Сепсис
Версия: Клинические протоколы МЗ РК — 2020 (Казахстан)
Категории МКБ:
Бактериальная инфекция неуточненная (A49.9), Диссеминированная герпетическая болезнь (B00.7), Другая септицемия (A41), Другие виды шока (R57.8), Другие гонококковые инфекции (A54.8), Инфекция, связанная с иммунизацией (T88.0), Кандидозная септицемия (B37.7), Острый или молниеносный мелиоидоз (A24.1), Сальмонеллезная септицемия (A02.1), Сибиреязвенная септицемия (A22.7), Синдром системного воспалительного ответа инфекционного происхождения с полиорганной недостаточностью (R65.1), Синдром токсического шока (A48.3), Стрептококковая септицемия (A40), Шок во время или после процедуры, не классифицированный в других рубриках (T81.1)
Разделы медицины:
Инфекционные и паразитарные болезни, Хирургия
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «01» апреля 2020 года
Протокол №89
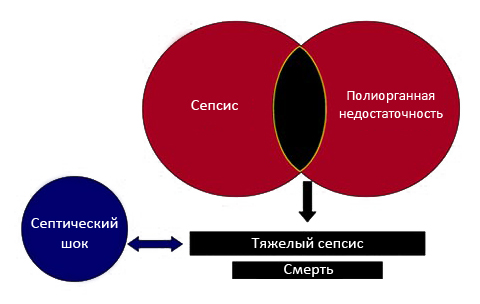
Сепсис – опасная для жизни дисфункция органов, вызванная нерегулируемой реакцией организма человека на инфекцию [29,30].
Септический шок – разновидность сепсиса с циркуляторной и клеточной/метаболической дисфункцией, связанной с более высоким риском смертности [29,30].
Примечание: Использовавшийся ранее термин «тяжелый сепсис» исключен из современных клинических руководств, вследствие трудности его клинической идентификации и отсутствии разницы в лечении с септическим шоком. Однако данный термин продолжает использоваться в текущем варианте МКБ-10 ВОЗ для статистических целей в странах, пока не принявших современные клинические рекомендации.
ВВОДНАЯ ЧАСТЬ
Название протокола: Сепсис
Код(ы) МКБ-10:
| Код | Название |
| А02.1 | Сальмонеллезный сепсис |
| А22.7 | Сибиреязвенный сепсис |
| А24.1 | Мелиоидозный сепсис (септицимия) |
| А40 | Стрептококковая септицемия |
| А41 | Другая септицемия |
| А48.3 | Синдром токсического шока |
| А49.9 | Бактериальная инфекция неуточненная (бактериемия) |
| А54.8 | Гонококковый сепсис |
| В00.7 | Сепсис, вызванный вирусом герпеса |
| B37.7 | Кандидозная септицемия |
| R65.1 | CCВО инфекционного происхождения с органной дисфункцией |
| R65.20 | Тяжелый сепсис без септического шока (рекомендуемый первичный код предварительного диагноза) |
| R65.21 | Тяжелый сепсис с септическим шоком (рекомендуемый первичный код предварительного диагноза) |
| Т81.1 | Эндотоксический шок, развившийся вследствие хирургических процедур не классифицированный в других рубриках |
| Т88.0 | Сепсис вследствие иммунизации |
| R57.8 | Другие виды шока. Эндотоксический шок неуточненный |
Дата разработки/пересмотра протокола: 2015 год (пересмотр 2020 г.)
Пользователи протокола: врачи стационаров и поликлиник, врачи и фельдшеры СП, врачи лечебно-оздоровительных комплексов, врачи ОРИТ.
Категория пациентов: взрослые.
Шкала уровня доказательности:
Обозначение уровня рекомендации:
Рекомендациям присваивается 1 уровень, если на основе текущих данных, эксперты убеждены в том, что в случае их применения польза для пациента будет перевешивать потенциальный риск. Рекомендациям присваивается 2 уровень в случае отсутствия конкретных данных по соотношению пользы и риска.
Обозначение уровня доказательств:
Соответствие уровня доказательности и степени рекомендаций клинических методов диагностики и лечения объему и характеру проведенных научных исследований и обзоров представлено в таблице 1.
Таблица 1. Соотнесение уровня доказательности методов диагностики и лечения сепсиса и септического шока объему и характеру проведенных научных исследований и обзоров, имеющих соответствующий уровень доказательности
| Классификация силы рекомендаций | |
| Уровень доказательности | Описание |
| I | Доказательства, полученные, по крайней мере, изодного качественного рандомизированного контролируемого испытания. |
| II-1 | Доказательства, полученные, из хорошо спланированного контролируемого исследования без рандомизации. |
| II-2 | Доказательства, полученные, из хорошо спланированного когортного исследования или исследования типа «случай — контроль», одно- или многоцентрового. |
| II-3 | Доказательства, полученные из нескольких серий случаев с наличием вмешательства и без вмешательства. |
| Степень рекомендаций | |
| Класс А | требует по крайней мере одного мета-анализа, систематического обзора или РКИ, или доказательства расценены как хорошие и непосредственно применимые для целевой популяции. |
| Класс В | требует доказательств, полученных из хорошо проведенных клинических испытаний, непосредственно применимых для целевой популяции и демонстрирует полную согласованность результатов; или доказательства экстраполированы из мета-анализа, систематического обзора и РКИ. |
| Класс С | требует доказательств, полученных из отчетов экспертных комиссий, или мнений и/или клинического опыта авторитетных лиц, указывает на недостаток клинических исследований хорошего качества. |
| Класс D | экспертное мнение без критической оценки, или основанное на клиническом опыте или лабораторных исследованиях. |
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация сепсиса
По характеру первичного очага: раневой, послеродовый, посттравматический, ожоговый, сепсис при заболеваниях внутренних органов;
По локализации первичного очага/генерализации инфекции: тонзилогенный, одонтогенный, риноотогенный, уросепсис, кардиогенный, гинекологический, абдоминальный, ангиогенный;
По клиническому течению: молниеносный (1-2 суток), острый (5-10 суток без ремиссии), подострый (2-12 недель), хронический, рецидивирующий сепсис (более 3-х месяцев);
По наличию или отсутствию первичного очага: первичный (очаг отсутствует) и вторичный (есть первичный очаг или входные ворота);
По особенностям развития клинической картины:ранний (до 3-х недель от внедрения инфекции) и поздний (позже 3-х недель от момента внедрения инфекции);
По виду и характеру возбудителя: аэробный сепсис, анаэробный, смешанный, грибковый, вирусный;
По характеру генерализации инфекции: септицемия, септикопиемия (образование метастатических, вторичных абсцессов (очагов инфекции) в различных органах и тканях);
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Жалобы и анамнез: Жалобы, связанные с наличием первичного воспалительного (инфекционного) очага (боль, дискомфорт, дисфункция в причинном органе, ткани) + неспецифические жалобы, связанные с интоксикацией, ССВО.
Общие (неспецифические) жалобы и симптомы:
- слабость, миалгия, недомогание, упадок сил, пассивное поведение;
- повышение температуры тела (жар, озноб, потливость).
Жалобы и симптомы в зависимости от вовлеченных органов:
- кашель, одышка, боли в грудной клетке;
- сердцебиение, аритмия;
- тошнота, рвота, потеря аппетита, желтушность кожи и слизистых, сухость во рту; боль в животе, вздутие живота, задержка стула;
- головные боли, эйфория, возбуждение, бред, заторможенность, нарушение сознания вплоть до комы;
- боль в пояснице, отсутствие или малый объем мочи (диурез менее 0,5 мл/кг/час более 2-х часов подряд);
- кровоизлияние под кожей, кровоточивость десен, носовое кровотечение.
Особенности течения сепсиса
Симптомы и признаки сепсиса могут быть малозаметными и, часто органная дисфункция, в случае его развития, нередко принимается за проявления других заболеваний (например, алкогольный делирий, заболевание сердца, эмболия легочной артерии), особенно у послеоперационных больных. У пациентов с сепсисом, как правило, отмечаются: лихорадка, тахикардия, обильное потоотделение и тахипноэ. Также должны присутствовать другие локальные признаки инфекции, являющиеся причиной сепсиса. По мере ухудшения состояния больного с сепсисом или при развитии септического шока ранним симптомом, особенно у пожилых людей может быть спутанность сознания или снижение активности. АД снижается, однако кожа остается парадоксально теплой. На поздних стадиях конечности становятся прохладными и бледными с периферическим цианозом. Дисфункция органов приводит к появлению дополнительных симптомов и признаков в зависимости от пораженного органа (например, олигурия, одышка и т.д.).
Анамнез:
• наличие предсуществующего воспалительного или гнойного заболевания/процесса в анамнезе.
Физикальное обследование:
Общий осмотр кожных покровов и слизистых:
- горячие кожные покровы;
- бледность, мраморность кожи;
- гиперемия лица, акроцианоз;
- желтушность склер и кожных покровов;
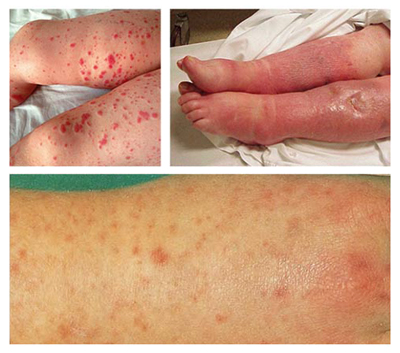
- геморрагическая сыпь (от точечных петехий до сливных экхимозов и крупных геморрагических и некротических очагов, появляется в ранние сроки, локализуется на передней поверхности грудной клетки, на животе и руках) при коагуолопатии и тромбоцитопении;
- увеличение размеров локальных лимфоузлов, полилимфоаденопатия.
Оценка состояния дыхания:
- тахипноэ, диспноэ, одышка смешанного характера;
- изменение перкуторной картины: над участками уплотнения легочной ткани, скопления жидкости в плевральной полости обнаруживается укорочение/притупление перкуторного звука;
- изменение голосового дрожания: его ослабление над участками с плевральным выпотом, усиление над участками консолидации/инфильтрации легочной ткани;
- изменение аускультативной картины над легкими:
— ослабленное, жесткое дыхание, бронхиальное дыхание;
— появление влажных хрипов и крепитации над пневмоническими участками.
Клиническое исследование сердца (аускультация и перкуссия сердца, исследование пульса и верхушечного толчка и пр.):
- ослабление звучности тонов сердца;
- тахикардия, тахиаритмия;
- расширение границ относительной тупости сердца (при развитии миокардита).
Исследование живота:
обратить внимание на наличие перитонеальных симптомов (выявление первичного инфекционного очага) и признаков внутриабдоминальной компрессии (ВАБК), как фактора, влияющего на дыхательный, гемодинамический статус, выделительную функцию почек и спланхнический кровоток (в органах брюшной полости);
— для сепсиса характерны спленомегалия и гепатомегалия;
— вздутие живота (тимпанит), ослабление или отсутствие перистальтики кишечника, гастростаз.
Лабораторные исследования:
Общий анализ крови: лейкоцитоз/лейкопения (>12х109 или <4х109 или количество незрелых форм превышает 10%), токсическая зернистость нейтрофилов, нейтрофилия, лимфопения (<1,2х109), повышенное СОЭ, повышение ЛИИ, снижение Hb, эритроцитов, Ht, тромбоцитопения (<100х109).
Биохимический анализ крови: повышение билирубина выше 20 мкмоль/л; повышение уровня трансаминаз (АЛТ, АСТ >2 норм); повышение креатинина в 1,5 раза или его прирост на 44 мкмоль/л за сутки (у пациентов с исходной гиперкреатининемией (ХПН)); снижение СКФ на 50% и более за сутки, повышение мочевины на 5,0 ммоль/л за сутки; снижение общего белка <60 г/л, альбумина < 35 г/л.
Коагулограмма: (+)продукты деградации фибриногена, (+)Д-димеры, ПТИ <70% или МНО>1,5; фибриноген <1,5 г/л, удлинение АЧТВ> 60 сек, тромбоцитопения <100
Кислотно-основное состояния крови: рН <7,35; дефицит оснований ≥5 ммоль/л, повышение уровня лактата крови >2 ммоль/л, РаО2 менее 60мм рт.ст., РаСО2 <35 или > 45 мм рт.ст.
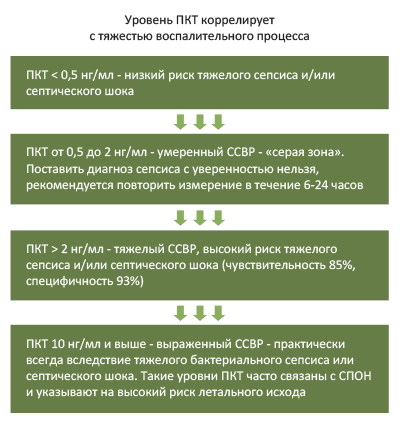
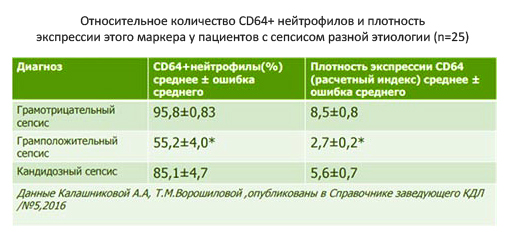
Биомаркеры сепсиса: повышение прокальцитонина, С-реактивного белка, пресепсина в 2 раза и более от референсных значений [29,30].
— Забор анализов, включая биосреды на микробиологическое исследование, при подозрении на сепсис рекомендуется производить после установки диагноза сепсис, в частности, до начала антибактериальной терапии[19, 24, 29], (Приложение 2 [30]). Однако допускается первоочередное введение противомикробных препаратов в пользу потенциального эффекта для пациента, если невозможно быстро получить биосреды на микробиологическое исследование (Приложение 2 [30]).
Лабораторные изменения могут быть разнообразными и свидетельствовать о наличии:
- печеночной недостаточности (гипоальбуминемия, увеличение МНО>1,5 раза);
- цитолизе клеток печени (повышение трансаминаз более чем в 2 раза);
- холестазе (увеличение щелочной фосфатазы);
- остром повреждении почек (повышение уровня креатинина и мочевины, снижение СКФ, декомпенсированный метаболический ацидоз);
- острой надпочечниковой недостаточности (гипонатриемия, гиперкалиемия, гипогликемия);
- развитии миокардита (повышение уровня тропонина);
- коагулопатии (дефицит факторов свертывающей и/или противосвертывающей систем, тромбоцитоз или тромбоцитопения, тромбоцитопатия);
- метаболическом и/или дыхательном ацидозе и компенсаторных реакциях;
- развитии ОРДС (уменьшение соотношения РаО2/FiO2 или SpO2/FiO2);
- реакции на инфекционное воспаление со стороны системы крови (лимфоцитоз или лимфопения, анемия, гемоконцентрация, тромбоцитопения).
Инструментальные обследования:
- Рентгенография органов грудной клетки – скопление жидкости в плевральных полостях, наличие инфильтратов в ткани легких, признаки отека легких характерны для плевропневмонии/ОРДС. Для ОРДС характерны билатеральные инфильтраты; расширение границ сердца может быть проявлением заболевания сердца (миокардит, СН).
- ЭКГ — нарушение ритма, сердечной проводимости, признаки миокардита; Исключить ОКС, индуцированные аритмией кардиогенные нарушения гемодинамики и дыхания.
- УЗИ органов брюшной полости – исследовать на наличие свободной жидкости, гепато-, спленомегалии, обструкции желчных протоков, гепатозов; панкреатита; поиск первичного или вторичного очага инфекции.
- УЗИ почек и забрюшинного пространства – увеличение размеров почек, признаки нефрита, острого повреждения почек; аномальный кровоток в почечной артерии, оценка корковых/мозговых структур, исследование на предмет нарушения оттока мочи; исследование паранефральной клетчатки, в рамках поиска потенциальных источников очаговой инфекции.
- Эхокардиография/эхокардиоскопия – исследовать на наличие структурной патологии сердца для дифференциальной диагностики с сердечными заболеваниями.В поздних стадиях септического шока гипердинамический тип кровообращения сменяется на гипокинетический вследствие прогрессирования шока и/или развития вторичного повреждения миокарда.
- Компьютерная томография легких — исследуйте на наличие ТЭЛА, пневмонии или ОРДС. Для ОРДС характерно сосуществование относительно хорошо аэрированных участков в вентральных отделах и картина «матового стекла» и плотные очаги консолидации легочной ткани в дорсальных (вентро-дорсальный градиент легочной плотности).
- Инвазивное или неинвазивное определение сердечного выброса (опционально). Неинвазивные методы – реография, метод EsCCO (мониторинг минутного сердечного выброса на основе ЭКГ, периферической сатурации и артериального давления).
Показания для инвазивного мониторинга сердечного выброса (СВ) и условия его использования: Измерение и мониторинг отдельных компонентов СВ требуется при СШ с неуправляемой гемодинамикой, когда требуется более точное и избирательное воздействие на отдельные гемодинамические компоненты (инфузия, вазопрессоры или инотропы) и/или когда риск объемной инфузии крайне опасен (отек мозга, ОРДС) и т.д.
Стандартный мониторинг при септическом шоке включает мониторинг лактатаартериальной крови, газов крови и КОС, оценка вариабельности контура пульсовой волны и пр.), центральной венозной линии (ЦВД, ScvO2, PvCO2) и ЭхоКГ (УО, КДО, клапаны, акинез стенок, ДЛА).
Мониторинг при септическом шоке [13, 27, 28,30]:
Измерение лактата сыворотки крови и забор крови на микробиологическое исследование должны быть выполнены в течение 1,5 часа момента установления предварительного диагноза «Сепсис» до начала терапии. При показателях лактата выше 2 ммоль/л анализ должен быть повторен через 2 часа, уже на фоне проводимой терапии, для оценки ответа на лечение.
Невозможность выполнить микробиологический посев крови (на аэробы/анаэробы/грибы), а также применить вирусологические, иммунологические методыобследования в течение одного часа не должна служить поводом для отсрочки начала антибактериальной терапии,невозможность выполнить измерение лактатаплазмы крови не должна препятствовать скорейшему началу инфузионной терапии. Прочие лабораторные тесты могут быть выполнены либо одновременно, либо в течение последующих 3-6 часов.
Правила забора крови на микробиологический посев, грибы и анаэробы:
Кровь для исследования необходимо забирать до назначения антибиотиков.
Необходимым минимумом забора являются 2 пробы, взятые из вен разных верхних конечностей с интервалом 30 мин. Оптимальным считается забор 3-х проб крови. Забор крови на высоте лихорадки не повышает чувствительности метода (УД – С).
Кровь для исследования необходимо забирать только из периферической вены.
Оптимальным является использование стандартных коммерческих флаконов с готовыми питательными средами.
Забор крови из периферической вены следует проводить с тщательным соблюдением асептики. Кожу в месте венепункции обрабатывают раствором йода или повидон-йода концентрическими движениями от центра к периферии в течение как минимум минуты. Непосредственно перед забором кожу обрабатывают 70% спиртом. При проведении венепункции используют стерильные перчатки. Крышку флакона со средой обрабатывают спиртом. Для каждой пробы забирают 10 мл крови.
Диагностические критерии постановки диагноза сепсис:
Диагностические критерии сепсиса [29,30].
В соответствии с текущими международными рекомендациями диагноз «Сепсис» устанавливается, если имеется подозреваемая или документированная инфекция в сочетании с остро возникшей органной дисфункцией, о развитии которой заключают по индексу шкалы SOFA (Приложение 1) на 2 балла и более от базового значения[26,29,30]. Исходный балл SOFA можно предположить равным нулю у пациентов, у которых ранее не было выявленной дисфункции органов.
Предварительный диагноз на догоспитальном этапе или вне отделения интенсивной терапии может быть выставлен по шкале q-SOFA (шкала для быстрой диагностики) [25,26,29,30] (Приложение 3), однако затем должен быть подтвержден по полноценной шкале SOFA и другим клиническим и лабораторным данным.
Согласно шкале q-SOFA диагноз «Сепсис» может быть предварительно выставлен, если присутствуют любые два из трех приведенных ниже симптомов:
- Частота дыхания более 22 в минуту
- Изменения ментального статуса (оценка по шкале Глазго 13 баллов и меньше).
- Артериальная гипотензия АДсистолическое менее 100 мм рт. ст.
Шкала q-SOFA не отменяет использования ССВО в определении сепсиса.
Показатель qSOFA≥2 может свидетельствовать о сепсисе [29,30], так как данная шкала является инструментом, позволяющим с достаточной долей вероятности предположить диагноз сепсис или ССВО при наличии очага инфекции [25].
Пациенты с септическим шоком могут быть клинически идентифицированы,как требующие применения вазопрессора для поддержания АДср. = 65 мм рт.ст. или выше, при отсутствии гиповолемии (или при адекватной инфузии) и имеющие уровень лактата в сыворотке более 2 ммоль/л.
Примечание: Изменения в определении термина «Сепсис» и критериев диагностики сепсиса связаны с тем, что статистически у пациентов с сепсисом не всегда присутствуют признаки ССВО (в 12,5%). Также подчеркивается необходимость в переносе акцента в текущем понимании термина «Сепсис» с воспаления на гипоперфузию, что очень важно клинически. Однако у большей части пациентов (87,5%) с сепсисом могут присутствовать признаки ССВО, что сохраняет диагностическую ценность признаков ССВО[29].
Признаки синдрома системного воспалительного ответа (ССВО):
Общие изменения:
- лихорадка (температура тела >38.3°C);
- гипотермия (температура тела <36°C);
- ЧСС более 90 в мин или больше;
- тахипноэ > 20/мин или РаСО2< 32 мм рт.ст.;
- нарушения сознания (менее 15 баллов по ШКГ);
- видимые отеки или положительный водный баланс (задержка жидкости) более 20 мл/кг/сутки;
- гипергликемия (глюкоза плазмы >7,7 ммоль/л) при отсутствии сахарного диабета.
Воспалительные изменения:
- лейкоцитоз (>12* 109/л) или лейкопения (<4* 109/л);
- нормальное число лейкоцитов при наличии 10% незрелых форм;
- С — реактивный белок более 2 стандартных отклонений выше нормальной величины;
- прокальцитонин плазмы более 2 стандартных отклонений выше нормальной величины
- пресепсин≥300 пг/мл [13,19,34];
Нарушения гемодинамики:
•
ЧСС более 90 в мин или больше,артериальная гипотензия (САД<90 ммрт. ст., АДcр< 70 мм рт.ст.или снижение САД> 40 мм рт. ст. или менее двух стандартных отклонений ниже привычных возрастных значений [14].
Нарушения органных функций:
Дыхательная система — тахипноэ > 20/мин, индекс оксигенации (PaO2/FiO2<300или SpO2/FiO2 < 250);
- наличие инфильтратов на рентгенограмме или необходимость проведения ИВЛ.
Почки
— острая олигурия (темп диуреза < 0.5 мл/кг/час в течение не менее 2 часов, несмотря на адекватную регидратацию; повышение креатинина > 176 мкмоль/л; или прирост более 44 мкмоль/л/сут (у пациентов с ХПН).
- Коагулопатия (МНО>1.5 или АЧТВ> 60 сек); учитывать гепаринотерапию и прием антикоагулянтов некоторыми пациентами!
- Тромбоцитопения (<100*109/л).
- Парез кишечника — ослабление перистальтики; вздутие живота, гастростаз (рвота, желудочное/кишечное отделяемое по зонду, сброс по зонду вводимых жидкостей).
- Гипербилирубинемия> 20 мкмоль/л.
- Нарушения тканевой перфузии: повышение лактата (>2ммоль/л); необходимо учитывать нагрузку лактатом (ЗПТ с использованием лактатного буфера, инфузияРингер-лактата, введение адреналина), нарушение элиминации лактата при печеночной дисфункции.
- Признаки нарушения микроциркуляции: бледность, мраморность кожных покровов, синдром «белого пятна» (при сдавлении ногтевого ложа наполнение задерживается на 3 сек и более).
Дополнительная оценка нарушения тканевого кровотока: (сублингвальная микроскопия капиллярного кровотока; лазерная допплерометрия: кровоток в капиллярах; ближняя инфракрасная спектроскопия; тканевая оксигенация;рСО2 слизистой оболочки желудка (оценка спланхнического кровотока); скорость эритроцитов или кровоток в капиллярах кожи. Данные исследования — при наличии технической возможности.
Примечание: Общая тяжесть состояния определяется по шкале APACHEII (AcutePhysiologyAndChronicHealthEvaluation) (Приложение 2).
Показания для консультации специалистов:
- консультация инфекциониста — при наличии вирусных гепатитов, зоонозных и других инфекций;
- консультация клинического фармаколога – для рационального использования лекарственных средств и оценки их взаимодействия;
- консультация хирурга — при наличии хирургических заболеваний, являющихся источником сепсиса или септического шока;
- консультация травматолога — при наличии травмы;
- консультация терапевта — при наличии заболеваний терапевтического профиля;
- консультация кардиолога — при наличии нарушений со стороны ЭКГ, патологии сердца;
- консультация невропатолога — при наличии неврологической симптоматики;
- консультация гематолога — в случае тромбоцитопении, лейкопении и прочих тромбоцитопатий для исключения болезней крови и аутоиммунных гемолитических анемий, гемолитико-уремического синдрома (ГУС) и пр.;
- консультация акушер-гинеколога — при наличии беременности/при выявлении патологии репродуктивных органов;
- консультация гастроэнтеролога — при наличии патологии желудочно-кишечного тракта;
- консультация ревматолога — при появлении симптомов системного заболевания;
- консультация оториноларинголога — при выявлении очага инфекции с последующей санацией;
- консультация стоматолога — при выявлении очагов инфекции с последующей санацией.
Диагностический алгоритм при вынесении диагноза Сепсиса и септического шока [29,30]: Приложение 4.
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований:
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза септического шока |
| Анафилактический шок |
Развитие шока/гипотензии, ПОН |
Общий анализ крови (повышенный уровень иммуноглобулинов E, эозинофилов, триптаза тучных клеток, гистамин сыворотки крови, (повышение) |
Внезапная гипотензия на фоне полного здоровья, сопровождается другими аллергическими проявлениями (эритема, крапивница, зуд, отек и пр.), спец. лабораторными признаками. Связь развития шока с повторным введением лекарственного средства, поступлением в организм аллергена (ужаление, вдыхание паров различных веществ,прием пищевых продуктов), появление уртикароподобной сыпи, бронхоспазма, отсутствие активного очага инфекции |
| Гиповолемический шок | Наличие артериальной гипотензии, тахикардии, признаков нарушения микроциркуляции, олигурии |
АД, ЧСС, ЭхоКГ, динамические и статические тесты надля выявления эффективной ответной реакции организма к инфузонной терапии, электролиты и осмолярность плазмы. Общий анализ крови |
Наличие клинических признаков дегидратации, обусловленных причинным фактором (рвота, диарея, полиурия, алиментарное ограничение объема жидкости, парез кишечника), нередко гипотермия |
| Системные васкулиты | Наличие лихорадки, геморрагической сыпи, полинейропатии |
Общий анализ крови: Непрямая реакция иммунофлюоресценции: антинейтрофильные цитоплазматические антитела (АНЦА), антитела к цитоплазме нейтрофилов (ANCA) Ангиография: поражение сосудов малого и среднего диаметра |
Наличие, как правило, артериальной гипертензии. Преимущественное поражение кожи, опорно-двигательного аппарат (боли в суставах, мышцах). Отсутствие очага инфекции, отр. маркеры сепсиса |
| Синдром токсического шока (СТШ) | Наличие признаков ССВО тяжелой степени |
Общий анализ крови, биохимический анализ крови, коагулограмма, общий анализ мочи, кислотно-щелочное состояние крови. Рентгенография органов грудной клетки, УЗИ органов брюшной полости, ЭКГ, Бак.исследование крови |
Наличие продромального периода (до 24 часов) в виде недомогания, полиморфной кожной сыпи, диареи, озноба. Характерный контингент пациентов: наличие менструации, ранний послеродовый период, ожоги. Микробиологическоеопределение в крови/очаге – стрептококка или стафилококка, продуцирующих токсин |
| Кардиогенный шок | Развитие артериальной гипотензии с полиорганной дисфункцией (сердечная дисфункция, одышка, снижение диуреза, энцефалопатия, гепатомегалия и пр.) |
ЭКГ, тропониновый тест, Рентгенография органов грудной клетки; ЭХОКГ, Коронароангиография |
Нарушение ритма, ангинозный синдром, ишемические изменения на ЭКГ, положительныйтропонин; коронароангиография – значимое поражение коронарного русла, ЭХОКГ — гипо-, акинезия различных участков миокарда; отсутствие гипертермии, очага инфекции, лабораторных признаков инфекции; |
|
Обструктивный шок (ТЭЛА, тампонада сердца,гидроперикард, напряженный пневмоторакс, тромбы в полостях сердца) |
Наличие быстро развивающейся артериальной гипотензии, нарушений ритма и проводимости сердца, нарушения дыхания |
Общий анализ крови, биохимический анализ крови. Для исключения ТЭЛА: D-димеры крови, тропониновый тест, Рентгенография органов грудной клетки. КТ грудной клетки ЭКГ. |
ТЭЛА – резкое начало в виде артериальной гипотензии, тахипноэ, болей в области сердца, изменения на ЭХОКГ- резкое увеличение давление в правых отделах сердца, характерные изменения на ЭКГ, при рентгенографии органов грудной клетки, томографии грудной клетки. Предпосылки ТГВ
|
Дифференциальная диагностика:
Исходя из определения сепсиса и септического шока и их патофизиологии, сепсис следует дифференцировать:
- С любыми инфекциями без признаков сепсиса, т.е. без органной недостаточности и гипоперфузии органов и тканей.
- С синдромом ССВО, вызванным неинфекционными повреждающими факторами.
- С шоками любой другой этиологии: анафилактическим, кардиогенным, гиповолемическим, обструктивным.
- С любыми состояниями, вызывающими острую гипотензию и/или периферическую вазодилятацию (острые отравления, острый панкреатит, острая надпочечниковая недостаточность и др.).
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Организация помощи на амбулаторном этапе (скорая медицинская помощь, поликлиника) должна быть направлена на выявление пациентов с предположительным диагнозом сепсис и/или септический/шок (шкала q-SOFA) и быстрейшую доставку данного пациента в стационар.
Немедикаментозное лечение: начало оксигенотерапии [12] через носовые канюли (1-6 л/мин) или лицевую маску 5-10 л/мин [9], неинвазивная/инвазивная респираторная поддержка, проведение базовой сердечно-легочной реанимации при развитии клинической смерти.
Медикаментозное лечение: смотрите приложение 5 к настоящему протоколу.
Хирургическое вмешательство: нет.
Дальнейшее ведение: на стационарном уровне.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе:
Временные критерии:
- начало инфузионной терапии кристаллоидными растворами от момента диагностики септического шока (УД – IА, SSC 2016) при необходимости с возможным применением вазопрессоров (Приложение 5);
- стабилизация уровня АД (увеличение АДср выше 65 мм рт.ст.);
- достижение пульсоксиметрической сатурации крови> 90%[15].
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Цели лечения:
- раннее определение/выявление и санация источника генерализации инфекции – в течение не более 6-12 часов (целевое время – 6 часов и ранее) после постановки диагноза [30], в идеале должно быть осуществлено, как можно скорее [30];
- ранняя и рациональная антимикробная терапия (эмпирическая АМТ, скорейшая идентификация возбудителя и деэскалация, эрадикация инфекции, предупреждение ре-, суперинфекции);
- поддержание, протезирование и контроль нарушенных витальных функций (седация, поддержание гемодинамики, респираторная поддержка, доставка кислорода в ткани, метаболические нарушения, ЗПТ, коррекция коагулопатии, профилактика и/или коррекция синдрома ВАБК);
- общее лечение (профилактика ТЭО, нутритивная поддержка, профилактика пролежней, профилактика острых язв, симптоматическое лечение);
- контроль метаболизма и нормализация метаболических констант (гликемия, рН крови, лактата крови, сатурация центральной венозной крови, осмолярность, электролиты плазмы крови);
- профилактика осложнений (терминальной недостаточности органов и систем, ре – и суперинфекции).
Начальная интенсивная терапия сепсиса
- Поддержание целевого АДср 65-75 мм рт.ст. Поддержание АДср более 75 мм рт.ст. с помощью вазопрессоров/инотропов не целесообразно, т.к. повышает риск аритмий. Поддержание АДср на уровне 75-85 мм рт.ст. оправдано только у больных с сопутствующей АГ, т.к. уменьшает выраженность острого повреждения почек и у больных с цереброваскулярной болезнью, для которых привычные цифры АД выше нормальных значений.
- Раннее начало инфузионной терапии: начало в течение первого часа (в объеме 30 мл/кг в течение 3 часов от момента постановки диагноза «сепсис») – снижает летальность [13,23].
- Лактат является хорошим маркером тканевой гипоперфузии. Быстрая нормализация лактата (снижение на 20% и более за 12 часов)– признак хорошего ответа на лечение (SSC 2016). Гиперлактатемия может быть вызвана не только тканевой гипоперфузией, но и введением адреналина, лактатсодержащих сред, печеночной дисфункцией. Лактат более 8 ммоль/л однозначно связан с тканевой гипоперфузией и ассоциирован с неблагоприятным прогнозом.
- При неэффективности инфузионной терапии – своевременное подключение вазопрессоров снижает летальность [32]. При жизнеугрожающей гипотензии краткосрочное введение вазопрессоров может потребоваться еще до достижения целевых показателей преднагрузки с помощью инфузии.
- Положительныйгидробаланс с 3-х сутот диагностики сепсиса ассоциируется с неблагоприятным исходом [23].
Карта наблюдения пациента, маршрутизация пациента: смотрите приложение 6 к настоящему протоколу.
Немедикаментозное лечение
Выбор способа питания:
- естественное пероральное питание — преимущественно;
- зондовое питание (через зонд назогастральный или назоинтестинальный) при невозможности самостоятельного питания(дисфункция нервной системы, нарушения глотания,кашля, травмы, последствия хирургических вмешательств, ИВЛ и пр.). Рекомендуется раннее энтеральное питание (ЭП) – подключается в течение 24-48 часов от установки диагноза после стабилизации гемодинамики;
- парентеральное питание (внутривенное введение питательных средств) — при невозможности или недостаточности перорального или зондового питания. Противопоказания для энтерального/зондового питания:
- механическая кишечная непроходимость;
- продолжающееся желудочно-кишечное кровотечение;
- нестабильная гемодинамика.
Противопоказания (показание для ограничения) энтерального,зондового/парентерального питания:
• неустраняемая гипоксемия на фоне ОРДС.
Примечание:
Дотация калорий в первые 7 дней с момента постановки диагноза может составлять 500 ккал/сут (10-20 ккал/час), так называемое трофическое (гипокалорийное) питание (ТП). При переносимости ТП дотацию калорий можно расширить до 70-80% от суточной нормы (УД – 2В). Для пациентов с избыточной массой тела расчеты питания производятся исходя из идеальной массы тела.
Идеальная масса тела: для муж 50,0 + 0,91 (рост(см) – 152,4)
для жен 45,5 +0,9 1(рост (см) — 152,4)
При стойком гастропарезе, непереносимости зондового кормления (рвота, вздутие живота или большом остаточном объеме желудочного содержимого), которые приводят к прерыванию энтерального питания, рекомендуется использование постпилорических зондов для питания.
Парентеральное питание (ПП): Современные данные не подтверждают пользу от раннего парентерального питания в течение первых 7 дней ухода за пациентами с противопоказаниями или непереносимостью энтерального питания, т.к. раннее парентеральное питание в комбинации или без энтерального питания не было связано со снижением смертности (УД – IIА) [29,30].
Подключение ПП рекомендуется в постепенно нарастающем объеме с соблюдением предписанной скорости в/в введения питательных субстратов (аминокислоты и липиды не более 0,1 г/кг/час; глюкоза не более 0,5 г/кг/час от ИМТ). Карнитин, глютамин, аргинин, иммунное питание, селен, омега-3 ЖК – не рекомендуются для ПП при сепсисе (SSC 2016).
Противопоказания к ПП:
— возможность орального или энтерального питания до 70% от сут нормы (расчет от ИМТ);
— нестабильное клиническое состояние (шок, гипоксемия, гиперкапния, рН ниже 7,2; осмолярность плазмы более 330 мосм/л; выраженные нарушения водного баланса (дегидратация/гипергидратация)) [29,30].
Искусственная вентиляция легких [2,6,24,29,30]:
Показания к переводу на ИВЛ:
- нарушение сознания (менее 8 баллов по шкале Глазго) и другие признаки энцефалопатии, требующей седации;
- тяжелое утомление мышц, слабость дыхательной мускулатуры, участие в дыхании вспомогательной дыхательной мускулатуры
- тахипное более 35 в минуту;
- устойчивое снижение SpO2 ниже 90%;
- РаО2 ниже 55 мм рт.ст.;
- РаСО2> 55 мм рт.ст. или < 25 мм рт.ст.;
Общие принципы ИВЛ при сепсисе:
- ИВЛ показана больным с острым респираторным дистресс-синдромом (ОРДС), вызванным сепсисом, нарушениями вентиляционной функции легких, септическом шоке, сопровождающихся показаниями к ИВЛ. Тяжесть ОРДС и динамика состояния легких определяется по индексу оксигенации — РаО2/FiO2: легкий – 200-300, среднетяжелый – 100-200 и тяжелый — <100 (УД – IА) [24,29,30];
- возможно начало респираторной поддержки у пациентов с ОРДС при помощи неинвазивной вентиляции при сохранении сознания, контакта с пациентом, индексе рaO2/FiO2 более 175 мм рт. ст., стабильной гемодинамике [2] только под тщательным контролем дыхательных объемов [30]. При неэффективности неинвазивной вентиляции – гипоксемии, метаболическом ацидозе или отсутствии увеличения индекса PaO2/FiO2 в течение 2 ч, высокой работе дыхания (десинхронизация с респиратором, участие вспомогательных мышц, «провалы» во время триггирования вдоха на кривой давление – время), показана интубация трахеи [2];
- необходимо соблюдать принципы протективной (защитной)и адекватной вентиляции. При этом могут быть использованы как режимы, регулируемые по давлению, так и по объему (SSC 2016);
- более высокий уровень PEEP улучшает исходы при среднетяжелом и тяжелом ОРДС;
- необходимо избегать больших ДО и высоких давлений пиковых и плато. В случае если для достижения ДО 6мл/кг требуется давление плато/пиковое выше регламентированного, то следует уменьшить ДО до 4 мл/кг. Если достигнуты предельные значения ДО и МВЛ, допустимы умеренная гипоксемия/гиперкапния если нет внутричерепной гипертензии, рН крови находится в пределах выше 7,15.
При невозможности использовать тактику допустимой гипоксемии/гиперкапнии при рефрактерной гипоксемии – использовать режим APRV или ЭКМО (SSC 2016).
Рекомендуется использование прон-позиции при РаО2/FiO ниже 150 при отсутствии противопоказаний к положению на животе.(SSC 2016).
Рекомендуется использование миорелаксантов (до 48ч) при РаО2/FiO ниже 150 для снижения опасного уровня пикового давления вдоха и синхронизации с ИВЛ аппаратом (SSC 2016).
Головной конец кровати должен быть поднят на 30-45 градусов (если нет противопоказаний (низкое АД, нарушенный церебральный кровоток, травма позвоночника)) для профилактики аспирации желудочного содержимого и ВАП (SSC 2016)
«Концепция открытых легких» – проведениерекрутмента альвеол, выбор «оптимального РЕЕР», избегатьдерекрутмента: после рекрутмент-маневра необходимо поддерживать раскрытыми альвеолы как можно дольше (исключить утечки из контура, избегать «лишних» дисконнекций контура), т.к. частый рекрутмент-дерекрутмент также является фактором повреждения легких (ателектотравма). После любого вынужденного рассоединения дыхательного контура необходимо повторное проведение рекрутмента.
Способы профилактики дерекрутмента: использование закрытых аспирационных систем, тепло-влагообменных фильтров вместо активного увлажнителя (для уменьшения конденсации жидкости в контур) или использование специальнныхвлагосборников, позволяющих сливать конденсат без разгерметизации дыхательного контура (при использовании активного увлажнения).
Рекомендуется использовать протокол отлучения пациентов на ИВЛ с сепсис-индуцированной дыхательной недостаточностью, которые готовы к отлучению (УД – 1С) (SSC 2016)
Для верификации диагноза ОРДС можно использовать следующие критерии:
- Быстрое развитие синдрома (в течение пяти-семи дней от момента воздействия причинного фактора на легкие).
- Двусторонние инфильтраты на рентгенограмме ОГК, которые нельзя объяснить плевральным выпотом, ателектазами.
- Исключен гемодинамический механизм отека легких или перегрузка жидкостью (при необходимости – провести ЭхоКГ для исключения ЛЖ недостаточности).
- Нарушение оксигенации (PaO2/FiO2 ≤ 300 или SpO2/FiO2 ≤ 250).
Задачи респираторной поддержки при ОРДС:
— оптимизация газообмена.
— уменьшение работы дыхания.
— снижение системного потребления О2.
— предотвращение волюмо-, баро-, био- и ателектотравмы, атрофии дыхательной мускулатуры.
- Рекомендации для настройки параметров вентиляции при сепсис-индуцированном ОРДС:
— дыхательный объем составляет 6 мл/кг (должной массы тела) (УД – 1В).
При Pплато менее 25 см вод.ст. допускается увеличение ДО до 8 мл/кг для повышения комфортности. Не более чем через 4 ч снизить ДО до 7 мл/кг, а затем до 6 мл/кг (минимум 4 мл/кг);
— Pпик– не более 35 см Н2О;
— Pплато – не более 30 см Н2О;
— скорость потока – 40-90 л/мин (у пациентов под седацией и миорелаксацией. При сохранении сознания лучше использовать режим PRVC или autoflow (автопоток) с автоматическим подбором скорости оптимального потока);
— поток – нисходящий (при использованиирежима с контролем по объему);
— целевоеFiO2 – менее 60% (если возможно), но без ущерба для оксигенации для обеспечения SpO2 88-95 или РО2 55-80 мм.рт.ст. Допускается временное превышение FiO2 вплоть до 100% для профилактики опасной гипоксемии;
— предпочтительный режим вентиляции — вентиляция по давлению с поддержкой самостоятельного дыхания (SIMV(P), BiPAP). Верхняя граница давления должна составлять < 30 см вод.ст. (УД – 1В);
- при проведении ИВЛ допустимы умеренная гиперкапния (поддержание РаСО2 в пределах не выше 80 мм рт.ст. при медленном его повышении – не более 10 мм рт.ст./час)и умеренная гипоксемия (целевые значения РаО2 55-80 мм рт.ст.) [2], чтобы удержаться в рамках безопасных значений инспираторного давления и ДО и концентрации кислородной смеси (УД – 1С);
- следует регулировать значение положительного давления на выдохе (РЕЕР) в зависимости от РаО2/FiO2 — чем ниже РаО2/FiO2, тем выше РЕЕР (от 7 до 15 см вод.ст.).
- при выборе величины РЕЕР (ПДКВ) следует учитывать потенциальную рекрутабельность легких, которую можно определить несколькими способами (изменение КТ картины, показателей механики дыхания и оксигенации, ФОЕ, электро-импедансной томографии в процессе выполнения рекрутмент-маневра).
- оптимальный РЕЕР (ПДКВ) опосредован не только максимальным количеством раскрытых альвеол, но и возможностью гемодинамики обеспечивать перфузию этих раскрытых альвеол. При определенных высоких значениях РЕЕР на фоне раскрытия альвеол может ухудшаться перфузия легочных капилляров (пережимаются избыточным давлением) в результате чего результирующая диффузионная поверхность уменьшится, т.к. в диффузии принимают участие только раскрытые и перфузируемые альвеолы.
ПоископтимальногоРЕЕР (ПДКВ) по сатурации крови:
- убывающий вариант (рекомендован в раннюю стадию ОРДС, при непрямом ОРДС, может быть более эффективен для улучшения оксигенации): – рекрутмент (40 х 40 или другой метод) – ДО=6-8 мл/кг и РЕЕР =20 см вод.ст. – ступенчатое снижение РЕЕР на 2 см вод. ст. до уровня, при котором начинает снижаться SatO2 – повторный рекрутмент – установка РЕЕР на 2 см вод. ст. выше его предыдущей величины;
- возрастающий вариант (рекомендован при нестабильной гемодинамике, в фибропролиферативной стадии, при прямом ОРДС и негомогенном повреждении легких): – ступенчатое повышение РЕЕР на 2-3 см вод.ст. до уровня, обеспечивающего оптимальную SрO2.
В среднем, общее РЕЕР при легком ОРДС – 8-12 cм вод.ст. Общее РЕЕР при умеренном и тяжелом ОРДС – 12-18 cм вод. ст.;
- применять маневр раскрытия альвеол (рекрутмент) у пациентов с трудно поддающейся лечению острой гипоксемией (УД – IIC).
Методики рекрутмент-маневра:
- пошаговая методика увеличения Рinsp (Рвд) с фиксированным РЕЕР. Целевое увеличение ДО – до 2-х расчетных ДО (10-12мл/кг);
- пошаговая методика увеличения РЕЕР с фиксированным Рinsp (только на аппаратах, на которых Рinsp отсчитывается от РЕЕР);
- постепенное параллельное увеличение РЕЕР и Рinsp;
- медленный умеренный маневр «открытия» альвеол: увеличение РЕЕР до 15 см вод.ст. с паузой 7 с – 2 раза в мин в течение 15 мин (только на аппаратах, на которых Рinsp отсчитывается от РЕЕР);
- искусственный вздох: Pплато = 45 см вод.ст. 3 раза в мин;
- увеличение Pinsp до 40 см вод.ст. в течение 40 сек: методика «40 на 40». Затем — Pinsp на уровне, обеспечивающем ДО=6-8 мл/кг.
Примечание:
— Рекрутмент-маневр проводится только в режимах вентиляции «по давлению».
— При поддержке самостоятельного дыхания рекрутмент осуществляется по любой из приведенной выше методике с изменением одновременно величины Рinsp и Рsupр (Рподдержки).
— Для повышения эффективности рекрутмент-маневра и уменьшения частоты его выполнения рекомендуется после рекрутмент-маневра как можно дольше удерживать альвеолы легких открытыми (максимально сократить эпизоды разгерметизации контура, исключить утечки из контура).
Концепция «открой легкие и держи их открытыми». Для этого используйте ЗАС (закрытые аспирационные системы), переходники с клапанами, обеспечивающие проведение санационной бронхоскопии без разгерметизации контура, дыхательные фильтры, специальные влагосборники для слива конденсата без разгерметизации контура и т.д.).
Противопоказания к проведению рекрутмент-маневра:
- пневмоторакс или высокий риск пневмоторакса (буллезные изменения в легких)
- экстраальвеолярная утечка.
- недостаточный мониторинг.
- нестабильная гемодинамика.
- гиповолемия.
Примечание:
гидроторакс, синдром ВАБК, отек легких снижают эффективность рекрутмента и склоняют к более высоким уровням РЕЕР.
Прон-позиция
Пациенты с тяжелым ОРДС могут лежать на животе (прон-позиция) (УД – IIС). При экспозиции 12-20 ч, снижении PaCO2 – лучше исход [30].
Прон-позиция противопоказана при ранах и дренажах на передней грудной и брюшной стенке, повреждении спинного мозга, переломах ребер, таза, политравме;
- пациенты, которым проводится механическая вентиляция легких, должны находиться в позиции полусидя (если это не противопоказано) (УД – 1В), головной конец кровати должен быть поднят на 30-45° (УД – IIС);
- при уменьшении тяжести ОРДС следует стремиться к переводу больного с механической вентиляции на режимы вспомогательной вентиляции легких.
Седация и миорелаксация [21,26] смотрите приложение 7 к настоящему протоколу.
Методы детоксикации: плазмообмен, ультрафильтрация, гемодиафильтрация, гемодиализ.
Почечная заместительная терапия (УД – IIС) [29].
- Рекомендуется использовать либо непрерывную (CRRT), либо прерывистую (IRRТ) ПЗТ у пациентов с сепсисом и острым повреждением почек (слабая рекомендация, умеренное качество доказательств).
- Рекомендуется использовать CRRT для облегчения контроля водного баланса у гемодинамически нестабильных септических больных (слабые рекомендации, очень низкое качество доказательств).
- Не рекомендуется использование ПЗТ у пациентов с сепсисом и острым поражением почек только лишь для улучшения показателей креатинина или лечения олигурии без других определенных показаний к ПЗТ (слабые рекомендации, низкое качество доказательств).
Показания для ЗПТ при сепсисе:
- уровень калия плазмы 6,5 и выше, уровень магния плазмы более 4 ммоль/л при олиго-, анурии;
- гиперазотемия (мочевина более 30 ммоль/л; креатинин более 500мкмоль/л)
- метаболический ацидоз 7,15 и ниже;
- клинически значимаягипергидратация (отек легких, мозга), рефрактерная к медикаментозной коррекции;
- необходимость ультрафильтрации при олиго-, анурии для возможности проведения необходимых инфузий и питания.
Противопоказания:
- наличие клиники продолжающегося кровотечения;
- геморрагический синдром любого генеза (в случае развития жизнеугрожающих состояний при экстренной ПЗТ рекомендуется цитратная антикоагуляция);
- туберкулез внутренних органов;
- декомпенсированная сердечная недостаточность.
Режим проведения детоксикации:
Диуретики могут быть использованы для коррекции водной перегрузки (> 10% от общей массы тела) после выведения из шока. При высоком уровне мочевины на фоне олиго/анурии применение диуретиков не оправдано. В случае неэффективности диуретиков замещающая почечная терапия может быть применена для предотвращения водной перегрузки (УД – IIВ).
Необходим контроль водного баланса не только за сутки, но и общий результирующий, т.е. с начала инфузионной терапии, т.к. небольшой суточный прирост жидкости может остаться незамеченным, тогда как за несколько дней незамеченная кумуляция жидкости может составлять несколько литров. При увеличении веса на 10% и более необходимо продумать способ удаления избыточной жидкости. Так как избыточная жидкость является причиной не только отека легких и мозга, но и почек, брыжейки кишечника, миокарда, создавая и поддерживая условия для ПОН.
- при развитии почечной недостаточности с олигоанурией, либо при высоких показателях азотемии, опасных электролитных нарушениях проводится заместительная почечная терапия;
- применение интермиттирущего гемодиализа или продолжительной вено-венозной гемофильтрация (CVVH) не имеет преимуществ (УД – IIВ);
- CVVH более удобна для проведения у пациентов с нестабильной гемодинамикой (УД – IIВ);
- CVVH или интермиттирущий диализ может быть применен у пациентов с сопутствующим острым повреждением головного мозга или при других причинах повышения внутричерепного давления или генерализованном отеке мозга (УД – IIВ);
- правила применения почечно-замещающей терапии указаны в актуальном КП «Острая почечная недостаточность».
Медикаментозное лечение
Перечень основных лекарственных средств:
| Фармакотерапевтическая группа | Международное непатентованное наименование ЛС | Способ применения | Уровень доказательности |
| Кристаллоидные растворы | Физиологический раствор натрия хлорида | Для ранней регидратации в течение первых 3 часов следует ввести кристаллоидныйраствор в объеме не менее 30 мл/кг массы тела в течение 3 часов.Может потребоваться дополнительное введение жидкости, однако в этом случае требуется тщательная клиническая переоценка волемического статуса пациента | А |
| Кристаллоидные растворы | Рингера лактат |
В качестве одного из стартовых кристаллоидных буферных растворов. Объем зависит от волемического статуса и результатов КОС крови. |
С |
| Кристаллоидный раствор сбалансированный |
Натрия хлорид Калия хлорид Кальция хлорида дигидрат Магния хлорида гексагидрат Натрия ацетата тригидрат Кислота яблочная Вспомогательные вещества: Натрия гидроксид Вода для инъекций [2,21] |
500-1000 мл/сутв/в под контролем показателей гемодинамики, КЩС крови. | С |
| Коллоидный раствор | Альбумин |
Следует вводить при СШ с гипопротеинемией/ гипоальбуминемией. При необходимости введения больших объемов кристаллиодов. Вливание 20% раствораальбумина человека для достижения уровня альбумина плазмы более 30г/л уменьшает летальность при СШ (при сепсисе без шока и недостижении уровня 30г/л – не влияет на летальность). |
В |
|
|
Норэпинефрин* | В начале 0,02-0,5 мкг/кг/мин в/в, титровать до наступления эффекта, максимальная доза 30 мкг/мин | В |
| Эпинефрин | Вначале 0,05–2 мкг/кг/минв/в, титровать до наступления эффекта | В | |
| Инотроп/вазопрессор | Терлипрессин | Внутривенно струйно или капельно 1 мг с интервалом 4-6 часов | С |
| Инотроп/вазопрессор | Добутамин* |
Вначале 0,5–1 мкг/кг/минв/в, затем 2–20 мкг/кг/мин. Препарат выбора у пациентов при нормальномАДср и признаках гипоперфузии, несмотря на нормоволемию. При наличии монитора СВ – при снижении СИ/СВ и нормальном АДср и КДО/ГКДО |
В |
| Инотроп/вазопрессор | Допамин |
5–20 мкг/кг/мин в/в, титровать до наступления эффекта. У пациентов без ответа на регидратацию можно применять вазопрессоры. |
В |
|
Производные имидазола |
Метронидазол |
500 мг/100мл каждые 8 часов в/в. |
В |
|
Антибиотики/ Пенициллины с ингибиторами бета-лактамаз |
Ампициллин и ингибитор бета-лактамазы | 1200 мг каждые 8 часов в/в. | А |
| Антибиотики/ Пенициллины | Ампициллин | 1000 мг каждые 6 часов в/в. | А |
| Антибиотики/ Цефалоспорины второго поколения |
Цефуроксим |
1500 мг каждые 8 часов в/в. | C |
| Антибиотики/ Цефалоспоринытретьегопоколения | Цефтриаксон |
1000 мг каждые 8-часовв/в. |
А |
| Антибиотики/ Цефалоспоринычетвертогопоколения | Цефепим | 1000-2000 мг каждые 8-12 часов. | C |
| Антибиотики/ Аминогликозиды | Гентамицин | 3-5 мг/кг в день в разделенных дозах каждые 8 часов. | А |
| Антибиотики/ Аминогликозиды | Амикацин | по 5 мг/кг каждые 8 ч или по 7,5 мг/кг каждые 12 ч. | C |
| Противовирусные препараты прямого действия | Ацикловир | 5 мг/кг в/в в течение 60 мин каждые 8 часов в течение 5 дней | C |
| Антикоагулянты |
Надропарин кальций |
1 раз в сутки 2850-9500 МЕанти-Ха/0,3-1,0 млп/к. | C |
| Антикоагулянты | Эноксапарин натрия | 1 раз в сутки 2000- 10000 МЕ анти-Xa / 0,2-1,0 млп/к. | C |
| Антикоагулянты | Гепарин | 24000-48000 ЕД/сут в/в при непрерывной инфузии или 5000 ЕД п/к каждые 6-12 ч под контролем АЧТВ. | B |
|
*Лекарственные средства без регистрации в РК |
Перечень дополнительных лекарственных средств:
| Фармакотерапевтическая группа | Международное непатентованное наименование ЛС | Способ применения |
Уровень доказательности |
| Глюкокортикостероиды | Гидрокортизон |
Первичные варианты: гидрокортизон (кортизол): 50 мг в/в каждые 6 часов, но не более 200 мг/сутки. Предпочтительно в/в микроструйное введение 10мг/час для профилактики гипергликемии, гипернатриемии. |
В |
| Гипогликемическое средство | Инсулин |
Целевое значение глюкозы 7,8–10,0 ммоль/л (верхний предел 10 ммоль/л) |
В |
| Вазопрессор | Фенилэфрин | 0,02–0,5 мкг/кг/мин в/в, титровать до наступления эффекта. | С |
|
Антибиотик/ Комбинация бета-лактамовс ингибиторами бета-лактамаз |
Пиперациллинс Тазобактамом* |
3-4 раза в сутки в/ввкомбинации 4000 мг пиперациллинас 500 мг тазобактама. |
А |
| Антибиотик/ Фторхинолоны без антисинегнойной активностью | Моксифлоксацин | 1000 мг 2 раза в сутки в/в. | A |
| Антибиотик/ Фторхинолоны без антисинегнойной активностью |
Офлоксацин |
1000 мг 2 раза в сутки в/в. | C |
| Антибиотик/ Фторхинолоны с антисинегнойной активностью |
Ципрофлоксацин |
0,2% раствор по 100 мл, 600 мг 2 раза всуткиили400мг3разав сутки в/в. | A |
|
Антибиотик/ Карбапенемы |
Меропенем |
1000 мг каждые 8 часов в/в. |
A |
| Эртапенем | 1000 мг каждые 8 часов в/в. | C | |
| Имипенем с циластатином | 1000 мг каждые 8 часов в/в. | A | |
|
Антибиотик/ Антибиотики гликопептидной структуры, активные в отношении МRSA |
Ванкомицин | 1000 мг каждые 8-12 часовв/в. | A |
|
Антибиотики/ Полимиксины |
Колистиметат натрия* |
3 000 000 ЕД/сут в/в каждые 8 часов. При тяжелых инфекциях суточная доза может быть увеличена до 12 000 000 ЕД. |
C |
|
Антибиотики/ Макролиды |
Кларитромицин | 500 мг каждые 12 часов в/в. | A |
|
Эритромицин |
В качестве прокинетика 500 мг внутрь каждые 8 часов. |
A | |
|
Блокаторыгистаминовых H2-рецепторов |
Фамотидин | 40 мг 2 раза/сутки в/в. | C |
|
Противогрибковые средства |
Микафунгин | 150 мг/сут в/в однократно медленно в течение не менее 60 мин. | B |
| Флуконазол | 150 мг/сут в/в однократно медленно в течение не менее 60 мин. | B | |
| Вориконазол |
Насыщающая доза при всех показаниях (первые 24 часа): 6 мг/кг в/в через каждые 12 часов; поддерживающая доза (через 24 часа после начала лечения): 4 мг/кг в/в через каждые 12 ч. Вводить немедленно после приготовления раствора, со скоростью не более 3 мг/кг/ч в течение 1-3 часов. |
C | |
| Каспофунгин |
70 мг в первые сутки в/в в течение не менее 60 мин, со вторых суток 50 мг в/в. При резистентности Candida к флуконазолу. |
С | |
| Ингибиторы протонной помпы | Пантопразол | 40 мг 2 раза/сутки в/в. | С |
| Омепразол | 20 мг 2 раза/сутки в/в. | С | |
| *Лекарственные средства без регистрации в РК |
Инфузионно-трансфузионная терапия [16,19,24,27,29,30]:
1) Цель и задачи инфузионной терапии
Основными задачами инфузионной терапии у больных с сепсисом являются:
- восстановление и поддержание гемодинамики посредством нормализации объема циркулирующей крови (ОЦК);
- улучшение микроциркуляции и доставки кислорода к тканям;
- восстановление нормального содержания электролитов, поддержание адекватного уровня коллоидно-осмотического давления (КОД) плазмы, распределения жидкости между секторами организма – внутриклеточным, интерстициальным и сосудистым;
- снижение концентрации медиаторов септического каскада и токсических метаболитов с целью предотвращения активации каскадных систем, в том числе коагулопатии потребления;
- поддержание мочеотделения.
Первый шаг в проведении инфузионной терапии – это коррекция абсолютной гиповолемии. Относительная гиповолемия за счет патологической вазодилятации устраняется преимущественным применением вазопрессоров (смотрите далее).
Показанием для проведения инфузионной терапии является анамнестически установленные нарушения питания, патологические потери, гипотензия, увеличение концентрации сывороточного лактата до 4 ммоль/л и более, как результат метаболических нарушений вследствие неадекватной перфузии тканей на фоне гиповолемии.
- Стартовый раствор при сепсисе/септическом шоке: кристаллоидные растворы(изотонический раствор натрия хлорида (0,9%)), вводимыйдо 30 мл/кг в течение первых 3 часов (УД – IIА) [29,30] от момента начала инфузионной терапии (с момента установления показаний) при исходной гипотонии или уровне лактата в сыворотке более 4 ммоль/лс дальнейшей оценкой волемического статуса.
- Возможно использование других сбалансированных кристаллоидных растворов (Рингералактат) ( УД – IIС) [19,29,30].
Увеличение концентрации сывороточного лактата до 4 ммоль/л и более как результат метаболических нарушений вследствие неадекватной перфузии тканей на фоне гиповолемии, сопровождающейся гипотензией, является прямым показанием для проведения инфузионной терапии с целью восстановления тканевой перфузии.
Темп и количество инфузионных сред определяется исходным состоянием гемодинамики и ответом на быстрое болюсное введение 500 мл изотонического раствора натрия хлорида (инфузионная проба). Прирост ударного объема, конечно-диастолического объема, увеличение сердечного выброса на 8-15%, снижение тахикардии или увеличение АДср на 5 мм рт. ст. после окончания инфузионной пробы (через 15 минут) считаются основанием для продолжения инфузии под контролем гемодинамики и волемического статуса.
- У пациентов с исходной ХСН предпочтительным тестом, выполняемым с этой же целью является поднятие обеих ног (УД – IIА)[20,22].
- Пациентам с признаками гипергидратации (отеки), с дыхательной недостаточностью (ОРДС, отек легких), при исходной ХСН следует изначально ограничивать темп инфузии, делая упор на применение вазопрессоров (смотрите ниже);
- альбумин показал безопасность и эффективность также как и кристаллоиды (УД – IIС). Используют при гипопротеинемии/гипоальбуминемии или объемной инфузии кристаллоидов;
- Не рекомендуется использование раствора бикарбоната натрия (соды) для коррекции метаболического лактат-ацидоза при рН более 7,15 (УД – IIВ). Использование молярного (8,4%) и полумолярного (4,2%) раствора гидрокарбоната натрия при рН крови более 7,15 может усилить гипокалиемию, гипокальциемию, повысить осмолярность плазмы, способствовать развитию отека мозга, вызывать артериальную гипотензию, снижение сердечного выброса, увеличение содержания лактата в крови, внутриклеточной ацидоз. Гипотензия и уменьшение сердечного выброса могут быть результатом связывания ионов кальция анионами бикарбоната. При рН крови менее 7,15 показана немедленная коррекция метаболического ацидоза, включая растворы гидрокарбоната натрия [8,26,29,30].
При введении раствора бикарбоната натрия необходимо предусмотреть возможный риск критической гипокальциемии и гипокалиемии, т.к. при смещении рН в щелочную сторону уровни ионизированного кальция и калия снизятся. Если исходные концентрации ионизированного кальция и калия были субкритическими, то после защелачивания плазмы они могут стать критическими, что проявится тяжелой гипотензией и/или фатальной аритмией. Поэтому следует своевременно скорректировать уровни калия и кальция, если предполагается инфузия бикарбоната.
- Гипотонические кристаллоидные растворы, растворы на основе крахмала или желатина — противопоказаны (УД – 1В). По сравнению с кристаллоидными изотоническими растворами растворы на основе крахмала приводят к повышенному риску смерти и острому поражению почек [24].
Критерии безопасности инфузионной терапии:
- показатель ЦВД, как статический тест, не рекомендован [30] в виду низкой доказательной базы [20,30,31]. Рекомендуется использовать динамические тесты для определения достаточности преднагрузки и волемии (поднятие ног с последующей оценкой СВ, оценка пульсового давления или ударного объема в связи с изменениями внутригрудного давления, вызванными ИВЛ).
- при отсутствии гипотонии и возможности энтерального питания, инфузиядолжна проводиться строго по показаниям. Общий объем получаемой больным жидкости (энтерально и парентерально) – ориентировочно 40 мл/кг/сутки;
- при отсутствии гипотонии и невозможности энтерального или зондового питания проводиться парентеральное питание и инфузия необходимых лекарственных препаратов и корригирующих растворов. Общий объем получаемой больным парентерально жидкости – ориентировочно 40 мл/кг/сутки;
- суточный диурез в совокупности с другими потерями жидкости (раневые потери, асцит, стул, объем ультрафильтрации и т.п.) должен составлять не менее 80% от суммы объемов введенной энтерально и парентерально жидкости;
- избыточный объем жидкости, вводимой больному с сепсисом, может быть оправдан необходимостью поддержания приемлемого уровня АД при неэффективности вазопрессоров и синдроме «капиллярной утечки». В то же время врач должен понимать, что если положительный гидробаланс требуется более 3-х суток, то это ухудшает прогноз на выживание.
Вазопрессоры [13,19,27,29,30]:
- назначают при АДср менее 65 ммрт.ст., не ожидая эффекта от инфузионной терапии (IIA) или через 60 минут от начала инфузии при недостаточном приросте АД и СВ; При подключении вазопрессоров рекомендуется использовать инвазивный контроль АД;
- увеличение работы сердца и венозного возврата может вести к парадоксальному снижению ЦВД!;
- вазопрессоры назначают сразу при доказанной или предполагаемой сосудистой недостаточности — сниженное ОПСС (инвазивно или неинвазивно), теплые кожные покровы при гипотонии (УД – IIA);
- норэпинефрин- основной препарат (УД – 1В);
- эпинефрин добавляется, чтобы усилить действие норэпинефрина (УД – IIВ);
- допамин до 10-15 мкг/кг/мин в/в — альтернатива норэпинефрину у пациентов с низким рискомтахиаритмии и относительной или абсолютной брадикардией;
- фенилэфрин может применяться у пациентов с септическим шокомкак дополнение к норэпинефрину при выраженной компенсаторной тахикардии (ЧСС более 120 в 1 минуту), в случае отсутствия норэпинефрина или неэффективной комбинации инотроп/вазопрессор, показан у пациентов с высоким сердечным выбросом, низким ОПСС (при возможности измерения/мониторинга СВ) и низким АД; за исключением пациентов с тяжелой брадиаритмией;
- вазопрессин (до 0,03 ед/мин в/в) или терлипрессин – при рефрактерной гипотензии, как альтернативный вазопрессор (УД – IIС) [14,24,29,30]. Обладает пролонгированным действием;
- эффективность применения вазопрессоров определяется по приросту АД,снижению ЧСС, нормализации общего периферического сосудистого сопротивления.
Примечание: При повышенном ОПСС (холодные кожные покровы с нарушением микроциркуляции) необходимо исключение сердечной недостаточности, как причины гипотонии и более рациональное применение периферических вазодилятаторов и инотропных препаратов.
Инотропные препараты:
- добутамин в дозе до 20 мкг/кг/мин (возможно в сочетании с вазопрессорами) применяют при снижении сократимости миокарда, особенно при тахикардии, при нарастании признаков гипоперфузии, несмотря на адекватнуюволемию и АДср (УД – 1С);
- не рекомендуется увеличивать сердечный индекс выше нормальных величин.
Кортикостероиды:
- определенное количество пациентов с септическим шоком имеют острую или хроническую надпочечниковую недостаточность, которая требует назначения кортикостероидов. Определение уровня кортизола в экстренных ситуациях может быть недоступно, а прочие признаки (электролитные нарушения, гипогликемия и пр.) нивелироваться проводимой инфузионной терапией. Поэтому кортикостероиды показаны всем пациентам с рефрактерным септическим шоком без лабораторного подтверждения острой надпочечниковой недостаточности, которое может быть отложено. Терапия гидрокортизоном не снижает летальность, но снижает относительный риск смерти (ускоряет разрешение шока) и сокращает время нахождения в отделении интенсивной терапии;
- гидрокортизон в/в не используется у пациентов с септическим шоком, если адекватная инфузионная терапия и вазопрессоры стабилизируют гемодинамику, при сохраняющейся нестабильности гемодинамики, назначают 200 мг/сутки в/в в четыре приема (50 мг в/в каждые 6 часов, но не более 200 мг/сутки)или в/в микроструйно 200 мг/10 ч (УД – IIС);
- вместо гидрокортизона можно использовать:
дексаметазон 10 мг в/в (в разовой дозе) каждые 6 часов или метилпреднизолон30мг/кг каждые 6 часов в/в (при септическом шоке, тяжелом сепсисе) [33] или преднизолон до 75 мг/сутв/в (УД – ID) [14,15];
- глюкокортикоиды могут быть отменены, когда вазопрессоры больше не требуются для поддержания АД [14,30];
- метилпреднизолон может быть использован в фибропролиферативной стадии ОРДС для уменьшения степени фиброзирования легких;
- кортикостероиды не назначаются у пациентов с сепсисом без септического шока, т.к. это увеличивает рост инфекционных и др. осложнений (гипернатриемия, гипергликемия, полинейропатия) и ухудшает исход при внутрибольничной пневмонии (УД – 1D).
Компоненты крови:
- переливание эритроцитсодержащих компонентов крови следует назначать при уровне гемоглобина <70 г/л. Повышать уровень гемоглобина у взрослых следует до 70-90 г/л (УД – 1В);
- более высокий уровень гемоглобина может потребоваться больным с ишемией миокарда, системной венозной гипоксемией и кровотечением;
- не рекомендуется использовать эритропоэтин для лечения анемии, связанной с сепсисом
- необходимо назначать переливание СЗП с целью коррекции сниженного уровня факторов свертывающей системы любого генеза, только в случае геморрагического синдрома, кровотечении или при проведении запланированных инвазивных вмешательств (УД – IID).
Трансфузия свежезамороженной плазмы (СЗП) рекомендуется при наличии доказательств коагулопатии со снижением содержания факторов свертывания, с увеличением протромбинового времени или АЧТВ в сочетании с клинически манифестированным коагулопатическимкровотечением или без такового перед инвазивными процедурами [5].
Необходимо назначать переливание концентрата тромбоцитов (УД – IID), когда:
- количество тромбоцитов составляет <10х109/л без геморрагического синдрома;
- количество тромбоцитов составляет менее 20х109/л при значительном риске геморрагического синдрома или при его наличии;
- перед проведением хирургического/другого инвазивного вмешательства, когда требуется высокое количество тромбоцитов должно быть > 50х109/л;
- альбумин применяется при проведении объемной инфузионной терапии кристаллоидами для профилактики снижения коллоидно-осмотического (онкотического) давления при гипопротеинемии (менее 50 г/л) или гипоальбуминемии (менее 30 г/л);
Все трансфузии препаратов и компонентов крови проводятся в соответствии с Правилами хранения, переливания крови, ее компонентов и препаратов [5].
Коррекция гипергликемии:
Рекомендуется начинать дозированное введение инсулина, когда 2 последовательных значения уровня глюкозы крови >10 ммоль/л.
Целью инсулинотерапии является поддержание уровня глюкозы крови на уровне или ниже 7,8 ммоль/л, но не выше 10 ммоль/л (верхний предел 10 ммоль/л), что сопряжено с существенным снижением уровня смертности (УД – 1A) [24]. Главным моментом при коррекции гипергликемии является недопущение и избежание гипогликемии [24];
- инсулин вводиться подкожно или внутривенно с помощью шприца-дозатора или инфузомата;
- контролировать поступление глюкозы в организм и уровень глюкозы в крови каждые 1-2 часа (каждые 4 часа при стабильном состоянии) у пациентов, которым внутривенно вводится инсулин (УД – 1С). При использовании высодозных темпов в/в введения инсулина (0,1 Ед/кг/час) необходим ежечасный контроль гликемии независимо от стабильности гликемии;
- не использовать образцы капиллярной крови для измерения гликемии, более точно определение глюкозы в артериальной или венозной крови (УД – 1В).
Целевые параметры основных систем, которые рекомендуется достичь в первые 6 часов терапии:
- среднее артериальное давление ≥ 65мм рт.ст.;
- темп диуреза ≥ 0,5 мл/кг за час;
- нормализация оксигенации и сатурации артериальной крови и центральный венозной крови (УД – 1C)*;
- снижение уровня лактата (УД – IIC).
Примечание:
— ScvO2 более 70% – при отсутствии гипоксемии или(и) тяжелой анемии.
Антибактериальная терапия:
- эмпирическое назначение внутривенных антибиотиков в течение 1-го часа после постановки диагноза сепсиса, тяжелого сепсиса (УД – 1С), септического шока (УД – 1В) является целью, определяющей эффективность терапии;
- начальная эмпирическая терапия должна включать антибактериальные препараты, и/или противогрибковый препарат, и/или противовирусный препарат, в зависимости от того, какая инфекция предполагается;
- концентрация и биодоступность препаратов должна быть достаточной для проникновения и подавления предполагаемого источника инфекции (УД – 1В);
- суточная доза должна быть максимально разрешенной, с минимальными интервалами введения или в виде постоянной инфузии (в соответствии с инструкцией по применению препарата);
- эффективность антибактериальной терапии должна исследоваться ежедневно на предмет возможной деэскалации (УД – 1С);
- необходимо контролировать эффективность антибактериальной терапии по уровню температуры тела, количеству лейкоцитов и лейкоцитарной формуле, динамике С-реактивного белка или прокальцитонина для контроля эффективности эмпирической антибактериальной терапии, и возможности продолжения последней, у пациентов с признаками сепсиса, но без очевидного источника инфекции (УД – IIС);
- эмпирическая терапия должна включать комбинацию антибиотиков (не менее 2-х), особенно у пациентов с нейтропенией (УД – IIВ), резистентными формами Acinetobacterи Pseuodomonasspр. (УД – IIВ);
- при наличии бактериемии Streptococcuspneumoniae с септическим шоком необходима комбинация бета-лактамных антимикробных препаратов с препаратами других групп (аминогликозиды, фторхинолоны, трициклические гликопептиды, полимиксины) (УД – IIВ);
- в комбинации с антибиотиками без антианаэробной активности может применяться метронидазол;
- эмпирическая терапия не должна продолжаться более 3-5 дней. Деэскалационная терапия или соответствующая профилю инфекции антибактериальная терапия должна начаться сразу после бактериологической идентификации профиля инфекции и определения чувствительности (УД – 2В);
- в зависимости от очага инфекции рекомендовано [19] использование сочетания групп антимикробных препаратов:
— внебольничные инфекции у пациентов без факторов риска (цефалоспорины 3 поколения + метронидазол; ингибитор защищённые аминопенициллины/фторхинолоны);
— внебольничная инфекция у пациентов с факторами риска (наличие возбудителя с бета-лактамазой расширенного спектра): антимикробные препараты — аминогликозиды, фторхинолоны, карбапенемы;
— «ранняя» нозокомиальная инфекция вне ОРИТ (возбудителис бета-лактамазой расширенного спектра, MRSA) – антимикробные препараты аминогликозиды, фторхинолоны, карбапенемы ± антиMRSA;
— «поздняя» нозокомиальная инфекция (более 7 дней в стационаре или более 3 дней в ОРИТ) – карбапенемы ± антиMRSA, тигециклин +аминогликозиды/цефалоспорины/полимиксин;
— пациенты с кандидозным сепсисом – противогрибковые препараты;
- Деэскалационная терапия или соответствующая профилю инфекции антибактериальная терапия должна начаться сразу после бактериологической идентификации профиля инфекции и определения чувствительности (УД – IIВ);
- длительность терапии составляет в среднем 7-10 дней, более длительно — у пациентов с иммунодефицитом и медленным клиническим ответом, с не дренируемым источником инфекции, бактериемии S. аureus; некоторые грибковые и вирусные инфекции с иммунодефицитом, включая нейтропению (УД – IIС);
- противовирусная терапия должна проводиться как можно раньше у пациентов с сепсисом и септическим шоком вирусной этиологии (УД – IIС). Противовирусная терапия назначается по рекомендации врача инфекциониста;
- у пациентов с системным воспалительным ответом не бактериальной природы не должны применяться антибактериальные препараты.
Критерии эффективности антимикробной терапии при сепсисе [16,19]:
- стойкая нормализация температуры тела (максимальная температура менее 380С) в течение трех и более дней;
- положительная динамика основных симптомов инфекции;
- регрессия признаков системной воспалительной реакции;
- восстановление функции поврежденных органов;
- тенденция к нормализации количества лейкоцитов в крови, улучшение лейкоцитарной формулы;
- отрицательные бактериологические исследования (за исключением колонизации);
- снижение или нормализация концентрации прокальцитонина (УД – IIС) [11,30], С-реактивного белка и пресепсина в динамике.
Иммуномодуляторы, иммуноглобулины:
- не рекомендуется применение пероральных и парентеральных иммуномодуляторов, иммуноглобулинов при тяжелом сепсисе и септическом шоке (УД – IIB).
Профилактика тромбоза глубоких вен:
- если нет противопоказаний, следует использовать низкие дозы нефракционированного или низкомолекулярного гепарина (УД – 1А). Следует использовать профилактические изделия ((компрессионные чулки, устройства для перемежающей механической компрессии н/к), если противопоказано введение гепарина (УД – 1А);
- следует использовать комбинацию медикаментозного и механического лечения у пациентов с высоким уровнем риска развития тромбоза глубоких вен по шкале риска ТЭО типа Wells, Padua или локальным шкалам оценки венозных ТЭО (УД – IIС).
Профилактика стрессовых язв:
Факторы риска: ИВЛ более 48 ч, ЗПТ, гипокоагуляция, использование стероидов, отсутствие энтерального питания.
- следует проводить профилактику стрессовой язвы, используя блокаторы Н2-гистаминовых рецепторов или ингибиторы протонной помпы (УД – 1В);
- при профилактике стрессовых язв лучше использовать ингибиторы протонной помпы (УД – IIC);
- при отсутствии риска развития стрессовых поражений ЖКТ — восстановлении энтерального или зондового питания — антисекреторные препараты отменяют (УД – IIВ).
Хирургическое вмешательство
Хирургическое лечение при сепсисе:
Виды операций при сепсисе:
- дренирование гнойных полостей;
- удаление очагов инфекционного некроза;
- удаление внутренних источников контаминации.
Удаление внутренних источников контаминации.
- колонизированных имплантатов;
- искусственные клапана сердца;
- сосудистые/суставные протезы;
- инородных тел, временно с лечебной целью внедренных в ткани или внутренние среды организма (трубчатых дренажей и катетеров);
- удаление/проксимальное отключение (отведение) потока содержимого дефектов полых органов, рассматриваемых в качестве источников инфицирования.
Дренирование абсцесса:
- создание постоянного оттока жидкого содержимого из ограниченной гнойной полости.
Удаление очагов инфекционного некроза:
- удаление некротически измененных тканей необходимо выполнить после полноценного вскрытия очага деструкции и оценки состояния тканей;
- при наличии явных признаков некроза необходимо выполнить иссечение (некрэктомию);
- если до операции нет явных признаков инфицирования, то необходимо придерживаться выжидательной тактики с постоянным динамическим контролем;
- при нарастании местных и общих признаков инфицирования необходимо принять активную хирургическую тактику;
- при наличии тонкого слоя некротических тканей возможно использование гидрофильных повязок или препаратов, содержащих ферменты;
Удаление инородных тел:
- подлежат удалению инородные тела, которые поддерживают инфекционный процесс;
- при перфорации полого органа происходит постоянная контаминация микробами брюшной полости, это требует контроля и устранения источника перитонита (аппендэктомия, холецистэктомия, резекция кишки, ушивание перфорации и т.д.), тщательная санация брюшной полости антисептиками, дренирование брюшной полости;
- при отсутствии условий радикального устранения источника перитонита (тяжелое состояние больного, общие противопоказания выполнения обширной по объему операции) возможен вариант наложения свища, обходного анастомоза, что является менее опасным вмешательством на этот момент.
Завершение операции:
- одномоментный метод лечения;
- этапный метод лечения.
Этапный метод лечения подразумевает программированную лапаросанацию с целью контроля источника перитонита и его регресса.
Программированная лапаросанация:
Показания:
- распространенный фибринозно-гнойный/каловый перитонит;
- признаки анаэробного инфицирования брюшной полости;
- невозможность одномоментной ликвидации/надежной локализации источника перитонита;
- стадия перитонита соответствующему тяжелому сепсису/септическому шоку;
- состояние операционной раны не позволяющими закрыть дефект передней брюшной стенки;
- синдром внутриабдоминальной компрессии;
- инфицированный панкреонекроз с симптомами сепсиса (УД – В);
- сроки хирургического вмешательства при панкреонекрозе не ранее 14 дней, за исключением пациентов с тяжелым сепсисом, ПОН (УД – В).
Некрэктомия показана:
- при гнойно-воспалительных заболеваниях мягких тканей;
- инфицированных посттравматических ранах;
- при инфицированном панкреонекрозе (УД – А). При неэффективности или отсутствия местных условий выполнения транскутанного дренирования, а также невозможности удаления некротических масс, эффективного дренирования гнойных полостей, при сформировании другого очага инфекции выполняется лапаротомия;
- противопоказанием для повторных вмешательств является ПОН, рефрактерная к медикаментозному лечению. Исключение составляет внутрибрюшное или продолжающееся желудочно-кишечное кровотечение.
Подготовка к операции и обезболивание:
- хирургическому вмешательству обязательно предшествует активные интенсивная терапия по улучшению витальных функций органов и систем пациента, что снизит риск летальных исходов во время анестезии и операции;
- предоперационная подготовка проводится в течение не более 2-4 часов с целью стабилизации состояния: нормализации гемодинамики, коррекции имеющихся электролитных нарушений, уровня гликемии, нарушений свертывающей системы;
- во время подготовки по показаниям проводить необходимое дообследование;
- неэффективность подготовки в течение 2-4 часов не является противопоказанием для экстренной операции;
- при операциях вид анестезии: местная анестезия, общее обезболивание;
- регионарная анестезия (ЭДА, СА) при сепсисе противопоказана;
- в послеоперационном периоде обезболивание проводится ненаркотическими и наркотическими аналгетиками (при отсутствии противопоказаний);
- эпидуральная аналгезия с целью послеоперационного обезболивания, для планируемого частого обезболивания или с целью восстановления моторики кишечника может проводиться только после полной санации источника инфекции и при эффективности антибактериальной терапии, при стабилизации кровообращения и при отсутствии других противопоказаний.
Дальнейшее ведение:
- психо-эмоциональная реабилитация;
- коррекция режима и состава питания;
- санаторно-курортное лечение.
Индикаторы эффективности лечения:
- снижение степени интоксикации (клинически и лабораторно);
- нормализация параметров кровообращения;
- нормализация внешнего дыхания;
- нормализация функции почек.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации: нет.
Показания для экстренной госпитализации: наличие клиники ССВО, сепсиса/септического шока.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2020
- 1. Алгоритмы оказания скорой медицинской помощи вне медицинской организации. Пособие для медицинских работников выездных бригад скорой медицинской помощи СПб.: ИП Шевченко В.И. – 2018. – 158 с.
2. Грицан А.И. с соавт. Диагностика и интенсивная терапия острого респираторного дистресс-синдрома. Клинические рекомендации Федерации анестезиологов и реаниматологов РФ // Анестезиология и реаниматология. – 2016. – 61(1). – С. 62-70.
3. Миронов П.И. Сравнительная оценка клинической эффективности инфузионной терапии сбалансированными и несбалансированными растворами при сепсисе у детей. Российский вестник. Том 8. – №1.- 2018.- С. 44-48.
4. МКБ-10 https://icd.who.int/browse10/2016/en
5. Приказ Министра здравоохранения Республики Казахстан от 15 апреля 2019 года № ҚР ДСМ-38 – Дополнения и изменения к Приказу МЗ РК № 666 от 6 ноября 2009 года «Об утверждении Номенклатуры, Правил заготовки, переработки, хранения, реализации крови и ее компонентов, а также Правил хранения, переливания крови, ее компонентов и препаратов».
https://tengrinews.kz/zakon/pravitelstvo_respubliki_kazahstan_premer_ministr_rk/zdravoohranenie/id-V1900018533/.
6. СавельевВ.С., ГельфандБ.Р.Сепсис.Классификация,клинико-диагностическая концепция и лечение. Практическое руководство. Медицинское информационное агентство. – 2013. – 368 с.
7. Семидесятая сессия всемирной ассамблеи здравоохранения. Совершенствование профилактики, диагностики и клинического ведения сепсиса A70/13 Пункт 12.2, 13 апреля 2017 г.
8. Черний В.И. с соавт. Этиология, патогенез и интенсивная терапия метаболического ацидоза // Медицина неотложных состояний.- №6(77). – 2016. – С. 153-166.
9. Amanda Corley et al. Highflow nasal cannulae for respiratory support in adult intensive care patients. Cochrane Systematic Review — Intervention Version published: 30 May 2017.
10. Asfar P et al. High versus Low Blood-Pressure Target in Patients with Septic Shock. Engl J Med 2014; 370:1583-1593.
11. Chengfen Y, Tong L, Xinjing G, Zhibo L, Lei X. Accuracy of procalcitonin for diagnosis of sepsis in adults: a Meta-analysis. Zhonghua Wei Zhong Bing Ji Jiu Yi Xue. 2015Sep;27(9):743-749.
12. Christopher W. Seymour et al. Severe Sepsis in Pre-Hospital Emergency Care Analysis of Incidence, Care, and Outcome. Am J RespirCrit Care Med. 2012 Dec 15; 186(12): 1264–1271. Published online 2012 Dec 15.
13. Dellinger RP, Levy MM, Rhodes A, Annane D, Gerlach H et al. Surviving Sepsis Campaign Guidelines Committee including The Pediatric Subgroup. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock, 2012. Intensive Care Med. 2013 Feb;39(2): 165-228.
14. Dellinger RP, et al. Surviving Sepsis Campaign: International Guidelines for Management of Severe Sepsis and Septic Shock: 2012 Critical Care Medicine 2013;41:580-637.
15. Dunser MW, Festic E, Dondorp A, et al. Recommendations for sepsis management in resource-limited settings. Intensive Care Medicine 2012;38:557–74
16. Jiang LB, Zhang M, Jiang SY, Ma YF. Early goal-directed resuscitation for patients with severe sepsis and septic shock: insights and comparisons to ProCESS, ProMISe, and ARISE. Crit Care. 2016 Jul1;20(1): 160.
17. Leisman DE et al. Patterns and Outcomes Associated With Timeliness of Initial Crystalloid Resuscitation in a Prospective Sepsis and Septic Shock Cohort.Crit Care Med 2017; 45:1596-1606.
18. Leone M et al. Optimizing Mean Arterial Pressure in Septic Shock: A Critical Reappraisal of the Literature. Crit Care 2015 Mar 10;19:101.
19. Levy, Mitchell M. MD, MCCM; Evans, Laura E. MD et al The Surviving Sepsis Campaign Bundle: 2018 Update Critical Care Medicine: June 2018 — Volume 46 — Issue 6 — p 997-1000.
20. Maurizio Cecconi et al. Consensus on circulatory shock and hemodynamic monitoring. Task force of the European Society of Intensive Care Medicine Intensive Care Medicine volume 40, P. 1795–1815(2014) Published: 13 November 2014.
21. Michael C. Reade et al.Effect of Dexmedetomidine Added to Standard Care on Ventilator-Free Time in Patients With Agitated Delirium. A Randomized Clinical Trial JAMA. 2016;315(14):1460-1468. doi:10.1001/jama.2016.2707
22. Monnet X, Pail M, Jean-Louis Teboul. Passive leg raising for predicting fluid responsiveness: a systematic review and meta-analysis. Intensive Care Medicine volume 42, P.1935–1947(2016).
23. Sakr Y et al. Higher Fluid Balance Increases the Risk of Death From Sepsis: Results From a Large International Audit. Crit Care Med 2017; 45:386-394.
24. Scott L. Weiss, MD, MSCE, FCCM et al. Surviving Sepsis Campaign International Guidelines for the Management of Septic Shock and Sepsis-Associated Organ Dysfunction in Children.February 2020 Volume 21 Number 2. The Society of Critical Care Medicine and the World Federation of Pediatric Intensive and Critical Care Societies P. 52-106.
25. Seymour CW et al. Assessment of Clinical Criteria for Sepsis. The Third International Consensus Difinitions for Sepsis and Septic Shok.JAMA-2016.
26. Sepsis Management. By Young Ran Lee, Pharm.D., BCPS, BCCCP; and Taryn B. Bainum, Pharm.D., BCPS. CCSAP 2019 Book 1 • Infection Critical Care.
27. Sepsis: recognition, diagnosis and early management. NICE guideline [NG51]. Published: 13 July 2016.Last updated in April 2019.
28. SiddharthDugar, MD, Chirag Choudhary, MD, MBA, Abhijit Duggal, MD, MPH, MSc, FACP Sepsis and septic shock: Guideline-based management. Сleveland clinic journal of medicine volume 87, Number 1 January 2020. Р. 53-64.
29. Singer M, Deutschman CS, Seymour CW et al. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). JAMA. 2016;315(8):801–810. doi:10.1001/jama.2016.0287.
30. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016.
https://link.springer.com/article/10.1007/s00134-017-4683-6#Sec24.
31. T. G. Eskesen et al. Systematic review including re-analyses of 1148 individual data sets of central venous pressure as a predictor of fluid responsiveness. Intensive Care Medicine volume 42, P.324–332(2016) Published: 01 March 2016
32. Vincent JL et al. Albumin Administration in the Acutely Ill: What Is New and Where Next? Crit Care 2014, 18 (4), 231.
33. VolbedaМ et al. Glucocorticosteroids for sepsis: systematic review with meta-analysis and trial sequential analysis. Intensive Care Medicine volume 41, P.1220–1234(2015).
34. Westwood M, Ramaekers B, Whiting P, Tomini F, Joore M, Armstrong N, Ryder S, Stirk L, Severens J, Kleijnen J. Procalcitonin testing to guide antibiotic therapy for the treatment of sepsis in intensive care settings and for suspected bacterial infection in emergency department settings: a systematic review and cost-effectiveness analysis. Health Technol Assess. 2015 Nov;19(96):V-XXV, 1-236.
- 1. Алгоритмы оказания скорой медицинской помощи вне медицинской организации. Пособие для медицинских работников выездных бригад скорой медицинской помощи СПб.: ИП Шевченко В.И. – 2018. – 158 с.
Информация
Сокращения, используемые в протоколе:
| D-димер | – | продукт распада фибрина |
| FiO2 | – | содержание кислорода во вдыхаемой воздушно-кислородной смеси |
| Hb | – | гемоглобин |
| Ht | – | гематокрит |
| PaO2 | – | парциальное напряжение кислорода в артериальной крови |
| PaСO2 | – | парциальное напряжение углекислоты в артериальной крови |
| РЕЕР | – | положительное давление в дыхательных путях |
| Рinsp | – | инспираторное давление в дыхательных путях |
| ScvO2 | – | сатурация центральной венозной крови |
| SIRS | – | синдром системного воспалительного ответа |
| SvO2 | – | сатурация смешанной венозной крови |
| SаO2 | – | сатурация артериальной крови |
| АБП | – | антибактериальные препараты |
| АД | – | артериальное давление |
| АДср | – | артериальное давление среднее |
| АлАТ | – | аланинаминотрансфераза |
| АМТ | – | антимикробная терапия |
| АсАТ | – | аспартатаминотрансфераза |
| АЧТВ | – | активированное частичное тромбопластиновое время |
| ВАБК | – | внутриабдоминальная компрессия |
| ДВС | – | диссеминированное внутрисосудистое свертывание (крови) |
| ДЗЛА | – | давление заклинивания в легочной артерии |
| ДО | – | дыхательный объем |
| ЖК | – | жирные кислоты |
| ЖКТ | – | желудочно-кишечный тракт |
| ЗАС | – | закрытая аспирационная система |
| ЗПТ | – | заместительная почечная терапия |
| ИВЛ | – | искусственная вентиляция легких |
| ИТ | – | инфузионная терапия |
| ИТТ | – | инфузионно-трансфузионная терапия |
| КДО | – | конечно-диастолический объем |
| КОС | – | кислотно-основное состояние |
| КСО | – | конечно-систолический объем |
| КТ | – | компьютерная томография |
| ЛИИ | – | лейкоцитарный индекс интоксикации |
| МВЛ | – | минутная вентиляция легких |
| МНО | – | международное нормализованное отношение |
| ОКС | – | острый коронарный синдром |
| ОПП | – | острое повреждение почек |
| ОПСС | – | общее периферическое сосудистое сопротивление |
| ОРИТ | – | отделение реанимации и интенсивной терапии |
| ОРДС | – | острый респираторный дистресс-синдром |
| ОЦК | – | объем циркулирующей крови |
| ПВ | – | протромбиновое время |
| ПДКВ | – | положительное давление в конце выдоха |
| ПДФ | – | продукты деградации фибриногена |
| ПЗТ | – | почечная заместительная терапия |
| ПКТ | – | прокальцитонин |
| ПОН | – | полиорганная недостаточность |
| ПП | – | парентеральное питание |
| ПТИ | – | протромбиновый индекс |
| Рпик | – | пиковое давление в дыхательных путях (на высоте вдоха) |
| Рплато | – | давление плато в дыхательных путях (давление при распределении кислородо-воздушной смеси в легких) |
| СА | – | спинальная анестезия |
| САД | – | систолическое артериальное давление |
| СВ | – | сердечный выброс |
| СЗП | – | свежезамороженная плазма |
| СИ | – | сердечный индекс |
| СКФ | – | скорость клубочковой фильтрации |
| СОЭ | – | скорость оседания эритроцитов |
| СПОН | – | синдром полиорганной недостаточности |
| ССВО | – | синдром системного воспалительного ответа |
| СШ | – | септический шок |
| ТВ | – | тромбиновое время |
| ТМ | – | тромбоцитарная масса |
| УД | – | уровень доказательности |
| УЗИ | – | ультразвуковое исследование |
| УО | – | ударный объем сердца |
| ФА | – | фибринолитическая активность |
| ФВ | – | фракция выброса |
| ЦВД | – | центральное венозное давление |
| ЦНС | – | центральная нервная система |
| ЧД | – | частота дыхания |
| ЧСС | – | частота сердечных сокращений |
| ЭДА | – | эпидуральная анестезия |
| ЭКГ | – | электрокардиография |
| СРБ | – | С-реактивный белок (крови) |
| ТЭЛА | – | тромбоэмболия легочной артерии |
| ТЭО | – | тромбоэмболические осложнения |
| ТП | – | трофическое (гипокалорийное) питание |
| ХПН | – | хроническая почечная недостаточность |
| ХСН | – | хроническая сердечная недостаточность |
| ЭП | – | энтеральное апитание |
| SSC2016 | – | The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3) |
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
- Жумадилов Агзам Шаймарданович – руководитель Республиканского Центра критического акушерства ГКП на ПХВ «Городская многопрофильная больница №2» акимата г. Нур-Султан, председатель Правления Казахского общества анестезиологов-реаниматологов, доктор медицинских наук, профессор, руководитель Рабочей группы;
- Васильев Дмитрий Владимирович – заведующий кафедрой анестезиологии и реанимации НАО «Медицинский университет Караганды», кандидат медицинских наук, доцент, заместитель руководителя Рабочей группы;
- Ахмадьяр Нуржамал Садыровна – заведующая кафедрой клинической фармакологии АО «Медицинский университет Астана», доктор медицинских наук;
- Турсынбаев Нурбол Нурланович – заместитель директора по хирургии ГКП на ПХВ «Городская многопрофильная больница №2» акимата г. Нур-Султан, главный внештатный хирург г. Нур-Султан;
- Кожахметов Али Нурбатырович – заведующий отделением анестезиологии и реанимации АО «Научный центр акушерства, гинекологии и перинатологии», доктор медицинских наук, профессор;
- Мусилимов Аскар Балтабаевич – врач анестезиолог-реаниматолог высшей квалификационной категории ГУ «Медицинский центр Управления Делами Президента Республики Казахстан»;
- Чурсин Вадим Владимирович – заведующий кафедрой анестезиологии и реаниматологии АО «Казахский медицинский университет непрерывного образования», кандидат медицинских наук, доцент;
- Малтабарова Нурила Амангалиевна – заведующая кафедрой скорой медицинской помощи, анестезиологии и интенсивной терапии НАО «Медицинский университет Астана», кандидат медицинских наук, доцент;
- Конкаев Айдос Кабибулатович – заведующий кафедрой анестезиологии и реаниматологии НАО «Медицинский университет Астана», доктор медицинских наук, профессор;
- Жумабаев Мурат Болатович – доцент кафедры скорой медицинской помощи, анестезиологии и интенсивной терапии НАО «Медицинский университет Астана», кандидат медицинских наук
- Ким Сергей Иванович – заведующий отделением анестезиологии КГП на ПХВ «Многопрофильная больница им. профессора Х.Ж. Макажанова»;
- Кравцова Татьяна Геннадьевна – преподаватель отдела послевузовского образования АО «Научный центр акушерства, гинекологии и перинатологии», доктор медицинских наук, доцент, эксперт-консультант Рабочей группы.
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
Саркулова Жанслу Нукиновна – руководитель кафедры анестезиологии и реаниматологии НАО «Западно-Казахстанский медицинский университет им. Марата Оспанова», доктор медицинских наук, профессор.
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение 1
Шкала SOFA
Оценка Показатель 1 2 3 4
| Оксигенация | РаО2/ FiО2, мм рт. ст. | < 400 | < 300 | < 200 на ИВЛ | < 100 на ИВЛ |
| Коагуляция | Тромбоциты, Г/л | < 150 | < 100 | < 50 | < 20 |
| Печень |
Билирубин, мг/дл (мкмоль/л) |
1,2 – 1,9 | 2,0 – 5,9 | 6,0 – 11,9 | > 12,0 |
(20 – 32) (33 – 101) (102 – 204) (> 204)
|
Сердечно- сосудистая система |
Гипотензия или степень инотропной поддержки |
среднее АД <70 мм рт. ст. |
Допамин <5 мкг/кг/мин или добутамин |
допамин> 5 мкг/кг/мин или адреналин <0,1 мкг/кг/мин, или норадреналин <0,1 мкг/кг/мин |
> 15 мкг/кг/мин > 0,1 мкг/кг/мин > 0,1 мкг/кг/мин |
| ЦНС | Показатель по шкале ком Глазго | 13 — 14 | 10 — 12 | 6 — 9 | < 6 |
| Почки |
Креатинин, мг/дл (мкмоль/л) или олигурия |
1,2 – 1,9 (110 – 170) |
2,0 – 3,4 (171 – 299) |
3,5 – 4,9 (300 – 440) или < 500 мл/сут. |
> 5 (> 440) или <200 мл/сут. |
Примечание:
Минимальное число баллов – 0;
Максимальное число баллов – 24
Приложение 2
APACHEII Тяжесть состояния, септические осложнения и летальность
| Показатели | Баллы | |||||||||
| +4 +3 +2 +1 0 +1 +2 +3 +4 | +3 +4 | |||||||||
| Физиологические переменные величины | ||||||||||
|
Ректальная температура (°С) |
>41 | 39-40,9 | 38,5-38,9 | 36-38,4 | 34-35,9 | 32-33,9 | 30-31,9 | <29,9 | ||
| АД ср. (мм рт. ст.) | > 160 | 130-159 | 110-129 | 70-109 | 50-69 | <49 | ||||
| ЧСС в мин | > 180 | 140-179 | 110-139 | 70-109 | 55-69 | 4054 | <39 | |||
|
Частота дыхания (при спонтанном дыхании или на искусственной вентиляции) |
>50 | 35-49 | 25-34 | 12-24 | 10-11 | 6-9 | <5 | |||
|
Оксигенация: если FiO2 > 0,5, регистрируйте А-а DO2 если FiO2 < 0,5, регистрируйте только РаО2 (мм рт. ст.) |
>500 | 350-499 | 200-349 | <200 | >70 | 61-70 | 5560 | <55 | ||
|
рН артериальной крови |
>7,7 | 7,6-7,69 | 7,5-7,59 | 7,33-7,49 | 7,25-7,32 | 7,15-7,24 | < 7,15 | |||
| Концентрация натрия в сыворотке (ммоль/л) | > 180 | 160-179 | 155-159 | 150-154 | 130-149 | 120-129 | 111-119 | <110 | ||
| Концентрация калия в сыворотке (ммоль/л) | >7 | 6-6,9 | 5,5-5,9 | 3,5-5,4 | 3,0-3,4 | 2,5-2,9 | <2,5 | |||
| Концентрация креатинина в сыворотке (мкмоль/л) | >300 | 171-299 | 121-170 | 50-120 | <50 | |||||
| Гематокрит (%) | >60 | 50-59,9 | 46-49,9 | 30-45,9 | 20-29,9 | <20 | ||||
| Количество лейкоцитов (х 1000/мм3) | >40 | 20-39,9 | 15-19,9 | 3-14,9 | 1-2,9 | <1 |
Количество баллов по шкале комы Глазго (15- реальное количество баллов)
| Концентрация | > 180 | 160- | 155- | 150- | 130- | 120- | 111- | <110 | |
| натрия в | 179 | 159 | 154 | 149 | 129 | 119 | |||
| сыворотке | |||||||||
| (ммоль/л) | |||||||||
| Концентрация | >7 | 6-6,9 | 5,5- | 3,5- | 3,0- | 2,5- | <2,5 | ||
| калия в | 5,9 | 5,4 | 3,4 | 2,9 | |||||
| сыворотке | |||||||||
| (ммоль/л) |
Возрастные точки
| Возраст (годы) | <44 | 45-54 | 55-64 | 65-74 | >75 |
Точки 0 2 3 5 6
Точки хронической патологии
2 точки для избирательной госпитализации после операции или 5 точек приэкстренной операции или госпитализации не по поводу операции, если у пациента имеется выраженное хроническое заболевание печени, почек, сердечно-сосудистой, дыхательной систем или иммуносупрессия
Подсчет баллов по шкале APACHEII:
| APACHE II баллы | Септические осложнения, % | Летальность, % |
| < 10 | 18,2 | 0 |
| 10-19 | 24,6 | 15,8 |
| 20-29 | 27,7 | 21,3 |
| 30 и более | 37,5 | 75.0 |
Приложение 3
Шкала quickSofa (qSofa)
Предназначена для быстрой оценки состояния пациента с сепсисом
- Частота дыхания более 22 в минуту;
- Изменения ментального статуса (оценка по шкале Глазго 13 баллов и меньше);
- Артериальная гипотензия АД систолическое менее 100 мм.рт. ст.
Показатель qSOFA ≥2 свидетельствует о сепсисе
(SeymourCWetal. Assessment of Clinical Criteria for Sepsis.The Third International Consensus Difinitions for Sepsisand Septic Shok.JAMA-2016- Vol 315 №8.-З.762-774.)
Приложение 4
Диагностический алгоритм при вынесении диагноза Сепсис и септический шок
[Singer M, Deutschman CS, Seymour CW et al. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). JAMA.2016;315(8):801–810. doi:10.1001/jama.2016.0287]
Приложение 5
АЛГОРИТМ ДИАГНОСТИКИ И ЛЕЧЕНИЕ НА ЭТАПЕ СКОРОЙ НЕОТЛОЖНОЙ ПОМОЩИ (схемы)
Приложение 6
Карта наблюдения пациента, маршрутизация пациента:
Приложение 7
Седация и миорелаксация при проведении ИВЛ пациентам с сепсисом
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздрава России
С момента принятия и рекомендаций по использованию в клинической практике положений Калужской согласительной конференции 2004 прошло 10 лет. Несмотря на казалось бы совершенно чёткие указания по постановке диагноза сепсис, проблема за эти годы остаётся дискутабельной, а в рамках активного перехода на финансирование и работу в сфере обязательного медицинского страхования (ОМС) и стандартизированной медицины в условиях дефицита средств, приобрела новые оттенки. Нами ретроспективно изучены медицинские карты 100 больных с тяжелыми формами рожи нижних конечностей, находившихся на лечении в гнойно-хирургических отделениях клиники общей хирургии за 2011-2013 годы. Все больные ретроспективно одновременно имели два и более признаков системного воспаления, а при наличии инфекционного очага – рожи – сепсиса. Сепсис ретроспективно диагностирован у 64%, тяжелый сепсис у 23%, в состоянии септического шока госпитализировано 13% больных.
Что касается вынесения в диагноз самого понятия сепсис, то с учетом вышеуказанных обстоятельств в процесс формулировки диагноза вклинивается совсем новая, ранее неописанная проблема – административный фактор. В сложившихся условиях, относительно благоприятных для взаимодействия клиники и больницы на почве лечебной деятельности, административный фактор полностью негативно сказывается на устоявшихся десятилетиями взаимоотношениях. Несмотря на прошедшие 10 лет и неоднократное прохождение хирургами курсов усовершенствования по специальности, вопрос осведомленности администрации в вопросах диагностики сепсиса остается на уровне 80-х годов 20 века, даже при наличии относительно молодых кадров. Вынесение диагноза сепсис становится камнем преткновения, в том числе и в случае неблагоприятного исхода. В то время как стандарты лечения рожи относительно выполнимы, при появлении формулировки «сепсис» появляется значительное количество лечебно-диагностических пунктов, с финансовой и административной точки зрения, «лишних».
Таким образом, в проведенном нами исследовании при наличии сепсиса, вынесение его в диагноз не зафиксировано ни в одном случае. Соответствующие записи появлялись при наличии тяжелого сепсиса только при неблагоприятном течении заболевания и лишь явления септического шока заставляли выносить его в структуру диагноза.
Проблема сохраняет свою актуальность и для её решения в настоящее время требуется участие не только специалистов в данной сфере, но представителей администрации и управленческих структур здравоохранения.
Общие сведения
Сепсис (заражение крови) представляет собой патологический процесс, в основе которого реакция организма на патогенные факторы различной природы в виде генерализованного (системного) воспаления, сочетающего с остро возникшими симптомами системной дисфункции (полиорганной недостаточности) и/или микробной диссеминацией.
Зачастую заражение крови называется бактериальной инфекцией крови. Сепсис — инфекционно индуцированный синдром, проявляющийся в виде системного воспалительного ответа организма на эндотоксиновую агрессию. При этом бактериемия (наличие в крови живых бактерий) является важным, но не обязательным условием развития сепсиса. Отличием сепсиса от инфекции является не соответствующий норме ответ организма человека на инфекцию в сочетании с угрожающей жизни органной дисфункцией. То есть, возникновение сепсиса обусловлено не только свойствами возбудителя инфекции, но и состоянием макроорганизма — его неспособностью к локализации инфекционного агента, обусловленного недостаточностью иммунитета.
Актуальность проблем сепсиса обусловлена ростом его распространенности, высоким уровнем заболеваемости и летальности, что относит сепсис к важным медико-социальным проблемам. Данные эпидемиологических исследований в индустриально развитых странах свидетельствуют, что частота сепсиса варьирует в пределах 50-100 случаев/100 тыс. населения, а уровень смертности остается стабильно высоким (по данным разных авторов — от 15 до 75%) в зависимости от стадии сепсиса, его возбудителя, лечения (рис. ниже). Ведущей причиной смерти при сепсисе является прогрессирующая органная дисфункция.
Смертность при разных типах сепсиса
Существует ряд предпосылок, способствующих высокому риску развития сепсиса, в частности:
- Развитие и широкое внедрение в медицинскую практику инвазивных медицинских технологий/процедур, ассоциированных с контаминированностью оборудования и широким использованием внутрисосудистых устройств.
- Рост количества штаммов микроорганизмов устойчивых к антибиотикам, что обусловлено бесконтрольным/необоснованным применением препаратов широкого спектра действия.
Течение сепсиса в большинстве случаев проходит стадийно (рис. ниже), в соответствии с чем выделяют:
- Сепсис — как системный воспалительный ответ на инфекцию.
- Тяжелый сепсис — как сепсис с признаками гипоперфузии и органной дисфункции хотя бы одной из систем: дыхательной, сердечно-сосудистой, гемостаза, мочевыделительной, печени, центральной нервной системы.
- Септический шок — тяжелый сепсис с наличием полиорганной дисфункции (дисфункция по 2 и более системам/органам).
К группам высоким риском развития сепсиса относятся хирургические, онкологические, ожоговые больные, пациенты с иммунодефицитными состояниями, роженицы, недоношенные дети с малым весом, дети с хромосомными заболеваниями и врожденными пороками развития, длительно находящиеся в стационаре.
Стадии сепсиса
Также развитию сепсиса способствует длительная катетеризация сосудов, искусственная вентиляция легких, проведение длительной иммуносупрессивной терапии, длительный прием глюкокортикостероидных средств, хирургические вмешательства с высокой травматизацией тканей, прием инъекционных наркотиков.
Риск возникновения сепсиса определяется и локализацией первичного очага инфекции — брюшная полость, легкие, мочевыделительная система, раневая поверхность и др. Отмечается относительно высокая инцидентность сепсиса у пожилых пациентов, мужчин и среди детей раннего возраста.
Патогенез
Патогенез развития сепсиса достаточно сложен для краткого изложения и специфичен, в связи с чем перечислим лишь его основные патогенетические звенья:
- длительно сохраняющаяся (постоянная/дискретная) бактериемия/микробная токсемия, обусловленные гнойно-септическими заболеваниями;
- развитие эндогенной интоксикации (эндо/ауто-токсикоз) биологически активными веществами;
- системный деструктивный васкулит;
- нарастание процессов гиперкоагуляции с развитием коагулопатии, ДВС-синдрома;
- развитие выраженной иммунной недостаточности, обусловленной нарушением процессов регуляции иммунореактивности, формированием состояния иммунодепрессии с дезинтеграцией иммунной системы в целом;
- развитие и проявления полиорганной недостаточности.
Таким образом, с позиций современной науки — сепсисологии, развитие органно-системных повреждений обусловлено распространением из первичного очага инфекционного воспаления провоспалительных медиаторов с последующей их активацией в других органах/тканях под влиянием макрофагов и выделением эндогенных субстанций.
При неспособности регулирующих систем организма поддержать гомеостаз, начинает доминировать деструктивное действие цитокинов и других медиаторов, что вызывает нарушение функции и проницаемости эндотелия капилляров, развитие ДВС-синдрома и моно/полиорганной дисфункции.
Наблюдается нарушение метаболизма из-за выраженной интоксикации, нарастание процессов катаболизма (гипергликемия, гипоальбуминемия, диспротеинемия, гиповитаминоз, анемия и др.).
Классификация
Существует большое количество классификаций сепсиса в основу которых положены те или иные факторы/принципы. Рассмотрим лишь основные. Различают первичный (криптогенный сепсис) и вторичный сепсис.
Криптогенный сепсис встречается относительно редко. Как правило, криптогенный вид сепсиса связывают с аутоинфекцией (кариозными зубами, хроническим тонзиллитом или другой дремлющей инфекцией).
Вторичный сепсис является частой формой и развивается на фоне наличия гнойного очага в организме хозяина: гнойной раны, гнойного заболевания, оперативного вмешательства. Вторичный септический процесс в свою очередь, в зависимости от входных ворот инфекции подразделяется на:
- Одонтогенный сепсис – как правило, одонтогенный сепсис обусловлен различными заболеваниями со стороны зубочелюстной системы: гранулемами, кариесом, апикальным периодонтитом, околочелюстными флегмонами, периоститом, остеомиелитом челюстей и др.
- Хирургический сепсис – развивается при заносе инфекционного возбудителя в кровь из послеоперационной раны. Хирургический сепсис — один из наиболее часто встречаемых видов.
- Абдоминальный сепсис — как следствие первоначального развития деструктивного процесса в разных органах брюшной полости или забрюшинного пространства. Абдоминальный сепсис часто развивается при гнойно-некротическом деструктивном панкреатите.
- Акушерско-гинекологический сепсис — как следствие осложненных родов и абортов.
- Уросепсис – входными воротами при котором являются органы мочеполовой сферы. Уросепсис может развиваться при пиелонефритах, мочекаменной болезни и др.
- Ангиогенный сепсис — с локализацией первичного очага в сердце. Ангиогенный сепсис обусловлен абсцессами сердца, инфекционным эндокардитом.
- Неонатальный сепсис — это сепсис у новорожденных детей (ранний и поздний неонатальный сепсис).
- Плевро-легочный сепсис — развивается на фоне различных гнойных заболеваний легких: пневмонии, абсцесса легких, эмпиемы плевры и др.
- Отогенный — обусловлен воспалительными заболеваниями среднего уха.
- Кожный сепсис — источником инфекции являются гнойные заболевания кожи: ожоги, фурункулы, абсцессы, инфицированные раны и др.
По клиническому течению выделяют:
- молниеносный сепсис с генерализацией воспалительного процесса в течение 12-24 часов и летальным исходом в течение 1-2 суток;
- острый — клиническая симптоматика проявляются в течение нескольких дней и продолжительностью до 4 недель;
- подострый с продолжительностью 6-12 недель;
- рецидивирующий сепсис —протекает в виде периодических обострений и ремиссий, длительностью до 6 месяцев;
- хронический сепсис — может протекать на протяжении ряда лет; хронический сепсис протекает со слабо выраженными периодическими обострениями и длительными ремиссиями.
По анатомо-клиническим признакам:
- Септицемия — сепсис крови с отсутствием в тканях/органах гнойных очагов-метастазов.
- Септикопиемия — воспаление крови с диссеминацией возбудителей, формированием вторичных метастатических гнойных очагов со стойкой бактериемией. По фазам течения сепсиса: фазы напряжения, катаболическая, анаболическая и реабилитационная.
По этиологическому фактору различают бактериальный (пневмококковый, стафилококковый, стрептококковый и др.), вирусный, грибковый, вызванный простейшими и др.
Причины сепсиса
Сепсис — полиэтиологическое заболевание, которое могут вызывать различные патогенные/условно-патогенные микроорганизмы. К основным возбудителям сепсиса относятся:
- энтеробактерии — кишечная палочка (Escherichia coli), синегнойная палочка (Pseudomonas spp.), клебсиелла (Klebsiella spp.) и др.;
- грамположительные кокки — стафилококки (Staphylococcus aureus, Enterococcus spp., Staphylococcus epidermidis), стрептококки (Streptococcus A и B spp.);
- пневмококки (Streptococcus pneumoniae);
- неспорообразующие анаэробы (пептострептококки, пептококки и др.);
- вирусы (аденовирусная, энтеровирусная инфекция и инфекция, вызываемая респираторно-синцитиальным вирусом);
На рисунке ниже приведена этиологическая структура возбудителей сепсиса:
Этиологическая структура нозокомиальных инфекций крови
Во многих случаях причины заражения крови обусловлены смешанной — бактериально-вирусной инфекцией (микробными ассоциациями). Как правило, это гнойно-септические инфекции, вызываемые госпитальными штаммами (внутрибольничная инфекция), обладающих наряду с высокой вирулентностью выраженной полирезистентностью к целому ряду антибактериальных препаратов.
В развитии тяжелых госпитальных инфекций, все большее значение имеют грибы (Candida spp). Согласно современным данным сепсис, вызванный грамотрицательной микрофлорой, сопряжен с развитием септического шока и сопровождается более высокой смертностью, чем сепсис, обусловленный грамположительной микрофлорой (стрептококковый сепсис или пневмококковый сепсис). Также осложняют течение сепсиса и ухудшают его исход микст-формы микроорганизмов. Возбудители могут как заноситься в кровь из очагов первичной гнойной инфекции, так и попадать в кровь из окружающей среды.
Важнейшие причины (факторы), приводящие к срыву устойчивости организма к инфекционным агентам и развитию сепсиса:
- качественные и количественные свойства инфекционного возбудителя: вирулентность, массивность, генерализация процесса в организме через кровь/лимфу;
- наличие септического очага в организме человека, связанного периодически/постоянно с кровяным или лимфатическим руслом, развитие иммунодефицита.
Симптомы сепсиса
Какие симптомы при заражении крови у человека? Как таковых патогномоничных симптомов для сепсиса нет. Клиническими критериями сепсиса у взрослых, как варианта ССВО, являются:
- температура тела выше 38 °C или меньше 36 °C;
- частота дыхания 20 вдохов в минуту и более;
- тахикардия 90 ударов в минуту и более;
- лейкопения менее 4000 в 1 мкл;
- лейкоцитоз более 12000 в 1 мкл.
Симптоматика сепсиса чрезвычайно полиморфна и зависит от этиологии и возбудителя, локализации первичного очага инфекции, формы и тяжести течения заболевания. Основные симптомы сепсиса у взрослых обусловлены общей интоксикацией, локализацией метастазов и выраженностью полиорганных нарушений.
В случаях наиболее часто встречающейся острой форме сепсиса симптомы у взрослых, как правило, проявляются:
- Нарушением общего состояния и функции нервной системы, что проявляется раздражительностью, бессонницей, головной болью, помрачением/потерей сознания. Характерна повышенная потливость и периодически наступающие ознобы. Температура тела в большинстве случаев держится на высоком уровне со значительными колебаниями на протяжении дня, вечером, особенно в случаях наличия метастазов. Характерно истощение больного, у большинства происходит существенное снижение массы тела. На коже в ряде случаев появляется геморрагическая сыпь. При этом при пневмококковом сепсисе характерно появление на коже грудной клетки мелкоточечной сыпи; при стафилококковом сепсисе геморрагическая сыпь появляется на ладонной поверхности пальцев. При менингококцемии полиморфная геморрагическая сыпь появляется на лице, туловище, конечностях. Отмечается нарушения со стороны системы пищеварения: сухой, обложенный язык, отсутствие аппетита, могут присутствовать тошнота и рвота, реже упорные септические поносы.
- Практически у всех больных симптомы заражения крови проявляются поражением дыхательной системы, клинические проявления которого могут широко варьировать, начиная от влажных хрипов при аускультации и одышки до развития выраженных нарушений газообменных/негазообменных функций легких (респираторный дистресс-синдром).
- Признаки сепсиса у взрослых проявляются и нарушениями со стороны сердечно-сосудистой системы в виде не соответствующей повышению температуры тела тахикардии, уменьшении наполнения пульса, снижении артериального/венозного давления. Возможны сосудистые и трофические расстройства в виде отеков, пролежней, тромбозов, тромбофлебитов, лимфангитов. В ряде случаев сепсис может осложниться кардиомиопатией, токсическим миокардитом, развитием острой сердечно-сосудистой недостаточности.
- Ухудшением функции печени, зачастую с появлением желтухи и развитием явлений гепатита, увеличением селезенки.
- Нарушением функция почек. Отмечается микрогематурия, снижение относительной плотности мочи, альбуминурия, цилиндрурия, часто развивается олигурия (анурия).
- Со стороны крови первые признаки: лейкоцитоз со сдвигом лейкоцитарной формулы влево, анемия, ускоренная СОЭ, токсическая зернистость нейтрофилов, диспротеинемия, гипербиллирубинемия, увеличение содержания креатинина и мочевины.
Следует отметить, что первые признаки заражения крови при остром течении могут развиваться бурно и проявляется за несколько часов/суток в отличие от хронического сепсиса, для которого характерно вялое течение с малозаметными изменениями, которые протекают длительно. Для рецидивирующего сепсиса характерна периодическая смена обострений с выраженными клиническими проявлениями и ремиссий, когда заметной симптоматики сепсиса выявить не удается.
Ниже на рисунке приведены фото больных сепсисом:
Следует отметить, что наличие клинических проявлений без проведения комплекса лабораторных исследований не позволяет распознать и однозначно поставить диагноз «сепсис».
Также при сепсисе происходят характерные изменения и в первичном очаге инфекции — замедляется заживление ран, грануляции приобретают бледную окраску, становятся вялыми, кровоточащими, а дно раны покрывается участками некроза и грязно-сероватым налетом. Отделяемое из раны приобретает зловонный запах и мутный цвет.
В случаях образования метастатических очагов в различных органах и тканях, происходит наслоение дополнительной специфической симптоматики, характерной для гнойно-септического процесса конкретной локализации. Так в результате заноса инфекции в легкие развивается клиническая симптоматика абсцессов легкого, гнойного плеврита, пневмонии.
При метастазах в почки присутствует клинические симптомы пиелитов, паранефритов. При поражении головного мозга возникают абсцессы головного мозга и гнойный менингит. Появление метастатических очагов в опорно-двигательной системе проявляется симптомами остеомиелита/артрита. При метастазах в сердце — эндокардит/перикардит, в органы брюшной полости (абсцессы печени), подкожно-жировую клетчатку или мышцы — абсцессы мягких тканей и т.д.
Анализы и диагностика сепсиса

- температуру тела — более 38 °C или менее 36 °C;
- частоту дыхания — более 20 вдохов в минуту;
- сердечный ритм — более 90 ударов в минуту;
- количество лейкоцитов — более 12000 на 1 мкл или менее 4000 на 1 мкл;
- наличие в крови более 10% незрелых форм лейкоцитов.
Диагноз «сепсис» ставится при наличии ≥ 2 критериев и наличии установленного/предполагаемого инфекционного очага. Вместе с тем в ряде случаев (в частности, на фоне неинфекционного системного воспалительного ответа) эти критерии становятся низкоспецифичными и малоинформативными. Следует отметить, что микробиологическое исследование биологических сред, хотя и определяется как «золотой стандарт» обследования осложнений гнойно-септических инфекций, тем не менее, без клинико-лабораторного подтверждения считается лишь транзиторной бактериемией.
Современные алгоритмы диагностики сепсиса включают использование лабораторных маркеров, которые позволяют связать наличие в организме инфекции, оценить уровень воспалительной реакции и наличие сепсиса. К основным маркерам относятся:
- Прокальцитониновый тест (ПКТ). Уровень прокальцитонина является одним из маркеров системного воспаления (ССВР), при этом, его концентрация при тяжелых бактериальных инфекциях повышается, что позволяет дифференцировать бактериальное воспаление от не бактериального, оценивать тяжесть больного и эффективность терапевтических мероприятий. Уровень прокальцитонина в норме не превышает показатель 0,5 нг/мл. Его увеличение интервале 0,5 2,0 нг/мл сепсис не исключает, однако может свидетельствовать об обширном высвобождении провоспалительных цитокинов, обусловленном обширной травмой, ожогом большой площади тела, хирургическом вмешательстве с обширной травматизацией тканей и др. При показателе прокальцитонина на уровне, превышающим 2 нг/мл с высокой долей вероятности можно предположить развитие сепсиса, а при 10 нг/мл и более – тяжелый сепсис/септический шок (рис. ниже).
- Пресепсин маркер (P-SEP). Пресепсин-маркер относится к более чувствительным и специфическим диагностическим маркерам в диагностике сепсиса. При этом, концентрация P-SEP в плазме у инфицированных пациентов значительно выше, чем у неинфицированных. Этот биомаркер можно использовать не только для ранней диагностики сепсиса, но и для адекватной оценки его тяжести и дальнейшего прогноза. Важно и то, что при развитии сепсиса увеличение концентраций P-SEP происходит значительно быстрее, чем других маркеров сепсиса (в течение 1,5–2,0 часов после появления системного ответа организма на инфекцию).
- С-реактивный белок (СРБ). Не является специфическим маркером сепсиса. Показатель С-реактивного белка, превышающий два стандартных отклонений от среднего значения, свидетельствует о наличии воспаления.
- Интерлейкин-6 (ИЛ-6). Не специфический маркер. Его продукция существенно повышается на фоне острых воспалительных реакций различной этиологии. Мониторинг уровня ИЛ-6 в сыворотке крови важен для оценки выраженности ССВР, сепсиса и септического шока, является важнейшим ранним маркером неонатального сепсиса. Как правило, его показатели положительно коррелирует с показателями других лабораторных тестов (СРБ, Р-SEP) и тяжестью клинических проявлений.
- Маркер neutrophil CD64. Наличие на поверхности нейтрофилов гликопротеина CD64 является достоверным признаком инфекции и сепсиса с показателями чувствительности и специфичности соответственно 85 и 76% (рис. ниже).
Зависимость уровня ПКТ от тяжести воспалительного процесса
Для поиска источника инфекции могут использоваться различные инструментальные методы: рентгенографию, компьютерную томографию, УЗИ, пункцию предполагаемого абсцесса и др.
Следует отметить, что ни один из маркеров не может использоваться в отдельности и лишь комплексная оценка всех показателей в динамике в совокупности с клиническими проявлениями, данными объективного обследования (частота сердечных сокращений АД, мониторинг кислородного статуса, данными анализа крови, включающий лейкоцитарную формулу, показатели, креатинина, электролитов), бактериологическим посевом биологических жидкостей/биоптата и инструментальными исследованиями позволяет поставить диагноз.
Лечение сепсиса
Лечится ли заражение крови? Безусловно, лечится, однако эффективность лечения сепсиса определяется целым рядом фактором, в том числе и быстротой начала эмпирической антибактериальной терапии.
Как лечить сепсис? Прежде всего, пациенты с септическим шоком должны быть переведены в отделении интенсивной терапии с почасовым контролем за параметрами центральной гемодинамики, уровнем глюкозы, электролитов и лактата в крови, пульсометрией, газовым составом артериальной крови, функцией почек.
Даже при наличии незначительного первичного очага в виде гнойной раны не следует забывать о риске развития сепсиса и заниматься санацией очага самостоятельно, посещая форум о сепсисе (септический форум), где даются непрофессиональные рекомендации. Адекватное удаление инородных тел и дренирование гнойного экссудата должно осуществляться лишь в лечебном учреждении. Лечение заражение крови базируется на комплексе мероприятий и алгоритмы лечение сепсиса направлены на:
- эрадикацию микроорганизмов из кровотока;
- стабилизацию состояния пациента;
- осуществление неотложных мер в очаге инфекции (санация источника инфекции).
Эрадикация микроорганизмов из кровотока осуществляется назначением антибиотикотерапии, включающей, как минимум, два класса антибиотиков с широким спектром действия для воздействия на максимально широкий спектр патогенов, в том числе бактерий, грибов и вирусов.
Антибиотикотерапия. Назначение эмпирической внутривенной антибактериальной терапии — обязательное условие эффективности лечения и должно быть начато в течение 1 часа после выявления первых симптомов сепсиса или сразу после идентификации возбудителя. Для этиотропной терапии рекомендуется комбинированная терапия 2 или даже 3 антимикробными препаратами, например цефалоспорины в комбинации с аминогликозидами и препаратами с антианаэробной активностью или, например, монотерапия карбапенемами (имипенем, Меропенем). Однако, после комбинированной терапии переход на монотерапию возможен только после получения однозначных и достоверных результатов микробиологического исследования.
При назначении эмпирической терапии необходимо ориентироваться на вероятность присутствия той или иной группы патогенов (наиболее вероятный спектр возбудителей). Так, при высокой вероятности развития внебольничного грамположительного сепсиса рекомендуется назначать бета-лактамные антибиотики с выраженной антистафилококковой активностью (Цефазолин, Оксациллин), а при высокой вероятности развития грамположительного внутрибольничного сепсиса – гликолипидные антибиотики (Ванкомицин).
В случаях подозрения на сепсис, вызванный анаэробной инфекцией, назначается Клиндамицин или Метронидазол. Следует не забывать, что неадекватная антибиотикотерапия более чем в 2 раза превышает летальности пациентов, чем больных, получающих адекватную терапию. Длительность антибиотикотерапии решается индивидуально, составляя в среднем 10-12 дней, однако, может быть продолжена до достижения стойкой положительной динамики, стабилизации гемодинамики и купирования клинических симптомов инфекции.
Меры по стабилизации состояния пациента включают:
- В случаях нарушениях сознания — восстановление проходимости дыхательных путей. Для устранения гипокапнии и поддержания адекватного насыщения крови кислородом проводится интубация и искусственная вентиляция легких, являющаяся обязательной при развитии респираторного дистресс-синдрома, внутричерепной гипертензии.
- При снижении АД и наличии микроциркуляторных нарушений требуется быстрое восстановление объема циркулирующей крови. При этом, кровинфузионная терапия для каждого пациента должна быть индивидуальной. В большинстве случаев при необходимости восполнения внутрисосудистого объема, оптимальным выбором являются коллоиды (растворы гидроксиэтилкрахмалов: Стабизол, Гекодез, Рефортан, Хаэс-Стерил, Полигидроксиэтилкрахмал, Инфукол и др.), в то время как кристаллоиды (солевые растворы К, Mg аспарагинат, раствор Гартмана, Рингера, Мафусол) показаны преимущественно для коррекции внесосудистого дефицита жидкости. Инфузия жидкости осуществляется в объеме 500–1000 мл кристаллоидов/300–500 мл коллоидов в течение 30 мин и если АД или мочеотделение не увеличились и признаков перегрузки сосудистого русла отсутствуют инфузия повторяется. Установлено, что адекватная ранняя инфузионная терапия способствует повышению выживаемости больных с сепсисом.
- Вазопрессоры. Введение вазопрессоров начинают в случаях неэффективности инфузионной терапии (не восстанавливается перфузия органов) и АД. К препаратам выбора относятся Норадреналин и Допамин. Возможно использование вазопрессина у пациентов резистентным к высоким дозам вазопрессоров.
- Инотропы. Показаны при низком сердечном индексе (Добутамин).
- Введение других групп препаратов (кортикостероидов, иммуноглобулинов, антикоагулянтов, анальгетиков) решаются в каждом конкретном случае. У пациентов с сепсисом при остром повреждении почек показано применение методов заместительной почечной терапии.
Меры в очаге инфекции
Экстренная санация источника микробной контаминации проводится лишь после проведения всего комплекса адекватных реанимационных мероприятий. Включает обследование пациента для установления локализации источника инфекции и радикальное удаление поврежденных/некротизированных тканей, дренирование абсцессов и санацию септического очага инфекции. При этом, важно качество санации инфекционного очага (адекватное дренирование, лаваж), поскольку любые методы терапии, в том числе и антибиотики не будут эффективными при наличии гнойного содержимого (гной в крови и содержимом раны).
Механическое промывание является даже более важным, чем местное назначение антисептиков/антибиотиков. В случаях необходимости (невзирая на тяжесть состояния пациента) должно проводиться своевременное хирургическое вмешательство (санация/дренирование брюшной полости, лапаротомия, спленэктомия и др.), поскольку альтернативы хирургической тактике не существует, невзирая даже на риск развития СШ. В любом случае в очаге гноя быть не должно.
Санация в целом не ограничивается хирургической санацией, а предполагает и другие методы, например, санацию трахеобронхиального дерева с помощью фибробронхоскопии при септической пневмонии. Лишь следуя принципу тщательной санации септического очага можно предотвратить прогресс системного воспаления и повысить прогноз выживаемости.
Доктора
Лекарства
- Имипенем
- Меропенем
- Цефазолин
- Оксациллин
- Ванкомицин
- Клиндамицин
- Метронидазол
- Стабизол
- Гекодез
- Хаэс-Стерил
- Полигидроксиэтилкрахмал
- Инфукол
- Раствор Хартмана
- Раствор Рингера
- Мафусол
- Норадреналин
- Допамин
- Добутамин
Процедуры и операции
Дренирование, лаваж очага инфекции. Оперативное вмешательство по показаниям (санация/дренирование брюшной полости, лапаротомия, спленэктомия и др.) направленное на ликвидацию, как первичного очага, так и метастатических гнойных очагов.
Сепсис у детей
Сепсис является одной из основных причин летальности у детей. Особую актуальность представляет сепсис новорожденных, частота развития которого у доношенных новорожденных составляет 0,2%, а у недоношенных малышей — 1,5%. Большое значение в повышении восприимчивости к инфекции и развитию сепсиса имеет иммунологическая недостаточность у ребенка в период новорожденности, что обусловлено недостаточным количеством антител, передающихся от матери трансплацентарным путем и быстрым снижением их уровня.
Соответственно организм ребенка не в состоянии вызвать высокий своевременный каскадный иммунный ответ на инфекцию. К тому же, у ребенка имеет место выраженная дефектность бактерицидных субстанций макрофагов/нейтрофилов. Из факторов, способствующих иммунологической недостаточности новорожденных особое значение имеет наличие гипотрофии (врожденной/приобретенной) и искусственное вскармливание. К важнейшим предпосылкам развития сепсиса относятся:
- инфицирование ребенка госпитальными бактериальными штаммами;
- развитие дисбактериоза на фоне сопутствующих суперинфекций и неадекватной антибактериальной терапии.
Выделяют ранний и поздний сепсис у новорожденных детей. Ранний неонатальный сепсис – это сепсис, развившийся у детей в первые три дня жизни. Для него характерно внутриутробное инфицирование или раннее постнатальное заражение, в связи с чем, у новорожденных детей первичный гнойный очаг отсутствует, а наиболее частой формой его проявления является так называемая «внутриутробная пневмония». Источником инфекции, как правило, являются патогены, колонизирующие родовые пути матери, реже наблюдается и трансплацентарное инфицирование.
Если клиническая манифестация сепсиса (симптомы) проявляется в более поздние сроки, его относят к позднему неонатальному сепсису, при котором инфицирование ребенка происходит постнатально. Обычно присутствует первичный очаг инфекции и чаще регистрируется септикопиемия (наличие септикопиемических или метастатических, гнойно-воспалительных очагов).
Факторы риска бактериального инфицирования плода/новорожденного и генерализации бактериальной инфекции:
- Заболевания у беременной инфекционно-воспалительного генеза: кольпит, пиелонефрит, аднексит.
- Наличие инфекции у роженицы: мастит, эндометрит.
- Длительный безводный период в родах (более 6 часов).
- Инфицирование амниона («грязные» воды).
- Внебольничные роды, наследственные заболевания, пороки развития.
- Тяжелая асфиксия на фоне внутриутробной хронической гипоксии.
- Недоношенность с выраженным при рождении дефицитом массы тела.
- Ятрогенные факторы: хирургические вмешательств, аппаратная ИВЛ (интубация трахеи) длительностью более 3 суток, частая катетеризация периферических вен, длительность внутривенных инфузий.
Симптомы сепсиса у детей могут значительно варьировать. Основными клиническими признаками полиорганной недостаточности являются:
- Со стороны ЦНС: возбуждение/угнетение, судороги.
- Со стороны сердечно-сосудистой систем: бради/тахикардия, нитевидный пульс, глухость сердечных тонов, гипо/гипертензия.
- Со стороны дыхательной системы: апноэ/тахипноэ, втяжение уступчивых мест на грудной клетке.
- Со стороны ЖКТ: диарея, парез кишечника, отказ от сосания, патологическая потеря массы.
- Со стороны мочевыделительной системы: олиго-/анурия.
- Кожные покровы: бледность, сыпь, отечность, серая/желтушная окраска, склерема, цианоз, симптом «белого пятна».
У детей старше 7 дней при наличие очага инфекции и хотя бы двух признаков полиорганной недостаточности позволяет предположить сепсис даже в случаях отсутствии в крови высева микроорганизмов, а в отделениях для недоношенных детей — в диагностике сепсиса принят угрозометрический подход. При наличии серьезного инфекционно-воспалительного очага в сочетании с 1-2 признаками ПОН или системной воспалительной реакции дается заключение о высокой угрозе развития сепсиса и начинает проводиться терапия как уже при начавшемся сепсисе.
Лечение сепсиса новорожденных сочетает этиотропную терапию с патогенетической коррекцией иммунных, метаболических и органных нарушений. Стартовая антибактериальная терапия включает цефалоспорин 3-го поколения в комбинации с аминогликозидами или монотерапию карбапенемом. После уточнения возбудителя: цефалоспорин 4-го поколения (Цефепим) в комбинации с резервным аминогликозидом, например Амикацин; монотерапия — Ванкомицин. При недостаточной эффективности — антибиотики глубокого резерва (Циластатин, Имипинем). По жизненным показаниям может назначаться фторхинолон (Ципрофлоксацин).
В терапии сепсиса у детей актуально применение иммунокорригирующих средств — препаратами с доказанной безопасностью и клинической эффективностью. Иммунозаместительная терапия предусматривает введение иммуноглобулинов, интерферона человеческого лейкоцитарного, рекомбинантных интерферонов (Виферон, Неоцитотект, Пентаглобин).
Важными компонентами лечения сепсиса у новорожденных является:
- коррекция дисбактериоза (эубиотики, пребиотики);
- метаболических/гемодинамических и расстройств;
- коррекция гипер/гипо-коагуляции;
- организация рационального (приоритет грудного) вскармливания ребенка;
- частичное парентеральное питание;
- лечение сопутствующих заболеваний.
При беременности
Среди различных инфекционных осложнений распространенность сепсиса в акушерско-гинекологической практике варьирует в пределах 0,2–0,3%. Послеродовой сепсис наиболее часто (в 90% случаев), возникает на фоне эндометрита и послеродовых септических заболеваний, значительно реже — в случаях наличия мастита, раневой инфекции, инфекции мочевых путей, постинъекционного абсцесса и др.
Ведущими факторами риска сепсиса являются: мертворождение, многоплодие, хроническая сердечная/печеночная недостаточности, ВИЧ-инфекция, инфекции генитального тракта/нижних мочевыводящих путей, инфекции дыхательных путей (пневмонии, грипп), внутрибольничные инфекции, осложненное течение родов (длительный безводный промежуток, обусловленный несвоевременным излитием околоплодных вод, задержка продуктов зачатия, пролонгированные роды, хориоамнионит, многократные влагалищные исследования, акушерские операции в родах — кесарево сечение, патологическая кровопотеря, травматизация тканей родовых путей), а также гнойно-септические заболевания в послеродовом периоде: параметрит, аднексит, тромбофлебит, послеродовый эндометрит и др.
Выраженность симптомов зависит от формы клинического течения. Клиническая симптоматика манифестирует, как правило, на второй-третий день после родов признаками общей интоксикации (слабостью, потерей аппетита, тахикардией, одышкой, реже рвотой и диареей), сукровично-гнойными выделениями и температурой до 39-40 °C с большим разбросом суточной температуры и периодическими ознобами. Больные жалуются на боли в животе/молочных железах, могут отмечаться генерализованные высыпания.
При молниеносном развитии акушерского сепсиса симптоматика нарастает в течение суток, а в случаях развития острого сепсиса клиническая картина манифестирует в течение 3-4 дней. При подострой форме симптомы менее выражены, процесс развивается на протяжении 1-2 недель. Хронический сепсис характеризуется вялым течением на протяжении многих месяцев со слабо выраженной симптоматикой (головокружениями, головной болью и сонливостью, субфебрилитетом, повышенным потоотделением, иногда диареей).
Рецидивирующая форма характерна для септикопиемии и протекает с периодами обострений и ремиссии. Ухудшение состояния обусловлено образованием вторичных гнойных метастазов. При отсутствии своевременного и адекватного лечения развивается тяжёлая форма сепсиса с шоковым синдромом с сильно выраженной интоксикацией организма.
В ранней («теплой») фазе акушерского сепсиса отмечается прогрессирующая слабость, головокружение, субфебрильная температура, тахикардия, гиперемированность кожных покровов. Иногда отмечается спутанность сознания, психозы, галлюцинации, возбуждение. Длительность этой стадии варьирует от 5-8 часов до суток.
Поздняя («холодная») фаза характеризуется брадикардией, падением температуры ниже нормы, затруднением дыхания. Возбуждение и беспокойство сменяется адинамией, затемнением сознания. Развивается олигурия, кожа покрывается липким холодным потом и приобретает землистый оттенок, иногда появляется желтуха.
Лечение акушерского сепсиса проводится согласно руководства МЗ N 15-4/10/2-728 и включает санацию первичного очага инфекции с одновременным проведением эмпирической антибактериальной, детоксикационной, инфузионно-трансфузионной, иммуномодулирующей, общеукрепляющей, десенсибилизирующей, симптоматической терапии, направленной на коррекцию нарушений функции жизненно важных органов и гемостаза.
При назначении антибиотиков необходимо учитывать клинические проявления, обсемененность первичного очага инфекции и вероятный вид возбудителя сепсиса. Как правило, антибиотики используются в максимально допустимой терапевтической дозировке.
Диета при сепсисе
Сепсис относится к категории заболеваний с быстро развивающейся трофической недостаточностью, что делает нутриционную поддержку в виде (энтерального/парентерального питания) важнейшим методом в интенсивной терапии заболевания, позволяющего активно противостоять резко нарастающему истощению пациентов. Метод нутриционной поддержки определяется исходным трофологическим статусом, функциональным состоянием ЖКТ и сохранностью глотательной функции.
При развитии септического шока активная алиментация до его разрешения не проводится, выполняются лишь мероприятия по энтеральной поддержке, основными положениями которой являются:
- Предпочтение во всех случаях необходимо отдавать естественному питанию в сочетании с дополнительным приемом перорально биологически ценных сбалансированных питательных смесей (ЭПС), содержащих не менее 6–10 г белка/100 мл и энергии 200 ккал/100 мл и пищевые волокна (Фортикер, Нутридринк компакт протеин, Эншур-2, Суппортан и др.), которые могут назначаться в качестве дополнительного питание к лечебному рациону (по 200 мл 2–3 раз/сут в виде отдельного приема).
- При невозможности питания больного естественным путем, а также в случаях резкого снижения объема алиментации и сохранности пищеварительной функции назначается зондовое питание с предпочтением назогастрального доступа (через нос) введения питательных смесей. При необходимости зондового питания сроком более 4 недель показано наложение стомы. Для зондового питания рекомендуются стандартные полимерные гиперкалорические, готовые к употреблению жидкие питательные смеси: Нутризон Энергия, Нутризон, Нутрикомп Энергия, Фрезубин Энергия, Нутризон Энергия с пищевыми волокнами, Суппортан и др.
- В основе назначения искусственного питания (парентерального/зондового) лежат показания, когда больные по разным причинам не могут питаться в достаточном количестве естественным путем или не могут/не должны/не хотят получать пероральное питание. Парентеральное питание назначается лишь в условиях невозможности использования энтерального доступа, а также невозможности обеспечения достаточной алиментации другими доступными методами.
Профилактика
Профилактика сепсиса в целом включает:
- Устранение/своевременное адекватное лечение очагов гнойной инфекции (ран, ожогов, локальных инфекционно-воспалительных процессов).
- Тщательное соблюдении требований асептики/антисептики при выполнении операций и лечебно-диагностических манипуляций.
- Сокращения времени пребывания пациентов в стационаре и выявление пациентов высокого риска развития сепсиса.
- Предупреждение развития госпитальной инфекции, что достигается регулярными дезинфекционными мероприятиями, мониторингом внутрибольничной флоры в каждом конкретном отделении лечебного учреждения, определением чувствительности микрофлоры к антибиотикам, эффективной политикой применения антибактериальных препаратов.
- Проведение вакцинации против менингококковой, пневмококковой инфекции и др.
Профилактические мероприятия послеродового сепсиса включают:
- Своевременное лечение воспалительных/гнойно-септических заболеваний.
- Борьбу с внебольничными вмешательствами (криминальными абортами, домашними родами, внутриматочными/вагинальными манипуляциями).
- Рациональную превентивную антибиотикотерапию при проведении оперативных вмешательств.
Профилактические мероприятия сепсиса новорожденных включают:
- Своевременное выявление и санацию инфекций мочеполовой сферы беременной, тщательный полноценный гигиенических уход за новорожденным, естественное вскармливание новорожденного.
- Соблюдение противоэпидемических мероприятий в отделениях новорожденных родильных домов.
Последствия сепсиса крови и осложнения
Последствия заражение крови зависят от формы сепсиса, наличия местатических очагов, проводимого лечения и включают нарушения функции сердечно сосудистой и дыхательной системы, почечные осложнения, нарушения в системе свертывания крови, расстройства метаболизма, неврологические осложнения, токсическое поражение ЦНС и другие.
Прогноз
Общая смертность пациентов, у которых развился септический шок, варьирует в пределах 40-50%. Как правило, высокие показатели смертности обусловлены несвоевременностью начала интенсивной терапии (более 6 часов после предположительного диагноза). В большинстве случаев септический шок в сочетании с выраженной полиорганной недостаточностью приводит к необратимым изменениям в организме и смерти.
Список источников
- Козлов В. К. Сепсис: этиология, иммунопатогенез, концепция современной иммунотерапии. СПб: Диалект, 2008. 296 с.
- Володин И.И., Антонов А.Г., Байбарина Е.Н. Сепсис новорожденных и доказательная медицинская практика — новый подход и повышение качества помощи // Педиатрия. 2003. № 5. С. 56-59.
- Савельев В. С., Гельфанд Б. Р. Сепсис: классификация, клинико-диагностическая концепция, лечение. М.: ООО Издательство «Медицинское информационное агентство», 2013. 360 с.
- Руднов В. А., Кулабухов В. В. Сепсис-3: Обновленные ключевые положения, потенциальные проблемы и дальнейшие практические шаги. Вестник анестезиологии и реаниматологии. 2016; 13 (4): 4–11.
- Международное руководство по управлению сепсисом и септическим шоком (Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016)
Сепсис — общая гнойная инфекция, развивающаяся вследствие проникновения и циркуляции в крови различных возбудителей и их токсинов. Клиническая картина сепсиса складывается из интоксикационного синдрома (лихорадки, ознобов, бледно-землистой окраски кожных покровов), тромбогеморрагического синдрома (кровоизлияний в кожу, слизистые, конъюнктиву), метастатического поражения тканей и органов (абсцессов различных локализаций, артритов, остеомиелитов и др.). Подтверждением сепсиса служит выделение возбудителя из культуры крови и локальных очагов инфекции. При сепсисе показано проведение массивной дезинтоксикационной, антибактериальной терапии, иммунотерапии; по показаниям – хирургическое удаление источника инфекции.
Общие сведения
Сепсис (заражение крови) – вторичное инфекционное заболевание, вызванное попаданием патогенной флоры из первичного локального инфекционного очага в кровяное русло. Сегодня ежегодно в мире диагностируется от 750 до 1,5 млн. случаев сепсиса. По статистике, чаще всего сепсисом осложняются абдоминальные, легочные и урогенитальные инфекции, поэтому данная проблема наиболее актуальная для общей хирургии, пульмонологии, урологии, гинекологии. В рамках педиатрии изучаются проблемы, связанные с сепсисом новорожденных. Несмотря на использование современных антибактериальных и химиотерапевтических препаратов, летальность от сепсиса остается на стабильно высоком уровне – 30-50%.
Сепсис
Причины сепсиса
Важнейшими факторами, приводящими к срыву противоинфекционной резистентности и развитию сепсиса, выступают:
- со стороны макроорганизма — наличие септического очага, периодически или постоянно связанного с кровяным или лимфатическим руслом; нарушенная реактивность организма
- со стороны инфекционного возбудителя – качественные и количественные свойства (массивность, вирулентность, генерализация по крови или лимфе)
Ведущая этиологическая роль в развитии большинства случаев сепсиса принадлежит стафилококкам, стрептококкам, энтерококкам, менингококкам, грамотрицательной флоре (синегнойной палочке, кишечной палочке, протею, клебсиелле, энтеробактер), в меньшей степени — грибковым возбудителям (кандидам, аспергиллам, актиномицетам).
Выявление в крови полимикробных ассоциаций в 2,5 раза увеличивает уровень летальности больных сепсисом. Возбудители могут попадать в кровь из окружающей среды или заноситься из очагов первичной гнойной инфекции.
Велико значение внутрибольничной инфекции: ее росту способствует широкое применение инвазивных диагностических процедур, иммуносупрессивных лекарственных препаратов (глюкокортикоидов, цитостатиков). В условиях иммунодефицита, на фоне травмы, операционного стресса или острой кровопотери инфекция из хронических очагов беспрепятственно распространяется по организму, вызывая сепсис. Развитию сепсиса более подвержены недоношенные дети, больные, длительно находящиеся на ИВЛ, гемодиализе; онкологические, гематологические пациенты; больные сахарным диабетом, ВИЧ-инфекцией, первичными и вторичными иммунодефицитами.
Патогенез
Механизм развития сепсиса многоступенчатый и очень сложный. Из первичного инфекционного очага патогены и их токсины проникают в кровь или лимфу, обуславливая развитие бактериемии. Это вызывает активацию иммунной системы, которая реагирует выбросом эндогенных веществ (интерлейкинов, фактора некроза опухолей, простагландинов, фактора активации тромбоцитов, эндотелинов и др.), вызывающих повреждение эндотелия сосудистой стенки. В свою очередь, под воздействием медиаторов воспаления активизируется каскад коагуляции, что в конечном итоге приводит к возникновению ДВС-синдрома. Кроме этого, под влиянием высвобождающихся токсических кислородсодержащих продуктов (оксида азота, перекиси водорода, супероксидов) снижается перфузия, а также утилизация кислорода органами. Закономерным итогом при сепсисе является тканевая гипоксия и органная недостаточность.
Сепсис
Классификация
Формы сепсиса классифицируются в зависимости от локализации первичного инфекционного очага. На основании этого признака различают первичный (криптогенный, эссенциальный, идиопатический) и вторичный сепсис. При первичном сепсисе входные ворота обнаружить не удается. Вторичный септический процесс подразделяется на:
- хирургический – развивается при заносе инфекции в кровь из послеоперационной раны
- акушерско-гинекологический – возникает после осложненных абортов и родов
- уросепсис – характеризуется наличием входных ворот в отделах мочеполового аппарата (пиелонефрит, цистит, простатит)
- кожный – источником инфекции служат гнойные заболевания кожи и поврежденные кожные покровы (фурункулы, абсцессы, ожоги, инфицированные раны и др.)
- перитонеальный (в т. ч. билиарный, кишечный) – с локализацией первичных очагов в брюшной полости
- плевро-легочный – развивается на фоне гнойных заболеваний легких (абсцедирующей пневмонии, эмпиемы плевры и др.)
- одонтогенный – обусловлен заболеваниями зубочелюстной системы (кариесом, корневыми гранулемами, апикальным периодонтитом, периоститом, околочелюстными флегмонами, остеомиелитом челюстей)
- тонзиллогенный – возникает на фоне тяжелых ангин, вызванных стрептококками или стафилококками
- риногенный – развивается вследствие распространения инфекции из полости носа и придаточных пазух, обычно при синуситах
- отогенный — связан с воспалительными заболеваниями уха, чаще гнойным средним отитом.
- пупочный – встречается при омфалите новорожденных
По времени возникновения сепсис подразделяется на ранний (возникает в течение 2-х недель с момента появления первичного септического очага) и поздний (возникает позднее двухнедельного срока). По темпам развития сепсис может быть молниеносным (с быстрым развитием септического шока и наступлением летального исхода в течение 1-2 суток), острым (длительностью 4 недели), подострым (3-4 месяца), рецидивирующим (продолжительностью до 6 месяцев с чередованием затуханий и обострений) и хроническим (продолжительностью более года).
Сепсис в своем развитии проходит три фазы: токсемии, септицемии и септикопиемии. Фаза токсемии характеризуется развитием системного воспалительного ответа вследствие начала распространения микробных экзотоксинов из первичного очага инфекции; в этой фазе бактериемия отсутствует. Септицемия знаменуется диссеминацией возбудителей, развитием множественных вторичных септических очагов в виде микротромбов в микроциркуляторном русле; наблюдается стойкая бактериемия. Для фазы септикопиемии характерно образование вторичных метастатических гнойных очагов в органах и костной системе.
Симптомы сепсиса
Симптоматика сепсиса крайне полиморфна, зависит от этиологической формы и течения заболевания. Основные проявления обусловлены общей интоксикацией, полиорганными нарушениями и локализацией метастазов.
В большинстве случаев начало сепсиса острое, однако у четверти больных наблюдается так называемый предсепсис, характеризующийся лихорадочными волнами, чередующимися с периодами апирексии. Состояние предсепсиса может не перейти в развернутую картину заболевания в том случае, если организму удается справиться с инфекцией. В остальных случаях лихорадка принимает интермиттирующую форму с выраженными ознобами, сменяющимися жаром и потливостью. Иногда развивается гипертермия постоянного типа.
Состояние больного сепсисом быстро утяжеляется. Кожные покровы приобретают бледновато-серый (иногда желтушный) цвет, черты лица заостряются. Могут возникать герпетические высыпания на губах, гнойнички или геморрагические высыпания на коже, кровоизлияния в конъюнктиву и слизистые оболочки. При остром течении сепсиса у больных быстро возникают пролежни, нарастает обезвоживание и истощение.
В условиях интоксикации и тканевой гипоксии при сепсисе развиваются полиорганные изменения различной степени тяжести. На фоне лихорадки отчетливо выражены признаки нарушения функций ЦНС, характеризующиеся заторможенностью или возбуждением, сонливостью или бессонницей, головными болями, инфекционными психозами и комой. Сердечно-сосудистые нарушения представлены артериальной гипотонией, ослаблением пульса, тахикардией, глухостью сердечных тонов. На этом этапе сепсис может осложниться токсическим миокардитом, кардиомиопатией, острой сердечно-сосудистой недостаточностью.
На происходящие в организме патологические процессы дыхательная система реагирует развитием тахипноэ, инфаркта легкого, респираторного дистресс-синдрома, дыхательной недостаточности. Со стороны органов ЖКТ отмечается анорексия, возникновение «септических поносов», чередующихся с запорами, гепатомегалии, токсического гепатита. Нарушение функции мочевыделительной системы при сепсисе выражается в развитии олигурии, азотемии, токсического нефрита, ОПН.
В первичном очаге инфекции при сепсисе также происходят характерные изменения. Заживление ран замедляется; грануляции становятся вялыми, бледными, кровоточащими. Дно раны покрывается грязно-сероватым налетом и участками некрозов. Отделяемое приобретает мутный цвет и зловонный запах.
Метастатические очаги при сепсисе могут выявляться в различных органах и тканях, что обусловливает наслоение дополнительной симптоматики, свойственной гнойно-септическому процессу данной локализации. Следствием заноса инфекции в легкие служит развитие пневмонии, гнойного плеврита, абсцессов и гангрены легкого. При метастазах в почки возникают пиелиты, паранефриты. Появление вторичных гнойных очагов в опорно-двигательной системе сопровождается явлениями остеомиелита и артрита. При поражении головного мозга отмечается возникновение церебральных абсцессов и гнойного менингита. Возможно наличие метастазов гнойной инфекции в сердце (перикардит, эндокардит), мышцах или подкожной жировой клетчатке (абсцессы мягких тканей), органах брюшной полости (абсцессы печени и др.).
Осложнения сепсиса
Основные осложнения сепсиса связаны с полиорганной недостаточностью (почечной, надпочечниковой, дыхательной, сердечно-сосудистой) и ДВС-синдромом (кровотечения, тромбоэмболии).
Тяжелейшей специфической формой сепсиса является септический (инфекционно-токсический, эндотоксический) шок. Он чаще развивается при сепсисе, вызванном стафилококком и грамотрицательной флорой. Предвестниками септического шока служат дезориентация больного, видимая одышка и нарушение сознания. Быстро нарастают расстройства кровообращения и тканевого обмена. Характерны акроцианоз на фоне бледных кожных покровов, тахипноэ, гипертермия, критическое падение АД, олигурия, учащение пульса до 120-160 уд. в минуту, аритмия. Летальность при развитии септического шока достигает 90%.
Сепсис 1
Диагностика сепсиса
Распознавание сепсиса основывается на клинических критериях (инфекционно-токсической симптоматике, наличии известного первичного очага и вторичных гнойных метастазов), а также лабораторных показателях (посев крови на стерильность).
Вместе с тем, следует учитывать, что кратковременная бактериемия возможна и при других инфекционных заболеваниях, а посевы крови при сепсисе (особенно на фоне проводимой антибиотикотерапии) в 20-30% случаев бывают отрицательными. Поэтому посев крови на аэробные и анаэробные бактерии необходимо проводить минимум трехкратно и желательно на высоте лихорадочного приступа. Также производится бакпосев содержимого гнойного очага. В качестве экспресс-метода выделения ДНК возбудителя сепсиса используется ПЦР. В периферической крови отмечается нарастание гипохромной анемии, ускорение СОЭ, лейкоцитоз со сдвигом влево.
Дифференцировать сепсис необходимо от лимфогранулематоза, лейкемии, брюшного тифа, паратифов А и В, бруцеллеза, туберкулеза, малярии и других заболеваний, сопровождающихся длительной лихорадкой.
Лечение сепсиса
Пациенты с сепсисом госпитализируются в отделение интенсивной терапии. Комплекс лечебных мероприятий включает в себя антибактериальную, дезинтоксикационную, симптоматическую терапию, иммунотерапию, устранение белковых и водно-электролитных нарушений, восстановление функций органов.
С целью устранения источника инфекции, поддерживающего течение сепсиса, проводится хирургическое лечение. Оно может заключаться во вскрытии и дренировании гнойного очага, выполнении некрэктомии, вскрытии гнойных карманов и внутрикостных гнойников, санации полостей (при абсцессе мягких тканей, флегмоне, остеомиелите, перитоните и др.). В некоторых случаях может потребоваться резекция или удаление органа вместе с гнойником (например, при абсцессе легкого или селезенки, карбункуле почки, пиосальпинксе, гнойном эндометрите и др.).
Борьба с микробной флорой предполагает назначение интенсивного курса антибиотикотерапии, проточное промывание дренажей, местное введение антисептиков и антибиотиков. До получения посева с антибиотикочувствительностью терапию начинают эмпирически; после верификации возбудителя при необходимости производится смена противомикробного препарата. При сепсисе для проведения эмпирической терапии обычно используются цефалоспорины, фторхинолоны, карбапенемы, различные комбинации препаратов. При кандидосепсисе этиотропное лечение проводится амфотерицином В, флуконазолом, каспофунгином. Антибиотикотерапия продолжается в течение 1-2 недель после нормализации температуры и двух отрицательных бакпосевов крови.
Дезинтоксикационная терапия при сепсисе проводится по общим принципам с использованием солевых и полиионных растворов, форсированного диуреза. С целью коррекции КОС используются электролитные инфузионные растворы; для восстановления белкового баланса вводятся аминокислотные смеси, альбумин, донорская плазма. Для борьбы с бактериемией при сепсисе широко используются процедуры экстракорпоральной детоксикации: плазмаферез, гемосорбция, гемофильтрация. При развитии почечной недостаточности применяется гемодиализ.
Иммунотерапия предполагает использование антистафилококковой плазмы и гамма-глобулина, переливание лейкоцитарной массы, назначение иммуностимуляторов. В качестве симптоматических средств используются сердечно-сосудистые препараты, анальгетики, антикоагулянты и др. Интенсивная медикаментозная терапия при сепсисе проводится до стойкого улучшения состояния больного и нормализации показателей гомеостаза.
Прогноз и профилактика
Исход сепсиса определяется вирулентностью микрофлоры, общим состоянием организма, своевременностью и адекватностью проводимой терапии. К развитию осложнений и неблагоприятному прогнозу предрасположены больные пожилого возраста, с сопутствующими общими заболеваниями, иммунодефицитами. При различных видах сепсиса летальность составляет 15-50%. При развитии септического шока вероятность летального исхода крайне высока.
Профилактические меры в отношении сепсиса состоят в устранении очагов гнойной инфекции; правильном ведении ожогов, ран, локальных инфекционно-воспалительных процессов; соблюдении асептики и антисептики при выполнении лечебно-диагностических манипуляций и операций; предупреждении госпитальной инфекции; проведении вакцинации (против пневмококковой, менингококковой инфекции и др.).
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу — его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
Место, через которое возбудитель проникает в организм, называется воротами инфекции.
Первичный гнойно-воспалительный очаг может возникать прямо у места входных ворот или во внутренних органах. В норме иммунные клетки организма быстро очищают кровь от чужеродных агентов. Но при ослабленном иммунитете инфекционный процесс распространяется и генерализуется, формируются вторичные септические очаги. Бактерии, «путешествуя» по крово- и лимфотоку, активно производят токсины, что приводит к интоксикации и может стать причиной инфекционно-токсического (септического) шока.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
По течению болезни выделяют:
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
Последние два вида обычно связаны с наличием хронического гнойно-воспалительного очага (эндокардит, пиелонефрит, тонзиллит и т.д.). Кроме того, некоторые классификации выделяют еще рецидивирующий сепсис.
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм > 10%.
2. Развитие синдрома системного воспалительного ответа на внедрение микроорганизмов при наличии двух и более признаков ССВО и обнаруженного очага инфекции. Другими словами, это системная воспалительная реакция, которая вызвана доказанной инфекцией.
3. Тяжелый сепсис – сепсис, сочетающийся с полиорганной дисфункцией по двум и более органам, снижением артериального давления <90 мм рт. ст., нарушениями кровотока в тканях и органах (может проявляться, например, уменьшением выделения мочи из-за гипоксии почек, нарушением сознания из-за недостаточного кровоснабжения головного мозга и др.).
4. Септический шок – тяжелый сепсис с артериальной гипотензией < 90 мм рт. ст., признаками снижения кровотока в тканях и органах, которые не устраняются с помощью адекватной инфузионной терапии и требуют применения вазопрессоров (препаратов, оказывающих сосудосуживающий эффект и способствующих повышению среднего артериального давления). При их неэффективности диагностируется рефрактерный септический шок.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Симптомы сепсиса
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно — за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Главные органы-мишени при сепсисе – легкие, почки, желудочно-кишечный тракт.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Диагностика сепсиса
Для постановки диагноза «сепсис» необходимо наличие установленного или предполагаемого очага инфекционного процесса и два или более признака синдрома системной воспалительной реакции.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
К каким врачам обращаться
Сепсис — это жизнеугрожающее состояние, которое требует незамедлительного оказания квалифицированной медицинской помощи. Диагностикой и лечением сепсиса традиционно занимаются
врачи-хирурги
вместе с инфекционистами и
терапевтами
.
Сепсис не лечат дома, помощь больному должна быть оказана в отделении интенсивной терапии, в хирургическом, терапевтическом или инфекционном стационаре.
Лечение сепсиса
Медицинские работники стараются как можно быстрее выявить возможный источник инфекции, подвергают его радикальной хирургической обработке и обеспечивают непрерывное удаление продуктов разрушения и микробной флоры из очага. Антибиотики назначаются эмпирически до выделения и определения возбудителя, т.е. врачи предполагают наиболее вероятный возбудитель и начинают антимикробную терапию, исходя из накопленного опыта. После подтверждения возбудителя терапия может быть скорректирована. Эффективные антимикробные препараты должны быть назначены внутривенно в первый час с момента постановки диагноза.
Коррекция гемодинамики и устранение шока является важнейшим аспектом лечения осложнений сепсиса. Пациенту внутривенно вводят растворы, восполняющие объем циркулирующей крови, при необходимости используются вазопрессоры.
Ряд пациентов с острой дыхательной недостаточностью вследствие синдрома системного воспалительного ответа и полиорганной недостаточности нуждаются в респираторной поддержке — инвазивной вентиляции легких.
Полиорганная недостаточность при сепсисе, как правило, сопровождается гиперметаболизмом – повышенным обменом веществ. В этой ситуации организм закрывает потребности в энергии за счет разрушения собственных клеточных структур (аутоканнибализм), что только усугубляет органную дисфункцию и усиливает эндотоксикоз (внутреннюю интоксикацию). Поэтому важно обеспечить адекватную питательную поддержку пациентам с сепсисом.
Важной составляющей лечения сепсиса является профилактика тромбоза глубоких вен и тромбоэмболических осложнений, а также стресс-язв и желудочно-кишечных кровотечений.
Осложнения
Осложнениями и причинами смерти при сепсисе могут стать инфекционно-токсический шок, органная и полиорганная недостаточность (почечная, дыхательная, сердечно-сосудистая), отек мозга, синдром диссеминированного внутрисосудистого свертывания, анемия, тромбоэмболия сосудов жизненно важных органов.
Профилактика сепсиса
Профилактикой сепсиса служит своевременное и полноценное лечение инфекций, вызвавших образование первичных очагов — ранняя правильная хирургическая обработка ран, своевременное лечение местных гнойных процессов и инфекционных заболеваний (особенно бактериальной этиологии).
Источники:
- Сепсис: классификация, клинико-диагностическая концепция и лечение / Под ред. акад. РАН Б.Р. Гельфанда. — 4-е изд., доп. и перераб. — Москва: ООО «Медицинское информационное агентство». – 2017.
- Тактика ведения пациентов с сепсисом и септическим шоком в многопрофильном стационаре. Ю.Ю. Сапичева и др. // Уч. Пособие. – М., — МОНИКИ. – 2015.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.