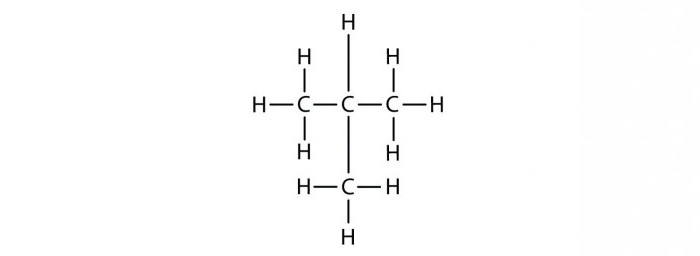
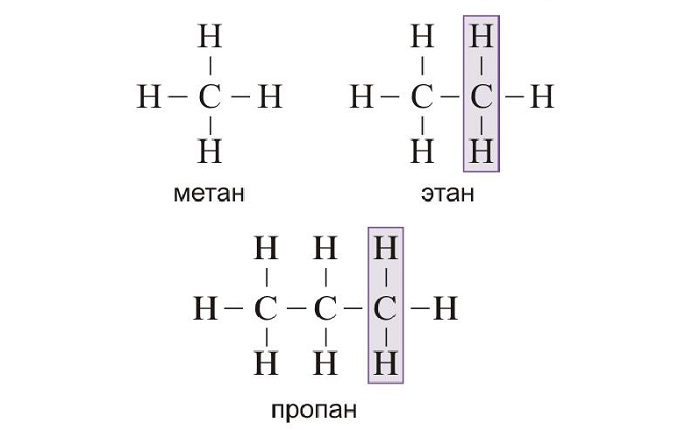
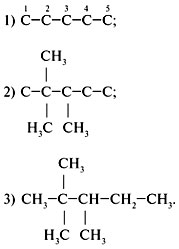
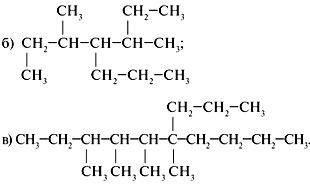
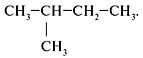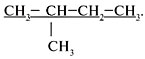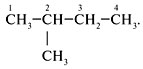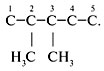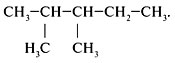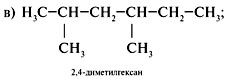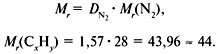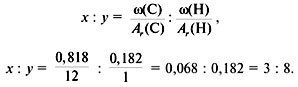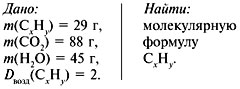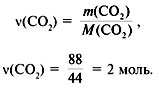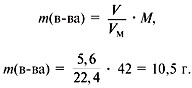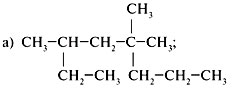Прежде чем анализировать, как составлять изомеры предельных углеводородов, выявим особенности данного класса органических веществ.
Насыщенные углеводороды
В органической химии выделяется множество классов CxHy. У каждого есть своя общая формула, гомологический ряд, качественные реакции, применение. Для насыщенных углеводородов класса алканов характерны одинарные (сигма) связи. Общая формула данного класса органических веществ CnH2n+2. Этим объясняются основные химические свойства: замещение, горение, окисление. Для парафинов не характерны присоединение, так как связи в молекулах этих углеводородов одинарные.
Изомерия
Такое явление, как изомерия объясняет многообразие органических веществ. Под изомерией принято понимать явление, при котором существует несколько органических соединений, имеющих одинаковый количественный состав (число атомов в молекуле), но различное расположение их в молекуле. Получаемые вещества называют изомерами. Они могут быть представителями нескольких классов углеводородов, а потому отличаются химическими свойствами. Разное соединение в молекуле алканов атомов С приводит к возникновению структурной изомерии. Как составлять изомеры алканов? Существует определенный алгоритм, согласно которому можно изобразить структурные изомеры данного класса органических веществ. Появляется подобная возможность только с четырех углеродных атомов, то есть, с молекулы бутана С4Н10.
Разновидности изомерии
Для того чтобы понять, как составлять формулы изомеров, важно иметь представление о ее видах. При наличии внутри молекулы одинаковых атомов в равном количестве, располагающихся в пространстве в разном порядке, идет речь о пространственной изомерии. Иначе ее называют стереоизомерией. В подобной ситуации применения одних только структурных формул будет явно недостаточно, потребуется использование специальных проекционных или пространственных формул. Предельные углеводороды, начиная с H3C–СН3 (этана), имеют различные пространственные конфигурации. Это обусловлено вращением внутри молекулы по связи С–С. Именно простая σ-связь создает конформационную (поворотную) изомерию.
Структурная изомерия парафинов
Поговорим о том, как составлять изомеры алканов. Класс имеет структурную изомерию, то есть, атом углерода образует разные цепи. Иначе возможность изменения положения в цепи атомов углерода называют изомерией углеродного скелета.
Изомеры гептана
Итак, как оставлять изомеры для вещества, имеющего состав C7H16? Для начала можно расположить все атомы углерода в одну длинную цепочку, добавить для каждого определенное число атомов С. Сколько? Учитывая, что валентность углерода равна четырем, у крайних атомов будет по три атома водорода, а у внутренних – по два. Полученная молекула имеет линейное строение, такой углеводород называют н – гептаном. Буква «н» подразумевает прямой углеродный скелет в данном углеводороде.
Теперь меняем расположение углеродных атомов, «укорачивая» при этом прямую углеродную цепочку в C7H16. Составить изомеры можно в развернутом либо сокращенном структурном виде. Рассмотрим второй вариант. Сначала один атом С расположим в виде радикала метил в разных положениях.
Данный изомер гептана имеет следующее химическое название: 2-метилгексан. Теперь «передвигаем» радикал к следующему углеродному атому. Полученный предельный углеводород называется: 3-метилгексан.
Если мы будем далее передвигать радикал, нумерация будет начинаться с правой стороны (ближе к началу располагается углеводородный радикал), то есть, мы получим такой изомер, который у нас уже есть. Поэтому думая над тем, как составлять формулы изомеров для исходного вещества, попробуем сделать скелет еще «короче».
Оставшиеся два углерода можно представить в виде двух свободных радикалов — метил.
Расположим сначала их у разных углеродов, входящих в главную цепь. Назовем полученный изомер -2,3 диметилпентан.
Теперь оставим один радикал на том же месте, а второй перенесем к следующему углеродному атому главной цепи. Данное вещество называется 2,4 диметилпентан.
Теперь расположим углеводородные радикалы у одного углеродного атома. Сначала у второго, получим 2,2 диметилпентан. Затем у третьего, получив 3,3 диметилпентан.
Теперь оставляем в основной цепи четыре атома углерода, оставшиеся три используем в качестве радикалов метил. Располагаем их следующим образом: два у второго атома С, один – у третьего углерода. Называем полученный изомер: 2,2, 3 триметилбутан.
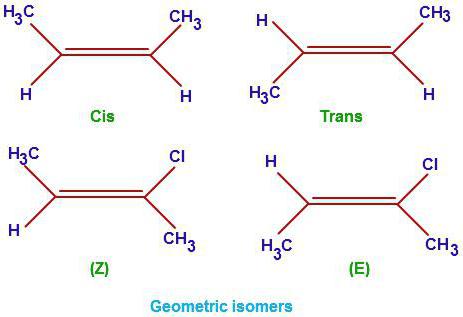
На примере гептана мы разобрали, как правильно составлять изомеры для предельных углеводородов. На фото представлены примеры структурных изомеров для бутена6 его хлорпроизводных.
Алкены
Данный класс органических веществ имеет общую формулу CnH2n. Помимо насыщенных связей С-С в данном классе есть также двойная связь. Именно она определяет основные свойства данного ряда. Поговорим о том, как оставлять изомеры алкенов. Попробуем выявить их отличия от предельных углеводородов. Помимо изомерии главной цепи (структурные формулы) для представителей данного класса органических углеводородов также характерны еще три разновидности изомеров: геометрические (цис- и трансформы), положения кратной связи, а также межклассовая изомерия (с циклоалканами).
Изомеры C6H12
Попробуем выяснить, как составить изомеры c6h12, учитывая тот факт, что вещество с данной формулой может принадлежать сразу к двум классам органических веществ: алкенам, циклоалканам.
Для начала подумаем, как составлять изомеры алкенов, если есть двойная связь в молекуле. Ставим прямую углеродную цепочку, поставим кратную связь после первого углеродного атома. Попробуем не только составить изомеры с6н12, но и назвать вещества. Данное вещество — гексен – 1. Цифрой указывается положение в молекуле двойной связи. При ее передвижении по углеродной цепочке, получаем гексен -2, а также гексен — 3
Теперь порассуждаем, как составлять изомеры для данной формулы, меняя количество атомов в главной цепи.
Для начала укоротим углеродный скелет на один углеродный атом, его будет рассматривать в качестве радикала метил. Двойную связь оставим после первого атома С. Полученный изомер по систематической номенклатуре будет иметь следующее название: 2 метилпентен – 1. Теперь передвигаем углеводородный радикал по главной цепи, оставив положение двойной связи неизменным. Данный непредельный углеводород разветвленного строения называют 3 метилпентен -1.
Возможен без изменения основной цепи и положения двойной связи еще один изомер: 4 метилпентен -1.
Для состава C6H12 можно попробовать переместить двойную связь из первого во второе положение, не преобразуя саму главную цепочку. Радикал при этом будет передвигать по углеродному скелету, начиная со второго атома С. Данный изомер имеет название 2 метилпентен-2. Кроме того, можно поместить радикал CH3 третьего атома углерода получив при этом 3 метилпентен-2
Если поместить радикал у четвертого углерода атома в данной цепи, образуется еще одно новое вещество непредельный углеводород с извилистым углеродным скелетом – 4 метилпентен-2.
При дальнейшем сокращении числа С в главной цепи, можно получить еще один изомер.
Двойную связь оставим после первого углеродного атома, а два радикала поставим к третьему атому С основной цепи, получаем 3,3 диметилутен-1.
Теперь поставим радикалы у соседних углеродных атомов, не меняя положения двойной связи, получим 2,3 диметилбутен-1. Попробуем, не меняя размер главной цепи, передвинуть двойную связь во второе положение. Радикалы при этом мы может поставить только у 2 и 3 атомов С, получив 2,3 диметилбутен-2.
Других структурных изомеров для данного алкена нет, любые попытки их придумать приведут к нарушению теории строения органических веществ А. М. Бутлерова.
Пространственные изомеры C6H12
Теперь выясним, как составлять изомеры и гомологи с точки зрения пространственной изомерии. Важно понимать, что цис- и трансформы алкенов возможны только для положения двойной связи 2 и 3.
При нахождении в одной плоскости углеводородных радикалов, образуется цис – измер гексена -2, а при расположении радикалов в разных плоскостях, транс-форма гексена – 2.
Межклассовые изомеры C6H12
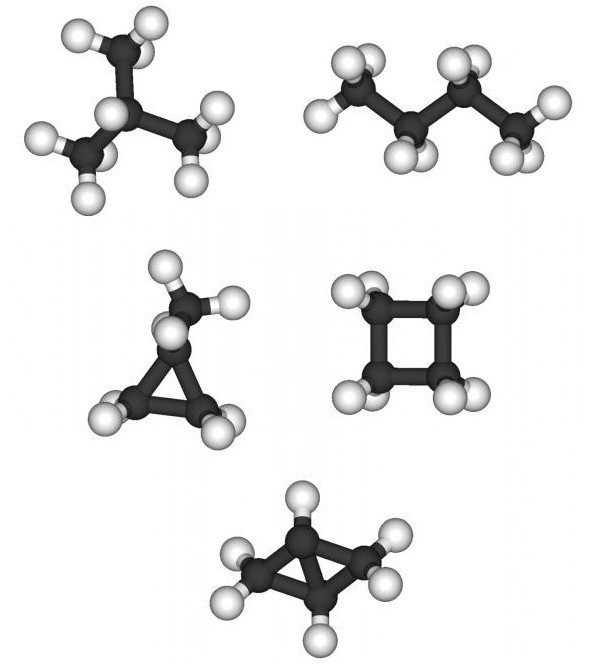
Рассуждая над тем, как составлять изомеры и гомологи, нельзя забывать и о таком варианте, как межклассовая изомерия. Для непредельных углеводородов ряда этилена, имеющих общую формулу CnH2n, такими изомерами являются циклоалканы. Особенностью данного класса углеводородов является наличие циклической (замкнутой) структуры при насыщенных одинарных связях между атомами углерода. Можно составить формулы циклогексана, метилциклопентана, диметилциклобутана, триметилциклопропана.
Заключение
Органическая химия многогранна, загадочна. Количество органических веществ превышает в сотни раз число неорганических соединений. Данный факт легко объясняется существованием такого уникального явления, как изомерия. Если в одном гомологическом ряду располагаются сходные по свойствам и строению вещества, то при изменении положения атомов углерода в цепи, появляются новые соединения, названные изомерами. Только после появления теории химического строения органических веществ удалось классифицировать все углеводороды, понять специфику каждого класса. Одно из положений данной теории, непосредственно касается явления изомерии. Великий русский химик сумел понять, объяснить, доказать, что именно от расположения углеродных атомов зависят химические свойства вещества, его реакционаня активность, практическое применение. Если сравнивать количество изомеров, образуемых предельными алканами и непредельными алкенами, лидируют, безусловно, алкены. Объясняется это тем, что в их молекулах есть двойная связь. Именно она позволяет этому классу органических веществ образовывать не только алкены разного вида и строения, но и вести речь о меклассовой изомерии с циклоалканами.
При изучении органической химии, отличающейся сложностью своих закономерностей, первое и основное, что следует понять — свойства и законы гомологических рядов.
Гомология, гомологи, гомологический ряд — определения и примеры
Гомология — химическое явление, при котором соединения отличаются друг от друга на определённое количество групп, обладают сходной характеристикой и проявляют похожие свойства.
Гомологический ряд — последовательность однотипных органических соединений, каждое из последующих имеет с предыдущим определённую гомологическую разность. При этом свойства веществ, состоящих в рядах, то есть гомологов, изменяются с определённой закономерностью.
Например, если говорить о гомологическом ряде алкинов, он состоит из следующих гомологов:
-
этин — C2H2;
-
пропин — C3H4;
-
бутин — C4H6;
-
пентин — C5H8 и т. д.
Гомологический ряд алканов в таблице
Алканы — ациклические предельные углеводороды:
-
всеобщая формула алканов — СnH2n+2;
-
названия веществ имеют суффикс -ан-.
Алканы обладают следующими свойствами:
-
в последовательности гомологического ряда происходят изменения агрегатных состояний веществ с газообразного на жидкое и на твёрдое;
-
нерастворимы в воде, но могут растворяться в неполярных растворителях;
-
используются в промышленности (метан — топливо, пропан — автомобильное топливо, бутан — сырье для производства каучука, пропан и бутан — балонные газы).
|
Метан |
СН4 |
|
Этан |
С2Н6 |
|
Пропан |
С3Н8 |
|
Бутан |
С4Н10 |
|
Пентан |
С5Н12 |
|
Гексан |
С6Н14 |
При изучении алканов стоит обращать внимание на их изомеры. Например, структурным изомером бутана является метилпропан, а пентана — метилбутан.
Алканы могут вступать в следующие реакции:
-
Горение в кислороде: СН4 + 2О2 = СО2 + 2Н2О.
-
Замещение с галогенами: CH4 + Cl2 = CH3Cl + HСl.
-
Разложение при высокой температуре: СН4 = C + 2H2.
Гомологический ряд алкенов в таблице
Алкены — углеводороды, имеющие ациклический непредельный характер.
Краткая характеристика:
-
общая формула — CnH2n;
-
имеют суффикс -ен-.
Алкены обладают следующими свойствами:
-
не способны растворяться в воде, но полностью растворяются при взаимодействии с органическими растворителями;
-
имеют очень высокую температуру плавления и кипения;
-
применяются в промышленности для синтеза таких важных соединений, как фенола, полипропилена, стирола, ацетона, глицерина и других.
|
Этилен |
C2H4 |
|
Пропен |
C3H6 |
|
Бутен |
C4H8 |
|
Пентен |
C5H10 |
|
Гексен |
C6H12 |
Алкены участвуют в следующих химических реакциях:
-
Горение в кислороде: C2H4 + 3O2 = 2CO2 + H2O.
-
Галогенирование (присоединение к галогенам): CH2=CH2 + Cl2 = Cl-CH2-CH2-Cl.
-
Присоединение к водороду (гидрирование): CH2=CH-CH3 + H2 = CH3-CH2-CH3.
-
Гидратация (присоединение к воде): CH2=CH2 + H2O = CH3-CH2OH.
-
Полимеризация: nCH2=CH2 = (-CH2-CH2-) * n.
Гомологический ряд альдегидов
Альдегиды — органические вещества, имеющие в своём составе группу -CHO.
Делятся на насыщенные и алифатические насыщенные, общая молекулярная формула первых — СnH2nO, вторых — СnH2n+1CHO соответственно.
Названия составляются с помощью суффикса -аль-.
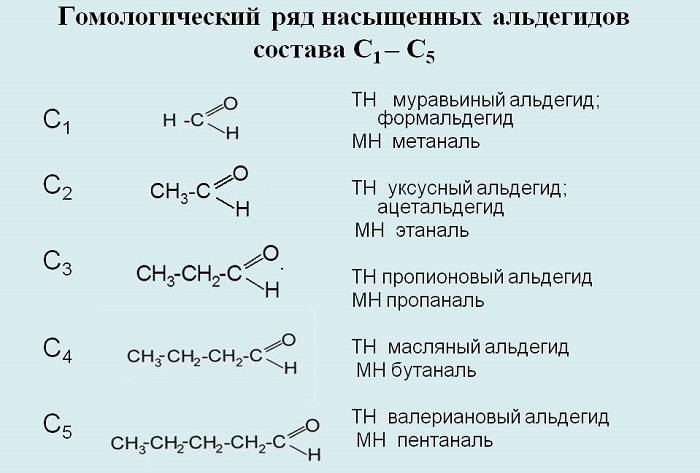
К примерам альдегидов относятся метаналь, этаналь, пропаналь, бутаналь, пентаналь, гексаналь и так далее.
Альдегиды принимают участие в следующих реакциях:
-
Присоединение воды: R-CH = O + H2O = R-CH(OH)-OH.
-
Присоединение спиртов: CH3-CH = O + C2H5OH = CH3-CH(OH)-O-C2H5.
-
Присоединение аминов: C6H5CH = O + H2NC6H5 = C6H5CH = NC6H5 + H2O.
-
Восстановление водородом: R-CH = O + H2 = R—CH2-OH.
Альдегиды обладают следующими свойствами:
-
низшие представители класса имеют резкий запах;
-
в гомологическом ряду происходит изменение агрегатных состояний от жидкого до твёрдого;
-
используются в лекарственной промышленности, парфюмерии и т. д.
Хоть органическая химия и требует внимательного изучения, совсем необязательно полностью зазубривать все классы веществ. Намного проще для понимания и качественного запоминания обращать внимание именно на закономерности изменения свойств и характеристик ближайших соединений, следуя плану.
И.М. ХАРЧЕВА
Учебно-методическое пособие
по органической химии
Тема 2.
Предельные углеводороды.
Циклопарафины
Знать: общие формулы алканов и
циклоалканов, строение алканов, гомологический
ряд алканов, изомерию и номенклатуру алканов и
циклоалканов, их физические и химические
свойства; получение, применение и механизмы
реакций замещения алканов и циклоалканов.
Уметь: давать названия алканам и
циклоалканам, составлять их формулы по названиям
веществ; составлять структурные формулы
гомологов и изомеров для предложенного алкана
или циклоалкана; составлять уравнения реакций,
характеризующих свойства алканов, циклоалканов
и галогеналканов; составлять структурные
формулы галогеналканов, называть их, графически
обозначать распределение электронной плотности
в молекулах; решать расчетные задачи на
нахождение молекулярной формулы вещества по
массовым долям элементов и по массе (объему)
продуктов сгорания.
Основные понятия: алканы, циклоалканы,
тетраэдрическое строение молекул, общая формула,
гомологи, гомологическая разность, взаимное
влияние атомов, заместитель, изомерия положения
заместителей, индукционный эффект, цепная
реакция, простейшая формула, истинная формула.
Алгоритм 2.1. Номенклатура алканов
Задание 1. Назвать вещество по
систематической номенклатуре:
Решение
1. Выбрать главную цепь (наиболее длинная цепь
углеродных атомов):
2. Пронумеровать атомы углерода в главной цепи с
того конца, к которому ближе стоит заместитель
(углеводородный радикал):
Последовательно назвать:
1) номер углеродного атома, с которым связан
радикал;2) радикал;
3) углеводород, которому соответствует длинная
цепь: 2-метилбутан.
Задание 2. Составить структурную
формулу углеводорода по его названию
«2,3-диметилпентан».
Решение
Анализируем название углеводорода, начиная с
конца слова.
1. «Пентан» – в главной цепи находится пять
атомов углерода:
2. «Диметил» – в состав углеводорода входят два
радикала CH3.
3. «2, 3-» – радикалы находятся у 2-го и 3-го
углеродных атомов:
4. Дописать недостающие атомы водорода,
соблюдая четырехвалентность атома углерода:
Алгоритм 2.2. Гомологи и изомеры
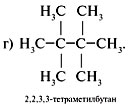
Задание. Для 2,2,3-триметилпентана
составить формулы двух гомологов и двух
изомеров.
Решение
1. Составить формулу исходного вещества,
используя задание 2 алгоритма 2.1:
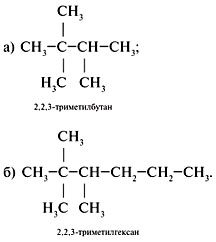
2. Составить формулы г о м о л о г о в, сохраняя
строение (разветвление 2,2,3-триметил-). Для этого
уменьшить главную цепь на группу СН2
(гомологическая разность) – пример а или
увеличить главную цепь на СН2 – пример б:
3. Составляя формулы и з о м е р о в, изменить
строение, сохраняя состав исходного
углеводорода (C8H18), примеры в, г:
Алгоритм 2.3. Решение расчетных задач на
вывод
молекулярной формулы вещества по массовым долям
элементов
Задача 1. Найти молекулярную формулу
вещества, содержащего 81,8% углерода и 18,2% водорода.
Относительная плотность вещества по азоту равна
1,57.
Решение
1. Записать условие задачи.
2. Вычислить относительную молекулярную массу Mr(CхHy)
по относительной плотности:
3. Найти индексы х и y по отношению :
4. Записать простейшую формулу: С3Н8.
Проверка: Мr(C3H8) = 44,
следовательно, C3H8 – истинная
формула.
Задача 2. Найти молекулярную формулу
предельного углеводорода, массовая доля
углерода в котором 83,3%.
Решение
1. Записать условие задачи.
2. Найти массовую долю водорода:
(Н) = 100%
– 83,3% = 16,7%.
3. Найти индексы и простейшую формулу для
углеводорода CхHy:
следовательно, простейшая формула – C2H5.
4. Найти истинную формулу. Поскольку общая
формула алканов СnH2n+2, то
истинная формула – С4Н10.
Алгоритм 2.4. Решение расчетных задач
на вывод
молекулярной формулы вещества по массе (объему)
продуктов сгорания
Задача 1. При сжигании 29 г углеводорода
образовалось 88 г углекислого газа и 45 г воды,
относительная плотность вещества по воздуху
равна 2. Найти молекулярную формулу углеводорода.
Решение
1. Записать условие задачи.
2. Найти относительную молекулярную массу
вещества:
Mr = Dвозд•Мr(возд.),
Mr(CхHy)= 2•29
= 58.
3. Найти количество вещества образовавшегося
оксида углерода(IV):
4. Найти количество вещества углерода в
сожженном веществе:
(C) =
(CO2) = 2 моль.
5. Найти количество вещества воды:
(H2O)
= 45/18 = 2,5 моль.
6. Найти количество вещества водорода в
сожженном веществе:
(H) = 2
(H2O),
(H) = 2,5•2 =
5 моль.
7. Найти простейшую формулу углеводорода:
(C) :
(Н) = 2 : 5,
следовательно, простейшая формула – С2Н5.
8. Найти истинную формулу углеводорода:
Мr(C2H5) = 29,
Mr (CхHy) = 58,
следовательно, истинная формула – C4H10.
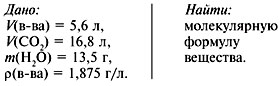
Задача 2. При сжигании 5,6 л (н.у.)
газообразного органического вещества было
получено 16,8 л (н.у.) углекислого газа и 13,5 г воды.
Масса 1 л исходного вещества при н.у. равна 1,875 г.
Найти его молекулярную формулу.
Решение
1. Записать условие задачи.
2. Найти молекулярную массу вещества из
пропорции:
1 л газа – 1,875 г,
22,4 л – m г.
Отсюда m = 42 г, M = 42 г/моль.
3. Найти количество вещества углекислого газа и
углерода:
(CO2)
= 16,8/22,4 = 0,75 моль,
(C) = 0,75
моль.
4. Найти количества веществ воды и водорода:
(H2O)
= 13,5/18 = 0,75 моль,
(H) = 0,75•2
= 1,5 моль.
5. Найти сумму масс углерода и водорода:
m(C) + m(H) = 0,75•12 +1,5•1 = 10,5 г.
6. Найти массу сожженного вещества:
Следовательно, вещество содержит только
углерод и водород.
7. Найти простейшую формулу углеводорода CхHy:
(C) :
(H) = 0,75 : 1,5 = 1 : 2,
следовательно, простейшая формула – СН2.
8. Найти истинную формулу углеводорода:
Mr(CH2) = 14,
Mr(в-ва) : Mr(CH2) =
42 : 14 = 3,
следовательно, истинная формула – С3Н6.
Контрольные вопросы
1. Какие углеводороды называют предельными?
2. Строение метана.
3. Физические свойства алканов.
4. Виды изомерии алканов и циклоалканов.
5. Причины инертности алканов.
6. Какие типы химических реакций характерны
для алканов, циклоалканов и галогеналканов?
7. Какова последовательность замещения
атомов водорода на галоген в алканах, содержащих
более двух углеродных атомов?
8. Каков механизм реакции замещения?
9. Каковы способы получения алканов,
галогеналканов и циклоалканов?
10. Дайте определения следующим понятиям: гомологи,
изомеры, заместитель, электронный эффект,
электронная плотность связи, индуктивный эффект,
электронодоноры, электроноакцепторы.
Задания для самоконтроля
1. Назвать предельные углеводороды:
2. Составить структурную формулу
2,4,5,5-тетраметил-3-этилоктана. Указать все
первичные, вторичные, третичные и четвертичные
углеродные атомы.
3. Составить структурные формулы трех
углеводородов, содержащих четвертичный
углеродный атом, выбирая из первых семи членов
ряда алканов С1–С7. Назвать эти
углеводороды.
4. Привести структуры и названия продуктов
взаимодействия следующих алканов с хлором (в
мольном соотношении 1:1):
а) пропан;
б) 2,2-диметилбутан;
в) 2,3-диметилбутан.
5. Написать уравнения реакций, которые нужно
провести для осуществления следующих
превращений:
CH3COONa CH4
CH3Br
C2H6
CO2
CO
CH4
C3H8.
6. Привести уравнения реакций получения и
названия дигалогеналканов, необходимых для
получения следующих соединений:
а) 1,2-диметилциклобутан;
б) пропилциклобутан;
в) метилциклопропан.
7. Органическое вещество содержит 84,21%
углерода и 15,79% водорода. Плотность паров
вещества по воздуху 3,93. Определить формулу
вещества.
Ответ. С8Н18.
8. Алкан имеет плотность паров по воздуху
4,414. Определить формулу алкана.
Ответ. С9Н20.
9. При сгорании 3,6 г алкана получили 5,6 л
оксида углерода(IV) (н.у.). Какие объемы кислорода и
воздуха затратились на эту реакцию?
Ответ. 8,96 л О2 и 42,67 л воздуха.
10. Углеводород содержит 82,76% углерода и 17,24%
водорода (по массе). При монохлорировании этот
углеводород образует два изомерных алкилхлорида
– первичный и третичный. Определить строение
исходного углеводорода.
Ответ. 2-метилпропан.
Онлайн-урок: Структурная формула органических соединений, изомеры, гомологи.
Вещества в органической химии принято записывать в виде структурных формул, именно они позволяют понимать, как именно связаны между собой атомы, сколько связей образует тот или иной атом. Уметь правильно записывать органические вещества, а так же давать им названия – это важный навык, который приобретается на курсе по органической химии в 9-10 классах на начальных этапах обучения.
Молекулярная формула органического вещества показывает качественный и количественный состав (С2Н6), то есть число атомов каждого элемента в молекуле, то структурная формула показывает последовательность соединения атомов в молекуле, дает представление о взаимном расположении атомов в молекуле друг относительно друга, дает понимание химического строения вещества.
Для правильного составления структурных формул нужно знать валентности атомов в молекуле, рассмотрим основные из них:
1. атом углерода (С) в органической химии всегда четырехвалентен, это означает, что он образует 4 связи с другими атомами:
2. атом кислорода (О) имеет валентность равную двум, значит, образует 2 связи с другими атомами:
3. атом водорода одновалентен, образует одну связь с другими атомами
4. азот – трехвалентен, три связи с другими атомами
Рассмотрим одни из главных базовых понятий в органической химии – это правило гомологических рядов, приведем примеры гомологов и изомеров, опираясь на теорию химического строения веществ. Гомологи – это вещества, имеющие сходные химические свойства и строение, которые относятся к одному классу веществ, отличаются они друг от друга по составу только на гомологическую разность, то есть на одну или несколько групп (-CH2-).
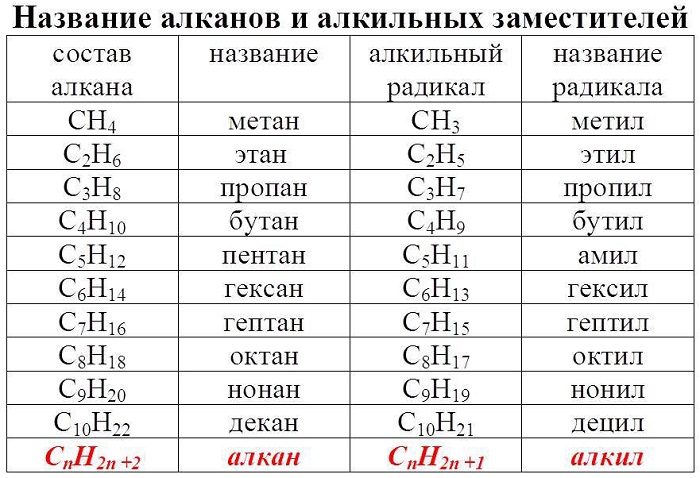
На начальных этапах изучения органической химии важно не только понимать кто такие гомологи, но и запомнить гомологический ряд алканов (предельных углеводородов), так как именно знание этих веществ дает возможность легко называть вещества из других классов. При запоминании алканов, обратите внимание на то, какой корень в названии соответствует какому количеству углерода в молекуле.
Для более точного понимания определений гомологи и гомологический ряд рассмотрим структурные формулы предельных углеводородов (помним, что атом углерода в органической химии четырехвалентен, а зачет образует 4 химических связи с другими атомами):
В данном гомологическом ряду все молекулы отличаются друг от друга на гомологическую разность, которая выделена жирным цветом. Записывая вещества в молекулярном виде, мы так же можем заметить, что в формулы отличаются на (СН2). Прибавляя каждый раз к формуле вещества, например, пропана гомологическую разность мы получаем формулу следующего представителя этого гомологического ряда, в данном случае ряда метана (алканов, предельных углеводородов). Гомологом пропана (C3H8) является бутан (C4H10).
Изомеры – это вещества, которые имеют одинаковый качественный и количественный состав, но имеющие разное строение и свойства. Другими словами, вещества имеют те же самые атомы в том же количестве, но соединены друг с другом они по-разному.
Например, бутан, имеющий линейное строение, то есть n-бутан (нормальный бутан) и i-бутан (изобутан). Часто в названиях веществ линейного строения опускают слово «нормальный». Качественный и количественный состав у них одинаковый, но атомы соединены по-разному, следовательно, это два совершенно разных вещества, которые по отношению друг к другу являются структурными изомерами.
Классификация органических соединений
В основу классификации органических веществ положены различия в строении углеродных цепей. В соответствии с этим все органические вещества делятся на ациклические и циклические.
Ациклические (алифатические) – соединения с открытой (незамкнутой) цепью углеродных атомов.
Ациклические соединения, в свою очередь, подразделяются на
-
Предельные (алканы),
-
Непредельные (алкены, алкины, диеновые углеводороды)
Циклические – соединения, в молекулах которых углеродные атомы замкнуты в кольцо.
-
Карбоциклические – если цикл образован только углеродными атомами,
-
Гетероциклические – если в состав цикла помимо углеродных атомов входят атомы других химических элементов (азота, кислорода, серы)
Карбоциклические соединения, в свою очередь, подразделяются алициклические (циклоалканы) и ароматические (соединения, содержащие в составе молекулы одно или несколько бензольных колец).
Классификация органических соединений по строению углеродной цепи представлена в следующей таблице.
В учебнике «Фоксфорд»
Углерод соединяется друг с другом одинарными и кратными связями (двойными и тройными), образуя прямые, разветвлённые и замкнутые цепи.
А) Прямая (неразветвлённая) цепь:
CH3 – CH2 – CH2 – CH3
СH2 = CH – CH2 – CH3
CH ≡ C – CH2 – CH3
CH2 = CH – CH = CH2
Б) Разветвлённая цепь:
К циклическим относятся карбоциклические – содержащие в цикле только атомы углерода и гетероциклические соединения – содержащие в цикле кроме атомов углерода атомы других элементов – кислорода, азота и др.
Функциональные производные углеводородов
Функциональная группа – структурный фрагмент молекулы, единый для конкретного гомологического ряда и определяющий характерные химические свойства данного класса соединений.
( -R или -СnH2n+1) — это углеводородный радикал, частица, образующаяся при отрыве атома водорода от молекулы предельного углеводорода (алкана)
Например,
-СН3 метил; -С2Н5 этил.
Среди многообразия органических соединений можно выделить группы веществ, которые сходны по химическим свойствам и отличаются друг от друга на группу -СН2.
Гомологи – это соединения, сходные по химическим свойствам, состав которых отличается друг от друга на одну или несколько групп -СН2.
Гомологи, расположенные в порядке возрастания их относительной молекулярной массы, образуют гомологический ряд.
Гомологическая разность – это группы -СН2.
Примером гомологического ряда может служить ряд предельных углеводородов (алканов).
Простейший его представитель – метан СН4.
Формула любого последующего гомолога может быть получена прибавлением к формуле предыдущего углеводорода гомологической разности.
Состав молекул всех членов гомологического ряда может быть выражен одной общей формулой, например, СnН2n+2, где n – число атомов углерода.
Гомологические ряды могут быть построены для всех классов органических соединений. Зная свойства одного из членов гомологического ряда, можно сделать выводы о свойствах других представителей того же ряда. Это обусловливает важность понятия гомологии при изучении органической химии.
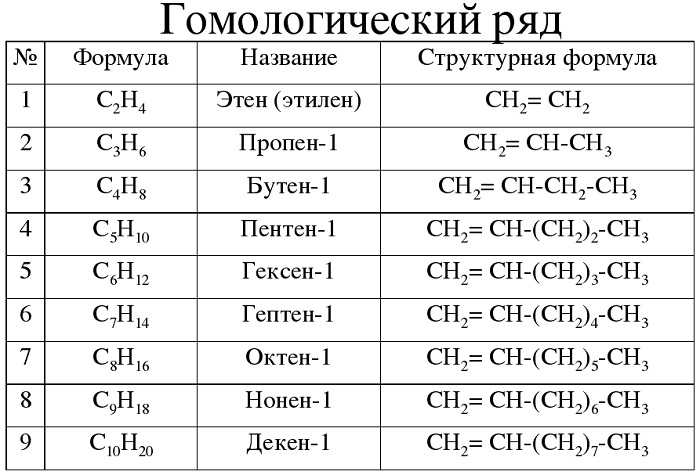
Примеры гомологических рядов алканов
Примеры гомологических рядов спиртов и альдегидов
Комитет образования и науки Курской области
Областное бюджетное образовательное учреждение
среднего профессионального образования
«Железногорский горно-металлургический колледж»

Бильдина Е. А.
Методические указания для студентов при написании формул и названий органических соединений и их гомологов
2018
ОДОБРЕНА
цикловой комиссией
требованиями
общеобразовательных дисциплин
Протокол заседания комиссии
№ от
Председатель
цикловой комиссии
___________Н.Г. Заносова
Автор _____________ Е.А.Бильдина
преподаватель химии и биологии
Рецензенты: _____________ А.С. Илюшин
Директор МОУ Средняя школа №7
Учитель химии
_____________ Н.А. Иванова
преподаватель химии
РЕЦЕНЗИЯ
на методическую разработку «Методические указания для студентов при написании формул и названий органических соединений и их гомологов»
преподавателя ФГОУ СПО ЖГМК Е.А.Бильдина
Представленная на рецензию методическая разработка предназначена для студентов при написании формул и названий органических соединений и их гомологов. В работе представлены рекомендации для выполнения различных заданий.
Данная методическая разработка поможет студентам правильнее и более эффективно выполнить полученные задания. В работе представлены указания для написания формул всех классов органических соединений, их названий и правильного написания изомеров.
Студенты при помощи данной методической разработки быстрее смогут понять, как правильно написать формулу органического вещества и назвать его.
Директор МОУ Средняя школа №7 А.С. Илюшин.
Преподаватель химии Н.А. Иванова.
ПОЯСНИТЕЛЬНАЯ ЗАПИСКА
Данная разработка «Методические указания для студентов при написании формул и названий органических соединений и их гомологов» предназначена для студентов при выполнении заданий по органической химии.
В работе представлены рекомендации для выполнения различных заданий. Пособие помогает наиболее эффективно выполнить задания.
Целью данной методической разработки является: развитие самостоятельной работы, логическое мышление, активизацию познавательной деятельности, способность анализировать и делать выводы. Кроме того, данная методическая разработка научит студентов как быстро и правильно называть органические вещества, составлять их формулы, строить изомеры.
1.Написние названий различных органических веществ.
-
Номенклатура алканов.
Алканы (предельные углеводороды) -это органические вещества в которых каждый атом углерода соединен одинарными связями с четырьмя другими атомами.
Общая формула – СпН2п+2
Простейший алкан – СН4 – метан, его гомологический ряд представлен в приложении А.
Для того чтобы дать названия алканам нужно выполнить следующие правила:
|
правило |
пример |
|
1. в формуле выбираем самую длинную углеводородную цепочку. |
СН3-СН2-СН-СН2-СН-СН3 | | СН3 СН3 |
|
2. нумеруем выбранную цепочку с того края, где ближе ответвление |
6 5 4 3 2 1 СН3-СН2-СН-СН2-СН-СН3 | | СН3 СН3 |
|
3.записываем цифры, под которыми стоят ответвления: -если несколько одинаковых радикалов, то перечисляем все цифры, под которыми они стоят; -если одинаковые радикалы стоят под одним и тем же атомом углерода, то его номер указываем столько раз, сколько радикалов под ним стоит; — если радикалы разные, то номер каждого указываем по отдельности |
6 5 4 3 2 1 СН3-СН2-СН-СН2-СН-СН3 | | СН3 СН3 2,4-…. |
|
4. Записываем названия радикалов: — если радикалов несколько, то используем греческое числительное: Ди- 2 Три – 3 Тетро – 4 — название радикалов можно смотреть в приложении Б |
6 5 4 3 2 1 СН3-СН2-СН-СН2-СН-СН3 | | СН3 СН3 2,4- диметил… |
|
5.Называем длинную цепь углерода в зависимости от того, сколько в ней атомов углерода. |
6 5 4 3 2 1 СН3-СН2-СН-СН2-СН-СН3 | | СН3 СН3 2,4-диметилгексан |
1.2Номенклатура алкенов.
Алкены – непредельные углеводороды, в молекуле которых имеется одна двойная связь.
Общая формула – СпН2п
Простейший алкен – С2Н4 –этен (этелен), его гомологический ряд представлен в приложении В.
Для того чтобы дать названия алкенам нужно выполнить следующие правила:
|
правило |
пример |
|
1. в формуле выбираем самую длинную углеводородную цепочку. |
СН3-СН2-СН=С-СН2-СН3 | | C2H5 CН3 |
|
2. нумеруем выбранную цепочку с того края, где ближе двойная связь |
1 2 3 4 5 6 СН3-СН2-СН=С-СН2-СН3 | | C2H5 CН3 |
|
3.записываем цифры, под которыми стоят ответвления: -если несколько одинаковых радикалов, то перечисляем все цифры, под которыми они стоят; -если одинаковые радикалы стоят под одним и тем же атомом углерода, то его номер указываем столько раз, сколько радикалов под ним стоит; — если радикалы разные, то номер каждого указываем по отдельности |
1 2 3 4 5 6 СН3-СН2-СН=С-СН2-СН3 | | C2H5 CН3 4-…. -5-…… |
|
4. Записываем названия радикалов: — если радикалов несколько, то используем греческое числительное: Ди- 2 Три – 3 Тетро – 4 — название радикалов можно смотреть в приложении Б |
1 2 3 4 5 6 СН3-СН2-СН=С-СН2-СН3 | | C2H5 CН3 4-этил-5-метил… |
|
5.Называем длинную цепь углерода в зависимости от того, сколько в ней атомов углерода + -ен. |
1 2 3 4 5 6 СН3-СН2-СН=С-СН2-СН3 | | C2H5 CН3 4- этил-5-метилгексен-… |
|
6.В конце названия ставится номер того атома, после которого стоит двойная связь. |
1 2 3 4 5 6 СН3-СН2-СН=С-СН2-СН3 | | C2H5 CН3 4- этил-5-метилгексен-3 |
1.3 Номенклатура алкинов.
Алкины – непредельные углеводороды, в молекуле которых присутствует одна тройная связь.
Общая формула – СпН2п-2
Простейший алкин – С2Н2 –этин (ацетилен), его гомологический ряд представлен в приложении Г.
Для того чтобы дать названия алкинам нужно выполнить следующие правила:
|
правило |
пример |
|
1. в формуле выбираем самую длинную углеводородную цепочку. |
СН3-СН-С≡С-СН2-СН3 | | СН3 CН3 |
|
2. нумеруем выбранную цепочку с того края, где ближе тройная связь |
1 2 3 4 5 6 7 СН3-СН-С≡С-СН2-СН2-СН3 | | СН3 CН3 |
|
3.записываем цифры, под которыми стоят ответвления: -если несколько одинаковых радикалов, то перечисляем все цифры, под которыми они стоят; -если одинаковые радикалы стоят под одним и тем же атомом углерода, то его номер указываем столько раз, сколько радикалов под ним стоит; — если радикалы разные, то номер каждого указываем по отдельности |
1 2 3 4 5 6 7 СН3-СН-С≡С-СН2-СН2-СН3 | | СН3 CН3 2,5 –… |
|
4. Записываем названия радикалов: — если радикалов несколько, то используем греческое числительное: Ди- 2 Три – 3 Тетро – 4 — название радикалов можно смотреть в приложении Б |
1 2 3 4 5 6 7 СН3-СН-С≡С-СН2-СН2-СН3 | | СН3 CН3 2,5 –диметил… |
|
5.Называем длинную цепь углерода в зависимости от того, сколько в ней атомов углерода + -ин |
1 2 3 4 5 6 7 СН3-СН-С≡С-СН2-СН2-СН3 | | СН3 CН3 2,5 –диметилгептин-… |
|
6.В конце названия ставится номер того атома, после которого стоит тройная связь |
1 2 3 4 5 6 7 СН3-СН-С≡С-СН2-СН2-СН3 | | СН3 CН3 2,5 –диметилгептин-3 |
1.4Номенклатура алкодиенов.
Алкодиены – непредельные углеводороды, в молекуле которых присутствуют две двойные связи.
Общая формула – СпН2п-2
Простейший алкодиен – С3Н4 –пропадиен, его гомологический ряд представлен в приложении Д.
Для того чтобы дать названия алкодиенам нужно выполнить следующие правила:
|
правило |
пример |
|
1. в формуле выбираем самую длинную углеводородную цепочку. |
СН2=СН-СН2-СН=СН-СН-СН3 | C2H5 |
|
2. нумеруем выбранную цепочку с того края, где ближе двойная связь |
1 2 3 4 5 6 7 8 СН2=СН-СН2-СН=СН-СН-СН3 | C2H5 |
|
3.записываем цифры, под которыми стоят ответвления: -если несколько одинаковых радикалов, то перечисляем все цифры, под которыми они стоят; -если одинаковые радикалы стоят под одним и тем же атомом углерода, то его номер указываем столько раз, сколько радикалов под ним стоит; — если радикалы разные, то номер каждого указываем по отдельности |
1 2 3 4 5 6 7 8 СН2=СН-СН2-СН=СН-СН-СН3 | C2H5 7-… |
|
4. Записываем названия радикалов: — если радикалов несколько, то используем греческое числительное: Ди- 2 Три – 3 Тетро – 4 — название радикалов можно смотреть в приложении Б |
1 2 3 4 5 6 7 8 СН2=СН-СН2-СН=СН-СН-СН3 | C2H5 7-этил… |
|
5.Называем длинную цепь углерода в зависимости от того, сколько в ней атомов углерода + -адиен |
1 2 3 4 5 6 7 8 СН2=СН-СН2-СН=СН-СН-СН3 | C2H5 7-этилоктадиен… |
|
6.В конце названия ставится номера тех атомов, после которых стоят двойные связи |
1 2 3 4 5 6 7 8 СН2=СН-СН2-СН=СН-СН-СН3 | C2H5 7-этилоктадиен -1,5 |
1.5 Номенклатура спиртов.
Спирты — органические вещества, молекулы которых содержат гидроксильные группы.
Общая формула спиртов – R-OH
Простейший представитель спиртов – СН3ОН – метиловый спирт, его гомологический ряд представлен в приложении Е.
Для того чтобы дать названия спиртам нужно выполнить следующие правила:
|
правило |
формула |
|
1. в формуле выбираем самую длинную углеводородную цепочку. |
СН3-СН-СН2-СН-СН2-ОН | | СН3 С2Н5 |
|
2. нумеруем выбранную цепочку с того края, где ближе гидроксогруппа |
5 4 3 2 1 СН3-СН-СН2-СН-СН2-ОН | | СН3 С2Н5 |
|
3.записываем цифры, под которыми стоят ответвления: -если несколько одинаковых радикалов, то перечисляем все цифры, под которыми они стоят; -если одинаковые радикалы стоят под одним и тем же атомом углерода, то его номер указываем столько раз, сколько радикалов под ним стоит; — если радикалы разные, то номер каждого указываем по отдельности |
5 4 3 2 1 СН3-СН-СН2-СН-СН2-ОН | | СН3 С2Н5 2-…-4…. |
|
4. Записываем названия радикалов: — если радикалов несколько, то используем греческое числительное: Ди- 2 Три – 3 Тетро – 4 — название радикалов можно смотреть в приложении Б |
5 4 3 2 1 СН3-СН-СН2-СН-СН2-ОН | | СН3 С2Н5 2-этил-4-метил…. |
|
5.Называем длинную цепь углерода в зависимости от того, сколько в ней атомов углерода + -ол |
5 4 3 2 1 СН3-СН-СН2-СН-СН2-ОН | | СН3 С2Н5 2-этил-4-метилпентанол-.. |
|
6.В конце названия ставится номер того атома, после которого стоит гидроксогруппа |
5 4 3 2 1 СН3-СН-СН2-СН-СН2-ОН | | СН3 С2Н5 2-этил-4-метилпентанол-1 |
|
7. Если гидроксогрупп несколько, то указываются все номера атомов, возле которых они находятся и добавляется греческое числительное: Ди- 2 Три – 3 Оно ставится перед окончанием — ол |
СН3-СН-СН-СН3 | | ОН ОН Бутандиол-2,3 |
1.6Номенклатура фенолов.
Фенолы – это гидроксильные соединения, в которых гидроксильная группа соединена непосредственно с атомом углерода бензольного кольца (С6Н5-)
ОН


1.Атомы нумеруют сверху по часовой стрелке.
2.Затем записывают цифры, под которыми стоят радикалы.
3.Называют радикалы, если нужно используются греческие числительные.
4. Если фенол двухатомный (т.е. содержит две гидроксогруппы), то название его зависит от расположения гидроксогрупп.

| | |


-ОН
|
OH
пара- орта- мета-
1.7 Номенклатура простых эфиров
Простые эфиры – органические соединения, имеющие в своем составе два радикала соединенные атомом кислорода.
Общая формула – R-O-R1, где – R и R1 – одинаковые или разные радикалы.
-
Названия простых эфиров складываются из названия радикалов (приложение Б), и слова «эфир».
-
Если радикалы в эфире одинаковые, то добавляем числительное ди-
Например, СН3-О-СН3 диметиловый эфир.
1.8 Номенклатура альдегидов.
Альдегиды – это кислородосодержащие органические вещества, которые имеют в своем составе карбонильную группу.
Общая формула альдегидов – R- C=О
|
H
Простейший представитель – СН3=О, его гомологический
|
H
ряд представлен в приложении Ж.
Для того чтобы дать названия альдегидам нужно выполнить следующие правила:
|
правило |
формула |
|
1. в формуле выбираем самую длинную углеводородную цепочку. |
СН3-СН-СН2-СН-С=О | | | СН3 С2Н5 H |
|
2. нумеруем выбранную цепочку с того края, где ближе карбонильная группа |
5 4 3 2 1 СН3-СН-СН2-СН-С=О | | | СН3 С2Н5 H |
|
3.записываем цифры, под которыми стоят ответвления: -если несколько одинаковых радикалов, то перечисляем все цифры, под которыми они стоят; -если одинаковые радикалы стоят под одним и тем же атомом углерода, то его номер указываем столько раз, сколько радикалов под ним стоит; — если радикалы разные, то номер каждого указываем по отдельности |
5 4 3 2 1 СН3-СН-СН2-СН-С=О | | | СН3 С2Н5 H 2-…-4…. |
|
4. Записываем названия радикалов: — если радикалов несколько, то используем греческое числительное: Ди- 2 Три – 3 Тетро – 4 — название радикалов можно смотреть в приложении Б |
5 4 3 2 1 СН3-СН-СН2-СН-С=О | | | СН3 С2Н5 H 2-этил-4-метил…. |
|
5.Называем длинную цепь углерода в зависимости от того, сколько в ней атомов углерода + -аль |
5 4 3 2 1 СН3-СН-СН2-СН-С=О | | | СН3 С2Н5 H 2-этил-4-метилпентаналь-.. |
|
6.В конце названия ставится номер того атома, после которого стоит карбонильная группа |
5 4 3 2 1 СН3-СН-СН2-СН-С=О | | | СН3 С2Н5 H 2-этил-4-метилпентаналь-1 |
Кроме этого можно называть альдегиды по традиционной номенклатуре. Эти названия аналогичны названиям карбоновых кислот (приложение З) с добавлением слова «альдегид».
1.9 Номенклатура кетонов.
Кетон – кислородосодержащее органическое вещество, в молекуле которого карбонильная группа соединена с двумя одинаковыми или разными радикалами.
Общая формула – R-C-R1
||
O
Простейший представитель кетонов – СН3-C-СН3 — ацетон
||
O
Для того чтобы дать названия кетонам нужно выполнить следующие правила:
|
правило |
формула |
|
1. в формуле выбираем самую длинную углеводородную цепочку. |
СН3-СН-СН2-С-СН2-СН3 | || CH3 O |
|
2. нумеруем выбранную цепочку с того края, где ближе ответвление |
1 2 3 4 5 6 СН3-СН-СН2-С-СН2-СН3 | || CH3 O |
|
3.записываем цифры, под которыми стоят ответвления: -если несколько одинаковых радикалов, то перечисляем все цифры, под которыми они стоят; -если одинаковые радикалы стоят под одним и тем же атомом углерода, то его номер указываем столько раз, сколько радикалов под ним стоит; — если радикалы разные, то номер каждого указываем по отдельности |
1 2 3 4 5 6 СН3-СН-СН2-С-СН2-СН3 | || CH3 O 2-…. |
|
4. Записываем названия радикалов: — если радикалов несколько, то используем греческое числительное: Ди- 2 Три – 3 Тетро – 4 — название радикалов можно смотреть в приложении Б |
1 2 3 4 5 6 СН3-СН-СН2-С-СН2-СН3 | || CH3 O 2-метил… |
|
5.Называем длинную цепь углерода в зависимости от того, сколько в ней атомов углерода + -он |
1 2 3 4 5 6 СН3-СН-СН2-С-СН2-СН3 | || CH3 O 2-метилгексанон-.. |
|
6.В конце названия ставится номер того атома, после которого стоит кетонная группа |
1 2 3 4 5 6 СН3-СН-СН2-С-СН2-СН3 | || CH3 O 2-метилгексанон — 4 |
Названия кетонов по традиционной номенклатуре складываются от названий радикалов (приложение Б) связанных с карбонильной группой с добавлением слова «кетон». Например, СН3-С-С3Н7
||
O метилпропилкетон
1.10 Номенклатура карбоновых кислот.
Карбоновые кислоты – органические вещества, в состав которых входит карбоксильная группа (СООН).
Общая формула – R-СООН
Простейшим представителем карбоновых кислот является – НСООН – муравьиная кислота, ее гомологический ряд представлен в приложении З.
Для того чтобы дать названия карбоновым кислотам
нужно выполнить следующие правила:
|
правило |
формула |
|
1. в формуле выбираем самую длинную углеводородную цепочку. |
СН3-СН-СН2-СН-СН2-СOOH | | CH3 C2H5 |
|
2. нумеруем выбранную цепочку с того края, где ближе карбоксильная группа |
6 5 4 3 2 1 СН3-СН-СН2-СН-СН2-СOOH | | CH3 C2H5 |
|
3.записываем цифры, под которыми стоят ответвления: -если несколько одинаковых радикалов, то перечисляем все цифры, под которыми они стоят; -если одинаковые радикалы стоят под одним и тем же атомом углерода, то его номер указываем столько раз, сколько радикалов под ним стоит; — если радикалы разные, то номер каждого указываем по отдельности |
6 5 4 3 2 1 СН3-СН-СН2-СН-СН2-СOOH | | CH3 C2H5 3-….-5-… |
|
4. Записываем названия радикалов: — если радикалов несколько, то используем греческое числительное: Ди- 2 Три – 3 Тетро – 4 — название радикалов можно смотреть в приложении Б |
6 5 4 3 2 1 СН3-СН-СН2-СН-СН2-СOOH | | CH3 C2H5 3-этил-5-метил… |
|
5.Называем длинную цепь углерода в зависимости от того, сколько в ней атомов углерода + -овая + кислота |
6 5 4 3 2 1 СН3-СН-СН2-СН-СН2-СOOH | | CH3 C2H5 3-этил-5-метилгексановая кислота |
Для некоторых карбоновых кислот используются тривиальные названия (приложение З).
1.11. Номенклатура сложных эфиров.
Сложные эфиры – это органические вещества, полученные в результате взаимодействия карбоновых кислот со спиртами.
Общая формула – R-C-О-R1, где R – радикал от кислоты, а
||
O
R1— радикал от спирта.
По современной номенклатуре названия эфиров строят из названий радикала соответствующего спирту и корня латинского названия кислоты с добавлением окончания –ат.
Н-С-О-С2Н5
||
О этилформиат
СН3-С-О-С2Н5
||
O этилацетат
Применяют также названия, состоящие из названий спирта и кислоты. Сначала пишется название радикала спирта + овый + эфир, затем тривиальное название карбоновой кислоты в родительном падеже (приложение З).
Н-С-О-С2Н5 этиловый эфир муравьиной кислоты
||
О
СН3-С-О-С2Н5 этиловый эфир уксусной кислоты
||
O
1.12 Номенклатура жиров.
Жиры – органические вещества, представляющие собой сложные эфиры глицерина и высших предельных карбоновых кислот (триглицериды).
Общая формула:
CH2-CO-O-R
|
CH-CO-O-R1
|
CH2-CO-O-R2, где R, R1, R2— одинаковые или разные радикалы
Названия жиров происходят от сочетания слова «триглицерид» и названия соответствующей высшей карбоновой кислоты (приложение З).
CH2-CO-O-С15Н31
|
CH-CO-O- С15Н31
|
CH2-CO-O- С15Н31 триглицерид пальмитиновой кислоты.
Если жиры образованы несколькими карбоновыми кислотами, то указываются все их названия.
CH2-CO-O-С15Н31
|
CH-CO-O- С15Н31
|
CH2-CO-O- С15Н35 триглицерид пальмитиновой и стеариновой кислот.
1.13 Номенклатурамылов.
Мыла – это натриевые или калиевые соли высших карбоновых кислот.
Общая формула – R-СОО-Na или R-COO-K
Названия производятся от сочетания названий соответствующих карбоновых кислот + -ат и названия металла, образующего мыло. Например, С17Н35СООNa –стеарат натрия, или C17H31COOK-памьмиат калия.
1.14 Номенклатура углеводов.
Углеводы – органические вещества состава Сп(Н2О)m, где n и m больше или равны 3.
Общая формула — Сп(Н2О)m
Название углеводов зависит от количества атомов углерода и + -оза. Например:
Н
|
H-C-OH
|
H-C-OH
|
H-C-OH
|
H триоза
Н
|
H-C-OH
|
H-C-OH
|
H-C-OH
|
H-C-OH
|
H тетроза
Н
|
H-C-OH
|
H-C-OH
|
H-C-OH
|
H-C-OH
|
H пентоза
В зависимости от расположения карбонильной группы добавляют приставки : альдо- — если карбонильная группа в конце или кето- — если карбонильная группа в середине.
Н
|
H—C=O
|
H-C-OH
|
H-C-OH
|
H-C-OH
|
H альдотетроза
Н
|
H-C-OH
|
C=O
|
ОН-С-H
|
H-C-OH
|
Н-С-ОH
|
H-C-OH
|
H кетогексоза
1.15. Номенклатура аминов.
Амины – органические производные аммиака, в котором один, два или три атома водорода замещены на радикалы.
Общая формула R-NH2
В зависимости от количества атомов замещенных в аммиаке на радикалы выделяют первичный, вторичный и третичный амин.
R-NH2 первичный амин
R-NH-R вторичный амин
R-N-R третичный амин
|
R
Радикалы в формулах могут быть различными или одинаковыми.
Название амина образуется из названия радикала + -амин.
Например, СН3-NH2 метиламин
Если радикалов несколько, то используются греческие числительные:
Ди – два
Три – три
Тетро – четыре
Например, СН3-NH-СН3 диметиламин.
Если радикалы разные, то называется каждый радикал по часовой стрелке + -амин. Например,
СН3-N-С2Н5
|
С3Н7 метилэитлпропиламин
1.16. Номенклатура аминокислот.
Аминокислоты – органические вещества в состав которых входят две функциональные группы: карбоксильноая (СООН) и аминогруппа (NH2).
Общая формула – СООН-R-NH2
Для того чтобы дать названия карбоновым кислотам
нужно выполнить следующие правила:
|
правило |
формула |
|
1. в формуле выбираем самую длинную углеводородную цепочку. |
СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 |
|
2. нумеруем выбранную цепочку с того края, где ближе аминогруппа |
1 2 3 4 5 6 СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 |
|
3.записываем номнр атома углерода под которым стоит аминогруппа + -амино |
1 2 3 4 5 6 СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 2 –амино… |
|
4.записываем цифры, под которыми стоят ответвления: -если несколько одинаковых радикалов, то перечисляем все цифры, под которыми они стоят; -если одинаковые радикалы стоят под одним и тем же атомом углерода, то его номер указываем столько раз, сколько радикалов под ним стоит; — если радикалы разные, то номер каждого указываем по отдельности |
1 2 3 4 5 6 СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 2-амино-4-… |
|
5. Записываем названия радикалов: — если радикалов несколько, то используем греческое числительное: Ди- 2 Три – 3 Тетро – 4 — название радикалов можно смотреть в приложении Б |
1 2 3 4 5 6 СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 2-амино-4-этил… |
|
6.Называем длинную цепь углерода в зависимости от того, сколько в ней атомов углерода + -овая + кислота |
1 2 3 4 5 6 СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 2-амино-4-этилгексановая кислота |
Кроме того, для аминокислот широко используются рациональные названия. Для этого применяются греческие буквы (α,β,γ).При построении таких названий выполняются следующие правила:
|
1.Буквами обозначаются атомы углерода, в цепи начиная с того атома, с которым соединена карбоксильная группа. |
ε δ γ β α СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 |
|
2.Выписатьбукву под которой стоит аминогруппа + -амино |
ε δ γ β α СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 δ-амино… |
|
3.Выписать букву под которой стоит радикал: -если несколько одинаковых радикалов, то перечисляем всебуквы, под которыми они стоят; -если одинаковые радикалы стоят под одним и тем же атомом углерода, то его букву указываем столько раз, сколько радикалов под ним стоит; — если радикалы разные, то букву каждого указываем по отдельности |
ε δ γ β α СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 δ-амино- β-… |
|
4. Записываем названия радикалов: — если радикалов несколько, то используем греческое числительное: Ди- 2 Три – 3 Тетро – 4 — название радикалов можно смотреть в приложении Б |
ε δ γ β α СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 δ-амино- β-этил… |
|
5 Называем длинную цепь углерода при помощи традиционного названия карбоновой кислоты (при этом учитываются только пронумерованные атомы, т.е. атом углерода в карбоксильной группе не считается) |
ε δ γ β α СН3-СН-СН2-СН-СН2-СOOH | | NH2 C2H5 δ-амино- β-этилкапроновая кислота |
Существуют также аминокислоты, содержащие несколько аминогрупп и карбоксильных групп. При их названии используются греческие числительные.
Если несколько аминогрупп, то греческое числительное указывается после номеров атомов, под которыми они стоят.
1 2 3 4 5 6
СН3-СН-СН2-СН-СН2-СOOH
| |
NH2 NH2 2,4 –диаминогексановая кислота
Если несколько карбоксильных групп, то греческое числительное ставится перед окончанием –овая. Нумерация при этом идет с того конца где ближе разветвление.
4 3 2 1
НООС-СН2-СН-СООН
|
NH2 2-аминобутандиовая кислота
Выделяют аминокислоты из природных соединений – белков, их названия приведены в приложении И.
2. Написание формул органических веществ по их названиям.
Для того чтобы правильно писать формулы органические вещества нужно использовать следующие рекомендации.
|
правило |
пример |
|
1.Выписываем название вещества |
2,3- диэтил- 4-метилгексан |
|
2.Обращаем внимание на последнее слово и в соответствии с ним строим цепочку из атомов углерода |
2,3- диэтил- 4-метилгексан С-С-С-С-С-С |
|
3. Затем нумеруем эту цепочку с того края, с которого удобнее |
1 2 3 4 5 6 С-С-С-С-С-С |
|
4.Ставим ответвления под указанными в названии цифрами |
2,3— диэтил- 4-метилгексан 1 2 3 4 5 6 С-С-С-С-С-С | | | |
|
5.Подписываем под ними соответствующие формулы радикалов (приложение Б) |
2,3- диэтил- 4-метилгексан 1 2 3 4 5 6 С — С – С – С – С — С | | | СН3 СН3 С2Н5 |
|
6.Дописывает недостающие атомы водорода, с условием того, что валентность углерода IV |
2,3- диэтил- 4-метилгексан 1 2 3 4 5 6 СН3-СН – СН – СН2 –СН2-СН3 | | | СН3 СН3 С2Н5 |
|
7.Если окончание названия: ен – ставится двойная связь ин – тройная связь диен – две двойные связи ол – гидроксогруппа. Связи и функциональные группы ставятся после тех атомов углерода, номера которых указаны в конце названия |
3.Построение изомеров и написание их названий.
Изомерия – проявление различных свойств веществами, имеющими одинаковый состав.
Выделяют несколько типов изомерии
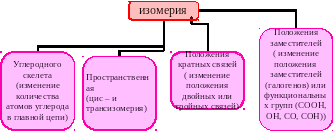
Для того чтобы правильно составить изомеры следует выполнить следующие правила:
|
правило |
Пример |
|
1.Написать формулу данного вещества в структурном виде |
СН3-СН2-СН2-СН2-СН2-СН3 |
|
2.Укоротить данную цепь на один атом углерода и записать полученную углеродную цепочку |
С – С – С – С – С |
|
3.Недостающиий атом углерода подставить к любому из средних атомов. |
С – С – С – С – С | С |
|
4.Дописать недостающие атомы водорода, при условии что валентность углерода IV |
СН3– СН – СН2 – СН2 – СН3 | СН3 |
|
5.Назвать полученное вещество (см. пункт1) |
2-метилпентан |
|
6.Далее укорачиваем цепочку до тех пор, пока возможно, т. е. учитывая, что валентность углерода IV. Называем каждое полученное вещество. |
СН3– СН – СН– СН3 | | СН3 СН3 1,2-диметилбутан |
|
7.Кроме того, радикалы можно писать различные, с учетом того, что общее количество атомов углерода не должно меняться |
СН3– СН2 – СН– СН3 | С2Н5 2-этилбутан |
|
8.Для вывода структурных формул изомеров по положению заместителей (галогенов) или функциональных групп (СО, ОН, СООН, СОН) нужно изменять положение заместителей и функциональных групп во всех структурных изомерах |
|
|
9.Для написания изомеров по положению кратных связей нужно: -написать все структурные изомеры и назвать их -перемещать кратную связь по углеродной цепочке с учетом того, что валентность углерода IV |
C4Н8 СН2=СН-СН2-СН3 бутен-1 СН2=С-СН3 2- метилпропен-1 | СН3 СН3-СН=СН-СН3 бутен-2 |
|
10. Для составления изомеров циклоалканов нужно: -укоротить цикл на 1,2…п атомов углерода -записать радикалы с учетом валентности углерода -нумерация производится таким образом, чтобы радикал имел наименьший номер |
СН2-СН2 | | СН2-СН2 циклобутан 3 СН2 2/ 1 СН2— СН- СН3 1-метилциклопропан |
|
11.Для составления пространственных изомеров используются следующие принципы: -если одинаковые атомы или группы атомов стоят по одну сторону от двойной связи, это цисизомер — если одинаковые атомы или группы атомов стоят по разные стороны от двойной связи, это трансизомер |
А А / С=С / В В А В / С=С / В А |
СПИСОК ЛИТЕРАТУРЫ
1.Аугуст Л.Г.Химия – Киев: «Вища школа»,1971
2.Ерохин Ю.М.Химия.- М.: «Академия»,2002.
3.Потапов В.М. Органическая химия.- М.: «Просвещение»,1970
4.Хомченко Ю.Г. Общая химия. – М.: «Издательство Новая волна», 1999
ПРИЛОЖЕНИЕ А.
Гомологический ряд алканов
|
формула |
Название |
|
СН4 |
Метан |
|
С2Н6 |
Этан |
|
С3Н8 |
Пропан |
|
С4Н10 |
Бутан |
|
С5Н12 |
Пентан |
|
С6Н14 |
Гексан |
|
С7Н16 |
Гептан |
|
С8Н18 |
Октан |
|
С9Н20 |
Нонан |
|
С10Н22 |
Декан |
ПРИЛОЖЕНИЕ Б.
Гомологический ряд радикалов
|
формула |
Название |
|
СН3— |
Метил |
|
С2Н5— |
Этил |
|
С3Н7— |
Пропил |
|
С4Н9— |
Бутил |
|
С5Н11— |
Пентил |
|
С6Н13— |
Гексил |
|
С7Н15— |
Гептил |
|
С8Н17— |
Октил |
|
С9Н19— |
Нонил |
|
С10Н21— |
Декил |
ПРИЛОЖЕНИЕ В.
Гомологический ряд алкенов
|
Формула |
Название |
|
С2Н4 |
Этен |
|
С3Н6 |
Пропен |
|
С4Н8 |
Бутен |
|
С5Н10 |
Пентен |
|
С6Н12 |
Гексен |
|
С7Н14 |
Гептен |
|
С8Н16 |
Октен |
|
С9Н18 |
Нонен |
|
С10Н20 |
Декен |
ПРИЛОЖЕНИЕ Г.
Гомологический ряд алкинов
|
Формула |
Название |
|
С2Н2 |
Этин |
|
С3Н4 |
Пропин |
|
С4Н6 |
Бутин |
|
С5Н8 |
Пентин |
|
С6Н10 |
Гексин |
|
С7Н12 |
Гептин |
|
С8Н14 |
Октин |
|
С9Н16 |
Нонин |
|
С10Н18 |
Декин |
ПРИЛОЖЕНИЕ Д.
Гомологический ряд алкодиенов
|
Формула |
Название |
|
С3Н4 |
Пропадиен |
|
С4Н6 |
Бутадиен |
|
С5Н8 |
Пентадиен |
|
С6Н10 |
Гексадиен |
|
С7Н12 |
Гептадиен |
|
С8Н14 |
Октадиен |
|
С9Н16 |
Нонадиен |
|
С10Н18 |
Декадиен |
ПРИЛОЖЕНИЕ Е.
Гомологический ряд одноатомных спиртов
|
формула |
Название |
|
СН3-ОН |
Метанол |
|
С2Н5-ОН |
Этанол |
|
С3Н7-ОН |
Пропанол |
|
С4Н9-ОН |
Бутанол |
|
С5Н11-ОН |
Пентанол |
|
С6Н13-ОН |
Гексанол |
|
С7Н15-ОН |
Гептанол |
|
С8Н17-ОН |
Октанол |
|
С9Н19-ОН |
Нонанол |
|
С10Н21-ОН |
Деканол |
ПРИЛОЖЕНИЕ Ж
Гомологический ряд альдегидов
|
формула |
Название |
|
|
НСОН |
Метаналь |
Формальдегид, муравьиный альдегид |
|
СН3-СНО |
Этаналь |
Уксусный альдегид |
|
С2Н5-СНО |
Пропаналь |
Пропионовый альдегид |
|
С3Н7-СНО |
Бутаналь |
Масляный альдегид |
|
С4Н9-СНО |
Пентаналь |
Валериановый альдегид |
|
С5Н11-СНО |
Гексаналь |
Капроновый альдегид |
|
С6Н13-СНО |
Гептаналь |
Энантовый альдегид |
|
С7Н15-СНО |
Октаналь |
|
|
С8Н17-СНО |
нонаналь |
|
|
С9Н19-СНО |
Деканаль |
ПРИЛОЖЕНИЕ З
Гомологический ряд предельных одноосновных карбоновых кислот
|
формула |
Название |
|
|
НСООН |
Метановая |
Муравьиная |
|
СН3СООН |
Этановая |
Уксусная |
|
С2Н5-СООН |
Пропановая |
Пропионовая |
|
С3Н7-СООН |
Бутановая |
Масляная |
|
С4Н9-СООН |
Пентановая |
Валериановая |
|
С5Н11-СООН |
Гексановая |
Капроновая |
|
С6Н13-СООН |
Гептановая |
Энантовая |
|
С7Н15-СООН |
Октановая |
|
|
С8Н17-СООН |
Нонановая |
|
|
С9Н19-СООН |
Декановая |
|
|
С15Н31СООН |
пентадиекановая |
Пальмитиновая |
|
С16Н33СООН |
гексадекановая |
Маргариновая |
|
С17Н35СООН |
гептадекановая |
стеариновая |
ПРИЛОЖЕНИЕ И.
|
формула |
Названия |
||
|
По заместительной номенклатуре |
По рациональной номенклатуре |
тривиальное |
|
|
NH2-CH2-COOH |
Аминоэнантовая |
Аминоуксусная |
глицин |
|
CH3-CHNH2-COOH |
2-аминопропановая |
α-аминопропионовая |
α-аланин |
|
CH3-CH(CH3)-CHNH2-COOH |
3-амино-3-метилбутановая |
α-аминоизовалериановая |
валин |
|
CH3-CH2-CH(CH3)-CHNH2-COOH |
2-амино-3-метилпентановая |
α-амино-βметил-β-пропионовая |
изолейцин |
|
CH3-CH(OH)-CH(NH2)-COOH |
2-амино-2-гидрокси-3-бутановая |
α-амино-β-гидроксимасляная |
Треонин |
|
CH2(SH)-CH(NH2)-COOH |
2-амино-3-тиопропановая |
α-амино-β-тиопропионовая |
Цистеин |
|
CH2(NH2)-(CH2)3-CH(NH2)-COOH |
2,6-диаминогексановая |
α,ε-диаминокапроновая |
Лизин |
|
HOOC-CH2-CH(NH2)-COOH |
2-аминобутандиовая |
α-аминоянтарная |
Аспарагин |
48