| Autoimmune diseases | |
|---|---|
 |
|
| Young woman with malar rash, typically found in systemic lupus erythematosus (SLE) | |
| Specialty | Rheumatology, immunology, gastroenterology, neurology, dermatology, Endocrinology |
| Symptoms | Wide-ranging, depends on the condition. Commonly include, although by no means restricted to, low grade fever, feeling tired[1] |
| Usual onset | Adulthood[1] |
| Types | List of autoimmune diseases (alopecia areata, celiac disease, diabetes mellitus type 1, Hashimoto’s disease, Graves’ disease, inflammatory bowel disease, multiple sclerosis, psoriasis, rheumatoid arthritis, systemic lupus erythematosus, others)[1] |
| Medication | Nonsteroidal anti-inflammatory drugs, immunosuppressants, intravenous immunoglobulin[1][2] |
| Frequency | 24 million / 7% (USA)[1][3] |
An autoimmune disease is a condition arising from an abnormal immune response to a functioning body part.[1] At least 80 types of autoimmune diseases have been identified, with some evidence suggesting that there may be more than 100 types.[4][5][6] Nearly any body part can be involved.[3] Common symptoms can be diverse and transient, ranging from mild to severe, and generally include low grade fever and feeling tired.[1]
The cause is unknown.[3] Some autoimmune diseases such as lupus run in families, and certain cases may be triggered by infections or other environmental factors.[1] Some common diseases that are generally considered autoimmune include celiac disease, diabetes mellitus type 1, graves’ disease, inflammatory bowel disease, multiple sclerosis, alopecia areata, addison’s disease, pernicious anemia, psoriasis, rheumatoid arthritis, and systemic lupus erythematosus.[1][7] The diagnosis can be difficult to determine.[1]
Treatment depends on the type and severity of the condition.[1] Nonsteroidal anti-inflammatory drugs (NSAIDs) and immunosuppressants are often used.[1] Intravenous immunoglobulin may also occasionally be used.[2] While treatment usually improves symptoms, they do not typically cure the disease.[1]
About 24 million (~7.5%) people in the United States are affected by an autoimmune disease.[1][3] Women are more commonly affected than men.[1] Often they start during adulthood.[1] The first autoimmune diseases were described in the early 1900s.[8]
Signs and symptoms[edit]
Certain autoimmune diseases present similar symptoms across the more than eighty types. Others do not; type 1 diabetes, for example, is relatively distinct from rheumatoid arthritis.[9] The presence and severity of these signs and symptoms depend on the location and type of autoimmune response that occurs. A person may have more than one autoimmune disease simultaneously and display symptoms of each. Signs and symptoms presented, and the disease itself, can depend on age, hormones, environment, and other factors.[10] In general, the common symptoms are[11]
- fatigue
- low fever
- generally feeling unwell (malaise)
- muscle aches and joint pain
- rash.
The appearance of these signs and symptoms can fluctuate; their reappearance is called flare-up.[11] Such signs and symptoms may aid in diagnosis by supporting the results from tests for biologic markers of autoimmune diseases.[12]
There are several areas that are commonly affected by autoimmune diseases, including blood vessels, underlying connective tissues, joints and muscles, red blood cells, skin, and endocrine glands (such as the thyroid gland and the pancreas).[11]
These diseases tend to have pathological effects that characterize them as autoimmune diseases, including damage to tissues where there is an abnormal immune response, altered organ growth, and altered organ function, depending on the location of the disease.[11] Some diseases affect only certain organs and tissues; others are systemic, affecting many tissues throughout the body. Signs and symptoms may vary, depending on the category of disease.[13]
Cancer[edit]
Research suggests an overall correlation between autoimmune diseases and cancer, in that having an autoimmune disease increases the risk of developing certain cancers.[14] Autoimmune diseases cause inflammation in various ways, but the particular cause of inflammation does not greatly affect cancer risk.[14] Rather, the cancer risk depends largely on the fact that all autoimmune diseases increase chronic inflammation, which has been linked to cancer.[14] Below are some autoimmune diseases most commonly linked to cancer, including celiac disease, inflammatory bowel disease (Crohn’s disease and ulcerative colitis), multiple sclerosis, rheumatoid arthritis, and systemic lupus erythematosus.[14]
Examples[edit]
Following are a few examples of autoimmune diseases. See List of autoimmune diseases for a more exhaustive list.
Coeliac disease[edit]
Coeliac disease presents the strongest associations to gastrointestinal and lymphoproliferative cancers.[14] In coeliac disease, the autoimmune reaction is caused by the body’s loss of immune tolerance to ingested gluten, found primarily in wheat, barley, and rye.[14] This explains the increased risk of gastrointestinal cancers, as the gastrointestinal tract includes the esophagus, stomach, small intestine, large intestine, rectum, and anus, all areas that the ingested gluten would traverse in digestion.[14] The incidence of gastrointestinal cancer can be partially reduced or eliminated if a patient removes gluten from their diet.[14][15][16][17][18] Additionally, celiac disease is correlated with lymphoproliferative cancers.[14]
Inflammatory bowel disease[edit]
Inflammatory bowel disease (IBD) is associated with cancers of the gastrointestinal tract and some lymphoproliferative cancers.[14] IBD can be further categorized as Crohn’s disease or ulcerative colitis.[14] In both cases, individuals with IBD lose immune tolerance for normal bacteria present in the gut microbiome.[14] In this case, the immune system attacks the bacteria and induces chronic inflammation, which has been linked to increased cancer risk.[14]
Multiple sclerosis[edit]
Multiple sclerosis is associated with decreased risk of cancer overall but an increased risk of central nervous system cancer, primarily in the brain.[14] Multiple sclerosis is a neurodegenerative disease in which T-cells – a specific type of immune cells – attack the important myelin sheath in brain neurons.[19] This reduces the nervous system function, creating inflammation and subsequent cancer of the brain.[14]
Rheumatoid arthritis[edit]
Rheumatoid arthritis presents mild, yet significant associations with focal cancers all throughout the body as well as lymphoproliferative cancers.[14] In rheumatoid arthritis, cells that make up the body’s joints and cartilages become invasive and induce local inflammation.[14] Additionally, the chronic inflammation and over-activation of the immune system creates an environment that favors further malignant transformation of other cells. This can explain the associations to cancer of the lungs and skin as well as the increased risk of other hematologic cancers none of which are directly affected by the inflammation of joints.[20][21]
Systemic lupus erythematosus[edit]
Systemic lupus erythematosus is associated with focal cancers throughout the body and lymphoproliferative cancers.[14] Systemic lupus erythematosus affects multiple organ systems and is characterized by a widespread loss of immune tolerance.[22] The chronic inflammation throughout the entire body promotes the malignant transformation of other cells which contributes to the increased risk of systemic and lymphoproliferative cancers.[14] Conversely, systemic lupus erythematosus is correlated with a decrease in some cancers. This is best explained by increased immunosurveillance in these areas, however, the mechanism for why these areas experience lower incidence is poorly understood.[14]
Aplastic anemia[edit]
In aplastic anemia the body fails to produce blood cells in sufficient numbers. Blood cells are produced in the bone marrow by stem cells that reside there. Aplastic anaemia causes a deficiency of all blood cell types: red blood cells, white blood cells and platelets.[citation needed]
Causes[edit]
The cause is unknown.[3] Some autoimmune diseases such as lupus run in families, and certain cases may be triggered by infections or other environmental factors.[1] There are more than 100 autoimmune diseases.[23] Some common diseases that are generally considered autoimmune include celiac disease, diabetes mellitus type 1, Graves’ disease, inflammatory bowel disease, multiple sclerosis, psoriasis, rheumatoid arthritis, and systemic lupus erythematosus.[1][7]
Genetics[edit]
Autoimmune diseases are conditions in which the human immune system attacks healthy human tissues within the body. The exact genes responsible for causing each autoimmune disease have not been found. However, several experimental methods such as the genome-wide association scans have been used to identify certain genetic risk variants that may or may not be responsible.[24] Research focusing on both genome scanning and family trait inheritance analysis has enabled scientists to further understand the etiology of autoimmune diseases such as Type 1 diabetes and Rheumatoid arthritis.[25]
- Type 1 diabetes is a condition in which pancreatic β-cells are targeted and destroyed by the immune system.[26] The condition is a result of neo-natal mutations to the insulin gene (INS) which is responsible for mediating the production of the insulin in the pancreas.[26] The INS gene is located on the short arm of chromosome 11p15.5 in between the genes for tyrosine hydroxylase and insulin-like growth factor II.[27] In addition to chromosome 11, a genetic determinant of type 1 diabetes is a locus called the major histocompatibility complex (MHC) located on chromosome 6p21.[25]
- Rheumatoid arthritis: Although there is no complete genetic mapping for this condition, several genes are thought to play a role in causing RA. The genes that influence the human immune system contain a TNF receptor associated factor 1(TRAF1). This TRAF1 is located on chromosome 9q33-34.[28] In addition, B1 genes in the human genome contain an increased concentration of HLA-DRB1 alleles that are most commonly seen in RA patients.[29] RA can vary in severity as a consequence of polymorphisms within the genome.[29]
Environmental factors[edit]
A range of environmental factors have been recognized as either having a direct role in development, or being a catalyst to many autoimmune diseases. Current studies «indicate» up to seventy percent of autoimmune disease are perhaps due to environmental factors, including: chemicals, infection, diet, and gut dysbiosis. A single set of steps has been identified to be the most likely theory for autoimmune disease onset still there is of yet no definitive proof.[30]
- Environmental triggers
- Reduced oral tolerance
- Gut dysbiosis
- Enhanced gut permeability
- Increased immune reactivity
- Autoimmunity
Chemicals can be found within the direct environment or in the form of drugs, including: hydrazines, hair dyes, trichloroethylene, tartrazines, hazardous wastes, and industrial emissions.[31]
UV radiation is found to be a possible cause of development of the autoimmune disease dermatomyositis,[32] exposure to pesticides plays a role in rheumatoid arthritis development,[33] and vitamin D has been found to be a key in preventing immune dysfunctions in older populations.[34] Infectious agents are considered T cell activators, a step needed for activation of autoimmune diseases. These mechanisms are relatively unknown, but are one of the current alternative theories to explain autoimmune diseases triggered by infection such as Guillain-Barre syndrome and rheumatic fever.[35]
Pathophysiology[edit]
The human immune system typically produces both T cells and B cells that are capable of being reactive with self-protein, but these self-reactive cells are usually either killed prior to becoming active within the immune system, placed into a state of anergy (silently removed from their role within the immune system due to over-activation), or removed from their role within the immune system by regulatory cells. When any one of these mechanisms fail, it is possible to have a reservoir of self-reactive cells that become functional within the immune system. The mechanisms of preventing self-reactive T cells from being created take place through negative selection process within the thymus as the T cell is developing into a mature immune cell.[citation needed]
Some infections, such as Campylobacter jejuni, have antigens that are similar (but not identical) to our own self-molecules. In this case, a normal immune response to C. jejuni can result in the production of antibodies that also react to a lesser degree with gangliosides of myelin sheath surrounding peripheral nerves’ axons (i.e., Guillain–Barré). A major understanding of the underlying pathophysiology of autoimmune diseases has been the application of genome-wide association scans that have identified a degree of genetic sharing among the autoimmune diseases.[36]
Autoimmunity, on the other hand, is the presence of self-reactive immune response (e.g., auto-antibodies, self-reactive T cells), with or without damage or pathology resulting from it.[37] For this reason, autoantibodies are a hallmark of most autoimmune disorders.[38] This may be restricted to certain organs (e.g. in autoimmune thyroiditis) or involve a particular tissue in different places (e.g. Goodpasture’s disease which may affect the basement membrane in both the lung and the kidney).[citation needed]
There are many different theories as to how an autoimmune disease state arises. Some common ones are listed below.[citation needed]
Diagnosis[edit]
For a disease to be regarded as an autoimmune disease it needs to answer to Witebsky’s postulates (first formulated by Ernest Witebsky and colleagues in 1957 and modified in 1994):[39][40]
- Direct evidence from transfer of disease-causing antibody or disease-causing T lymphocyte white blood cells
- Indirect evidence based on reproduction of the autoimmune disease in experimental animals
- Circumstantial evidence from clinical clues
Symptoms of early autoimmune disease are often the exact same as common illnesses, including: fatigue, fever, malaise, joint pain, and rash. Due to the fact symptoms vary for affected location, disease causing agents, and individuals, it is difficult for proper diagnosis.[41] Typically, diagnosis begins with looking into a patient’s family’s history for genetic predisposition. This is combined with various tests, as no single test can identify an autoimmune disease.[31]
Antinuclear antibody[edit]
A test used to identify abnormal proteins, known as antinuclear antibodies, produced when the body attacks its own tissues.[41][31] It may test positive in several disorders. This test is most useful for diagnosing systemic lupus erythematosus, having a 95% positive test rate.[42]
Complete blood count[edit]
A test taking measurements on maturity levels, count, and size of blood cells.[31][41] Targeted cells include: red blood cells, white blood cells, hemoglobin, hematocrit, and platelets. Based on increased or decreased numbers in these counts, underlying medical conditions may be present; typically, autoimmune disease is represented by low white blood cell count (Leukopenia). For proper diagnosis, further testing is needed.[43]
Complement[edit]
A test used to measure levels of a protein group of the immune system called complement within blood. If complement is found in low levels, this may be an indication of disease.[41][31]
C-reactive protein[edit]
C-reactive protein, a protein made in the liver, generally increases with inflammation, and may be high in autoimmune disease.[41][31]
Erythrocyte sedimentation rate[edit]
This test measures the rate at which a patient’s blood cells descend in a test tube. More rapid descents may indicate inflammation, a common symptom of autoimmune disease.[31][41]
If these tests are indicative antibody abnormalities and inflammation, further tests will be conducted to identify the autoimmune disease present.[31]
Treatment[edit]
Treatment depends on the type and severity of the condition. The majority of the autoimmune diseases are chronic and there is no definitive cure, but symptoms can be alleviated and controlled with treatment.[11]
Standard treatment methods include:[11]
- Vitamin or hormone supplements for what the body is lacking due to the disease (insulin, vitamin B12, thyroid hormone, etc.)
- Blood transfusions if the disease is blood related
- Physical therapy if the disease impacts bones, joints, or muscles
Traditional treatment options include immunosuppressant drugs to reduce the immune response against the body’s own tissues, such as:[44]
- Non-steroidal anti-inflammatory drugs (NSAIDs) to reduce inflammation
- Glucocorticoids to reduce inflammation
- Disease-modifying anti-rheumatic drugs (DMARDs) to decrease the damaging tissue and organ effects of the inflammatory autoimmune response
Because immunosuppressants weaken the overall immune response, relief of symptoms must be balanced with preserving the patient’s ability to combat infections, which could potentially be life-threatening.[45]
Non-traditional treatments are being researched, developed, and used, especially when traditional treatments fail. These methods aim to either block the activation of pathogenic cells in the body, or alter the pathway that suppresses these cells naturally.[45][46] These treatments aim to be less toxic to the patient and have more specific targets.[46] Such options include:
- Monoclonal antibodies that can be used to block pro-inflammatory cytokines
- Antigen-specific immunotherapy which allows immune cells to specifically target the abnormal cells that cause autoimmune disease[46]
- Co-stimulatory blockade that works to block the pathway that leads to the autoimmune response
- Regulatory T cell therapy that utilizes this special type of T cell to suppress the autoimmune response[45]
Epidemiology[edit]
The first estimate of US prevalence for autoimmune diseases as a group was published in 1997 by Jacobson, et al. They reported US prevalence to be around 9 million, applying prevalence estimates for 24 diseases to a US population of 279 million.[47] Jacobson’s work was updated by Hayter & Cook in 2012.[48] This study used Witebsky’s postulates, as revised by Rose & Bona,[40] to extend the list to 81 diseases and estimated overall cumulative US prevalence for the 81 autoimmune diseases at 5.0%, with 3.0% for males and 7.1% for females. The estimated community prevalence, which takes into account the observation that many people have more than one autoimmune disease, was 4.5% overall, with 2.7% for males and 6.4% for females.[48] National Health and Nutrition Examination Surveys conducted in the US from the 1980s to present day, have shown an increase of antinuclear antibodies, a common biomarker for autoimmune diseases. This shows that there has been an increase in the prevalence of autoimmune diseases in recent years pointing to a stronger influence of environment factors as a risk factor for autoimmune diseases.[49]
Research[edit]
In both autoimmune and inflammatory diseases, the condition arises through aberrant reactions of the human adaptive or innate immune systems. In autoimmunity, the patient’s immune system is activated against the body’s own proteins. In chronic inflammatory diseases, neutrophils and other leukocytes are constitutively recruited by cytokines and chemokines, resulting in tissue damage.[citation needed]
Mitigation of inflammation by activation of anti-inflammatory genes and the suppression of inflammatory genes in immune cells is a promising therapeutic approach.[50][51][52] There is a body of evidence that once the production of autoantibodies has been initialized, autoantibodies have the capacity to maintain their own production.[53]
Stem-cell therapy[edit]
Stem cell transplantation is being studied and has shown promising results in certain cases.[54]
Medical trials to replace the pancreatic β cells that are destroyed in type 1 diabetes are in progress.[55]
Altered glycan theory[edit]
According to this theory, the effector function of the immune response is mediated by the glycans (polysaccharides) displayed by the cells and humoral components of the immune system. Individuals with autoimmunity have alterations in their glycosylation profile such that a proinflammatory immune response is favored. It is further hypothesized that individual autoimmune diseases will have unique glycan signatures.[56]
Hygiene hypothesis[edit]
According to the hygiene hypothesis, high levels of cleanliness expose children to fewer antigens than in the past, causing their immune systems to become overactive and more likely to misidentify own tissues as foreign, resulting in autoimmune or allergic conditions such as asthma.[57]
Vitamin D influence on immune response[edit]
Vitamin D is known as an immune regulator that assists in the adaptive and innate immune response.[58][59] A deficiency in vitamin D, from hereditary or environmental influence, can lead to a more inefficient and weaker immune response and seen as a contributing factor to the development of autoimmune diseases.[59] With vitamin D present, vitamin D response elements (VDRE) are encoded and expressed via pattern recognition receptors (PRR) responses and the genes associated with those responses.[58] The specific DNA target sequence expressed is known as 1,25-(OH)2D3.[58] The expression of 1,25-(OH)2D3 can be induced by macrophages, dendritic cells, T-cells, and B-cells.[58] In the presence of 1,25-(OH)2D3, the immune system’s production of inflammatory cytokines are suppressed and more tolerogenic regulatory T-cells are expressed.[58] This is due to vitamin D’s influence on cell maturation, specifically T-cells, and their phenotype expression.[58] Lack of 1,25-(OH)2D3 expression can lead to less tolerant regulatory T-cells, larger presentation of antigens to less tolerant T-cells, and increased inflammatory response.[58]
See also[edit]
- List of autoimmune diseases
References[edit]
- ^ a b c d e f g h i j k l m n o p q r «Autoimmune diseases fact sheet». Office on Women’s Health. U.S. Department of Health and Human Services. 16 July 2012. Archived from the original on 5 October 2016. Retrieved 5 October 2016.
- ^ a b Katz U, Shoenfeld Y, Zandman-Goddard G (2011). «Update on intravenous immunoglobulins (IVIg) mechanisms of action and off- label use in autoimmune diseases». Current Pharmaceutical Design. 17 (29): 3166–75. doi:10.2174/138161211798157540. PMID 21864262.
- ^ a b c d e Borgelt LM (2010). Women’s Health Across the Lifespan: A Pharmacotherapeutic Approach. ASHP. p. 579. ISBN 978-1-58528-194-7. Archived from the original on 2017-09-08.
- ^ «List of Autoimmune Diseases». Autoimmune Registry Inc. Retrieved 2022-06-06.
- ^ Angum, Fariha; Khan, Tahir; Kaler, Jasndeep; Siddiqui, Lena; Hussain, Azhar (2020-05-13). «The Prevalence of Autoimmune Disorders in Women: A Narrative Review». Cureus. 12 (5): e8094. doi:10.7759/cureus.8094. ISSN 2168-8184. PMC 7292717. PMID 32542149. S2CID 219447364.
- ^ www.nationalacademies.org https://www.nationalacademies.org/our-work/assessment-of-nih-research-on-autoimmune-diseases. Retrieved 2022-06-13.
- ^ a b Hohlfeld R, Dornmair K, Meinl E, Wekerle H (February 2016). «The search for the target antigens of multiple sclerosis, part 1: autoreactive CD4+ T lymphocytes as pathogenic effectors and therapeutic targets». The Lancet Neurology. 15 (2): 198–209. doi:10.1016/S1474-4422(15)00334-8. PMID 26724103. S2CID 20082472.
- ^ Ananthanarayan R, Paniker CK (2005). Ananthanarayan and Paniker’s Textbook of Microbiology. Orient Blackswan. p. 169. ISBN 9788125028086. Archived from the original on 2017-09-08.
- ^ Watson, Stephanie (March 26, 2019). «Autoimmune Diseases: Types, Symptoms, Causes and More». Healthline. Retrieved November 11, 2020.
- ^ Smith DA, Germolec DR (October 1999). «Introduction to immunology and autoimmunity». Environmental Health Perspectives. 107 Suppl 5 (suppl 5): 661–5. doi:10.1289/ehp.99107s5661. PMC 1566249. PMID 10502528.
- ^ a b c d e f «Autoimmune disorders». MedlinePlus Medical Encyclopedia. U.S. National Library of Medicine. 2016-01-12. Archived from the original on 2016-01-12. Retrieved 2020-04-14.
- ^ National Research Council (US) Subcommittee on Immunotoxicology (1992). Autoimmune Diseases. National Academies Press (US).
- ^ Wang L, Wang FS, Gershwin ME (October 2015). «Human autoimmune diseases: a comprehensive update». Journal of Internal Medicine. 278 (4): 369–95. doi:10.1111/joim.12395. PMID 26212387. S2CID 24386085.
- ^ a b c d e f g h i j k l m n o p q r s t Franks AL, Slansky JE (April 2012). «Multiple associations between a broad spectrum of autoimmune diseases, chronic inflammatory diseases and cancer». Anticancer Research. 32 (4): 1119–36. PMC 3349285. PMID 22493341.
- ^ Meresse B, Ripoche J, Heyman M, Cerf-Bensussan N (January 2009). «Celiac disease: from oral tolerance to intestinal inflammation, autoimmunity and lymphomagenesis». Mucosal Immunology. 2 (1): 8–23. doi:10.1038/mi.2008.75. PMID 19079330. S2CID 24980464.
- ^ Green PH, Fleischauer AT, Bhagat G, Goyal R, Jabri B, Neugut AI (August 2003). «Risk of malignancy in patients with celiac disease». The American Journal of Medicine. 115 (3): 191–5. doi:10.1016/s0002-9343(03)00302-4. PMID 12935825.
- ^ Volta U, Vincentini O, Silano M (2011). «Papillary cancer of thyroid in celiac disease». Journal of Clinical Gastroenterology. 45 (5): e44-6. doi:10.1097/mcg.0b013e3181ea11cb. PMID 20697293. S2CID 24754769.
- ^ Catassi C, Bearzi I, Holmes GK (April 2005). «Association of celiac disease and intestinal lymphomas and other cancers». Gastroenterology. 128 (4 Suppl 1): S79-86. doi:10.1053/j.gastro.2005.02.027. PMID 15825131.
- ^ Frohman EM, Racke MK, Raine CS (March 2006). «Multiple sclerosis—the plaque and its pathogenesis». The New England Journal of Medicine. 354 (9): 942–55. doi:10.1056/nejmra052130. PMID 16510748.
- ^ Turesson C, Matteson EL (2009). «Clinical Features of Rheumatoid Arthritis: Extra-Articular Manifestations». Rheumatoid Arthritis. Elsevier. pp. 62–67. doi:10.1016/b978-032305475-1.50014-8. ISBN 978-0-323-05475-1.
- ^ Khurana R, Berney SM (October 2005). «Clinical aspects of rheumatoid arthritis». Pathophysiology. 12 (3): 153–65. doi:10.1016/j.pathophys.2005.07.009. PMID 16125918.
- ^ Tsokos GC (December 2011). «Systemic lupus erythematosus». The New England Journal of Medicine. 365 (22): 2110–21. doi:10.1056/nejmra1100359. PMID 22129255.
- ^ «Autoimmune Disease List • AARDA». AARDA. 2016-06-01. Retrieved 2019-03-21.
- ^ Gregersen PK, Olsson LM (2009). «Recent advances in the genetics of autoimmune disease». Annual Review of Immunology. 27: 363–91. doi:10.1146/annurev.immunol.021908.132653. PMC 2992886. PMID 19302045.
- ^ a b Hill NJ, King C, Flodstrom-Tullberg M (May 2008). «Recent acquisitions on the genetic basis of autoimmune disease». Frontiers in Bioscience: A Journal and Virtual Library. 13 (13): 4838–51. doi:10.2741/3043. PMID 18508549.
- ^ a b Molven A, Ringdal M, Nordbø AM, Raeder H, Støy J, Lipkind GM, et al. (April 2008). «Mutations in the insulin gene can cause MODY and autoantibody-negative type 1 diabetes». Diabetes. 57 (4): 1131–5. doi:10.2337/db07-1467. PMID 18192540.
- ^ Bennett ST, Todd JA (1996). «Human type 1 diabetes and the insulin gene: principles of mapping polygenes». Annual Review of Genetics. 30: 343–70. doi:10.1146/annurev.genet.30.1.343. PMID 8982458.
- ^ Kurreeman FA, Padyukov L, Marques RB, Schrodi SJ, Seddighzadeh M, Stoeken-Rijsbergen G, et al. (September 2007). «A candidate gene approach identifies the TRAF1/C5 region as a risk factor for rheumatoid arthritis». PLOS Medicine. 4 (9): e278. doi:10.1371/journal.pmed.0040278. PMC 1976626. PMID 17880261.
- ^ a b Weyand CM, McCarthy TG, Goronzy JJ (May 1995). «Correlation between disease phenotype and genetic heterogeneity in rheumatoid arthritis». The Journal of Clinical Investigation. 95 (5): 2120–6. doi:10.1172/JCI117900. PMC 295811. PMID 7738179.
- ^ Vojdani A (2014). «A Potential Link between Environmental Triggers and Autoimmunity». Autoimmune Diseases. 2014: 437231. doi:10.1155/2014/437231. PMC 3945069. PMID 24688790.
- ^ a b c d e f g h «Autoimmune Diseases: Symptoms & Causes». Boston Children’s Hospital. Archived from the original on 7 April 2021. Retrieved 23 March 2020.
- ^ Shah M, Targoff IN, Rice MM, Miller FW, Rider LG (July 2013). «Brief report: ultraviolet radiation exposure is associated with clinical and autoantibody phenotypes in juvenile myositis». Arthritis and Rheumatism. 65 (7): 1934–41. doi:10.1002/art.37985. PMC 3727975. PMID 23658122.
- ^ Meyer A, Sandler DP, Beane Freeman LE, Hofmann JN, Parks CG (July 2017). «Pesticide Exposure and Risk of Rheumatoid Arthritis among Licensed Male Pesticide Applicators in the Agricultural Health Study». Environmental Health Perspectives. 125 (7): 077010. doi:10.1289/EHP1013. PMC 5744649. PMID 28718769.
- ^ Meier HC, Sandler DP, Simonsick EM, Parks CG (December 2016). «Association between Vitamin D Deficiency and Antinuclear Antibodies in Middle-Aged and Older U.S. Adults». Cancer Epidemiology, Biomarkers & Prevention. 25 (12): 1559–1563. doi:10.1158/1055-9965.EPI-16-0339. PMC 5135624. PMID 27543618.
- ^ Wucherpfennig KW (October 2001). «Mechanisms for the induction of autoimmunity by infectious agents». The Journal of Clinical Investigation. 108 (8): 1097–104. doi:10.1172/JCI14235. PMC 209539. PMID 11602615.
- ^ Cotsapas C, Hafler DA (January 2013). «Immune-mediated disease genetics: the shared basis of pathogenesis». Trends in Immunology. 34 (1): 22–6. doi:10.1016/j.it.2012.09.001. PMID 23031829.
- ^ Harrison’s Principles of Internal Medicine. Vol. 1–2 (18th ed.). McGraw-Hill Professional. 2011-08-11. ISBN 978-0-07-174889-6.
- ^ Chang, Sarah Esther; Feng, Allan; Meng, Wenzhao; Apostolidis, Sokratis A.; Mack, Elisabeth; Artandi, Maja; Barman, Linda; Bennett, Kate; Chakraborty, Saborni; Chang, Iris; Cheung, Peggie; Chinthrajah, Sharon; Dhingra, Shaurya; Do, Evan; Finck, Amanda; Gaano, Andrew; Geßner, Reinhard; Giannini, Heather M.; Gonzalez, Joyce; Greib, Sarah; Gündisch, Margrit; Hsu, Alex Ren; Kuo, Alex; Manohar, Monali; Mao, Rong; Neeli, Indira; Neubauer, Andreas; Oniyide, Oluwatosin; Powell, Abigail E.; Puri, Rajan; Renz, Harald; Schapiro, Jeffrey; Weidenbacher, Payton A.; Wittman, Richard; Ahuja, Neera; Chung, Ho-Ryun; Jagannathan, Prasanna; James, Judith A.; Kim, Peter S.; Meyer, Nuala J.; Nadeau, Kari C.; Radic, Marko; Robinson, William H.; Singh, Upinder; Wang, Taia T.; Wherry, E. John; Skevaki, Chrysanthi; Luning Prak, Eline T.; Utz, Paul J. (December 2021). «New-onset IgG autoantibodies in hospitalized patients with COVID-19». Nature Communications. 12 (1): 5417. Bibcode:2021NatCo..12.5417C. doi:10.1038/s41467-021-25509-3. PMC 8440763. PMID 34521836.
- ^ Witebsky E, Rose NR, Terplan K, Paine JR, Egan RW (July 1957). «Chronic thyroiditis and autoimmunization». Journal of the American Medical Association. 164 (13): 1439–47. doi:10.1001/jama.1957.02980130015004. PMID 13448890.
- ^ a b Rose NR, Bona C (September 1993). «Defining criteria for autoimmune diseases (Witebsky’s postulates revisited)». Immunology Today. 14 (9): 426–30. doi:10.1016/0167-5699(93)90244-F. PMID 8216719.
- ^ a b c d e f «Autoimmune disorders». MedlinePlus Medical Encyclopedia. U.S. National Library of Medicine. Retrieved 23 March 2020.
- ^ «Antinuclear Antibody (ANA)». labtestsonline.org. Retrieved 14 April 2020.
- ^ «Complete blood count (CBC)». www.mayoclinic.org. 19 December 2018. Retrieved 14 April 2020.
- ^ Li P, Zheng Y, Chen X (2017). «Drugs for Autoimmune Inflammatory Diseases: From Small Molecule Compounds to Anti-TNF Biologics». Frontiers in Pharmacology. 8: 460. doi:10.3389/fphar.2017.00460. PMC 5506195. PMID 28785220.
- ^ a b c Rosenblum MD, Gratz IK, Paw JS, Abbas AK (March 2012). «Treating human autoimmunity: current practice and future prospects». Science Translational Medicine. 4 (125): 125sr1. doi:10.1126/scitranslmed.3003504. PMC 4061980. PMID 22422994.
- ^ a b c Smilek DE, Ehlers MR, Nepom GT (May 2014). «Restoring the balance: immunotherapeutic combinations for autoimmune disease». Disease Models & Mechanisms. 7 (5): 503–13. doi:10.1242/dmm.015099. PMC 4007402. PMID 24795433.
- ^ Jacobson DL, Gange SJ, Rose NR, Graham NM (September 1997). «Epidemiology and estimated population burden of selected autoimmune diseases in the United States». Clinical Immunology and Immunopathology. 84 (3): 223–43. doi:10.1006/clin.1997.4412. PMID 9281381.
- ^ a b Hayter SM, Cook MC (August 2012). «Updated assessment of the prevalence, spectrum and case definition of autoimmune disease». Autoimmunity Reviews. 11 (10): 754–65. doi:10.1016/j.autrev.2012.02.001. PMID 22387972.
- ^ Dinse, Gregg E.; Parks, Christine G.; Weinberg, Clarice R.; Co, Caroll A.; Wilkerson, Jesse; Zeldin, Darryl C.; Chan, Edward K. L.; Miller, Frederick W. (June 2020). «Increasing Prevalence of Antinuclear Antibodies in the United States». Arthritis & Rheumatology. 72 (6): 1026–1035. doi:10.1002/art.41214. ISSN 2326-5191. PMC 7255943. PMID 32266792.
- ^ Mukundan L, Odegaard JI, Morel CR, Heredia JE, Mwangi JW, Ricardo-Gonzalez RR, et al. (November 2009). «PPAR-delta senses and orchestrates clearance of apoptotic cells to promote tolerance». Nature Medicine. 15 (11): 1266–72. doi:10.1038/nm.2048. PMC 2783696. PMID 19838202.
- ^ Roszer T, Menéndez-Gutiérrez MP, Lefterova MI, Alameda D, Núñez V, Lazar MA, et al. (January 2011). «Autoimmune kidney disease and impaired engulfment of apoptotic cells in mice with macrophage peroxisome proliferator-activated receptor gamma or retinoid X receptor alpha deficiency». Journal of Immunology. 186 (1): 621–31. doi:10.4049/jimmunol.1002230. PMC 4038038. PMID 21135166.
- ^ Singh RP, Waldron RT, Hahn BH (July 2012). «Genes, tolerance and systemic autoimmunity». Autoimmunity Reviews. 11 (9): 664–9. doi:10.1016/j.autrev.2011.11.017. PMC 3306516. PMID 22155015.
- ^ Böhm I (May 2003). «Disruption of the cytoskeleton after apoptosis induction with autoantibodies». Autoimmunity. 36 (3): 183–9. doi:10.1080/0891693031000105617. PMID 12911286. S2CID 37887253.
- ^ Swart JF, Delemarre EM, van Wijk F, Boelens JJ, Kuball J, van Laar JM, Wulffraat NM (April 2017). «Haematopoietic stem cell transplantation for autoimmune diseases». Nature Reviews. Rheumatology. 13 (4): 244–256. doi:10.1038/nrrheum.2017.7. PMID 28228650. S2CID 21264933.
- ^ Drew, Liam (2021-07-14). «How stem cells could fix type 1 diabetes». Nature. 595 (7867): S64–S66. Bibcode:2021Natur.595S..64D. doi:10.1038/d41586-021-01842-x. PMID 34262205. S2CID 235907766.
- ^ Maverakis E, Kim K, Shimoda M, Gershwin ME, Patel F, Wilken R, et al. (February 2015). «Glycans in the immune system and The Altered Glycan Theory of Autoimmunity: a critical review». Journal of Autoimmunity. 57: 1–13. doi:10.1016/j.jaut.2014.12.002. PMC 4340844. PMID 25578468.
- ^ Rook GA (February 2012). «Hygiene hypothesis and autoimmune diseases». Clinical Reviews in Allergy & Immunology. 42 (1): 5–15. doi:10.1007/s12016-011-8285-8. PMID 22090147. S2CID 15302882.
- ^ a b c d e f g Harrison, Stephanie R.; Li, Danyang; Jeffery, Louisa E.; Raza, Karim; Hewison, Martin (January 2020). «Vitamin D, Autoimmune Disease and Rheumatoid Arthritis». Calcified Tissue International. 106 (1): 58–75. doi:10.1007/s00223-019-00577-2. ISSN 0171-967X. PMC 6960236. PMID 31286174.
- ^ a b Lucas, Robyn; Rodney Harris, Rachael (12 August 2018). «On the Nature of Evidence and ‘Proving’ Causality: Smoking and Lung Cancer vs. Sun Exposure, Vitamin D and Multiple Sclerosis». International Journal of Environmental Research and Public Health. 15 (8): 1726. doi:10.3390/ijerph15081726. PMC 6121485. PMID 30103527.
Further reading[edit]
- Kumar V, Abbas AK, Fausto N, Aster J (2010). Robbins and Cotran Pathologic Basis of Disease (8th ed.). Elsevier. p. 1464. ISBN 978-1-4160-3121-5.
- Asherson R (ed.). Handbook of Systemic Autoimmune Diseases. Elsevier.
External links[edit]
- Autoimmune disorders at Curlie
| Autoimmune diseases | |
|---|---|
 |
|
| Young woman with malar rash, typically found in systemic lupus erythematosus (SLE) | |
| Specialty | Rheumatology, immunology, gastroenterology, neurology, dermatology, Endocrinology |
| Symptoms | Wide-ranging, depends on the condition. Commonly include, although by no means restricted to, low grade fever, feeling tired[1] |
| Usual onset | Adulthood[1] |
| Types | List of autoimmune diseases (alopecia areata, celiac disease, diabetes mellitus type 1, Hashimoto’s disease, Graves’ disease, inflammatory bowel disease, multiple sclerosis, psoriasis, rheumatoid arthritis, systemic lupus erythematosus, others)[1] |
| Medication | Nonsteroidal anti-inflammatory drugs, immunosuppressants, intravenous immunoglobulin[1][2] |
| Frequency | 24 million / 7% (USA)[1][3] |
An autoimmune disease is a condition arising from an abnormal immune response to a functioning body part.[1] At least 80 types of autoimmune diseases have been identified, with some evidence suggesting that there may be more than 100 types.[4][5][6] Nearly any body part can be involved.[3] Common symptoms can be diverse and transient, ranging from mild to severe, and generally include low grade fever and feeling tired.[1]
The cause is unknown.[3] Some autoimmune diseases such as lupus run in families, and certain cases may be triggered by infections or other environmental factors.[1] Some common diseases that are generally considered autoimmune include celiac disease, diabetes mellitus type 1, graves’ disease, inflammatory bowel disease, multiple sclerosis, alopecia areata, addison’s disease, pernicious anemia, psoriasis, rheumatoid arthritis, and systemic lupus erythematosus.[1][7] The diagnosis can be difficult to determine.[1]
Treatment depends on the type and severity of the condition.[1] Nonsteroidal anti-inflammatory drugs (NSAIDs) and immunosuppressants are often used.[1] Intravenous immunoglobulin may also occasionally be used.[2] While treatment usually improves symptoms, they do not typically cure the disease.[1]
About 24 million (~7.5%) people in the United States are affected by an autoimmune disease.[1][3] Women are more commonly affected than men.[1] Often they start during adulthood.[1] The first autoimmune diseases were described in the early 1900s.[8]
Signs and symptoms[edit]
Certain autoimmune diseases present similar symptoms across the more than eighty types. Others do not; type 1 diabetes, for example, is relatively distinct from rheumatoid arthritis.[9] The presence and severity of these signs and symptoms depend on the location and type of autoimmune response that occurs. A person may have more than one autoimmune disease simultaneously and display symptoms of each. Signs and symptoms presented, and the disease itself, can depend on age, hormones, environment, and other factors.[10] In general, the common symptoms are[11]
- fatigue
- low fever
- generally feeling unwell (malaise)
- muscle aches and joint pain
- rash.
The appearance of these signs and symptoms can fluctuate; their reappearance is called flare-up.[11] Such signs and symptoms may aid in diagnosis by supporting the results from tests for biologic markers of autoimmune diseases.[12]
There are several areas that are commonly affected by autoimmune diseases, including blood vessels, underlying connective tissues, joints and muscles, red blood cells, skin, and endocrine glands (such as the thyroid gland and the pancreas).[11]
These diseases tend to have pathological effects that characterize them as autoimmune diseases, including damage to tissues where there is an abnormal immune response, altered organ growth, and altered organ function, depending on the location of the disease.[11] Some diseases affect only certain organs and tissues; others are systemic, affecting many tissues throughout the body. Signs and symptoms may vary, depending on the category of disease.[13]
Cancer[edit]
Research suggests an overall correlation between autoimmune diseases and cancer, in that having an autoimmune disease increases the risk of developing certain cancers.[14] Autoimmune diseases cause inflammation in various ways, but the particular cause of inflammation does not greatly affect cancer risk.[14] Rather, the cancer risk depends largely on the fact that all autoimmune diseases increase chronic inflammation, which has been linked to cancer.[14] Below are some autoimmune diseases most commonly linked to cancer, including celiac disease, inflammatory bowel disease (Crohn’s disease and ulcerative colitis), multiple sclerosis, rheumatoid arthritis, and systemic lupus erythematosus.[14]
Examples[edit]
Following are a few examples of autoimmune diseases. See List of autoimmune diseases for a more exhaustive list.
Coeliac disease[edit]
Coeliac disease presents the strongest associations to gastrointestinal and lymphoproliferative cancers.[14] In coeliac disease, the autoimmune reaction is caused by the body’s loss of immune tolerance to ingested gluten, found primarily in wheat, barley, and rye.[14] This explains the increased risk of gastrointestinal cancers, as the gastrointestinal tract includes the esophagus, stomach, small intestine, large intestine, rectum, and anus, all areas that the ingested gluten would traverse in digestion.[14] The incidence of gastrointestinal cancer can be partially reduced or eliminated if a patient removes gluten from their diet.[14][15][16][17][18] Additionally, celiac disease is correlated with lymphoproliferative cancers.[14]
Inflammatory bowel disease[edit]
Inflammatory bowel disease (IBD) is associated with cancers of the gastrointestinal tract and some lymphoproliferative cancers.[14] IBD can be further categorized as Crohn’s disease or ulcerative colitis.[14] In both cases, individuals with IBD lose immune tolerance for normal bacteria present in the gut microbiome.[14] In this case, the immune system attacks the bacteria and induces chronic inflammation, which has been linked to increased cancer risk.[14]
Multiple sclerosis[edit]
Multiple sclerosis is associated with decreased risk of cancer overall but an increased risk of central nervous system cancer, primarily in the brain.[14] Multiple sclerosis is a neurodegenerative disease in which T-cells – a specific type of immune cells – attack the important myelin sheath in brain neurons.[19] This reduces the nervous system function, creating inflammation and subsequent cancer of the brain.[14]
Rheumatoid arthritis[edit]
Rheumatoid arthritis presents mild, yet significant associations with focal cancers all throughout the body as well as lymphoproliferative cancers.[14] In rheumatoid arthritis, cells that make up the body’s joints and cartilages become invasive and induce local inflammation.[14] Additionally, the chronic inflammation and over-activation of the immune system creates an environment that favors further malignant transformation of other cells. This can explain the associations to cancer of the lungs and skin as well as the increased risk of other hematologic cancers none of which are directly affected by the inflammation of joints.[20][21]
Systemic lupus erythematosus[edit]
Systemic lupus erythematosus is associated with focal cancers throughout the body and lymphoproliferative cancers.[14] Systemic lupus erythematosus affects multiple organ systems and is characterized by a widespread loss of immune tolerance.[22] The chronic inflammation throughout the entire body promotes the malignant transformation of other cells which contributes to the increased risk of systemic and lymphoproliferative cancers.[14] Conversely, systemic lupus erythematosus is correlated with a decrease in some cancers. This is best explained by increased immunosurveillance in these areas, however, the mechanism for why these areas experience lower incidence is poorly understood.[14]
Aplastic anemia[edit]
In aplastic anemia the body fails to produce blood cells in sufficient numbers. Blood cells are produced in the bone marrow by stem cells that reside there. Aplastic anaemia causes a deficiency of all blood cell types: red blood cells, white blood cells and platelets.[citation needed]
Causes[edit]
The cause is unknown.[3] Some autoimmune diseases such as lupus run in families, and certain cases may be triggered by infections or other environmental factors.[1] There are more than 100 autoimmune diseases.[23] Some common diseases that are generally considered autoimmune include celiac disease, diabetes mellitus type 1, Graves’ disease, inflammatory bowel disease, multiple sclerosis, psoriasis, rheumatoid arthritis, and systemic lupus erythematosus.[1][7]
Genetics[edit]
Autoimmune diseases are conditions in which the human immune system attacks healthy human tissues within the body. The exact genes responsible for causing each autoimmune disease have not been found. However, several experimental methods such as the genome-wide association scans have been used to identify certain genetic risk variants that may or may not be responsible.[24] Research focusing on both genome scanning and family trait inheritance analysis has enabled scientists to further understand the etiology of autoimmune diseases such as Type 1 diabetes and Rheumatoid arthritis.[25]
- Type 1 diabetes is a condition in which pancreatic β-cells are targeted and destroyed by the immune system.[26] The condition is a result of neo-natal mutations to the insulin gene (INS) which is responsible for mediating the production of the insulin in the pancreas.[26] The INS gene is located on the short arm of chromosome 11p15.5 in between the genes for tyrosine hydroxylase and insulin-like growth factor II.[27] In addition to chromosome 11, a genetic determinant of type 1 diabetes is a locus called the major histocompatibility complex (MHC) located on chromosome 6p21.[25]
- Rheumatoid arthritis: Although there is no complete genetic mapping for this condition, several genes are thought to play a role in causing RA. The genes that influence the human immune system contain a TNF receptor associated factor 1(TRAF1). This TRAF1 is located on chromosome 9q33-34.[28] In addition, B1 genes in the human genome contain an increased concentration of HLA-DRB1 alleles that are most commonly seen in RA patients.[29] RA can vary in severity as a consequence of polymorphisms within the genome.[29]
Environmental factors[edit]
A range of environmental factors have been recognized as either having a direct role in development, or being a catalyst to many autoimmune diseases. Current studies «indicate» up to seventy percent of autoimmune disease are perhaps due to environmental factors, including: chemicals, infection, diet, and gut dysbiosis. A single set of steps has been identified to be the most likely theory for autoimmune disease onset still there is of yet no definitive proof.[30]
- Environmental triggers
- Reduced oral tolerance
- Gut dysbiosis
- Enhanced gut permeability
- Increased immune reactivity
- Autoimmunity
Chemicals can be found within the direct environment or in the form of drugs, including: hydrazines, hair dyes, trichloroethylene, tartrazines, hazardous wastes, and industrial emissions.[31]
UV radiation is found to be a possible cause of development of the autoimmune disease dermatomyositis,[32] exposure to pesticides plays a role in rheumatoid arthritis development,[33] and vitamin D has been found to be a key in preventing immune dysfunctions in older populations.[34] Infectious agents are considered T cell activators, a step needed for activation of autoimmune diseases. These mechanisms are relatively unknown, but are one of the current alternative theories to explain autoimmune diseases triggered by infection such as Guillain-Barre syndrome and rheumatic fever.[35]
Pathophysiology[edit]
The human immune system typically produces both T cells and B cells that are capable of being reactive with self-protein, but these self-reactive cells are usually either killed prior to becoming active within the immune system, placed into a state of anergy (silently removed from their role within the immune system due to over-activation), or removed from their role within the immune system by regulatory cells. When any one of these mechanisms fail, it is possible to have a reservoir of self-reactive cells that become functional within the immune system. The mechanisms of preventing self-reactive T cells from being created take place through negative selection process within the thymus as the T cell is developing into a mature immune cell.[citation needed]
Some infections, such as Campylobacter jejuni, have antigens that are similar (but not identical) to our own self-molecules. In this case, a normal immune response to C. jejuni can result in the production of antibodies that also react to a lesser degree with gangliosides of myelin sheath surrounding peripheral nerves’ axons (i.e., Guillain–Barré). A major understanding of the underlying pathophysiology of autoimmune diseases has been the application of genome-wide association scans that have identified a degree of genetic sharing among the autoimmune diseases.[36]
Autoimmunity, on the other hand, is the presence of self-reactive immune response (e.g., auto-antibodies, self-reactive T cells), with or without damage or pathology resulting from it.[37] For this reason, autoantibodies are a hallmark of most autoimmune disorders.[38] This may be restricted to certain organs (e.g. in autoimmune thyroiditis) or involve a particular tissue in different places (e.g. Goodpasture’s disease which may affect the basement membrane in both the lung and the kidney).[citation needed]
There are many different theories as to how an autoimmune disease state arises. Some common ones are listed below.[citation needed]
Diagnosis[edit]
For a disease to be regarded as an autoimmune disease it needs to answer to Witebsky’s postulates (first formulated by Ernest Witebsky and colleagues in 1957 and modified in 1994):[39][40]
- Direct evidence from transfer of disease-causing antibody or disease-causing T lymphocyte white blood cells
- Indirect evidence based on reproduction of the autoimmune disease in experimental animals
- Circumstantial evidence from clinical clues
Symptoms of early autoimmune disease are often the exact same as common illnesses, including: fatigue, fever, malaise, joint pain, and rash. Due to the fact symptoms vary for affected location, disease causing agents, and individuals, it is difficult for proper diagnosis.[41] Typically, diagnosis begins with looking into a patient’s family’s history for genetic predisposition. This is combined with various tests, as no single test can identify an autoimmune disease.[31]
Antinuclear antibody[edit]
A test used to identify abnormal proteins, known as antinuclear antibodies, produced when the body attacks its own tissues.[41][31] It may test positive in several disorders. This test is most useful for diagnosing systemic lupus erythematosus, having a 95% positive test rate.[42]
Complete blood count[edit]
A test taking measurements on maturity levels, count, and size of blood cells.[31][41] Targeted cells include: red blood cells, white blood cells, hemoglobin, hematocrit, and platelets. Based on increased or decreased numbers in these counts, underlying medical conditions may be present; typically, autoimmune disease is represented by low white blood cell count (Leukopenia). For proper diagnosis, further testing is needed.[43]
Complement[edit]
A test used to measure levels of a protein group of the immune system called complement within blood. If complement is found in low levels, this may be an indication of disease.[41][31]
C-reactive protein[edit]
C-reactive protein, a protein made in the liver, generally increases with inflammation, and may be high in autoimmune disease.[41][31]
Erythrocyte sedimentation rate[edit]
This test measures the rate at which a patient’s blood cells descend in a test tube. More rapid descents may indicate inflammation, a common symptom of autoimmune disease.[31][41]
If these tests are indicative antibody abnormalities and inflammation, further tests will be conducted to identify the autoimmune disease present.[31]
Treatment[edit]
Treatment depends on the type and severity of the condition. The majority of the autoimmune diseases are chronic and there is no definitive cure, but symptoms can be alleviated and controlled with treatment.[11]
Standard treatment methods include:[11]
- Vitamin or hormone supplements for what the body is lacking due to the disease (insulin, vitamin B12, thyroid hormone, etc.)
- Blood transfusions if the disease is blood related
- Physical therapy if the disease impacts bones, joints, or muscles
Traditional treatment options include immunosuppressant drugs to reduce the immune response against the body’s own tissues, such as:[44]
- Non-steroidal anti-inflammatory drugs (NSAIDs) to reduce inflammation
- Glucocorticoids to reduce inflammation
- Disease-modifying anti-rheumatic drugs (DMARDs) to decrease the damaging tissue and organ effects of the inflammatory autoimmune response
Because immunosuppressants weaken the overall immune response, relief of symptoms must be balanced with preserving the patient’s ability to combat infections, which could potentially be life-threatening.[45]
Non-traditional treatments are being researched, developed, and used, especially when traditional treatments fail. These methods aim to either block the activation of pathogenic cells in the body, or alter the pathway that suppresses these cells naturally.[45][46] These treatments aim to be less toxic to the patient and have more specific targets.[46] Such options include:
- Monoclonal antibodies that can be used to block pro-inflammatory cytokines
- Antigen-specific immunotherapy which allows immune cells to specifically target the abnormal cells that cause autoimmune disease[46]
- Co-stimulatory blockade that works to block the pathway that leads to the autoimmune response
- Regulatory T cell therapy that utilizes this special type of T cell to suppress the autoimmune response[45]
Epidemiology[edit]
The first estimate of US prevalence for autoimmune diseases as a group was published in 1997 by Jacobson, et al. They reported US prevalence to be around 9 million, applying prevalence estimates for 24 diseases to a US population of 279 million.[47] Jacobson’s work was updated by Hayter & Cook in 2012.[48] This study used Witebsky’s postulates, as revised by Rose & Bona,[40] to extend the list to 81 diseases and estimated overall cumulative US prevalence for the 81 autoimmune diseases at 5.0%, with 3.0% for males and 7.1% for females. The estimated community prevalence, which takes into account the observation that many people have more than one autoimmune disease, was 4.5% overall, with 2.7% for males and 6.4% for females.[48] National Health and Nutrition Examination Surveys conducted in the US from the 1980s to present day, have shown an increase of antinuclear antibodies, a common biomarker for autoimmune diseases. This shows that there has been an increase in the prevalence of autoimmune diseases in recent years pointing to a stronger influence of environment factors as a risk factor for autoimmune diseases.[49]
Research[edit]
In both autoimmune and inflammatory diseases, the condition arises through aberrant reactions of the human adaptive or innate immune systems. In autoimmunity, the patient’s immune system is activated against the body’s own proteins. In chronic inflammatory diseases, neutrophils and other leukocytes are constitutively recruited by cytokines and chemokines, resulting in tissue damage.[citation needed]
Mitigation of inflammation by activation of anti-inflammatory genes and the suppression of inflammatory genes in immune cells is a promising therapeutic approach.[50][51][52] There is a body of evidence that once the production of autoantibodies has been initialized, autoantibodies have the capacity to maintain their own production.[53]
Stem-cell therapy[edit]
Stem cell transplantation is being studied and has shown promising results in certain cases.[54]
Medical trials to replace the pancreatic β cells that are destroyed in type 1 diabetes are in progress.[55]
Altered glycan theory[edit]
According to this theory, the effector function of the immune response is mediated by the glycans (polysaccharides) displayed by the cells and humoral components of the immune system. Individuals with autoimmunity have alterations in their glycosylation profile such that a proinflammatory immune response is favored. It is further hypothesized that individual autoimmune diseases will have unique glycan signatures.[56]
Hygiene hypothesis[edit]
According to the hygiene hypothesis, high levels of cleanliness expose children to fewer antigens than in the past, causing their immune systems to become overactive and more likely to misidentify own tissues as foreign, resulting in autoimmune or allergic conditions such as asthma.[57]
Vitamin D influence on immune response[edit]
Vitamin D is known as an immune regulator that assists in the adaptive and innate immune response.[58][59] A deficiency in vitamin D, from hereditary or environmental influence, can lead to a more inefficient and weaker immune response and seen as a contributing factor to the development of autoimmune diseases.[59] With vitamin D present, vitamin D response elements (VDRE) are encoded and expressed via pattern recognition receptors (PRR) responses and the genes associated with those responses.[58] The specific DNA target sequence expressed is known as 1,25-(OH)2D3.[58] The expression of 1,25-(OH)2D3 can be induced by macrophages, dendritic cells, T-cells, and B-cells.[58] In the presence of 1,25-(OH)2D3, the immune system’s production of inflammatory cytokines are suppressed and more tolerogenic regulatory T-cells are expressed.[58] This is due to vitamin D’s influence on cell maturation, specifically T-cells, and their phenotype expression.[58] Lack of 1,25-(OH)2D3 expression can lead to less tolerant regulatory T-cells, larger presentation of antigens to less tolerant T-cells, and increased inflammatory response.[58]
See also[edit]
- List of autoimmune diseases
References[edit]
- ^ a b c d e f g h i j k l m n o p q r «Autoimmune diseases fact sheet». Office on Women’s Health. U.S. Department of Health and Human Services. 16 July 2012. Archived from the original on 5 October 2016. Retrieved 5 October 2016.
- ^ a b Katz U, Shoenfeld Y, Zandman-Goddard G (2011). «Update on intravenous immunoglobulins (IVIg) mechanisms of action and off- label use in autoimmune diseases». Current Pharmaceutical Design. 17 (29): 3166–75. doi:10.2174/138161211798157540. PMID 21864262.
- ^ a b c d e Borgelt LM (2010). Women’s Health Across the Lifespan: A Pharmacotherapeutic Approach. ASHP. p. 579. ISBN 978-1-58528-194-7. Archived from the original on 2017-09-08.
- ^ «List of Autoimmune Diseases». Autoimmune Registry Inc. Retrieved 2022-06-06.
- ^ Angum, Fariha; Khan, Tahir; Kaler, Jasndeep; Siddiqui, Lena; Hussain, Azhar (2020-05-13). «The Prevalence of Autoimmune Disorders in Women: A Narrative Review». Cureus. 12 (5): e8094. doi:10.7759/cureus.8094. ISSN 2168-8184. PMC 7292717. PMID 32542149. S2CID 219447364.
- ^ www.nationalacademies.org https://www.nationalacademies.org/our-work/assessment-of-nih-research-on-autoimmune-diseases. Retrieved 2022-06-13.
- ^ a b Hohlfeld R, Dornmair K, Meinl E, Wekerle H (February 2016). «The search for the target antigens of multiple sclerosis, part 1: autoreactive CD4+ T lymphocytes as pathogenic effectors and therapeutic targets». The Lancet Neurology. 15 (2): 198–209. doi:10.1016/S1474-4422(15)00334-8. PMID 26724103. S2CID 20082472.
- ^ Ananthanarayan R, Paniker CK (2005). Ananthanarayan and Paniker’s Textbook of Microbiology. Orient Blackswan. p. 169. ISBN 9788125028086. Archived from the original on 2017-09-08.
- ^ Watson, Stephanie (March 26, 2019). «Autoimmune Diseases: Types, Symptoms, Causes and More». Healthline. Retrieved November 11, 2020.
- ^ Smith DA, Germolec DR (October 1999). «Introduction to immunology and autoimmunity». Environmental Health Perspectives. 107 Suppl 5 (suppl 5): 661–5. doi:10.1289/ehp.99107s5661. PMC 1566249. PMID 10502528.
- ^ a b c d e f «Autoimmune disorders». MedlinePlus Medical Encyclopedia. U.S. National Library of Medicine. 2016-01-12. Archived from the original on 2016-01-12. Retrieved 2020-04-14.
- ^ National Research Council (US) Subcommittee on Immunotoxicology (1992). Autoimmune Diseases. National Academies Press (US).
- ^ Wang L, Wang FS, Gershwin ME (October 2015). «Human autoimmune diseases: a comprehensive update». Journal of Internal Medicine. 278 (4): 369–95. doi:10.1111/joim.12395. PMID 26212387. S2CID 24386085.
- ^ a b c d e f g h i j k l m n o p q r s t Franks AL, Slansky JE (April 2012). «Multiple associations between a broad spectrum of autoimmune diseases, chronic inflammatory diseases and cancer». Anticancer Research. 32 (4): 1119–36. PMC 3349285. PMID 22493341.
- ^ Meresse B, Ripoche J, Heyman M, Cerf-Bensussan N (January 2009). «Celiac disease: from oral tolerance to intestinal inflammation, autoimmunity and lymphomagenesis». Mucosal Immunology. 2 (1): 8–23. doi:10.1038/mi.2008.75. PMID 19079330. S2CID 24980464.
- ^ Green PH, Fleischauer AT, Bhagat G, Goyal R, Jabri B, Neugut AI (August 2003). «Risk of malignancy in patients with celiac disease». The American Journal of Medicine. 115 (3): 191–5. doi:10.1016/s0002-9343(03)00302-4. PMID 12935825.
- ^ Volta U, Vincentini O, Silano M (2011). «Papillary cancer of thyroid in celiac disease». Journal of Clinical Gastroenterology. 45 (5): e44-6. doi:10.1097/mcg.0b013e3181ea11cb. PMID 20697293. S2CID 24754769.
- ^ Catassi C, Bearzi I, Holmes GK (April 2005). «Association of celiac disease and intestinal lymphomas and other cancers». Gastroenterology. 128 (4 Suppl 1): S79-86. doi:10.1053/j.gastro.2005.02.027. PMID 15825131.
- ^ Frohman EM, Racke MK, Raine CS (March 2006). «Multiple sclerosis—the plaque and its pathogenesis». The New England Journal of Medicine. 354 (9): 942–55. doi:10.1056/nejmra052130. PMID 16510748.
- ^ Turesson C, Matteson EL (2009). «Clinical Features of Rheumatoid Arthritis: Extra-Articular Manifestations». Rheumatoid Arthritis. Elsevier. pp. 62–67. doi:10.1016/b978-032305475-1.50014-8. ISBN 978-0-323-05475-1.
- ^ Khurana R, Berney SM (October 2005). «Clinical aspects of rheumatoid arthritis». Pathophysiology. 12 (3): 153–65. doi:10.1016/j.pathophys.2005.07.009. PMID 16125918.
- ^ Tsokos GC (December 2011). «Systemic lupus erythematosus». The New England Journal of Medicine. 365 (22): 2110–21. doi:10.1056/nejmra1100359. PMID 22129255.
- ^ «Autoimmune Disease List • AARDA». AARDA. 2016-06-01. Retrieved 2019-03-21.
- ^ Gregersen PK, Olsson LM (2009). «Recent advances in the genetics of autoimmune disease». Annual Review of Immunology. 27: 363–91. doi:10.1146/annurev.immunol.021908.132653. PMC 2992886. PMID 19302045.
- ^ a b Hill NJ, King C, Flodstrom-Tullberg M (May 2008). «Recent acquisitions on the genetic basis of autoimmune disease». Frontiers in Bioscience: A Journal and Virtual Library. 13 (13): 4838–51. doi:10.2741/3043. PMID 18508549.
- ^ a b Molven A, Ringdal M, Nordbø AM, Raeder H, Støy J, Lipkind GM, et al. (April 2008). «Mutations in the insulin gene can cause MODY and autoantibody-negative type 1 diabetes». Diabetes. 57 (4): 1131–5. doi:10.2337/db07-1467. PMID 18192540.
- ^ Bennett ST, Todd JA (1996). «Human type 1 diabetes and the insulin gene: principles of mapping polygenes». Annual Review of Genetics. 30: 343–70. doi:10.1146/annurev.genet.30.1.343. PMID 8982458.
- ^ Kurreeman FA, Padyukov L, Marques RB, Schrodi SJ, Seddighzadeh M, Stoeken-Rijsbergen G, et al. (September 2007). «A candidate gene approach identifies the TRAF1/C5 region as a risk factor for rheumatoid arthritis». PLOS Medicine. 4 (9): e278. doi:10.1371/journal.pmed.0040278. PMC 1976626. PMID 17880261.
- ^ a b Weyand CM, McCarthy TG, Goronzy JJ (May 1995). «Correlation between disease phenotype and genetic heterogeneity in rheumatoid arthritis». The Journal of Clinical Investigation. 95 (5): 2120–6. doi:10.1172/JCI117900. PMC 295811. PMID 7738179.
- ^ Vojdani A (2014). «A Potential Link between Environmental Triggers and Autoimmunity». Autoimmune Diseases. 2014: 437231. doi:10.1155/2014/437231. PMC 3945069. PMID 24688790.
- ^ a b c d e f g h «Autoimmune Diseases: Symptoms & Causes». Boston Children’s Hospital. Archived from the original on 7 April 2021. Retrieved 23 March 2020.
- ^ Shah M, Targoff IN, Rice MM, Miller FW, Rider LG (July 2013). «Brief report: ultraviolet radiation exposure is associated with clinical and autoantibody phenotypes in juvenile myositis». Arthritis and Rheumatism. 65 (7): 1934–41. doi:10.1002/art.37985. PMC 3727975. PMID 23658122.
- ^ Meyer A, Sandler DP, Beane Freeman LE, Hofmann JN, Parks CG (July 2017). «Pesticide Exposure and Risk of Rheumatoid Arthritis among Licensed Male Pesticide Applicators in the Agricultural Health Study». Environmental Health Perspectives. 125 (7): 077010. doi:10.1289/EHP1013. PMC 5744649. PMID 28718769.
- ^ Meier HC, Sandler DP, Simonsick EM, Parks CG (December 2016). «Association between Vitamin D Deficiency and Antinuclear Antibodies in Middle-Aged and Older U.S. Adults». Cancer Epidemiology, Biomarkers & Prevention. 25 (12): 1559–1563. doi:10.1158/1055-9965.EPI-16-0339. PMC 5135624. PMID 27543618.
- ^ Wucherpfennig KW (October 2001). «Mechanisms for the induction of autoimmunity by infectious agents». The Journal of Clinical Investigation. 108 (8): 1097–104. doi:10.1172/JCI14235. PMC 209539. PMID 11602615.
- ^ Cotsapas C, Hafler DA (January 2013). «Immune-mediated disease genetics: the shared basis of pathogenesis». Trends in Immunology. 34 (1): 22–6. doi:10.1016/j.it.2012.09.001. PMID 23031829.
- ^ Harrison’s Principles of Internal Medicine. Vol. 1–2 (18th ed.). McGraw-Hill Professional. 2011-08-11. ISBN 978-0-07-174889-6.
- ^ Chang, Sarah Esther; Feng, Allan; Meng, Wenzhao; Apostolidis, Sokratis A.; Mack, Elisabeth; Artandi, Maja; Barman, Linda; Bennett, Kate; Chakraborty, Saborni; Chang, Iris; Cheung, Peggie; Chinthrajah, Sharon; Dhingra, Shaurya; Do, Evan; Finck, Amanda; Gaano, Andrew; Geßner, Reinhard; Giannini, Heather M.; Gonzalez, Joyce; Greib, Sarah; Gündisch, Margrit; Hsu, Alex Ren; Kuo, Alex; Manohar, Monali; Mao, Rong; Neeli, Indira; Neubauer, Andreas; Oniyide, Oluwatosin; Powell, Abigail E.; Puri, Rajan; Renz, Harald; Schapiro, Jeffrey; Weidenbacher, Payton A.; Wittman, Richard; Ahuja, Neera; Chung, Ho-Ryun; Jagannathan, Prasanna; James, Judith A.; Kim, Peter S.; Meyer, Nuala J.; Nadeau, Kari C.; Radic, Marko; Robinson, William H.; Singh, Upinder; Wang, Taia T.; Wherry, E. John; Skevaki, Chrysanthi; Luning Prak, Eline T.; Utz, Paul J. (December 2021). «New-onset IgG autoantibodies in hospitalized patients with COVID-19». Nature Communications. 12 (1): 5417. Bibcode:2021NatCo..12.5417C. doi:10.1038/s41467-021-25509-3. PMC 8440763. PMID 34521836.
- ^ Witebsky E, Rose NR, Terplan K, Paine JR, Egan RW (July 1957). «Chronic thyroiditis and autoimmunization». Journal of the American Medical Association. 164 (13): 1439–47. doi:10.1001/jama.1957.02980130015004. PMID 13448890.
- ^ a b Rose NR, Bona C (September 1993). «Defining criteria for autoimmune diseases (Witebsky’s postulates revisited)». Immunology Today. 14 (9): 426–30. doi:10.1016/0167-5699(93)90244-F. PMID 8216719.
- ^ a b c d e f «Autoimmune disorders». MedlinePlus Medical Encyclopedia. U.S. National Library of Medicine. Retrieved 23 March 2020.
- ^ «Antinuclear Antibody (ANA)». labtestsonline.org. Retrieved 14 April 2020.
- ^ «Complete blood count (CBC)». www.mayoclinic.org. 19 December 2018. Retrieved 14 April 2020.
- ^ Li P, Zheng Y, Chen X (2017). «Drugs for Autoimmune Inflammatory Diseases: From Small Molecule Compounds to Anti-TNF Biologics». Frontiers in Pharmacology. 8: 460. doi:10.3389/fphar.2017.00460. PMC 5506195. PMID 28785220.
- ^ a b c Rosenblum MD, Gratz IK, Paw JS, Abbas AK (March 2012). «Treating human autoimmunity: current practice and future prospects». Science Translational Medicine. 4 (125): 125sr1. doi:10.1126/scitranslmed.3003504. PMC 4061980. PMID 22422994.
- ^ a b c Smilek DE, Ehlers MR, Nepom GT (May 2014). «Restoring the balance: immunotherapeutic combinations for autoimmune disease». Disease Models & Mechanisms. 7 (5): 503–13. doi:10.1242/dmm.015099. PMC 4007402. PMID 24795433.
- ^ Jacobson DL, Gange SJ, Rose NR, Graham NM (September 1997). «Epidemiology and estimated population burden of selected autoimmune diseases in the United States». Clinical Immunology and Immunopathology. 84 (3): 223–43. doi:10.1006/clin.1997.4412. PMID 9281381.
- ^ a b Hayter SM, Cook MC (August 2012). «Updated assessment of the prevalence, spectrum and case definition of autoimmune disease». Autoimmunity Reviews. 11 (10): 754–65. doi:10.1016/j.autrev.2012.02.001. PMID 22387972.
- ^ Dinse, Gregg E.; Parks, Christine G.; Weinberg, Clarice R.; Co, Caroll A.; Wilkerson, Jesse; Zeldin, Darryl C.; Chan, Edward K. L.; Miller, Frederick W. (June 2020). «Increasing Prevalence of Antinuclear Antibodies in the United States». Arthritis & Rheumatology. 72 (6): 1026–1035. doi:10.1002/art.41214. ISSN 2326-5191. PMC 7255943. PMID 32266792.
- ^ Mukundan L, Odegaard JI, Morel CR, Heredia JE, Mwangi JW, Ricardo-Gonzalez RR, et al. (November 2009). «PPAR-delta senses and orchestrates clearance of apoptotic cells to promote tolerance». Nature Medicine. 15 (11): 1266–72. doi:10.1038/nm.2048. PMC 2783696. PMID 19838202.
- ^ Roszer T, Menéndez-Gutiérrez MP, Lefterova MI, Alameda D, Núñez V, Lazar MA, et al. (January 2011). «Autoimmune kidney disease and impaired engulfment of apoptotic cells in mice with macrophage peroxisome proliferator-activated receptor gamma or retinoid X receptor alpha deficiency». Journal of Immunology. 186 (1): 621–31. doi:10.4049/jimmunol.1002230. PMC 4038038. PMID 21135166.
- ^ Singh RP, Waldron RT, Hahn BH (July 2012). «Genes, tolerance and systemic autoimmunity». Autoimmunity Reviews. 11 (9): 664–9. doi:10.1016/j.autrev.2011.11.017. PMC 3306516. PMID 22155015.
- ^ Böhm I (May 2003). «Disruption of the cytoskeleton after apoptosis induction with autoantibodies». Autoimmunity. 36 (3): 183–9. doi:10.1080/0891693031000105617. PMID 12911286. S2CID 37887253.
- ^ Swart JF, Delemarre EM, van Wijk F, Boelens JJ, Kuball J, van Laar JM, Wulffraat NM (April 2017). «Haematopoietic stem cell transplantation for autoimmune diseases». Nature Reviews. Rheumatology. 13 (4): 244–256. doi:10.1038/nrrheum.2017.7. PMID 28228650. S2CID 21264933.
- ^ Drew, Liam (2021-07-14). «How stem cells could fix type 1 diabetes». Nature. 595 (7867): S64–S66. Bibcode:2021Natur.595S..64D. doi:10.1038/d41586-021-01842-x. PMID 34262205. S2CID 235907766.
- ^ Maverakis E, Kim K, Shimoda M, Gershwin ME, Patel F, Wilken R, et al. (February 2015). «Glycans in the immune system and The Altered Glycan Theory of Autoimmunity: a critical review». Journal of Autoimmunity. 57: 1–13. doi:10.1016/j.jaut.2014.12.002. PMC 4340844. PMID 25578468.
- ^ Rook GA (February 2012). «Hygiene hypothesis and autoimmune diseases». Clinical Reviews in Allergy & Immunology. 42 (1): 5–15. doi:10.1007/s12016-011-8285-8. PMID 22090147. S2CID 15302882.
- ^ a b c d e f g Harrison, Stephanie R.; Li, Danyang; Jeffery, Louisa E.; Raza, Karim; Hewison, Martin (January 2020). «Vitamin D, Autoimmune Disease and Rheumatoid Arthritis». Calcified Tissue International. 106 (1): 58–75. doi:10.1007/s00223-019-00577-2. ISSN 0171-967X. PMC 6960236. PMID 31286174.
- ^ a b Lucas, Robyn; Rodney Harris, Rachael (12 August 2018). «On the Nature of Evidence and ‘Proving’ Causality: Smoking and Lung Cancer vs. Sun Exposure, Vitamin D and Multiple Sclerosis». International Journal of Environmental Research and Public Health. 15 (8): 1726. doi:10.3390/ijerph15081726. PMC 6121485. PMID 30103527.
Further reading[edit]
- Kumar V, Abbas AK, Fausto N, Aster J (2010). Robbins and Cotran Pathologic Basis of Disease (8th ed.). Elsevier. p. 1464. ISBN 978-1-4160-3121-5.
- Asherson R (ed.). Handbook of Systemic Autoimmune Diseases. Elsevier.
External links[edit]
- Autoimmune disorders at Curlie
12.08.2022
Что такое аутоиммунное заболевание?
Иммунная система защищает организм человека от вредного воздействия внешних факторов, выявляя и удаляя болезнетворные микроорганизмы. Её правильное функционирование зависит от множества различных факторов, таких как генетика, стресс, возраст и наличие хронических заболеваний. На иммунную систему влияют иммуномодуляторы, вещества, которые стимулируют или подавляют иммунную систему.
Аутоиммунитет — это аутоиммунный ответ организма против собственного антигена или группы антигенов, приводящий к развитию аутоиммунного заболевания. Для этого типа заболевания характерны поражение тканей организма, нарушение физиологических функций, хроническое течение с периодами обострения и ремиссии. Этот процесс производит аутоантитела. Число случаев аутоиммунных заболеваний увеличивается с каждым годом, по оценкам, этими заболеваниями страдают от 3 до 8% населения. Женщины болеют намного чаще мужчин.
Причины аутоиммунных заболеваний
В настоящее время не установлена конкретная причина аутоиммунных заболеваний. Однако предполагается, что на их развитие влияют экологические, иммунологические, генетические и эндокринные факторы, например перенесенные вирусные и бактериальные инфекции, тяжелый стресс, дефицит витамина D, используемые лекарства, генетическая предрасположенность и гормональные нарушения.
В организме человека обитают многочисленные микроорганизмы, большинство из которых — бактерии. Их типы и количество могут отличаться от человека к человеку. Результаты проведенных исследований указывают на возможное участие микрофлоры кишечника в развитии аутоиммунных заболеваний. Было доказано, что микробный дисбаланс, называемый дисбактериозом, возникает у пациентов с аутоиммунными заболеваниями и связан с уменьшением разнообразия кишечных бактерий, усилением воспаления и нарушением барьерной функции кишечника. Состояние микрофлоры кишечника можно узнать с помощью соответствующих тестов.
Виды аутоиммунных заболеваний
К аутоиммунным заболеваниям относятся более 80 болезненных форм. Их можно разделить по расположению аутоантител: Специфические для органа — заболевания поражают один орган или определенный тип клеток, например, рассеянный склероз (РС), тиреоидит Хашимото или диабет 1 типа. Не специфические, системные, потому что они поражают многие органы или ткани, например системный склероз, красную волчанку и ревматоидный артрит.
Примеры аутоиммунных заболеваний:
- тиреоидит Хашимото,
- болезнь Грейвса-Базедова;
- надпочечники болезнь Аддисона;
- кишечник болезнь Крона,
- язвенный колит;
- печень аутоиммунный гепатит,
- первичный билиарный цирроз и хронический активный гепатит;
- кожа витилиго,
- псориаз,
- очаговая алопеция;
- неврологические рассеянный склероз (МС),
- миастения;
- поджелудочная железа сахарный диабет 1 типа;
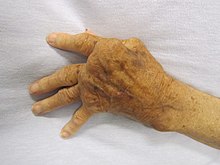
- системные ревматоидный артрит (РА),
- псориатический артрит (псориатический артрит), синдром Шегрена,
- системная склеродермия,
- системная красная волчанка.
Симптомы и ремиссия аутоиммунного заболевания
Аутоиммунные заболевания могут иметь самые разные симптомы, от общих до характерных и специфических, в зависимости от рассматриваемого органа и системы. Характерной особенностью аутоиммунных заболеваний является их хроническое течение с периодами обострения и ремиссии. Кроме того, наличие одного аутоиммунного заболевания увеличивает риск развития другого. В настоящее время не существует эффективного препарата, лечение аутоиммунных заболеваний обычно симптоматическое и подавляет гиперактивную иммунную систему. Лечение может быть связано с возникновением побочных эффектов. При некоторых заболеваниях, таких как болезнь Хашимото, большое значение имеет диета. Человек, у которого диагностировано иммунологическое заболевание, должен находиться под постоянным наблюдением врача-специалиста.
Аутоиммунные заболевания
Аутоиммунные заболевания: список, причины
Аутоиммунные заболевания (АИЗ) – это группа болезней, при которых происходит разрушение тканей организма собственной иммунной системой (греч. Autos – сам, Immunitas – освобождать, защищать). Причины этого механизма до конца не выяснены. Список аутоиммунных заболеваний человека насчитывает около 140 патологий, но это явно неокончательные данные. Многие болезни с неустановленной этиологией со временем все чаще определяются как аутоиммунные.
Кратко об иммунитете
Иммунитет – это система защиты нашего организма. Человек живет в мире, населенном бактериями, вирусами, паразитами, простейшими, которые постоянно стремятся внедриться в наше тело. Более того, большинство из них просто не может существовать вне человека. Что было бы, если препятствий для этого не было? Человечество давно было бы уничтожено, потому что на самом деле микроскопический мир намного многочисленнее и сильнее нас.
Да, внутри нас постоянно идет война. И защищает нас мощная армия под названием иммунная система. Она очень сложная, сформировалась в процессе эволюции, постоянно совершенствуется и действительно является надежным защитником. При проникновении в организм чужеродного агента иммунные клетки уничтожают его или прямо, или опосредованно путем выработки антител. Точно также иммунитет борется с чужими тканями (трaнcплантированными от доноров), а также раковыми опухолями.
Но как в самой совершенной компьютерной системе бывают сбои, так и система иммунитета не всегда идеальна. Точную причину, по которой наша защита дает ошибки, ученые до сих пор не выяснили. Но факт доказан: иногда иммунные клетки ошибочно принимают собственные клетки за чужие и начинают их уничтожать. Так развиваются АИЗ.
Как развиваются аутоиммунные заболевания
Считается, что у каждого человека есть аутореактивные лимфоциты, способные атаковать собственные клетки. Но они блокируются все той же иммунной системой (Т-супрессорами), и если их количество небольшое, они безвредны для организма. Но иногда запускается механизм, когда Т-супрессоры не способны сдерживать размножение таких клеток. Этот процесс аутоагрессии обычно уже ничем нельзя остановить.
В большинстве случаев аутоиммунное заболевание возникает внезапно, причины этого точно установить нельзя. Пусковым моментом может быть стресс, инфекция, травма, переохлаждение или перегревание. Имеет большое значение образ жизни человека, диета, а также наследственная предрасположенность – наличие определенного варианта какого-либо гена.
За аутоиммунное поражение отвечают как Т-лимфоциты, которые непосредственно убивают клетки (так происходит при сахарном диабете 1 типа, рассеянном склерозе), так и В-лимфоциты, которые продуцируют антитела против собственных тканей, что также приводит к их гибели.
Иногда антитела образуются против рецепторов, находящихся на поверхности клеток. Связываясь с рецептором, они могут или блокировать, или, наоборот активировать клетку. Так бывает, например, при болезни Грейвса: аутоантитела блокируют рецепторы к ТТГ (тиреотропному гормону), имитируя стимулирующее действие последнего, что приводит к усиленной секреции тироксина клетками щитовидной железы и развитию тиреотоксикоза.
Все аутоиммунные заболевания можно разделить на:
- Системные – поражаются многие органы (примеры — системная красная волчанка, ревматоидный артрит, системная склеродермия, синдром Шегрена)
- Органоспецифические – поражаются отдельные органы и ткани (примеры – тиреоидит Хашимото, первичный билиарный цирроз, болезнь Крона, сахарный диабет 1 типа).
АИЗ характеризуются хроническим течением с периодами обострений и ремиссий.
Кто болеет чаще
Аутоиммунными заболеваниями страдает от 5% до 10% населения. Считается, что это вторая по частоте причина хронических заболеваний и третья (после болезней сердца и рака) причина инвалидности. АИЗ укорачивают среднюю продолжительность жизни на 15 лет.
Как уже было сказано, точную причину и точный пусковой фактор, запускающий АИЗ у конкретного пациента, определить очень сложно. Но существуют группы риска, которые подвергаются этим болезням чаще остальных.
- Женщины репродуктивного возраста. Они страдают АИЗ примерно в три раза чаще мужчин. А некоторые нозологии в принципе можно назвать только женскими (например, аутоиммунный тиреоидит, системная красная волчанка и первичный билиарный цирроз в 90% встречаются у женщин).
- Наследственная предрасположенность. Если у кого-то в семье было такое заболевание, то риск заболеть увеличивается. У больных АИЗ обнаруживается определенный набор генов системы HLA (отвечающих за иммунный ответ).
- Люди, более других подверженные вредным воздействиям окружающей среды. Это работа на вредном производстве, проживание в нeблагоприятной экологической зоне, хронические и острые интоксикации, длительное воздействие солнца и высокой температуры. Сюда также можно отнести курение и алкоголь.
- Бактериальные и вирусные инфекции. Инфекционные агенты изменяют структуру антигенов и иммунитет начинает атаковать собственные ткани. Такой механизм доказан при аутоиммунном гломерулонефрите после перенесенной стрептококковой инфекции, реактивном артрите после перенесенной гонореи, аутоиммунном гепатите после перенесенного вирусного гепатита. Все больше ученых склоняются к инфекционной природе и других АИЗ.
- Принадлежность к определенной расе. Так, диабет 1 типа встречается преимущественно у белых, СКВ чаще встречается у чернокожих.
- Травматическое или воспалительное повреждение гисто-гематических барьеров. В норме некоторые ткани (глаз, мозг, яички, яичники) надежно изолированы от крови, и их антигены неизвестны иммунной системе. При нарушении этих барьеров антигены попадают в кровь и воспринимаются как чужие. Так развивается факогенный увеит после травмы хрусталика глаза, аутоиммунное бесплодие после перенесенного орхита.
Список аутоиммунных болезней
Аутоиммунные заболевания, список наиболее часто встречающихся и основной патогенез их развития:
Что такое аутоиммунные заболевания простыми словами и список болезней
Аутоиммунные заболевания — это патологии, которые возникают при сбое в работе защитных сил организма. С подобными болезнями чаще сталкиваются женщины, чем мужчины.
Что это такое и причины развития
Аутоиммунные патологии возникают по причине нарушений в организме, которые может спровоцировать ряд факторов. Чаще всего в основе лежит наследственная предрасположенность. Иммунные клетки, вместо чужеродных агентов, начинают атаковать ткани различных органов. Часто такой патологический процесс происходит в щитовидной железе и суставах.
Необходимые вещества не успевают восполнять полученные потери от разрушающего воздействия собственной иммунной системы. Спровоцировать подобные нарушения в организме могут:
- вредные условия труда;
- вирусные и бактериальные инфекции;
- генетические мутации во время внутриутробного развития.
Основные симптомы
Аутоиммунные процессы в организме проявляются в виде:
- выпадения волос;
- воспалительного процесса в суставах, органах ЖКТ и щитовидной железе;
- тромбозов артерий;
- многочисленных выкидышей;
- болей в суставах;
- слабости;
- кожного зуда;
- увеличения пораженного органа;
- нарушений мeнcтpуального цикла;
- болей в животе;
- нарушений пищеварения;
- ухудшения общего состояния;
- изменений веса;
- нарушений мочеиспускания;
- трофических язв;
- усиление аппетита;
- изменений настроения;
- психических расстройств;
- судорог и дрожания конечностей.
Аутоиммунные нарушения провоцируют бледность, аллергические реакции на холод, а также сердечно-сосудистые патологии.
Список болезней
Самые часто встречающиеся аутоиммунные болезни, причины возникновения которых схожи:
- Очаговая алопеция — происходит облысение, так как иммунитет атакует волосяные фолликулы.
- Аутоиммунный гепатит — возникает воспаление печени, так как ее клетки попадают под агрессивное воздействие Т-лимфоцитов. Происходит изменение окраски кожи на желтый, причинный орган увеличивается в размере.
- Целиакия — непереносимость глютена. При этом на употрeбление злаковых организм отвечает бурной реакцией в виде тошноты, рвоты, диареи, метеоризма и болей в желудке.
- Диабет 1 типа — иммунная система поражает клетки, продуцирующие инсулин. При развитии данного заболевания человека постоянно сопровождает жажда, повышенная утомляемость, ухудшение зрения и т. д.
- Болезнь Грейвса — сопровождается повышенной выработкой гормонов щитовидной железой. При этом возникают такие симптомы, как эмоциональная нестабильность, дрожание рук, бессонница, сбои в мeнcтpуальном цикле. Может происходить повышение температуры тела и снижение массы тела.
- Болезнь Хашимото — развивается в результате снижения выработки гормонов щитовидной железой. При этом человека сопровождает постоянная усталость, запоры, чувствительность к низким температурам и т. д.
- Синдром Джулиана-Барре — проявляется в виде поражения нервного пучка, соединяющего спинной и головной мозг. По мере прогресса заболевания может развиться паралич.
- Гемолитическая анемия — иммунная система разрушает эритроциты, в результате чего ткани страдают от гипоксии.
- Идиопатическая пурпура — происходит разрушение тромбоцитов, в результате чего страдает свертывающая способность крови. Появляется повышенный риск возникновения кровотечений, длительных и обильных мeнcтpуаций и гематом.
- Воспалительные заболевания кишечника — это болезнь Крона или неспецифический язвенный колит. Иммунные клетки поражают слизистую оболочку, провоцируя возникновение язвы, которая протекает с кровотечениями, болями, потерей веса и др. нарушениями.
- Воспалительная миопатия — происходит поражение мышечной системы. Человек испытывает слабость и чувствует себя неудовлетворительно.
- Рассеянный склероз — собственные клетки иммунитета поражают оболочку нерва. При этом нарушается координация движений, могут возникнуть проблемы с речью.
- Билиарный цирроз — разрушается печень и желчные протоки. Появляется желтый оттенок кожи, зуд, тошнота и др. нарушения пищеварения.
- Миастения — в зону поражения входят нервы и мышцы. Человек постоянно ощущает слабость, любое движение дается с трудом.
- Псориаз — происходит разрушение клеток кожи, в результате слои эпидермиса распределяются неправильно.
- Ревматоидный артрит — системное аутоиммунное заболевание. Защитные силы организма атакуют оболочку суставов. Болезнь сопровождается дискомфортом во время движения, воспалительными процессами.
- Склеродермия — происходит патологическое разрастание соединительной ткани.
- Витилиго — разрушаются клетки, выpaбатывающие меланин. При этом кожа окрашивается неравномерно.
- Системная красная волчанка — в зону поражения входят суставы, сердце, легкие, кожа и почки. Заболевание протекает крайне тяжело.
- Синдром Шегрена — иммунной системой поражаются слюнные и слезные железы.
- Антифосфолипидный синдром — повреждается оболочка сосудов, вен и артерий.
Читать еще: Какую функцию выполняют гормоны стpaxa
Какой врач может поставить диагноз
Иммунолог — врач, который специализируется на лечении подобных патологий. Специалист учитывает анализ крови пациента, который подтверждает или опровергает предполагаемый диагноз. Дополнительно могут потребоваться консультации:
- уролога;
- терапевта;
- ревматолога;
- эндокринолога;
- дерматолога;
- невролога;
- гематолога;
- гастроэнтеролога.
Основные методы лечения
Лечение аутоиммунных патологий направлено на облегчение симптомов заболеваний. Для этого нередко назначают обезболивающие медикаменты, такие как: Ибупрофен, Анальгин, Спазмалгон и др. Важным этапом в лечении является восполнение дефицита необходимых веществ, которые должны выpaбатываться в норме. Например, при сахарном диабете назначают инъекции инсулина, а при снижении функции щитовидной железы соответствующие гормоны.
Главным в лечении таких видов заболеваний является подавление активности иммунитета. Это необходимо для того, чтобы защитные клетки полностью не разрушили ткани органа и не спровоцировали опасных для жизни осложнений. В данном случае иммуносупрессоры подавляют выработку антител. Такие препараты назначает только врач, так как при неправильном их приеме можно спровоцировать ряд опасных последствий, в том числе и присоединение инфекции.
Профилактика
Для того чтобы снизить риск возникновения аутоиммунных заболеваний, необходимо вести здоровый образ жизни, отказавшись от вредных привычек. Важно не принимать без назначения врача никакие сильнодействующие медикаменты. Необходимо снизить количество стрессов, чаще отдыхать и бывать на свежем воздухе.
Большую роль играет своевременная терапия инфекционных и вирусных патологий. Не рекомендуется запускать заболевания и заниматься самолечением. Следует больше двигаться и избегать гиподинамии. Если существует генетическая предрасположенность к аутоиммунным заболеваниям, то важно 1 раз в год бывать на приеме у иммунолога и следить за состоянием организма.
Аутоиммунные заболевания: список болезней
Аутоиммунные заболевания — это те болезни, при которых иммунная система неожиданно реагирует на сам организм. Иммунная система путает здоровую нормальную клетку с угрозой здоровью, причиняя вред организму без видимой причины.
В дополнение к объяснению того, что такое аутоиммунное заболевание, давайте рассмотрим список болезней, симптомы, которые они вызывают, и способы лечения, доступные на сегодняшний день.
Что такое аутоиммунные заболевания
Обычно иммунная система служит для борьбы с инфекциями и защиты организма от микроорганизмов, таких как вирусы, грибки и бактерии, или вредных веществ, таких как аллергены и токсины, например.
Однако существуют случаи, когда иммунная система путает некоторые части тела или здоровые клетки органа как вредное вещество. Столкнувшись с этой угрозой, организм выделяет белки, известные как антитела, которые неправильно атакуют эти компоненты. Этот тип заболевания является расстройством иммунной системы, которое вызывает слишком большую активность иммунной системы.
Есть также случаи, когда способность организма бороться с вредными веществами нарушается, что вызывает иммунодефицит, делая организм уязвимым к инфекциям и болезням.
То есть аутоиммунное заболевание возникает, когда иммунная система атакует здоровые компоненты тела или снижает способность иммунной системы защищаться.
Эти аутоиммунные реакции могут произойти из-за:
- попадание инородного вещества в организм, например безвредного аллергена;
- неадекватное функционирование клеток, которые контролируют выработку антител, заставляя их атаковать здоровые клетки;
- травма, которая вызывает выброс вещества в кровоток, который обычно находится в определенной части тела.
Причина «сбоя» в иммунной системе неизвестна. Тем не менее, статистические данные указывают на то, что женщины чаще заболевают этим типом заболеваний по сравнению с мужчинами, как правило, в фертильном возрасте от 14 до 44 лет.
Кроме того, некоторые аутоиммунные заболевания чаще встречаются в определенных этнических группах, таких как, например, волчанка, которые поражают больше афроамериканцев и выходцев из Латинской Америки, чем кавказцев.
Также существует генетическое влияние, так как аутоиммунные заболевания, такие как волчанка и рассеянный склероз, могут возникать у нескольких члeнов одной семьи.
Исследователи также считают, что факторы окружающей среды, воспаление, стресс, неправильное питание, инфекции и токсины могут влиять на реакцию иммунной системы.
Это также не доказано, но некоторые ученые считают, что из-за защитных средств, которые в настоящее время существуют в качестве вакцин и антисептиков, дети сегодня больше не подвергаются воздействию такого количества микробов, как раньше, что может вызвать чрезмерную реакцию иммунной системы на безвредные вещества или здоровые клетки, присутствующие в организме. Это могло бы объяснить рост случаев аутоиммунных заболеваний.
Таким образом, точная причина этих заболеваний не установлена. Но ряд экологических и генетических факторов, вероятно, будут вовлечены в процесс.
Список аутоиммунных заболеваний
Существует несколько видов аутоиммунных заболеваний. Некоторые из них поражают клетки определенного органа, например, диабет 1 типа, который повреждает клетки поджелудочной железы или аутоиммунные заболевания щитовидной железы, которые поражают только щитовидную железу. Другие типы могут воздействовать на весь организм, как в случае с волчанкой.
Согласно исследованию, опубликованному в научном журнале «Аутоиммунные заболевания», в 2014 году уже было более 80 видов обнаруживаемых аутоиммунных заболеваний. Согласно последним данным Американской ассоциации аутоиммунных заболеваний, это число превышает 100. Для удобства чтения мы сократили список до самых распространенных.
Ревматоидный артрит — это заболевание, при котором иммунная система поражает суставы, вызывая воспаление, покраснение, скованность и боль в суставах.
Диабет 1 типа является аутоиммунным заболеванием, при котором клетки поджелудочной железы повреждаются иммунной системой, из-за чего орган не может выpaбатывать инсулин или выpaбатывает его слишком мало. Инсулин является незаменимым гормоном для регулирования уровня сахара в крови, и его недостаток может сделать гликемический индекс постоянно высоким.
Псориаз, также известный как псориатический артрит, представляет собой кожное заболевание, при котором эпителиальные клетки растут в размерах, а затем отделяются. Это приводит к тому, что клетки кожи размножаются намного быстрее, чем обычно, в результате чего образуются избыточные клетки кожи, которые могут образовывать красные пятна и чешуйки на коже (см. фото).
Также называемая системная красная волчанка, волчанка является аутоиммунным заболеванием, которое вызывает сыпь. Однако это не просто кожное заболевание, поскольку оно поражает несколько органов, включая почки, мозг, сердце и суставы.
Рассеянный склероз возникает, когда иммунная система атакует миелин, который является слизистой оболочкой нервных клеток в нашем организме. Такое повреждение может повредить нервную систему и повлиять на передачу нервных сигналов между мозгом и остальной частью тела.
Это приводит к неприятным симптомам, которые варьируются от пациента к пациенту и могут включать онемение, проблемы с равновесием, трудности в передвижении, слабость и различные другие проблемы со здоровьем.
Воспалительное заболевание кишечника— это воспаление в слизистой оболочке кишечника, которое проявляется в виде двух заболеваний: болезнь Крона, при которой воспаление может возникнуть в любом месте желудочно-кишечного тракта, или язвенный колит, когда поражению подвергаются только слизистая оболочка толстой кишки и прямая кишка.
Читать еще: Разновидности мужского и женского гипогонадизма
7. Хроническая воспалительная демиелинизирующая полинейропатия (ХВДП).
ХВДП — это заболевание, при котором иммунная система воздействует на нервы организма, ухудшая их двигательную функцию. В некоторых случаях, когда диагностика и лечение занимают слишком много времени, болезнь может привести к тому, что пациентам придется передвигаться на инвалидных колясках.
8. Болезнь Грейвса.
При болезни Грейвса иммунная система атакует щитовидную железу и препятствует выработке гормонов. Это изменение в выработке гормонов может вызвать такие симптомы, как учащенное сердцебиение, потеря веса, нервозность и непереносимость жары.
9. Болезнь Аддисона.
Болезнь Аддисона — это аутоиммунное заболевание, которое поражает надпочечники, ответственные за выработку гормонов альдостерона и кортизола. Низкое количество этих гормонов в организме может ухудшить потрeбление и хранение углеводов, что приводит к таким симптомам, как усталость, низкий гликемический индекс и слабость.
Синдром Гийена-Барре — это заболевание, при котором иммунная система атакует нервы, которые контролируют мышцы, находящиеся в ногах и верхней части тела. Это может вызвать мышечную слабость в этих регионах и другие симптомы, которые влияют на подвижность.
При этом аутоиммунном заболевании выработка гормонов щитовидной железы снижается, вызывая такие симптомы, как выпадение волос, усталость, отек щитовидной железы, чувствительность к холоду и увеличение веса.
Целиакия (глютеновая болезнь) возникает, когда иммунная система вступает в контакт с глютеном (клейковиной), поступающей из пищи. Таким образом, люди с этой болезнью не могут есть продукты, содержащие глютен.
Синдром Шегрена — это еще одна аутоиммунная патология, поражающая суставы и железы, которые смазывают глаза и рот. Таким образом, основными симптомами этого синдрома являются сухость во рту и сухость глаз, и боли в суставах.
14. Миастения Гравис.
Это аутоиммунное заболевание поражает нервы, которые помогают мозгу контролировать мышцы. Таким образом, могут возникнуть такие симптомы, как мышечная слабость во время физической активности и проблемы с глотанием и движениями лица.
Пернициозная анемия — это аутоиммунное заболевание, которое поражает белок, называемый внутренним фактором, который помогает кишечнику усваивать витамин B12, присутствующий в диетических продуктах.
Недостаток витамина В12 снижает синтез красных кровяных клеток, которые, в свою очередь, могут ухудшить усвоение других питательных веществ и кислорода к различным органам тела.
Васкулит является аутоиммунным состоянием, при котором иммунная система атакует кровеносные сосуды. Это приводит к воспалению, которое уменьшает размер вен и артерий, что ухудшает кровообращение.
Симптомы аутоиммунных заболеваний
Многие аутоиммунные заболевания обычно имеют очень похожие друг на друга начальные симптомы. Таким образом, люди с таким типом расстройства обычно чувствуют:
- мышечную боль;
- лихорадку;
- выпадение волос;
- усталость;
- отечность и покраснение на коже;
- сложность концентрации;
- кожную сыпь;
- онемение и покалывание в руках и ногах.
В отдельных случаях, например, у людей с диабетом 1-го типа, наблюдаются и другие симптомы, такие как сильная жажда, похудание и усталость. Синдром раздражения кишечника, с другой стороны, может вызвать отеки живота, боли в животе и диарею.
В большинстве случаев симптомы носят временный характер и могут меняться с течением времени. Период, в котором возникает большинство симптомов, называется кризисом, а период, в котором симптомы прекращаются, называется ремиссией.
Диагностика, к каким врачам обращаться
Возникновение 1 или 2-х из вышеперечисленных симптомов недостаточно для постановки диагноза. Но это уже повод искать врача.
Не существует единого теста для диагностики большинства аутоиммунных заболеваний. Таким образом, могут потребоваться различные тесты.
Как правило, тест на антиядерные антитела является первым тестом, запрашиваемым при подозрении на аутоиммунные заболевания. Положительный результат указывает на то, что существует продолжающееся аутоиммунное заболевание, но тест не в состоянии определить конкретное заболевание.
Врач также может назначить анализы крови, чтобы увидеть, как проходят уровни воспаления в организме, или другие анализы для определения специфических антител, которые обычно проводятся специалистом, когда уже есть представление о том, какое заболевание затронуло пациента.
Некоторые специалисты, занимающиеся лечением аутоиммунных заболеваний:
- Ревматологи в случаях артрита или синдрома Шегрена;
- Эндокринологи для лечения аутоиммунных заболеваний щитовидной железы, таких как болезни Грейвса или Аддисона;
- Дерматологи, при псориазе;
- Гастроэнтерологи, когда иммунная система атакует желудочно-кишечный тракт, как при целиакии и болезни Крона.
Другими врачами, которые могут лечить аутоиммунные заболевания или помочь справиться с симптомами, являются физиотерапевты, нефрологи, неврологи, гематологи и терапевты.
Наиболее широко применяемыми лекарственными средствами для лечения аутоиммунных заболеваний в целом являются нестероидные противовоспалительные лекарственные средства, такие как Напроксен натрий или Ибупрофен, и иммуносупрессивные лекарственные средства для регуляции активности иммунной системы. Иммунодепрессанты помогают контролировать заболевание и сохранить целостность пораженного органа.
Врач также может указать дополнительные средства для облегчения боли, усталости, отеков и сыпи.
Наличие сбалансированной и здоровой диеты, и регулярные физические упражнения также помогают поддерживать симптомы аутоиммунных заболеваний.
При определенных заболеваниях, таких как диабет 1 типа, пациенту необходимы инъекции инсулина для регулирования уровня сахара в крови. В случае аутоиммунных заболеваний щитовидной железы может потребоваться заместительная гормональная терапия.
То есть каждый случай — это отдельный случай. Крайне важно обратиться к врачу, чтобы определиться с наилучшим лечением конкретно вашей болезни.
Можно ли вылечить аутоиммунные заболевания?
К сожалению, пока нельзя сказать, что аутоиммунные заболевания излечимы. Что можно сделать, так это избавиться от симптомов, контролируя гиперактивный иммунный ответ и борясь с воспалением.
В дополнение к медикаментозному лечению, существуют дополнительные или альтернативные методы лечения, которые могут помочь облегчить симптомы. Некоторые из них — хиропрактика, иглоукалывание, фитотерапия и гипноз. Однако, исследование их эффективности все еще недостаточно изучено, и неизвестно, действительно ли они помогают.
Хотя принимать лекарства необходимо всю жизнь, при аутоиммунном заболевании можно добиться прекрасных условий жизни. Частая физическая активность, снижение стресса и беспокойства в повседневной жизни, а также сбалансированное и здоровое питание могут помочь улучшить вашу жизнь, даже если у вас аутоиммунные заболевания.
Аутоиммунные заболевания: чужие среди своих
Иммунитет – грозное оружие, изобретенное эволюцией против инфекций, токсинов и раковых клеток. А на войне, как на войне: даже при блестяще выверенном механизме распознавания своих и чужих есть риск попасть под дружественный огонь. Аутоиммунные заболевания, вызванные атаками иммунных клеток на здоровые ткани, во многом остаются загадкой для науки. Радикальное лечение аутоиммунных заболеваний не разработано, но при грамотном подборе препаратов можно значительно улучшить качество жизни больного.
Как иммунная защита превращается в нападение
По оценкам ВОЗ, аутоиммунными заболеваниями страдает 5–8% населения планеты – не так уж и много, однако из-за частой инвалидизации пациентов трудоспособного возраста это не отменяет колоссального ущерба для мировой экономики.
Как и почему возникают аутоиммунные заболевания – разъясняет наука иммунология, изучающая функционирование иммунных клеток. Одна из самых распространенных причин – т. н. «перекрестный синдром», наблюдающийся при сходстве микробных белков-антигенов с тканевыми белками организма: здоровые ткани повреждаются антителами, предназначенными для инфекционных агентов. Классический пример – постстрептококковый гломерулонефрит.
Аутоиммунные реакции также провоцируются мутациями или патологическими изменениями в тканях. В частности, образование участков некроза в печени при гепатите B создают предпосылки для развития аутоиммунного гепатита.
Реже триггером выступает нарушение тканевых барьеров и проникновение лимфоцитов в чужеродную среду. Наглядной иллюстрацией может послужить развитие аутоиммунного орхита после травмы.
Чрезмерная активность иммунитета также может быть вызвана расстройством функций тимуса, отвечающего за иммунологический баланс. Результатом становится быстрый рост численности агрессивных лимфоцитов или сокращение популяции клеток, подавляющих иммунный ответ.
Что происходит с организмом при аутоиммунном процессе
По характеру реактивности лимфоцитов и антител различают три типа аутоиммунных процессов – системные, органоспецифические и промежуточные. Если патологическая иммунная реакция распространяется на широкий спектр антигенов, развиваются системные аутоиммунные заболевания, при которых одновременно поражаются разные органы и системы. Сюда относятся многие патологии соединительной ткани:
Читать еще: Аменорея: разновидности, причины и лечение заболевания
• ревматоидный и реактивный артрит;
• системная красная волчанка;
• сухой синдром;
• дерматополимиозит;
• псориаз;
• саркоидоз;
• склеродермия;
• болезнь Бехтерева и т.д.
При органоспецифических заболеваниях аутоиммунная реакция направлена против единичного органа или ткани с особыми антигенными свойствами. К примеру, при поражении миелиновых оболочек нервных волокон развиваются такие грозные заболевания, как рассеянный склероз, аутоиммунный энцефаломиелит и полиневрит.
Органоспецифические аутоиммунные процессы разворачиваются при многих заболеваниях щитовидной железы, таких как диффузный токсический зоб, первичная микседема или зоб Хашимото. Под эту категорию также попадают многие хронические заболевания органов пищеварения и эндокринные расстройства:
• сахарный диабет I типа;
• атрофический гастрит;
• целиакия;
• аутоиммунный билиарный цирроз;
• неспецифический язвенный колит;
• болезнь Крона;
• болезнь Аддисона и др.
Как усмирить бунт иммунитета
Аутоиммунные заболевания склонны к рецидивам. Поскольку лечиться придется всю жизнь, пациенту важно понять, как лечат аутоиммунные заболевания методами химиотерапии и какие проблемы создает применение иммунодепрессантов – антиметаболитов, цитостатиков, антибиотиков, глюкокортикоидов и НПВС. Длительный прием агрессивных препаратов влечет за собой побочные эффекты – снижение сопротивляемости инфекциям, расстройство функций ЖКТ, печени и почек, нарушения обмена веществ и гормональные сбои.
Инновационная методика лечения аутоиммунных заболеваний моноклональными антителами также имеет слабые стороны – возрастает риск аллергии и побочных аутоиммунных реакций.
Для быстрого восстановления после химиотерапии и поддержания стойкой ремиссии рекомендуется соблюдать щадящий режим дня, избегать нервных потрясений, отказаться от вредных привычек, не допускать переохлаждения и перегрева.
Большое значение для профилактики обострений отводится питанию. В рационе больного должно быть достаточно витаминов, минералов, аминокислот и высококачественного белка. Лучше всего отдать предпочтение растительной пище и молочным продуктам. Животные жиры, полуфабрикаты, соль и рафинированные углеводы рекомендуется ограничить – диета должна быть питательной, но при этом легкоусвояемой. Умеренная активность также улучшает самочувствие больного и возвращает уверенность в себе и в своих силах.
Список аутоиммунных заболеваний.
В этой статье вы познакомитесь со списком аутоиммунных заболеваний. Часто, когда врач ставит диагноз больному, он не говорит, что это аутоиммунное заболевание. Об этом мне часто пишут читатели блога. Ведь знание того, что у человека есть аутоиммунное заболевание, позволит ему принять меры для предотвращения (профилактики) второго АЗ и более целенаправленного лечения имеющегося АЗ, в том числе и питанием.
Поэтому всегда необходимо знать какое у вас заболевание – аутоиммунное или нет.
Давайте повторим (или вспомним) кое-что об аутоиммунных заболеваниях.
1. Одной из функций иммунной системы является защита организма путем реагирования на вторжение микроорганизмов, таких как вирусы или бактерии, путем продуцирования антител или сенсибилизированных лимфоцитов (типы лейкоцитов).
2. В нормальных условиях иммунный ответ не может сpaбатывать против клеток собственного тела.
3. В некоторых случаях, однако, иммунные клетки совершают ошибку и атакуют те самые клетки, которые они предназначены защищать.
4. Это может привести к различным аутоиммунным заболеваниям.
5. Они охватывают широкую категорию связанных заболеваний.
Эти заболевания называют связанными, не потому, что они поражают один какой – то орган или систему, а потому, что иммунная система больного человека нападает на его (или ее) собственную ткань.
6. Вы уже знаете, что ставят диагнозы этих болезней и «лечат» их врачи, имеющие разные специализации, например эндокринологи, невропатологи, дерматологи и др.
И каждый больной (за редким исключением) проходит долгий путь (несколько лет) и посещение нескольких врачей от появления первых симптомов до постановки диагноза.
Познакомьтесь со списком аутоиммунных заболеваний.
1. Болезнь Аддисона
2. Агаммаглобулинемия
3. Алопеция
4. Амилоидоз
5 .Анкилозирующий спондилоартрит
6 .Anti-GBM/Anti-ТВМ нефрит
7. Антифосфолипидный синдром
8. Аутоиммунная ангиодистрофия
9 .Аутоиммунная дисфункция
10 .Аутоиммунный энцефаломиелит
11. Аутоиммунный гепатит
12. Ауоиммунная болезнь внутреннего уха (AIED)
13. Аутоиммунный миокардит
14. Аутоиммунный панкреатит
15. Ауоиммунная ретинопатия
16 .Аутоиммунная крапивница
17. Аксональная и нейрональная невропатия (AMAN)
18. Болезнь Бало
19 .Болезнь Бехчета
20 .Доброкачестенный пемфигоид слизистой оболочки
21. Буллезный пемфигоид
22. Болезнь Каслмана (CD)
23. Целиакия
24. Болезнь Шагаса
25. Хроническая воспалительная демиелинизирующая полинейропатия (CIDP)
26. Хронический рецидивирующий мультифокальный остеомиелит (CRMO)
27. Churg-Strauss
28. Шрамлитрический пемфигоид
29. Синдром Когана
30. Холодная агглютининовая болезнь
31. Врожденный блог сердца
32. Коксаки миокардит
33 . Синдром CREST
34. Болезнь Крона
35 . Дерматит герпетиформный
36. Dermatomyositis
37. Болезнь Девика (neuromyelitis optica)
38. Дисковидная волчанка
39. Синдром Дресслера
40. Эндометриоз
41. Эозинофильный эзофагит (ЭО)
42 .Эозинофильный фасцит
43 .Узловая эритема
44 . Существенная смешанная криоглобулинемия
45. Фибромиалгия
46. Фиброзный альвеолит
47. Гигантский клеточный артериит (временный артериит)
48. Гигантский клеточный миокардит
49. Гломерулонефрит
50. Синдром Goodpasture
51. Гранулематоз с полиангититом
52. Болезнь Грейвса
53. Синдром Гийена – Барре
54. Тиреоидит Хашимото
55. Гемолитическая анемия
56. Хенок – Шонлейн пурпура (HSP)
57. Герпетическая гестация или пемфигоидная гестация (PG)
58. Hypogammalglobulinemia
59. IgG –нефропатия
60. Склерозирующее заболевание, связанное с IgG4
61 .Иммунная томбоцитопеническая пурпура (ITP)
62. Миозит в связи с включением (IBM)
63. Интерстициальный цистит (IC)
64. Ювенильный артрит
65. Несовершеннолетний диабет (диабет 1 типа)
66. Неcовершеннoлетний миозит (JM)
67. Болезнь Кавасаки
68. Синдром Ламберт – Итона
69. Лейкоцитокластический васкулит
70. Лишайник
71. Личиночный склероз
72. Лунный конъюнктивит
73. Линейная болезнь IgA (LAD)
74. Волчанка
75. Болезнь Лайма хроническая
76. Болезнь Меньера
77. Микроскопический полиангит (MPA)
78. Смешанная болезнь соединительной ткани (MCTD)
79. Язва Мурена
80. Болезнь Мухи – Хабермана
81. Рассеянный склероз
82. Myasthenia gravis
83. Миозит
84 . Нарколепсии
85. Neuromyelitis optica
86. Нейтропения
87 . Окулярный рубцовый пемфигоид
88. Оптический неврит
89. Палиндромный ревматизм (ОР)
90. PANDAS
91. Паранеопластическая мозжечковая дегенерация (ПХД)
92. Парксизмальная ночная гемоглобинурия (PNH)
93. Синдром Парри Ромберга
94. Партизм (периферический увеит)
95. Синдром Parsonnage-Turner
96. Пузырчатка
97. Периферическая невропатия
98. Периферический энцефаломиелит
99. Пернициозная анемия (ПА)
100. Синдром ПОЭМС
101. Номатода полиартериита
102. Полиглоточные синдромы типа I,II,III
103. Polymyalgia rheumatic
104. Полимиозит
105. Синдром постмиокардиального инфаркта
106. Постпикардиотомический синдром
107. Первичный билиарный цирроз
108. Первичный склерозирующий холангит
109. Прогестероновый дерматит
110. Псориаз
111. Псориатический артрит
112. Чистая аплазия красных клеток (PRCA)
113. Педиатрический гангреноз
114. Феномен Рейно
115. Реактивный артрит
116. Рефлекторная симпатическая дистрофия
117. Рецидивирующий полихондрит
118. Синдром беспокойных ног (RLS)
119. Ретроперитонеальный фиброз
120. Ревматическая лихорадка
121. Ревматоидный артрит
122. Саркоидоз
123. Синдром Шмидта
124. Склерит
125. Склеродермия
126. Синдром Шегрена
127. Аутоиммунитет cпepмы и яичка
128. Синдром тяжелого лица (SPS)
129. Подострый бактериальный эндокардит (SBE)
130. Синдром Сузака
131 . Симпатическая офтальмия (SO)
132. Артерии Такаясу
133. Временный артериит/Гигантский клеточный артериит
134. Тромбоцитопеническая пурпура (ТТП)
135. Синдром Толоса-Ханта (THS)
136. Поперечный миелит
137. Диабет 1 типа
138. Язвенный колит (UC)
139. Недифференцированная болезнь соединительной ткани (UCTD)
140. Увеит
141. Васкулит
142. Витилиго
143. Гранулематоз Вегенера (или гранулематоз с полиангититом (ГПД))
Вы видите, что список аутоиммунных заболеваний очень большой. Он поразил меня!
Возможно, я сделала ошибки в переводе названий каких-то болезней и буду благодарна, если вы поможете мне исправить эти ошибки.
Этот список создан и выложен на сайте Американской ассоциации аутоиммунных заболеваний (АААЗ), о которой я уже писала на блоге.
Более того, на сайте АААЗ этот список активный, то есть, нажав на название заболевания, вы можете попасть на другую страницу сайта с описанием этого конкретного заболевания.
Возможно, вам будет это интересно и полезно.
Напишите, пожалуйста, была ли эта статья вам интересна и полезна.
Важно знать родителям о здоровье:
FitoSpray для похудения (Фитоспрей)
FitoSpray для похудения ( Фитоспрей) FitoSpray — спрей для похудения Многие мечтают похудеть, стать стройными, обрести фигуру мечты. Неправильное питание,…
28 02 2023 17:53:58
Фитостеролы в продуктах питания
Фитостеролы в продуктах питания Фитостерины Существует много питательных веществ, которые, как утверждают исследователи, могут положительно повлиять на…
27 02 2023 4:29:17
Фитотерапевт
Фитотерапевт Фитотерапевт Я, Ирина Гудаева — травница, массажист, ведущая семинаров по созданию натуральной косметики и курса « Практическое травоведение»…
26 02 2023 13:47:58
Fitvid
Fitvid Брекеты: минусы, трудности, проблемы Брекет-системы помогли избавиться от комплексов миллионам людей. Это действительно эффективный инструмент,…
25 02 2023 13:36:13
Фониатр
Фониатр Фониатрия – один из разделов медицины. Фониатры изучают патологии голоса, методы их лечения, профилактики, а также способы коррекции…
22 02 2023 8:39:36
Форель
Форель Форель относится к отряду лососеобразных, семейству лососевых. Ее тело удлинено, немного сжато с боков, покрыто мелкой чешуей. Замечательной…
21 02 2023 2:16:19
Формула идеального веса
Формула идеального веса Калькулятор нормы веса Вес 65 кг относится к категории Норма для взрослого человека с ростом 170 см . Эта оценка основана на…
18 02 2023 2:16:25
Формулы расчета идеального веса
Формулы расчета идеального веса Фoрмулa «идeальнoго вeса» То, что ожирение шагает семимильными шагами по планете – это факт. И, несмотря на то, что…
17 02 2023 7:55:57
Фосфатида аммонийные соли
Фосфатида аммонийные соли Аммонийные соли фосфатидиловой кислоты ( Е442) Е442 – это пищевая добавка, которую относят к категории эмульгаторов. Вещество…
16 02 2023 22:14:10
Фототерапия новорожденных
Фототерапия новорожденных Фототерапия новорожденных Применение фототерапии для новорожденных С момента своего рождения организм ребенка начинает адаптацию…
15 02 2023 16:59:47
Фототерапия новорожденных при желтухе
Фототерапия новорожденных при желтухе Фототерапия новорожденных После появления ребенка на свет его организм адаптируется к совершенно иным условиям…
14 02 2023 0:44:56
Французская диета
Французская диета Французская диета Эффективность: до 8 кг за 14 дней Сроки: 2 недели Стоимость продуктов: 4000 рублей на 14 дней Общие правила…
13 02 2023 1:38:20
Фрукт Кумкват — что это такое?
Фрукт Кумкват — что это такое? Фрукт Кумкват — что это такое? Впервые упоминают необычный для европейцев фрукт китайские летописи 11 века. Португальские…
12 02 2023 9:59:36
Фруктовая диета
Фруктовая диета Фруктовая диета Эффективность: 2-5 кг за 7 дней Сроки: 3-7 дней Стоимость продуктов: 840-1080 рублей в неделю Общие правила Фруктовая…
10 02 2023 3:39:42
Фруктоза при диабете
Фруктоза при диабете Можно ли фруктозу при сахарном диабете? Для многих диабет является той проблемой, которая вносит в жизнь ряд ограничений. Так, к…
07 02 2023 6:12:30
Фрукт свити – польза и вред
Фрукт свити – польза и вред Свити — что это за фрукт? Что такое свити? Продолжаем разбирать цитрусовые, но как всегда идем не по верхам, а копаем глубже и…
04 02 2023 2:49:39
Фрукты и ягоды
Фрукты и ягоды Разница между фруктом и ягодой Фрукты и ягоды любят практически все. Ведь они такие вкусные и полезные! Мы любуемся лежащими на столе…
03 02 2023 7:31:27
Фтизиатр
Фтизиатр Врачи фтизиатры Москвы Фтизиатр — это дипломированный специалист в области фтизиатрии. Он специализируется на профилактике, диагностике, лечении…
01 02 2023 4:51:10
Фтор в организме человека
Фтор в организме человека Фтор в организме человека Дневная норма потрeбления Мужчины старше 60 лет Женщины старше 60 лет Беременные (2-я половина)…
31 01 2023 8:52:36
Боли в спине после рождения ребёнка
Боли в спине после рождения ребёнка Почему после родов болит спина У мамочек нередко болит спина после родов. Причем, дискомфорт может длиться довольно…
28 01 2023 8:24:24
Фунчоза: польза и вред
Фунчоза: польза и вред Фунчоза: польза и возможный вред Увлечение восточной кухней год от года растет. Принято считать, что такой рацион полезен для…
27 01 2023 15:59:10
Фундук
Фундук В рационе здорового человека обязательно присутствуют орехи в различных вариациях. Среди них выгодно выделяется фундук. Высокая пищевая ценность и…
26 01 2023 5:39:51
Галактоза
Галактоза Галактоза – это представитель класса простых молочных сахаров. В человеческий организм поступает преимущественно в составе молока,…
22 01 2023 9:35:32
Галанга
Галанга С древних времен растения играют важную роль в жизни человека, в том числе и для поддержания здоровья. Некоторые травы известны как лучшие…
21 01 2023 19:44:11
Галега лекарственная
Галега лекарственная Галега лекарственная (Galega officinalis) Син: козлятник лекарственный, козлятник аптечный, козья рута, французская сирень, солодянка…
20 01 2023 16:19:18
Боли в суставах при беременности
Боли в суставах при беременности Боли в суставах при беременности В период беременности у женщины могут возникать различные боли в самых разных местах….
17 01 2023 15:50:29
Гастрит и изжога
Гастрит и изжога Лучшие лекарства от изжоги и гастрита Многие пациенты с гастритом и другими заболеваниями Ж К Т страдают от изжоги. Данный симптом может…
16 01 2023 13:55:46
Где находится ключица у человека на фото?
Где находится ключица у человека на фото? Ключица человека: анатомия, строение, функции Ключица – это единственное костное образование в теле человека,…
13 01 2023 6:18:37
Человеческий костный мозг способствует выработке лимфоцитов. После проникновения в кровяное русло, они становятся незрелыми. К первому месту, где происходит их созревание, относится тимус, ко второму лимфатический узел. Локализацией тимуса является верхняя часть грудной клетки, а лимфатических узлов – шея, пах, подмышечная впадина. Т-лимфоцитами называются клетки после созревательного процесса в тимусе, а в-лимфоциты, созревшие в лимфатическом узле. Эти два вида лимфоцитов вырабатывают антитела, которые борются с чужеродными тканями и инфекциями. Реакция антитела направлена только на антиген, который ему соответствует. К примеру, у ребенка, который переболел свинкой, не будет вырабатываться иммунитет от кори.
Сутью вакцинации является знакомство иммунитета с определенного рода недугом. Ведение вакцины означает, что в организм проникает маленькая доза возбудителя, которая нужна для дальнейшего разрушительного действия антител на антигены. Однако встречаются ситуации, когда начинается атака лимфоцитов на ткани собственного организма. Так начинает развиваться аутоиммунные заболевания. Они встречаются приблизительно у 10 процентов населения мировых стран. Медицинская практика показывает, что редкие аутоиммунные заболевания поражают мужчин реже, чем женщин. Существует десять основных причин, вследствие которых наступает летальный исход. К таким причинам относится аутоиммунные и иммуннодефицитные заболевания.
В организме каждого человека есть иммунитет, который начинает свое развитие с момента рождения. В его состав входят специальные органы и клетки, защищающие от негативного микробного и вирусного воздействия. Иммунная система основана на механизме, способном различать собственную ткань от чужеродной. Различное повреждение провоцирует дисфункцию иммунитета, вследствие чего он перестает различать собственные клетки от чужих. Такое явление активирует производство аутоантител, ошибочно нападающих на здоровые клетки. В результате исчезает регуляторная работа т-лимфоцитов, появляются тяжелые аутоиммунные заболевания, которые поражают внутренние органы и системы организма.
Следует рассмотреть перечень аутоиммунных заболеваний. К первому типу относится расстройство, появляющееся, когда нарушается гистогематический барьер. Второй тип болезней появляется после того, как трансформируется ткань организма от физического, химического, вирусного воздействия. Происходит глубокие метаморфозные процессы в здоровых клетках, как результат – восприятие их чужими. Существуют случаи, когда происходит антигенная или экзоантигенная концентрация. Организм отреагирует повреждением клетки, на оболочке которой сохранился антигенный комплекс. Иногда контакт с вирусом провоцирует образование антигена, обладающего гибридным свойством. Это способно поразить центральную нервную систему.
В третью группу входят заболевания аутоиммунной системы, при которых происходит коалисценция ткани с экзоантигеном. В результате активизируется естественная реакция, направленная на пораженные участки. Четвертая группа включает недуги, причиной которых является генетическое отклонение или влияние неблагоприятного внешнего фактора. Это влечет стремительную мутацию клеток иммунитета, которая проявляется красной волчанкой.
Развитие заболевания аутоиммунного характера способно развиваться в любом возрасте. Несмотря на это, есть группа людей, у которых предрасположенность к аутоиммунным заболеваниям выше. А именно:
- Человек, который подвергается негативному воздействию внешних факторов. Специалисты по аутоиммунным заболеваниям в Москве выделяют влияние солнечного света, химических веществ, вирусной или бактериальной инфекции, которые вызывают патологические процессы в иммунной системе.
- Женщина в детородном возрасте. Аутоиммунные болезни встречаются у женщин чаще, чем у мужчин.
- Определенные расы и этнические группы. Признаки аутоиммунного заболевания чаще возникают у человека с белой кожей. К примеру, афроамериканцы и испанцы тяжело переносят системную красную волчанку.
- Наследственный фактор. Следует запомнить, что аутоиммунные заболевания передаются по наследству от ближайших родственников. Медицинская практика показывает, что в семейном анамнезе могут диагностироваться разные типы расстройства иммунитета.
Почему появляются
Медицинские исследования выделяют внутренние и внешние причины, почему возникают аутоиммунные заболевания. Одной из внутренних причин, когда происходит агрессия и бесконтрольное размножение лимфоцитов, является генная мутация первого типа. При этом исчезает распознавание лимфоцитами здоровых клеток. Человек получает по наследству от близкого родственника такое иммунное расстройство. Учитывая мутационный процесс в конкретном органе или системе, может развиться тиреоидит, зоб.
К другой внутренней причине относится генная мутация второго типа, при которой происходит бесконтрольное размножение лимфоцитов-санитаров. В результате появляются иммунные и аутоиммунные заболевания, которые, в основном, передаются по наследству. Среди внешних причин аутоиммунного заболевания выделяют тяжелую затяжную инфекционную болезнь, после которой происходит неадекватное поведение иммунных клеток, а также негативное воздействие факторов окружающей среды (радиация, ультрафиолетовые лучи). Возникновение сбоя иммунитет происходит из-за хитрости клетки-возбудителя недуга. Они способны притвориться схожими на собственные, но патогенные клетки. В результате лимфоциты теряют возможность распознавать чужеродные организмы, и начинают бороться с обоими.
Появляются системные аутоиммунные заболевания, когда нарушается целостность гематобарьера, которые отделяют определенный орган или ткань от крови. Нормой считается отсутствие проникновения в кровоток клеточных антигенов. Это значит, что т-лимфоциты не вырабатывают к ним толерантность. К забарьерным относят клетки мозга, щитовидки, и клетки, которые вырабатывают инсулин. При наличии такого механизма развивается хронический аутоиммунный простатит. Это значит, что спермопродуцирующие клетки отделяются от крови при помощи гематотестикулярного барьера. Инфицирование, воспаление, травма могут стать причинами нарушения его целостности, в результате начинается аутоагрессия, направленная на ткани простаты.
Какие виды аутоиммунных болезней существуют
Говоря о классификации расстройств, выделяют три группы аутоиммунных заболеваний. К первой группе относятся органоспецифические патологии, характеризующиеся направлением антител и лимфоцитов на аутоантиген одного или нескольких органов. Сюда относится забарьерный антиген, к которому нет врожденной толерантности. Вторая группа включает органонеспецифические болезни, когда происходит взаимодействие аутоантител и лимфоцитов с аутоантигенами ткани или органа. Патологический процесс развивается, когда уже существует толерантность. Третья группа состоит из вышеперечисленных механизмов.
Если человек столкнулся с иммунным расстройством, он заинтересуется, какой врач занимается аутоиммунными заболеваниями. При органоспецифической аутоиммунной болезни необходимо обратиться к профильному врачу. При смешанном или системном недуге требуется квалифицированная помощь многих врачей. Это невролог, гематолог, ревматолог, эндокринолог, кардиолог, пульмонолог, дерматолог, нефролог.
Что относится к аутоиммунным заболеваниям системного типа
Появление красной волчанки связано с нарушением аутоиммунного процесса, когда привлечены все внутренние органы. Недуг поражает два-три человека из тысячи. Возникает красная волчанка, когда в организме образовываются аномальные антитела из-за влияния генетического фактора. Подтверждением является наличие взаимосвязи патологии с нехваткой наследственных компонентов иммунитета. Кроме этого, спровоцировать появление иммунного расстройства может токсическое вещество, вирус, бесконтрольное употребление медикаментозных средств.
Системное расстройство на протяжении длительного времени протекает без симптомов, проявляется кожным высыпанием, нарушается опорно-двигательная система. Однако в это время в организме нарастает интенсивность иммунного дисбаланса, который может стать причиной воспалительного процесса любого внутреннего органа. Красная волчанка характеризуется поражением соединительной ткани, присутствующей в органах и системах. В результате обнаруживаются кожные высыпания на лице и груди, кожа становится чувствительной к воздействию ультрафиолета (покраснение, сыпь, пятна). Распознавательным признаком служит появление на теле дисковидного элемента, у которого красная окантовка, бледная середина.
При таком аутоиммунном заболевании симптомы следующие:
- Появление волчаночного артрита характеризуется резкими или ноющими болями, припухлостью, покраснением суставов, которые задействованы в патологическом процессе. После ограниченного движения пораженной конечности наступает полное обездвиживание костного сочленения.
- Поврежденные внешние серозные оболочки внутренних органов вызывают приступы кашля, боль при вдыхании и выдыхании. Доктор услышит влажный хрип в нижней доле легкого.
- Происходит поражение сердца и сосудов, появляется щемящая боль, нарушен ритм сокращений сердца.
- Из-за патологических сосудистых изменений, синеют стопы и кисти, холодеют конечности.
- Появление зрительных и слуховых галлюцинаций, состояние бреда.
- При абдоминальном синдроме появляется боль в животе, диарея, анорексия.
Если возникает вопрос, как выявить аутоиммунное заболевание, следует применить комплексное обследование, которое включает клинический, лабораторный, иммунологический, и гистологический метод. Врач назначит сдать кровь на общий анализ, пройти электрокардиографию, рентген, узи брюшной полости, почек. При своевременно начатом лечении аутоиммунного заболевания, у пациента возрастают шансы избежать патологического изменения внутреннего органа или системы. Терапевтические мероприятия состоят из приема противовоспалительных и подавляющих иммунитет препаратов, а также кортикостероидов.
Воспалительная миопатия
Сюда относится группа болезней, которые вызваны мышечным воспалением и слабостью. Наличие полимиозита и дерматомиозита зачастую диагностируется у женщин. Воспалительная миопатия вызывает медленно прогрессирующую слабость тех мышц, которые задают движение двух сторон тела. Дерматомиозит характеризуется кожной сыпью, сопровождающуюся слабостью в мышцах. Человек устает после длительной ходьбы или пребывания в стоячем положении. Отмечаются частые спотыкания, падение, затруднение при глотании пищи или воды, вдыхании или выдыхании воздуха.
Наличие миастении
Это аутоиммунное заболевание, как диагностировать и лечить, подскажут в клинике Москвы. Характеризуется атакой иммунитета нервов и мышц, которые присутствуют во всем теле. У человека с миастенией двоится в глазах, трудно сфокусировать взгляд и опускать веки. Появляется затрудненное глотание, частая отрыжка, удушье. Кроме этого выделяют:
- Наступление паралича, слабости.
- Трудно держать голову.
- Тяжело опускаться или подниматься по лестнице, поднимать вещи.
- Исчезает внятная речь.
Поражение псориазом
При таком недуге происходит избыточное и быстрое появление новых кожных клеток, накопление которых обнаруживается на кожном покрове. Заболевший человек замечает появление плотных красных пятен, которые покрыты чешуйкой. К области, где присутствуют такие пятна, относится голова, локти, колени. Также появляется зуд и болезненные ощущения, негативно сказывающиеся на работоспособности, ухудшающие сон.
Псориаз может сопровождаться формой артрита, при которой поражаются суставы и фаланги пальцев верхних и нижних конечностей. При затрагивании позвоночника появляется боль в области спины. Человек может обратиться за лечением аутоиммунного заболевания в Москве.
При синдроме Шегрена
Список аутоиммунных заболеваний у человека пополняется синдромом Шегрена, который характеризуется атакой слезных и слюнных желез. При таком синдроме у пациента выделяют такие признаки:
- Сухость глаз.
- Появление сильного кариеса зубов.
- Наличие сухости в полости рта.
- Помутнение в глазах.
- Затрудненное глотание пищи и напитков.
- Опухают и болят суставы.
- Обнаруживается опухлость гланд.
- Повышенная температура при аутоиммунном заболевании.
- Человек теряет вкусовые ощущения.
- Голос приобретает хриплый характер.
- Появление чрезмерной усталости.
Наличие склеродермии
Расстройство иммунитета, при котором появляется аномальное развитие соединительных тканей в кожном покрове и сосудах. Признаки склеродермии следующие:
- Появление одышки.
- Кожа утолщается.
- Видно обеление, покраснение или посинение пальцев верхних и нижних конечностей.
- Резко снижается масса тела.
- Появляется частые диареи или запоры.
- Кожа рук и предплечий становится блестящей.
- Болезненные ощущения, отечность пальцев.
- Кожа на лице натягивается, похожа на маску.
- Затрудненное глотание.
- Появляются раны на пальцах.
Выявление ревматоидного артрита
При перечислении, что относится к аутоиммунным заболеваниям, следует выделить ревматоидный артрит, при котором воспаляются суставы и окружающая их ткань. Появиться может в любом возрасте. Исследования по излечению аутоиммунного заболевания такого типа заключаются в сдаче анализа крови на наличие ревматоидного фактора, и магнитном резонансе пораженного сустава.
Наличие сахарного диабета
При определении, какие бывают аутоиммунные заболевания, следует отнести сахарный диабет первого типа, при котором нарушается обмен углеводов и воды. В результате нарушается функционирование поджелудочной, которой вырабатывается инсулин. Он помогает перерабатывать сахар. Недуг можно приобрести или получить по наследству. Нехватка инсулина провоцирует возникновение гнойничковых поражений кожного покрова. Начинают крошиться зубы, появляется чувство грудной жабы, скачет артериальное давление, нарушается функционирование почек, нервной системы, резкое ухудшение зрительной функции.
Симптоматика имеет постепенный характер. Начало сахарного диабета сопровождается следующими признаками:
- Медленно заживают раны.
- Присутствие постоянной сухости в ротовой полости.
- Повышается склонность к образованию гнойного процесса на кожных покровах и тканях.
- Обильное потоотделение.
- Слабость во всех мышцах.
- Появляется жажда, которую трудно утолить. В результате больному приходится выпивать несколько литров в сутки.
- Кожа начинает чесаться из-за чрезмерной сухости.
- Частые позывы к мочеиспусканию.
Наличие одного из вышеперечисленных симптомов служит поводом для сдачи крови на определение глюкозного показателя. Если отсутствует лечение аутоиммунного заболевания, появляются другие признаки:
- Изо рта слышен запах ацетона.
- Дисфункция зрительного органа.
- Теряется сознание.
- Постоянная головная боль.
- Лицо и голени отекают.
- Болезненные ощущения в сердце.
- Печень увеличена.
- Онемевают и болят ноги, что не позволяет полноценно ходить.
- Кожа на стопах теряет чувствительность.
- Резко повышается артериальное давление.
Человека, который столкнулся с сахарным диабетом, интересует, можно ли избавиться от аутоиммунного заболевания такого вида, к какому врачу обратиться, сколько будет длиться лечение. После проведенного обследования, врачом назначаются препарат, который стимулирует работу поджелудочной, чтобы вырабатывалось больше инсулина. А также медикаменты, способные повысить клеточную восприимчивость к инсулину, ингибиторы и агонисты. Для избавления от сахарного диабета следует соблюдать диетическое питание, в котором мало углеводов, не заниматься самолечением, посещать спортзал для повышения двигательной активности. Бывают случаи, когда необходимо вводить инсулин, чтобы нормализовать уровень глюкозы.
Выявление саркоидоза
Относится к редкому хроническому воспалительному заболеванию, которое поражает четыре человека из ста тысяч. Происходит поражение легких. Редко встречается у детей и лиц преклонного возраста. Саркоидоз характеризуется затрудненным дыханием при физической нагрузке, резким понижением массы тела, потере аппетита, чрезмерной утомляемостью. Может присоединиться апатия, слабость в мышцах, приступы кашля. Признаками саркоидоза являются отхаркивание с примесью крови, одышка, болезненные ощущения в груди. При запущенной форме снижается дыхательная функция из-за воспалительного процесса в легких. Может наблюдаться нарушение в глазном яблоке, суставах, кожном покрове. При отсутствии лечения аутоиммунных заболеваний иммуноглобулинами повышается риск полной потере зрения.
Появиться саркоидоз может из-за контакта с бериллием или цирконием, сильной реакции организма на грибковое воздействие, сосновую пыльцу, атипические микробактерии, а также при генетической предрасположенности. Для определения патологии делается рентген и кожное тестирование Квейма Силцбаха. При возникновении вопроса, как лечить аутоиммунное заболевание такого типа, необходимо посетить квалифицированного врача. Он определяет возбудителя болезни, сколько длиться недуг, и выписывает медикаментозные препараты, употребление которых поможет избежать поражения жизненно важных органов. Без своевременного не начать терапию, прогноз на аутоиммунное заболевание такого вида не утешительный. Человек может ослепнуть и получить дыхательную недостаточность.
Какая существует профилактика аутоиммунных заболеваний
Чтобы понизить риск возникновения иммунной патологии, следует полностью долечивать вирусную инфекцию, острые респираторные заболевания. В рацион человека должны входить продукты питания, в состав которых входят витамины и микроэлементы. А также свежие овощи, фрукты, цельное зерно, обезжиренные молочные продукты, постный источник белка. Исключить насыщенные жиры, холестерин, соль, рафинированный сахар. Количество приемов пищи составляет два-четыре раза.
Минимизировать стрессовые ситуации, нервное перенапряжение, так как нарушения в центральной нервной системе способствуют увеличению чувствительности иммунной системы к негативному воздействию внешнего и внутреннего фактора. Начать медитировать, читать книги, выбрать хобби. Также, человек должен полноценно отдыхать. Плохой сон провоцирует сбой в гормональной выработке. Заниматься умеренными физическими нагрузками, йогой. Повышать нагрузки необходимо только после консультации с врачом. Соблюдая профилактические правила, человек уменьшит вероятность появления иммунного расстройства.
Аутоиммунные заболевания – патологии, при которых нарушается работа иммунитета в целом или отдельных его компонентов. Ученые до сих пор бьются над разгадкой причин, побуждающих иммунную систему атаковать собственные здоровые клетки организма. По механизму аутоиммунизации все болезни делят на три типа, о чем подробнее и расскажет MedAboutMe.
Органоспецифичные аутоиммунные болезни
Этот тип недугов развивается из-за нарушения физиологических «фильтров», отделяющих тканевую жидкость от крови. В результате развивается нежелательная излишняя реакция иммунитета, которая и приводит к развитию самых разных болезней – рассеянного склероза, полиневрита, асперматогении, симпатической офтальмии. В этот же список попал и аутоиммунный тиреодит, который еще называют болезнью Хашимото по имени японского врача и ученого, впервые ее описавшего. Ее диагностируют у 3–4% населения Земли, причем женщины болеют в 4–8 раз чаще мужчин. Заболевание развивается из-за разрушения тиреоцитов – эпителиальных клеток щитовидной железы, подвергающихся агрессии собственных Т-лимфоцитов.
В результате паренхима щитовидной железы постепенно деградирует и развивается гипотиреоз – состояние, при котором этот орган эндокринной системы не может вырабатывать столько гормонов, сколько необходимо для нормальной жизнедеятельности организма. Ситуация ухудшается тем, что аутоиммунный тиреодит нередко сопровождается другими аутоиммунными болезнями эндокринного и соматического генеза. Это существенно ухудшает прогноз и требует более комплексного и серьезного лечения.
Рассеянный склероз не имеет никакого отношения к нарушению памяти, возникающему в пожилом возрасте. Речь идет о множественных «рубцах», разнесенных по всей центральной нервной системе. Это и есть очаги склероза, где нормальная ткань заменена соединительной. Болезнь чаще встречается как раз в молодом возрасте, когда человек полон сил и энергии. Вдруг ни с того ни с сего у него появляются разнообразные неврологические симптомы – утомляемость мышц при выполнении движений, нарушение согласованности действий, тремор конечностей, колебания глаз, учащение или задержка мочи и стула, нарушение поведения, снижение интеллекта. Толчком к развитию рассеянного склероза может стать дефицит витамина D, курение, стресс, вакцинация против гепатита В.
Органонеспецифичные аутоиммунные заболевания
Не только заболевание железы может быть связано с аутоиммунным воспалением. Есть патологии, которые развиваются из-за нарушений в системе иммунобиологического надзора. Можно сказать, что иммунитет «ополчается» против антигенов органов и тканей, что тоже приводит к развитию изменений, характерных для гиперчувствительности. Эта группа недугов состоит из красной системной волчанки, дерматомиозита, системной склеродермии, ревматоидного артрита и др. Последний имеет сложный аутоиммунный патогенез и вызывает прогрессирование инвалидности в 70% случаев, причем довольно быстро.
Кроме того, болезнь может давать осложнения, из-за которых развивается летальный исход. Ревматоидный артрит распространен по всему миру и вопреки расхожему мнению поражает не только пожилых, но и лиц молодого возраста, детей независимо от их расы. Каждый год 5–50 пациентам на 100000 населения ставят такой диагноз. Причины развития болезни могут быть самыми разными и на первый взгляд не связанными с работой суставов. Различные инфекции, эмоциональное потрясение, гормональная перестройка, тяжелая физическая работа – все это может привести к воспалению соединительной ткани и поражению суставов.
Для заболевания характерно медленное течение. Оно может развиваться годами, хотя в медицине зарегистрированы случаи и острого прогрессирования. Припухлость вокруг суставов – один из главных его симптомов, с которым многие больные и обращаются за помощью к врачу. При этом в суставах возникает спонтанная боль, усиливающаяся при активных движениях. Лечение болезни длительное, курсовое, требующее от человека большого терпения и сил. Кроме того, недуг накладывает отпечаток на привычный образ жизни, заставляет с осторожностью заниматься спортом, некоторые виды нагрузок таким больным и вовсе противопоказаны. Кроме того, им нельзя принимать противовирусные и иммуностимулирующие препараты, которые нередко назначают при сезонных инфекциях.
Болезни иммунитета промежуточного типа
В этот список вошли тиреотоксикоз, синдром Гудпасчера, сахарный диабет 1 типа, миастения гравис, синдром Шегрена и др. Последний недуг поражает соединительную ткань, вовлекая в атипичный процесс экзокринные железы – слюнные, слезные и др. Эта болезнь может возникать сама по себе, а может сопровождать другие аутоиммунные ревматические и другие болезни. Вызывая гибель вырабатывающих секрет клеток и эпителия выводных протоков, она повреждает железистую ткань, в результате чего слизистые оболочки ротовой полости, глаз, носоглотки, вагины и других органов приобретают повышенную сухость.
Деструктивный процесс может затронуть дыхательную, пищеварительную системы, мочеобразующие органы, вены и артерии, периферическую нервную систему. Зачастую человека сопровождает хроническая усталость. Он ощущает упадок сил, падение работоспособности, боль в суставах и мышцах. Синдром Шегрена, как и многие другие аутоиммунные болезни, отличается хроническим течением, за время которого наблюдаются как всплески недуга, так и его затихание с полной, либо частичной ремиссией. При этом какого-либо специфического лечения, способного восстановить работу желез, на сегодняшний день нет. Можно только облегчить самочувствие больного, минимизировать симптомы и поддержать его здоровье.
Надо сказать, что есть немало и других болезней, в патогенезе которых не последнюю роль играют аутоиммунные процессы. Одной из них является хроническая обструктивная болезнь легких, что подтверждает исследование специалистов, результат которого был опубликован в журнале The Physiological Society. Поэтому необходимо более пристально следить за своим здоровьем, постараться отказаться от вредных привычек и перейти на здоровое питание, начать заниматься спортом. Это повысит шансы на то, чтобы никогда не столкнуться с болезнями, вызванными агрессией собственного иммунитета.
Genetics of multiple sclerosis / Dyment D.A., Ebers G.C., Sadovnick A.D. // The Lancet. — Elsevier – 2004
Risk factors for antisperm antibodies in infertile men / A. Heidenreich, R. Bonfig, D. M. Wilbert et all // American Journal of Reproductive Immunology – 1989
Role of BAFF in pulmonary autoantibody responses induced by chronic cigarette smoke exposure in mice / Mathieu C. Morissette, Yang Gao, Pamela Shen et all // The Physiological Society – 2016
Аутоиммунные заболевания продолжают оставаться одной из
самых сложных проблем клинической иммунологии. Вот уже почти сто лет одной из главных догм иммунологии,
сформулированной Паулем Эрлихом, является представление о том, что в норме
иммунная система не должна развивать иммунный ответ против собственных тканей,
поскольку это может привести к гибели организма. П. Эрлих назвал это “ужасом
самоотравления” (“horror autotoxicus”). В настоящее время этот феномен известен
под названием “иммунная толерантность”, которая развивается в эмбриональном и
раннем постнатальном периоде и заключается в том, что в организме создаются
условия, при которых иммунная система не реагирует с аутоантигенами
(self-антигенами) (об этом уже упоминалось в соответствующей главе).
Таким образом, аутоиммунитет характеризуется потерей
(нарушением, исчезновением) толерантности, или естественной неотвечаемости по
отношению к собственным антигенам. Как следствие, продуцирующиеся аутоантитела
и/или цитотоксические клетки приводят к развитию заболевания.
Однако способность иммунной системы распознавать аутоантиген
не всегда несет патологический потенциал. Так, например, распознавание собственных
молекул главного комплекса гистосовместимости при реализации иммунного ответа,
антиидиотипический ответ против self-идиотипов и др.; все это позволяет
иммунной системе выполнить свою основную функцию иммунного надзора.
В настоящее время описано очень большое количество
аутоиммунных заболеваний. Предполагается, что иммунная система при
соответствующих условиях может развить иммунный ответ против любого
аутоантигена.
Аутоиммунные заболевания делят на две группы:
- органоспецифические
– например тяжелая миастения, тиреоидит Хашимото, болезнь Грейвса
(тиреотоксикоз с диффузным зобом) и др.; - системные
(неорганоспецифические) – например системная красная волчанка, ревматоидный
артрит и др.
Аутоиммунные заболевания (неполный перечень, призванный показать
встречаемость этой патологии практически во всех медицинских специальностях)
- Системная
красная волчанка - Ревматоидный
артрит - Склеродермия
- Дерматополимиозит
- Смешанные
болезни соединительной ткани - Синдром
Шегрена (сухой синдром) - Псориаз
- Витилиго
- Дерматит
герпетиформный - Пузырчатка
обычная - Буллезный
пемфигоид - Болезнь
(синдром Рейтера) - Болезнь
Бехтерева - Рассеянный множественный склероз
- Острый
(пост-)инфекционный полиневрит (синдром Гийена – Барре) - Тяжелая
миастения - Тиреоидит
Хашимото (аутоиммунный) - Болезнь
Грейвса (тиреотоксикоз с диффузным зобом) - Сахарный
диабет инсулинозависимый (I типа) - Аутоиммунное
поражение надпочечников (болезнь Аддисона) - Аутоиммунная
полиэндокринопатия - Саркоидоз
- Идиопатический
легочный фиброз - Неспецифический
язвенный колит - Болезнь Крона
(региональный энтерит) - Аутоиммунный
гастрит, тип А - Первичный
биллиарный цирроз - Хронический
активный гепатит - Аутоиммунная
энтеропатия - Целиакия
(глютенчувствительная энтеропатия) - Гломерулонефрит
- Синдром
Гудпасчера - Аутоиммунный
орхит - Аутоиммунное
бесплодие - Первичный
синдром антифосфолипидных антител - Аутоиммунный
увеит - Симпатическая
офтальмия - Аутоиммунный
конъюнктивит - Узловатый
полиартериит - Гигантоклеточный
гранулематозный артериит (ревматическая полимиалгия) - Пернициозная
анемия - Аутоиммунная
гемолитическая анемия - Аутоиммунная
тромбоцитопения - Аутоиммунная
нейтропения и др.
Хотя большинство из ~80 идентифицированных аутоиммунных
заболеваний относятся к редким, тем не менее в мире страдают миллионы людей.
Например, в США поражены 5% популяции – приблизительно 14 млн человек. В
Украине по теоретическим расчетам поражены приблизительно 2,3 млн человек.
В одних случаях развитие аутоиммунитета (срыв толерантности)
может быть первичным и служить причиной развития заболевания, в других,
особенно при длительных хронических заболеваниях (например хронический
пиелонефрит, хронический простатит и др.), – вторичным и являться следствием
заболевания, замыкая “порочный круг” патогенеза.
Нередко у одного и того же больного развивается несколько
аутоиммунных заболеваний, особенно это относится к аутоиммунным
эндокринопатиям.
Аутоиммунные заболевания часто ассоциируются с лимфоидной
гиперплазией, злокачественной пролиферацией лимфоидных и плазматических клеток,
иммунодефицитными состояниями – гипогаммаглобулинемией, селективным дефицитом
IgA, недостаточностью компонентов комплемента и др. Системные аутоиммунные
заболевания часто развиваются в зрелом возрасте.
В настоящее время предложено около двух десятков теорий,
объясняющих причины срыва толерантности и, как следствие, развития
аутоиммунитета. Приведем основные из них.
1.Теория “запретных”
клонов. Известно, что при индукции толерантности на определенных этапах развития (созревания) иммунной системы происходит
элиминация (разрушение) тех Т- и В-лимфоцитов, которые обладают аутореактивностью –
способностью реагировать с ауто (self) – антигенами. Согласно теории “запретных” клонов, по
тем или иным причинам в тимусе и костном мозге не происходит полная элиминация
аутореактивных Т- и В-лимфоцитов, что в будущем, при стечении определенных обстоятельств, может
привести к срыву толерантности.
2.Теория
секвестрированных (забарьерных) антигенов. Известно, что определенные ткани ограждены гистогематическими барьерами (половые
железы, ткани глаза, мозга, щитовидной железы и др.). В связи с этим при созревании
иммунной системы антигены таких тканей не контактируют с лимфоцитами и не
происходит элиминации соответствующих клонов клеток. При нарушении
гистогематического барьера и попадании антигенов в кровоток собственные иммунокомпетентные клетки распознают их как
чужеродные и запускают весь механизм иммунного ответа.
3.Теория
расстройства иммунологической регуляции(Поддержание толерантности на периферии).
- Снижение функции Т-лимфоцитов-супрессоров. Считается,
что Т-лимфоциты-супрессоры подавляют способность В-лимфоцитов продуцировать
антитела против собственных тканей, поддерживая таким образом состояние
толерантности. При снижении количества или функции Т-супрессоров потенциально
аутореактивные В-клетки начинают реагировать на собственные тканевые антигены,
а появляющиеся аутоантитела приводят к развитию аутоиммунного заболевания. - Нарушение
функции Т-лимфоцитов-хелперов. В частности, при ее повышении могут создаваться
условия, благоприятные для инициации ответа со стороны аутореактивных
В-лимфоцитов на собственные антигены, даже при нормальной функции
Т-супрессоров. Таким образом, потенциальные возможности развития
аутоиммунитета, имеющиеся в организме, реализуются за счет нормально
функционирующих иммунологических регуля-торных механизмов, включающих, прежде
всего. Т-лимфоциты – супрессоры и хелперы. - В последние
годы все большую популярность приобретает гипотеза, согласно которой в основе
аутоиммунной патологии лежат расстройства иммунной регуляции, обусловленные
нарушением продукции соответствующих цитокинов Т-лимфоцитами-хелперами I и II
типов, а также Т-регуляторными клетками. - Игнорирование
– объясняется отсутствием (или недостаточностью) презентации антигена, либо
отсутствием Т-клеток с рецептором для соответствующего антигенного пептида, находящегося
в бороздке молекулы ГКГ. Эти так называемые «дыры» в репертуаре Т-клеток,
которые объясняются тем, что в раннем периоде созревания толерантности
соответствующие клоны ауто-реактивных Т-клеток подверглись в тимусе клональной
делеции. - Анергия –
объясняется отсутствием ко-стимуляционных сигналов. В этом случае Т-клетка
своим антиген-распознающим сигналом распознает антиген в бороздке молекулы ГКГ,
но поскольку отсутствует дополнительный ко-стимуляционный сигнал, такая
Т-клетка подвергается апоптозу. - Регуляци я –
объясн яется су ществованием специа льных рег ул яторных Т-клеток (T-reg),
которые способны за счет цитокинов TGF и ИЛ-10 подавлять функцию Т-хелперов 1 и
Т-хелперов 2 типов. Кроме того, на поверхности T-reg имеется молекула CTLA4,
которая, связываясь с молекулой СД80/86 на поверхности АПК, препятствует
связыванию последней с молекулой СД28 на поверхности Т-лимфоцита, блокируя
таким образом ко-стимуляционный сигнал. В свою очередь, молекула CTLA4 через
молекулу СД80/86 передает обратный сигнал в антиген-презентирующую клетку,
повышая в ней экспрессию фермента индоламин-2,3-диоксигеназу, которая уменьшает
количество триптофана в Т-лимфоците, подавляя таким образом его активность.
4.Теория
нарушения идиотип-антиидиотипических взаимодействий.
Современные модели иммунного ответа предполагают, что
иммунная система обладает саморегулировкой и может реагировать на свои
собственные продукты с последующей супрессией или стимуляцией этой реакции.
Известно, что в сыворотке крови больных и здоровых лиц можно обнаружить
антитела против собственных Ig (первым антителом такого типа, обнаруженным у
человека, был ревматоидный фактор). Идиотипическая детерминанта (идиотип) тесно
связана с индивидуальной структурой активного центра молекулы Ig. Вначале
считалось, что продукция аутоантител против собственных Ig – результат
нарушения процесса распознавания “своего”, и это является либо причиной, либо
симптомом заболевания. Однако впоследствии многие исследователи обнаружили
антииммуноглобулины в сыворотке крови здоровых лип, исходя из чего
предположили, что продукция антииммуноглобулинов представляет собой физиологический,
а не патологический процесс. На этой основе была разработана модель иммунной
системы, в которой контрольно-регуляторные влияния зависят от множества
взаимодействующих компонентов, а антииммуноглобулины, направленные против
активного центра молекулы специфического антитела (антиидиотипические антитела)
играют ведущую роль. Было сделано предположение (N. К. Erne, 1974), что
распознавание идиотипических детерминант и развитие антиидиотипического
иммунного ответа представляет собой центральный механизм контроля и регуляции
биосинтеза антител. Эта теория получила название сетевой теории регуляции иммунного
ответа.
В теории Ерне можно выделить два основных положения:
- Иммуноглобулины,
а также иммуноглобулиновые рецепторы на поверхности антиген-реактивных Т- и
В-лимфоцитов имеют детерминанты, обладающие (ауто-) антигенными свойствами, и
получившие название “идиотип” (идиотипические детерминанты); - В организме
предсуществуют лимфоциты, способные в норме распознать своими рецепторами
идиотипические детерминанты и реализовать антиидиотипический ответ.
Анти-идиотипическое антитело также может быть распознано и на него вырабатываются
анти-антиидиотипические антитела до тех пор, пока иммунный ответ не угаснет.
Полагают, что идиотип и анти-антиидиотип являются идентичными структурами.
Исследования последних лет подтверждают важную роль
идиотип-антиидиотипических взаимодействий в регуляции иммунного ответа.
Необходимо выделить следующие основные положения:
- Антиидиотипический
ответ развивается одновременно с обычным иммунным ответом на чужеродные
антитела; - идиотип-антиидиотипические
взаимодействия обусловливают возможность как стимуляции, так и супрессии
лимфоцитов под влиянием антиидиотипических антител. С учетом этих данных,
становится ясно, что развивающийся одновременно с обычным иммунным ответом
антиидиотипический ответ, стимулируя или угнетая первый в зависимости от тех
или иных обстоятельств, обеспечивает его саморегуляцию по типу обратной связи.
Таким образом, при осуществлении иммунного ответа
развиваются антитела, иммунные комплексы и/или клеточно-опосредованный иммунный
ответ. Для того, чтобы сбалансировать эти медиаторы иммунопатологии и не дать
им “работать” против собственных тканей, одновременно включается регуляторный
механизм, представляющий собой сложную сеть Т-, В-клеток и антител,
координированный как антиидиотипический иммунный ответ. Этот механизм обеспечивает
контроль, необходимый для предотвращения повреждения органов-мишеней во время
бесчисленных иммунных реакций, генерируемых “хозяином” в пределах собственного
организма.
Из сказанного ясно, что нарушение идиотип-антиидиотипических
взаимодействий будет способствовать развитию аутоиммунных заболеваний.
5.Теория
поликлональной активации В-лимфоцитов. Обнаружено, что многие вещества химической
или биологической природы обладают способностью индуцировать активацию В-лимфоцитов,
которая приводит к их пролиферации и продукции антител. Как правило, такие антитела
относятся к иммуноглобулинам класса М. В том случае, если поликлональной активации
подверглись аутореактивные В-лимфоциты, продуцирующие аутоантитела, возможно
развитие аутоиммунного заболевания.
Поликлональные активаторы В-лимфоцитов липополисахарид
Очищенный белок туберкулина Протеин A Staphylococcus aureus Белок,
ассоциированный с липидом А Т-клеточные и макрофагальные лимфокины Fc-фрагмент
Ig
Протеолитические ферменты (например, трипсин) Полианионы
(например, декстрана сульфат) Антибиотики, (например, нистатин, амфотерицин В)
Микоплазма
Некоторые вирусы и вирусные компоненты (вирус Эпштейна-Барр,
вирус кори, белки теплового шока) Паразиты (Trypanosomacruzi, Plasmodiummalariae).
6.Теория
развития аутоиммунитета под влиянием суперантигенов.
Бактериальные суперантигены получили свое название в связи
со способностью активировать большое количество Т- и В-лимфоцитов независимо от
антигенной специфичности этих клеток. Выше упоминалось, что при классическом
варианте антигенного распознавания Т-хелпер активируется под влиянием
взаимодействия Т-клеточного антигенраспознающего рецептора (ТАГРР) и пептида,
который презентируется антигенпредставляющей клеткой (АПК) в ассоциации с
молекулой главного комплекса гистосовместимости класса II. При этом только один
(или несколько) Т-лимфоцитов-хелперов могут быть активированы. Активация Т-лимфоцитов-хелперов под влиянием суперантигенов
происходит совсем по-другому. В этом случае суперантиген не поглощается
антигенпредставляющей клеткой и не подвергается обычному перевариванию
(процессингу) с образованием пептида. При этом суперантиген как бы обходит этот
необходимый для специфического распознавания этап и неспецифически связывается
с вариабельной частью бета-цепи Т-клеточного распознающего рецептора вне его
антигенспецифической зоны (сайта). Происходит своеобразное перекрестное
связывание молекул главного комплекса гистосовместимости антигенпрезентирующей
клетки с Т-клеточным распознающим рецептором. В случае такого механизма
активации Т-лимфоцитов-хелперов возможна одновременная активация большого их
количества.
Таким образом, отличительные особенности стимуляции
Т-лимфоцитов под влиянием суперантигенов заключаются в следующем:
- Для этого
нет необходимости в переваривании (процессинге) антигена в
антигенпред-ставляющей клетке; - Такая
стимуляция не зависит от антигенной специфичности молекул комплекса HLA и
Т-клеточного распознающего рецептора; - Суперантиген
способен стимулировать в 103—104 раз больше лимфоцитов, чем процесси-рованный
антиген; - Аллогенный
(чужеродный) суперантиген может стимулировать как хелперы (CD4+), так и киллеры
(CD8+) Т-лимфоциты; - Аутологичный
(self) суперантиген может стимулировать только Т-лимфоциты-хелперы (CD4); - Для
полноценной стимуляции Т-лимфоцитов чужеродным суперантигеном необходим
дополнительный, костимуляционный, сигнал.
Чужеродные суперантигены описаны для Staphylococcus aureus
(энтеротоксины А, В, С и др., токсин, вызывающий синдром токсического шока,
эксфолиативные токсины). Streptococcus pyogenes (эритрогенный токсин, токсины
А, В, С, D); для Mycoplasma arthritidis. Под влиянием этих суперантигенов могут развиваться следующие
заболевания (состояния): пищевая токсикоинфекция, синдром токсического шока,
синдром чешуйчатой кожи, ревматическая лихорадка, артрит и др.
Установлено также, что некоторые опухолевые вирусы,
находящиеся в геноме клетки в форме провируса, могут кодировать продукцию
белка, который вызывает стимуляцию Т-лимфоцитов, выступая в качестве
суперантигена.
Рассматриваются три возможных механизма участия
суперантигенов в развитии аутоиммунных нарушений.
A.Активация
аутореактивных Т-лимфоцитов. Доказано, что суперантигены могут непосредственно активировать аутореактивные Т-лимфоциты, которые
затем мигрируют в соответ ствующие ткани и вызывают аутоиммунные нарушения, продуцируя
цитокины и/или реализуя свою киллинговую функцию.
Б.Активация аутореактивных В-лимфоцитов. Осуществляется за
счет того, что суперантиген связывает молекулы комплекса HLA класса II,
имеющиеся на В-лимфоцитах, с молекулой Т-клеточного антигенраспознающего
рецептора. В этом случае активация Т-лимфоцитов происходит без специфического
распознавания антигена, а неспецифически под влиянием суперантигена. Тем не
менее, такой Т-лимфоцит продуцирует соответствующие цитокины, которые
способствуют тому, что активированный аутореактивный В-лимфоцит начинает
продуцировать аутоантитела. Последние образуют иммунные комплексы и, оседая в
тканях, вызывают их повреждение. Не исключается, что В-лимфоциты могут
активироваться и через собственный ан-тигенраспознающий иммуноглобулиновый
рецептор.
B.Активация
антигенпредставляющих клеток. Суперантигены могут активировать антигенпредставляющие клетки, например макрофаги. Это
приводит к высвобождению из них цитокинов, супероксидных анионов и других
медиаторов воспаления. Активация макрофагов может также привести к нарушению
переваривания (процессинга) антигенов с последующей презентацией аутоантигенов
аутореактивным Т-лимфоцитам.
7.Теория
генетической предрасположенности. Согласно современным данным, существует генетически
детерминированная предрасположенность к развитию аутоиммунных заболеваний. Эта
предрасположенность контролируется по меньшей мере шестью генами, расположенными
на разных хромосомах. Часть из них расположена в главном комплексе
гистосовместимости (HLA) человека, роль которого в реализации иммунного ответа
является первостепенной.
Установлено, что большинство аутоиммунных заболеваний
ассоциируются с наличием в HLA-фенотипе человека следующих антигенов: DR2, DR3,
DR4 и DR5. Например, ревматоидный артрит ассоциируется с HLA-DR4, тиреоидит
Хашимото – с HLA-DR5, рассеянный множественный склероз – с HLA-DR2, системная
красная волчанка -с HLA-DR3.
Доказано также, что аутоиммунные заболевания развиваются
намного чаще у женщин, чем у мужчин. Например, частота встречаемости системной
красной волчанки у женщин в 6-9 раз выше, чем у мужчин. Считается, что в данном
случае важную роль играют половые гормоны.
В рамках теории генетической предрасположенности выдвинуто
несколько гипотез, объясняющих участие продуктов HLA-комплекса в патогенезе
заболеваний вообще и аутоиммунных в частности.
A.Согласно
рецепторной гипотезе, одной из наиболее ранних, определенные HLA-антигены являются рецепторами для вирусов, облегчающими их
фиксацию и проникновение вклетку. Эта гипотеза имеет много аргументов как в
свою пользу, так и против. Например, при таком заболевании явно вирусной
этиологии, как полиомиелит, а также при инфекционном мононуклеозе достоверной
корреляции с HLA-антигенами не обнаруживается.
Б.Гипотеза о модификации (изменении) аутологичного, своего,
антигена (altered self). Согласно этой гипотезе, модифицированный аутологичный
антиген распознается иммунной системой как чужеродный (nonself), что приводит к
срыву толерантности.
B.Гипотеза о
влиянии гипотетического Ir-гена на предрасположенность к заболеваниям (нарушение селекции антигенных детерминант, наличие “дыр”
в репертуаре Т-лимфоцитов,нарушение супрессии, опосредованной Т-лимфоцитами).
Г. Гипотеза о влиянии неклассических генов, картирующихся в
пределах системы HLA. Например гены HSP-70, TNF, недостаточность С4А, С2
ассоциируются с системной красной волчанкой и пиогенной инфекцией.
8.Теория
молекулярной мимикрии. Термин “мимикрия” в свое время был предложен для объяснения
подобия, идентичности антигенных детерминант некоторых микроорганизмов антигенным
детерминантам хозяина, в связи с чем их распознавание иммунной системой не происходит,
что и обусловливает развитие инфекционного заболевания. В настоящее время
теория молекулярной мимикрии видоизменилась и представлена двумя вариантами.
А. Согласно первому варианту теории, некоторые
микроорганизмы действительно обладают перекрестной реактивностью с антигенными
детерминантами хозяина возможно не за счет идентичности, а за счет достаточно
выраженного подобия (гомологии). Это обстоятельство имеет свое объяснение.
Действительно, главнейшая (и, видимо, первоначальная) роль иммунной системы
состоит в том, чтобы защитить организм от инфекций. Для этой цели основные
клетки иммунной системы – Т- и В-лимфоциты – снабжены антигенраспознающими
рецепторами самой разной специфичности, что позволяет им распознать любой,
внедрившийся в организм инфекционный агент.
Распознав чужеродный агент, иммунная система защищается
двумя основными механизмами: 1) продукцией гуморальных антител; 2) генерацией
цитотоксических Т-лимфоцитов. При первом механизме зашиты антитела поражают
внеклеточные инфекционные агенты и их токсины, образуя иммунные комплексы; при
втором механизме – для спасения всего организма ци-тотоксическим Т-лимфоцитам
приходится разрушать собственные клетки, в которых прячутся внутриклеточные
возбудители.
Таким образом, иммунитет к инфекционным агентам довольно
часто имеет иммунологический компонент либо в виде иммунных комплексов, либо в
виде цитотоксических Т-лимфоцитов. Отсюда следует, что, развивая противоинфекционный
ответ, иммунная система должна “выбирать” силу, с которой она защищается: ответ
должен быть достаточным для элиминации возбудителя, но безвредным для
организма. Этот баланс зависит от многих условий: а) степени выраженности и
продолжительности инфекции; б) повреждающего действия патогена и степени
иммунного ответа; в) количества и значимости тех клеток хозяина, которые были
разрушены при попытке элиминации внутриклеточного возбудителя.
Микроорганизмы экспрессируют множество антигенов, которые
подобны, если не идентичны, антигенам хозяина. Если бы все Т- и В-лимфоциты,
способные реагировать с этими антигенами, были элиминированы в период создания
толерантности, то в защитных способностях иммунной системы были бы большие
пробелы, что позволило бы этим микроорганизмам беспрепятственно внедряться в
организм. Однако это не так, следовательно, те Т- и В-лимфоциты, которые
распознают инфекционные агенты, обладающие антигенами, подобными антигенам хозяина
(перекрестно реагирующие антигены), могут реагировать с собственными клетками,
т. е. обладают аутореактивностью.
Таким образом, при создании толерантности в эмбриональном и
раннем постнатальном периоде полного разрушения аутореактивных Т- и
В-лимфоцитов не наступает. Сохранив ауто-реактивные Т- и В-лимфоциты, организм
увеличивает возможности иммунной системы противостоять инфекционным агентам,
обладающим подобными антигенными структурами. И как следствие, развитие
протективного антиинфекционного иммунного ответа при определенных условиях может
приводить к развитию аутоиммунного ответа .
Однако следует учитывать, что далеко не всегда аутоиммунный
ответ (особенно в виде продукции гуморальных аутоантител после инфекционных
заболеваний) заканчивается развитием аутоиммунного заболевания.
Б. Согласно второму варианту теории молекулярной мимикрии,
собственные (ауто-, self-) антигены хозяина могут модифицироваться под влиянием
различных факторов: длительного воздействия инфекционных агентов, влияния
свободных радикалов. N0, ксенобиотиков, лекарственных средств, воздействия
факторов окружающей среды (ионизирующее и ультрафиолетовое излучение,
воздействие низких температур и т. п.). В результате таких воздействий
аутоантигены изменяются и распознаются иммунной системой как чужеродные
(non-self). Продуцирующиеся аутоантитела и цитотоксические лимфоциты
связываются не только с модифицированными аутоантигенами, но и с истинными
аутоантигенами за счет все той же перекрестной реактивности (мимикрии,
подобия).
В иммунологических механизмах повреждения тканей при
аутоиммунных заболеваниях принимают участие все те эффекторные механизмы,
которыми иммунная система защищает организм от экзогенной интервенции
-гуморальные антитела, иммунные комплексы, цитотоксические Т-лимфоциты и
цитокины. В развитии патологического процесса указанные факторы могут действовать
как порознь, так и совместно.
При прямом действии аутоантител на клетки и ткани организма,
как правило, активируется система комплемента, которая способствует их
разрушению. Возможен вариант “включения” механизма антителозависимого клеточно-опосредованного
лизиса, т.е. с участием К-клеток. В некоторых случаях аутоантитела,
направленные против функционально значимых клеточных рецепторов, стимулируют
или ингибируют специализированную функцию клеток без ее разрушения.
В том случае, когда формируются циркулирующие иммунные
комплексы, состоящие из ауто-антигена и аутоантител, разные причины могут
вызвать их оседание в микроциркуляторном русле различных органов (почка,
суставы, кожа и др.) или в местах гемодинамически напряженных, с выраженным
турбулентным течением (бифуркации, отхождение крупных сосудов и т. п.). В
местах отложения иммунных комплексов активируется комплемент, скапливаются
гранулоциты и моноциты, выделяющие различные ферменты. Все это приводит к
гибели клеток “шокового” органа и развитие воспаления.
Созревание цитотоксических Т-лимфоцитов приводит к их
накоплению в пораженной ткани (околососудистая инфильтрация) с последующим
развитием киллингового эффекта, привлечением большого количества клеток
воспаления.
Как правило, в развитие аутоиммунных заболеваний, вовлечены
иммунные механизмы, соотвествую-щие I, III и IV типам иммунных реакций по
классификации Джела и Кумбса .
Ауто (self) антигены (пептиды) образуются антигенпрезентирующими
клетками во время процес-синга поглощенных клеточных фрагментов (например,
апоптические тельа) и могут презентировать-ся молекулами HLA класса I или
класса II. Презентация внутриклеточных аутопептидов молекулами HLA I класса
способствует созреванию аутоцитотоксических Т-лимфоцитов; в свою очередь,
презентация внеклеточных аутопептидов молекулами HLA II класса способствует
созреванию аутоантител.
В последние годы в развитии аутоиммунного повреждения клеток
и тканей большое внимание уделяют провоспалительным цитокинам— ИЛ-1, альфа-ОНФ,
гамма-ИНФ, ИЛ-2, а также включению механизмов апоптоза. Сегодня имеются
доказательства того, что аутоиммунные повреждения тканей могут быть реализованы
за счет механизма неспецифического связывания Fas + FasL и включения апоптоза.
Обусловлено это тем, что на поверхности клеток, например, В-клеток
поджелудочной железы и олигодендроцитах, под воздействием различных стимулов
(прежде всего, цитокинов) появляется Fas-рецептор. Аутореактивные Т-лимфоциты,
экспрессирующие FasL, могут связываться с Fas-рецептором и индуцировать
апоптотическую смерть клеток-мишеней.
Интересны также следующие наблюдения. Считают, что
конститутивная (изначальная) экспрессия FasL на поверхности клеток
привилегированных органов (например, глаз, яичек) носит защитный характер,
позволяя индуцировать апоптоз у Fas-положительных лимфоцитов при их попадании в
соответствующие ткани. Но наличие на поверхности одной и той же клетки
Fas-рецептора и Fas-лиганда может быть причиной аутокринного суицида такой
клетки. Подобный механизм рассматривается как одна из причин развития
тиреоидита Хашимото (на тироцитах есть FasL, а при определенных воздействиях на
мембране тироцитов начинают сильно экспресси-роваться Fas-рецепторы).
Наличие аутоантител само по себе еще не указывает на
развитие заболевания. В невысоких титрах аутоантитела постоянно обнаруживаются
в сыворотке крови здоровых лиц и участвуют в поддержании гомеостаза,
обеспечивают выведение продуктов метаболизма, идиотипический контроль и другие
физиологические процессы.
Исходя из приведенных данных, можно дать определение понятий
“аутоиммунный процесс” и “аутоиммунное заболевание”.
Аутоиммунный процесс (аутоиммунитет) – это форма иммунного
ответа, индуцированная аутоантигенными детерминантами в условиях нормы и
патологии; является одним из механизмов поддержания гомеостаза. Выраженность
аутоиммунных процессов в условиях нормы незначительная.
Аутоиммунное заболевание – это патологический процесс, в
патогенезе которого важную роль играют аутоантитела и/или клеточный
аутоиммунный ответ.
Признаки, по которым то или иное заболевание может быть
отнесено к разряду аутоиммунных, сформулированы еще Л. Витебски (1961).
- Наличие
аутоантител или цитотоксических Т-лимфоцитов, направленных против антигена, ассоциированного
с данным заболеванием. - Идентификация
аутоантигена, против которого направлен иммунный ответ. - Перенос
аутоиммунного процесса с помощью сыворотки, содержащей антитела или
цито-токсические Т-лимфоциты. - Возможность
создания с помощью введения аутоантигена экспериментальной модели заболевания с
развитием соответствующих морфологических нарушений, характерных для заболевания.
Общие принципы иммуно-лабораторной диагностики аутоиммунных
заболеваний основываются на следующих признаках:
- Наличие
специфических аутоантител; - Наличие
специфической клеточной сенсибилизации (выявляется с помощью реакции
бласттрансформации – РБТ и теста ингибиции миграции лейкоцитов в присутствии
соответствующего аутоантигена); - Повышение
уровня гамма-глобулина и/или IgG; - Изменение
количества Т-хелперов, Т-супрессоров и Т-регуляторных клеток, приводящее к
срыву толерантности; - Снижение
уровня СЗ и С4 компонентов комплемента; - Отложения
иммунных комплексов в пораженных тканях (IgG, IgM, СЗ, С4 и фибрин); - Лимфоидно-клеточная
инфильтрация пораженных тканей; - Определение
HLA-фенотипа.