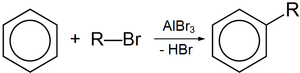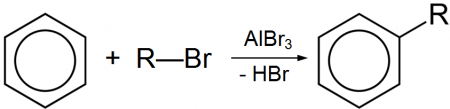| Бромид алюминия | |
 |
|
 |
|
| Общие | |
|---|---|
| Систематическое наименование | Бромид алюминия |
| Химическая формула | AlBr3, Al2Br6 |
| Эмпирическая формула | AlBr3 |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Молярная масса | 266,69 г/моль |
| Плотность | 3,205[1] г/см³ |
| Термические свойства | |
| Температура плавления | 97,5[1] °C |
| Температура кипения | 255[2] °C |
| Энтальпия образования (ст. усл.) | − 514; − 422 (AlBr3, газ); − 971(Al2Br6, газ)[3] кДж/моль |
| Структура | |
| Кристаллическая структура | моноклинная |
| Классификация | |
| Рег. номер CAS | 7727-15-3 |
| Рег. номер EINECS | 231-779-7 |
Броми́д алюми́ния (бромистый алюминий) — это неорганическое бинарное соединение. Химическая формула 
Содержание
- 1 Физические свойства
- 2 Химические свойства
- 3 Получение
- 4 Применение
- 5 Опасность для здоровья
- 6 Литература
- 7 Примечания
Физические свойства
Безводный бромид алюминия представляет собой бесцветное кристаллическое вещество, плавящееся при температуре 97,5 °C; температура кипения: 255 °C.
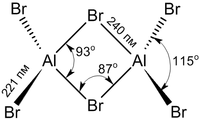
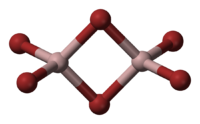
В твёрдой и жидкой фазе существует в форме димера Al2Br6, частично диссоциирующего в AlBr3, в газовой фазе масс-спектры показывают наличие ди-, тетра- и гексаформ: Al2Br6, Al4Br12, Al6Br18 соответственно.
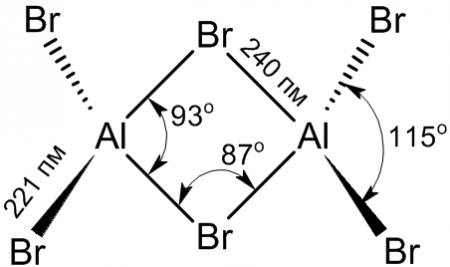
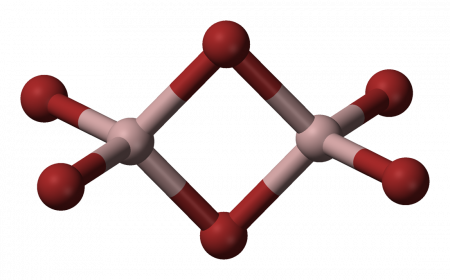
Структура молекулы бромида алюминия Al2Br6 представляет собой сдвоенные тетраэдры, в центре которых расположены атомы алюминия, ковалентно связанные с атомами брома[4].
Координационное число алюминия в молекуле бромида равно 4[5].
Энергия разрыва связи Al—Br в молекуле бромида алюминия составляет примерно 358 кДж/моль[6].
Вещество очень гигроскопично: на воздухе расплывается, легко поглощая влагу с образованием гексагидрата AlBr3•6H2O[7]. Хорошо растворимо в воде, спирте, сероуглероде, ацетоне[8]; плотность водного раствора при 20 °C составляет: 1079,2 кг/м³ (10%-ный раствор), 1172,5 кг/м³ (20%-ный раствор)[9].
Химические свойства
- Безводный бромид алюминия очень энергично реагирует с водой выделяя при растворении много тепла и, частично гидролизуясь:
- При нагревании водного раствора гидролиз можно провести полностью:
- Вступает в реакцию со щелочами:
- При пропускании безводного сероводорода через раствор бромида алюминия в сероуглероде выпадает осадок комплексного соединения[10]:
- При высокой температуре разлагается:
- При нагревании бромида алюминия с алюминием в газовой фазе (1000 °C) образуется нестабильный монобромид алюминия[2]:
- С гидридом лития образует алюмогидрид:
- Бромид алюминия — сильный акцептор электронных пар (кислота Льюиса) — легко присоединяет молекулы доноры (на этом, в частности, основано его применение в органическом синтезе)[7]:
Получение
Безводный бромид алюминия получают взаимодействием элементов (Al и Br2) при нагревании:
Водный раствор можно получить реакцией алюминиевой стружки с бромоводородной кислотой:
Применение
Коммерческое применение бромида алюминия в настоящий момент относительно небольшое.
Бромид алюминия входит как основной компонент в состав ксилольных электролитов для электроосаждения алюминиевых покрытий[11].
Безводный бромид алюминия используется в органическом синтезе, в частности, в реакции алкилирования по Фриделю-Крафтсу, по аналогии с хлоридом алюминия.
Соединение может выступать катализатором в реакции изомеризации бромалканов, например[12]:
Также бромид алюминия может выступать в качестве бромирующего агента, например в реакции с хлороформом[13]:
Опасность для здоровья
При контакте с кожей бромид алюминия может вызывать ожоги.
Соединение умеренно ядовито: ЛД50 (крысы) ≈ 1600 мг/кг (перорально); ЛД50 (крысы) ≈ 815 мг/кг (внутрибрюшинно)[14].
Литература
- Downs A.J. Chemistry of aluminium, gallium, indium, and thallium. — First edition. — London: Chapman & Hall, 1993. — 526 p. — ISBN 0-7514-0103-X
Примечания
- ↑ 1 2 Лидин Р.А., Андреева Л.Л., Молочко В.А. Глава 3. Физические свойства // Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 74. — ISBN 5-7107-8085-5
- ↑ 1 2 Турова Н.Я. Неорганическая химия в таблицах. — М.: Высший химический колледж РАН, 1997. — С. 67.
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Часть IV. Термодинамика. Глава 1. Энтальпия образования, энтропия и энергия Гиббса образования веществ // Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 441. — ISBN 5-7107-8085-5
- ↑ Chambers C., Holliday A.K. Modern inorganic chemistry. — Chichester: Butterworth & Co (Publishers) Ltd, 1975. — P. 153.
- ↑ Дроздов А.А., Зломанов В.П., Мазо Г.Н., Спиридонов Ф.М. Неорганическая химия. Т.2: Химия непереходных элементов / Под ред. акад. Ю.Н.Третьякова. — М.: Издательский центр «Академия», 2004. — Т. 2. — С. 86. — ISBN 5-7695-1436-1
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Глава 6. Энергия связи для многоатомных частиц // Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 384. — ISBN 5-7107-8085-5
- ↑ 1 2 Ахметов Н.С. Общая и неорганическая химия. Учебник для вузов. — 4-е изд., исправленное. — М.: «Высшая школа», 2001. — С. 498. — ISBN 5-06-003363-5
- ↑ Алюминий // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1988. — Т. 1. — С. 207.
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Часть VII. Плотность воды и водных растворов. Глава 3. Соли // Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 641. — ISBN 5-7107-8085-5
- ↑ Гофман У., Рюдорф В., Хаас А. и др. Руководство по неорганическому синтезу. — Пер. с нем., под ред. Г.Брауэра. — М.: «Мир», 1985. — Т. 3. — С. 899.
- ↑ Спиридонов Б.А., Федянин В.И. Исследование процесса электроосаждения алюминия из пара-ксилольных электролитов.. Российское общество гальванотехников и специалистов в области обработки поверхности.(недоступная ссылка — история) Проверено 26 октября 2009.
- ↑ Douwes H.S.A. The kinetics of the aluminium bromide catalyzed isomerization of 1-propyl bromide (англ.) // Journal of Molecular Catalysis A: Chemical. — 2005. — Т. 240. — № 1-2. — С. 82-90.
- ↑ Unated States Patent 2553518. Production of Organic Bromides (англ.) (pdf). FreePatentsOnline (May, 1951). Архивировано из первоисточника 9 апреля 2012. Проверено 26 октября 2009.
- ↑ Safety data for aluminium bromide (англ.). The Physical and Theoretical Chemistry Laboratory Oxford University. Архивировано из первоисточника 9 апреля 2012. Проверено 26 октября 2009.
|
Растворимость кислот, оснований и солей в воде |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
Соединения алюминия |
|---|
|
Алюминат лития (LiAlO2) • Алюминат натрия (NaAlO2) • Алюмогидрид кальция (Ca[AlH4]2) • Алюмогидрид лития (LiAlH4) • Алюмосиликаты • Антимонид алюминия (AlSb) • Арсенид алюминия (AlAs) • Ацетат алюминия (Al(CH3COO)3) • Бромид алюминия (AlBr3) • Гексафтороалюминат аммония ((NH3)3[AlF6]) • Гексафтороалюминат натрия (Na3[AlF6]) • Гидрид алюминия (AlH3) • Гидроксид алюминия (Al(OH)3) • Диборид алюминия (AlB2) • Додекаборид алюминия (AlB12) • Иодид алюминия (AlI3) • Карбид алюминия (Al4C3) • Метагидроксид алюминия (AlO(OH)) • Молибдат алюминия (Al2(MoO4)3) • Монооксид алюминия (AlO) • Монофторид алюминия (AlF) • Монохлорид алюминия (AlCl) • Нитрат алюминия (Al(NO3)3) • Нитрид алюминия (AlN) • Оксид алюминия (Al2O3) • Оксинитрид алюминия (AlON) • Селенид алюминия (Al2Se3) • Силикат алюминия (Al2SiO5) • Сульфат алюминия (Al2(SO4)3) • Сульфат алюминия-калия (KAl(SO4)2) • Сульфид алюминия (Al2S3) • Тетрагидридоалюминат лития (Li[AlH4]) • Тетрагидридоалюминат натрия (Na[AlH4]) • Тетрагидридоалюминат калия (K[AlH4]) • Тетрагидридоалюминат цезия (Cs[AlH4]) • Триизобутилалюминий (Al(C4H9)3) • Триметилалюминий (Al(CH3)3) • Трифенилалюминий (Al(C6H5)3) • Трифторид алюминия (AlF3) • Триэтилалюминий (Al(C2H5)3) • Фосфат алюминия (AlPO4) • Фосфид алюминия (AlP) • Хлорид алюминия (AlCl3) |
|
Соединения брома |
|---|
|
Бромат калия (KBrO3) • Бромат кальция (Ca(BrO3)2) • Бромат натрия (NaBrO3) • Бромат серебра (AgBrO3) • Бромат стронция (Sr(BrO3)2) • Броматы • Бромид алюминия (AlBr3) • Бромид бора(III) (BBr3) • Бромид диртути(2+) (Hg2Br2) • Бромид магния (MgBr2) • Бромид меди(I) (CuBr) • Бромид меди(II) (CuBr2) • Бромиды • Бромистая кислота (HBrO2) • Бромистоводородная кислота (HBr) • Бромная кислота (HBrO4) • Бромноватая кислота (HBrO3) • Бромноватистая кислота (HBrO) • Бромопентакарбонилрений(I) (Re(CO)5Br) • Броморганические соединения • Гипобромистая кислота (HOBr) • Диоксид брома (BrO2) • Оксид брома (Br2O) • Пербромат калия (KBrO4) • Фторид брома(I) (BrF) • Фторид брома(III) (BrF3) • Фторид брома(V) (BrF5) • Хлорид брома (BrCl) |
Aluminum, one of the components of aluminium bromide, accounts for over 8.1 percent of the Earth’s crust, making it one of the most prevalent minerals on the planet. Despite the fact that it is present in a wide range of compounds on Earth, aluminium is rarely discovered in its free metal state. Instead, it is frequently found in minerals such as bauxite and cryolite. Bromine, the other component of aluminium bromide, is a poisonous, oily, crimson liquid. Bromine, in addition to being employed in the manufacture of dyes, pesticides, and fertilizers, is occasionally detected in trace amounts in living species, although having no known biological purpose in humans.
What is Aluminium Bromide?
Aluminum bromide is a pale yellow chemical solution, also known as tribromoalumane or aluminium tribromide (the most common form). It is a colorless, hygroscopic solid that may be sublimated. Its molecular or chemical formula is AlBr3.
It appears in its anhydrous state as a white to yellowish-red compound with a lumpy solid and a strong odour. It appears as a liquid in its watery form. It is extremely damaging to the eyes, mucous membranes, and skin. It is frequently utilized in the production of many compounds. It is a solution in a wide range of organic solvents, including benzene, toluene, simple hydrocarbons, nitrobenzene, and xylene.
Structure of Aluminium Bromide
The formula of Aluminium Bromide is made up of one aluminium cation (Al3+) and one bromide anion (Br–). Therefore, the molecular or chemical formula of Barium sulfate is AlBr3. Its chemical formula reveals that it is composed of one aluminium atom and three bromine atoms. It has a molecular mass of 266.694 g/mol as an anhydrous chemical and 374.785 g/mol as a hexahydrate. It has a monoclinic crystalline structure with a positive dipole moment.
Physical Properties of Aluminium Bromide
- Aluminium Bromide is a white to pale yellow powder with a pungent smell.
- It is a colorless, sublimable hygroscopic solid which occurs mostly in the form of Aluminium tribromide.
- The density of Aluminium Bromide is 3.2 g/cm3 as anhydrous and 2.54 g/cm3 as a hexahydrate.
- The melting point of Aluminium Bromide is 97.5 °C as an anhydrous and 93 °C as a hexahydrate.
- The boiling point of Aluminium Bromide is 255 °C as an anhydrous and 252 °C as a hexahydrate.
- The heat capacity of Aluminium Bromide is 100.6 J J/mol K.
- The standard molar entropy of Aluminium Bromide is 180.2 J J/mol K.
- The standard enthalpy of formation of Aluminium Bromide is −572.5 kJ/mol.
- Its aqueous solution is neutral in nature with a pH of 6 at 14 °C.
- It is slightly soluble in methanol, diethyl ether, acetone but entirely soluble in water.
Chemical Properties of Aluminium Bromide
- At 100 °C, aluminium tribromide combines with carbon tetrachloride to produce carbon tetrabromide.
4 AlBr3 + 3 CCl4 → 4 AlCl3 + 3 CBr4
- It reacts with phosgene gas to produce carbonyl bromide and aluminium chlorobromide.
AlBr3 + COCl2 → COBr2 + AlCl2Br
- Water hydrolyzes Al2Br6 in line with the properties of Lewis acid. Furthermore, water hydrolysis occurs during the development of HBr and the production of the Al-OH-Br species. It also reacts fast with alcohol and carboxylic acids.
Uses of Aluminium Bromide
- It is used as a catalyst in Friedel–Crafts reactions.
- It is used as a medication in the field of health.
- As it is a more powerful Lewis acid than Al2Cl6, it is employed in industries to create various substances.
- It acts as an electron pair acceptor to increase the reactivity of a substrate.
- It has a number of specific chemical uses in synthesis and extractive metallurgy.
Sample Questions
Question 1: What is the process for the preparation of Aluminium Bromide?
Solution:
Aluminium bromide is prepared by the reaction of Hydrogen bromide (HBr) with aluminium metal (Al).
2 Al + 6 HBr → Al2Br6 + 3 H2
The second method to obtain Aluminium Bromide is through bromination.
2 Al + 3 Br2 → Al2Br6
Question 2: How does aluminium bromide exist in nature?
Solution:
In the solid state, solutions in noncoordinating solvents (e.g., CS2), the melt, and the gas phase, the dimeric form of aluminium tribromide (Al2Br6) predominates. These dimers only break down into monomers at high temperatures.
Al2Br6 → 2 AlBr3 (ΔH°diss = 59 kJ/mol)
Question 3: What are the side effects of aluminium bromide?
Solution:
Aluminum Bromide can harm you if inhaled. It is a highly corrosive chemical and direct contact can severely irritate and burn the skin and eyes, perhaps causing eye damage. It may irritate the nose, throat, and lungs, resulting in coughing, wheezing, and/or shortness of breath. Aluminum bromide is a reactive chemical that might cause an explosion.
Question 4: How can one check if he/she is exposed to aluminium bromide?
Solution:
The exposure of hazardous materials such as aluminium bromide should be assessed on a regular basis. This might entail taking personal and regional air samples. A worker’s employer can provide him with copies of the sample findings.
Question 5: Explain some methods of reducing exposure to aluminium bromide.
Solution:
Methods of Reducing Exposure to Aluminium Bromide are:
- Enclose activities and employ local exhaust ventilation at the place of chemical discharge wherever practicable. Respirators should be worn if no local exhaust ventilation or enclosure is employed.
- Wear appropriate job clothes.
- Wash carefully after being exposed to aluminum bromide and at the end of the workshift.
- Furthermore, as part of a continuing education and training effort, communicate to potentially exposed personnel all information on the health and safety concerns of Aluminum Bromide.
Aluminum, one of the components of aluminium bromide, accounts for over 8.1 percent of the Earth’s crust, making it one of the most prevalent minerals on the planet. Despite the fact that it is present in a wide range of compounds on Earth, aluminium is rarely discovered in its free metal state. Instead, it is frequently found in minerals such as bauxite and cryolite. Bromine, the other component of aluminium bromide, is a poisonous, oily, crimson liquid. Bromine, in addition to being employed in the manufacture of dyes, pesticides, and fertilizers, is occasionally detected in trace amounts in living species, although having no known biological purpose in humans.
What is Aluminium Bromide?
Aluminum bromide is a pale yellow chemical solution, also known as tribromoalumane or aluminium tribromide (the most common form). It is a colorless, hygroscopic solid that may be sublimated. Its molecular or chemical formula is AlBr3.
It appears in its anhydrous state as a white to yellowish-red compound with a lumpy solid and a strong odour. It appears as a liquid in its watery form. It is extremely damaging to the eyes, mucous membranes, and skin. It is frequently utilized in the production of many compounds. It is a solution in a wide range of organic solvents, including benzene, toluene, simple hydrocarbons, nitrobenzene, and xylene.
Structure of Aluminium Bromide
The formula of Aluminium Bromide is made up of one aluminium cation (Al3+) and one bromide anion (Br–). Therefore, the molecular or chemical formula of Barium sulfate is AlBr3. Its chemical formula reveals that it is composed of one aluminium atom and three bromine atoms. It has a molecular mass of 266.694 g/mol as an anhydrous chemical and 374.785 g/mol as a hexahydrate. It has a monoclinic crystalline structure with a positive dipole moment.
Physical Properties of Aluminium Bromide
- Aluminium Bromide is a white to pale yellow powder with a pungent smell.
- It is a colorless, sublimable hygroscopic solid which occurs mostly in the form of Aluminium tribromide.
- The density of Aluminium Bromide is 3.2 g/cm3 as anhydrous and 2.54 g/cm3 as a hexahydrate.
- The melting point of Aluminium Bromide is 97.5 °C as an anhydrous and 93 °C as a hexahydrate.
- The boiling point of Aluminium Bromide is 255 °C as an anhydrous and 252 °C as a hexahydrate.
- The heat capacity of Aluminium Bromide is 100.6 J J/mol K.
- The standard molar entropy of Aluminium Bromide is 180.2 J J/mol K.
- The standard enthalpy of formation of Aluminium Bromide is −572.5 kJ/mol.
- Its aqueous solution is neutral in nature with a pH of 6 at 14 °C.
- It is slightly soluble in methanol, diethyl ether, acetone but entirely soluble in water.
Chemical Properties of Aluminium Bromide
- At 100 °C, aluminium tribromide combines with carbon tetrachloride to produce carbon tetrabromide.
4 AlBr3 + 3 CCl4 → 4 AlCl3 + 3 CBr4
- It reacts with phosgene gas to produce carbonyl bromide and aluminium chlorobromide.
AlBr3 + COCl2 → COBr2 + AlCl2Br
- Water hydrolyzes Al2Br6 in line with the properties of Lewis acid. Furthermore, water hydrolysis occurs during the development of HBr and the production of the Al-OH-Br species. It also reacts fast with alcohol and carboxylic acids.
Uses of Aluminium Bromide
- It is used as a catalyst in Friedel–Crafts reactions.
- It is used as a medication in the field of health.
- As it is a more powerful Lewis acid than Al2Cl6, it is employed in industries to create various substances.
- It acts as an electron pair acceptor to increase the reactivity of a substrate.
- It has a number of specific chemical uses in synthesis and extractive metallurgy.
Sample Questions
Question 1: What is the process for the preparation of Aluminium Bromide?
Solution:
Aluminium bromide is prepared by the reaction of Hydrogen bromide (HBr) with aluminium metal (Al).
2 Al + 6 HBr → Al2Br6 + 3 H2
The second method to obtain Aluminium Bromide is through bromination.
2 Al + 3 Br2 → Al2Br6
Question 2: How does aluminium bromide exist in nature?
Solution:
In the solid state, solutions in noncoordinating solvents (e.g., CS2), the melt, and the gas phase, the dimeric form of aluminium tribromide (Al2Br6) predominates. These dimers only break down into monomers at high temperatures.
Al2Br6 → 2 AlBr3 (ΔH°diss = 59 kJ/mol)
Question 3: What are the side effects of aluminium bromide?
Solution:
Aluminum Bromide can harm you if inhaled. It is a highly corrosive chemical and direct contact can severely irritate and burn the skin and eyes, perhaps causing eye damage. It may irritate the nose, throat, and lungs, resulting in coughing, wheezing, and/or shortness of breath. Aluminum bromide is a reactive chemical that might cause an explosion.
Question 4: How can one check if he/she is exposed to aluminium bromide?
Solution:
The exposure of hazardous materials such as aluminium bromide should be assessed on a regular basis. This might entail taking personal and regional air samples. A worker’s employer can provide him with copies of the sample findings.
Question 5: Explain some methods of reducing exposure to aluminium bromide.
Solution:
Methods of Reducing Exposure to Aluminium Bromide are:
- Enclose activities and employ local exhaust ventilation at the place of chemical discharge wherever practicable. Respirators should be worn if no local exhaust ventilation or enclosure is employed.
- Wear appropriate job clothes.
- Wash carefully after being exposed to aluminum bromide and at the end of the workshift.
- Furthermore, as part of a continuing education and training effort, communicate to potentially exposed personnel all information on the health and safety concerns of Aluminum Bromide.
From Wikipedia, the free encyclopedia

|
|

|
|
| Names | |
|---|---|
| Preferred IUPAC name
Aluminium bromide |
|
| Other names
Aluminic bromide Aluminium(III) bromide Aluminium tribromide |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChemSpider |
|
| ECHA InfoCard | 100.028.891 |
| EC Number |
|
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
| UN number | 1725 |
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
AlBr3 Al2Br6 AlBr3·6H2O (hexahydrate) |
| Molar mass | 266.694 g/mol (anhydrous) 374.785 g/mol (hexahydrate)[1] |
| Appearance | white to pale yellow powder[1] |
| Odor | pungent |
| Density | 3.2 g/cm3 (anhydrous) 2.54 g/cm3 (hexahydrate)[1] |
| Melting point | 97.5 °C (anhydrous) 93 °C (hexahydrate)[1] |
| Boiling point | 255 (anhydrous)[1] |
|
Solubility in water |
very soluble, partially hydrolyses indicated by a fuming solution and an optional appearance of white precipitate |
| Solubility | slightly soluble in methanol, diethyl ether, acetone |
| Structure[2] | |
|
Crystal structure |
Monoclinic, mP16 (anhydrous) |
|
Space group |
P21/c, No. 14 |
|
Lattice constant |
a = 0.7512 nm, b = 0.7091 nm, c = 1.0289 nm α = 90°, β = 96.44°, γ = 90° |
|
Formula units (Z) |
4 |
| Thermochemistry[1] | |
|
Heat capacity (C) |
100.6 J/(mol·K) |
|
Std molar |
180.2 J/(mol·K) |
|
Std enthalpy of |
-572.5 kJ/mol |
| Hazards | |
| GHS labelling: | |
|
Pictograms |
 
|
|
Signal word |
Danger |
|
Hazard statements |
H302, H314 |
|
Precautionary statements |
P260, P264, P270, P280, P301+P312, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P310, P321, P330, P363, P405, P501 |
| NFPA 704 (fire diamond) |
3 1 1 |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
1598 mg/kg (oral, rat) |
| Related compounds | |
|
Other anions |
aluminium trichloride aluminium triiodide |
|
Other cations |
boron tribromide |
|
Related compounds |
iron(III) bromide |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Aluminium bromide is any chemical compound with the empirical formula AlBrx. Aluminium tribromide is the most common form of aluminium bromide.[3] It is a colorless, sublimable hygroscopic solid; hence old samples tend to be hydrated, mostly as aluminium tribromide hexahydrate (AlBr3·6H2O).
Structure[edit]
The dimeric form of aluminium tribromide (Al2Br6) predominates in the solid state, in solutions in noncoordinating solvents (e.g. CS2), in the melt, and in the gas phase. Only at high temperatures do these dimers break up into monomers:
- Al2Br6 → 2 AlBr3 ΔH°diss = 59 kJ/mol
The species aluminium monobromide forms from the reaction of HBr with Al metal at high temperature. It disproportionates near room temperature:
- 6/n «[AlBr]n» → Al2Br6 + 4 Al
This reaction is reversed at temperatures higher than 1000 °C. Aluminium monobromide has been crystallographically characterized in the form the tetrameric adduct Al4Br4(NEt3)4 (Et = C2H5). This species is electronically related to cyclobutane. Theory suggest that the diatomic aluminium monobromide condenses to a dimer and then a tetrahedral cluster Al4Br4, akin to the analogous boron compound.[4]
Al2Br6 consists of two AlBr4 tetrahedra that share a common edge. The molecular symmetry is D2h.
The monomer AlBr3, observed only in the vapor, can be described as trigonal planar, D3h point group. The atomic hybridization of aluminium is often described as sp2. The Br-Al-Br bond angles are 120 °.
Synthesis[edit]
Experiment showing synthesis of aluminum bromide from the elements.
By far the most common form of aluminium bromide is Al2Br6. This species exists as hygroscopic colorless solid at standard conditions. Typical impure samples are yellowish or even red-brown due to the presence of iron-containing impurities. It is prepared by the reaction of HBr with Al:
- 2 Al + 6 HBr → Al2Br6 + 3 H2
Alternatively, the direct bromination occurs also:
- 2 Al + 3 Br2 → Al2Br6
Reactions[edit]
A demonstration of the reaction of the exothermic reaction of the strong Lewis acid (Al2Br6) and strong Lewis base (H2O).
Al2Br6 dissociates readily to give the strong Lewis acid, AlBr3. Regarding the tendency of Al2Br6 to dimerize, it is common for heavier main group halides to exist as aggregates larger than implied by their empirical formulae. Lighter main group halides such as boron tribromide do not show this tendency, in part due to the smaller size of the central atom.
Consistent with its Lewis acidic character, Al2Br6 is hydrolyzed by water with evolution of HBr and formation of Al-OH-Br species. Similarly, it also reacts quickly with alcohols and carboxylic acids, although less vigorously than with water. With simple Lewis bases (L), Al2Br6 forms adducts, such as AlBr3L.
Aluminium tribromide reacts with carbon tetrachloride at 100 °C to form carbon tetrabromide:
- 4 AlBr3 + 3 CCl4 → 4 AlCl3 + 3 CBr4
and with phosgene yields carbonyl bromide and aluminium chlorobromide:[citation needed]
- AlBr3 + COCl2 → COBr2 + AlCl2Br
Al2Br6 is used as a catalyst for the Friedel-Crafts alkylation reaction.[3] Related Lewis acid-promoted reactions include as epoxide ring openings and decomplexation of dienes from iron carbonyls. It is a stronger Lewis acid than the more common Al2Cl6.
Safety[edit]
Aluminium tribromide is a highly reactive material.[5]
References[edit]
- ^ a b c d e f Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton, FL: CRC Press. p. 4.45. ISBN 1-4398-5511-0.
- ^ Troyanov, Sergey I.; Krahl, Thoralf; Kemnitz, Erhard (2004). «Crystal structures of GaX3(X= Cl, Br, I) and AlI3«. Zeitschrift für Kristallographie. 219 (2–2004): 88–92. doi:10.1524/zkri.219.2.88.26320. S2CID 101603507.
- ^ a b Paquette, Leo A. (2001). Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X. hdl:10261/236866. ISBN 0471936235.
- ^ Dohmeier, Carsten; Loos, Dagmar; Schnöckel, Hansgeorg (1996). «Aluminum(I) and Gallium(I) Compounds: Syntheses, Structures, and Reactions». Angewandte Chemie International Edition in English. 35 (2): 129. doi:10.1002/anie.199601291.
- ^ Renfew, Malcom M. (1991). «Hazardous laboratory chemicals: Disposal guide (Armour, M.A.)». Journal of Chemical Education. 68 (9): A232. Bibcode:1991JChEd..68Q.232R. doi:10.1021/ed068pA232.2.
From Wikipedia, the free encyclopedia

|
|

|
|
| Names | |
|---|---|
| Preferred IUPAC name
Aluminium bromide |
|
| Other names
Aluminic bromide Aluminium(III) bromide Aluminium tribromide |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChemSpider |
|
| ECHA InfoCard | 100.028.891 |
| EC Number |
|
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
| UN number | 1725 |
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
AlBr3 Al2Br6 AlBr3·6H2O (hexahydrate) |
| Molar mass | 266.694 g/mol (anhydrous) 374.785 g/mol (hexahydrate)[1] |
| Appearance | white to pale yellow powder[1] |
| Odor | pungent |
| Density | 3.2 g/cm3 (anhydrous) 2.54 g/cm3 (hexahydrate)[1] |
| Melting point | 97.5 °C (anhydrous) 93 °C (hexahydrate)[1] |
| Boiling point | 255 (anhydrous)[1] |
|
Solubility in water |
very soluble, partially hydrolyses indicated by a fuming solution and an optional appearance of white precipitate |
| Solubility | slightly soluble in methanol, diethyl ether, acetone |
| Structure[2] | |
|
Crystal structure |
Monoclinic, mP16 (anhydrous) |
|
Space group |
P21/c, No. 14 |
|
Lattice constant |
a = 0.7512 nm, b = 0.7091 nm, c = 1.0289 nm α = 90°, β = 96.44°, γ = 90° |
|
Formula units (Z) |
4 |
| Thermochemistry[1] | |
|
Heat capacity (C) |
100.6 J/(mol·K) |
|
Std molar |
180.2 J/(mol·K) |
|
Std enthalpy of |
-572.5 kJ/mol |
| Hazards | |
| GHS labelling: | |
|
Pictograms |
 
|
|
Signal word |
Danger |
|
Hazard statements |
H302, H314 |
|
Precautionary statements |
P260, P264, P270, P280, P301+P312, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P310, P321, P330, P363, P405, P501 |
| NFPA 704 (fire diamond) |
3 1 1 |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
1598 mg/kg (oral, rat) |
| Related compounds | |
|
Other anions |
aluminium trichloride aluminium triiodide |
|
Other cations |
boron tribromide |
|
Related compounds |
iron(III) bromide |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Aluminium bromide is any chemical compound with the empirical formula AlBrx. Aluminium tribromide is the most common form of aluminium bromide.[3] It is a colorless, sublimable hygroscopic solid; hence old samples tend to be hydrated, mostly as aluminium tribromide hexahydrate (AlBr3·6H2O).
Structure[edit]
The dimeric form of aluminium tribromide (Al2Br6) predominates in the solid state, in solutions in noncoordinating solvents (e.g. CS2), in the melt, and in the gas phase. Only at high temperatures do these dimers break up into monomers:
- Al2Br6 → 2 AlBr3 ΔH°diss = 59 kJ/mol
The species aluminium monobromide forms from the reaction of HBr with Al metal at high temperature. It disproportionates near room temperature:
- 6/n «[AlBr]n» → Al2Br6 + 4 Al
This reaction is reversed at temperatures higher than 1000 °C. Aluminium monobromide has been crystallographically characterized in the form the tetrameric adduct Al4Br4(NEt3)4 (Et = C2H5). This species is electronically related to cyclobutane. Theory suggest that the diatomic aluminium monobromide condenses to a dimer and then a tetrahedral cluster Al4Br4, akin to the analogous boron compound.[4]
Al2Br6 consists of two AlBr4 tetrahedra that share a common edge. The molecular symmetry is D2h.
The monomer AlBr3, observed only in the vapor, can be described as trigonal planar, D3h point group. The atomic hybridization of aluminium is often described as sp2. The Br-Al-Br bond angles are 120 °.
Synthesis[edit]
Experiment showing synthesis of aluminum bromide from the elements.
By far the most common form of aluminium bromide is Al2Br6. This species exists as hygroscopic colorless solid at standard conditions. Typical impure samples are yellowish or even red-brown due to the presence of iron-containing impurities. It is prepared by the reaction of HBr with Al:
- 2 Al + 6 HBr → Al2Br6 + 3 H2
Alternatively, the direct bromination occurs also:
- 2 Al + 3 Br2 → Al2Br6
Reactions[edit]
A demonstration of the reaction of the exothermic reaction of the strong Lewis acid (Al2Br6) and strong Lewis base (H2O).
Al2Br6 dissociates readily to give the strong Lewis acid, AlBr3. Regarding the tendency of Al2Br6 to dimerize, it is common for heavier main group halides to exist as aggregates larger than implied by their empirical formulae. Lighter main group halides such as boron tribromide do not show this tendency, in part due to the smaller size of the central atom.
Consistent with its Lewis acidic character, Al2Br6 is hydrolyzed by water with evolution of HBr and formation of Al-OH-Br species. Similarly, it also reacts quickly with alcohols and carboxylic acids, although less vigorously than with water. With simple Lewis bases (L), Al2Br6 forms adducts, such as AlBr3L.
Aluminium tribromide reacts with carbon tetrachloride at 100 °C to form carbon tetrabromide:
- 4 AlBr3 + 3 CCl4 → 4 AlCl3 + 3 CBr4
and with phosgene yields carbonyl bromide and aluminium chlorobromide:[citation needed]
- AlBr3 + COCl2 → COBr2 + AlCl2Br
Al2Br6 is used as a catalyst for the Friedel-Crafts alkylation reaction.[3] Related Lewis acid-promoted reactions include as epoxide ring openings and decomplexation of dienes from iron carbonyls. It is a stronger Lewis acid than the more common Al2Cl6.
Safety[edit]
Aluminium tribromide is a highly reactive material.[5]
References[edit]
- ^ a b c d e f Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton, FL: CRC Press. p. 4.45. ISBN 1-4398-5511-0.
- ^ Troyanov, Sergey I.; Krahl, Thoralf; Kemnitz, Erhard (2004). «Crystal structures of GaX3(X= Cl, Br, I) and AlI3«. Zeitschrift für Kristallographie. 219 (2–2004): 88–92. doi:10.1524/zkri.219.2.88.26320. S2CID 101603507.
- ^ a b Paquette, Leo A. (2001). Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X. hdl:10261/236866. ISBN 0471936235.
- ^ Dohmeier, Carsten; Loos, Dagmar; Schnöckel, Hansgeorg (1996). «Aluminum(I) and Gallium(I) Compounds: Syntheses, Structures, and Reactions». Angewandte Chemie International Edition in English. 35 (2): 129. doi:10.1002/anie.199601291.
- ^ Renfew, Malcom M. (1991). «Hazardous laboratory chemicals: Disposal guide (Armour, M.A.)». Journal of Chemical Education. 68 (9): A232. Bibcode:1991JChEd..68Q.232R. doi:10.1021/ed068pA232.2.
| Бромид алюминия | ||
|---|---|---|
|
||
| Систематическое наименование |
Бромид алюминия | |
| Хим. формула | AlBr3, Al2Br6 | |
| Рац. формула | AlBr3 | |
| Состояние | твёрдое | |
| Молярная масса | 266,69 г/моль | |
| Плотность | 3,205 | |
| Температура | ||
| • плавления | 97,5 | |
| • кипения | 255 °C | |
| Энтальпия | ||
| • образования | − 514; − 422 (AlBr3, газ); − 971(Al2Br6, газ) кДж/моль |
|
| Кристаллическая структура | моноклинная | |
| Рег. номер CAS | 7727-15-3 | |
| PubChem | 24409 | |
| Рег. номер EINECS | 231-779-7 | |
| SMILES |
[Al](Br)(Br)Br |
|
| InChI |
1S/Al.3BrH/h;3*1H/q+3;;;/p-3 PQLAYKMGZDUDLQ-UHFFFAOYSA-K |
|
| RTECS | BD0350000 | |
| Номер ООН | 1725 | |
| ChemSpider | 22818 | |
| Пиктограммы ECB |  |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. |
Бромид алюминия (бромистый алюминий) — это неорганическое бинарное соединение. Химическая формула Al+3Br3−1. Вещество представляет собой соль алюминия и бромоводородной кислоты. В твердом и жидком состоянии существует в форме димера: Al2Br6.
Физические свойства
Безводный бромид алюминия представляет собой бесцветное кристаллическое вещество, плавящееся при температуре 97,5 °C; температура кипения: 255 °C.
В твёрдой и жидкой фазе существует в форме димера Al2Br6, частично диссоциирующего в AlBr3, в газовой фазе масс-спектры показывают наличие ди-, тетра- и гексаформ: Al2Br6, Al4Br12, Al6Br18 соответственно.
Структура молекулы бромида алюминия Al2Br6 представляет собой сдвоенные тетраэдры, в центре которых расположены атомы алюминия, ковалентно связанные с атомами брома.
Координационное число алюминия в молекуле бромида равно 4.
Энергия разрыва связи Al—Br в молекуле бромида алюминия составляет примерно 358 кДж/моль.
Вещество очень гигроскопично: на воздухе расплывается, легко поглощая влагу с образованием гексагидрата AlBr3•6H2O. Хорошо растворимо в воде, спирте, сероуглероде, ацетоне; плотность водного раствора при 20 °C составляет: 1079,2 кг/м³ (10%-ный раствор), 1172,5 кг/м³ (20%-ный раствор).
Химические свойства
- Безводный бромид алюминия очень энергично реагирует с водой выделяя при растворении много тепла и, частично гидролизуясь:
- AlBr3 + 4 H2O ⇆ [Al(H2O)4]3+ + 3Br−
- [Al(H2O)4]3+ + H2O ⇆ [Al(H2O)3(OH)]2+ + H3O+
- При нагревании водного раствора гидролиз можно провести полностью:
- AlBr3 + 3 H2O = Al(OH)3 ↓ + 3 HBr ↑
- Вступает в реакцию со щелочами:
- AlBr3 + 3 NaOH = Al(OH)3 ↓ + 3 NaBr
- AlBr3 + 4 NaOH = Na[Al(OH)4] + 3 NaBr
- При пропускании безводного сероводорода через раствор бромида алюминия в сероуглероде выпадает осадок комплексного соединения:
- AlBr3 + H2S = AlBr3 ⋅ H2S
- При высокой температуре разлагается:
- 2 AlBr3 = 2 Al + 3 Br2
- При нагревании бромида алюминия с алюминием в газовой фазе (1000 °C) образуется нестабильный монобромид алюминия:
- AlBr3 + 2 Al ⇆ 3 AlBr
- С гидридом лития образует алюмогидрид:
- AlBr3 + 4 LiH = Li[AlH4] + 3 LiBr
- Бромид алюминия — сильный акцептор электронных пар (кислота Льюиса) — легко присоединяет молекулы-доноры (на этом, в частности, основано его применение в органическом синтезе):
- AlBr3 + C2H5Br → [C2H5]+[AlBr4]−
Получение
Безводный бромид алюминия получают взаимодействием простых веществ (Al и Br2):
2 Al + 3 Br2 = Al2Br6
Водный раствор можно получить реакцией алюминиевой стружки с бромоводородной кислотой:
2 Al + 6 HBr = 2 AlBr3 + 3 H2 ↑
Применение
Коммерческое применение бромида алюминия в настоящий момент относительно небольшое.
Бромид алюминия входит как основной компонент в состав ксилольных электролитов для электроосаждения алюминиевых покрытий.
Безводный бромид алюминия используется в органическом синтезе, в частности, в реакции алкилирования по Фриделю-Крафтсу, по аналогии с хлоридом алюминия.
Соединение может выступать катализатором в реакции изомеризации бромалканов, например:
CH3−CH2−CH2Br →AlBr3 CH3−CHBr−CH3
Также бромид алюминия может выступать в качестве бромирующего агента, например в реакции с хлороформом:
CHCl3 + HBr →90oC; AlBr3 CHBrCl2 + HCl
Опасность для здоровья
При контакте с кожей бромид алюминия может вызывать ожоги.
Соединение умеренно ядовито: ЛД 50 (крысы) ≈ 1600 мг/кг (перорально); ЛД50 (крысы) ≈ 815 мг/кг (внутрибрюшинно).
Поиск химических веществ по названиям или формулам.
Справочник содержит названия веществ и описания химических формул (в т.ч. структурные формулы и скелетные формулы).
Введите часть названия или формулу для поиска:
Языки:
По умолчанию |
Все возможные |
Из списка
|
Применить к найденному
Бромид алюминия
Брутто-формула:
AlBr3
CAS# 7727-15-3
Категории:
Неорганические соли
PubChem CID: 24409
| ChemSpider ID: 22818
| NSC 87608
Названия
Русский:
- Бромид алюминия [Wiki]
- бромистый алюминий
English:
- Aluminic bromide
- Aluminium bromide [Wiki]
- Aluminium tribromide(IUPAC)
- Aluminium(III) bromide
- EINECS:231-779-7
- UN1725
- UN2580
- tribromoalumane(IUPAC)
Варианты формулы:
AlBr3
Al(+3)Br(-1)3
BrAl<|Br>/Br
Br-Al<`|Br>-Br
Br^-$L(1.3)Al^3+<|0Br^->/0Br^-
Вещества, имеющие отношение…
Анион:
Бромиды
Химический состав
Реакции, в которых участвует Бромид алюминия
-
{M}{X}3 + 3{R}OH -> {M}(OH)3″|v» + 3{R}{X}
, где M =
Al Cr Fe Ti La; X =
Cl F Br I; R =
Li Na K Rb Cs NH4 -
Al(OH)3 + 3H{X} -> Al{X}3 + 3H2O
, где X =
F Cl Br I (NO3) -
{M}2O3 + 6H{X} = 2{M}{X}3 + 3H2O
, где M =
Fe Al Cr La Sc Y; X =
F Cl Br I (NO3) -
2Al + 3{Hal}2 -> 2Al{Hal}3
, где Hal =
Cl Br I -
BF3 + AlBr3 -> BBr3 + AlF3
И ещё 6 реакций…

![mathsf{AlBr_3+4H_2Oleftrightarrows[Al(H_2O)_4]^{3+}+3Br^-}](https://dic.academic.ru/dic.nsf/ruwiki/4b4850934f1fecf0f7830b90b164b2f9.png)
![mathsf{[Al(H_2O)_4]^{3+}+H_2Oleftrightarrows[Al(H_2O)_3(OH)]^{2+}+H_3O^+}](https://dic.academic.ru/dic.nsf/ruwiki/51e539c3c99b08e5edf9857931a76ac0.png)


![mathsf{AlBr_3+4NaOH=Na[Al(OH)_4]+3NaBr}](https://dic.academic.ru/dic.nsf/ruwiki/411fb48a9f778abdf77899ceb50e49c1.png)



![mathsf{AlBr_3+4LiH=Li[AlH_4]+3LiBr}](https://dic.academic.ru/dic.nsf/ruwiki/a1ae581c91cd2fb06aba3e5ca5d6683b.png)
![mathsf{AlBr_3+C_2H_5Br}rightarrowmathsf{[C_2H_5]^+[AlBr_4]^-}](https://dic.academic.ru/dic.nsf/ruwiki/451e23f43e27bf26f1f5d4be76e0a970.png)