| Brucellosis | |
|---|---|
| Other names | undulant fever, undulating fever, Mediterranean fever, Malta fever, Cyprus fever, rock fever (Micrococcus melitensis)[1] |
| Specialty | Infectious disease |
| Symptoms | fever, chills, loss of appetite, sweats, weakness, fatigue, Joint, muscle and back pain, Headache.[2] |
| Complications | central nervous system infections, inflammation and infection of the spleen and liver, inflammation and infection of the testicles (epididymo-orchitis), Arthritis, Inflammation of the inner lining of the heart chambers (endocarditis).[2] |
| Diagnostic method | x-rays, computerized tomography (CT) scan or magnetic resonance imaging (MRI), cerebrospinal fluid culture, echocardiography.[3] |
| Prevention | avoid unpasteurized dairy foods, cook meat thoroughly, wear gloves, take safety precautions in high-risk workplaces, vaccinate domestic animals.[2] |
| Treatment | antibiotics |
| Medication | tetracyclines, rifampicin, aminoglycosides |
Brucellosis[4][5] is a highly contagious zoonosis caused by ingestion of unpasteurized milk or undercooked meat from infected animals, or close contact with their secretions.[6] It is also known as undulant fever, Malta fever, and Mediterranean fever.[7]
The bacteria causing this disease, Brucella, are small, Gram-negative, nonmotile, nonspore-forming, rod-shaped (coccobacilli) bacteria. They function as facultative intracellular parasites, causing chronic disease, which usually persists for life. Four species infect humans: B. abortus, B. canis, B. melitensis, and B. suis. B. abortus is less virulent than B. melitensis and is primarily a disease of cattle. B. canis affects dogs. B. melitensis is the most virulent and invasive species; it usually infects goats and occasionally sheep. B. suis is of intermediate virulence and chiefly infects pigs. Symptoms include profuse sweating and joint and muscle pain. Brucellosis has been recognized in animals and humans since the early 20th century.[8][9]
Signs and symptoms[edit]
A graph of the cases of brucellosis in humans in the United States from the years 1993–2010 surveyed by the Centers for Disease Control and Prevention through the National Notifiable Diseases Surveillance System[10]
The symptoms are like those associated with many other febrile diseases, but with emphasis on muscular pain and night sweats. The duration of the disease can vary from a few weeks to many months or even years.
In the first stage of the disease, bacteremia occurs and leads to the classic triad of undulant fevers, sweating (often with characteristic foul, moldy smell sometimes likened to wet hay), and migratory arthralgia and myalgia (joint and muscle pain).[citation needed] Blood tests characteristically reveal a low number of white blood cells and red blood cells, show some elevation of liver enzymes such as aspartate aminotransferase and alanine aminotransferase, and demonstrate positive Bengal rose and Huddleston reactions. Gastrointestinal symptoms occur in 70% of cases and include nausea, vomiting, decreased appetite, unintentional weight loss, abdominal pain, constipation, diarrhea, an enlarged liver, liver inflammation, liver abscess, and an enlarged spleen.[citation needed]
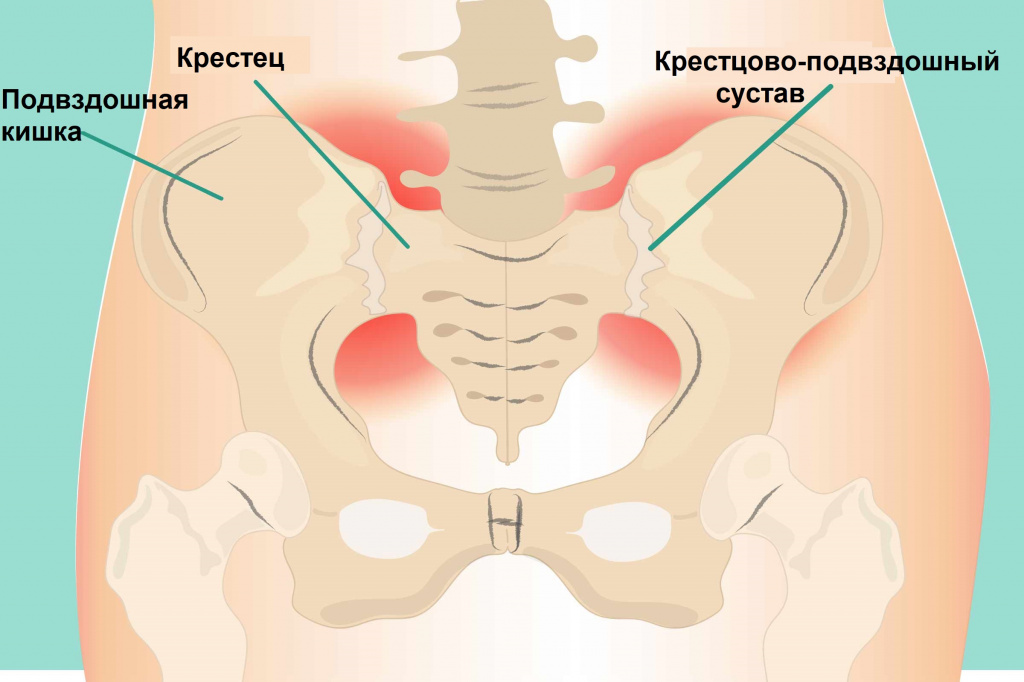
This complex is, at least in Portugal, Israel, Syria, and Jordan, known as Malta fever. During episodes of Malta fever, melitococcemia (presence of brucellae in the blood) can usually be demonstrated by means of blood culture in tryptose medium or Albini medium. If untreated, the disease can give origin to focalizations[clarification needed] or become chronic. The focalizations of brucellosis occur usually in bones and joints, and osteomyelitis or spondylodiscitis of the lumbar spine accompanied by sacroiliitis is very characteristic of this disease. Orchitis is also common in men.
The consequences of Brucella infection are highly variable and may include arthritis, spondylitis, thrombocytopenia, meningitis, uveitis, optic neuritis, endocarditis, and various neurological disorders collectively known as neurobrucellosis.
Cause[edit]
Brucellosis in humans is usually associated with consumption of unpasteurized milk and soft cheeses made from the milk of infected animals—primarily goats, infected with B. melitensis and with occupational exposure of laboratory workers, veterinarians, and slaughterhouse workers.[11] Some vaccines used in livestock, most notably B. abortus strain 19, also cause disease in humans if accidentally injected. Brucellosis induces inconstant fevers, miscarriage, sweating, weakness, anemia, headaches, depression, and muscular and bodily pain. The other strains, B. suis and B. canis, cause infection in pigs and dogs, respectively.[citation needed]
Overall findings support that brucellosis poses an occupational risk to goat farmers with specific areas of concern including weak awareness of disease transmission to humans and lack of knowledge on specific safe farm practices such as quarantine practices.[12]
Diagnosis[edit]
Brucella Coombs Gel Test. Seropositivity detected to GN177
The diagnosis of brucellosis relies on:[citation needed]
- Demonstration of the agent: blood cultures in tryptose broth, bone marrow cultures: The growth of brucellae is extremely slow (they can take up to two months to grow) and the culture poses a risk to laboratory personnel due to high infectivity of brucellae.
- Demonstration of antibodies against the agent either with the classic Huddleson, Wright, and/or Bengal Rose reactions, either with ELISA or the 2-mercaptoethanol assay for IgM antibodies associated with chronic disease
- Histologic evidence of granulomatous hepatitis on hepatic biopsy
- Radiologic alterations in infected vertebrae: the Pedro Pons sign (preferential erosion of the anterosuperior corner of lumbar vertebrae) and marked osteophytosis are suspicious of brucellic spondylitis.
Definite diagnosis of brucellosis requires the isolation of the organism from the blood, body fluids, or tissues, but serological methods may be the only tests available in many settings. Positive blood culture yield ranges between 40 and 70% and is less commonly positive for B. abortus than B. melitensis or B. suis. Identification of specific antibodies against bacterial lipopolysaccharide and other antigens can be detected by the standard agglutination test (SAT), rose Bengal, 2-mercaptoethanol (2-ME), antihuman globulin (Coombs’) and indirect enzyme-linked immunosorbent assay (ELISA). SAT is the most commonly used serology in endemic areas.[13][14] An agglutination titre greater than 1:160 is considered significant in nonendemic areas and greater than 1:320 in endemic areas.[citation needed]
Due to the similarity of the O polysaccharide of Brucella to that of various other Gram-negative bacteria (e.g. Francisella tularensis, Escherichia coli, Salmonella urbana, Yersinia enterocolitica, Vibrio cholerae, and Stenotrophomonas maltophilia), the appearance of cross-reactions of class M immunoglobulins may occur. The inability to diagnose B. canis by SAT due to lack of cross-reaction is another drawback. False-negative SAT may be caused by the presence of blocking antibodies (the prozone phenomenon) in the α2-globulin (IgA) and in the α-globulin (IgG) fractions.[citation needed]
Dipstick assays are new and promising, based on the binding of Brucella IgM antibodies, and are simple, accurate, and rapid. ELISA typically uses cytoplasmic proteins as antigens. It measures IgM, IgG, and IgA with better sensitivity and specificity than the SAT in most recent comparative studies.[15] The commercial Brucellacapt test, a single-step immunocapture assay for the detection of total anti-Brucella antibodies, is an increasingly used adjunctive test when resources permit. PCR is fast and should be specific. Many varieties of PCR have been developed (e.g. nested PCR, realtime PCR, and PCR-ELISA) and found to have superior specificity and sensitivity in detecting both primary infection and relapse after treatment.[16] Unfortunately, these are not standardized for routine use, and some centres have reported persistent PCR positivity after clinically successful treatment, fuelling the controversy about the existence of prolonged chronic brucellosis.[citation needed]
Other laboratory findings include normal peripheral white cell count, and occasional leucopenia with relative lymphocytosis. The serum biochemical profiles are commonly normal.[17]
Prevention[edit]
Surveillance using serological tests, as well as tests on milk such as the milk ring test, can be used for screening and play an important role in campaigns to eliminate the disease. Also, individual animal testing both for trade and for disease-control purposes is practiced. In endemic areas, vaccination is often used to reduce the incidence of infection. An animal vaccine is available that uses modified live bacteria. The World Organisation for Animal Health Manual of Diagnostic Test and Vaccines for Terrestrial Animals provides detailed guidance on the production of vaccines. As the disease is closer to being eliminated, a test and eradication program is required to eliminate it.[citation needed]
The main way of preventing brucellosis is by using fastidious hygiene in producing raw milk products, or by pasteurizing all milk that is to be ingested by human beings, either in its unaltered form or as a derivative, such as cheese.[citation needed]
Treatment[edit]
Antibiotics such as tetracyclines, rifampicin, and the aminoglycosides streptomycin and gentamicin are effective against Brucella bacteria. However, the use of more than one antibiotic is needed for several weeks, because the bacteria incubate within cells.[citation needed]
The gold standard treatment for adults is daily intramuscular injections of streptomycin 1 g for 14 days and oral doxycycline 100 mg twice daily for 45 days (concurrently). Gentamicin 5 mg/kg by intramuscular injection once daily for 7 days is an acceptable substitute when streptomycin is not available or contraindicated.[18] Another widely used regimen is doxycycline plus rifampicin twice daily for at least 6 weeks. This regimen has the advantage of oral administration. A triple therapy of doxycycline, with rifampicin and co-trimoxazole, has been used successfully to treat neurobrucellosis.[19] Doxycycline plus streptomycin regimen (for 2 to 3 weeks) is more effective than doxycycline plus rifampicin regimen (for 6 weeks).[20]
Doxycycline is able to cross the blood–brain barrier, but requires the addition of two other drugs to prevent relapse. Ciprofloxacin and co-trimoxazole therapy is associated with an unacceptably high rate of relapse. In brucellic endocarditis, surgery is required for an optimal outcome. Even with optimal antibrucellic therapy, relapses still occur in 5 to 10% of patients with Malta fever.[citation needed]
Prognosis[edit]
The mortality of the disease in 1909, as recorded in the British Army and Navy stationed in Malta, was 2%. The most frequent cause of death was endocarditis. Recent advances in antibiotics and surgery have been successful in preventing death due to endocarditis. Prevention of human brucellosis can be achieved by eradication of the disease in animals by vaccination and other veterinary control methods such as testing herds/flocks and slaughtering animals when infection is present. Currently, no effective vaccine is available for humans. Boiling milk before consumption, or before using it to produce other dairy products, is protective against transmission via ingestion. Changing traditional food habits of eating raw meat, liver, or bone marrow is necessary, but difficult to implement.[citation needed] Patients who have had brucellosis should probably be excluded indefinitely from donating blood or organs. Exposure of diagnostic laboratory personnel to Brucella organisms remains a problem in both endemic settings and when brucellosis is unknowingly imported by a patient.[21] After appropriate risk assessment, staff with significant exposure should be offered postexposure prophylaxis and followed up serologically for 6 months.[22]
Epidemiology[edit]
Argentina[edit]
According to a study published in 2002, an estimated 10–13% of farm animals are infected with Brucella species.[23] Annual losses from the disease were calculated at around $60 million. Since 1932, government agencies have undertaken efforts to contain the disease. Currently, all cattle of ages 3–8 months must receive the Brucella abortus strain 19 vaccine.[24]
Australia[edit]
Australia is free of cattle brucellosis, although it occurred in the past. Brucellosis of sheep or goats has never been reported. Brucellosis of pigs does occur. Feral pigs are the typical source of human infections.[25][26]
Canada[edit]
On 19 September 1985, the Canadian government declared its cattle population brucellosis-free. Brucellosis ring testing of milk and cream, and testing of cattle to be slaughtered ended on 1 April 1999. Monitoring continues through testing at auction markets, through standard disease-reporting procedures, and through testing of cattle being qualified for export to countries other than the United States.[27]
China[edit]
An outbreak infecting humans took place in Lanzhou in 2020 after the Lanzhou Biopharmaceutical Plant, which was involved in vaccine production, accidentally pumped out the bacteria into the atmosphere in exhaust air due to use of expired disinfectant. The outbreak affected over 6,000 people.[28][29]
Europe[edit]
Disease incidence map of B. melitensis infections in animals in Europe during the first half of 2006
never reported
not reported in this period
confirmed clinical disease
confirmed infection
no information
Malta[edit]
Until the early 20th century, the disease was endemic in Malta to the point of it being referred to as «Maltese fever». Since 2005, due to a strict regimen of certification of milk animals and widespread use of pasteurization, the illness has been eradicated from Malta.[30]
Republic of Ireland[edit]
Ireland was declared free of brucellosis on 1 July 2009. The disease had troubled the country’s farmers and veterinarians for several decades.[31][32] The Irish government submitted an application to the European Commission, which verified that Ireland had been liberated.[32] Brendan Smith, Ireland’s then Minister for Agriculture, Food and the Marine, said the elimination of brucellosis was «a landmark in the history of disease eradication in Ireland».[31][32] Ireland’s Department of Agriculture, Food and the Marine intends to reduce its brucellosis eradication programme now that eradication has been confirmed.[31][32]
UK[edit]
Mainland Britain has been free of brucellosis since 1979, although there have been episodic re-introductions since.[33] The last outbreak of brucellosis in Great Britain was in cattle in Cornwall in 2004.[33][34] Northern Ireland was declared officially brucellosis-free in 2015.[33]
New Zealand[edit]
Brucellosis in New Zealand is limited to sheep (B. ovis). The country is free of all other species of Brucella.[35]
United States[edit]
Dairy herds in the U.S. are tested at least once a year to be certified brucellosis-free[36] with the Brucella milk ring test.[37] Cows confirmed to be infected are often killed. In the United States, veterinarians are required[citation needed] to vaccinate all young stock, to further reduce the chance of zoonotic transmission. This vaccination is usually referred to as a «calfhood» vaccination. Most cattle receive a tattoo in one of their ears, serving as proof of their vaccination status. This tattoo also includes the last digit of the year they were born.[38]
The first state–federal cooperative efforts towards eradication of brucellosis caused by B. abortus in the U.S. began in 1934.[citation needed]
Brucellosis was originally imported to North America with non-native domestic cattle (Bos taurus), which transmitted the disease to wild bison (Bison bison) and elk (Cervus canadensis). No records exist of brucellosis in ungulates native to America until the early 19th century.[39]
History[edit]
David Bruce (centre), with members of the Mediterranean Fever Commission (Brucellosis)
Brucellosis first came to the attention of British medical officers in the 1850s in Malta during the Crimean War, and was referred to as Malta Fever. Jeffery Allen Marston (1831–1911) described his own case of the disease in 1861. The causal relationship between organism and disease was first established in 1887 by David Bruce.[40][41] Bruce considered the agent spherical and classified it as a coccus.[citation needed]
In 1897, Danish veterinarian Bernhard Bang isolated a bacillus as the agent of heightened spontaneous abortion in cows, and the name «Bang’s disease» was assigned to this condition. Bang considered the organism rod-shaped and classified it as a bacillus. So at the time, no one knew that this bacillus had anything to do with the causative agent in Malta fever.[42]
Maltese scientist and archaeologist Themistocles Zammit identified unpasteurized goat milk as the major etiologic factor of undulant fever in June 1905.[43]
In the late 1910s, American bacteriologist Alice C. Evans was studying the Bang bacillus and gradually realized that it was virtually indistinguishable from the Bruce coccus.[44] The short-rod versus oblong-round morphologic borderline explained the leveling of the erstwhile bacillus/coccus distinction (that is, these «two» pathogens were not a coccus versus a bacillus but rather were one coccobacillus).[44] The Bang bacillus was already known to be enzootic in American dairy cattle, which showed itself in the regularity with which herds experienced contagious abortion.[44] Having made the discovery that the bacteria were certainly nearly identical and perhaps totally so, Evans then wondered why Malta fever was not widely diagnosed or reported in the United States.[44] She began to wonder whether many cases of vaguely defined febrile illnesses were in fact caused by the drinking of raw (unpasteurized) milk.[44] During the 1920s, this hypothesis was vindicated. Such illnesses ranged from undiagnosed and untreated gastrointestinal upset to misdiagnosed[44] febrile and painful versions, some even fatal. This advance in bacteriological science sparked extensive changes in the American dairy industry to improve food safety. The changes included making pasteurization standard and greatly tightening the standards of cleanliness in milkhouses on dairy farms. The expense prompted delay and skepticism in the industry,[44] but the new hygiene rules eventually became the norm. Although these measures have sometimes struck people as overdone in the decades since, being unhygienic at milking time or in the milkhouse, or drinking raw milk, are not a safe alternative.[citation needed]
In the decades after Evans’s work, this genus, which received the name Brucella in honor of Bruce, was found to contain several species with varying virulence. The name «brucellosis» gradually replaced the 19th-century names Mediterranean fever and Malta fever.[45]
Neurobrucellosis, a neurological involvement in brucellosis, was first described in 1879. In the late 19th century, its symptoms were described in more detail by M. Louis Hughes, a Surgeon-Captain of the Royal Army Medical Corps stationed in Malta who isolated brucella organisms from a patient with meningo-encephalitis.[46] In 1989, neurologists in Saudi Arabia made significant contributions to the medical literature involving neurobrucellosis.[47][48]
These obsolete names have previously been applied to brucellosis:[45][49]
- Crimean fever
- Cyprus fever
- Gibraltar fever
- Goat fever
- Italian fever
- Neapolitan fever
Biological warfare[edit]
Brucella species were weaponized by several advanced countries by the mid-20th century. In 1954, B. suis became the first agent weaponized by the United States at its Pine Bluff Arsenal near Pine Bluff, Arkansas. Brucella species survive well in aerosols and resist drying. Brucella and all other remaining biological weapons in the U.S. arsenal were destroyed in 1971–72 when the American offensive biological warfare program was discontinued by order of President Richard Nixon.[50]
The experimental American bacteriological warfare program focused on three agents of the Brucella group:[citation needed]
- Porcine brucellosis (agent US)
- Bovine brucellosis (agent AA)
- Caprine brucellosis (agent AM)
Agent US was in advanced development by the end of World War II. When the United States Air Force (USAF) wanted a biological warfare capability, the Chemical Corps offered Agent US in the M114 bomblet, based on the four-pound bursting bomblet developed for spreading anthrax during World War II. Though the capability was developed, operational testing indicated the weapon was less than desirable, and the USAF designed it as an interim capability until it could eventually be replaced by a more effective biological weapon.[citation needed]
The main drawback of using the M114 with Agent US was that it acted mainly as an incapacitating agent, whereas the USAF administration wanted weapons that were deadly. The stability of M114 in storage was too low to allow for storing it at forward air bases, and the logistical requirements to neutralize a target were far higher than was originally planned. Ultimately, this would have required too much logistical support to be practical in the field.[citation needed]
Agents US and AA had a median infective dose of 500 organisms/person, and for Agent AM it was 300 organisms/person. The incubation time was believed to be about 2 weeks, with a duration of infection of several months. The lethality estimate was, based on epidemiological information, 1 to 2
per cent. Agent AM was believed to be a somewhat more virulent disease, with a fatality rate of 3 per cent being expected.[citation needed]
Other animals[edit]
Species infecting domestic livestock are B. abortus (cattle, bison, and elk), B. canis (dogs), B. melitensis (goats and sheep), B. ovis (sheep), and B. suis (caribou and pigs). Brucella species have also been isolated from several marine mammal species (cetaceans and pinnipeds).[citation needed]
Cattle[edit]
B. abortus is the principal cause of brucellosis in cattle. The bacteria are shed from an infected animal at or around the time of calving or abortion. Once exposed, the likelihood of an animal becoming infected is variable, depending on age, pregnancy status, and other intrinsic factors of the animal, as well as the number of bacteria to which the animal was exposed.[51] The most common clinical signs of cattle infected with B. abortus are high incidences of abortions, arthritic joints, and retained placenta.[citation needed]
The two main causes for spontaneous abortion in animals are erythritol, which can promote infections in the fetus and placenta,[clarification needed] and the lack of anti-Brucella activity in the amniotic fluid. Males can also harbor the bacteria in their reproductive tracts, namely seminal vesicles, ampullae, testicles, and epididymises.[citation needed]
Dogs[edit]
The causative agent of brucellosis in dogs, B. canis, is transmitted to other dogs through breeding and contact with aborted fetuses. Brucellosis can occur in humans who come in contact with infected aborted tissue or semen. The bacteria in dogs normally infect the genitals and lymphatic system, but can also spread to the eyes, kidneys, and intervertebral discs. Brucellosis in the intervertebral disc is one possible cause of discospondylitis. Symptoms of brucellosis in dogs include abortion in female dogs and scrotal inflammation and orchitis in males. Fever is uncommon. Infection of the eye can cause uveitis, and infection of the intervertebral disc can cause pain or weakness. Blood testing of the dogs prior to breeding can prevent the spread of this disease. It is treated with antibiotics, as with humans, but it is difficult to cure.[52]
Aquatic wildlife[edit]
Brucellosis in cetaceans is caused by the bacterium B. ceti. First discovered in the aborted fetus of a bottlenose dolphin, the structure of B. ceti is similar to Brucella in land animals. B. ceti is commonly detected in two suborders of cetaceans, the Mysticeti and Odontoceti. The Mysticeti include four families of baleen whales, filter-feeders, and the Odontoceti include two families of toothed cetaceans ranging from dolphins to sperm whales. B. ceti is believed to transfer from animal to animal through sexual intercourse, maternal feeding, aborted fetuses, placental issues, from mother to fetus, or through fish reservoirs. Brucellosis is a reproductive disease, so has an extreme negative impact on the population dynamics of a species. This becomes a greater issue when the already low population numbers of cetaceans are taken into consideration. B. ceti has been identified in four of the 14 cetacean families, but the antibodies have been detected in seven of the families. This indicates that B. ceti is common amongst cetacean families and populations. Only a small percentage of exposed individuals become ill or die. However, particular species apparently are more likely to become infected by B. ceti. The harbor porpoise, striped dolphin, white-sided dolphin, bottlenose dolphin, and common dolphin have the highest frequency of infection amongst odontocetes. In the mysticetes families, the northern minke whale is by far the most infected species. Dolphins and porpoises are more likely to be infected than cetaceans such as whales. With regard to sex and age biases, the infections do not seem influenced by the age or sex of an individual. Although fatal to cetaceans, B. ceti has a low infection rate for humans.[53]
Terrestrial wildlife[edit]
The disease in its various strains can infect multiple wildlife species, including elk (Cervus canadensis), bison (Bison bison), African buffalo (Syncerus caffer), European wild boar (Sus scrofa), caribou (Rangifer tarandus), moose (Alces alces), and marine mammals (see section on aquatic wildlife above).[54][55] While some regions use vaccines to prevent the spread of brucellosis between infected and uninfected wildlife populations, no suitable brucellosis vaccine for terrestrial wildlife has been developed.[56] This gap in medicinal knowledge creates more pressure for management practices that reduce spread of the disease.[56]
Wild bison and elk in the greater Yellowstone area are the last remaining reservoir of B. abortus in the US. The recent transmission of brucellosis from elk back to cattle in Idaho and Wyoming illustrates how the area, as the last remaining reservoir in the United States, may adversely affect the livestock industry. Eliminating brucellosis from this area is a challenge, as many viewpoints exist on how to manage diseased wildlife. However, the Wyoming Game and Fish Department has recently begun to protect scavengers (particularly coyotes and red fox) on elk feedgrounds, because they act as sustainable, no-cost, biological control agents by removing infected elk fetuses quickly.[57]
The National Elk Refuge in Jackson, Wyoming asserts that the intensity of the winter feeding program affects the spread of brucellosis more than the population size of elk and bison.[54] Since concentrating animals around food plots accelerates spread of the disease, management strategies to reduce herd density and increase dispersion could limit its spread.[54]
Effects on hunters[edit]
Hunters may be at additional risk for exposure to brucellosis due to increased contact with susceptible wildlife, including predators that may have fed on infected prey. Hunting dogs can also be at risk of infection.[58] Exposure can occur through contact with open wounds or by directly inhaling the bacteria while cleaning game.[59] In some cases, consumption of undercooked game can result in exposure to the disease.[59] Hunters can limit exposure while cleaning game through the use of precautionary barriers, including gloves and masks, and by washing tools rigorously after use.[56][60] By ensuring that game is cooked thoroughly, hunters can protect themselves and others from ingesting the disease.[59] Hunters should refer to local game officials and health departments to determine the risk of brucellosis exposure in their immediate area and to learn more about actions to reduce or avoid exposure.[citation needed]
See also[edit]
- Brucella suis
References[edit]
- ^ Wyatt HV (2014). «How did Sir David Bruce forget Zammit and his goats ?» (PDF). Journal of Maltese History. Malta: Department of History, University of Malta. 4 (1): 41. ISSN 2077-4338. Archived from the original (PDF) on 2016-07-21. Journal archive
- ^ a b c «Brucellosis». mayoclinic.org. Mayo Clinic. Retrieved June 5, 2022.
- ^ «Brucellosis». mayoclinic.org. Mayo Clinic. Retrieved June 5, 2022.
- ^ «Brucellosis». American Heritage Dictionary. Archived from the original on 2011-06-06.
- ^ «Maltese Fever». wrongdiagnosis.com. February 25, 2009.
- ^ «Diagnosis and Management of Acute Brucellosis in Primary Care» (PDF). Brucella Subgroup of the Northern Ireland Regional Zoonoses Group. August 2004. Archived from the original (PDF) on 2007-10-13.
- ^ Di Pierdomenico A, Borgia SM, Richardson D, Baqi M (July 2011). «Brucellosis in a returned traveller». CMAJ. 183 (10): E690-2. doi:10.1503/cmaj.091752. PMC 3134761. PMID 21398234.
- ^ Park. K., Park’s textbook of preventive and social medicine, 23 editions. Page 290-91
- ^ Roy, Rabindra (2013), «Chapter-23 Biostatistics», Mahajan and Gupta Textbook of Preventive and Social Medicine, Jaypee Brothers Medical Publishers (P) Ltd, pp. 434–449, retrieved 2022-11-13
- ^ «Brucellosis: Resources: Surveillance». CDC. 2018-10-09.
- ^ Wyatt HV (October 2005). «How Themistocles Zammit found Malta Fever (brucellosis) to be transmitted by the milk of goats». Journal of the Royal Society of Medicine. The Royal Society of Medicine Press. 98 (10): 451–4. doi:10.1177/014107680509801009. OCLC 680110952. PMC 1240100. PMID 16199812.
- ^ Peck ME, Jenpanich C, Amonsin A, Bunpapong N, Chanachai K, Somrongthong R, et al. (January 2019). «Knowledge, Attitudes and Practices Associated with Brucellosis among Small-Scale Goat Farmers in Thailand». Journal of Agromedicine. 24 (1): 56–63. doi:10.1080/1059924X.2018.1538916. PMID 30350754. S2CID 53034163.
- ^ Franco MP, Mulder M, Gilman RH, Smits HL (December 2007). «Human brucellosis». The Lancet. Infectious Diseases. 7 (12): 775–86. doi:10.1016/S1473-3099(07)70286-4. PMID 18045560.
- ^ Al Dahouk S, Nöckler K (July 2011). «Implications of laboratory diagnosis on brucellosis therapy». Expert Review of Anti-Infective Therapy. 9 (7): 833–45. doi:10.1586/eri.11.55. PMID 21810055. S2CID 5068325.
- ^ Mantur B, Parande A, Amarnath S, Patil G, Walvekar R, Desai A, et al. (August 2010). «ELISA versus conventional methods of diagnosing endemic brucellosis». The American Journal of Tropical Medicine and Hygiene. 83 (2): 314–8. doi:10.4269/ajtmh.2010.09-0790. PMC 2911177. PMID 20682874.
- ^ Yu WL, Nielsen K (August 2010). «Review of detection of Brucella spp. by polymerase chain reaction». Croatian Medical Journal. 51 (4): 306–13. doi:10.3325/cmj.2010.51.306. PMC 2931435. PMID 20718083.
- ^ Vrioni G, Pappas G, Priavali E, Gartzonika C, Levidiotou S (June 2008). «An eternal microbe: Brucella DNA load persists for years after clinical cure». Clinical Infectious Diseases. 46 (12): e131-6. doi:10.1086/588482. PMID 18462106.
- ^ Hasanjani Roushan MR, Mohraz M, Hajiahmadi M, Ramzani A, Valayati AA (April 2006). «Efficacy of gentamicin plus doxycycline versus streptomycin plus doxycycline in the treatment of brucellosis in humans». Clinical Infectious Diseases. 42 (8): 1075–80. doi:10.1086/501359. PMID 16575723.
- ^ McLean DR, Russell N, Khan MY (October 1992). «Neurobrucellosis: clinical and therapeutic features». Clinical Infectious Diseases. 15 (4): 582–90. doi:10.1093/clind/15.4.582. PMID 1420670.
- ^ Yousefi-Nooraie R, Mortaz-Hejri S, Mehrani M, Sadeghipour P (October 2012). «Antibiotics for treating human brucellosis». The Cochrane Database of Systematic Reviews. 10: CD007179. doi:10.1002/14651858.cd007179.pub2. PMC 6532606. PMID 23076931.
- ^ Yagupsky P, Baron EJ (August 2005). «Laboratory exposures to brucellae and implications for bioterrorism». Emerging Infectious Diseases. 11 (8): 1180–5. doi:10.3201/eid1108.041197. PMC 3320509. PMID 16102304.
- ^ Centers for Disease Control Prevention (CDC) (January 2008). «Laboratory-acquired brucellosis—Indiana and Minnesota, 2006». MMWR. Morbidity and Mortality Weekly Report. 57 (2): 39–42. PMID 18199967.
- ^ Samartino LE (December 2002). «Brucellosis in Argentina». Veterinary Microbiology. 90 (1–4): 71–80. doi:10.1016/s0378-1135(02)00247-x. PMID 12414136.
- ^ «SENASA – Direcci n Nacional de Sanidad Animal». viejaweb.senasa.gov.ar. Archived from the original on 2016-02-16. Retrieved 2016-02-10.
- ^ «Queensland Health: Brucellosis». State of Queensland (Queensland Health). 2010-11-24. Archived from the original on 2011-04-22. Retrieved 2011-06-06.
- ^
Lehane, Robert (1996) Beating the Odds in a Big Country: The eradication of bovine brucellosis and tuberculosis in Australia, CSIRO Publishing, ISBN 0-643-05814-1 - ^ «Reportable Diseases». Accredited Veterinarian’s Manual. Canadian Food Inspection Agency. Retrieved 2007-03-18.
- ^ China reports outbreak of brucellosis disease ‘way larger’ than originally thought 18 September 2020 www.news.com.au, accessed 18 September 2020
- ^ «兰州药厂泄漏事件布病患者:肿痛无药可吃,有人已转成慢性病_绿政公署_澎湃新闻-The Paper». www.thepaper.cn. Retrieved 2 June 2021.
- ^ Naudi JR (2005). Brucellosis, The Malta Experience. Malta: Publishers Enterprises group (PEG) Ltd. ISBN 978-99909-0-425-3.
- ^ a b c «Ireland free of brucellosis». RTÉ. 2009-07-01. Retrieved 2009-07-01.
- ^ a b c d «Ireland declared free of brucellosis». The Irish Times. 2009-07-01. Archived from the original on 2021-04-03. Retrieved 2009-07-01.
Michael F Sexton, president of Veterinary Ireland, which represents vets in practice, said: «Many vets and farmers in particular suffered significantly with brucellosis in past decades and it is greatly welcomed by the veterinary profession that this debilitating disease is no longer the hazard that it once was.»
- ^ a b c Monitoring brucellosis in Great Britain 3 September 2020 veterinary-practice.com, accessed 18 September 2020
- ^ Guidance Brucellosis: how to spot and report the disease 18 October 2018 www.gov.uk, accessed 18 September 2020
- ^ «MAF Biosecurity New Zealand: Brucellosis». Ministry of Agriculture and Forestry of New Zealand. Archived from the original on 2012-03-20. Retrieved 2011-06-06.
- ^ Brucellosis Eradication APHIS 91–45–013. United States Department of Agriculture. October 2003. p. 14.
- ^ Hamilton AV, Hardy AV (March 1950). «The brucella ring test; its potential value in the control of brucellosis». American Journal of Public Health and the Nation’s Health. 40 (3): 321–3. doi:10.2105/AJPH.40.3.321. PMC 1528431. PMID 15405523.
- ^ Vermont Beef Producers. «How important is calfhood vaccination?» (PDF). Archived from the original (PDF) on 2008-05-09.
- ^ Meagher M, Meyer ME (September 1994). «On the Origin of Brucellosis in Bison of Yellowstone National Park: A Review» (PDF). Conservation Biology. 8 (3): 645–653. doi:10.1046/j.1523-1739.1994.08030645.x. JSTOR 2386505. Archived from the original (PDF) on 2017-01-08. Retrieved 2017-01-07.
- ^ Wilkinson L (1993). «Brucellosis». In Kiple KF (ed.). The Cambridge World History of Human Disease. Cambridge University Press.
- ^ Brucellosis named after Major-General Sir David Bruce at Who Named It?
- ^ Evans, Alice (1963). Dr. Alice C. Evans Memoir.
- ^ Wyatt HV (2015). «The Strange Case of Temi Zammit’s missing experiments» (PDF). Journal of Maltese History. Malta: Department of History, University of Malta. 4 (2): 54–56. ISSN 2077-4338. Archived from the original (PDF) on 2016-07-21. Journal archive
- ^ a b c d e f g de Kruif P (1932). «Ch. 5 Evans: death in milk». Men Against Death. New York: Harcourt, Brace. OCLC 11210642.
- ^ a b Wyatt HV (31 July 2004). «Give A Disease A Bad Name». British Medical Journal. BMJ Publishing Group Ltd. 329 (7460): 272–278. doi:10.1136/bmj.329.7460.272. ISSN 0959-535X. JSTOR 25468794. OCLC 198096808. PMC 498028.
- ^ Madkour, M. Monir (2014). Brucellosis. Elsevier Science. p. 160. ISBN 9781483193595.
- ^ Malhotra R (2004). «Saudi Arabia». Practical Neurology. 4 (3): 184–185. doi:10.1111/j.1474-7766.2004.03-225.x.
- ^ Al-Sous MW, Bohlega S, Al-Kawi MZ, Alwatban J, McLean DR (March 2004). «Neurobrucellosis: clinical and neuroimaging correlation». AJNR. American Journal of Neuroradiology. 25 (3): 395–401. PMC 8158553. PMID 15037461.
- ^ «Medicine: Goat Fever». Time. 1928-12-10. ISSN 0040-781X. Retrieved 2017-05-01.
- ^ Woods, Jon B. (April 2005). USAMRIID’s Medical Management of Biological Casualties Handbook (PDF) (6th ed.). Fort Detrick, Maryland: U.S. Army Medical Institute of Infectious Diseases. p. 53. Archived from the original (PDF) on 2007-06-09.
- ^ Radostits, O.M., C.C. Gay, D.C. Blood, and K.W. Hinchcliff. (2000). Veterinary Medicine, A textbook of the Diseases of Cattle, Sheep, Pigs, Goats and Horses. Harcourt Publishers Limited, London, pp. 867–882. ISBN 0702027774.
- ^ Ettinger SJ, Feldman EC (1995). Textbook of Veterinary Internal Medicine (4th ed.). W.B. Saunders Company. ISBN 978-0-7216-4679-4.
- ^ Guzmán-Verri C, González-Barrientos R, Hernández-Mora G, Morales JA, Baquero-Calvo E, Chaves-Olarte E, Moreno E (2012). «Brucella ceti and brucellosis in cetaceans». Frontiers in Cellular and Infection Microbiology. 2: 3. doi:10.3389/fcimb.2012.00003. PMC 3417395. PMID 22919595.
- ^ a b c «Brucellosis». www.fws.gov. U.S. Fish &Wildlife Service. 2016. Archived from the original on 2016-10-09. Retrieved 2016-10-03.
- ^ Godfroid J (August 2002). «Brucellosis in wildlife» (PDF). Revue Scientifique et Technique. 21 (2): 277–86. doi:10.20506/rst.21.2.1333. PMID 11974615. Archived from the original (PDF) on 2015-06-06. Retrieved 2016-10-07.
- ^ a b c Godfroid J, Garin-Bastuji B, Saegerman C, Blasco JM (April 2013). «Brucellosis in terrestrial wildlife» (PDF). Revue Scientifique et Technique. 32 (1): 27–42. CiteSeerX 10.1.1.1020.9652. doi:10.20506/rst.32.1.2180. PMID 23837363. Archived from the original (PDF) on 2015-06-06. Retrieved 2016-10-07.
- ^ Cross PC, Maichak EJ, Brennan A, Scurlock BM, Henningsen J, Luikart G (April 2013). «An ecological perspective on Brucella abortus in the western United States» (PDF). Revue Scientifique et Technique. 32 (1): 79–87. doi:10.20506/rst.32.1.2184. PMID 23837367.
- ^ CDC — Hunters Risks — Animals That Can Put Hunters at Risk
- ^ a b c «CDC – Home – Brucellosis». www.cdc.gov. Center for Disease Control. 2016. Retrieved 2016-10-03.
- ^ «Zoonoses – Brucellosis». www.who.int/en/. World Health Organization. 2016. Archived from the original on March 9, 2005. Retrieved 2016-10-03.
Further reading[edit]
- Fact sheet on Brucellosis from World Organisation for Animal Health
- Brucella genomes and related information at PATRIC, a Bioinformatics Resource Center funded by NIAID
- Prevention about Brucellosis from Centers for Disease Control
- Capasso L (August 2002). «Bacteria in two-millennia-old cheese, and related epizoonoses in Roman populations». The Journal of Infection. 45 (2): 122–7. doi:10.1053/jinf.2002.0996. PMID 12217720. – re high rate of brucellosis in humans in ancient Pompeii
- Brucellosis, factsheet from European Centre for Disease Prevention and Control
| Brucellosis | |
|---|---|
| Other names | undulant fever, undulating fever, Mediterranean fever, Malta fever, Cyprus fever, rock fever (Micrococcus melitensis)[1] |
| Specialty | Infectious disease |
| Symptoms | fever, chills, loss of appetite, sweats, weakness, fatigue, Joint, muscle and back pain, Headache.[2] |
| Complications | central nervous system infections, inflammation and infection of the spleen and liver, inflammation and infection of the testicles (epididymo-orchitis), Arthritis, Inflammation of the inner lining of the heart chambers (endocarditis).[2] |
| Diagnostic method | x-rays, computerized tomography (CT) scan or magnetic resonance imaging (MRI), cerebrospinal fluid culture, echocardiography.[3] |
| Prevention | avoid unpasteurized dairy foods, cook meat thoroughly, wear gloves, take safety precautions in high-risk workplaces, vaccinate domestic animals.[2] |
| Treatment | antibiotics |
| Medication | tetracyclines, rifampicin, aminoglycosides |
Brucellosis[4][5] is a highly contagious zoonosis caused by ingestion of unpasteurized milk or undercooked meat from infected animals, or close contact with their secretions.[6] It is also known as undulant fever, Malta fever, and Mediterranean fever.[7]
The bacteria causing this disease, Brucella, are small, Gram-negative, nonmotile, nonspore-forming, rod-shaped (coccobacilli) bacteria. They function as facultative intracellular parasites, causing chronic disease, which usually persists for life. Four species infect humans: B. abortus, B. canis, B. melitensis, and B. suis. B. abortus is less virulent than B. melitensis and is primarily a disease of cattle. B. canis affects dogs. B. melitensis is the most virulent and invasive species; it usually infects goats and occasionally sheep. B. suis is of intermediate virulence and chiefly infects pigs. Symptoms include profuse sweating and joint and muscle pain. Brucellosis has been recognized in animals and humans since the early 20th century.[8][9]
Signs and symptoms[edit]
A graph of the cases of brucellosis in humans in the United States from the years 1993–2010 surveyed by the Centers for Disease Control and Prevention through the National Notifiable Diseases Surveillance System[10]
The symptoms are like those associated with many other febrile diseases, but with emphasis on muscular pain and night sweats. The duration of the disease can vary from a few weeks to many months or even years.
In the first stage of the disease, bacteremia occurs and leads to the classic triad of undulant fevers, sweating (often with characteristic foul, moldy smell sometimes likened to wet hay), and migratory arthralgia and myalgia (joint and muscle pain).[citation needed] Blood tests characteristically reveal a low number of white blood cells and red blood cells, show some elevation of liver enzymes such as aspartate aminotransferase and alanine aminotransferase, and demonstrate positive Bengal rose and Huddleston reactions. Gastrointestinal symptoms occur in 70% of cases and include nausea, vomiting, decreased appetite, unintentional weight loss, abdominal pain, constipation, diarrhea, an enlarged liver, liver inflammation, liver abscess, and an enlarged spleen.[citation needed]
This complex is, at least in Portugal, Israel, Syria, and Jordan, known as Malta fever. During episodes of Malta fever, melitococcemia (presence of brucellae in the blood) can usually be demonstrated by means of blood culture in tryptose medium or Albini medium. If untreated, the disease can give origin to focalizations[clarification needed] or become chronic. The focalizations of brucellosis occur usually in bones and joints, and osteomyelitis or spondylodiscitis of the lumbar spine accompanied by sacroiliitis is very characteristic of this disease. Orchitis is also common in men.
The consequences of Brucella infection are highly variable and may include arthritis, spondylitis, thrombocytopenia, meningitis, uveitis, optic neuritis, endocarditis, and various neurological disorders collectively known as neurobrucellosis.
Cause[edit]
Brucellosis in humans is usually associated with consumption of unpasteurized milk and soft cheeses made from the milk of infected animals—primarily goats, infected with B. melitensis and with occupational exposure of laboratory workers, veterinarians, and slaughterhouse workers.[11] Some vaccines used in livestock, most notably B. abortus strain 19, also cause disease in humans if accidentally injected. Brucellosis induces inconstant fevers, miscarriage, sweating, weakness, anemia, headaches, depression, and muscular and bodily pain. The other strains, B. suis and B. canis, cause infection in pigs and dogs, respectively.[citation needed]
Overall findings support that brucellosis poses an occupational risk to goat farmers with specific areas of concern including weak awareness of disease transmission to humans and lack of knowledge on specific safe farm practices such as quarantine practices.[12]
Diagnosis[edit]
Brucella Coombs Gel Test. Seropositivity detected to GN177
The diagnosis of brucellosis relies on:[citation needed]
- Demonstration of the agent: blood cultures in tryptose broth, bone marrow cultures: The growth of brucellae is extremely slow (they can take up to two months to grow) and the culture poses a risk to laboratory personnel due to high infectivity of brucellae.
- Demonstration of antibodies against the agent either with the classic Huddleson, Wright, and/or Bengal Rose reactions, either with ELISA or the 2-mercaptoethanol assay for IgM antibodies associated with chronic disease
- Histologic evidence of granulomatous hepatitis on hepatic biopsy
- Radiologic alterations in infected vertebrae: the Pedro Pons sign (preferential erosion of the anterosuperior corner of lumbar vertebrae) and marked osteophytosis are suspicious of brucellic spondylitis.
Definite diagnosis of brucellosis requires the isolation of the organism from the blood, body fluids, or tissues, but serological methods may be the only tests available in many settings. Positive blood culture yield ranges between 40 and 70% and is less commonly positive for B. abortus than B. melitensis or B. suis. Identification of specific antibodies against bacterial lipopolysaccharide and other antigens can be detected by the standard agglutination test (SAT), rose Bengal, 2-mercaptoethanol (2-ME), antihuman globulin (Coombs’) and indirect enzyme-linked immunosorbent assay (ELISA). SAT is the most commonly used serology in endemic areas.[13][14] An agglutination titre greater than 1:160 is considered significant in nonendemic areas and greater than 1:320 in endemic areas.[citation needed]
Due to the similarity of the O polysaccharide of Brucella to that of various other Gram-negative bacteria (e.g. Francisella tularensis, Escherichia coli, Salmonella urbana, Yersinia enterocolitica, Vibrio cholerae, and Stenotrophomonas maltophilia), the appearance of cross-reactions of class M immunoglobulins may occur. The inability to diagnose B. canis by SAT due to lack of cross-reaction is another drawback. False-negative SAT may be caused by the presence of blocking antibodies (the prozone phenomenon) in the α2-globulin (IgA) and in the α-globulin (IgG) fractions.[citation needed]
Dipstick assays are new and promising, based on the binding of Brucella IgM antibodies, and are simple, accurate, and rapid. ELISA typically uses cytoplasmic proteins as antigens. It measures IgM, IgG, and IgA with better sensitivity and specificity than the SAT in most recent comparative studies.[15] The commercial Brucellacapt test, a single-step immunocapture assay for the detection of total anti-Brucella antibodies, is an increasingly used adjunctive test when resources permit. PCR is fast and should be specific. Many varieties of PCR have been developed (e.g. nested PCR, realtime PCR, and PCR-ELISA) and found to have superior specificity and sensitivity in detecting both primary infection and relapse after treatment.[16] Unfortunately, these are not standardized for routine use, and some centres have reported persistent PCR positivity after clinically successful treatment, fuelling the controversy about the existence of prolonged chronic brucellosis.[citation needed]
Other laboratory findings include normal peripheral white cell count, and occasional leucopenia with relative lymphocytosis. The serum biochemical profiles are commonly normal.[17]
Prevention[edit]
Surveillance using serological tests, as well as tests on milk such as the milk ring test, can be used for screening and play an important role in campaigns to eliminate the disease. Also, individual animal testing both for trade and for disease-control purposes is practiced. In endemic areas, vaccination is often used to reduce the incidence of infection. An animal vaccine is available that uses modified live bacteria. The World Organisation for Animal Health Manual of Diagnostic Test and Vaccines for Terrestrial Animals provides detailed guidance on the production of vaccines. As the disease is closer to being eliminated, a test and eradication program is required to eliminate it.[citation needed]
The main way of preventing brucellosis is by using fastidious hygiene in producing raw milk products, or by pasteurizing all milk that is to be ingested by human beings, either in its unaltered form or as a derivative, such as cheese.[citation needed]
Treatment[edit]
Antibiotics such as tetracyclines, rifampicin, and the aminoglycosides streptomycin and gentamicin are effective against Brucella bacteria. However, the use of more than one antibiotic is needed for several weeks, because the bacteria incubate within cells.[citation needed]
The gold standard treatment for adults is daily intramuscular injections of streptomycin 1 g for 14 days and oral doxycycline 100 mg twice daily for 45 days (concurrently). Gentamicin 5 mg/kg by intramuscular injection once daily for 7 days is an acceptable substitute when streptomycin is not available or contraindicated.[18] Another widely used regimen is doxycycline plus rifampicin twice daily for at least 6 weeks. This regimen has the advantage of oral administration. A triple therapy of doxycycline, with rifampicin and co-trimoxazole, has been used successfully to treat neurobrucellosis.[19] Doxycycline plus streptomycin regimen (for 2 to 3 weeks) is more effective than doxycycline plus rifampicin regimen (for 6 weeks).[20]
Doxycycline is able to cross the blood–brain barrier, but requires the addition of two other drugs to prevent relapse. Ciprofloxacin and co-trimoxazole therapy is associated with an unacceptably high rate of relapse. In brucellic endocarditis, surgery is required for an optimal outcome. Even with optimal antibrucellic therapy, relapses still occur in 5 to 10% of patients with Malta fever.[citation needed]
Prognosis[edit]
The mortality of the disease in 1909, as recorded in the British Army and Navy stationed in Malta, was 2%. The most frequent cause of death was endocarditis. Recent advances in antibiotics and surgery have been successful in preventing death due to endocarditis. Prevention of human brucellosis can be achieved by eradication of the disease in animals by vaccination and other veterinary control methods such as testing herds/flocks and slaughtering animals when infection is present. Currently, no effective vaccine is available for humans. Boiling milk before consumption, or before using it to produce other dairy products, is protective against transmission via ingestion. Changing traditional food habits of eating raw meat, liver, or bone marrow is necessary, but difficult to implement.[citation needed] Patients who have had brucellosis should probably be excluded indefinitely from donating blood or organs. Exposure of diagnostic laboratory personnel to Brucella organisms remains a problem in both endemic settings and when brucellosis is unknowingly imported by a patient.[21] After appropriate risk assessment, staff with significant exposure should be offered postexposure prophylaxis and followed up serologically for 6 months.[22]
Epidemiology[edit]
Argentina[edit]
According to a study published in 2002, an estimated 10–13% of farm animals are infected with Brucella species.[23] Annual losses from the disease were calculated at around $60 million. Since 1932, government agencies have undertaken efforts to contain the disease. Currently, all cattle of ages 3–8 months must receive the Brucella abortus strain 19 vaccine.[24]
Australia[edit]
Australia is free of cattle brucellosis, although it occurred in the past. Brucellosis of sheep or goats has never been reported. Brucellosis of pigs does occur. Feral pigs are the typical source of human infections.[25][26]
Canada[edit]
On 19 September 1985, the Canadian government declared its cattle population brucellosis-free. Brucellosis ring testing of milk and cream, and testing of cattle to be slaughtered ended on 1 April 1999. Monitoring continues through testing at auction markets, through standard disease-reporting procedures, and through testing of cattle being qualified for export to countries other than the United States.[27]
China[edit]
An outbreak infecting humans took place in Lanzhou in 2020 after the Lanzhou Biopharmaceutical Plant, which was involved in vaccine production, accidentally pumped out the bacteria into the atmosphere in exhaust air due to use of expired disinfectant. The outbreak affected over 6,000 people.[28][29]
Europe[edit]
Disease incidence map of B. melitensis infections in animals in Europe during the first half of 2006
never reported
not reported in this period
confirmed clinical disease
confirmed infection
no information
Malta[edit]
Until the early 20th century, the disease was endemic in Malta to the point of it being referred to as «Maltese fever». Since 2005, due to a strict regimen of certification of milk animals and widespread use of pasteurization, the illness has been eradicated from Malta.[30]
Republic of Ireland[edit]
Ireland was declared free of brucellosis on 1 July 2009. The disease had troubled the country’s farmers and veterinarians for several decades.[31][32] The Irish government submitted an application to the European Commission, which verified that Ireland had been liberated.[32] Brendan Smith, Ireland’s then Minister for Agriculture, Food and the Marine, said the elimination of brucellosis was «a landmark in the history of disease eradication in Ireland».[31][32] Ireland’s Department of Agriculture, Food and the Marine intends to reduce its brucellosis eradication programme now that eradication has been confirmed.[31][32]
UK[edit]
Mainland Britain has been free of brucellosis since 1979, although there have been episodic re-introductions since.[33] The last outbreak of brucellosis in Great Britain was in cattle in Cornwall in 2004.[33][34] Northern Ireland was declared officially brucellosis-free in 2015.[33]
New Zealand[edit]
Brucellosis in New Zealand is limited to sheep (B. ovis). The country is free of all other species of Brucella.[35]
United States[edit]
Dairy herds in the U.S. are tested at least once a year to be certified brucellosis-free[36] with the Brucella milk ring test.[37] Cows confirmed to be infected are often killed. In the United States, veterinarians are required[citation needed] to vaccinate all young stock, to further reduce the chance of zoonotic transmission. This vaccination is usually referred to as a «calfhood» vaccination. Most cattle receive a tattoo in one of their ears, serving as proof of their vaccination status. This tattoo also includes the last digit of the year they were born.[38]
The first state–federal cooperative efforts towards eradication of brucellosis caused by B. abortus in the U.S. began in 1934.[citation needed]
Brucellosis was originally imported to North America with non-native domestic cattle (Bos taurus), which transmitted the disease to wild bison (Bison bison) and elk (Cervus canadensis). No records exist of brucellosis in ungulates native to America until the early 19th century.[39]
History[edit]
David Bruce (centre), with members of the Mediterranean Fever Commission (Brucellosis)
Brucellosis first came to the attention of British medical officers in the 1850s in Malta during the Crimean War, and was referred to as Malta Fever. Jeffery Allen Marston (1831–1911) described his own case of the disease in 1861. The causal relationship between organism and disease was first established in 1887 by David Bruce.[40][41] Bruce considered the agent spherical and classified it as a coccus.[citation needed]
In 1897, Danish veterinarian Bernhard Bang isolated a bacillus as the agent of heightened spontaneous abortion in cows, and the name «Bang’s disease» was assigned to this condition. Bang considered the organism rod-shaped and classified it as a bacillus. So at the time, no one knew that this bacillus had anything to do with the causative agent in Malta fever.[42]
Maltese scientist and archaeologist Themistocles Zammit identified unpasteurized goat milk as the major etiologic factor of undulant fever in June 1905.[43]
In the late 1910s, American bacteriologist Alice C. Evans was studying the Bang bacillus and gradually realized that it was virtually indistinguishable from the Bruce coccus.[44] The short-rod versus oblong-round morphologic borderline explained the leveling of the erstwhile bacillus/coccus distinction (that is, these «two» pathogens were not a coccus versus a bacillus but rather were one coccobacillus).[44] The Bang bacillus was already known to be enzootic in American dairy cattle, which showed itself in the regularity with which herds experienced contagious abortion.[44] Having made the discovery that the bacteria were certainly nearly identical and perhaps totally so, Evans then wondered why Malta fever was not widely diagnosed or reported in the United States.[44] She began to wonder whether many cases of vaguely defined febrile illnesses were in fact caused by the drinking of raw (unpasteurized) milk.[44] During the 1920s, this hypothesis was vindicated. Such illnesses ranged from undiagnosed and untreated gastrointestinal upset to misdiagnosed[44] febrile and painful versions, some even fatal. This advance in bacteriological science sparked extensive changes in the American dairy industry to improve food safety. The changes included making pasteurization standard and greatly tightening the standards of cleanliness in milkhouses on dairy farms. The expense prompted delay and skepticism in the industry,[44] but the new hygiene rules eventually became the norm. Although these measures have sometimes struck people as overdone in the decades since, being unhygienic at milking time or in the milkhouse, or drinking raw milk, are not a safe alternative.[citation needed]
In the decades after Evans’s work, this genus, which received the name Brucella in honor of Bruce, was found to contain several species with varying virulence. The name «brucellosis» gradually replaced the 19th-century names Mediterranean fever and Malta fever.[45]
Neurobrucellosis, a neurological involvement in brucellosis, was first described in 1879. In the late 19th century, its symptoms were described in more detail by M. Louis Hughes, a Surgeon-Captain of the Royal Army Medical Corps stationed in Malta who isolated brucella organisms from a patient with meningo-encephalitis.[46] In 1989, neurologists in Saudi Arabia made significant contributions to the medical literature involving neurobrucellosis.[47][48]
These obsolete names have previously been applied to brucellosis:[45][49]
- Crimean fever
- Cyprus fever
- Gibraltar fever
- Goat fever
- Italian fever
- Neapolitan fever
Biological warfare[edit]
Brucella species were weaponized by several advanced countries by the mid-20th century. In 1954, B. suis became the first agent weaponized by the United States at its Pine Bluff Arsenal near Pine Bluff, Arkansas. Brucella species survive well in aerosols and resist drying. Brucella and all other remaining biological weapons in the U.S. arsenal were destroyed in 1971–72 when the American offensive biological warfare program was discontinued by order of President Richard Nixon.[50]
The experimental American bacteriological warfare program focused on three agents of the Brucella group:[citation needed]
- Porcine brucellosis (agent US)
- Bovine brucellosis (agent AA)
- Caprine brucellosis (agent AM)
Agent US was in advanced development by the end of World War II. When the United States Air Force (USAF) wanted a biological warfare capability, the Chemical Corps offered Agent US in the M114 bomblet, based on the four-pound bursting bomblet developed for spreading anthrax during World War II. Though the capability was developed, operational testing indicated the weapon was less than desirable, and the USAF designed it as an interim capability until it could eventually be replaced by a more effective biological weapon.[citation needed]
The main drawback of using the M114 with Agent US was that it acted mainly as an incapacitating agent, whereas the USAF administration wanted weapons that were deadly. The stability of M114 in storage was too low to allow for storing it at forward air bases, and the logistical requirements to neutralize a target were far higher than was originally planned. Ultimately, this would have required too much logistical support to be practical in the field.[citation needed]
Agents US and AA had a median infective dose of 500 organisms/person, and for Agent AM it was 300 organisms/person. The incubation time was believed to be about 2 weeks, with a duration of infection of several months. The lethality estimate was, based on epidemiological information, 1 to 2
per cent. Agent AM was believed to be a somewhat more virulent disease, with a fatality rate of 3 per cent being expected.[citation needed]
Other animals[edit]
Species infecting domestic livestock are B. abortus (cattle, bison, and elk), B. canis (dogs), B. melitensis (goats and sheep), B. ovis (sheep), and B. suis (caribou and pigs). Brucella species have also been isolated from several marine mammal species (cetaceans and pinnipeds).[citation needed]
Cattle[edit]
B. abortus is the principal cause of brucellosis in cattle. The bacteria are shed from an infected animal at or around the time of calving or abortion. Once exposed, the likelihood of an animal becoming infected is variable, depending on age, pregnancy status, and other intrinsic factors of the animal, as well as the number of bacteria to which the animal was exposed.[51] The most common clinical signs of cattle infected with B. abortus are high incidences of abortions, arthritic joints, and retained placenta.[citation needed]
The two main causes for spontaneous abortion in animals are erythritol, which can promote infections in the fetus and placenta,[clarification needed] and the lack of anti-Brucella activity in the amniotic fluid. Males can also harbor the bacteria in their reproductive tracts, namely seminal vesicles, ampullae, testicles, and epididymises.[citation needed]
Dogs[edit]
The causative agent of brucellosis in dogs, B. canis, is transmitted to other dogs through breeding and contact with aborted fetuses. Brucellosis can occur in humans who come in contact with infected aborted tissue or semen. The bacteria in dogs normally infect the genitals and lymphatic system, but can also spread to the eyes, kidneys, and intervertebral discs. Brucellosis in the intervertebral disc is one possible cause of discospondylitis. Symptoms of brucellosis in dogs include abortion in female dogs and scrotal inflammation and orchitis in males. Fever is uncommon. Infection of the eye can cause uveitis, and infection of the intervertebral disc can cause pain or weakness. Blood testing of the dogs prior to breeding can prevent the spread of this disease. It is treated with antibiotics, as with humans, but it is difficult to cure.[52]
Aquatic wildlife[edit]
Brucellosis in cetaceans is caused by the bacterium B. ceti. First discovered in the aborted fetus of a bottlenose dolphin, the structure of B. ceti is similar to Brucella in land animals. B. ceti is commonly detected in two suborders of cetaceans, the Mysticeti and Odontoceti. The Mysticeti include four families of baleen whales, filter-feeders, and the Odontoceti include two families of toothed cetaceans ranging from dolphins to sperm whales. B. ceti is believed to transfer from animal to animal through sexual intercourse, maternal feeding, aborted fetuses, placental issues, from mother to fetus, or through fish reservoirs. Brucellosis is a reproductive disease, so has an extreme negative impact on the population dynamics of a species. This becomes a greater issue when the already low population numbers of cetaceans are taken into consideration. B. ceti has been identified in four of the 14 cetacean families, but the antibodies have been detected in seven of the families. This indicates that B. ceti is common amongst cetacean families and populations. Only a small percentage of exposed individuals become ill or die. However, particular species apparently are more likely to become infected by B. ceti. The harbor porpoise, striped dolphin, white-sided dolphin, bottlenose dolphin, and common dolphin have the highest frequency of infection amongst odontocetes. In the mysticetes families, the northern minke whale is by far the most infected species. Dolphins and porpoises are more likely to be infected than cetaceans such as whales. With regard to sex and age biases, the infections do not seem influenced by the age or sex of an individual. Although fatal to cetaceans, B. ceti has a low infection rate for humans.[53]
Terrestrial wildlife[edit]
The disease in its various strains can infect multiple wildlife species, including elk (Cervus canadensis), bison (Bison bison), African buffalo (Syncerus caffer), European wild boar (Sus scrofa), caribou (Rangifer tarandus), moose (Alces alces), and marine mammals (see section on aquatic wildlife above).[54][55] While some regions use vaccines to prevent the spread of brucellosis between infected and uninfected wildlife populations, no suitable brucellosis vaccine for terrestrial wildlife has been developed.[56] This gap in medicinal knowledge creates more pressure for management practices that reduce spread of the disease.[56]
Wild bison and elk in the greater Yellowstone area are the last remaining reservoir of B. abortus in the US. The recent transmission of brucellosis from elk back to cattle in Idaho and Wyoming illustrates how the area, as the last remaining reservoir in the United States, may adversely affect the livestock industry. Eliminating brucellosis from this area is a challenge, as many viewpoints exist on how to manage diseased wildlife. However, the Wyoming Game and Fish Department has recently begun to protect scavengers (particularly coyotes and red fox) on elk feedgrounds, because they act as sustainable, no-cost, biological control agents by removing infected elk fetuses quickly.[57]
The National Elk Refuge in Jackson, Wyoming asserts that the intensity of the winter feeding program affects the spread of brucellosis more than the population size of elk and bison.[54] Since concentrating animals around food plots accelerates spread of the disease, management strategies to reduce herd density and increase dispersion could limit its spread.[54]
Effects on hunters[edit]
Hunters may be at additional risk for exposure to brucellosis due to increased contact with susceptible wildlife, including predators that may have fed on infected prey. Hunting dogs can also be at risk of infection.[58] Exposure can occur through contact with open wounds or by directly inhaling the bacteria while cleaning game.[59] In some cases, consumption of undercooked game can result in exposure to the disease.[59] Hunters can limit exposure while cleaning game through the use of precautionary barriers, including gloves and masks, and by washing tools rigorously after use.[56][60] By ensuring that game is cooked thoroughly, hunters can protect themselves and others from ingesting the disease.[59] Hunters should refer to local game officials and health departments to determine the risk of brucellosis exposure in their immediate area and to learn more about actions to reduce or avoid exposure.[citation needed]
See also[edit]
- Brucella suis
References[edit]
- ^ Wyatt HV (2014). «How did Sir David Bruce forget Zammit and his goats ?» (PDF). Journal of Maltese History. Malta: Department of History, University of Malta. 4 (1): 41. ISSN 2077-4338. Archived from the original (PDF) on 2016-07-21. Journal archive
- ^ a b c «Brucellosis». mayoclinic.org. Mayo Clinic. Retrieved June 5, 2022.
- ^ «Brucellosis». mayoclinic.org. Mayo Clinic. Retrieved June 5, 2022.
- ^ «Brucellosis». American Heritage Dictionary. Archived from the original on 2011-06-06.
- ^ «Maltese Fever». wrongdiagnosis.com. February 25, 2009.
- ^ «Diagnosis and Management of Acute Brucellosis in Primary Care» (PDF). Brucella Subgroup of the Northern Ireland Regional Zoonoses Group. August 2004. Archived from the original (PDF) on 2007-10-13.
- ^ Di Pierdomenico A, Borgia SM, Richardson D, Baqi M (July 2011). «Brucellosis in a returned traveller». CMAJ. 183 (10): E690-2. doi:10.1503/cmaj.091752. PMC 3134761. PMID 21398234.
- ^ Park. K., Park’s textbook of preventive and social medicine, 23 editions. Page 290-91
- ^ Roy, Rabindra (2013), «Chapter-23 Biostatistics», Mahajan and Gupta Textbook of Preventive and Social Medicine, Jaypee Brothers Medical Publishers (P) Ltd, pp. 434–449, retrieved 2022-11-13
- ^ «Brucellosis: Resources: Surveillance». CDC. 2018-10-09.
- ^ Wyatt HV (October 2005). «How Themistocles Zammit found Malta Fever (brucellosis) to be transmitted by the milk of goats». Journal of the Royal Society of Medicine. The Royal Society of Medicine Press. 98 (10): 451–4. doi:10.1177/014107680509801009. OCLC 680110952. PMC 1240100. PMID 16199812.
- ^ Peck ME, Jenpanich C, Amonsin A, Bunpapong N, Chanachai K, Somrongthong R, et al. (January 2019). «Knowledge, Attitudes and Practices Associated with Brucellosis among Small-Scale Goat Farmers in Thailand». Journal of Agromedicine. 24 (1): 56–63. doi:10.1080/1059924X.2018.1538916. PMID 30350754. S2CID 53034163.
- ^ Franco MP, Mulder M, Gilman RH, Smits HL (December 2007). «Human brucellosis». The Lancet. Infectious Diseases. 7 (12): 775–86. doi:10.1016/S1473-3099(07)70286-4. PMID 18045560.
- ^ Al Dahouk S, Nöckler K (July 2011). «Implications of laboratory diagnosis on brucellosis therapy». Expert Review of Anti-Infective Therapy. 9 (7): 833–45. doi:10.1586/eri.11.55. PMID 21810055. S2CID 5068325.
- ^ Mantur B, Parande A, Amarnath S, Patil G, Walvekar R, Desai A, et al. (August 2010). «ELISA versus conventional methods of diagnosing endemic brucellosis». The American Journal of Tropical Medicine and Hygiene. 83 (2): 314–8. doi:10.4269/ajtmh.2010.09-0790. PMC 2911177. PMID 20682874.
- ^ Yu WL, Nielsen K (August 2010). «Review of detection of Brucella spp. by polymerase chain reaction». Croatian Medical Journal. 51 (4): 306–13. doi:10.3325/cmj.2010.51.306. PMC 2931435. PMID 20718083.
- ^ Vrioni G, Pappas G, Priavali E, Gartzonika C, Levidiotou S (June 2008). «An eternal microbe: Brucella DNA load persists for years after clinical cure». Clinical Infectious Diseases. 46 (12): e131-6. doi:10.1086/588482. PMID 18462106.
- ^ Hasanjani Roushan MR, Mohraz M, Hajiahmadi M, Ramzani A, Valayati AA (April 2006). «Efficacy of gentamicin plus doxycycline versus streptomycin plus doxycycline in the treatment of brucellosis in humans». Clinical Infectious Diseases. 42 (8): 1075–80. doi:10.1086/501359. PMID 16575723.
- ^ McLean DR, Russell N, Khan MY (October 1992). «Neurobrucellosis: clinical and therapeutic features». Clinical Infectious Diseases. 15 (4): 582–90. doi:10.1093/clind/15.4.582. PMID 1420670.
- ^ Yousefi-Nooraie R, Mortaz-Hejri S, Mehrani M, Sadeghipour P (October 2012). «Antibiotics for treating human brucellosis». The Cochrane Database of Systematic Reviews. 10: CD007179. doi:10.1002/14651858.cd007179.pub2. PMC 6532606. PMID 23076931.
- ^ Yagupsky P, Baron EJ (August 2005). «Laboratory exposures to brucellae and implications for bioterrorism». Emerging Infectious Diseases. 11 (8): 1180–5. doi:10.3201/eid1108.041197. PMC 3320509. PMID 16102304.
- ^ Centers for Disease Control Prevention (CDC) (January 2008). «Laboratory-acquired brucellosis—Indiana and Minnesota, 2006». MMWR. Morbidity and Mortality Weekly Report. 57 (2): 39–42. PMID 18199967.
- ^ Samartino LE (December 2002). «Brucellosis in Argentina». Veterinary Microbiology. 90 (1–4): 71–80. doi:10.1016/s0378-1135(02)00247-x. PMID 12414136.
- ^ «SENASA – Direcci n Nacional de Sanidad Animal». viejaweb.senasa.gov.ar. Archived from the original on 2016-02-16. Retrieved 2016-02-10.
- ^ «Queensland Health: Brucellosis». State of Queensland (Queensland Health). 2010-11-24. Archived from the original on 2011-04-22. Retrieved 2011-06-06.
- ^
Lehane, Robert (1996) Beating the Odds in a Big Country: The eradication of bovine brucellosis and tuberculosis in Australia, CSIRO Publishing, ISBN 0-643-05814-1 - ^ «Reportable Diseases». Accredited Veterinarian’s Manual. Canadian Food Inspection Agency. Retrieved 2007-03-18.
- ^ China reports outbreak of brucellosis disease ‘way larger’ than originally thought 18 September 2020 www.news.com.au, accessed 18 September 2020
- ^ «兰州药厂泄漏事件布病患者:肿痛无药可吃,有人已转成慢性病_绿政公署_澎湃新闻-The Paper». www.thepaper.cn. Retrieved 2 June 2021.
- ^ Naudi JR (2005). Brucellosis, The Malta Experience. Malta: Publishers Enterprises group (PEG) Ltd. ISBN 978-99909-0-425-3.
- ^ a b c «Ireland free of brucellosis». RTÉ. 2009-07-01. Retrieved 2009-07-01.
- ^ a b c d «Ireland declared free of brucellosis». The Irish Times. 2009-07-01. Archived from the original on 2021-04-03. Retrieved 2009-07-01.
Michael F Sexton, president of Veterinary Ireland, which represents vets in practice, said: «Many vets and farmers in particular suffered significantly with brucellosis in past decades and it is greatly welcomed by the veterinary profession that this debilitating disease is no longer the hazard that it once was.»
- ^ a b c Monitoring brucellosis in Great Britain 3 September 2020 veterinary-practice.com, accessed 18 September 2020
- ^ Guidance Brucellosis: how to spot and report the disease 18 October 2018 www.gov.uk, accessed 18 September 2020
- ^ «MAF Biosecurity New Zealand: Brucellosis». Ministry of Agriculture and Forestry of New Zealand. Archived from the original on 2012-03-20. Retrieved 2011-06-06.
- ^ Brucellosis Eradication APHIS 91–45–013. United States Department of Agriculture. October 2003. p. 14.
- ^ Hamilton AV, Hardy AV (March 1950). «The brucella ring test; its potential value in the control of brucellosis». American Journal of Public Health and the Nation’s Health. 40 (3): 321–3. doi:10.2105/AJPH.40.3.321. PMC 1528431. PMID 15405523.
- ^ Vermont Beef Producers. «How important is calfhood vaccination?» (PDF). Archived from the original (PDF) on 2008-05-09.
- ^ Meagher M, Meyer ME (September 1994). «On the Origin of Brucellosis in Bison of Yellowstone National Park: A Review» (PDF). Conservation Biology. 8 (3): 645–653. doi:10.1046/j.1523-1739.1994.08030645.x. JSTOR 2386505. Archived from the original (PDF) on 2017-01-08. Retrieved 2017-01-07.
- ^ Wilkinson L (1993). «Brucellosis». In Kiple KF (ed.). The Cambridge World History of Human Disease. Cambridge University Press.
- ^ Brucellosis named after Major-General Sir David Bruce at Who Named It?
- ^ Evans, Alice (1963). Dr. Alice C. Evans Memoir.
- ^ Wyatt HV (2015). «The Strange Case of Temi Zammit’s missing experiments» (PDF). Journal of Maltese History. Malta: Department of History, University of Malta. 4 (2): 54–56. ISSN 2077-4338. Archived from the original (PDF) on 2016-07-21. Journal archive
- ^ a b c d e f g de Kruif P (1932). «Ch. 5 Evans: death in milk». Men Against Death. New York: Harcourt, Brace. OCLC 11210642.
- ^ a b Wyatt HV (31 July 2004). «Give A Disease A Bad Name». British Medical Journal. BMJ Publishing Group Ltd. 329 (7460): 272–278. doi:10.1136/bmj.329.7460.272. ISSN 0959-535X. JSTOR 25468794. OCLC 198096808. PMC 498028.
- ^ Madkour, M. Monir (2014). Brucellosis. Elsevier Science. p. 160. ISBN 9781483193595.
- ^ Malhotra R (2004). «Saudi Arabia». Practical Neurology. 4 (3): 184–185. doi:10.1111/j.1474-7766.2004.03-225.x.
- ^ Al-Sous MW, Bohlega S, Al-Kawi MZ, Alwatban J, McLean DR (March 2004). «Neurobrucellosis: clinical and neuroimaging correlation». AJNR. American Journal of Neuroradiology. 25 (3): 395–401. PMC 8158553. PMID 15037461.
- ^ «Medicine: Goat Fever». Time. 1928-12-10. ISSN 0040-781X. Retrieved 2017-05-01.
- ^ Woods, Jon B. (April 2005). USAMRIID’s Medical Management of Biological Casualties Handbook (PDF) (6th ed.). Fort Detrick, Maryland: U.S. Army Medical Institute of Infectious Diseases. p. 53. Archived from the original (PDF) on 2007-06-09.
- ^ Radostits, O.M., C.C. Gay, D.C. Blood, and K.W. Hinchcliff. (2000). Veterinary Medicine, A textbook of the Diseases of Cattle, Sheep, Pigs, Goats and Horses. Harcourt Publishers Limited, London, pp. 867–882. ISBN 0702027774.
- ^ Ettinger SJ, Feldman EC (1995). Textbook of Veterinary Internal Medicine (4th ed.). W.B. Saunders Company. ISBN 978-0-7216-4679-4.
- ^ Guzmán-Verri C, González-Barrientos R, Hernández-Mora G, Morales JA, Baquero-Calvo E, Chaves-Olarte E, Moreno E (2012). «Brucella ceti and brucellosis in cetaceans». Frontiers in Cellular and Infection Microbiology. 2: 3. doi:10.3389/fcimb.2012.00003. PMC 3417395. PMID 22919595.
- ^ a b c «Brucellosis». www.fws.gov. U.S. Fish &Wildlife Service. 2016. Archived from the original on 2016-10-09. Retrieved 2016-10-03.
- ^ Godfroid J (August 2002). «Brucellosis in wildlife» (PDF). Revue Scientifique et Technique. 21 (2): 277–86. doi:10.20506/rst.21.2.1333. PMID 11974615. Archived from the original (PDF) on 2015-06-06. Retrieved 2016-10-07.
- ^ a b c Godfroid J, Garin-Bastuji B, Saegerman C, Blasco JM (April 2013). «Brucellosis in terrestrial wildlife» (PDF). Revue Scientifique et Technique. 32 (1): 27–42. CiteSeerX 10.1.1.1020.9652. doi:10.20506/rst.32.1.2180. PMID 23837363. Archived from the original (PDF) on 2015-06-06. Retrieved 2016-10-07.
- ^ Cross PC, Maichak EJ, Brennan A, Scurlock BM, Henningsen J, Luikart G (April 2013). «An ecological perspective on Brucella abortus in the western United States» (PDF). Revue Scientifique et Technique. 32 (1): 79–87. doi:10.20506/rst.32.1.2184. PMID 23837367.
- ^ CDC — Hunters Risks — Animals That Can Put Hunters at Risk
- ^ a b c «CDC – Home – Brucellosis». www.cdc.gov. Center for Disease Control. 2016. Retrieved 2016-10-03.
- ^ «Zoonoses – Brucellosis». www.who.int/en/. World Health Organization. 2016. Archived from the original on March 9, 2005. Retrieved 2016-10-03.
Further reading[edit]
- Fact sheet on Brucellosis from World Organisation for Animal Health
- Brucella genomes and related information at PATRIC, a Bioinformatics Resource Center funded by NIAID
- Prevention about Brucellosis from Centers for Disease Control
- Capasso L (August 2002). «Bacteria in two-millennia-old cheese, and related epizoonoses in Roman populations». The Journal of Infection. 45 (2): 122–7. doi:10.1053/jinf.2002.0996. PMID 12217720. – re high rate of brucellosis in humans in ancient Pompeii
- Brucellosis, factsheet from European Centre for Disease Prevention and Control
Значение слова «бруцеллёз»

-
БРУЦЕЛЛЁЗ, -а, м. Заразное заболевание коз, овец, крупного рогатого скота, свиней, способное передаваться от них человеку.
[По имени английского врача D. Bruce, открывшего микроб бруцелла]
Источник (печатная версия): Словарь русского языка: В 4-х
т. / РАН,
Ин-т лингвистич.
исследований; Под ред. А. П. Евгеньевой. — 4-е изд., стер. — М.: Рус. яз.;
Полиграфресурсы,
1999;
(электронная версия): Фундаментальная
электронная
библиотека
- Бруцеллёз (лат. brucellosis) — зооантропонозная инфекция, передающаяся от больных животных человеку, характеризующаяся множественным поражением органов и систем организма человека. Микробов — виновников этой болезни — впервые в 1886 году обнаружил английский учёный Дэвид Брюс. В его честь их и назвали бруцеллами, а вызываемое ими заболевание — бруцеллёзом.
Источник: Википедия
-
бруцеллёз
1. зоонозная инфекция, передающаяся от больных животных человеку
Источник: Викисловарь
Делаем Карту слов лучше вместе
Привет! Меня зовут Лампобот, я компьютерная программа, которая помогает делать
Карту слов. Я отлично
умею считать, но пока плохо понимаю, как устроен ваш мир. Помоги мне разобраться!
Спасибо! Я стал чуточку лучше понимать мир эмоций.
Вопрос: митрополия — это что-то нейтральное, положительное или отрицательное?
Синонимы к слову «бруцеллёз»
Предложения со словом «бруцеллёз»
- Волевой, активный человек, он тяжело переживал вынужденный отрыв от жизни, когда в 1932 году заболел бруцеллёзом и надолго оказался прикованным к постели.
- Сейчас считается, что коров поразил бруцеллёз, но поселенцы этого учёного слова, конечно, не знали, винили во всём «змеиный корень», беду свою именовали «коровьей болезнью», – a когда смекнули, что от коров она передаётся и людям, было уже поздно.
- Прожитые годы не украшают её: на голове не благородная седина, а давно нечёсаные короткие волосы непонятного цвета, она трясётся от перенесённого сорок лет назад бруцеллёза, а один глаз больше другого, наверное, от глаукомы.
- (все предложения)
Отправить комментарий
Дополнительно
Смотрите также
-
Волевой, активный человек, он тяжело переживал вынужденный отрыв от жизни, когда в 1932 году заболел бруцеллёзом и надолго оказался прикованным к постели.
-
Сейчас считается, что коров поразил бруцеллёз, но поселенцы этого учёного слова, конечно, не знали, винили во всём «змеиный корень», беду свою именовали «коровьей болезнью», – a когда смекнули, что от коров она передаётся и людям, было уже поздно.
-
Прожитые годы не украшают её: на голове не благородная седина, а давно нечёсаные короткие волосы непонятного цвета, она трясётся от перенесённого сорок лет назад бруцеллёза, а один глаз больше другого, наверное, от глаукомы.
- (все предложения)
- токсоплазмоз
- сальмонеллёз
- бронхопневмония
- сифилис
- уретрит
- (ещё синонимы…)
- при хроническом бруцеллёзе
- (полная таблица сочетаемости…)
- Разбор по составу слова «бруцеллёз»
- Как правильно пишется слово «бруцеллёз»
Бруцеллёз

Бруцеллёз — это инфекция, которую вызывают бактерии рода Brucella. Человек может заболеть, если выпьет непастеризованного молока, съест плохо прожаренное мясо или просто погладит заражённое животное. На ранней стадии бруцеллёз легко вылечить, без лечения заболевание приводит к разрушению внутренних органов.
СОДЕРЖАНИЕ
Бруцеллёз: определение болезни
Бруцеллёз: определение болезни
Бруцеллёз (болезнь Банга, мальтийская лихорадка, гибралтарская лихорадка, кипрская лихорадка, ундулирующая лихорадка) — острая бактериальная инфекция, которая передаётся людям от заражённых животных.
Бруцеллёз может протекать остро, подостро и хронически. Некоторые инфицированные выздоравливают даже без лечения, у остальных заболевание может переходить в хроническую форму, постепенно разрушая сердце, печень, почки и другие органы.
У переболевших формируется нестойкий иммунитет, который сохраняется от 8 до 10 месяцев. Наличие антител не препятствует повторному инфицированию и формированию бактерионосительства, но способствует более лёгкому течению болезни.
Код МКБ
В Международной статистической классификации болезней и проблем, связанных со здоровьем, одиннадцатого пересмотра (МКБ-11) бруцеллёз входит в группу «Некоторые зоонозные и бактериальные инфекции» и обозначается кодом 1C45. В МКБ-10 код А23.0—А23.9
Источник инфекции
Возбудитель бруцеллёза — небольшая сферическая бактерия рода Brucella из класса альфа-протеобактерий. Род назван в честь шотландского военного врача Дэвида Брюса, который первым выделил и описал микроорганизмы на Мальте в 1887 году.
Бруцеллы — неподвижные грамотрицательные бактерии, похожие на микроскопические рисовые зёрна
По международной классификации род Brucella объединяет семь видов, но опасны для человека только четыре.
Виды бруцелл, способные инфицировать человека:
- Brucella abortus (основной хозяин — крупный рогатый скот);
- Brucella melitensis (основной хозяин — овцы и козы);
- Brucella suis (основной хозяин — свиньи, зайцы, олени);
- Brucella canis (основной хозяин — собаки).
Все бруцеллы способны длительно выживать вне организма-носителя. Так, в почве или воде они сохраняются более 2 месяцев, в сыром мясе — 3 месяца, в сыре — более 2 месяцев, в засоленном мясе — месяц.
В сыром молоке при температуре холодильника возбудитель бруцеллёза сохраняется до 10 дней, в сливочном масле — более 4 недель, во внутренних органах, костях, мышцах и лимфатических узлах инфицированных туш — в течение 1 месяца и более. В замороженных инфицированных мясных и молочных продуктах бруцеллы остаются жизнеспособными в течение всего срока хранения.
Бруцеллы могут до 70 дней сохраняться в непастеризованных молочных продуктах
При нагревании до 60 °С бруцеллы погибают только через 30 мин, при кипячении — практически моментально.
Природные хозяева бруцелл — овцы, козы, крупный рогатый скот и свиньи. Отмечены случаи заражения людей бруцеллёзом от северных оленей. В редких случаях источником заражения могут быть лошади, верблюды, яки и некоторые другие животные, которые выделяют возбудителя с молоком, мочой, калом, околоплодной жидкостью.
Причины бруцеллёза
Причина заболевания — бактерии рода Brucella, которые живут в организме животных (как правило, сельскохозяйственных) и могут передаваться человеку, если он близко контактирует с источником инфекции или употребляет недостаточно термически обработанные молочные и мясные продукты.
Группы риска
В группе риска по заражению бруцеллёзом — люди, которые держат дома коров, коз, овец и других сельскохозяйственных животных. Есть и другие группы риска.
Группы риска по заражению бруцеллёзом:
- фермеры, занимающиеся разведением домашних животных;
- охотники;
- ветеринары;
- сотрудники бактериологических лабораторий;
- рабочие мясокомбинатов, боен, шерстеперерабатывающих фабрик;
- туристы.
В зоне риска заражения бруцеллёзом — фермеры, занимающиеся разведением домашних животных
Заражение бруцеллёзом от коз и овец чаще диагностируют весной и летом, от крупного рогатого скота — в течение всего года.
Пути передачи бруцеллёза
Бруцеллёз — это зоонозная инфекция, которая может передаваться человеку от животных.
Обычно заражаются люди, которые часто контактируют с сельскохозяйственными животными, а также те, кто пьёт сырое (непастеризованное) молоко или ест продукты, приготовленные из него (сыр, творог). Кроме того, бактерии могут остаться в недостаточно проваренном или прожаренном мясе.
Возможны и другие механизмы передачи бруцеллёза.
Контактный механизм передачи бруцеллёза. Заражение происходит при попадании возбудителя на повреждённую кожу и слизистую оболочку.
Аэрогенный механизм передачи бруцеллёза. Заражение происходит при вдыхании частиц шерсти, пыли, навоза или земли, на которых остались бруцеллы. Заболеть можно при стрижке овец, сортировке шерсти, вычёсывании пуха, а также при уборке помещений и территорий, где содержат больных животных.
Трансплацентарный механизм передачи бруцеллёза. Бактерии передаются к ребёнку через плаценту от заражённой матери.
Лабораторное заражение бруцеллёзом. Инфицирование происходит при работе с культурами бактерий.
Распространённость
Бруцеллёз распространён в Грузии, Армении, Португалии, Испании, Турции, Италии, Греции, Мексике и некоторых других странах с развитым животноводством. Кроме того, в национальной кухне этих стран немало блюд из сырого мяса и непастеризованного молока.
Бруцеллёз в России
На территории России заболевание чаще встречается в Краснодарском крае, Сибири и на Северном Кавказе. Это связано с тем, что в перечисленных регионах развито фермерское животноводство, а бруцеллёз — профессиональное заболевание работников этой сферы (пастухов, доярок, ветеринаров и зоотехников, рабочих мясокомбинатов, боен и фабрик по переработке шерсти).
Классификация бруцеллёза
В зависимости от длительности течения заболевания бруцеллёз бывает острым (до 3 месяцев), подострым (до 6 месяцев) и хроническим (более 6 месяцев). Отдельно выделяют резидуальную, так называемую остаточную форму болезни, которая включает изменения, сохраняющиеся свыше 2 лет после полного излечения от инфекции: воспаление или боль в суставах, поражение нервной, репродуктивной, сердечно-сосудистой системы. Но зачастую границы перехода стадий инфекционного процесса установить сложно, поэтому указанные временные промежутки весьма относительны.
Кроме того, выделяют пять форм хронического бруцеллёза (по Г. П. Рудневу), которые отличаются локализацией поражений.
Формы хронического бруцеллёза (по Г. П. Рудневу):
- висцеральная — поражение внутренних органов (сердца, сосудов, лёгких, печени или селезёнки);
- костно-суставная — поражение суставов и костей;
- неврологическая — поражение нервной системы;
- урогенитальная — поражение органов мочеполовой системы;
- комбинированная — объединяет поражения со стороны разных систем организма.
Симптомы бруцеллёза
Время от момента попадания бактерии в организм и до появления первых симптомов называют инкубационным периодом. При бруцеллёзе он составляет в среднем от 1 до 3 недель, но может достигать и 5 месяцев. Симптомы будут зависеть от формы болезни.
Симптомы острого и подострого бруцеллёза
Острая и подострая формы заболевания, как правило, начинаются с резкого ухудшения самочувствия и появления характерных клинических симптомов, которые схожи с ОРВИ или гриппом.
Симптомы острого бруцеллёза:
- высокая температура (до 39–40 °С);
- озноб;
- потеря аппетита;
- вялость и слабость;
- сильная головная боль;
- диарея и рвота;
- боль в мышцах, суставах, пояснице;
- покраснение кожи, сыпь;
- увеличение лимфатических узлов.
На ранней стадии симптомы постепенно нарастают, спустя некоторое время состояние больного может нормализоваться.
У пожилых людей заболевание часто начинается стёрто: сначала пациенты испытывают лёгкое недомогание, затем их самочувствие ухудшается, поднимается температура, появляются боли в мышцах и суставах.
Боль в пояснице в сочетании с высокой температурой может свидетельствовать о заражении бруцеллёзом
Подострой форме болезни свойственно волнообразное течение: симптомы, характерные для разгара болезни (повышение температуры, недомогание, боль в мышцах) то появляются, то пропадают.
Симптомы хронического бруцеллёза
Когда бруцеллы долго находятся в организме, они могут поражать многие органы и системы, включая репродуктивную систему, печень, сердце, головной и спинной мозг.
Симптомы поражения опорно-двигательного аппарата: воспаление и болезненность суставов, ограничение подвижности, воспаление крестцово-подвздошных сочленений (сакроилеит).
После нескольких месяцев болезни (если человек не получает лечения) развиваются хронические артриты с повторяющимися приступами ноющей боли в суставах, которые могут длиться от пары часов до нескольких месяцев.
Артрит может переходить с одного сустава на другой, чаще всего поражаются коленные суставы.
Чаще всего от бруцеллёза страдают коленные суставы
Симптомы поражения нервной системы: психоорганический синдром, судорожные приступы, простреливающие боли по ходу нервных стволов, нарушение чувствительности в конечностях, ухудшение зрения, шум в ушах.
Симптомы хронического бруцеллёза (со стороны нервной системы):
- паралич лицевого нерва,
- менингит,
- онемение рук и ног,
- корешковые боли,
- нарушение координации движений,
- потеря памяти,
- сложности с концентрацией внимания,
- нарушения сна.
Изменения со стороны вегетативной нервной системы: повышенная потливость, учащение сердцебиения. Сердечно-сосудистые нарушения развиваются у части заболевших. Пациенты отмечают нарушения ритма сердца, головокружение, одышку и другие симптомы.
Симптомы поражения мочеполовой системы: зуд и жжение при мочеиспускании, боль при половом контакте, нарушения менструального цикла у женщин.
Висцеральные нарушения. У части заболевших развивается гепатит. Обычно он протекает в безжелтушной форме, иногда возможны жалобы на снижение аппетита, боль и тяжесть в правом подреберье (связаны с увеличением печени).
При бруцеллёзе у части заболевших развивается спленомегалия — увеличение селезёнки, потому что орган активно включается в патологический процесс.
Кроме того, при бруцеллёзе может развиваться острая почечная недостаточность — уменьшается объём мочи, повышается артериальное давление, человек ощущает слабость и недомогание.
Часто при хроническом бруцеллёзе развиваются смешанные поражения, например со стороны нервной системы и опорно-двигательного аппарата.
По мере прогрессирования болезни может развиться спленомегалия — увеличение селезёнки (слева нормальная селезёнка, справа — увеличенная)
Симптомы резидуального бруцеллёза
Резидуальный бруцеллёз — отсроченные последствия инфекции, которые, как правило, связаны с глубинным нарушением иммунных реакций, структурных и функциональных нарушений в работе органов и систем. Так, у человека может появиться постоянная субфебрильная (слегка повышенная) температура тела, рецидивирующие боли или воспаление суставов.
Кроме того, бруцеллёз может оставлять после себя серьёзные изменения в области нервных стволов и сплетений. В результате возникает неврологическая симптоматика: нарушение чувствительности и координации движений, онемение конечностей. Также длительное течение заболевания способствует формированию стойких нарушений со стороны опорно-двигательного аппарата: деформации суставов, атрофии мышц.
Бруцеллёз при беременности
Возбудители бруцеллёза — бактерии рода Brucella — могут проникать через плаценту и инфицировать плод (врождённый бруцеллёз).
Заражение женщины бруцеллёзом во время вынашивания ребёнка повышает риск развития акушерских осложнений: преждевременных родов, выкидыша. Кроме того, внутриутробное заражение может привести к патологиям развития нервной и сердечно-сосудистой системы плода.
Диагностика бруцеллёза
Если у человека поднимается температура, ухудшается самочувствие, болят кости и суставы, следует как можно скорее обратиться к терапевту или вызвать врача на дом.
Обратиться за консультацией к специалисту также следует, если через некоторое время после контакта с сельскохозяйственными животными или употребления непастеризованного молока появились необычные симптомы.
Симптомы, с которыми следует обратиться к врачу:
- повышение температуры тела;
- боль в суставах и в нижней части спины;
- нарушение координации движений, походки;
- корешковые боли в виде прострелов;
- асимметрия лица, онемение пальцев рук или ног;
- бессонница, эйфория, неадекватное поведение, судорожные приступы, головная боль.
К какому врачу обращаться при подозрении на бруцеллёз
Как правило, пациенты сначала обращаются к врачу-терапевту, который, при подозрении на бруцеллёз, направляет их дальше к профильному специалисту — врачу-инфекционисту.
На консультации врач проведёт опрос и осмотр и, возможно, назначит инструментальные и лабораторные исследования.
Лабораторная диагностика
Для диагностики бруцеллёза назначают клинические и биохимические исследования крови, анализы на антитела к бруцеллам.
Клинический анализ крови проводят, чтобы оценить общее состояние человека.
3.9.1. Вен. кровь (+220 ₽) 
Вен. кровь (+220 ₽) 1 день

Биохимический анализ крови позволяет оценить состояние печени и почек на фоне болезни и избежать развития осложнений. При типичном неосложнённом течении в результатах анализа не будет существенных отклонений.
28.339. Вен. кровь (+220 ₽) 
Вен. кровь (+220 ₽) 1 день

Чтобы оценить тяжесть воспаления, врач может назначить анализ крови на основные маркеры воспаления — С-реактивный белок и скорость оседания эритроцитов.
1.50. Вен. кровь (+220 ₽) 
Вен. кровь (+220 ₽) Колич. 1 день

3.3.1. Вен. кровь (+220 ₽) 
Вен. кровь (+220 ₽) Колич. 1 день

Чтобы понять, болел ли человек бруцеллёзом, или уточнить стадию инфекции, используют тесты на антитела. На разных стадиях заболевания синтезируются антитела разных классов — M (IgM), G (IgG) или А (IgA). При заражении бруцеллёзом в кровь сначала поступают иммуноглобулины класса M, примерно через 10–14 дней после заражения — G, затем — A. Важно сдавать кровь на антитела IgG в динамике методом парных сывороток: нарастание титра подтверждает диагноз «бруцеллёз».
20.127. Вен. кровь (+220 ₽) 
Вен. кровь (+220 ₽) Кач. 2 дня

20.128. Вен. кровь (+220 ₽) 
Вен. кровь (+220 ₽) 2 дня

Кроме того, врач может назначить анализ на антитела к бруцеллёзу для дифференциальной диагностики с гриппом, брюшным тифом, малярией, инфекционным мононуклеозом, лептоспирозом, лимфогранулематозом, ревматоидным полиартритом.
Инструментальные методы исследования
Врач может направить пациента на инструментальные обследования, чтобы оценить тяжесть поражения внутренних органов и нервной системы.
Как правило, для диагностики используются:
- рентгенография и диагностическая пункция суставов — позволяют оценить степень поражения соединительной ткани;
- электрокардиография (ЭКГ) — диагностика поражений сердца;
- КТ и МРТ головного и спинного мозга, электроэнцефалография (ЭЭГ) и люмбальная пункция с исследованием ликвора — диагностика неврологических нарушений.
Лечение бруцеллёза
Независимо от формы болезни лечение проводится в стационаре инфекционного профиля или в инфекционном отделении.
Терапия, направленная на уничтожение возбудителя бруцеллёза, бактерии рода Brucella, наиболее эффективна в остром периоде заболевания (в первые 3 суток). При длительном течении болезни (подострая и хроническая форма) курс лечения включает дополнительные препараты для лечения поражений внутренних органов и систем и составляет не менее 6 недель.
Симптоматическое лечение
Для уменьшения симптомов бруцеллёза врач может назначить симптоматические лекарственные средства: от боли — нестероидные противовоспалительные препараты, глюкокортикоиды; при выраженной интоксикации — инфузионную терапию.
Антибактериальная терапия
Для лечения бруцеллёза, как правило, назначают курс антибактериальной терапии. Такая терапия помогает пациентам на любой стадии болезни.
Курс лечения длительный и составляет в среднем 21 день. Чем тяжелее стадия — тем дольше терапия.
Пробиотики
Антибактериальная терапия, которая применяется для лечения бруцеллёза, приводит к гибели не только патогенных, но и полезных бактерий. Особенно страдают представители нормальной микрофлоры кишечника. В результате после курса антибактериальной терапии у человека могут появиться симптомы дисбактериоза: диарея или запор, вздутие живота. Чтобы восстановить баланс полезных бактерий в кишечнике, врач может рекомендовать пробиотики.
Но у врачей и учёных нет единого мнения о том, нужно ли принимать пробиотики в процессе лечения антибиотиками. Чтобы сделать однозначное заявление, необходимы дополнительные исследования.
Прогноз бруцеллёза
Бруцеллёз, диагностированный на ранней стадии, хорошо поддаётся лечению антибиотиками — прогноз благоприятный. По мере прогрессирования болезни возможно увеличение продолжительности приёма препаратов, но шанс на выздоровление всё равно большой.
Без лечения заболевание может приводить к массивному разрушению внутренних органов, суставов, костей и центральной нервной системы — развиваются деформации суставов, контрактуры, человеку становится сложно двигаться и брать в руки предметы, истончается кожа, снижается память, формируются глубокие поведенческие и личностные нарушения.
Формируется ли иммунитет после болезни?
У переболевших формируется нестойкий иммунитет, который сохраняется от 6 до 9 месяцев.
Вероятность заболеть повторно высокая.
Профилактика бруцеллёза
Чаще всего бруцеллы передаются человеку от инфицированных сельскохозяйственных животных, поэтому наиболее эффективный способ профилактики — ограничение контакта с ними. Если это невозможно, следует придерживаться правил личной гигиены, чтобы снизить вероятность попадания бактерий на кожу и слизистые оболочки.
Правила личной гигиены для профилактики бруцеллёза:
- мыть руки до и после общения с животными;
- менять и стирать одежду сразу после контакта с животными;
- контактировать с животными и необработанными продуктами животноводства в перчатках, маске, очках и спецодежде.
Если контакта с животными не избежать, нужно использовать защитную спецодежду, перчатки, маску
Кроме того, следует употреблять в пищу только пастеризованные и хорошо термически обработанные продукты: молоко, мясо, яйца.
На фермах, в животноводческих хозяйствах, ветеринарных клиниках, бактериологических лабораториях для профилактики бруцеллёза следует регулярно использовать дезинфицирующие средства. При этом проводят систематическое профилактическое обследование персонала, занятого работой с животными (не реже 1 раза в год).
Владельцы ферм и животноводческих хозяйств в соответствии с Законом Российской Федерации «О ветеринарии» также обязаны регулярно проверять животных на бруцеллёз. Молоко и мясо от инфицированных особей не допускается к реализации.
Существует ли прививка от бруцеллёза
В качестве вспомогательной меры в эндемичных по бруцеллёзу регионах вакцинируют животных, а также работников сельскохозяйственных предприятий и ферм.
Людей, которые не входят в группы риска по развитию бруцеллёза, вакцинировать не рекомендуют.
Источники
- Губанова М. Н., Копченко Т. Г., Резникова О. М. и др. Бруцеллёз: обследование доноров крови Ставропольского края // Трансфузиология, 2017. № 3. С. 37–43.
- Эпидемиологический надзор и лабораторная диагностика бруцеллёза : методические указания / Федеральный центр гигиены и эпидемиологии Роспотребнадзора. М., 2017.
- Tuon F., Gondolfo R., Cerchiari N. Human-to-human transmission of Brucella — a systematic review // Trop Med Int Health, 2017. Vol. 22(5). P. 539–546. doi:10.1111/tmi.12856
- Брико Н. И., Онищенко Г. Г. , Покровский В. И. Руководство по эпидемиологии инфекционных болезней. М., 2019. Т. 1.
Информацию проверил
врач-эксперт
Информацию проверил врач-эксперт
Екатерина Демьяновская
Врач-невролог, кандидат медицинских наук
Оцените статью:
Полезная статья? Поделитесь в социальных сетях:
ВАЖНО
Информация из данного раздела не может служить достаточным основанием для постановки диагноза или назначения лечения. Решение об этом должен принимать врач на основании всех имеющихся у него данных.
Вам может быть интересно
Вам телеграм.
Telegram-канал,
которому, на наш взгляд,
можно доверять
| Бруцеллёз | ||
|---|---|---|
|
|
||
| МКБ-10 | A2323. | |
| МКБ-9 | 023023 | |
| DiseasesDB | 1716 | 1716 |
| MedlinePlus | 000597 | 000597 |
| eMedicine | med/248 | med/248 |
Бруцеллёз (лат. brucellosis) — зоонозная инфекция, передающаяся от больных животных человеку, характеризующаяся множественным поражением органов и систем организма человека. Микробов — виновников этой болезни — впервые в 1886 году обнаружил английский учёный Дэвид Брюс (англ.)русск.. В его честь их и назвали бруцеллами, а вызываемое ими заболевание — бруцеллёзом[1].
Синонимы — мальтийская лихорадка, лихорадка Кипра, лихорадка Гибралтара, волнообразная лихорадка, септицемия Брюса, болезнь Банга.
Содержание
- 1 Причины
- 2 Эпидемиология
- 3 Патогенез
- 4 Патологическая анатомия
- 5 Клиническая картина
- 6 Формы течения
- 7 Диагноз
- 8 Прогноз
- 9 Лечение
- 10 Профилактика
- 11 Примечания
- 12 Литература
- 13 Ссылки
Причины[править | править вики-текст]
Возбудитель заболевания — группа микроорганизмов рода бруцелл. Патогенными для человека являются три: возбудитель бруцеллёза мелкого рогатого скота (Brucella melitensis), возбудитель бруцеллёза крупного рогатого скота (Brucella abortus), возбудитель бруцеллёза свиней (Brucella suis)[2] .
Эпидемиология[править | править вики-текст]
Источником опасных для человека бруцелл являются главным образом козы, овцы (B. melitensis), коровы (B. abortus) и свиньи (B. suis), выделяющие возбудителя с молоком, мочой, околоплодными водами, более того переносчиком бруцеллёза является Жигалка осенняя (Stomaxys calcitrans). Заражение человека происходит при непосредственном контакте с животными-носителями или при употреблении в пищу заражённых продуктов — сырого молока, сыра, изготовленного из непастеризованного молока.
Патогенез[править | править вики-текст]
Ворота — микротравмы кожи, слизистые оболочки органов пищеварения и респираторного тракта. На месте ворот и в лимфатических путях регионарных лимфоузлов изменений нет. Лимфаденопатия при бруцеллёзе является генерализованной, что свидетельствует о гематогенной диссеминации микробов. Размножение и накопление в лимфоузлах — периодически в крови. Выраженная аллергическая перестройка организма, резко выраженая гиперчувствительность замедленного типа сохраняется длительное время после очищения организма от возбудителя. Бруцеллёз отличается склонностью к хроническому течению. Формируется иммунитет, но не длительный (через 3—5 лет возможна реинфекция). На проявления бруцеллёза существенно влияет и вид бруцелл, вызвавших заболевание. Наиболее тяжёлое течение бруцеллёза — мелитенсис, остальные вызывают более лёгкие формы.
Патологическая анатомия[править | править вики-текст]
Возможные источники инфекции
При исследовании под микроскопом поражённых бруцеллёзом органов и тканей видны характерные гранулёмы, весьма похожие на туберкулёзные, редко однако подвергающиеся казеозному некрозу. Исключение составляет инфекция B. suis, при которой часто наблюдаются абсцессы.
Клиническая картина[править | править вики-текст]
Инкубационный период составляет 1—2 недели. Заболевание развивается, как правило, постепенно и не имеет специфических черт. Но больные обычно предъявляют четыре основные жалобы:
- перемежающаяся боль в суставах, преимущественно в нижних конечностях, иногда весьма сильная и мучительная.
- повышение температуры тела в виде длительного субфебрилитета (до 38 °C) или волнообразного типа с резкими подъёмами и падениями.
- усиленная потливость, испарина, иногда ночная потливость.
- резкая слабость и упадок сил.
Системные поражения многообразны и затрагивают практически все органы. Встречаются:
- Опорно-двигательный аппарат
- септический моноартрит, асимметричный полиартрит коленного, тазобедренного, плечевого сакроилиального и грудиноключичного соединений, остеомиелит позвоночника, миалгия.
- Сердце
- эндокардит, миокардит, перикардит, абсцесс корня аорты, тромбофлебит, причём эндокардит может развиться и на неизменённых ранее клапанах.
- Дыхательная система
- бронхит и пневмония.
- Пищеварительная система
- безжелтушный гепатит, анорексия и потеря веса.
- Мочеполовая система
- эпидидимит, орхит, простатит, тубоовариальный абсцесс, сальпингит, цервицит, острый пиелонефрит.
- Центральная нервная система
- менингит, энцефалит, менингоэнцефалит, миелит, церебральные абсцессы, синдром Гийена — Барре, атрофия зрительного нерва, поражение III, IV и VI пар.
- Лимфатические узлы, селезёнка
- лимфаденит, увеличение селезёнки
- Глаза
- кератит, язвы роговицы, увеит, эндофтальмит.
Примерная частота данных анамнеза и некоторых симптомов/жалоб у больных бруцеллёзом (в %)
|
|
Н. И. Рагоза выделяет 4 фазы: фаза компенсированной инфекции (первично-латентная), фазу острого сепсиса без местных поражений (декомпенсация), фазу подострого или хронического рецидивирующего заболевания с образованием местных поражений (декомпенсация или субкомпенсация) и фазу восстановления компенсации с остаточными явлениями или без них.
Клинические формы бруцеллёза: 1) форма первично-латентная; 2) форма остросептическая; 3) форма первично-хроническая метастатическая; 4) форма вторично-хроническая метастатическая; 5) форма вторично-латентная.
Первично-латентная состояние практического здоровья. При ослаблении защитных сил она может превратиться или в остросептическую, или в первично-хроническую метастатическую форму. Иногда микросимптомы: небольшого увеличения периферических лимфатических узлов, иногда повышается температура тела до субфебрильной, повышенная потливость при физическом напряжении. Они считают себя здоровыми и сохраняют работоспособность.
Остросептическая форма лихорадкой (39—40 °С), температурная кривая волнообразная, неправильного (септического) типа с большими суточными размахами, повторными ознобами и потами. Самочувствие остается хорошим (при температуре 39 °C и выше может читать книги, играть в шахматы, смотреть телевизор). Отсутствуют и другие признаки общей интоксикации. Не угрожает жизни больного, даже без этиотропного лечения она заканчивается выздоровлением. Все группы лимфоузлов умеренно увеличены, некоторые чувствительны. К концу первой недели — увеличение печени и селезёнки. При исследовании крови лейкопения, СОЭ не повышена. Главным отличием является отсутствие очаговых изменений (метастазов). Без антибиотикотерапии длительность лихорадки 3—4 недели и более.
Хронические формы иногда развиваются сразу, минуя острую, иногда спустя время после остросептической формы. По клинике первично-хроническая метастатическая и вторично-хроническая метастатическая формы не различаются. Отличие — наличие или отсутствие остросептической формы в анамнезе. Клиника: длительную субфебрильную температуру, слабость, повышенную раздражительность, плохой сон, нарушение аппетита, снижение работоспособности. Генерализованная лимфаденопатия мягкие, чувствительные или болезненные при пальпации, отмечаются мелкие очень плотные безболезненные склерозированные лимфоузлы (0,5—0,7 см в диаметре). Увеличение печени и селезенки. На этом фоне выявляются органные поражения, наиболее часто со стороны опорно-двигательного аппарата, затем идут нервная и половая системы. Боли в мышцах и суставах, преимущественно в крупных, полиартрит, при новом обострении появляются другие по локализации метастазы. Периартрит, параартрит, бурситы, экзостозы, не отмечается остеопорозов. Суставы опухают, подвижность в них ограничена, кожа над ними нормальной окраски. Нарушение подвижности и деформация обусловлены разрастанием костной ткани. Поражается позвоночник, чаще в поясничном отделе. Типичны сакроилеиты (симптом Эриксена: на стол на спину или на бок и производят давление на гребень верхней подвздошной кости при положении на боку или сдавливают обеими руками передние верхние гребни подвздошных костей в положении на спине. При одностороннем сакроилеите боли на пораженной стороне, при двухстороннем — боли в крестце с двух сторон). Симптом Нахласа, укладывают на стол лицом вниз и сгибают ноги в коленных суставах. При подъёме конечности боль в поражённом крестцово-подвздошном сочленении. Симптом Ларрея на стол на спине, врач берётся обеими руками за выступы крыльев подвздошных костей и растягивает их в стороны, при этом появляется боль в поражённой стороне (при одностороннем сакроилеите). Симптом Джона—Бера: больной в положении на спине, при давлении на лонное сочленение перпендикулярно вниз боль в крестцово-подвздошном сочленении.
Миозиты боли в поражённых мышцах. Боли тупые, продолжительные, интенсивность их связана с изменениями погоды. При пальпации определяются более болезненные участки, а в толще мышц прощупываются болезненные уплотнения различной формы и размеров. Фиброзиты (целлюлиты) в подкожной клетчатке на голенях, предплечьях, спине и пояснице. Размеры от 5—10 мм до 3—4 см мягкие овальные образования, болезненные или чувствительные. В дальнейшем они уменьшаются, могут полностью рассосаться или склерозируются и остаются на длительное время в виде небольших плотных образований, безболезненных.
Поражение нервной системы: невриты, полиневриты, радикулиты. Поражение центральной нервной системы (миелиты, менингиты, энцефалиты, менингоэнцефалиты) редко, протекают длительно и тяжело.
Изменения половой системы у мужчин — орхитах, эпидидимитах, снижении половой функции. У женщин сальпингиты, метриты, эндометриты. Возникает аменорея, может развиться бесплодие. У беременных женщин часто возникают аборты, мертворождения, преждевременные роды, врождённый бруцеллёз у детей.
Вторично-хроническая форма протекает так же. Вторично-латентная форма отличается от первично-латентной тем, что она чаще переходит в манифестные формы (рецидивирует).
Формы течения[править | править вики-текст]
- Острая — длительностью до 1,5 месяцев;
- подострая — длительностью 1,5–3 месяцев;
- хроническая — более 3 месяцев.
Диагноз[править | править вики-текст]
- Данные анамнеза: контакт с животными, употребление в пищу термически необработанных продуктов животноводства, специальность больного, эндемические очаги.
- Клиническая картина.
- Лабораторный диагноз:
- Посев крови на питательные среды положителен в 50—70 % случаев у больных бруцеллёзом:
- реакция Райта — положительна на 10-й день;
- реакция Кумбса — диагноз хронического бруцеллёза;
- 2-меркаптоэтанол-аглютинитовый тест;
- реакция Хеддлсона;
- кожная проба Бюрне;
- выявление ДНК Brucella spp. методами амплификации нуклеиновых кислот (ПЦР).
Прогноз[править | править вики-текст]
Бруцеллёз редко становится причиной смерти. Даже до появления антибиотиков смертность при нём не превышала 2 % и была в основном обусловлена эндокардитом. Однако бруцеллёз нередко заканчивается инвалидностью. Тяжесть остаточных дефектов зависит от вида возбудителя. Самые тяжёлые последствия оставляет бруцеллёз, вызванный Brucella melitensis. Одна из причин инвалидности — неврологические расстройства, в том числе поражение спинного мозга и параплегия. Описана нейросенсорная тугоухость как осложнение менингоэнцефалита и лечения стрептомицином.
Лечение[править | править вики-текст]
Антибиотикотерапия: два, три препарата из следующих: тетрациклин, стрептомицин, доксициклин, рифампицин, гентамицин — только при остром бруцеллёзе, в сочетании с препаратами, проникающими внутриклеточно, бисептол, нетилмицин. Наиболее эффективны в лечении бруцеллёза у людей фторхинолоны (ципрофлоксацин, норфлоксацин, офлоксацин), самый эффективный из них — флероксацин.
Возможные схемы:
- Доксициклин + стрептомицин или гентамицин
- Доксициклин + нетилмицин (некоторыми авторами упоминается как самая результативная схема)
- Доксициклин + рифампицин
- Фторхинолоны + Доксициклин, или нетилмицин, или рифампицин
- Фторхинолоны в монотерапии
- Триметoприм/Сульфаметоксазол (бисептол) + рифампицин
Бруцеллёз переходит в хроническую форму в 37–80 % случаев, особенно при несвоевременном или неадекватном лечении.
Профилактика[править | править вики-текст]
- Пастеризация или кипячение молока
- Санитарно-гигиеническое просвещение населения работающего с животными или их продуктами
- Профилактические прививки у лиц высокой группы риска (короткий период действия — около 2 лет)
- Массовые профилактические прививки животных не дали ожидаемого результата
Примечания[править | править вики-текст]
- ↑ По материалу Панацея.ру — Бруцеллез
- ↑ Л.Б.Борисов. Медицинская микробиология, вирусология и иммунология. — МИА, 2005. — С. 423. — ISBN 5-89481-278-X.
Литература[править | править вики-текст]
- Harrison’s Principles of Internal Medicine, 14th Edition, McGraw-Hill, Health Professions Division
- ΕΣΩΤΕΡΙΚΗ ΠΑΘΟΛΟΓΙΑ ΑΠΘ, ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ-ΤΟΜΕΑΣ ΠΑΘΟΛΟΓΙΑΣ, ΔΙΕΥ/ΤΗΣ: ΚΑΘΗΓΗΤΗΣ Μ.ΠΑΠΑΔΗΜΗΤΡΙΟΥ
- Справочник по инфекционным болезням, проф. Л. А. Тришкова, доц. С. А. Богатырёва
- Справочник по дифференциальной диагностике инфекционных болезней. Под редакцией профессора А. Ф. Фролова, профессора Б. Л. Угрюмова, д-ра мед. наук Е. К. Тринус. Киев
Ссылки[править | править вики-текст]
- http://www.cbwinfo.com/Biological/Pathogens/BM.html
- http://www.aphis.usda.gov/vs/nahps/brucellosis/
- http://www.cdc.gov/ncidod/dbmd/diseaseinfo/brucellosis_g.htm
- http://www.hpa.org.uk/infections/topics_az/zoonoses/brucellosis/gen_info.htm
- http://www.emedicine.com/emerg/topic883.htm
- http://www.wrongdiagnosis.com/b/brucellosis/intro.htm
- College of Veterinary Medicine. The University of Georgia
- Department of Health
- Бруцеллез
- Международное рабочее совещание в НИЦ ТБП (Серпуховский район)
- Бруцеллез . Санитарные правила СП 3.1.085-96 Ветеринарные правила ВП 13.3.1302-96
- Всероссийский научно-исследовательский институт бруцеллёза и туберкулёза животных Российской академии сельскохозяйственных наук
|
|
|
|---|---|
| Современные акты биотеррора | Биотеррористическая атака в Орегоне • Атака средиземноморской плодовой мухи на Калифорнию • Письма со спорами сибирской язвы • Рицин в лондонском метро • Письма с рицином (2003) • Письма с рицином (2013) |
| Противодействие биотерроризму | Австралийская группа • Центр биобезопасности • Центры по контролю и профилактике заболеваний США • Конвенция Совета Европы о предупреждении терроризма • DARPA • Агентство по сокращению военной угрозы • Европейский Центр профилактики и контроля заболеваний • Глобальная инициатива по безопасности здоровья • Health Threat Unit (European Commission) • Лабораторная сеть быстрого реагирования • Центр национальной биозащиты, анализа и контрмер • Национальный научный консультативный совет по биобезопасности • Институт медицинских исследований инфекционных болезней армии США |
| Биологические агенты (переносчики) | Сибирская язва • Птичий грипп • Ботулотоксин • Бруцеллёз • Burkholderia pseudomallei • Chlamydophila psittaci • Coxiella burnetii • Геморрагическая лихорадка Эбола • Венесуэльский лошадиный энцефалит • Восточный лошадиный энцефалит • Западный лошадиный энцефалит • Пищевое отравление • Грибы • Сап • Хантавирусы • Henipavirus • Легионеллёз • Вирус Марбург • Плесневые грибы • Бубонная чума • Рицин • Salmonella enterica (кишечная сальмонелла) • Сальмонеллёзы • Брюшной тиф • Натуральная оспа • Стафилококк • Туляремия • Сыпной тиф • Геморрагическая лихорадка |
| Связанные темы | Агротерроризм • Бактерии • Биологическая безопасность • Биологическая опасность • Биологическое оружие • Дезактивация • Энтомологическое оружие • Инфекционные заболевания • Вирусы • Токсин • Терроризм |
Бруцеллез: причины появления, симптомы, диагностика и способы лечения.
Определение
Бруцеллез — инфекционное заболевание, которое вызывают бактерии рода Brucella.
Эти бактерии обладают высокой устойчивостью в окружающей среде и способны длительно сохранять жизнеспособность.
На территории России заболевание встречается в южных регионах, где развито фермерское животноводство. Профессии, связанные с повышенным риском заражения бруцеллезом, – пастухи, доярки, ветеринарные и зоотехнические работники, сотрудники бактериологических лабораторий, рабочие мясокомбинатов, боен и фабрик, занятых переработкой шерсти животных.
Причины появления бруцеллеза
Бруцелла передается людям от больных животных, преимущественно коз и овец.
Передача бруцелл происходит через продукты питания (термически необработанное молоко и молочные продукты, мясо), непосредственно при контакте с больными животными, а также при вдыхании бруцелл, содержащихся в пыли в местах обитания больных животных и во время разделки их туш.
Бруцелла может проникать через плаценту, приводя к внутриутробному заражению плода, а также выделяться с грудным молоком.
Иными способами передача бруцелл от человека человеку невозможна.
После попадания в организм человека бруцелла интенсивно размножается в лимфоидной ткани.
Бруцеллы могут длительно и незаметно для человека сохраняться в организме, обуславливая хроническое течение инфекции.
Классификация заболевания
Бруцеллез может развиваться в результате инфицирования различными видами бруцелл, например Вruсеllа melitensis, Вruсеllа abortus, Имеются определенные особенности течения бруцеллеза, вызванного различными видами возбудителя, однако эти отличия касаются преимущественно эпидемиологических аспектов.
В зависимости от длительности течения заболевания бруцеллез бывает острым, подострым и хроническим. Отдельно выделяют резидуальные (остаточные) изменения, сохраняющиеся после излечения от инфекции и освобождения организма от возбудителя.
Симптомы бруцеллеза
Первые симптомы болезни появляются, как правило, спустя 1–6 недель после заражения.
Чаще бруцеллез начинается подостро — возникают неспецифические симптомы, такие как слабость, недомогание, головная, суставная и мышечная боли.
Повышение температуры в подостром периоде незначительное с последующим подъемом до более высоких значений. Лихорадка часто имеет волнообразное течение. В редких случаях наблюдается увеличение лимфатических узлов, обнаруживаются болезненные подкожные узелки.
Для бруцеллеза характерны аллергические проявления на коже (диффузное покраснение, высыпания и т.д.).
Со стороны сердечно-сосудистой системы отмечается снижение артериального давления, учащение пульса, возможно развитие воспалительных процессов в сердце. Также может возникнуть поражение дыхательной системы (бронхиты, пневмонии и т.д.).
Для хронического бруцеллеза характерно поражение опорно-двигательного аппарата, выражающееся суставными и мышечными болями, ограничением подвижности суставов.
Поражения нервной системы проявляются жжением и покалыванием по ходу нервных волокон.
Диагностика бруцеллеза
Диагностика бруцеллеза складывается из тщательного сбора анамнеза и объективного исследования больного.
К лабораторным методам, используемым при диагностике бруцеллеза, относится клинический анализ крови с определением лейкоцитарной формулы, в котором можно обнаружить признаки воспалительного процесса в организме. Однако данный метод не обеспечивает идентификации возбудителя. С этой целью применяются бактериологический, серологический и молекулярно-генетический методы.
Для бактериологического анализа, цель которого – выявление непосредственного возбудителя, проводят забор крови, мочи, мокроты и других биологических материалов в зависимости от пораженных органов. Производят посев на питательные среды с дальнейшим микроскопическим и иным исследованием полученных культур. Данный метод является золотым стандартом диагностики бруцеллеза. Однако такое исследование, как правило, занимает несколько дней.
Серологический метод основан на выявлении специфических антител классов IgM , IgА и IgG к бруцеллам. Эти белки появляются в организме в ответ на инфицирование бруцеллами и отражают наличие иммунного ответа.
Бруцелла-IgM (Brucella, IgM)
Серологический показатель ранних стадий бруцеллёза.
Бруцеллез (лат. Brucellosis) – бактериальная инфекционно-аллергическая болезнь, относящаяся к группе �…
Бруцелла-IgG (Brucella, IgG)
Специфические антитела к возбудителю бруцеллёза, свидетельствующие о текущей или перенесённой в прошлом инфекции.
Бруцеллез (лат. Brucellosis) – бактериал�…
Высокой специфичностью и чувствительностью обладает метод ПЦР, цель которого – обнаружение генетического материала (ДНК) бруцеллы. Данный метод способен выявлять микроорганизм, содержащийся в самых минимальных количествах в исследуемых средах.
Используемые ранее аллергические пробы для выявления бруцеллеза сейчас имеют весьма ограниченное применение.
С целью выявления поражения различных органов и систем может потребоваться биохимический анализ крови с показателями функции печени (общий белок, альбумины, аланинаминотрансфераза (АлАТ), аспартатаминотрансфераза (АсАТ), билирубин и его фракции), почек (мочевина, креатинин с подсчетом скорости клубочковой фильтрации).
Общий белок (в крови) (Protein total)
Синонимы: Общий белок сыворотки крови; Общий сывороточный белок.
Total Protein; Serum Тotal Protein; Total Serum Protein; TProt; ТР.
Краткая характеристика определяемого вещества Общий бе�…
Альбумин (в крови) (Albumin)
Синонимы: Человеческий сывороточный альбумин; ЧСА; Альбумин плазмы;
Human Serum Albumin; ALB.
Краткая характеристика исследуемого вещества Альбумин
Альбумин – эт…
Билирубин общий (Bilirubin total)
Синонимы: Общий билирубин крови; Общий билирубин сыворотки.
Totalbilirubin; TBIL.
Краткая характеристика определяемого вещества Билирубин общий
Билирубин – это пигм…
Мочевина (в крови) (Urea)
Синонимы: Диамид угольной кислоты; Карбамид; Мочевина в крови; Азот мочевины.
Urea nitrogen; Urea; Blood Urea Nitrogen (BUN); Urea; Plasma Urea.
Краткая характеристика аналита Мочевина
Моче�…
Инструментальные исследования включают электрокардиографию, эхокардиографию, рентгенографию органов грудной клетки, суставов и позвоночника, ультразвуковое исследование органов брюшной полости и др.
ЭКГ за 5 минут
Исследование функциональных возможностей сердца – быстро, безболезненно и информативно.
Эхокардиография
Исследование, позволяющее оценить функциональные и органические изменения сердца, его сократимость, а также состояние клапанного аппарата.
Рентген тазобедренного сустава
Рентгенологическое исследование тазобедренного сустава и окружающих тканей для оценки патологических изменений и травматических повреждений.
К каким врачам обращаться
Первичная диагностика бруцеллеза требует исключения ряда заболеваний неинфекционного происхождения. Поэтому первым врачом, к которому обращаются при появлении симптомов, характерных для бруцеллеза, является терапевт или педиатр. На основании жалоб, истории заболевания, выяснения деталей эпидемиологического риска заражения у конкретного больного, данных клинического и лабораторного исследований устанавливается диагноз. Далее пациента консультирует врач-инфекционист и другие специалисты (в зависимости от наличия поражений тех или иных органов): кардиолог, хирург, репродуктолог и т.д.
Лечение бруцеллеза
Лечение бруцеллеза основано, в первую очередь, на освобождении организма от возбудителя. С этой целью используются антибактериальные препараты, активные в отношении бруцелл.
Своевременная диагностика и назначение соответствующей противомикробной терапии предотвращают хронизацию процесса и развитие инвалидизирующих осложнений (например, серьезных нарушений в работе опорно-двигательного аппарата).
Кроме того, проводится терапия, направленная на купирование тех или иных синдромов. В перечень применяемых препаратов входят иммунокорректоры, противовоспалительные средства, витамины, нейропротекторы и др.
Комплексная терапия проводится только под наблюдением врачей и включает контроль состояния пациента при помощи лабораторно-инструментальных методов.
Осложнения
Осложнения бруцеллеза могут касаться самых различных органов. Так, со стороны сердца могут развиваться блокады проведения импульса, аритмии, поражения клапанов, сердечная недостаточность.
Хроническое течение бруцеллеза нередко приводит к формированию контрактур (стойкому ограничению подвижности суставов за счет изменения его структур), дистрофии мышц. Это значительно ограничивает движения в крупных суставах (например, крестцово-подвздошном сочленении — сакроилеиту), реже поражаются мелкие суставы.
Одним из тяжелых осложнений является бесплодие. Оно может развиться в результате поражения бруцеллезом половых органов у лиц как мужского, так и женского пола.
Среди острых осложнений бруцеллеза стоит отметить менингит – воспаление мозговых оболочек, энцефалит – воспаление мозгового вещества. Данные состояния представляют угрозу жизни пациента. Хронический нейробруцеллез может привести к развитию параличей, стойким изменениям психики и другим тяжелым последствиям.
Профилактика бруцеллеза
Профилактика бруцеллеза подразделяется на специфическую и неспецифическую.
К специфической профилактике относится вакцинация, которая осуществляется по эпидемиологическим показаниям лицам, чья профессиональная деятельность связана с высоким риском заражения.
Кроме того, представители этих профессий подлежат регулярному лабораторному обследованию в рамках диспансеризации.
Неспецифическая профилактика включает использование средств защиты и соблюдение правил техники безопасности при работе со скотом, тщательную термическую обработку продуктов животного происхождения, вынужденный забой скота при наличии признаков заражения бруцеллезом или подозрении на возможное заражение.
Источники
- Клинические рекомендации «Бруцеллез у взрослых». Разраб.:Национальное научное общество инфекционистов (НОИ). – 2019.
- Инфекционные болезни у детей, учебник // В.Ф. Учайкин, О.В. Шамшева. – М. ГОЭТАР-Медиа. 2018. 800 с.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы — 19 лет
Поделитесь этой статьей сейчас
Рекомендации
-
13060
01 Марта
-
13059
23 Февраля
-
4419
21 Февраля
Похожие статьи
Энтеробиоз
Энтеробиоз: причины появления, симптомы, диагностика и способы лечения.
Чесотка
Чесотка: причины появления, симптомы, диагностика и способы лечения.
Туннельные синдромы
Туннельные синдромы: причины появления, симптомы, диагностика и способы лечения.
Ларингит
Ларингит – это воспаление слизистой оболочки гортани. В большинстве случаев причиной возникновения ларингита являются различные респираторные вирусы. Заболеванию подвержены люди любого возраста, особенно дети от полугода до двух лет и взрослые от 18 до 40 лет.
Кератит
Кератит: причины появления, симптомы, диагностика и способы лечения.