1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
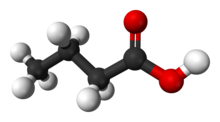
Бутановая кислота
Полезное
Смотреть что такое «Бутановая кислота» в других словарях:
-
Изобутановая кислота — н бутановая кислота изобутановая кислота Масляная кислота (бутановая кислота) С3Н7СООН – бесцветная жидкость с запахом прогорклого масла. Соли и эфиры масляной кислоты называются бутиратами. Масляная кислота и её эфиры содержатся в коровьем масле … Википедия
-
Жирная кислота — Жирные кислоты (алифатические кислоты) многочисленная группа исключительно неразветвлённых одноосновных карбоновых кислот с открытой цепью. Название определяется, во первых, химическими свойствами данной группы веществ основанными на присутствии… … Википедия
-
МАСЛЯНАЯ КИСЛОТА — (бутановая к та, этилуксусная к та) СН 3 СН 2 СН 2 СООН. В статье рассмотрена также изомасляная к та (2 метилпропановая к та, диметилуксусная к та) (СН 3)2 СНСООН (И. к.). Мол. м. 88,11; бесцв. жидкости, М. к. с запахом прогорклого масла. Для М.… … Химическая энциклопедия
-
Одноосновные предельные карбоновые кислоты — (одноосновные насыщенные карбоновые кислоты) карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH Номенклатура Систематические названия… … Википедия
-
Насыщенные монокарбоновые кислоты — Одноосновные предельные карбоновые кислоты (одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH, где n … Википедия
-
Одноосновные насыщенные карбоновые кислоты — Одноосновные предельные карбоновые кислоты (одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH, где n … Википедия
-
Предельные монокарбоновые кислоты — Одноосновные предельные карбоновые кислоты (одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH, где n … Википедия
-
Жирные кислоты — алифатические одноосновные карбоновые кислоты с открытой цепью, содержащиеся в этерифицированной форме в жирах, маслах и восках растительного и животного происхождения. Жирные кислоты, как правило, содержат неразветвленную цепь из четного числа… … Википедия
-
Кислоты и ангидриды — КИСЛОТЫ И АНГИДРИДЫ. Кислоты класс химических соединений характеризующихся диссоциацией в водном растворе с образованием гидратированных ионов H+. Ангидриды химические соединения, производные органических и неорганических кислот, образующиеся при … Российская энциклопедия по охране труда
-
Карбоновые кислоты — Карбоновые кислоты класс органических соединений, молекулы которых содержат одну или несколько функциональных карбоксильных групп COOH. Кислые свойства объясняются тем, что да … Википедия
бутановая кислота
Изомеры
Гомологи
Вид структурной изомерии
Все
Межклассовая
карбоновая кислота
|
||
 |
||
| Названия | ||
|---|---|---|
| Предпочтительное название IUPAC Бутановая кислота | ||
| Другие названия Этилуксусная кислота. 1-пропанкарбоновая кислота. Пропилформиновая кислота. C4: 0 (Липидные числа ) | ||
| Идентификаторы | ||
| Номер CAS |
|
|
| 3D модель (JSmol ) |
|
|
| ChEBI |
|
|
| ChEMBL |
|
|
| ChemSpider |
|
|
| DrugBank |
|
|
| ECHA InfoCard | 100.003.212 |
|
| Номер EC |
|
|
| IUPHAR / BPS |
|
|
| KEGG |
|
|
| MeSH | Butyric + acid | |
| PubChem CID |
|
|
| Номер RTECS |
|
|
| UNII |
|
|
| Номер ООН | 2820 | |
| CompTox Dashboard (EPA ) |
|
|
InChI
|
||
УЛЫБАЕТСЯ
|
||
| Свойства | ||
| Химическая формула | C. 3H. 7COOH | |
| Молярная масса | 88,106 г · моль | |
| Внешний вид | Бесцветная жидкость | |
| Запах | Неприятный, похожий на запах рвоты или тела | |
| Плотность | 1,135 г / см (-43 ° C). 0,9528 г / см (25 ° C) | |
| Точка плавления | -5,1 ° С (22,8 ° F; 268,0 K) | |
| Температура кипения | 163,75 ° C (326,75 ° F; 436,90 K) | |
| Условия сублимации. | Сублимирует при -35 ° C. Δ subl H = 76 кДж / моль | |
| Растворимость в воде | Смешивается | |
| Растворимость | Слабо растворим в CCl 4 Смешивается с этанолом, эфиром | |
| log P | 0,79 | |
| Давление пара | 0,112 кПа (20 ° C). 0,74 кПа (50 ° C). 9,62 кПа (100 ° C) | |
| закон Генри. константа (kH) | 5,35 · 10 л · атм / моль | |
| Кислотность (pK a) | 4,82 | |
| Магнитная восприимчивость (χ) | -55,10 · 10 см / моль | |
| Теплопроводность | 1,46 · 10 Вт / м · K | |
| Показатель преломления (nD) | 1,398 (20 ° C) | |
| Вязкость | 1,814 c P (15 ° C). 1,426 сП (25 ° C) | |
| Структура | ||
| Кристаллическая структура | Моноклинная (-43 ° C) | |
| Пространственная группа | C2 / m | |
| Постоянная решетки | a = 8.01 Å, b = 6,82 Å, c = 10,14 Å α = 90 °, β = 111,45 °, γ = 90 ° | |
| Дипольный момент | 0,93 D (20 ° C) | |
| Термохимия | ||
| Теплоемкость (C) | 178,6 Дж / моль · K | |
| Стандартная молярная. энтропия (S 298) | 222,2 Дж / моль · K | |
| Стандартная энтальпия образования. (ΔfH298) | −533,9 кДж / моль | |
| Стандартная энтальпия. горения (ΔcH298) | 2183,5 кДж / моль | |
| Опасности | ||
| Паспорт безопасности | Внешний паспорт безопасности материала | |
| Пиктограммы GHS |  |
|
| Сигнальное слово GHS | Опасно | |
| Указания об опасности GHS | H314 | |
| Меры предосторожности GHS | P280, P305 + 351 + 338, P310 | |
| NFPA 704 (огненный алмаз) |  2 3 0 2 3 0 |
|
| Температура вспышки | от 71 до 72 ° C (От 160 до 162 ° F; От 344 до 345 K) | |
| Самовоспламенение. температура | 440 ° C (824 ° F; 713 K) | |
| Пределы взрываемости | 2,2–13,4% | |
| Смертельная доза или концентрация (LD, LC): | ||
| LD50(средняя доза ) | 2000 мг / кг (перорально, крыса) | |
| Родственные соединения | ||
| Другие анионы | Бутират | |
| Родственные Карбоновые кислоты | Пропионовая кислота, Пентановая кислота | |
| Родственные соединения | 1-Бутанол. Бутиральдегид. Метилбутират | |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | ||
| Ссылки в ink | ||
Масляная кислота (из Древнегреческий : βούτῡρον, что означает «масло»), также известный под систематическим названием бутановая кислота, представляет собой карбоновую кислоту со структурной формулой CH 3CH2CH2CO2H. Это маслянистая бесцветная жидкость, растворимая в воде, этаноле и эфире. Изомасляная кислота (2-метилпропановая кислота) представляет собой изомер. Соли и сложные эфиры масляной кислоты известны как бутираты или бутаноаты. Кислота не встречается в природе, но ее сложные эфиры широко распространены. Это обычный промышленный химикат.
Содержание
- 1 Возникновение
- 2 Приготовление и выделение
- 3 История
- 4 Использование
- 5 Биохимия
- 5.1 Микробный биосинтез
- 5.2 Ферментируемое волокно источники
- 6 Фармакология
- 6.1 Фармакодинамика
- 6.2 Фармакокинетика
- 6.2.1 Метаболизм
- 7 Исследования
- 7.1 Периферические эффекты
- 7.1.1 Иммуномодуляция и воспаление
- 7.1.2 Рак
- 7.2 Зависимость
- 7.1 Периферические эффекты
- 8 См. Также
- 9 Примечания
- 10 Ссылки
- 11 Внешние ссылки
Возникновение
Триглицериды масляной кислоты составляют 3–4% масла. Когда масло становится прогорклым, масляная кислота высвобождается из глицерида в результате гидролиза. Это одна из подгруппы жирных кислот, которая называется короткоцепочечные жирные кислоты. Масляная кислота — это кислота средней силы, которая реагирует с основаниями и влияет на многие металлы. Масляная кислота содержится в животном жире и растительных маслах, коровьем молоке, грудном молоке, сливочное масло, сыр пармезан и как продукт анаэробной ферментации (в том числе в толстой кишке и как запах тела, и рвота ). Масляная кислота имеет вкус, чем-то напоминающий масло, и неприятный запах. Млекопитающие с хорошей способностью обнаруживать запах, такие как собаки, могут обнаруживать его с концентрацией 10 частей на миллиард, тогда как люди могут обнаруживать его только в концентрациях выше 10 частей на миллион. В производстве пищевых продуктов он используется в качестве ароматизатора.
У людей масляная кислота является одним из двух основных эндогенных агонистов человеческого рецептора 2 гидроксикарбоновой кислоты. (HCA 2), Gi/o-связанный рецептор, связанный с белком G.
Масляная кислота или масляная кислота ферментации также присутствует в виде сложного эфира октилбутирата в пастернаке (Pastinaca sativa) и в семенах дерева гинкго.
Получение и выделение
Масляная кислота получают промышленным способом путем окисления бутиральдегид.
Его можно отделить от водных растворов путем насыщения солями, такими как хлорид кальция. Кальциевая соль Ca (C 4H7O2)2·H2O менее растворима в горячей воде, чем в холодной.
История
Масляная кислота была впервые обнаружена в нечистой форме в 1814 году французским химиком Мишель Эжен Шеврёль. К 1818 году он очистил его в достаточной степени, чтобы охарактеризовать его. Однако Шеврёль не публиковал свои ранние исследования масляной кислоты; вместо этого он сдал свои результаты в виде рукописи секретарю Академия наук в Париже, Франция. Анри Браконно, французский химик, также исследовал состав масла и публиковал свои открытия, что привело к спорам о приоритете. Еще в 1815 году Шеврёль утверждал, что обнаружил вещество, вызывающее запах масла. К 1817 году он опубликовал некоторые из своих открытий относительно свойств масляной кислоты и назвал их. Однако только в 1823 году он представил свойства масляной кислоты. в деталях.Название масляной кислоты происходит от латинского слова, обозначающего масло, butyrum (или buturum), вещество, в котором впервые была обнаружена масляная кислота.
Использование
Масляная кислота используется для получения различных сложных эфиров бутирата. Он используется для производства бутирата ацетата целлюлозы (CAB), который используется в широком спектре инструментов, деталей и покрытий и более устойчив к разрушению, чем ацетат целлюлозы. Однако CAB может разлагаться под воздействием тепла и влаги, выделяя масляную кислоту.
Низкомолекулярные сложные эфиры масляной кислоты, такие как метилбутират, в основном имеют приятный аромат или вкус. Как следствие, они используются как пищевые и парфюмерные добавки. Это одобренный в ЕС пищевой ароматизатор (номер 08.005).
Из-за сильного запаха его также использовали в качестве добавки к рыболовной наживке. Многие коммерчески доступные ароматизаторы, используемые в приманках для карпа (Cyprinus carpio), используют масляную кислоту в качестве сложноэфирной основы; однако неясно, привлекает ли рыбу сама масляная кислота или добавленные к ней вещества. Однако масляная кислота была одной из немногих органических кислот, которые оказались вкусными как для линя, так и для горчинки. Вещество также использовалось вонючей бомбой Обществом охраны морских пастухов для уничтожения японских китобойных экипажей.
Биохимия
Микробный биосинтез
продуцируется несколькими процессами ферментации, выполняемыми облигатными анаэробными бактериями. Этот путь ферментации был открыт Луи Пастером в 1861 году. Примеры продуцирующих бутират видов бактерий:
- Clostridium butyricum
- Clostridium kluyveri
- Clostridium pasteurianum
- Faecalibacterium prausnitzii
- Fusobacterium nucleatum
- Butyrivibrio fibrisolvens
- Eubacterium limosum
Путь начинается с гликолитического расщепления глюкозы на две молекулы из пирувата, как это происходит у большинства организмов. Пируват окисляется в ацетилкофермент A, катализируемый пируватом: ферредоксин оксидоредуктазой. Две молекулы диоксида углерода (CO 2) и две молекулы элементарного водорода (H2) образуются как отходы. Впоследствии, как можно видеть, на последней стадии ферментации вырабатывается АТФ. На каждую молекулу глюкозы вырабатываются три молекулы АТФ, что дает относительно высокий выход. Сбалансированное уравнение для этой ферментации:
- C6H12O6→ C 4H8O2+ 2 CO 2 + 2 H 2
Другие пути бутирата включают восстановление сукцината и диспропорционирование кротоната.
| Действие | Ответственный фермент |
|---|---|
| Ацетилкофермент A превращается в ацетоацетилкофермент A | ацетил-CoA-ацетилтрансфераза |
| Ацетоацетилкофермент A превращается в β-гидроксибутирил CoA | β-гидроксибутирил-КоА дегидрогеназа |
| β-гидроксибутирил-КоА превращается в кротонил-КоА | кротоназу |
| Кротонил-КоА превращается в бутирил-КоА (CH 3CH2CH2C = O -CoA) | бутирил-КоА-дегидрогеназа |
| A фосфатная группа заменяет CoA с образованием бутирилфосфата | |
| Фосфатная группа присоединяется к ADP с образованием ATP и бутират | бутираткиназа |
Некоторые виды образуют ацетон и н-бутанол альтернативным путем, который начинается с ферментации бутирата. Некоторые из этих видов:
- Clostridium acetobutylicum, наиболее известный продуцент ацетона и пропианола, используемый также в промышленности
- Clostridium beijerinckii
Эти бактерии начинают ферментацию бутирата, как описано выше, но когда pH падает ниже 5, они переключаются на производство бутанола и ацетона, чтобы предотвратить дальнейшее снижение pH. На каждую молекулу ацетона образуется две молекулы бутанола.
Изменение пути происходит после образования ацетоацетил-КоА. Затем это промежуточное соединение принимает два возможных пути:
- ацетоацетил-КоА → ацетоацетат → ацетон
- ацетоацетил-КоА → бутирил-КоА → бутиральдегид → бутанол
Источники ферментируемого волокна
Остатки волокон с высокой степенью ферментации, такие как остатки резистентного крахмала, овсяных отрубей, пектина и гуара, трансформируются посредством бактерии толстой кишки в короткоцепочечные жирные кислоты (SCFA), включая бутират, производя больше SCFA, чем менее ферментируемые волокна, такие как целлюлозы. Одно исследование показало, что устойчивый крахмал постоянно производит больше бутирата, чем другие типы пищевых волокон. Производство SCFA из волокон жвачных животных, таких как крупный рогатый скот, отвечает за содержание бутирата в молоке и масле.
Фруктаны являются еще одним источником пребиотических растворимых пищевых волокон, которые можно переваривать для получения бутират. Они часто встречаются в растворимых волокнах пищевых продуктов с высоким содержанием серы, таких как лук и овощи семейства крестоцветных. Источники фруктанов включают пшеницу (хотя некоторые сорта пшеницы, такие как полба, содержат меньшие количества), рожь, ячмень, лук, чеснок, иерусалим и артишок, спаржа, свекла, цикорий, листья одуванчика, лук-порей, радиккио, белая часть зеленого лука, брокколи, брюссельская капуста, капуста, фенхель и пребиотики, например фруктоолигосахариды (FOS ), олигофруктоза и инулин.
Фармакология
| Ингибированный фермент | IC50 (nM) | Вводная запись |
|---|---|---|
| HDAC1 | 16000 | |
| HDAC2 | 12,000 | |
| HDAC3 | 9,000 | |
| HDAC4 | 2,000,000 | Нижняя граница |
| HDAC5 | 2,000,000 | Нижняя граница |
| HDAC6 | 2,000,000 | Нижняя граница |
| HDAC7 | 2,000,000 | Нижняя граница |
| HDAC8 | 15000 | |
| HDAC9 | 2,000,000 | Нижняя граница |
| CA1 | 511, 000 | |
| CA2 | 1,032,000 | |
| GPCR target | pEC 50 | Примечания к записи |
| FFAR2 | 2.9–4.6 | Полный агонист |
| FFAR3 | 3,8–4,9 | Полный агонист |
| HCA2 | 2,8 | Агонист |
Фармакодинамика
Масляная кислота является одним из двух основных эндогенных агонистов человеческого рецептора 2 гидроксикарбоновой кислоты (HCA 2, также известного как GPR109A), a G i / o -связанный Рецептор, связанный с G-белком (GPCR),
Как и другие короткоцепочечные жирные кислоты (SCFA), бутират является агонистом рецепторов свободных жирных кислот FFAR2 и FFAR3, которые функционируют как датчики питательных веществ, которые облегчают гомеостатический контроль энергетического баланса ; однако среди группы SCFA только бутират является агонистом HCA 2. Масляная кислота метаболизируется митохондриями, особенно в колоноцитах и печени, с образованием аденозинтрифосфата (АТФ) во время метаболизма жирных кислот. Масляная кислота также является ингибитором HDAC (в частности, HDAC1, HDAC2, HDAC3 и HDAC8), лекарством, которое ингибирует функцию ферментов гистондеацетилазы, тем самым способствуя ацетилированному состоянию гистоны в клетках. Ацетилирование гистонов ослабляет структуру хроматина за счет уменьшения электростатического притяжения между гистонами и ДНК. В целом считается, что факторы транскрипции не смогут получить доступ к областям, в которых гистоны тесно связаны с ДНК (т.е. неацетилированы, например, гетерохроматин). Следовательно, считается, что масляная кислота усиливает транскрипционную активность промоторов, которые обычно подавляются или подавляются из-за активности гистондеацетилазы.
Фармакокинетика
Бутират, который продуцируется в толстой кишке в результате микробной ферментации пищевых волокон, в первую очередь абсорбируется и метаболизируется колоноцитами и печенью для образования АТФ во время энергетического метаболизма; однако некоторое количество бутирата абсорбируется в дистальном отделе толстой кишки, который не связан с воротной веной, тем самым обеспечивая системное распределение бутирата по системам многих органов через систему кровообращения. Бутират, достигший системного кровообращения, может легко преодолевать гематоэнцефалический барьер через переносчики монокарбоксилата (т. Е. Некоторых членов группы переносчиков SLC16A ). Другие переносчики, которые опосредуют прохождение бутирата через липидные мембраны, включают SLC5A8 (SMCT1), SLC27A1 (FATP1) и SLC27A4 (FATP4).
Метаболизм
Масляная кислота метаболизируется различными ХМ-лигазами человека (ACSM1, ACSM2B, ASCM3, ACSM4, ACSM5 и ACSM6), также известными как бутират-КоА-лигаза. В результате этой реакции образуется метаболит бутирил – КоА, который образуется следующим образом:
- аденозинтрифосфат + масляная кислота + кофермент A → аденозинмонофосфат + пирофосфат + бутирил-КоА
As a короткоцепочечные жирные кислоты, бутират метаболизируется митохондриями как источник энергии (т. е. аденозинтрифосфат или АТФ) посредством метаболизма жирных кислот.
в у людей пролекарство бутирата трибутирин метаболизируется триацилглицерин липазой и превращается в бутират в результате реакции:
- трибутирин + H 2 O → дибутирин + масляная кислота
Исследования
Периферийные эффекты
Бутират оказывает множество эффектов на энергетический гомеостаз и связанные с ним заболевания (диабет и ожирение ), воспаление и иммунная функция (например, оно оказывает выраженное антимикробное и антиканцерогенное эффекты) у людей. Эти эффекты проявляются в его метаболизме в митохондриях с образованием АТФ во время метаболизма жирных кислот или через одну или несколько его гистон-модифицирующих ферментов мишеней (т. Е. гистоновые деацетилазы класса I ) и рецептор, связанный с G-белком, мишени (т.е. FFAR2, FFAR3 и HCA 2 ).
Иммуномодуляция и воспаление
Действие бутирата на иммунную систему опосредовано ингибированием гистондеацетилаз класса I и активацией его рецептора, связанного с G-белком, мишени: HCA 2 (GPR109A), FFAR2 (GPR43) и FFAR3 (GPR41). Среди короткоцепочечных жирных кислот бутират является наиболее мощный промотор кишечных регуляторных Т-клеток in vitro и единственный в группе лиганд HCA 2. Было показано, что он является критическим медиатором воспалительной реакции толстой кишки. Обладает как профилактическим, так и терапевтическим потенциалом для противодействия воспалению. n-опосредованный язвенный колит и колоректальный рак.
Бутират обладает антимикробными свойствами у людей, которые опосредуются антимикробным пептидом LL-37, который он индуцирует посредством ингибирования HDAC гистона H3. In vitro бутират увеличивает экспрессию гена FOXP3 (регулятор транскрипции для Treg ) и способствует развитию регуляторных Т-клеток толстой кишки (Tregs) посредством ингибирования гистондеацетилаз класса I ; благодаря этим действиям он увеличивает экспрессию интерлейкина 10, противовоспалительного цитокина. Бутират также подавляет воспаление толстой кишки, ингибируя пути передачи сигналов IFN-γ — STAT1, что частично опосредуется посредством ингибирования гистондеацетилазы. В то время как временная передача сигналов IFN-γ обычно связана с нормальным иммунным ответом хозяина, хроническая передача сигналов IFN-γ часто связана с хроническим воспалением. Было показано, что бутират ингибирует активность HDAC1, который связан с промотором гена Fas в Т-клетках, что приводит к гиперацетилированию промотора Fas и усилению регуляции рецептора Fas на поверхности Т-клеток. 444>
Подобно другим изученным агонистам HCA 2, бутират также оказывает заметное противовоспалительное действие в различных тканях, включая мозг, желудочно-кишечный тракт, кожу и сосудистую ткань. Связывание бутирата в FFAR3 вызывает высвобождение нейропептида Y и способствует функциональному гомеостазу слизистой оболочки толстой кишки и кишечной иммунной системе.
Масляная кислота является важным источником энергии (АТФ ) источником клеток, выстилающих толстую кишку млекопитающих (колоноциты). Без масляной кислоты для получения энергии клетки толстой кишки подвергаются усиленной аутофагии (т. Е. Самоперевариванию).
Рак
Бутират оказывает различное воздействие на здоровые и раковые клетки; это известно как «парадокс бутирата». В частности, бутират подавляет опухолевые клетки толстой кишки и стимулирует пролиферацию здоровых эпителиальных клеток толстой кишки. Сигнальный механизм не совсем понятен. Производство летучих жирных кислот, таких как бутират, из ферментируемых волокон может способствовать роли пищевых волокон при раке толстой кишки. Короткоцепочечные жирные кислоты, в том числе масляная кислота, производятся полезные бактерии толстой кишки (пробиотики ), которые питаются или ферментируют пребиотики, которые представляют собой растительные продукты, содержащие пищевые волокна. Эти короткоцепочечные жирные кислоты приносят пользу колоноцитам, увеличивая выработку энергии, и могут защищать от рака толстой кишки, подавляя пролиферацию клеток.
И наоборот, некоторые исследователи пытались исключить бутират и рассматривать его как потенциальную движущую силу рака. Исследования на мышах показывают, что она стимулирует трансформацию MSH2-дефицитных эпителиальных клеток толстой кишки.
Зависимость
Масляная кислота — это HDAC ингибитор, селективный в отношении HDAC класса I у человека. HDAC — это модифицирующие гистоны ферменты, которые могут вызывать деацетилирование гистонов и подавление экспрессии генов. HDAC являются важными регуляторами синаптического образования, синаптической пластичности и формирования долговременной памяти. Известно, что несколько HDAC (в частности, HDAC класса I) участвуют в опосредовании развития зависимости. Масляная кислота и другие ингибиторы HDAC использовались в доклинических исследованиях для оценки транскрипционных, нервных и поведенческих эффектов ингибирования HDAC у животных, зависимых от наркотиков.
См. Также
- Список насыщенных жирных кислот
- Бутираты
- Гистон
- Фермент, модифицирующий гистоны
- Гистонацетилаза
- Гистондеацетилаза
- Фермент, модифицирующий гистоны
- Оксимасляная кислота
- α-Оксимасляная кислота
- β-Оксимасляная кислота
- γ-Оксимасляная кислота
- β-Метилмасляная кислота
- β-Гидрокси β-метилмасляная кислота
- Бутират натрия
- Синбиотики
Примечания
Ссылки
Эта статья включает текст из публикации, находящейся сейчас в общественное достояние : Чисхолм, Хью, изд. (1911). «Масляная кислота ». Encyclopædia Britannica (11-е изд.). Cambridge University Press.
Внешние ссылки
- Международной картой химической безопасности 1334
|
||

|
||
| Имена | ||
|---|---|---|
|
Предпочтительное название IUPAC
Бутановая кислота |
||
| Другие имена
Этилуксусная кислота |
||
| Идентификаторы | ||
|
Количество CAS |
|
|
|
3D модель ( JSmol ) |
|
|
| ЧЭБИ |
|
|
| ЧЭМБЛ |
|
|
| ChemSpider |
|
|
| DrugBank |
|
|
| ECHA InfoCard |
100.003.212 |
|
| Номер ЕС |
|
|
|
IUPHAR / BPS |
|
|
| КЕГГ |
|
|
| MeSH | Масляная + кислота | |
|
PubChem CID |
|
|
| Номер RTECS |
|
|
| UNII |
|
|
| Номер ООН | 2820 | |
|
Панель управления CompTox ( EPA ) |
|
|
|
ИнЧИ
|
||
|
Улыбки
|
||
| Характеристики | ||
|
Химическая формула |
C 3ЧАС 7COOH |
|
| Молярная масса | 88,106 г · моль -1 | |
| Появление | Бесцветная жидкость | |
| Запах | Неприятный, похожий на запах рвоты или тела | |
| Плотность | 1,135 г / см 3 (-43 ° C) 0,9528 г / см 3 (25 ° C) |
|
| Температура плавления | -5,1 ° С (22,8 ° F, 268,0 К) | |
| Точка кипения | 163,75 ° С (326,75 ° F, 436,90 К) | |
|
|
Сублимы при −35 ° C Δ subl H |
|
|
Растворимость в воде |
Смешиваемый | |
| Растворимость | Смешивается с этанолом , эфиром . Слабо растворим в CCl 4 | |
| журнал P | 0,79 | |
| Давление газа | 0,112 кПа (20 ° C) 0,74 кПа (50 ° C) 9,62 кПа (100 ° C) |
|
|
|
5,35 · 10 −4 л · атм / моль | |
| Кислотность (p K a ) | 4.82 | |
|
Магнитная восприимчивость (χ) |
-55,10 · 10 -6 см 3 / моль | |
| Теплопроводность | 1,46 · 10 5 Вт / м · К | |
|
Показатель преломления ( n D ) |
1,398 (20 ° С) | |
| Вязкость | 1,814 гр Р (15 ° С) 1,426 сП (25 ° С) |
|
| Состав | ||
|
Кристальная структура |
Моноклинический (−43 ° C) | |
|
Космическая группа |
C2 / м | |
|
Постоянная решетки |
a = 8,01 Å, b = 6,82 Å, c = 10,14 Å α = 90 °, β = 111,45 °, γ = 90 ° |
|
|
Дипольный момент |
0,93 Д (20 ° С) | |
| Термохимия | ||
|
Теплоемкость ( C ) |
178,6 Дж / моль · К | |
|
Стандартная мольная |
222,2 Дж / моль · К | |
|
Std энтальпия |
−533,9 кДж / моль | |
|
Стандартная энтальпия |
2183,5 кДж / моль | |
| Опасности | ||
| Паспорт безопасности | Внешний паспорт безопасности материала | |
| Пиктограммы GHS |

|
|
| Сигнальное слово GHS | Опасность | |
|
Формулировки опасности GHS |
H314 | |
|
Меры предосторожности GHS |
P280 , P305 + 351 + 338 , P310 | |
| NFPA 704 (огненный алмаз) |
3 2 0 |
|
| точка возгорания | От 71 до 72 ° C (от 160 до 162 ° F, от 344 до 345 K) | |
|
самовоспламенения |
440 ° С (824 ° F, 713 К) | |
| Пределы взрываемости | 2,2–13,4% | |
| Смертельная доза или концентрация (LD, LC): | ||
|
LD 50 ( средняя доза ) |
2000 мг / кг (перорально, крыса) | |
| Родственные соединения | ||
|
Родственные карбоновые кислоты |
Пропионовая кислота , пентановая кислота | |
|
Родственные соединения |
1-бутанол, бутиральдегид, метилбутират |
|
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
||
| Ссылки на инфобоксы | ||
Масляная кислота (от древнегреческого : βούτῡρον , что означает «масло»), также известная под систематическим названием бутановая кислота , представляет собой алкилкарбоновую кислоту с прямой цепью с химической формулой CH 3 CH 2 CH 2 CO 2 H. Это маслянистая , бесцветная жидкость с неприятным запахом . Изомасляная кислота (2-метилпропановая кислота) является изомером . Соли и сложные эфиры масляной кислоты известны как бутираты или бутаноаты . Кислота не встречается в природе, но ее сложные эфиры широко распространены. Это обычное промышленное химическое вещество и важный компонент в кишечнике млекопитающих.
История
Масляная кислота в нечистой форме была впервые обнаружена в 1814 году французским химиком Мишелем Эженом Шеврёлем . К 1818 году он достаточно очистил его, чтобы охарактеризовать его. Однако Шеврёль не опубликовал свои ранние исследования масляной кислоты; вместо этого он передал свои находки в виде рукописи секретарю Академии наук в Париже, Франция. Анри Браконно , французский химик, также исследовал состав масла и публиковал свои открытия, что привело к спорам о приоритете. Еще в 1815 году Шеврёль утверждал, что он обнаружил вещество, ответственное за запах масла. К 1817 году он опубликовал некоторые из своих открытий относительно свойств масляной кислоты и назвал ее. Однако только в 1823 году он подробно описал свойства масляной кислоты. Название масляная кислота происходит от древнегреческого : βούτῡρον , что означает «масло», вещество, в котором она была впервые обнаружена. Латинское название butyrum (или бутурум ) похоже.
Вхождение
Триглицериды масляной кислоты составляют 3–4% масла. Когда масло становится прогорклым, масляная кислота высвобождается из глицерида путем гидролиза . Это одна из подгруппы жирных кислот, называемых короткоцепочечными жирными кислотами . Масляная кислота — это типичная карбоновая кислота, которая реагирует с основаниями и влияет на многие металлы. Он содержится в животных жиров и растительных масел , коровьего молока , грудное молоко , сливочное масло , пармезан сыр , запах тела , рвотой , и как продукт анаэробного брожения ( в том числе и в толстой кишке ). Имеет вкус сливочного масла и неприятный запах . Млекопитающие с хорошими способностями к обнаружению запаха, такие как собаки , могут обнаружить его в концентрации 10 частей на миллиард , тогда как люди могут обнаружить его только в концентрациях выше 10 частей на миллион . В пищевой промышленности он используется в качестве ароматизатора .
В организме человека, масляная кислота является одним из двух основных эндогенных агонистов человеческой гидроксикарбоновой кислоты рецептора 2 (ГКО 2 ), A G I / O -coupled G-белок рецептора .
Масляная кислота присутствует в виде своего октилового эфира в пастернаке ( Pastinaca sativa ) и в семенах дерева гинкго .
Производство
Промышленные
В промышленности масляная кислота производится гидроформилированием из пропена и синтез-газа с образованием масляного альдегида , который окисляется до конечного продукта.
- H 2 + CO + CH 3 CH = CH 2 → CH 3 CH 2 CH 2 CHO → масляная кислота
Его можно отделить от водных растворов путем насыщения солями, такими как хлорид кальция . Кальциевая соль Ca (C 4 H 7 O 2 ) 2 · H 2 O менее растворима в горячей воде, чем в холодной.
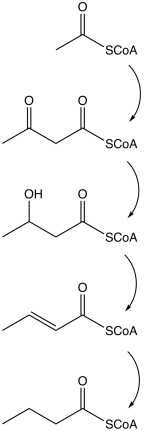
Микробный биосинтез
Один из путей биосинтеза бутирата. Соответствующие ферменты: ацетоацетил-КоА тиолаза, НАД- и НАДФ-зависимая 3-гидроксибутирил-КоА дегидрогеназа, 3-гидроксибутирил-КоА дегидратаза и НАД-зависимая бутирил-КоА дегидрогеназа.
Бутират производится несколькими процессами ферментации, выполняемыми облигатными анаэробными бактериями . Этот путь ферментации был открыт Луи Пастером в 1861 году. Примеры видов бактерий, продуцирующих бутират :
- Clostridium butyricum
- Clostridium kluyveri
- Clostridium pasteurianum
- Faecalibacterium prausnitzii
- Fusobacterium nucleatum
- Butyrivibrio fibrisolvens
- Eubacterium limosum
Путь начинается с гликолитическим расщеплением глюкозы до двух молекул из пирувата , как это происходит в большинстве организмов. Пируват окисляется до ацетилкофермента А, катализируемого пируватом: ферредоксин оксидоредуктазой . Две молекулы диоксида углерода (CO 2 ) и две молекулы элементарного водорода (H 2 ) образуются как отходы. Впоследствии АТФ производится на последнем этапе ферментации. На каждую молекулу глюкозы вырабатываются три молекулы АТФ, что дает относительно высокий выход. Сбалансированное уравнение для этого брожения:
- С 6 Н 12 О 6 → С 4 Н 8 О 2 + 2 СО 2 + 2 Н 2
Другие пути образования бутирата включают восстановление сукцината и диспропорционирование кротоната.
| Действие | Ответственный фермент |
|---|---|
| Ацетилкофермент А превращается в ацетоацетилкофермент А | ацетил-КоА-ацетилтрансфераза |
| Ацетоацетил-кофермент А превращается в β-гидроксибутирил-КоА. | β-гидроксибутирил-КоА дегидрогеназа |
| β-гидроксибутирил-КоА превращается в кротонил-КоА | кротоназ |
| Кротонил-КоА превращается в бутирил-КоА (CH 3 CH 2 CH 2 C = O-CoA) | бутирил-КоА дегидрогеназа |
| Фосфат группа замещает CoA с образованием бутирили фосфат | фосфобутирилаза |
| Фосфатная группа присоединяется к АДФ с образованием АТФ и бутирата. | бутираткиназа |
Некоторые виды образуют ацетон и н- бутанол альтернативным путем, который начинается с ферментации бутирата. Некоторые из этих видов:
- Clostridium acetobutylicum , самый известный производитель ацетона и бутанола, также используется в промышленности.
- Clostridium beijerinckii
- Clostridium tetanomorphum
- Clostridium aurantibutyricum
Эти бактерии начинают ферментацию бутирата, как описано выше, но, когда pH падает ниже 5, они переключаются на производство бутанола и ацетона, чтобы предотвратить дальнейшее снижение pH. На каждую молекулу ацетона образуется две молекулы бутанола.
Изменение пути происходит после образования ацетоацетил-КоА. Затем это промежуточное звено принимает два возможных пути:
- ацетоацетил-КоА → ацетоацетат → ацетон
- ацетоацетил-КоА → бутирил-КоА → бутиральдегид → бутанол
Источники ферментируемого волокна
Остатки высоко ферментируемых волокон, например, из устойчивого крахмала , овсяных отрубей , пектина и гуара , трансформируются бактериями толстой кишки в короткоцепочечные жирные кислоты (SCFA), включая бутират, производя больше SCFA, чем менее ферментируемые волокна, такие как целлюлозы . Одно исследование показало, что резистентный крахмал постоянно производит больше бутирата, чем другие типы пищевых волокон . Производство SCFA из волокон у жвачных животных, таких как крупный рогатый скот, отвечает за содержание бутирата в молоке и масле.
Фруктаны — еще один источник растворимых пищевых волокон пребиотиков, которые могут перевариваться с образованием бутирата. Они часто встречаются в растворимых волокнах продуктов с высоким содержанием серы , таких как лук и овощи семейства крестоцветных . Источники фруктановы включают пшеницу (хотя некоторые из пшеницы штаммов , такая как пишется содержат меньшие количества), рожь , ячмень , лук , чеснок , Иерусалим и артишок , спаржа , свекла , цикорий , листы одуванчика , лук — порей , радиккио , белая часть зеленого луки , брокколи , брюссельская капуста , капуста , фенхель и пребиотики , такие как фруктоолигосахариды ( ФОС ), олигофруктоза и инулин .
Реакции
Масляная кислота реагирует как типичная карбоновая кислота: она может образовывать амидные , сложноэфирные , ангидридные и хлоридные производные. Последний, бутирилхлорид, обычно используется в качестве промежуточного продукта для получения других.
Использует
Масляная кислота используется для получения различных сложных эфиров бутирата. Он используется для производства бутирата ацетата целлюлозы (CAB), который используется в широком спектре инструментов, красок и покрытий и более устойчив к разрушению, чем ацетат целлюлозы . CAB может разлагаться под воздействием тепла и влаги с выделением масляной кислоты.
Низкомолекулярные эфиры масляной кислоты, такие как метилбутират , в основном имеют приятный аромат или вкус. Как следствие, они используются как пищевые и парфюмерные добавки. Это одобренный пищевой ароматизатор в базе данных EU FLAVIS (номер 08.005).
Из-за сильного запаха он также использовался в качестве добавки к рыболовной наживке. Многие коммерчески доступные ароматизаторы, используемые в приманках для карпа ( Cyprinus carpio ), используют масляную кислоту в качестве сложноэфирной основы. Неясно, привлекает ли рыбу сама масляная кислота или добавленные в нее вещества. Масляная кислота была одной из немногих органических кислот, которые оказались вкусными как для линя, так и для горького . Вещество используется как вонь бомбы по морской пастух общество охраны нарушить японские китобойные экипажей.
Фармакология
| Ингибированный фермент | IC 50 ( нМ ) | Въездная записка |
|---|---|---|
| HDAC1 | 16 000 | |
| HDAC2 | 12 000 | |
| HDAC3 | 9 000 | |
| HDAC4 | 2 000 000 | Нижняя граница |
| HDAC5 | 2 000 000 | Нижняя граница |
| HDAC6 | 2 000 000 | Нижняя граница |
| HDAC7 | 2 000 000 | Нижняя граница |
| HDAC8 | 15 000 | |
| HDAC9 | 2 000 000 | Нижняя граница |
| CA1 | 511 000 | |
| CA2 | 1 032 000 | |
| Цель GPCR | пЭК 50 | Въездная записка |
| FFAR2 | 2,9–4,6 | Полный агонист |
| FFAR3 | 3,8–4,9 | Полный агонист |
| ГКА 2 | 2,8 | Агонист |
Фармакодинамика
Масляная кислота (pK a 4,82) полностью ионизируется при физиологическом pH , поэтому ее анион является материалом, который в основном важен в биологических системах. Это один из двух основных эндогенных агонистов человеческого гидроксикарбоновой кислоты рецептора 2 (ГКА 2 , он же GPR109A), A G I / O -coupled G-белком рецепторов (GPCR) , ,
Подобно другим короткоцепочечным жирным кислотам (SCFA), бутират является агонистом рецепторов свободных жирных кислот FFAR2 и FFAR3 , которые действуют как сенсоры питательных веществ, которые облегчают гомеостатический контроль энергетического баланса ; однако среди группы SCFA только бутират является агонистом HCA 2 . Это также ингибитор HDAC (в частности, HDAC1, HDAC2, HDAC3 и HDAC8), лекарство, которое ингибирует функцию ферментов гистондеацетилазы , тем самым способствуя ацетилированному состоянию гистонов в клетках. Ацетилирование гистонов ослабляет структуру хроматина за счет уменьшения электростатического притяжения между гистонами и ДНК . В целом считается, что факторы транскрипции не могут получить доступ к областям, в которых гистоны тесно связаны с ДНК (т. Е. Неацетилированы, например, гетерохроматин). Следовательно, считается, что масляная кислота усиливает транскрипционную активность промоторов, которые обычно подавляются или подавляются из-за активности гистондеацетилазы.
Фармакокинетика.
Бутират, который вырабатывается в толстой кишке в результате микробной ферментации пищевых волокон, в первую очередь абсорбируется и метаболизируется колоноцитами и печенью для образования АТФ во время энергетического метаболизма; однако некоторое количество бутирата всасывается в дистальном отделе толстой кишки , который не связан с воротной веной, тем самым обеспечивая системное распределение бутирата по системам многих органов через систему кровообращения. Бутират, достигший системного кровообращения, может легко преодолевать гематоэнцефалический барьер через переносчики монокарбоксилатов (т.е. некоторых членов группы переносчиков SLC16A ). Другие переносчики, которые опосредуют прохождение бутирата через липидные мембраны, включают SLC5A8 (SMCT1), SLC27A1 (FATP1) и SLC27A4 (FATP4).
Метаболизм
Масляная кислота метаболизируется различными ХМ-лигазами человека (ACSM1, ACSM2B, ASCM3, ACSM4, ACSM5 и ACSM6), также известными как бутират-КоА-лигаза. Метаболитом, продуцируемым в этой реакции, является бутирил-КоА , который образуется следующим образом:
- Аденозинтрифосфат + масляная кислота + кофермент А → аденозинмонофосфат + пирофосфат + бутирил-КоА
Будучи короткоцепочечной жирной кислотой , бутират метаболизируется митохондриями в качестве источника энергии (например, аденозинтрифосфата или АТФ) посредством метаболизма жирных кислот . В частности, это важный источник энергии для клеток, выстилающих толстую кишку млекопитающих (колоноцитов). Без бутиратов клетки толстой кишки подвергаются аутофагии (т. Е. Самоперевариванию) и погибают.
У людей предшественник бутирата трибутирин , который в природе присутствует в масле, метаболизируется триацилглицерин липазой в дибутирин и бутират в результате реакции:
- Трибутирин + H 2 O → дибутирин + масляная кислота
Биохимия
Бутират оказывает многочисленные эффекты на энергетический гомеостаз и связанные с ним заболевания ( диабет и ожирение ), воспаление и иммунную функцию (например, он оказывает выраженное антимикробное и антиканцерогенное действие) у людей. Эти эффекты проявляются в его метаболизме в митохондриях для выработки АТФ во время метаболизма жирных кислот или через одну или несколько его гистон-модифицирующих ферментов- мишеней (т. Е. Гистоновых деацетилаз класса I ) и мишеней рецепторов, связанных с G-белком (т. Е. FFAR2 , FFAR3 , и ГКА 2 ).
В кишечнике млекопитающих
Бутират необходим для поддержания иммунного гомеостаза организма. Хотя роль и значение бутирата в кишечнике до конца не изучены, многие исследователи утверждают, что истощение запасов бутират-продуцирующих бактерий у пациентов с несколькими васкулитами имеет важное значение для патогенеза этих заболеваний. Истощение бутирата в кишечнике обычно вызвано отсутствием или истощением бактерий, продуцирующих бутират (BPB). Это истощение BPB приводит к микробному дисбактериозу . Это характеризуется общим низким биоразнообразием и истощением основных элементов, производящих бутират. Бутират является важным микробным метаболитом, который играет жизненно важную роль в качестве модулятора правильной иммунной функции хозяина. Было показано, что дети с дефицитом ДГП более подвержены аллергическим заболеваниям и диабету 1 типа. Бутират также снижается при диете с низким содержанием клетчатки, которая может вызывать воспаление и иметь другие неблагоприятные эффекты, поскольку эти короткоцепочечные жирные кислоты активируют PPAR-γ .
Бутират играет ключевую роль в поддержании иммунного гомеостаза как локально (в кишечнике), так и системно (через циркулирующий бутират). Было показано, что он способствует дифференцировке регуляторных Т-клеток . В частности, циркулирующий бутират вызывает образование экстратимических регуляторных Т-клеток. Низкие уровни бутирата у людей могут способствовать снижению опосредованного регуляторными Т-клетками контроля, тем самым способствуя мощному иммунопатологическому Т-клеточному ответу. С другой стороны, кишечный бутират ингибирует местные провоспалительные цитокины. Следовательно, отсутствие или истощение этих BPB в кишечнике может быть возможным помощником в чрезмерно активной воспалительной реакции. Бутират в кишечнике также защищает целостность кишечного эпителиального барьера. Таким образом, снижение уровня бутирата приводит к повреждению или дисфункции кишечного эпителиального барьера.
В исследовании 2013 года, проведенном Furusawa et al., Было обнаружено, что бутират микробного происхождения играет важную роль в индукции дифференцировки регуляторных Т-клеток толстой кишки у мышей. Это имеет большое значение и, возможно, имеет отношение к патогенезу и васкулиту, связанному со многими воспалительными заболеваниями, поскольку регуляторные Т-клетки играют центральную роль в подавлении воспалительных и аллергических реакций. В нескольких исследованиях было продемонстрировано, что бутират индуцирует дифференцировку регуляторных Т-клеток in vitro и in vivo. Противовоспалительная способность бутирата была тщательно проанализирована и подтверждена многими исследованиями. Было обнаружено, что бутират, продуцируемый микроорганизмами, ускоряет производство регуляторных Т-клеток, хотя конкретный механизм, с помощью которого это происходит, неясен. Совсем недавно было показано, что бутират играет важную и прямую роль в модуляции экспрессии генов цитотоксических Т-клеток. Бутират также оказывает противовоспалительное действие на нейтрофилы, уменьшая их миграцию в раны. Этот эффект опосредуется рецептором HCA 1.
Иммуномодуляция и воспаление
Воздействие бутирата на иммунную систему опосредуется посредством ингибирования гистоновых деацетилаз класса I и активации его рецепторов- мишеней, связанных с G-белком : HCA 2 (GPR109A), FFAR2 (GPR43) и FFAR3 (GPR41). Среди короткоцепочечных жирных кислот бутират является наиболее мощным промотором регуляторных Т-клеток кишечника in vitro и единственным из группы, который является лигандом HCA 2 . Было показано, что он является важным медиатором воспалительной реакции толстой кишки. Он обладает как профилактическим, так и терапевтическим потенциалом для противодействия язвенному колиту, опосредованному воспалением, и колоректальному раку .
Бутират обладает антимикробными свойствами у людей, которые опосредуются антимикробным пептидом LL-37 , который он индуцирует посредством ингибирования HDAC гистона H3. В пробирке, бутират увеличивает экспрессию гена из FOXP3 (далее регулятор транскрипции для Tregs ) и способствует ободочной регуляторных Т — клеток (Tregs) через ингибирование класса I гистондезацетилаз ; благодаря этим действиям он увеличивает экспрессию интерлейкина 10 , противовоспалительного цитокина . Бутират также подавляет воспаление толстой кишки, ингибируя пути передачи сигналов IFN-γ — STAT1 , что частично опосредуется ингибированием гистондеацетилазы . В то время как временная передача сигналов IFN-γ обычно связана с нормальным иммунным ответом хозяина , хроническая передача сигналов IFN-γ часто связана с хроническим воспалением. Было показано, что бутират ингибирует активность HDAC1, который связан с промотором гена Fas в Т-клетках, что приводит к гиперацетилированию промотора Fas и усилению регуляции рецептора Fas на поверхности Т-клеток.
Подобно другим изученным агонистам HCA 2 , бутират также оказывает заметное противовоспалительное действие в различных тканях, включая мозг, желудочно-кишечный тракт, кожу и сосудистую ткань . Связывание бутирата в FFAR3 индуцирует высвобождение нейропептида Y и способствует функциональному гомеостазу слизистой оболочки толстой кишки и кишечной иммунной системы.
Рак
Было показано, что бутират является важным медиатором воспалительной реакции толстой кишки. Он отвечает за около 70% энергии колоноцитов, являясь критически важным SCFA в гомеостазе толстой кишки . Бутират обладает как профилактическим, так и терапевтическим потенциалом для противодействия язвенному колиту (ЯК), опосредованному воспалением, и колоректальному раку . Он оказывает различное воздействие на здоровые и раковые клетки: это известно как «парадокс бутирата». В частности, бутират подавляет опухолевые клетки толстой кишки и стимулирует пролиферацию здоровых эпителиальных клеток толстой кишки. Объяснение того, почему бутират является источником энергии для нормальных колоноцитов и индуцирует апоптоз в раковых клетках толстой кишки , заключается в эффекте Варбурга в раковых клетках, который приводит к тому, что бутират не метаболизируется должным образом. Это явление приводит к накоплению бутирата в ядре, действующего как ингибитор гистондеацетилазы (HDAC). Одним из механизмов, лежащих в основе функции бутирата при подавлении воспаления толстой кишки, является ингибирование сигнальных путей IFN-γ / STAT1 . Было показано, что бутират ингибирует активность HDAC1, который связан с промотором гена Fas в Т-клетках , что приводит к гиперацетилированию промотора Fas и усилению регуляции рецептора Fas на поверхности Т-клеток. Таким образом, предполагается, что бутират усиливает апоптоз Т-клеток в ткани толстой кишки и тем самым устраняет источник воспаления (продукцию IFN-γ). Бутират подавляет ангиогенез , инактивируя активность фактора транскрипции Sp1 и подавляя экспрессию гена фактора роста эндотелия сосудов .
Таким образом, производство летучих жирных кислот, таких как бутират, из ферментируемых волокон может способствовать роли пищевых волокон при раке толстой кишки. Короткоцепочечные жирные кислоты , в том числе масляная кислота, вырабатываются полезными бактериями толстой кишки ( пробиотиками ), которые питаются или ферментируют пребиотики, которые представляют собой растительные продукты, содержащие пищевые волокна. Эти короткоцепочечные жирные кислоты приносят пользу колоноцитам, увеличивая выработку энергии, и могут защищать от рака толстой кишки, подавляя пролиферацию клеток.
И наоборот, некоторые исследователи пытались исключить бутират и считать его потенциальным возбудителем рака. Исследования на мышах показывают, что он стимулирует трансформацию эпителиальных клеток толстой кишки с дефицитом MSH2 .
Возможные способы лечения восстановления бутирата
Из-за важности бутирата как регулятора воспаления и фактора, способствующего развитию иммунной системы, истощение запасов бутирата может быть ключевым фактором, влияющим на патогенез многих васкулитов . Таким образом, важно поддерживать здоровый уровень бутирата в кишечнике. Трансплантаты фекальной микробиоты (для восстановления BPB и симбиоза в кишечнике) могут быть эффективны за счет восполнения уровня бутирата. При этом лечении здоровый человек сдает свой стул для трансплантации человеку с дисбактериозом. Менее инвазивным вариантом лечения является введение бутирата в виде пероральных добавок или клизм, которые оказались очень эффективными в купировании симптомов воспаления с минимальными побочными эффектами или их отсутствием. В исследовании, в котором пациентов с язвенным колитом лечили клизмами с бутиратом, воспаление значительно уменьшилось, и кровотечение полностью прекратилось после введения бутирата.
Зависимость
Масляная кислота является ингибитором HDAC , который селективен в отношении HDAC класса I у людей. HDAC представляют собой модифицирующие гистоны ферменты, которые могут вызывать деацетилирование гистонов и подавление экспрессии генов. HDAC являются важными регуляторами синаптического образования, синаптической пластичности и формирования долговременной памяти . Известно, что HDAC класса I участвуют в опосредовании развития зависимости . Масляная кислота и другие ингибиторы HDAC использовались в доклинических исследованиях для оценки транскрипционных, нервных и поведенческих эффектов ингибирования HDAC у животных, зависимых от наркотиков.
Бутиратные соли и сложные эфиры
Бутират или бутановой , ион является С 3 Н 7 С О О — , то сопряженное основание масляной кислоты. Это форма, обнаруженная в биологических системах при физиологическом pH . Масляное или бутановое соединение представляет собой карбоксилатную соль или сложный эфир масляной кислоты.
Примеры
Соли
- Бутират натрия
Сложные эфиры
- Бутилбутират
- Бутирил-КоА
- Бутират ацетата целлюлозы (авиационный допинг)
- Бутират бензоата эстрадиола
- Этилбутират
- Метилбутират
- Пентилбутират
- Трибутирин
Смотрите также
- Список насыщенных жирных кислот
-
Гистон
-
Фермент, модифицирующий гистоны
- Гистоновая ацетилаза
- Гистоновая деацетилаза
-
Фермент, модифицирующий гистоны
-
Оксимасляные кислоты
- α-гидроксимасляная кислота
- β-гидроксимасляная кислота
- γ-оксимасляная кислота
-
β-метилмасляная кислота
- β-гидрокси β-метилмасляная кислота
Примечания
использованная литература
Эта статья включает текст из публикации, которая сейчас находится в общественном достоянии : Chisholm, Hugh, ed. (1911). « Масляная кислота ». Британская энциклопедия (11-е изд.). Издательство Кембриджского университета.
внешние ссылки
- Стандартные справочные данные NIST для бутановой кислоты
| Бутановая кислота | ||

|
||
| Идентификация | ||
|---|---|---|
| Название ИЮПАК | Бутановая кислота | |
| Синонимы |
масляная |
|
| Н о CAS | 107-92-6 | |
| N о ИК | 100 003 212 | |
| N о ЕС | 203-532-3 | |
| DrugBank | DB03568 | |
| PubChem | 264 | |
| FEMA | 2221 | |
| Улыбки | ||
| ИнЧИ | ||
| Появление | бесцветная маслянистая жидкость с характерным запахом. | |
| Химические свойства | ||
| Грубая формула | C 4 H 8 O 2 [изомеры] | |
| Молярная масса | 88,1051 ± 0,0044 г / моль C 54,53%, H 9,15%, O 36,32%, |
|
| Молекулярный диаметр | 0,560 нм | |
| Физические свойства | ||
| Т ° плавления | −7,9 ° С | |
| T ° кипения | 164 ° С | |
| Растворимость | в воде: смешивается, смешивается с этанолом , эфиром |
|
| Параметр растворимости δ |
21,5 МПа 1/2 ( 25 ° С );
25,1 Дж 1/2 · см -3/2 ( 25 ° C ) |
|
| Объемная масса |
0,959 г · мл от -1 до 20 ° C 0,964 г · мл от -1 до 25 ° C |
|
| Температура самовоспламенения | 452 ° С | |
| точка возгорания | 72 ° C (закрытая чашка) | |
| Пределы взрываемости в воздухе | 2 — 10 % по объему | |
| Давление насыщающего пара | при 20 ° C : 57 Па | |
| Критическая точка | 52,7 бар , 354,85 ° C | |
| Термохимия | ||
| C p | ||
| Электронные свойства | ||
| 1 повторно энергия ионизации | 10,17 ± 0,05 эВ (газ) | |
| Оптические свойства | ||
| Показатель преломления |
 1,398 1,398
|
|
| Меры предосторожности | ||
| SGH | ||
|
H314, |
||
| WHMIS | ||
|
Неклассифицированный продукт |
||
| NFPA 704 | ||
|
2 3 0 |
||
| Транспорт | ||
|
||
| Экотоксикология | ||
| DL 50 | 8,79 г · кг -1 (крысы, перорально) | |
| LogP | 0,79 | |
|
|
||
| Единицы СИ и СТП, если не указано иное. | ||
Бутановая кислота , также называемая масляная кислота греческого βουτυρος ( масло ) представляет собой карбоновую кислоту , насыщенной формулой СН 3 СН 2 СН 2 -СООН
Он содержится, например, в прогорклом масле , пармезане и содержимом желудка , где он испускает сильный и неприятный запах. Масляная кислота содержится в концентрации от 5 до 40 мкг / м 3 в зависимости от источника.
Под стандартных условиях температуры и давления , бутановая кислота представляет собой слегка маслянистая жидкость , которая затвердевает при -8 ° С и чья температура кипения составляет 164 ° С . Он легко растворяется в воде , этаноле и эфире и отделяется от растворителя при добавлении хлорида кальция . Дихромат калия и серная кислота окислять в диоксид углерода и уксусную кислоту , в то время как перманганат калий щелочного оксид только диоксид углерода . Кроме того, его изомер конституции 2-метилпропановая , который обязан своим вторым именем изомасляной кислоты.
Это также короткоцепочечная жирная кислота, содержащаяся в растительных маслах и животных жирах. Глицерид ( эфир из глицерина ) масл ной кислоты содержит от 3% до 4% масла. Когда масло становится прогорклым, глицериды гидролизуются , выделяя масляную кислоту с неприятным запахом. Обычная масляная кислота или масляная кислота ферментации также содержится в виде гексилового эфира в масле Heracleum giganteum и в виде сложного октилового эфира в масле пастернака ( Pastinaca sativa ); он также присутствует в потоотделении .
Это, как правило , получают с помощью ферментации из сахара или крахмала , вызванное добавлением гниению сыр , к которому карбонат кальция добавляют для нейтрализации кислот , образованных в процессе. Масляному брожению крахмала способствует прямое добавление Bacillus subtilis .
Из масляной кислоты получают различные сложные эфиры. Эти сложные эфиры называют бутиратом или, правильнее, бутаноатом . Те, у кого низкая молярная масса, такие как метилбутаноат , имеют в основном приятный аромат. Таким образом, они используются в качестве пищевых добавок или в парфюмерии.
Его неочищенная формула такая же, как у пропилформиата .
Использовать
Бутановая кислота используется для приготовления различных ароматизаторов ( эфиры бутаноата), сложные эфиры масляной кислоты с низким молекулярным весом, такие как метилбутаноат, по большей части имеют приятный аромат или вкус. Поэтому их используют в качестве добавок к пище и парфюмерии.
Благодаря сильному запаху его также используют в качестве добавки к рыболовной наживке. Многие имеющиеся на рынке ароматизаторы для прикормки карпа ( Cyprinus carpio ) используют масляную кислоту в качестве сложноэфирной основы, но неясно, привлекает ли рыбу сама масляная кислота или другие добавленные вещества. Однако масляная кислота — одна из немногих органических кислот, которые оказались вкусными как для линя, так и для жуков .
Как ни странно, это вещество также использовалось в качестве нетоксичного, вызывающего тошноту и портящего плоть репеллента китов командой «Морской пастух» против корабля-фабрики японских китобоев и активистами против абортов; некоторые полицейские силы также рассматривают возможность использования его в качестве несмертельного оружия .
Производство бутиратов
Классическое брожение
Бутираты или, точнее, бутаноаты, сложные эфиры бутановой кислоты, происходят в результате ферментации с участием анаэробных бактерий . Этот процесс был открыт Луи Пастером в 1861 году . Основными бактериями, продуцирующими бутираты, являются:
- Clostridium butyricum ;
- Clostridium kluyveri ;
- Clostridium pasteurianum ;
- Fusobacterium nucleatum ;
- Butyrivibrio fibrisolvens ;
- Eubacterium limosum ;
- Clostridium tyrobutyricum .
Результаты реакции следующие:
- С 6 Н 12 О 6 → С 4 Н 8 О 2 + 2 СО 2 + 2 Н 2
Первый шаг в производстве butanoates следует метаболическую цепь из гликолиза , что приводит к образованию двух молекул из пирувата на одну молекулу глюкозы . Полученный пируват затем окисляется до этаноата ( ацетата в форме этаноил-кофермента А ) с помощью уникального ферментативного процесса, включающего ряд ферментов, называемых комплексом пируватдегидрогеназы , с параллельным образованием диоксида углерода (CO 2), который затем покидает клетку путем диффузии и восстановления NAD + до NADH.
- Этаноил-кофермент А превращается в ацетоацетил-кофермент А. Ответственным ферментом является ацетил-КоА-ацетил-трансфераза.
- Ацетоацетил-кофермент А превращается в β-гидроксибутирил-КоА. ответственный фермент — β-кетоацил-КоА редуктаза (кофермент: НАДН).
- Β-Гидроксибутирил-КоА превращается в кротонил-КоА. ответственный фермент — β-гидроксиацилдегидратаза.
- Кротонил-СоА становится бутил-КоА (СН 3 СН 2 СН 2). ответственный фермент — еноил-КоА-редуктаза (кофермент: НАДН).
- Фосфатная группа заменяет КоА с образованием бутилфосфата. Ответственный фермент — фосфобутирилаза.
- Фосфатная группа присоединяется к АДФ с образованием АТФ и бутиратов; ответственный фермент является бутират киназы .
Ацетон и ферментация бутиратов
Некоторые бактерии производят ацетон и бутанол с помощью другого процесса, начинающегося с ферментации бутиратов, например:
- Clostridium acetobutylicum : (наиболее важный, используется в химической промышленности)
- Clostridium beijerinckii
- Clostridium tetanomorphum
- Clostridium aurantibutyricum
Эти бактерии следуют процессу ферментации, описанному выше, но, когда pH ниже 5, они переключаются на производство бутанола и ацетона, чтобы предотвратить дальнейшее падение pH, которое было бы для них фатальным. Две молекулы бутанола производятся из одной молекулы ацетона. Модификация происходит после образования ацетоацетил-КоА. В этих условиях посредник может действовать двумя новыми способами:
- Ацетоацетил-КоА → ацетоацетат → ацетон
- Ацетоацетил-КоА → бутирил-КоА → бутаналь → бутанол.
Физиологическая активность бутановой кислоты
Масляная кислота может ингибировать функцию гистона деацетилаз, тем самым увеличивая долю ацетилированных гистонов, которые имеют более низкое сродство к ДНК , чем неацетилированный форму (из — за электростатических причинам отталкивающих свойств). Принято считать, что связывание факторов транскрипции с ДНК ухудшается из-за присутствия неацетилированных гистонов (имеющих низкое сродство к ДНК). Таким образом, можно сделать вывод, что масляная кислота увеличивает транскрипционную активность клетки на уровне промоторов, регулируемых гистондеацетилазами.
Масляная кислота вырабатывается кишечной микробиотой млекопитающих. Его производство усиливается пребиотическими агентами ( растворимыми волокнами ). Он служит топливом для слизистой оболочки кишечника и иммуностимулятором местного и системного действия. Это позволило бы иммунной системе различать колонизацию симбиотическими бактериями и патогенами, такими как холера .
В катионной или сложноэфирной форме масляная кислота обладает противовирусными, противогрибковыми и антибактериальными свойствами. Его интерес к этой форме заключается, прежде всего, в ее способности регулировать раковые клетки и индуцировать клеточную дифференцировку.
Источник
- ( fr ) Эта статья частично или полностью взята из статьи в Википедии на английском языке под названием « Масляная кислота » ( см. список авторов ) .
- ↑ a b c d e f g h и i БУТИРИНОВАЯ КИСЛОТА , паспорт (-ы) безопасности Международной программы по химической безопасности , проверено 9 мая 2009 г.
- ↑ a и b (in) Ицхак Маркус, Свойства растворителей , т. 4, Англия, John Wiley & Sons Ltd,1999 г., 239 с. ( ISBN 0-471-98369-1 )
- ↑ рассчитывается молекулярная масса от « атомных весов элементов 2007 » на www.chem.qmul.ac.uk .
- ↑ (in) Джеймс Э. Марк, Руководство по физическим свойствам полимеров , Springer,2007 г., 2- е изд. , 1076 с. ( ISBN 0387690026 , читать онлайн ) , стр. 294
- ↑ a b и c (ru) Роберт Х. Перри и Дональд В. Грин , Perry’s Chemical Engineers ‘Handbook , США, McGraw-Hill,1997 г., 7- е изд. , 2400 с. ( ISBN 0-07-049841-5 ) , стр. 2-50
- ↑ « Свойства различных газов » на flexwareinc.com (по состоянию на 12 апреля 2010 г. )
- ↑ (in) Карл Л. Яс, Справочник по термодинамическим диаграммам , Vol. 1, Хьюстон, Техас, паб Gulf. Co.,1996 г.( ISBN 0-88415-857-8 )
- ↑ (in) Дэвид Р. Лид, Справочник по химии и физике , CRC,2008 г., 89- е изд. , 2736 с. ( ISBN 978-1-4200-6679-1 ) , стр. 10-205
- ↑ Индексный номер 607-135-00-X в таблице 3.1 приложения VI постановления ЕС № 1272/2008 (16 декабря 2008 г.)
- ↑ « Масляная кислота » в базе данных химических продуктов Reptox в CSST (организации Квебека , ответственного за охрану труда и здоровья), доступ к 25 апреля 2009
- ↑ « Глава 4, Острые, репротоксические риски и восприятие запаха » , на invs.sante.fr
- ↑ (in) « Морозильные приманки » , Nutrabaits
- ↑ АО Касумян и КБ Døving , « Вкусовые предпочтения у рыб », рыбы и рыбное хозяйство , т. 4,2003 г., стр. 289–347 ( DOI 10.1046 / j.1467-2979.2003.00121.x )
- ↑ (in) « Японские китобои, раненые активистами , поджигающими кислоту » , newser.com,2010 г.
-
↑ (in) « История насилия: атаки масляной кислоты » , Национальная федерация абортов,
1998 г. - ↑ PR Pouillart , « Роль масляной кислоты и ее производных в лечении колоректального рака и гемоглобинопатий », Life Sciences , vol. 63,1 — го января 1998, стр. 1739-1760 ( ISSN 0024-3205 , PMID 9820119 , читать онлайн , по состоянию на 29 декабря 2015 г. )
- ↑ (en-US) « Пребиотики: забота о нашем внутреннем саду | NutritionFacts.org » (по состоянию на 24 февраля 2019 г. )
- ↑ Филипп Р. Пуйяр , Флоре Депейн , Афиф Абдельнур и Летиция Деремо , « Нутриоза, пребиотик с низким уровнем усвояемости углеводов, стимулирует иммунитет слизистой оболочки кишечника и предотвращает вызванный TNBS колит у поросят », Воспалительные заболевания кишечника , т. 16,1 — го мая 2010, стр. 783-794 ( ISSN 1536-4844 , PMID 19998458 , DOI 10.1002 / ibd.21130 , читать онлайн , по состоянию на 29 декабря 2015 г. )
Библиография
Voet & Voet; Джон Уайли и сыновья, 1995
Смотрите также
- Список кислот
- Изобутановая кислота
- Летучие жирные кислоты
|
в · м Жирная кислота |
|||||||||
|---|---|---|---|---|---|---|---|---|---|
| Основная классификация |
|
||||||||
| Насыщенный |
|
||||||||
| Ненасыщенный |
|
||||||||
| Эйкозаноиды |
|
||||||||
| Другой |
|
||||||||
|
Основные семейства биомолекул :
|
Поиск химических веществ по названиям или формулам.
Справочник содержит названия веществ и описания химических формул (в т.ч. структурные формулы и скелетные формулы).
Введите часть названия или формулу для поиска:
Общее число найденных записей: 40.
Показано записей: 20.
- Страницы:
- 1
- 2
- Следующая»
1. Масляная кислота
Брутто-формула:
C4H8O2
CAS# 107-92-6
Названия
Русский:
- Масляная кислота [Wiki]
- бутановая кислота(IUPAC)
;
;
English:
- 1-Propanecarboxylic acid
- Butanoic acid(IUPAC)(CAS)
- Butyric acid [Wiki]
- C4:0
- Honey robber
- Propanecarboxylic acid
- Propylformic acid
- n-Butanoic acid
;
;
;
;
;
;
;
;
German:
- Butansäure
- Buttersäure(IUPAC) [Wiki]
- Propylcarbonsäure
- n-Butansäure
;
;
;
;
Español:
- Ácido butanoico(IUPAC)
- Ácido butírico [Wiki]
;
;
French:
- Acide butanoïque(IUPAC) [Wiki]
- acide butyrique(IUPAC)
- acide n-butanoïque
- acide éthylacétique
;
;
;
;
Latina:
- Acidum butyricum [Wiki]
;
Italiano:
- Acido butirrico [Wiki]
- Acido etilacetico
- Acido n-butanoico(IUPAC)
- Acido n-butirrico
- Acido propano-1-carbossilico
;
;
;
;
;
日本語:
- ブタン酸(IUPAC)
- ブチル酸
- 酪酸 [Wiki]
;
;
;
中文:
- 丁酸 [Wiki]
;
Ελληνικά:
- Βουτανικό οξύ(IUPAC) [Wiki]
- Βουτυρικό οξύ
;
;
Português:
- Ácido butanoico(IUPAC) [Wiki]
- Ácido butírico
;
;
H-C-C-C-C<//O>O-H; H|#2|H; H|#3|H; H|#4|H
2. Валин
Брутто-формула:
C5H11NO2
CAS# 72-18-4
Названия
Русский:
- (S)-2-амино-3-метилбутановая кислота(IUPAC)
- Валин [Wiki]
;
;
English:
- (2S)-2-amino-3-methylbutanoic acid(IUPAC)
- 2-amino-3-methylbutanoic acid
- DL-Valine
- L-Valine(CAS)
- Valine(IUPAC) [Wiki]
;
;
;
;
;
German:
- (S)-Valin
- 2-Amino-3-methyl-butansäure
- 2-Aminoisovaleriansäure
- L-Valin
- Valin [Wiki]
;
;
;
;
;
العربية:
- فالين [Wiki]
;
Ελληνικά:
- 2-αμινο-3-μεθυλοβουτανικό οξύ(IUPAC)
- Βαλίνη [Wiki]
;
;
Español:
- Valina [Wiki]
- Ácido 2-amino-3-metilbutanoico
;
;
French:
- L ou S(+)-valine
- Valine [Wiki]
- acide 2-amino-3-méthylbutanoïque(IUPAC)
;
;
;
Italiano:
- Valina [Wiki]
- acido 2(S)-ammino-3-metilbutanoico(IUPAC)
;
;
日本語:
- バリン [Wiki]
;
中文:
- 缬氨酸 [Wiki]
;
H3C/<`|CH3><|NH2>/`|O|OH
H2N/|O`|/OH;H_(A60,d-)#2_(A-60,w+)<->_q6
$color(blue)CH3-CH<|CH3>$color()-CH<|NH2>-COOH
H2N-C-H; COOH|#C|$color(red)CH<`-H3C>|CH3$color()
$slope(45)HN<`/H>-C-C/O`/OH;H|#C|CH<`/H3C>CH3
CH3`/<`-H3C><-NH2>`/<`=O>OH
3. Метионин
Брутто-формула:
C5H11NO2S
CAS# 63-68-3
Названия
Русский:
- (S)-2-амино-4-(метилтио)бутановая кислота(IUPAC)
- Метионин [Wiki]
;
;
English:
- (S)-2-amino-4-(methylthio)butanoic acid
- Methionine(IUPAC) [Wiki]
;
;
German:
- (S)-(–)-Methionin
- (S)-2-Amino-4-(methylsulfanyl)butansäure(IUPAC)
- 2-Amino-4-methylmercaptobuttersäure
- L-Methionin
- Methionin [Wiki]
- α-Amino-γ-methylmercaptobuttersäure
;
;
;
;
;
;
العربية:
- ميثيونين [Wiki]
;
Ελληνικά:
- (S)-2-αμινο-4-(μεθυλοθειο)βουτανικό οξύ(IUPAC)
- Μεθειονίνη [Wiki]
;
;
Español:
- Metionina [Wiki]
;
French:
- L-méthionine
- Méthionine [Wiki]
- S-méthionine
- acide 2-amino-3-mercapto-propionique
- acide 2-amino-4-(méthylsulfanyl)butanoïque(IUPAC)
;
;
;
;
;
Italiano:
- L-Homo-S-metil-cisteina
- L-metionina
- Metionina [Wiki]
- acido 2(S)-ammino-4-metilmercaptobutanoico(IUPAC)
;
;
;
;
日本語:
- メチオニン [Wiki]
;
中文:
- (S)-2-氨基-4-甲硫基丁酸
- 甲硫氨酸 [Wiki]
;
;
Português:
- (S)-2-amino-4-(methylsulfanyl)-butanoic acid
- Metionina [Wiki]
;
;
H2N/|O`|/OH;H_(A60,d-)#2_(A-60,w+)/S/
H3C-S/-/<_q4H2N><wH>/<`\O>-OH
H3C/S/<|wNH3^+>/`|O|O^-
4. Треонин
Брутто-формула:
C4H9NO3
CAS# 72-19-5
Названия
Русский:
- (2S,3R)-2-амино-3-гидроксибутановая кислота(IUPAC)
- L-Треонин
- Треонин [Wiki]
;
;
;
English:
- (2S,3R)-2-amino-3-hydroxybutanoic acid(IUPAC)
- L-(-)-Threonine
- L-Threonine (2S,3R)
- Threonine(IUPAC) [Wiki]
;
;
;
;
German:
- (2S,3R)-2-Amino-3-hydroxybutansäure
- L-Threonin
- Threonin [Wiki]
;
;
;
العربية:
- ثريونين [Wiki]
;
Ελληνικά:
- (2S,3R)-2-αμινο-3-υδροξυβουτανοϊκό οξύ(IUPAC)
- L-θρεονίνη (2S,3R)
- Θρεονίνη [Wiki]
;
;
;
Español:
- Treonina(IUPAC) [Wiki]
- Ácido 2-amino-3-hidroxibutanoicoÁcido 2-amino-3-hidroxibutanoico
;
;
French:
- L-thréonine (2S,3R)
- Thréonine [Wiki]
- acide (2S,3R)-2-amino-3-hydroxybutanoïque(IUPAC)
;
;
;
Italiano:
- L-treonina
- Treonina [Wiki]
- acido 2(S)-ammino-3(R)-idrossibutanoico(IUPAC)
;
;
;
日本語:
- トレオニン [Wiki]
;
中文:
- (2S,3R)-2-氨基-3-羥基丁酸(IUPAC)
- 蘇氨酸 [Wiki]
;
;
Português:
- (2S,3R)-2-Amino-3-hydroxybutanoic acid(IUPAC)
- Treonina [Wiki]
;
;
H3C/<`|wOH><|wNH2>/`|O|OH
-</wOH><-dNH2>`/<\O>`-HO
H3C/<`|wOH><|wNH3^+>/`|O|O^-
H3C-<`|HO><|dH>-<`|NH2><|wH>-<//O>OH
HO/`|O|<|dNH2>/<`|CH3>wOH
5. D-Треонин
Брутто-формула:
C4H9NO3
CAS# 632-20-2
Названия
Русский:
- (2R,3S)-2-амино-3-гидроксибутановая кислота
- D-Треонин
;
;
English:
- (2R,3S)-2-Amino-3-hydroxybutanoic acid
- (2R,3S)-2-Amino-3-hydroxybutyric acid
- D-(+)-Threonine
- D-Threonine (2R,3S)
- D-α-Amino-β-hydroxybutyric acid
- EINECS:211-171-8
- H-D-Thr-OH
;
;
;
;
;
;
;
German:
- D-Threonin
;
Ελληνικά:
- D-θρεονίνη (2R,3S)
;
French:
- D-thréonine (2R,3S)
;
日本語:
- D-トレオニン(2R,3S)
;
HO/`|O|<|wNH2>/<`|wOH>CH3
H3C-<`|HO><|wH>-<`|NH2><|dH>-<//O>OH
`|<`dHO>/<`|wNH2>/O`/|OH
H3C/<`|dOH><|dNH2>/`|O|OH
H3C/<`|dOH><|dNH3^+>/`|O|O^-
6. L-аллотреонин
Брутто-формула:
C4H9NO3
CAS# 28954-12-3
Названия
Русский:
- (2S,3S)-2-амино-3-гидроксибутановая кислота(IUPAC)
- L-аллотреонин
;
;
English:
- (2S,3S)-2-Amino-3-hydroxybutyric acid
- (2S,3S)-2-amino-3-hydroxybutanoic acid(IUPAC)
- EINECS:249-327-2
- H-allo-Thr-OH
- L(+)-allo-Threonine
- L-Allothreonine
- L-allo-Threonine
- L-allo-Threonine (2S,3S)
- allo-threonine
;
;
;
;
;
;
;
;
;
Ελληνικά:
- L-αλλο-θρεονίνη (2S,3S)
;
French:
- L-allo-thréonine (2S,3S)
;
Italiano:
- L-allo-Treonina (2S,3S)
;
日本語:
- L-アロトレオニン(2S,3S)
;
H3C/<`|dOH><|wNH2>/`|O|OH
CH3|<`-HO><_(x.9,d+)H>_(y1.2)<`-H2N><|dH>-<//O>OH
H3C/<`|dOH><|wNH2>/`|O|OH
H3C/<`|dOH><|wNH3^+>/`|O|O^-
`|<`dHO>/<`|dNH2>/O`/|OH
7. D-аллотреонин
Брутто-формула:
C4H9NO3
CAS# 24830-94-2
Названия
Русский:
- (2R,3R)-2-амино-3-гидроксибутановая кислота(IUPAC)
- D-аллотреонин
;
;
English:
- (2R,3R)-2-amino-3-hydroxybutanoic acid(IUPAC)
- D(-)-allo-Threonine
- D-Allothreonine
- D-allo-Threonine
- D-allo-Threonine (2R,3R)
- allo-D-Threonine
;
;
;
;
;
;
German:
- D-allo-Threonin
;
Ελληνικά:
- D-αλλο-θρεονίνη (2R,3R)
;
French:
- D-allo-thréonine (2R,3R)
;
Italiano:
- D-allo-Treonina (2R,3R)
;
日本語:
- D-アロトレオニン(2R,3R)
;
HO/`|O|<|wNH2>/<`|dOH>CH3
H3C/<`|wOH><|dNH2>/`|O|OH
H3C/<`|wOH><|dNH3^+>/`|O|O^-
`|<`wHO>/<`|wNH2>/O`/|OH
8. Ацетоуксусная кислота
Брутто-формула:
C4H6O3
CAS# 4387-93-3
Названия
Русский:
- 3-оксобутановая кислота(IUPAC)
- β-кетомасляная кислота
- Ацетоуксусная кислота [Wiki]
- бета-кетомасляная кислота
;
;
;
;
English:
- 3-Ketobutyric acid
- 3-ketobutyrate
- 3-oxo-butanoic acid
- 3-oxobutanoic acid(IUPAC)
- 3-oxobutyric acid
- Acetoacetic acid [Wiki]
- acetoacetate
- beta-ketobutyric acid
- diacetic acid
- oxobutyrate
;
;
;
;
;
;
;
;
;
;
German:
- 3-Oxobutansäure
- 3-Oxobuttersäure
- Acetessigsäure [Wiki]
;
;
;
Español:
- Ácido 3-oxibutanoico(IUPAC)
- Ácido acetoacético [Wiki]
;
;
French:
- Acide acétylacétique [Wiki]
- acide 3-oxobutanoique(IUPAC)
;
;
Italiano:
- Acido acetoacetico [Wiki]
- acido 3-ossobutanoico(IUPAC)
- acido diacetico
- acido β-chetobutirrico
;
;
;
;
日本語:
- 3-オキソブタン酸(IUPAC)
- アセト酢酸 [Wiki]
;
;
中文:
- 3-丁酮酸
- β-丁酮酸
- 乙酰乙酸 [Wiki]
- 乙酰醋酸
;
;
;
;
CH3-C<`||O>-CH2-C<`||O>-OH
H-C-C<`|O|>-C<`|H><|H>-C<`||O>-O-H; H|#2|H
9. Гамма-аминомасляная кислота
Брутто-формула:
C4H9NO2
CAS# 56-12-2
Названия
Русский:
- 4-аминобутановая кислота(IUPAC)
- γ-aминомасляная кислота
- Аминомасляная кислота
- ГАМК
- Гамма-аминомасляная кислота
;
;
;
;
;
English:
- 3-Carboxypropylamine
- 4-Aminobuttersaure
- 4-aminobutanoic acid(IUPAC)
- 4-aminobutyric acid
- Acide 4-aminobutyrique
- Aminalon
- Butanoic acid, 4-amino-(CAS)
- GABA
- Gaballon
- Gammalon
- Mielogen
- Piperidic acid
- Piperidinic acid
- acido 4-aminobutirico
- gamma-Aminobutyric acid
- γ-Aminobutanoic acid
- γ-Aminobutryic acid
- γ-Aminobutyric acid
- ω-Aminobutyric acid
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
German:
- 4-Aminobutansäure
- 4-Aminobuttersäure
- Piperidinsäure
- γ-Aminobutansäure
- γ-Aminobuttersäure
- γ-Aminobutyrat
;
;
;
;
;
;
Español:
- Ácido 4-aminobutanoico(IUPAC)
- Ácido γ-aminobutírico
;
;
French:
- Acide γ-aminobutyrique
- acide amino-4 butanoïque(IUPAC)
;
;
Italiano:
- Acido γ-amminobutirrico
- acido 4-amminobutanoico(IUPAC)
- acido piperidinico
;
;
;
日本語:
- γ-アミノ酪酸
;
中文:
- γ-氨基丁酸
;
10. изовалериановая кислота
Брутто-формула:
C5H10O2
CAS# 503-74-2
Названия
Русский:
- 3-метилбутановая кислота(IUPAC)
- 3-метилмасляная кислота
- изовалериановая кислота
;
;
;
English:
- 3-Methylbutyrate
- 3-Methylbutyric acid
- 3-methylbutanoic acid(IUPAC) [Wiki]
- Butanoic acid, 3-methyl-(CAS)
- Delphinic acid
- Isopentanoic acid
- Isopropylacetic acid
- beta-Methylbutyric acid
- isovaleric acid
;
;
;
;
;
;
;
;
;
日本語:
- 3-メチルブタン酸(IUPAC) [Wiki]
- イソ吉草酸
;
;
German:
- 3-Methylbutansäure
- 3-Methylbuttersäure
- Delphinsäure
- Isopentansäure
- Isopropylessigsäure
- Isovaleriansäure [Wiki]
;
;
;
;
;
;
French:
- Acide 3-méthylbutanoïque(IUPAC) [Wiki]
- acide iso-butanoïque
- acide isovalérianique
;
;
;
中文:
- 3-甲基丁酸 [Wiki]
;
CH3-CH<|CH3>-CH2-C<//O>OH
11. 2-метилбутановая кислота
Брутто-формула:
C5H10O2
CAS# 116-53-0
Названия
Русский:
- 2-метилбутановая кислота(IUPAC)
- 2-метилмасляная кислота
;
;
English:
- (+/-)-2-Methyl Butyric Acid
- (±)-2-Methylbutyric acid
- 2-Ethylpropanoic acid
- 2-METHYLBUTYRIC ACID
- 2-Methybutyric acid
- 2-Methylbutyrate
- 2-methylbutanoic acid
- Butanoic acid, 2-methyl-
- Butyric acid, 2-methyl-
- DL-2-Methylbutanoic acid
- DL-2-Methylbutyric acid
- DL-α-Methylbutyric acid
- EINECS:204-145-2
- Ethylmethylacetic acid
- METHYL-2-BUTYRIC ACID
- Methylethylacetic acid
- α-Methyl-n-butyric acid
- α-Methylbutyric acid
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
日本語:
- ヒドロアンゲリカ酸 [Wiki]
;
French:
- Acide 2-méthylbutanoïque
;
German:
- 2-Methylbutansäure
;
CH3-CH2-CH<|CH3>-C<//O>OH
12. Гамма-оксимасляная кислота
Брутто-формула:
C4H8O3
CAS# 591-81-1
Названия
Русский:
- 4-гидроксибутановая кислота
- 4-гидроксимасляная кислота
- 4-оксимасляная кислота
- γ-Оксимасляная кислота
- ГОМК
- Гамма-оксимасляная кислота
;
;
;
;
;
;
English:
- 4-Hydroxybutyric acid
- 4-hydroxy-butyric acid
- 4-hydroxybutanoic acid(IUPAC)
- Butanoic acid, 4-hydroxy-
- Butanoic acid,4-hydroxy-(CAS)
- Butyric acid, 4-hydroxy-
- GHB
- Hydroxybutyric acid
- gamma-Hydroxybutyric acid
- γ-Hydroxybutyric acid
;
;
;
;
;
;
;
;
;
;
German:
- 4-Hydroxybutansäure
- 4-Hydroxybuttersäure
- HGHB steht für die freie Säure
- γ-Hydroxybutansäure
- γ-Hydroxybuttersäure
;
;
;
;
;
Español:
- Ácido 4-hidroxibutanoico(IUPAC)
- Ácido γ-hidroxibutírico
;
;
French:
- Acide 4-hydroxybutanoïque(IUPAC)
- Acide gamma-hydroxybutyrique
- gamma-hydroxybutyrate
;
;
;
Italiano:
- 4-idrossibutanoato(IUPAC)
- gamma-idrossibutirrato
- γ-idrossibutirrato
;
;
;
日本語:
- γ-ヒドロキシ酪酸
;
中文:
- γ-羟基丁酸
;
13. 2-оксобутановая кислота
Брутто-формула:
C4H6O3
CAS# 600-18-0
Названия
Русский:
- 2-оксобутановая кислота
;
English:
- 2-Oxobutanoic acid
- 2-ketobutyric acid
- 2-oxobutanoate
- 2-oxobutyrate
- 2-oxobutyric acid
- Butanoic acid, 2-oxo-(CAS)
- Butyric acid, 2-oxo-
- EINECS:209-986-9
- Ketobutyrate
- a-Oxobutyric acid
- a-keto-n-butyric acid
- a-ketobutyric acid
- a-oxo-n-butyric acid
- alpha-Ketobutyric acid [Wiki]
- methyl-Pyruvic acid
- propionyl- Formic acid
- α-oxobutyric acid
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
German:
- 2-Oxobutansäure(IUPAC) [Wiki]
;
French:
- Acide 2-oxobutanoïque(IUPAC)
- Acide alpha-cétobutyrique [Wiki]
- acide 2-cétobutyrique
- acide 2-oxobutyrique
;
;
;
;
日本語:
- 2-オキソブタン酸
- α-ケト酪酸 [Wiki]
;
;
中文:
- α-丁酮酸 [Wiki]
;
14. янтарный полуальдегид
Брутто-формула:
C4H6O3
CAS# 692-29-5
Названия
Русский:
- 4-оксобутановая кислота(IUPAC)
- янтарный полуальдегид
;
;
English:
- 3-Formylpropanoate
- 3-Formylpropanoic acid
- 3-Formylpropionic acid
- 4-Oxobutanoic acid(IUPAC)
- 4-Oxobutyric acid
- Butanoic acid, 4-oxo-(CAS)
- Butryaldehydate
- Butryaldehydic acid
- Butyraldehydic acid
- Propanoic acid,3-formyl-
- Succinaldehydate
- Succinaldehydic acid
- Succinaldehydicacid (6CI,7CI,8CI)
- Succinic acid semialdehyde
- beta-Formylpropionic acid
- gamma-Oxybutyric acid
- succinic semialdehyde
- β-Formylpropionate
- β-formylpropionic acid
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
日本語:
- コハク酸セミアルデヒド
;
15. 2-циано-3-метилбутановая кислота
Брутто-формула:
C6H9NO2
CAS# 22426-27-3
Названия
Русский:
- 2-циано-3-метилбутановая кислота
;
English:
- 2-Cyano-3-methylbutyric acid
- 2-cyano-3-methylbutanoic acid(IUPAC)
- Butanoic acid,2-cyano-3-methyl-(CAS)
- Butyricacid, 2-cyano-3-methyl- (6CI,8CI)
;
;
;
;
HO2C-CH<`|CN>-CH<|CH3>-CH3
16. 2-Бромбутановая кислота
Брутто-формула:
C4H7BrO2
CAS# 80-58-0
Названия
Русский:
- 2-Бромбутановая кислота
- RS-2-бромбутановая кислота
- dl-2-броммасляная кислота
- α-бромбутановая кислота
- Кислота альфа-броммасляная
;
;
;
;
;
English:
- (RS)-2-Bromobutyric acid
- (RS)-a-Bromobutyric acid
- 2-Bromobutanoic acid
- 2-Bromobutyric acid [Wiki]
- 2-bromo-butanoicaci
- Butanoic acid, 2-bromo-
- Butyric acid, 2-bromo-
- Butyric acid, alpha-bromo-
- Butyricacid, 2-bromo- (6CI,7CI,8CI)
- EINECS:201-294-5
- alpha-Bromobytyric acid
- dl-2-Bromobutyric acid
- dl-2-Bromobutyricacid
- α-Bromobutyricacid
;
;
;
;
;
;
;
;
;
;
;
;
;
;
German:
- (RS)-2-Brombuttersäure
- 2-Brombutansäure [Wiki]
- 2-Brombuttersäure
- α-Brombutansäure
;
;
;
;
H-C-C-C-C<//O>OH; H|#2|H; H|#3|H; Br|#4|H
17. (2R)-2-бромбутановая кислота
Брутто-формула:
C4H7BrO2
CAS# 2681-94-9
Названия
Русский:
- (2R)-2-бромбутановая кислота
;
English:
- (2R)-2-bromobutanoic acid(IUPAC)
- (R)-2-BROMOBUTANOICACID
- (R)-2-Bromobutanoic Acid
- (R)-2-Bromobutyric Acid
- (R)-2-Bromobutyricacid
- (R)-α-Bromobutyric acid
- Butanoic acid, 2-bromo-, (2R)-(CAS)
- Butanoicacid, 2-bromo-, (R)-
- Butyric acid, 2-bromo-, D- (8CI)
- D-2-Bromobutanoic acid
- D-2-Bromobutyric acid
;
;
;
;
;
;
;
;
;
;
;
German:
- (R)-2-Brombuttersäure
;
HO2C/<`|dBr><_(y.5,N0)$itemColor1(gray)»R»>{Et}
18. (2S)-2-бромбутановая кислота
Брутто-формула:
C4H7BrO2
CAS# 32659-49-7
Названия
Русский:
- (2S)-2-бромбутановая кислота
;
English:
- (2S)-2-Bromobutanoic acid(IUPAC)
- (S)-2-Bromobutanoicacid
- (S)-2-Bromobutyric acid
- S-2-Bromobutyric acid
;
;
;
;
German:
- (S)-2-Brombuttersäure
;
HO2C/<`|wBr><_(y.5,N0)$itemColor1(gray)»S»>{Et}
CH3`/`<`|Br><`dH>`/|O`|`HO
19. 3-бромбутановая кислота
Брутто-формула:
C4H7BrO2
CAS# 2623-86-1
Названия
Русский:
- 3-бромбутановая кислота
;
English:
- 3-Bromobutyric acid
- 3-bromobutanoic acid(IUPAC)
- Butanoic acid, 3-bromo-(CAS)
- Butyricacid, 3-bromo- (7CI,8CI)
- EINECS:220-082-3
- β-Bromobutyric acid
;
;
;
;
;
;
German:
- 3-Brombutansäure [Wiki]
- 3-Brombuttersäure
;
;
20. 4-бромбутановая кислота
Брутто-формула:
C4H7BrO2
CAS# 2623-87-2
Названия
Русский:
- 4-бромбутановая кислота(IUPAC)
;
English:
- 4-Bromo-n-butyric acid
- 4-Bromobutanoic acid(IUPAC)
- 4-Bromobutyric acid
- 4-Bromobutyricacid
- 4-bromobutanoate
- Butanoic acid, 4-bromo-
- Butyric acid, 4-bromo-
- EINECS:220-083-9
;
;
;
;
;
;
;
;
German:
- 4-Brombutansäure(IUPAC)
;
French:
- Acide 4-bromobutanoïque(IUPAC)
;
Br-C-C-C-C<//O>OH; H|#2|H; H|#3|H; H|#4|H
- Страницы:
- 1
- 2
- Следующая»



