From Wikipedia, the free encyclopedia
|
|

Li+ O2− H+ |
|

|
|
| Names | |
|---|---|
| IUPAC name
Lithium hydroxide |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChEBI |
|
| ChemSpider |
|
| ECHA InfoCard | 100.013.804 |
|
Gmelin Reference |
68415 |
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
| UN number | 2680 |
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
LiOH |
| Molar mass |
|
| Appearance | Hygroscopic white solid |
| Odor | none |
| Density |
|
| Melting point | 462 °C (864 °F; 735 K) |
| Boiling point | 924 °C (1,695 °F; 1,197 K) (decomposes) |
|
Solubility in water |
|
| Solubility in methanol |
|
| Solubility in ethanol |
|
| Solubility in isopropanol |
|
| Acidity (pKa) | 14.4[3] |
| Conjugate base | Lithium monoxide anion |
|
Magnetic susceptibility (χ) |
−12.3·10−6 cm3/mol |
|
Refractive index (nD) |
|
|
Dipole moment |
4.754 D[4] |
| Thermochemistry[5] | |
|
Heat capacity (C) |
49.6 J/(mol·K) |
|
Std molar |
42.8 J/(mol·K) |
|
Std enthalpy of |
−487.5 kJ/mol |
|
Gibbs free energy (ΔfG⦵) |
−441.5 kJ/mol |
|
Enthalpy of fusion (ΔfH⦵fus) |
20.9 kJ/mol (at melting point) |
| Hazards | |
| Occupational safety and health (OHS/OSH): | |
|
Main hazards |
Corrosive |
| NFPA 704 (fire diamond) |
3 0 0 |
| Flash point | Non-flammable |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
210 mg/kg (oral, rat)[6] |
| Safety data sheet (SDS) | «ICSC 0913». «ICSC 0914». (monohydrate) |
| Related compounds | |
|
Other anions |
Lithium amide |
|
Other cations |
|
|
Related compounds |
Lithium oxide |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Lithium hydroxide is an inorganic compound with the formula LiOH. It can exist as anhydrous or hydrated, and both forms are white hygroscopic solids. They are soluble in water and slightly soluble in ethanol. Both are available commercially. While classified as a strong base, lithium hydroxide is the weakest known alkali metal hydroxide.
Production[edit]
The preferred feedstock is hard-rock spodumene, where the lithium content is expressed as % lithium oxide.
Lithium carbonate route[edit]
Lithium hydroxide is often produced industrially from lithium carbonate in a metathesis reaction with calcium hydroxide:[7]
- Li2CO3 + Ca(OH)2 → 2 LiOH + CaCO3
The initially produced hydrate is dehydrated by heating under vacuum up to 180 °C.
Lithium sulfate route[edit]
An alternative route involves the intermediacy of lithium sulfate:[8][9]
- α-spodumene → β-spodumene
- β-spodumene + CaO → Li2O + …
- Li2O + H2SO4 → Li2SO4 + H2O
- Li2SO4 + 2 NaOH → Na2SO4 + 2 LiOH
The main by-products are gypsum and sodium sulphate, which have some market value.
Commercial setting[edit]
According to Bloomberg, Ganfeng Lithium Co. Ltd.[10] (GFL or Ganfeng)[11] and Albemarle were the largest producers in 2020 with around 25kt/y, followed by Livent Corporation (FMC) and SQM.[10] Significant new capacity is planned, to keep pace with demand driven by vehicle electrification. Ganfeng are to expand lithium chemical capacity to 85,000 tons, adding the capacity leased from Jiangte, Ganfeng will become the largest lithium hydroxide producer globally in 2021.[10]
Albemarle’s Kemerton WA plant, originally planned to deliver 100kt/y has been scaled back to 50kt/y.[12]
In 2020 Tianqi Lithium’s, plant in Kwinana, Western Australia is the largest producer, with a capacity of 48kt/y.[13]
Applications[edit]
Lithium ion batteries[edit]
Lithium hydroxide is mainly consumed in the production of cathode materials for lithium ion batteries such as lithium cobalt oxide (LiCoO2) and lithium iron phosphate. It is preferred over lithium carbonate as a precursor for lithium nickel manganese cobalt oxides.[14]
Grease[edit]
A popular lithium grease thickener is lithium 12-hydroxystearate, which produces a general-purpose lubricating grease due to its high resistance to water and usefulness at a range of temperatures.
Carbon dioxide scrubbing[edit]
Lithium hydroxide is used in breathing gas purification systems for spacecraft, submarines, and rebreathers to remove carbon dioxide from exhaled gas by producing lithium carbonate and water:[15]
- 2 LiOH·H2O + CO2 → Li2CO3 + 2 H2O
or
- 2 LiOH + CO2 → Li2CO3 + H2O
The latter, anhydrous hydroxide, is preferred for its lower mass and lesser water production for respirator systems in spacecraft. One gram of anhydrous lithium hydroxide can remove 450 cm3 of carbon dioxide gas. The monohydrate loses its water at 100–110 °C.
Precursor[edit]
Lithium hydroxide, together with lithium carbonate, is a key intermediates used for the production of other lithium compounds, illustrated by its use in the production of lithium fluoride:[7]
- LiOH + HF → LiF + H2O
Other uses[edit]
It is also used in ceramics and some Portland cement formulations, where it is also used to suppress ASR (concrete cancer).[16]
Lithium hydroxide (isotopically enriched in lithium-7) is used to alkalize the reactor coolant in pressurized water reactors for corrosion control.[17]
It is good radiation protection against free neutrons.
Price[edit]
In 2012, the price of lithium hydroxide was about $5-6/kg.[18]
In December 2020 it had risen to $9/kg[19]
On 18 March 2021 the price had risen to US$11.50/kg[20]
See also[edit]
- Soda lime
References[edit]
- ^ Lide, David R., ed. (2006). CRC Handbook of Chemistry and Physics (87th ed.). Boca Raton, FL: CRC Press. ISBN 0-8493-0487-3.
- ^ a b c Khosravi J (2007). Production of Lithium Peroxide and Lithium Oxide in an Alcohol Medium. Chapter 9: Results. ISBN 978-0-494-38597-5.
- ^ Popov K, Lajunen LH, Popov A, Rönkkömäki H, Hannu-Kuure H, Vendilo A (2002). «7Li, 23Na, 39K and 133Cs NMR comparative equilibrium study of alkali metal cation hydroxide complexes in aqueous solutions. First numerical value for CsOH formation». Inorganic Chemistry Communications. 5 (3): 223–225. doi:10.1016/S1387-7003(02)00335-0. Retrieved 21 January 2017.
- ^ CRC handbook of chemistry and physics : a ready-reference book of chemical and physical data. William M. Haynes, David R. Lide, Thomas J. Bruno (2016-2017, 97th ed.). Boca Raton, Florida. 2016. ISBN 978-1-4987-5428-6. OCLC 930681942.
{{cite book}}: CS1 maint: others (link) - ^ CRC handbook of chemistry and physics : a ready-reference book of chemical and physical data. William M. Haynes, David R. Lide, Thomas J. Bruno (2016-2017, 97th ed.). Boca Raton, Florida. 2016. ISBN 978-1-4987-5428-6. OCLC 930681942.
{{cite book}}: CS1 maint: others (link) - ^ Chambers M. «ChemIDplus – 1310-65-2 – WMFOQBRAJBCJND-UHFFFAOYSA-M – Lithium hydroxide anhydrous – Similar structures search, synonyms, formulas, resource links, and other chemical information». chem.sis.nlm.nih.gov. Retrieved 12 April 2018.
- ^ a b Wietelmann U, Bauer RJ (2000). Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a15_393.
- ^ «Proposed Albemarle Plant Site» (PDF). Albemarle. Retrieved 4 December 2020.
- ^ «Corporate presentation» (PDF). Nemaska Lithium. May 2018. Retrieved 5 December 2020.
- ^ a b c «China’s Ganfeng to Be Largest Lithium Hydroxide Producer». BloombergNEF. 10 September 2020. Retrieved 4 December 2020.
- ^ «Ganfeng Lithium Group». Ganfeng Lithium. Retrieved 25 March 2021.
- ^ Stephens, Kate; Lynch, Jacqueline (27 August 2020). «Slowing demand for lithium sees WA’s largest refinery scaled back». www.abc.net.au.
- ^ «Largest of its kind lithium hydroxide plant launched in Kwinana». Government of Western Australia. 10 September 2019. Retrieved 4 December 2020.
- ^ Barrera, Priscilla (27 June 2019). «Will Lithium Hydroxide Really Overtake Lithium Carbonate? | INN». Investing News Network. Retrieved 5 December 2020.
- ^ Jaunsen JR (1989). «The Behavior and Capabilities of Lithium Hydroxide Carbon Dioxide Scrubbers in a Deep Sea Environment». US Naval Academy Technical Report. USNA-TSPR-157. Archived from the original on 2009-08-24. Retrieved 2008-06-17.
{{cite journal}}: CS1 maint: unfit URL (link) - ^ Kawamura M, Fuwa H (2003). «Effects of lithium salts on ASR gel composition and expansion of mortars». Cement and Concrete Research. 33 (6): 913–919. doi:10.1016/S0008-8846(02)01092-X. OSTI 20658311. Retrieved 2022-10-17.
- ^ Managing Critical Isotopes: Stewardship of Lithium-7 Is Needed to Ensure a Stable Supply, GAO-13-716 // U.S. Government Accountability Office, 19 September 2013; pdf
- ^ «Lithium Prices 2012». investingnews.com. Investing News Network. 14 June 2012. Archived from the original on 11 March 2018. Retrieved 12 April 2018.
- ^ «London Metal Exchange: Lithium prices». London metal exchange. Retrieved 4 December 2020.
- ^ «LITHIUM AT THE LME». LME The London Metal Exchange. 18 March 2021. Retrieved 22 March 2021.
External links[edit]
- International Chemical Safety Card 0913 (anhydrous)
- International Chemical Safety Card 0914 (monohydrate)
From Wikipedia, the free encyclopedia

|
|

Li+ O2− H+ |
|

|
|
| Names | |
|---|---|
| IUPAC name
Lithium hydroxide |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChEBI |
|
| ChemSpider |
|
| ECHA InfoCard | 100.013.804 |
|
Gmelin Reference |
68415 |
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
| UN number | 2680 |
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
LiOH |
| Molar mass |
|
| Appearance | Hygroscopic white solid |
| Odor | none |
| Density |
|
| Melting point | 462 °C (864 °F; 735 K) |
| Boiling point | 924 °C (1,695 °F; 1,197 K) (decomposes) |
|
Solubility in water |
|
| Solubility in methanol |
|
| Solubility in ethanol |
|
| Solubility in isopropanol |
|
| Acidity (pKa) | 14.4[3] |
| Conjugate base | Lithium monoxide anion |
|
Magnetic susceptibility (χ) |
−12.3·10−6 cm3/mol |
|
Refractive index (nD) |
|
|
Dipole moment |
4.754 D[4] |
| Thermochemistry[5] | |
|
Heat capacity (C) |
49.6 J/(mol·K) |
|
Std molar |
42.8 J/(mol·K) |
|
Std enthalpy of |
−487.5 kJ/mol |
|
Gibbs free energy (ΔfG⦵) |
−441.5 kJ/mol |
|
Enthalpy of fusion (ΔfH⦵fus) |
20.9 kJ/mol (at melting point) |
| Hazards | |
| Occupational safety and health (OHS/OSH): | |
|
Main hazards |
Corrosive |
| NFPA 704 (fire diamond) |
3 0 0 |
| Flash point | Non-flammable |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
210 mg/kg (oral, rat)[6] |
| Safety data sheet (SDS) | «ICSC 0913». «ICSC 0914». (monohydrate) |
| Related compounds | |
|
Other anions |
Lithium amide |
|
Other cations |
|
|
Related compounds |
Lithium oxide |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Lithium hydroxide is an inorganic compound with the formula LiOH. It can exist as anhydrous or hydrated, and both forms are white hygroscopic solids. They are soluble in water and slightly soluble in ethanol. Both are available commercially. While classified as a strong base, lithium hydroxide is the weakest known alkali metal hydroxide.
Production[edit]
The preferred feedstock is hard-rock spodumene, where the lithium content is expressed as % lithium oxide.
Lithium carbonate route[edit]
Lithium hydroxide is often produced industrially from lithium carbonate in a metathesis reaction with calcium hydroxide:[7]
- Li2CO3 + Ca(OH)2 → 2 LiOH + CaCO3
The initially produced hydrate is dehydrated by heating under vacuum up to 180 °C.
Lithium sulfate route[edit]
An alternative route involves the intermediacy of lithium sulfate:[8][9]
- α-spodumene → β-spodumene
- β-spodumene + CaO → Li2O + …
- Li2O + H2SO4 → Li2SO4 + H2O
- Li2SO4 + 2 NaOH → Na2SO4 + 2 LiOH
The main by-products are gypsum and sodium sulphate, which have some market value.
Commercial setting[edit]
According to Bloomberg, Ganfeng Lithium Co. Ltd.[10] (GFL or Ganfeng)[11] and Albemarle were the largest producers in 2020 with around 25kt/y, followed by Livent Corporation (FMC) and SQM.[10] Significant new capacity is planned, to keep pace with demand driven by vehicle electrification. Ganfeng are to expand lithium chemical capacity to 85,000 tons, adding the capacity leased from Jiangte, Ganfeng will become the largest lithium hydroxide producer globally in 2021.[10]
Albemarle’s Kemerton WA plant, originally planned to deliver 100kt/y has been scaled back to 50kt/y.[12]
In 2020 Tianqi Lithium’s, plant in Kwinana, Western Australia is the largest producer, with a capacity of 48kt/y.[13]
Applications[edit]
Lithium ion batteries[edit]
Lithium hydroxide is mainly consumed in the production of cathode materials for lithium ion batteries such as lithium cobalt oxide (LiCoO2) and lithium iron phosphate. It is preferred over lithium carbonate as a precursor for lithium nickel manganese cobalt oxides.[14]
Grease[edit]
A popular lithium grease thickener is lithium 12-hydroxystearate, which produces a general-purpose lubricating grease due to its high resistance to water and usefulness at a range of temperatures.
Carbon dioxide scrubbing[edit]
Lithium hydroxide is used in breathing gas purification systems for spacecraft, submarines, and rebreathers to remove carbon dioxide from exhaled gas by producing lithium carbonate and water:[15]
- 2 LiOH·H2O + CO2 → Li2CO3 + 2 H2O
or
- 2 LiOH + CO2 → Li2CO3 + H2O
The latter, anhydrous hydroxide, is preferred for its lower mass and lesser water production for respirator systems in spacecraft. One gram of anhydrous lithium hydroxide can remove 450 cm3 of carbon dioxide gas. The monohydrate loses its water at 100–110 °C.
Precursor[edit]
Lithium hydroxide, together with lithium carbonate, is a key intermediates used for the production of other lithium compounds, illustrated by its use in the production of lithium fluoride:[7]
- LiOH + HF → LiF + H2O
Other uses[edit]
It is also used in ceramics and some Portland cement formulations, where it is also used to suppress ASR (concrete cancer).[16]
Lithium hydroxide (isotopically enriched in lithium-7) is used to alkalize the reactor coolant in pressurized water reactors for corrosion control.[17]
It is good radiation protection against free neutrons.
Price[edit]
In 2012, the price of lithium hydroxide was about $5-6/kg.[18]
In December 2020 it had risen to $9/kg[19]
On 18 March 2021 the price had risen to US$11.50/kg[20]
See also[edit]
- Soda lime
References[edit]
- ^ Lide, David R., ed. (2006). CRC Handbook of Chemistry and Physics (87th ed.). Boca Raton, FL: CRC Press. ISBN 0-8493-0487-3.
- ^ a b c Khosravi J (2007). Production of Lithium Peroxide and Lithium Oxide in an Alcohol Medium. Chapter 9: Results. ISBN 978-0-494-38597-5.
- ^ Popov K, Lajunen LH, Popov A, Rönkkömäki H, Hannu-Kuure H, Vendilo A (2002). «7Li, 23Na, 39K and 133Cs NMR comparative equilibrium study of alkali metal cation hydroxide complexes in aqueous solutions. First numerical value for CsOH formation». Inorganic Chemistry Communications. 5 (3): 223–225. doi:10.1016/S1387-7003(02)00335-0. Retrieved 21 January 2017.
- ^ CRC handbook of chemistry and physics : a ready-reference book of chemical and physical data. William M. Haynes, David R. Lide, Thomas J. Bruno (2016-2017, 97th ed.). Boca Raton, Florida. 2016. ISBN 978-1-4987-5428-6. OCLC 930681942.
{{cite book}}: CS1 maint: others (link) - ^ CRC handbook of chemistry and physics : a ready-reference book of chemical and physical data. William M. Haynes, David R. Lide, Thomas J. Bruno (2016-2017, 97th ed.). Boca Raton, Florida. 2016. ISBN 978-1-4987-5428-6. OCLC 930681942.
{{cite book}}: CS1 maint: others (link) - ^ Chambers M. «ChemIDplus – 1310-65-2 – WMFOQBRAJBCJND-UHFFFAOYSA-M – Lithium hydroxide anhydrous – Similar structures search, synonyms, formulas, resource links, and other chemical information». chem.sis.nlm.nih.gov. Retrieved 12 April 2018.
- ^ a b Wietelmann U, Bauer RJ (2000). Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a15_393.
- ^ «Proposed Albemarle Plant Site» (PDF). Albemarle. Retrieved 4 December 2020.
- ^ «Corporate presentation» (PDF). Nemaska Lithium. May 2018. Retrieved 5 December 2020.
- ^ a b c «China’s Ganfeng to Be Largest Lithium Hydroxide Producer». BloombergNEF. 10 September 2020. Retrieved 4 December 2020.
- ^ «Ganfeng Lithium Group». Ganfeng Lithium. Retrieved 25 March 2021.
- ^ Stephens, Kate; Lynch, Jacqueline (27 August 2020). «Slowing demand for lithium sees WA’s largest refinery scaled back». www.abc.net.au.
- ^ «Largest of its kind lithium hydroxide plant launched in Kwinana». Government of Western Australia. 10 September 2019. Retrieved 4 December 2020.
- ^ Barrera, Priscilla (27 June 2019). «Will Lithium Hydroxide Really Overtake Lithium Carbonate? | INN». Investing News Network. Retrieved 5 December 2020.
- ^ Jaunsen JR (1989). «The Behavior and Capabilities of Lithium Hydroxide Carbon Dioxide Scrubbers in a Deep Sea Environment». US Naval Academy Technical Report. USNA-TSPR-157. Archived from the original on 2009-08-24. Retrieved 2008-06-17.
{{cite journal}}: CS1 maint: unfit URL (link) - ^ Kawamura M, Fuwa H (2003). «Effects of lithium salts on ASR gel composition and expansion of mortars». Cement and Concrete Research. 33 (6): 913–919. doi:10.1016/S0008-8846(02)01092-X. OSTI 20658311. Retrieved 2022-10-17.
- ^ Managing Critical Isotopes: Stewardship of Lithium-7 Is Needed to Ensure a Stable Supply, GAO-13-716 // U.S. Government Accountability Office, 19 September 2013; pdf
- ^ «Lithium Prices 2012». investingnews.com. Investing News Network. 14 June 2012. Archived from the original on 11 March 2018. Retrieved 12 April 2018.
- ^ «London Metal Exchange: Lithium prices». London metal exchange. Retrieved 4 December 2020.
- ^ «LITHIUM AT THE LME». LME The London Metal Exchange. 18 March 2021. Retrieved 22 March 2021.
External links[edit]
- International Chemical Safety Card 0913 (anhydrous)
- International Chemical Safety Card 0914 (monohydrate)
Морфемный разбор слова:
Однокоренные слова к слову:
Гидроксид лития: способы получения и химические свойства
Гидроксид лития при стандартных условиях представляет собой бесцветные кристаллы. Растворяется в воде.
Относительная молекулярная масса Mr = 23, 95; относительная плотность для тв. и ж. состояния d = 1, 46; tпл = 471◦ C;
Способы получения
1. Гидроксид лития получают электролизом раствора хлорида лития :
2LiCl + 2H2O → 2LiOH + H2 + Cl2
2. При взаимодействии лития, оксида лития, гидрида лития и пероксида лития с водой также образуется гидроксид лития:
2Li + 2H2O → 2LiOH + H2
Li2O + H2O → 2LiOH
2LiH + 2H2O → 2LiOH + H2
3. Карбонат лития при взаимодействии с гидроксидом кальция образует гидроксид лития:
Качественная реакция
Химические свойства
1. Гидроксид лития реагируют со всеми кислотами (и сильными, и слабыми, и растворимыми, и нерастворимыми). При этом образуются средние или кислые соли, в зависимости от соотношения реагентов:
в растворе образуется комплексная соль — тетрагидроксоалюминат:
4. С кислыми солями гидроксид лития также может взаимодействовать. При этом образуются средние соли, или менее кислые соли:
5. Гидроксид лития взаимодействует с простыми веществами-неметаллами (кроме инертных газов, азота, кислорода, водорода и углерода).
При этом кремний окисляется до силиката и водорода:
Фтор окисляет щелочь. При этом выделяется молекулярный кислород:
Другие галогены, сера и фосфор — диспропорционируют в растворе гидроксида лития:
Сера взаимодействует с гидроксидом лития только при нагревании:
В растворе образуются комплексная соль и водород:
2LiOH + 2Al + 6Н2О = 2Li[Al(OH)4] + 3Н2
Хлорид меди (II) реагирует с гидроксидом лития с образованием хлорида лития и осадка гидроксида меди (II):
2LiOH + CuCl2 = Cu(OH)2↓+ 2LiCl
NH4Cl + LiOH = NH3 + H2O + LiCl
8. Гидроксид лития разлагается при нагревании до температуры 600°С:
2LiOH → Li2O + H2O
LiOH ↔ Li + + OH —
4LiOH → 4Li + O2 + 2H2O
Источник
Гидроксид лития
| Гидроксид лития | |
 |
|
 |
|
| Общие | |
|---|---|
| Систематическое наименование | Гидроксид лития |
| Химическая формула | LiOH |
| Эмпирическая формула | LiOH |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Молярная масса | 23,94637 г/моль |
| Плотность | 1,46 (25 °C) г/см³ |
| Термические свойства | |
| Температура плавления | 462 [1] °C |
| Температура кипения | 925 [1] °C |
| Температура разложения | 930 [1] °C |
| Энтальпия образования (ст. усл.) | -487,2 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 12,7 (0 °C) г/100 мл |
| Классификация | |
| Рег. номер CAS | 1310-65-2 |
| RTECS | OJ6307070 |
Гидроксид лития — неорганическое основание щелочного металла лития, имеющее формулу LiOH.
Содержание
Описание
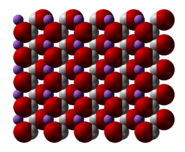
Гидроксид лития при стандартных условиях представляет собой бесцветные кристаллы с тетрагональной решёткой. [2] При работе с ним необходимо проявлять осторожность, избегать попадания на кожу и слизистые оболочки.
Получение
Химические свойства
Применение
Гидроксид лития используют для получения солей лития; как компонент электролитов в щелочных аккумуляторах и поглотитель углекислого газа в противогазах, подводных лодках и космических кораблях. Он также используется как катализатор полимеризации. Применяется в стекольной и керамической промышленности. При производстве водоупорных смазочных материалов, обладающих механической стабильностью в широком диапазоне температур.
Примечания
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | Н | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Гидроксид лития» в других словарях:
Гидроксид алюминия — Гидроксид алюминия, вещество с формулой (а также … Википедия
Гидроксид калия — Гидроксид калия … Википедия
Гидроксид железа(II) — У этого термина существуют и другие значения, см. Гидроксиды железа. Гидроксид железа(II) … Википедия
Гидроксид хрома(II) — Общие Систематическое наименование Гидроксид хрома(II) Традиционные названия гидроокись хрома Химическая формула Сr(OH)2 Физические свойства … Википедия
Гидроксид хрома(III) — Гидроксид хрома (III) сложное неорганическое вещество с химической формулой Cr(OH)3. Описание Гидроксид хрома (III) амфотерный гидроксид. Серо зеленого цвета, разлагается при нагревании, теряя воду и образуя зеленый метагидроксид CrO(OH). Не… … Википедия
Гидроксид марганца(II) — Общие Систематическое наименование Гидроксид марганца(II) Традиционные названия Гидроокись марганца Химическая формула Mn(OH)2 Физические свойства … Википедия
ЛИТИЯ ГИДРОКСИД — LiOH, сильное основание (щелочь). Бесцветные кристаллы. Хорошо растворим в воде. Применяют: в щелочных аккумуляторах, для получения смазок; соединения лития, как поглотитель CO2 в противогазах, подводных лодках, самолетах и космических кораблях … Большой Энциклопедический словарь
лития гидроксид — LiOH, сильное основание (щёлочь). Бесцветные кристаллы. Хорошо растворим в воде. Применяют в щелочных аккумуляторах, для получения смазок, соединения лития, как поглотитель CO2 в противогазах, подводных лодках, самолётах и космических кораблях. * … Энциклопедический словарь
ЛИТИЯ ГИДРОКСИД — LiOH, бесцв. кристаллы с тетрагон, решеткой ( а =0,3549 нм, с= 6,4334 нм, z = 2, пространств. группа Р4/ птт); т. пл. 473 °С, при более высокой т ре испаряется и частично диссоциирует на Li2O и Н 2 О; в парах при 820 870 °С содержится 90% … Химическая энциклопедия
ЛИТИЯ ГИДРОКСИД — LiOH, сильное основание (щёлочь). Бесцв. кристаллы. Хорошо растворим в воде. Применяют в щелочных аккумуляторах, для получения смазок, соед. лития, как поглотитель СО2 в противогазах, подводных лодках, самолётах и космич. кораблях … Естествознание. Энциклопедический словарь
Источник
Гидроксид лития (LiOH) формула, свойства, риски и применение
гидроксид лития представляет собой химическое соединение формулы LiOH (EMBL-EBI, 2008). Гидроксид лития является основным неорганическим соединением. Это используется в значительной степени в органическом синтезе, чтобы продвинуть реакцию из-за ее сильной основности.
Гидроксид лития не встречается в природе свободно. Он очень реактивный, и если бы он был в природе, он мог бы легко реагировать с образованием других соединений. Однако некоторые минералы лития / алюминия, которые образуют различные смеси, могут быть найдены в различных минералах..
С этого момента индустрия атомной энергетики США начала использовать большое количество гидроксида лития, что привело к неожиданному развитию литиевой промышленности (Lithium hydroxide, 2016).
Большая часть гидроксида лития образуется в результате реакции между карбонатом лития и гидроксидом кальция (формула гидроксида лития, S.F.). Эта реакция дает гидроксид лития, а также карбонат кальция:
Его также готовят из реакции оксида лития и воды:
Гидроксид лития использовался в качестве абсорбента углекислого газа на подводной лодке и надувном источнике армейского воздушного шара в 1944 году..
Физико-химические свойства
В водном растворе он образует кристаллическую жидкость с едким ароматом. Его молекулярная масса составляет 23,91 г / моль. Он существует в двух формах: безводный и моногидрат LiOH.H2O, который имеет молекулярную массу 41,96 г / мес. Соединение имеет плотность 1,46 г / мл для безводной формы и 1,51 г / мл для моногидратированной формы..
Его температуры плавления и кипения составляют 462 ° C и 924 ° C соответственно. Гидроксид лития является единственным щелочным гидроксидом, который не имеет полиморфизма, а его сеть имеет тетрагональную структуру. Это соединение очень хорошо растворяется в воде и слабо растворяется в этаноле (Royal Society of Chemistry, 2015).
Гидроксид лития и другие щелочные гидроксиды (NaOH, KOH, RbOH и CsOH) очень универсальны для использования в органическом синтезе, потому что они являются более сильными основаниями, которые легко реагируют.
Может реагировать с водой и углекислым газом при комнатной температуре. Он также может реагировать со многими металлами, такими как Ag, Au, Cu и Pt, поэтому он является важным исходным материалом в металлоорганическом синтезе..
Растворы гидроксида лития экзотермически нейтрализуют кислоты с образованием солей и воды. Они реагируют с определенными металлами (такими как алюминий и цинк) с образованием оксидов или гидроксидов металлов и образуют газообразный водород. Они могут инициировать реакции полимеризации в полимеризуемых органических соединениях, особенно эпоксидах..
Он может генерировать легковоспламеняющиеся и / или токсичные газы с солями аммония, нитридами, галогенированными органическими соединениями, различными металлами, пероксидами и гидропероксидами. Может служить катализатором.
Реагирует при нагревании выше примерно 84 ° C с водными растворами редуцирующих сахаров, кроме сахарозы, с образованием токсичных уровней окиси углерода (CAMEO, 2016).
Реактивность и опасности
Гидроксид лития является стабильным соединением, хотя он несовместим с сильными кислотами, углекислым газом и влагой. Вещество разлагается при разогреве (924 ° C) с образованием токсичных паров.
Раствор в воде является сильной основой, бурно реагирует с кислотой и вызывает коррозию алюминия и цинка. Реагирует с окислителями.
Это вещество вызывает коррозию глаз, кожи, дыхательных путей и проглатывания. Вдыхание вещества может вызвать отек легких.
Симптомы отека легких часто проявляются только через несколько часов и усиливаются при физической нагрузке. Воздействие может привести к смерти. Последствия могут быть отсрочены (Национальный институт безопасности и гигиены труда, 2015 г.).
Если соединение попало в глаза, контактные линзы должны быть проверены и удалены. Глаза следует немедленно промыть большим количеством воды в течение не менее 15 минут холодной водой.
При попадании на кожу пораженный участок следует немедленно промыть в течение не менее 15 минут большим количеством воды или слабой кислоты, например, уксуса, при снятии загрязненной одежды и обуви..
Покройте раздраженную кожу смягчающим средством. Стирайте одежду и обувь перед тем, как использовать их снова. Если контакт сильный, промойте дезинфицирующим мылом и покройте кожу, загрязненную антибактериальным кремом.
В случае вдыхания пострадавшего следует перенести в прохладное место. Если вы не дышите, вам дадут искусственное дыхание. Если дыхание затруднено, обеспечьте кислород.
При проглатывании соединения не следует вызывать рвоту. Ослабьте тесную одежду, такую как воротник рубашки, ремень или галстук.
Во всех случаях требуется немедленная медицинская помощь (паспорт безопасности материала Гидроксид лития, 21).
приложений
Гидроксид лития используется при производстве литиевых солей (мыл) стеариновой кислоты и других жирных кислот.
Эти мыла широко используются в качестве загустителей в консистентных смазках для улучшения термостойкости, водостойкости, стабильности и механических свойств. Жировые добавки можно использовать в подшипниках автомобиля, самолета, крана и т. Д..
Обожженный твердый гидроксид лития может использоваться в качестве поглотителя углекислого газа для членов экипажа космического корабля и подводной лодки..
Космический аппарат проектов НАСА «Меркурий», «Джеминни» и «Аполлон» использовал гидроксид лития в качестве абсорбентов. Он имеет надежную производительность и может легко поглощать углекислый газ из водяного пара. Химическая реакция:
1 г безводного гидроксида лития может абсорбировать диоксид углерода объемом 450 мл. Только 750 г безводного гидроксида лития может поглощать выдыхаемый углекислый газ одним человеком каждый день.
Гидроксид лития и другие соединения лития недавно использовались для разработки и исследования щелочных батарей (ENCYCLOPÆDIA BRITANNICA, 2013).
Источник
Гидроксид лития, характеристика, свойства и получение, химические реакции
Гидроксид лития, характеристика, свойства и получение, химические реакции.
Гидроксид лития – неорганическое вещество, имеет химическую формулу LiOH.
Краткая характеристика гидроксида лития:
Гидроксид лития – неорганическое вещество белого цвета.
Химическая формула гидроксида лития LiOH.
Не растворяется в этаноле.
На воздухе гидрооксид лития поглощает углекислый газ и образует карбонат лития, токсичность которого определяется наличием лития.
Гидроксид лития – едкое, токсическое и коррозионно-активное вещество. Оно относится к веществам первого класса опасности. Поэтому при работе с ним требуется соблюдать осторожность. При попадании на кожу, слизистые оболочки и в глаза образуются серьёзные химические ожоги.
Гидрооксид лития пожаро- и взрывобезопасен.
Является сильным основанием, но наиболее слабым основанием среди щелочных металлов.
Физические свойства гидроксида лития:
| Наименование параметра: | Значение: |
| Химическая формула | LiOН |
| Синонимы и названия иностранном языке | lithium hydroxide (англ.) |
литиевый щелок (рус.)
гидрат окиси лития (рус.)
едкий литий (рус.) Тип вещества неорганическое Внешний вид бесцветные тетрагональные кристаллы Цвет белый, бесцветный Вкус —* Запах без запаха Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) твердое вещество Плотность (состояние вещества – твердое вещество, при 25 °C), кг/м 3 1460 Плотность (состояние вещества – твердое вещество, при 25 °C), г/см 3 1,46 Температура кипения, °C 925 Температура плавления, °C 462 Температура разложения, °C 930 Гигроскопичность гигроскопичен Молярная масса, г/моль 23,94637
Получение гидроксида лития:
Гидроксид лития получается в результате следующих химических реакций:
– путем взаимодействия металлического лития с водой:
– путем взаимодействия оксида лития с водой:
– путем взаимодействия карбоната лития с гидроксидом кальция:
Li2CO3 + Ca(OH)2 → 2LiOH + CaCO3 (t Химические свойства гидроксида лития. Химические реакции гидроксида лития:
Гидроксид лития – химически активное вещество, сильное химическое основание.
Водные растворы LiOH имеют сильную щелочную реакцию.
Химические свойства гидроксида лития аналогичны свойствам гидроксидов других щелочных металлов. Поэтому для него характерны следующие химические реакции:
1. реакция гидроксида лития с хлором:
2LiOH + Cl2 → LiClO + LiCl + H2O.
В результате реакции образуются хлорид лития, гипохлорит лития и вода. При этом гидроксид лития в качестве исходного вещества используется в виде холодного концентрированного раствора.
2. реакция гидроксида лития с серой:
В результате реакции образуются сульфид лития, сероводород и оксид серы.
3. реакция гидроксида лития с йодом:
В результате реакции образуются йодид лития, иодат лития и вода.
4. реакция гидроксида лития с цинком и водой:
5. реакция гидроксида лития с ортофосфорной кислотой:
6. реакция гидроксида лития с азотной кислотой:
Аналогично проходят реакции гидроксида лития и с другими кислотами.
7. реакция гидроксида лития с сероводородом:
В результате реакции образуются сульфид лития и вода.
8. реакция гидроксида лития с фтороводородом:
HF + LiOH → LiF + H2O.
В результате реакции образуются фторид лития и вода.
9. реакция гидроксида лития с бромоводородом:
HBr + LiOH → LiBr + H2O.
В результате реакции образуются бромид лития и вода.
10. реакция гидроксида лития с йодоводородом:
HI + LiOH → LiI + H2O.
В результате реакции образуются йодид лития и вода.
11. реакция гидроксида лития с оксидом алюминия:
Оксид алюминия является амфотерным оксидом. В результате реакции образуются алюминат лития и вода.
12. реакция гидроксида лития с оксидом углерода ( углекислым газом ):
Оксид углерода является кислотным оксидом. В результате реакции образуются карбонат лития и вода. В ходе реакции используется концентрированный раствор гидроксида лития. Реакция протекает при комнатной температуре.
Также данная реакция протекает на воздухе. Гидрооксид лития поглощает углекислый газ и образуется карбонат лития.
13. реакция гидроксида лития с оксидом серы (IV):
Оксид серы (IV) является кислотным оксидом. В результате реакции образуются сульфит лития и вода. В ходе реакции используется насыщенный раствор гидроксида лития.
14. реакция гидроксида лития с оксидом серы (VI):
Оксид серы (VI) является кислотным оксидом. В результате реакции образуются сульфат лития и вода.
15. реакция гидроксида лития с оксидом кремния:
В результате реакции образуются ортосиликат лития и вода. В ходе реакции используется разбавленный раствор гидроксида лития. Реакция протекает при комнатной температуре.
16. реакция гидроксида лития с гидроксидом цинка:
Гидроксид цинка является амфотерным основанием. В результате реакции образуется тетрагидроксоцинкат лития.
17. реакция гидроксида лития с сульфатом железа:
В результате реакции образуются гидроксид железа и сульфат лития.
18. реакция гидроксида лития с хлоридом железа:
В результате реакции образуются гидроксид железа и хлорид лития.
19. реакция гидроксида лития с нитратом цинка:
В результате реакции образуются гидроксид цинка и нитрат лития.
20. реакция гидроксида лития с хлоридом меди:
В результате реакции образуются гидроксид меди и хлорид лития.
Аналогично проходят реакции гидроксида лития и с другими солями.
21. реакция термического разложения гидроксида лития:
Применение и использование гидроксида лития:
Гидроксид лития используется во множестве отраслей промышленности и для бытовых нужд:
– в химической промышленности для получения солей лития;
– как компонент электролитов в щелочных аккумуляторах,
– как поглотитель углекислого газа в противогазах, подводных лодках и космических кораблях,
– в химической промышленности как катализатор полимеризации,
– в стекольной и керамической промышленности;
– при производстве водоупорных смазочных материалов, обладающих механической стабильностью в широком диапазоне температур.
Примечание: © Фото //www.pexels.com, //pixabay.com

гидроксид лития реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие гидроксида лития
реакции
Источник
Теперь вы знаете какие однокоренные слова подходят к слову Как пишется гидроксид лития, а так же какой у него корень, приставка, суффикс и окончание. Вы можете дополнить список однокоренных слов к слову «Как пишется гидроксид лития», предложив свой вариант в комментариях ниже, а также выразить свое несогласие проведенным с морфемным разбором.
LiOH, бесцв. Кристаллы с тетрагон, решеткой ( а =0,3549 нм, с= 6,4334 нм, z = 2, пространств. Группа Р4/ птт). Т. Пл. 473 °С, при более высокой т-ре испаряется и частично диссоциирует на Li2O и Н 2 О. В парах при 820-870 °С содержится 90% (LiOH)2. Плотн. 1,44г/см 3. С 0p.>49,58 Дж/(моль. К). DH0 пл 20,9 кДж/моль, DH0 обр -484,90 кДж/моль. S029842,76 Дж/(моль. К). Образует моногидрат-бесцв. Кристаллы с моноклинной решеткой (а= 0,737 нм, b= 0,826 нм, с= 0,319 нм, b = 110°, z = 4, пространств. Группа С2/m). Плотн. 1,51 г/см 3. C0p 79,5 Дж/(моль. К). DH0 обр -788,3 кДж/моль. S029871,4 Дж/(моль. К). Обезвоживание наблюдается уже при 40 °С (давление пара 20,66 гПа), полностью теряет воду при 108,9°С. Р-римостъ LiOH в воде меньше, чем гидроксидов др.
Щелочных металлов, и составляет (г в 100 г Н 2 О). 10,90 при 0°С, 12,48 при 25 °С, 13,02 при 50 °С, 17,55 при 100°С Т. Пл. Эвтектич. Системы LiOH-H2O (10,5% по массе LiOH) Ч 18,2°С. DH0 растворения для бесконечно разб. Р-ра Ч 23,58 кДж/моль. Плохо раств. В этаноле. Л. Г. — сильное основание (щелочь). С NaOH и КОН образует твердые р-ры и двойные гидроксиды (напр., LiOH.NaOH), с RbOH — соед. 3LiOH.RbOH, с Н 2 О 2 — пероксиды Li2O2.Н 2 О 2.пН 2 О ( п =2 или 3), Li2O2.2Н 2 О 2. Расплавы LiOH и его водные р-ры разрушают стекло, фарфор, взаимод. Со мн. Силикатами, подвергают коррозии в присут. Кислорода Fe, Pt, монель-металл. К действию Л. Г. Устойчивы Ni, Ag и Au. Получают Л. Г. Взаимод. Li, Li2O и LiH с Н 2 О в атмосфере Аr или Н 2.
Обменной р-цией в водных р-рах Li2SO4 с КОН, Са(ОН)2 или Ва(ОН)2 в инертной атмосфере. В пром-сти -электролизом LiCl с движущимся ртутным катодом или методом каустификации нагретой до кипения водной суспензии Li2CO3 гидроксидом Са. Li2CO3 + Са(ОН)2 D2LiOH + СаСО 3. Л. Г. — добавка к электролиту щелочных аккумуляторов. Реагент для получения соед. Li, в частности олеатор, стеаратов и пальмитатов. Поглотитель СО 2 в противогазах, подводных лодках, самолетах и космич. Кораблях. Лит. Иткина Л. С. Гидроксиды лития, рубидия и цезия, М., 1973. См. Также лит. При ст. Литий. Б. Д. Cmenuн..
На нашем сайте Вы найдете значение «Лития Гидроксид» в словаре Химическая энциклопедия, подробное описание, примеры использования, словосочетания с выражением Лития Гидроксид, различные варианты толкований, скрытый смысл.
Первая буква «Л». Общая длина 15 символа
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 7 октября 2021 года; проверки требуют 5 правок.
Гидроксид лития, характеристика, свойства и получение, химические реакции.
Гидроксид лития – неорганическое вещество, имеет химическую формулу LiOH.
Краткая характеристика гидроксида лития
Физические свойства гидроксида лития
Получение гидроксида лития
Химические свойства гидроксида лития
Химические реакции гидроксида лития
Применение и использование гидроксида лития
Краткая характеристика гидроксида лития:
Гидроксид лития – неорганическое вещество белого цвета.
Химическая формула гидроксида лития LiOH.
Хорошо растворяется в воде, при этом выделяя тепловую энергию. Его растворимость в воде составляет 12,7 г/100 см3 при 25 °C. Растворимость с повышением температуры увеличивается и он полностью диссоциирует на оксид лития и воду при температуре 1000 °С.
Не растворяется в этаноле.
На воздухе гидрооксид лития поглощает углекислый газ и образует карбонат лития, токсичность которого определяется наличием лития.
Гидроксид лития – едкое, токсическое и коррозионно-активное вещество. Оно относится к веществам первого класса опасности. Поэтому при работе с ним требуется соблюдать осторожность. При попадании на кожу, слизистые оболочки и в глаза образуются серьёзные химические ожоги.
Гидрооксид лития пожаро- и взрывобезопасен.
Является сильным основанием, но наиболее слабым основанием среди щелочных металлов.
Физические свойства гидроксида лития:
| Наименование параметра: | Значение: |
| Химическая формула | LiOН |
| Синонимы и названия иностранном языке | lithium hydroxide (англ.)
литиевый щелок (рус.) гидрат окиси лития (рус.) едкий литий (рус.) |
| Тип вещества | неорганическое |
| Внешний вид | бесцветные тетрагональные кристаллы |
| Цвет | белый, бесцветный |
| Вкус | —* |
| Запах | без запаха |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность (состояние вещества – твердое вещество, при 25 °C), кг/м3 | 1460 |
| Плотность (состояние вещества – твердое вещество, при 25 °C), г/см3 | 1,46 |
| Температура кипения, °C | 925 |
| Температура плавления, °C | 462 |
| Температура разложения, °C | 930 |
| Гигроскопичность | гигроскопичен |
| Молярная масса, г/моль | 23,94637 |
* Примечание:
— нет данных.
Получение гидроксида лития:
Гидроксид лития получается в результате следующих химических реакций:
– путем взаимодействия металлического лития с водой:
2Li + 2H2O → 2LiOH + H2.
– путем взаимодействия оксида лития с водой:
Li2O + H2O → 2LiOH.
– путем взаимодействия карбоната лития с гидроксидом кальция:
Li2CO3 + Ca(OH)2 → 2LiOH + CaCO3 (t < 600°C).
Реакция протекает при нагревании до температуры не более 600°C.
– обменными реакциями солей лития с гидроксидами других металлов:
Li2SO4 + Ba(OH)2 → 2LiOH + BaSO4.
Химические свойства гидроксида лития. Химические реакции гидроксида лития:
Гидроксид лития – химически активное вещество, сильное химическое основание.
Водные растворы LiOH имеют сильную щелочную реакцию.
Химические свойства гидроксида лития аналогичны свойствам гидроксидов других щелочных металлов. Поэтому для него характерны следующие химические реакции:
1. реакция гидроксида лития с хлором:
2LiOH + Cl2 → LiClO + LiCl + H2O.
В результате реакции образуются хлорид лития, гипохлорит лития и вода. При этом гидроксид лития в качестве исходного вещества используется в виде холодного концентрированного раствора.
2. реакция гидроксида лития с серой:
2LiOH + 3S → Li2S + H2S + SO2 (t = 445 °C).
В результате реакции образуются сульфид лития, сероводород и оксид серы.
3. реакция гидроксида лития с йодом:
6LiOH + 3I2 → 5KI + KIO3 + H2O (t = 80 °C).
В результате реакции образуются йодид лития, иодат лития и вода.
4. реакция гидроксида лития с цинком и водой:
Zn + 2LiOH + 2H2O → Li2[Zn(OH)4] + H2.
В результате реакции образуются тетрагидроксоцинкат натрия и водород. В ходе реакции используется концентрированный раствор гидроксида лития.
5. реакция гидроксида лития с ортофосфорной кислотой:
H3PO4 + 3LiOH → Li3PO4 + 3H2O.
В результате реакции образуются ортофосфат лития и вода.
6. реакция гидроксида лития с азотной кислотой:
LiOH + HNO3 → LiNO3 + H2O.
В результате реакции образуются нитрат лития и вода.
Аналогично проходят реакции гидроксида лития и с другими кислотами.
7. реакция гидроксида лития с сероводородом:
H2S + 2LiOH → Li2S + 2H2O.
В результате реакции образуются сульфид лития и вода.
8. реакция гидроксида лития с фтороводородом:
HF + LiOH → LiF + H2O.
В результате реакции образуются фторид лития и вода.
9. реакция гидроксида лития с бромоводородом:
HBr + LiOH → LiBr + H2O.
В результате реакции образуются бромид лития и вода.
10. реакция гидроксида лития с йодоводородом:
HI + LiOH → LiI + H2O.
В результате реакции образуются йодид лития и вода.
11. реакция гидроксида лития с оксидом алюминия:
Al2O3 + 2LiOH → 2LiAlO2 + H2O.
Оксид алюминия является амфотерным оксидом. В результате реакции образуются алюминат лития и вода.
12. реакция гидроксида лития с оксидом углерода (углекислым газом):
2LiOH + CO2 → Li2CO3 + H2O.
Оксид углерода является кислотным оксидом. В результате реакции образуются карбонат лития и вода. В ходе реакции используется концентрированный раствор гидроксида лития. Реакция протекает при комнатной температуре.
Также данная реакция протекает на воздухе. Гидрооксид лития поглощает углекислый газ и образуется карбонат лития.
13. реакция гидроксида лития с оксидом серы (IV):
2LiOH + SO2 → Li2SO3 + H2O.
Оксид серы (IV) является кислотным оксидом. В результате реакции образуются сульфит лития и вода. В ходе реакции используется насыщенный раствор гидроксида лития.
14. реакция гидроксида лития с оксидом серы (VI):
2LiOH + SO3 → Li2SO4 + H2O.
Оксид серы (VI) является кислотным оксидом. В результате реакции образуются сульфат лития и вода.
15. реакция гидроксида лития с оксидом кремния:
4LiOH + SiO2 ⇄ Li4SiO4 + 2H2O.
В результате реакции образуются ортосиликат лития и вода. В ходе реакции используется разбавленный раствор гидроксида лития. Реакция протекает при комнатной температуре.
16. реакция гидроксида лития с гидроксидом цинка:
Zn(OH)2 + 2LiOH → Li2[Zn(OH)4].
Гидроксид цинка является амфотерным основанием. В результате реакции образуется тетрагидроксоцинкат лития.
17. реакция гидроксида лития с сульфатом железа:
FeSO4 + 2LiOH → Fe(OH)2 + Li2SO4.
В результате реакции образуются гидроксид железа и сульфат лития.
18. реакция гидроксида лития с хлоридом железа:
FeCl3 + 3LiOH → Fe(OH)3 + 3LiCl.
В результате реакции образуются гидроксид железа и хлорид лития.
19. реакция гидроксида лития с нитратом цинка:
Zn(NO3)2 + 2LiOH → Zn(OH)2 + 2LiNO3.
В результате реакции образуются гидроксид цинка и нитрат лития.
20. реакция гидроксида лития с хлоридом меди:
CuCl2 + 2LiOH → Cu(OH)2 + 2LiCl.
В результате реакции образуются гидроксид меди и хлорид лития.
Аналогично проходят реакции гидроксида лития и с другими солями.
21. реакция термического разложения гидроксида лития:
2LiOH → Li2O + H2O (t = 800-1000°C).
В результате реакции образуются оксид лития и вода. Реакция протекает в атмосфере водорода.
Применение и использование гидроксида лития:
Гидроксид лития используется во множестве отраслей промышленности и для бытовых нужд:
– в химической промышленности для получения солей лития;
– как компонент электролитов в щелочных аккумуляторах,
– как поглотитель углекислого газа в противогазах, подводных лодках и космических кораблях,
– в химической промышленности как катализатор полимеризации,
– в стекольной и керамической промышленности;
– при производстве водоупорных смазочных материалов, обладающих механической стабильностью в широком диапазоне температур.
Примечание: © Фото //www.pexels.com, //pixabay.com
карта сайта
гидроксид лития реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие гидроксида лития
реакции
Коэффициент востребованности
5 588
Физические свойства
Гидроксид лития при стандартных условиях представляет собой бесцветные кристаллы. Растворяется в воде.
Относительная молекулярная масса Mr = 23, 95; относительная плотность для тв. и ж. состояния d = 1, 46; tпл = 471◦ C;
Способы получения
1. Гидроксид лития получают электролизом раствора хлорида лития:
2LiCl + 2H2O → 2LiOH + H2 + Cl2
2. При взаимодействии лития, оксида лития, гидрида лития и пероксида лития с водой также образуется гидроксид лития:
2Li + 2H2O → 2LiOH + H2
Li2O + H2O → 2LiOH
2LiH + 2H2O → 2LiOH + H2
Li2O2 + H2O → 2LiOH + H2O2
3. Карбонат лития при взаимодействии с гидроксидом кальция образует гидроксид лития:
Li2CO3 + Ca(OH)2 → CaCO3↓ + 2LiOH
Качественная реакция
Качественная реакция на гидроксид лития — окрашивание фенолфталеина в малиновый цвет.
Химические свойства
1. Гидроксид лития реагируют со всеми кислотами (и сильными, и слабыми, и растворимыми, и нерастворимыми). При этом образуются средние или кислые соли, в зависимости от соотношения реагентов:
3LiOH + H3PO4 → Li3PO4 + H2O
2LiOH + H3PO4 → Li2HPO4 + 2H2O
LiOH + H3PO4 → LiH2PO4 + H2O
2. Гидроксид лития реагирует с кислотными оксидами. При этом образуются средние или кислые соли, в зависимости от соотношения реагентов:
2LiOH(избыток) + CO2 → Li2CO3 + H2O
LiOH + CO2 (избыток) → LiHCO3
3. Гидроксид лития реагирует с амфотерными оксидами и гидроксидами. При этом в расплаве образуются средние соли, а в растворе комплексные соли:
2LiOH + Al2O3 → 2LiAlO2 + H2O
в растворе образуется комплексная соль — тетрагидроксоалюминат:
2LiOH + Al2O3 + 3H2O → 2Li[Al(OH)4]
4. С кислыми солями гидроксид лития также может взаимодействовать. При этом образуются средние соли, или менее кислые соли:
LiOH + LiHCO3 → Li2CO3 + H2O
5. Гидроксид лития взаимодействует с простыми веществами-неметаллами (кроме инертных газов, азота, кислорода, водорода и углерода).
При этом кремний окисляется до силиката и водорода:
2LiOH + Si + H2O → Li2SiO3 + H2
Фтор окисляет щелочь. При этом выделяется молекулярный кислород:
4LiOH + 2F2 → 4LiF + O2 (OF2) + 2H2O
Другие галогены, сера и фосфор — диспропорционируют в растворе гидроксида лития:
3LiOH + P4 + 3H2O = 3LiH2PO2 + PH3↑
2LiOH(холодный) + Cl2 = LiClO + LiCl + H2O
6LiOH(горячий) + 3Cl2 = LiClO3 + 5LiCl + 3H2O
Сера взаимодействует с гидроксидом лития только при нагревании:
6LiOH + 3S = 2Li2S + Li2SO3 + 3H2O
6. Гидроксид лития взаимодействует с амфотерными металлами, кроме железа и хрома. При этом в расплаве образуются соль и водород:
2LiOH + Zn → Li2ZnO2 + H2
В растворе образуются комплексная соль и водород:
2LiOH + 2Al + 6Н2О = 2Li[Al(OH)4] + 3Н2
7. Гидроксид лития вступает в обменные реакции с растворимыми солями.
Хлорид меди (II) реагирует с гидроксидом лития с образованием хлорида лития и осадка гидроксида меди (II):
2LiOH + CuCl2 = Cu(OH)2↓+ 2LiCl
Также с гидроксидом лития взаимодействуют соли аммония.
Например, при взаимодействии хлорида аммония и гидроксида лития образуются хлорид лития, аммиак и вода:
NH4Cl + LiOH = NH3 + H2O + LiCl
8. Гидроксид лития разлагается при нагревании до температуры 600°С:
2LiOH → Li2O + H2O
9. Гидроксид лития проявляет свойства сильного основания. В воде практически полностью диссоциирует, образуя щелочную среду и меняя окраску индикаторов.
LiOH ↔ Li+ + OH—
10. Гидроксид лития в расплаве подвергается электролизу. При этом на катоде восстанавливается сам литий, а на аноде выделяется молекулярный кислород:
4LiOH → 4Li + O2 + 2H2O
| Гидроксид лития | |
|---|---|
 |
|
| Систематическое наименование |
Гидроксид лития |
| Хим. формула | LiOH |
| Рац. формула | LiOH |
| Состояние | твёрдое |
| Молярная масса | 23,94637 г/моль |
| Плотность | 1,46 (25 °C) |
| Т. плав. | 462 |
| Т. кип. | 925 °C |
| Т. разл. | 930 |
| Энтальпия образования | -487,2 кДж/моль |
| Растворимость в воде | 12,7 (0 °C) |
| ГОСТ | ГОСТ 8595-83 |
| Рег. номер CAS | 1310-65-2 |
| PubChem | 3939 |
| Рег. номер EINECS | 215-183-4 |
| SMILES |
[Li+].[OH-] |
| InChI |
1S/Li.H2O/h;1H2/q+1;/p-1 WMFOQBRAJBCJND-UHFFFAOYSA-M |
| RTECS | OJ6307070 |
| ChEBI | 33979 |
| Номер ООН | 2680 |
| ChemSpider | 3802 и 21170131 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. |
Гидроксид лития — неорганическое основание щелочного металла лития, имеющее формулу LiOH. Является сильным основанием, но наиболее слабым основанием среди щелочных металлов.
Физические свойства
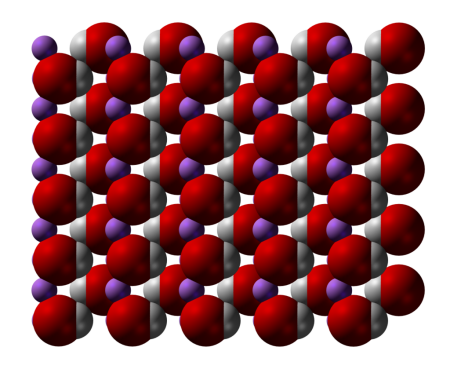
Гидроксид лития при стандартных условиях представляет собой бесцветные кристаллы с тетрагональной решёткой. При работе с ним необходимо проявлять осторожность, избегать попадания на кожу и слизистые оболочки.
Растворяется в воде, 12,24 г/100 см3 при 25 °C, растворимость с температурой практически не повышается. В этаноле, в отличие от гидроксида натрия, почти не растворяется.
Получение
- Взаимодействие металлического лития с водой:
-
- 2Li + 2H2O ⟶ 2LiOH + H2↑
- Взаимодействие оксида лития с водой:
-
- Li2O + H2O ⟶ 2LiOH
- Взаимодействие карбоната лития с гидроксидом кальция:
-
- Li2CO3 + Ca(OH)2 ⟶ 2LiOH + CaCO3↓
- Обменными реакциями:
-
- Li2SO4 + Ba(OH)2 ⟶ 2LiOH + BaSO4↓
Химические свойства
- Взаимодействие с кислотами с образованием соли и воды (реакция нейтрализации):
-
- LiOH + HCl ⟶ LiCl + H2O
- 2LiOH + H2SO4 ⟶ Li2SO4 + 2H2O
- Взаимодействие с кислотными оксидами с образованием соли и воды:
-
- 2LiOH + CO2 ⟶ Li2CO3 + H2O
- 2LiOH + SO3 ⟶ Li2SO4 + H2O
- При нагревании в инертной атмосфере (Ar) разлагается:
-
- 2LiOH →800oC,A r Li2O + H2O
Применение
Гидроксид лития используют для получения солей лития; как компонент электролитов в щелочных аккумуляторах и поглотитель углекислого газа в противогазах, подводных лодках и космических кораблях. Он также используется как катализатор полимеризации. Применяется в стекольной и керамической промышленности. При производстве водоупорных смазочных материалов, обладающих механической стабильностью в широком диапазоне температур.
ЛИТИЯ ГИДРОКСИД
- ЛИТИЯ ГИДРОКСИД
- LiOH, бесцв. кристаллы с тетрагон, решеткой ( а =0,3549 нм, с= 6,4334 нм, z = 2, пространств. группа Р4/ птт); т. пл. 473 °С, при более высокой т-ре испаряется и частично диссоциирует на Li2O и Н 2 О; в парах при 820-870 °С содержится 90% (LiOH)2; плотн. 1,44г/см 3; С 0p.>49,58 Дж/(моль. К); DH0 пл 20,9 кДж/моль, DH0 обр -484,90 кДж/моль; S029842,76 Дж/(моль. К). Образует моногидрат-бесцв. кристаллы с моноклинной решеткой (а= 0,737 нм, b= 0,826 нм, с= 0,319 нм, b = 110°, z = 4, пространств. группа С2/m); плотн. 1,51 г/см 3; C0p 79,5 Дж/(моль. К); DH0 обр -788,3 кДж/моль; S029871,4 Дж/(моль. К); обезвоживание наблюдается уже при 40 °С (давление пара 20,66 гПа), полностью теряет воду при 108,9°С. Р-римостъ LiOH в воде меньше, чем гидроксидов др. щелочных металлов, и составляет (г в 100 г Н 2 О): 10,90 при 0°С, 12,48 при 25 °С, 13,02 при 50 °С, 17,55 при 100°С Т. пл. эвтектич. системы LiOH-H2O (10,5% по массе LiOH) Ч 18,2°С; DH0 растворения для бесконечно разб. р-ра Ч 23,58 кДж/моль. Плохо раств. в этаноле. Л. г. — сильное основание (щелочь). С NaOH и КОН образует твердые р-ры и двойные гидроксиды (напр., LiOH.NaOH), с RbOH — соед. 3LiOH.RbOH, с Н 2 О 2 — пероксиды Li2O2.Н 2 О 2.пН 2 О ( п =2 или 3), Li2O2.2Н 2 О 2. Расплавы LiOH и его водные р-ры разрушают стекло, фарфор, взаимод. со мн. силикатами, подвергают коррозии в присут. кислорода Fe, Pt, монель-металл. К действию Л. г. устойчивы Ni, Ag и Au. Получают Л. г.: взаимод. Li, Li2O и LiH с Н 2 О в атмосфере Аr или Н 2; обменной р-цией в водных р-рах Li2SO4 с КОН, Са(ОН)2 или Ва(ОН)2 в инертной атмосфере; в пром-сти -электролизом LiCl с движущимся ртутным катодом или методом каустификации нагретой до кипения водной суспензии Li2CO3 гидроксидом Са: Li2CO3 + Са(ОН)2 D2LiOH + СаСО 3. Л. г. — добавка к электролиту щелочных аккумуляторов; реагент для получения соед. Li, в частности олеатор, стеаратов и пальмитатов; поглотитель СО 2 в противогазах, подводных лодках, самолетах и космич. кораблях. Лит.: Иткина Л. С. Гидроксиды лития, рубидия и цезия, М., 1973. См. также лит. при ст. Литий. Б. Д. Cmenuн.
Химическая энциклопедия. — М.: Советская энциклопедия.
.
1988.
Полезное
Смотреть что такое «ЛИТИЯ ГИДРОКСИД» в других словарях:
-
ЛИТИЯ ГИДРОКСИД — LiOH, сильное основание (щелочь). Бесцветные кристаллы. Хорошо растворим в воде. Применяют: в щелочных аккумуляторах, для получения смазок; соединения лития, как поглотитель CO2 в противогазах, подводных лодках, самолетах и космических кораблях … Большой Энциклопедический словарь
-
лития гидроксид — LiOH, сильное основание (щёлочь). Бесцветные кристаллы. Хорошо растворим в воде. Применяют в щелочных аккумуляторах, для получения смазок, соединения лития, как поглотитель CO2 в противогазах, подводных лодках, самолётах и космических кораблях. * … Энциклопедический словарь
-
ЛИТИЯ ГИДРОКСИД — LiOH, сильное основание (щёлочь). Бесцв. кристаллы. Хорошо растворим в воде. Применяют в щелочных аккумуляторах, для получения смазок, соед. лития, как поглотитель СО2 в противогазах, подводных лодках, самолётах и космич. кораблях … Естествознание. Энциклопедический словарь
-
Гидроксид лития — Гидроксид лития … Википедия
-
Гидроксид алюминия — Гидроксид алюминия, вещество с формулой (а также … Википедия
-
Гидроксид калия — Гидроксид калия … Википедия
-
Гидроксид железа(II) — У этого термина существуют и другие значения, см. Гидроксиды железа. Гидроксид железа(II) … Википедия
-
Гидроксид хрома(II) — Общие Систематическое наименование Гидроксид хрома(II) Традиционные названия гидроокись хрома Химическая формула Сr(OH)2 Физические свойства … Википедия
-
Гидроксид хрома(III) — Гидроксид хрома (III) сложное неорганическое вещество с химической формулой Cr(OH)3. Описание Гидроксид хрома (III) амфотерный гидроксид. Серо зеленого цвета, разлагается при нагревании, теряя воду и образуя зеленый метагидроксид CrO(OH). Не… … Википедия
-
Гидроксид марганца(II) — Общие Систематическое наименование Гидроксид марганца(II) Традиционные названия Гидроокись марганца Химическая формула Mn(OH)2 Физические свойства … Википедия