Содержание
- Структурная формула
- Русское название
- Английское название
- Латинское название вещества Кальция хлорид
- Брутто формула
- Фармакологическая группа вещества Кальция хлорид
- Нозологическая классификация
- Код CAS
- Фармакологическое действие
- Характеристика
- Фармакология
- Применение вещества Кальция хлорид
- Противопоказания
- Побочные действия вещества Кальция хлорид
- Способ применения и дозы
- Особые указания
- Торговые названия с действующим веществом Кальция хлорид
Структурная формула
Русское название
Кальция хлорид
Английское название
Calcium chloride
Латинское название вещества Кальция хлорид
Calcii chloridum (род. Calcii chloridi)
Фармакологическая группа вещества Кальция хлорид
Нозологическая классификация
Список кодов МКБ-10
- N93 Другие аномальные кровотечения из матки и влагалища
- E58 Алиментарная недостаточность кальция
- E83.5.1* Гипокальциемия
- Z39.1 Помощь и обследование кормящей матери
- K92.2 Желудочно-кишечное кровотечение неуточненное
- N95.1 Менопаузное и климактерическое состояние у женщин
- L30.9 Дерматит неуточненный
- L40 Псориаз
- T56.8 Других металлов
- T80.6 Другие сывороточные реакции
- T66 Неуточненные эффекты излучения
- K75.8 Другие уточненные воспалительные болезни печени
- R04.0 Носовое кровотечение
- R60.0 Локализованный отек
- J45 Астма
- J18 Пневмония без уточнения возбудителя
- T56.0 Свинца и его соединений
- R25.2 Судорога и спазм
- I78.8 Другие болезни капилляров
- L50 Крапивница
- N70 Сальпингит и оофорит
- E55.0 Рахит активный
- O62.2 Другие виды слабости родовой деятельности
- I77.6 Артериит неуточненный
- A16.2 Туберкулез легких без упоминания о бактериологическом или гистологическом подтверждении
- K71 Токсическое поражение печени
- T65.8 Других уточненных веществ
- O25 Недостаточность питания при беременности
- N05 Нефритический синдром неуточненный
- N71 Воспалительные болезни матки, кроме шейки матки
- O15 Эклампсия
- R04.8 Кровотечение из других отделов дыхательных путей
- E83.5 Нарушения обмена кальция
- L29 Зуд
- G83.8 Другие уточненные паралитические синдромы
- R58 Кровотечение, не классифицированное в других рубриках
- M83.9 Остеомаляция у взрослых неуточненная
- R29.0 Тетания
- T78.3 Ангионевротический отек
- R09.1 Плеврит
- E20 Гипопаратиреоз
- T78.4 Аллергия неуточненная
Фармакологическое действие
—
гемостатическое, дезинтоксикационное, противоаллергическое, противовоспалительное, снижающее проницаемость капилляров.
Характеристика
Бесцветные кристаллы без запаха, горько-соленого вкуса. Кальция хлорид очень легко растворим в воде (4:1) с сильным охлаждением раствора, легко растворим в этаноле. Очень гигроскопичен, на воздухе расплывается. Содержит 27% кальция. Молекулярная масса 110,98.
Фармакология
Восполняет дефицит ионов кальция, необходимых для передачи нервных импульсов, сокращения скелетных и гладких мышц, деятельности сердца, формирования костной ткани, свертывания крови. Кальций снижает проницаемость клеточных мембран и сосудистой стенки, предотвращает развитие воспалительных реакций, повышает сопротивляемость организма инфекциям и усиливает фагоцитоз. При в/в введении стимулирует симпатический отдел вегетативной нервной системы, увеличивает выделение надпочечниками адреналина, оказывает умеренное диуретическое действие.
Применение вещества Кальция хлорид
Гипокальциемия, повышенная потребность в кальции (беременность, кормление грудью, период усиленного роста организма), недостаточное поступление кальция с пищей, нарушение обмена кальция, в т.ч. в постменопаузном периоде, повышенное выведение кальция (хроническая диарея, вторичная гипокальциемия, в т.ч. на фоне длительного приема некоторых диуретиков, противосудорожных ЛС или глюкокортикоидов), кровотечения различной этиологии и локализации (легочные, желудочно-кишечные, носовые, маточные и др.), аллергические заболевания и реакции, в т.ч. сывороточная болезнь, крапивница, зуд, отек Квинке, бронхиальная астма, воспалительные и экссудативные процессы, в т.ч. пневмония, плеврит, аднексит, эндометрит, повышенная проницаемость сосудов (геморрагический васкулит, лучевая болезнь), дистрофические алиментарные отеки, гипопаратиреоз, гипокальциемия, спазмофилия, свинцовые колики, тетания, гиперкалиемическая форма пароксизмальной миоплегии, туберкулез легких, рахит и остеомаляция, гепатит (паренхиматозный, токсический), нефрит, эклампсия, отравление солями магния, щавелевой и фтористой кислотами, экзема, псориаз, слабость родовой деятельности.
Противопоказания
Гиперчувствительность, гиперкальциемия, атеросклероз, склонность к тромбозам.
Побочные действия вещества Кальция хлорид
При приеме внутрь — боль в эпигастрии, изжога, тошнота, рвота, гастрит. При в/в введении — ощущение жара, гиперемия лица, брадикардия; при быстром в/в введении — фибрилляция желудочков сердца; местные реакции при в/в введении — боль и гиперемия по ходу вены.
Способ применения и дозы
В/в, медленно (по 6 капель/мин) — перед введением 5–10 мл 10% раствора, разбавляют в 100–200 мл изотонического раствора натрия хлорида или 5% раствора декстрозы. Внутрь, после еды, в виде 5–10% раствора 2–3 раза в сутки: взрослым — 10–15 мл на прием, детям — 5–10 мл.
Особые указания
Нельзя вводить п/к и в/м — возможен некроз тканей (кальция хлорид, начиная с концентрации 5%, оказывает сильное раздражающее действие). При в/в введении кальция хлорида появляется ощущение жара сначала в полости рта, а затем по всему телу (этот эффект ранее использовали при определении скорости кровотока — регистрировали время между моментом введения в вену кальция хлорида и появлением ощущения жара).
Торговые названия с действующим веществом Кальция хлорид
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Кальция хлорид |
от 47.00 до 55.00 |
| Хлорид кальция | |
 |
|
| Общие | |
|---|---|
| Систематическое наименование | Хлорид кальция |
| Традиционные названия | Хлористый кальций |
| Химическая формула | CaCl2 |
| Физические свойства | |
| Молярная масса | 111.08 г/моль |
| Плотность | 2.15 г/см³ |
| Термические свойства | |
| Температура плавления | 772 °C |
| Температура кипения | 1935 °C |
| Химические свойства | |
| pKa | 8-9 |
| Растворимость в воде | 74.5 г/100 мл |
| Структура | |
| Координационная геометрия | Октаэдральная |
| Классификация | |
| Рег. номер CAS | 10043-52-4 |
| Регистрационный номер EC | 233-140-8 |
| RTECS | EV9800000 |
Хлори́д ка́льция, CaCl2 — кальциевая соль соляной кислоты. Зарегистрирован в качестве пищевой добавки E509. Считается безвредным (как добавка).
Содержание
- 1 Свойства
- 1.1 Кристаллогидраты хлорида кальция
- 2 Получение
- 3 Применение
- 4 См. также
- 5 Источник
Свойства
Бесцветные кристаллы плотностью 2,51 г/см³, tпл 772 °C. Обладает высокими гигроскопическими свойствами. Растворимость (г на 100 г H2O): 74 (20 °C) и 159 (100 °C). Водные растворы хлорида кальция замерзают при низких температурах (20%-ный — при −18,57 °C, 30%-ный — при −48 °C).
Кристаллогидраты хлорида кальция
CaCl2 образует гидрат CaCl2·6H2O, устойчивый до 29,8 °C; при более высоких температурах из насыщенного раствора выпадают кристаллогидраты с 4, 2 и 1 молекулами H2O. При смешении CaCl2*6H2O (58,8 %) со снегом или льдом (41,2 %) температура понижается до —55 °C (криогидратная точка).
Природный минерал гексагидрата хлорида кальция, ставший известным как антарктикит[ru], был впервые обнаружен на дне солёного озера Дон-Жуан на Земле Виктории в Антрактиде.
Получение
Хлорид кальция получают как побочный продукт в производстве соды.
В быту можно получить технический хлорид кальция нагреванием хлорной извести.
Применение
Применяют для получения металлического кальция, для осушки и понижения точки росы технологического и импульсного газа:
- На ГРС[прояснить], КС[прояснить] магистральных газопроводов;
- На АГНКС[прояснить];
- На объектах газодобычи при подготовке газа к транспортировке;
- В холодильном деле;
- Как ускоритель схватывания цемента;
- Для обеспыливания гравийных дорог;
- Как противогололёдное средство;
- Как отвердитель в продуктах питания;
- В молокоперерабатывающей промышленности при производстве ферментированных молочных продуктов, и играет большую роль в формировании сгустка. Добавление хлористого кальция ведет к увеличению выхода конечного продукта, а также улучшает его свойства;
- В медицине.
См. также
- Хлорид кальция (лекарственное средство)
Источник
| Хлорид кальция на Викискладе? |
- применение хлорида кальция в пищевой промышленности
- Хлорид кальция как пищевая добавка
|
Соединения кальция |
|---|
|
Алюминаты кальция (mCaO·nAl2O3) • Алюмогидрид кальция (Ca[AlH4]2) • Амид кальция (Ca(NH2)2) • Арсенат кальция (Ca3(AsO4)2) • Ацетат кальция ((CH3COO)2Ca) • Бисульфид кальция (Ca(HS)2) • Борат кальция (Ca3(BO3)2) • Бромид кальция (CaBr2) • Вольфрамат кальция (CaWO4) • Гексаборид кальция (CaB6) • Гексафторсиликат кальция (CaSiF6) • Гидрид кальция (CaH2) • Гидроксид кальция (Ca(OH)2) • Гидроортофосфат кальция (CaHPO4) • Гипофосфит кальция (Ca(PH2O2)) • Гипохлорит кальция (Ca(ClO)2) • Глицерофосфат кальция (C3H7CaO6P) • Глюконат кальция (C12H22CaO14) • Дигидрокарбонат кальция (Ca(HCO3)2) • 2,5-дигидроксибензолсульфонат кальция (C12H10CaO10S2) • Дигидроортофосфат кальция (Ca(H2PO4)2) • Иодат кальция (Ca(IO3)2) • Иодид кальция (CaI2) • Карбид кальция (CaC2) • Карбонат кальция (CaCO3) • Моносилицид кальция (CaSi) • Нитрат кальция (Са(NО3)2) • Нитрид кальция (Ca3N2) • Оксалат кальция (СаС2О4) • Оксид кальция (CaO) • Ортофосфат кальция (Ca3(PO4)2) • Перманганат кальция (Ca(MnO4)2) • Пероксид кальция (CaO2) • Пирофосфат кальция (Ca2P2O7) • Силикат кальция (CaSiO3) • Силицид дикальция (Ca2Si) • Силицид кальция (CaSi2) • Сульфат кальция (CaSO4) • Сульфид кальция (CaS) • Сульфит кальция (CaSO3) • Тетрагидроалюминат кальция (Ca(AlH4)2) • Титанат кальция (CaTiO3) • Триметафосфат кальция (Ca3(P3O9)2) • Флюорит (CaF2) • Формиат кальция (Ca(HCOO)2) • Фосфид кальция (Ca3P2) • Фторид кальция (CaF2) • Хлорат кальция (Ca(ClO3)2) • Хлорид кальция (CaCl2) • Хлорная известь (Ca(Cl)OCl) • Хромат кальция (CaCrO4) • Цианамид кальция (CaCN2) • Цианид кальция (Ca(CN)2) • Цитрат кальция (Ca3(C6H5O7)2) • |
Плазмозамещающие и перфузионные растворы — АТХ код: B05
Определение и формула
Это неорганическое химическое соединение, относящееся к классу солей. Название по другой номенклатуре – хлористый кальций.
Химическая формула
CaCl2
Cтруктурная схема
Получение химического соединения
Хлорид кальция в свободном виде в природе не встречается. Его синтезируют химическими путями.
Естественные источники получения
В природе хлористый кальций встречается исключительно в виде кристаллогидрата с химической формулой СаСl2 · 6Н2O. Под воздействием высоких температур при нагревании свыше 29,8°C кристаллогидрат теряет молекулы воды.
Искусственные источники получения
В лабораторных условиях хлористый кальций синтезируют при взаимодействии гидроксида кальция с хлоридом аммония.
2NH4Cl + Ca(OH)2 → 2NH3↑ + CaCl2 + 2H2O
Рассмотренная химическая реакция лежит в основе промышленного производства соды. Второй продукт взаимодействия – аммиак, в качестве побочного продукта выделяется вода.
Альтернативный способ – обработка кальцийсодержащего сырья (кристаллического карбоната кальция) соляной кислотой.
СаСО3 + 2HCl → CaCl2 + СО2↑ + Н2О
Свойства хлористого кальция
Физические свойства
Хлористый кальций – это твердое вещество белого цвета. Кристаллы, имеющие кубическую форму, обладают высокой гигроскопичностью и быстро поглощают влагу из окружающего воздуха. Хорошо растворим в низших спиртах и органических растворителях (ацетоне).
Прочие физические свойства:
| плотность | 2,15 г/см³ |
| молярная масса | 111,08 г/моль |
| температура кипения | 1935 °C |
| температура плавления | 772 °C |
| растворимость в воде | 74,5 г/100 мл |
Химические свойства
Хлорид кальция проявляет все типичные свойства солей.
| Свойство | Уравнение |
|---|---|
| Подергается обратимому гидролизу. Диссоциирует на катиона кальция и хлорид-анионы. | CaCl2↔Ca2+ + 2Cl— |
| Взаимодействует с водными растворами щелочей. | CaCl2 + 2NaOH(conc) →Ca(OH)2↓ + 2NaCl |
| Вступают в химическое взаимодействие с сильными кислотами. | CaCl2 + H2SO4(conc) → CaSO4↓ + 2HCl↑ |
| Вступает в химические реакции с другими солями при условии, что один из продуктов выпадает в осадок или улетучивается. В противоположном случае реакция будет обратимой. | CaCl2+ Na2CO3 → CaCO3↓ + 2NaCl |
| Вступает во взаимодействие с водородом при нагревании до 600-700°C и в присутствии катализаторов – Pt, Ni, Fe. | CaCl2 + H2↔ CaH2 + 2HCl |
Применение хлористого кальция
Хлористый кальций активно применяется в медицине, промышленности, пищевом производстве. Вещество используют:
• как сырье для получения кальция;
• как наполнитель для осушающих конструкций в форме трубок (при изоляции водяных паров и осушении газообразных веществ);
• на газораспределительных станциях;
• для быстрого схватывания цемента;
• как средство от гололеда;
• для регулирования жесткости воды при производстве напитков;
• в качестве консерванта;
• в качестве отвердителя в пищевых продуктах (безопасная для здоровья добавка E509);
• для смягчения мяса;
• в качестве лекарственного средства для восполнения дефицита кальция в организме;
• в медицине для лечения проявлений аллергии, при токсических отравлениях, гепатите, для укрепления стенок сосудов, улучшения работы сердца.
Тест по теме «Хлорид кальция»
| Хлорид кальция | |
|---|---|
 |
|
| Систематическое наименование |
Хлорид кальция |
| Традиционные названия | Хлористый кальций |
| Хим. формула | CaCl₂ |
| Рац. формула | CaCl2 |
| Молярная масса | 111,08 г/моль |
| Плотность | 2,15 г/см³ |
| Т. плав. | 772 °C |
| Т. кип. | 1935 °C |
| pKa | 8—9 |
| Растворимость в воде | 74,5 г/100 мл |
| Координационная геометрия | Октаэдральная |
| ГОСТ | ГОСТ 450-77 |
| Рег. номер CAS | 10043-52-4 |
| PubChem | 5284359 |
| Рег. номер EINECS | 233-140-8 |
| SMILES |
[Cl-].[Cl-].[Ca+2] |
| InChI |
1S/Ca.2ClH/h;2*1H/q+2;;/p-2 UXVMQQNJUSDDNG-UHFFFAOYSA-L |
| Рег. номер EC | 233-140-8 |
| Кодекс Алиментариус | E509 |
| RTECS | EV9800000 |
| ChEBI | 3312 |
| ChemSpider | 23237 |
| ЛД50 | 1 г/кг (крысы, перорально) |
| Пиктограммы СГС | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. |
О хлориде кальция как лекарственном средстве см. Хлорид кальция (лекарственное средство).
Хлорид кальция, CaCl2 — кальциевая соль соляной кислоты. Зарегистрирован в качестве пищевой добавки E509. Считается безвредным.
Содержание
- 1 Свойства
- 1.1 Кристаллогидраты хлорида кальция
- 2 Получение
- 3 Применение
Свойства
Белые кристаллы плотностью 2,15 г/см³, tпл 772 °C. Обладает высокими гигроскопическими свойствами. Растворимость (г на 100 г H2O): 74 (20 °C) и 159 (100 °C). Водные растворы хлорида кальция замерзают при низких температурах (20%-ный — при −18,57 °C, 30%-ный — при −48 °C).
Кристаллогидраты хлорида кальция
CaCl2 образует гидрат CaCl2·6H2O, устойчивый до 29,8 °C; при более высоких температурах из насыщенного раствора выпадают кристаллогидраты с 4, 2 и 1 молекулами H2O. При смешении CaCl2*6H2O (58,8 %) со снегом или льдом (41,2 %) температура понижается до —55 °C (криогидратная точка).
Природный минерал гексагидрата хлорида кальция, ставший известным как антарктикит (или антарктицит), был впервые обнаружен на дне солёного озера Дон-Жуан на Земле Виктории в Антарктиде.
Получение
Хлорид кальция получают как побочный продукт в производстве соды (в процессе рекуперации аммиака):
- 2NH4Cl + Ca(OH)2 → 2NH3↑ + CaCl2 + 2H2O.
Применение
В химической лаборатории хлорид кальция применяется в качестве наполнителя для осушающих трубок, также называемых хлоркальциевыми, предназначенных для изоляции веществ в сосуде от водяных паров атмосферы и для осушки газов. В первом случае такая трубка прямая или согнута под углом 90 градусов и имеет один шарообразный участок, во втором она согнута в виде буквы U и имеет два шарообразных участка.
Хлорид кальция также применяют для получения металлического кальция, для осушки и понижения точки росы технологического и импульсного газа:
- На газораспределительных станциях, компрессорных станциях магистральных газопроводов;
- На автогазонаполнительных компрессорных станциях;
- На объектах газодобычи при подготовке газа к транспортировке.
Кроме того, он применяется в следующих областях:
- В смягчении говядины и баранины (снижение затрат на заморозку, хранение и погрузку);
- В консервировании овощей и фруктов (хранение яблок с пропиткой 8 % раствором)
- Как ускоритель схватывания цемента;
- Для обеспыливания гравийных дорог;
- Как противогололёдное средство;
- Как отвердитель в продуктах питания (Загуститель для получения низкокалорийных желе);
- В молокоперерабатывающей промышленности при производстве ферментированных молочных продуктов, и играет большую роль в формировании сгустка. Добавление хлористого кальция ведёт к увеличению выхода конечного продукта, а также улучшает его свойства;
- В медицине.
- В регулировании жёсткости воды при производстве слабоалкогольных и безалкогольных напитков
- В изготовлении хлеба (консервант)
- При транспортировке замороженных грузов морем — для избежания замерзания воды в дренажной системе
- Для приготовления жидкости глушения при проведении ремонта на нефтяных и газовых скважинах.
Общее понятие о хлористом кальции
Хлористый кальций (хлорид кальция, кальция хлорид или СаCl2) 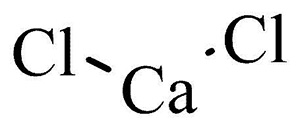
Хлористый кальций в жидком виде (водный или технический кальций) представляет собой прозрачный (возможно слегка мутный, зеленого или желто-серого цвета) раствор.
Области применения
Благодаря своим полезным свойствам в настоящее время 
— сельское хозяйство (для мелиорации почв, улучшения качества кормов, удобрений);
— строительство (ускоритель для загустения цемента, бетона);
— пищевая (безвредная пищевая добавка E509). В настоящее время входит в состав многих продуктов питания. Классифицируется как эмульгатор и используется как отвердитель. Применяется при изготовлении кисло-молочных продуктов (творога, кефира, сыра, брынзы, сметаны, масла, сухого молока), так как ионы калия связывают белки, он служит прекрасным загустителем продуктов. С этой целью его добавляют в мармелад, джем, желе, шоколад, консервированные фрукты и овощи, в хлебобулочные изделия);
— химическая (при производстве каучука, латекса, резинотехнических изделий);
— противогололедное средство;
— нефтяная (для увеличения нефтеотдачи, очиститель газа);
— целлюлозно-бумажная (для улучшения качества продукции);
— деревообрабатывающая (пропитка древесины для огнестойкости);
— горная (предотвращает самовозгорание угля);
— машиностроительная (антифриз).
Хлористый кальций – как лекарственный препарат
Немаловажную роль в жизнедеятельности организма играет макро и микроэлементы, среди них — хлористый кальций. В организме он находится в виде неионизированных соединений в скелетной ткани, в ионизированных – в тканевой жидкости и крови.
Хлористый кальций – синтетический лекарственный препарат, восполняющий недостаток кальция в организме. Он является «строительным материалом» для формирования внутренних органов и костной ткани, необходим для передачи нервных импульсов, сокращения мышц, свертывания крови и т.д. Его недостаток может привести к серьезным нарушениям, к рахиту, а у беременных женщин – к выкидышу.
Кальция хлорид оказывает противовоспалительное, противоаллергическое и кровоостанавливающее действие, поэтому его применяют при лечении:
— аллергических заболеваний (крапивницы, ангионевротических отеков, бронхиальной астмы, сенной лихорадки) и аллергических реакций на лекарства;
— кожных заболеваний (псориаз, экзема);
— пневмонии;
— катаракты;
— при токсическом поражении печени;
— наружных и внутренних кровотечениях (легочных, маточных, носовых, желудочно-кишечных).
Хлорид кальция принимают внутрь или вводят внутривенно (струйно или капельно). При быстром введении данного препарата могут возникнуть побочные действия: сначала жар во рту, позже – во всем теле. Запрещается вводить его внутримышечно и подкожно, так как он может вызвать сильное раздражение и даже некроз (омертвление) тканей. Первая помощь при попадании под кожу – отсосать шприцом. Противопоказан больным, склонным к тромбозам и с повышенным содержанием кальция в крови. Применять данный лекарственный препарат нужно только по назначению врача.
Кальций хлористый купить
«Прайм Кеммикалс Групп» — это магазин химических реактивов, который предлагает широкий ассортимент лабораторного оборудования и приборов, лабораторной посуды, фильтровальной бумаги, весов электронных лабораторных для научных и производственных целей.
Цена на хлористый кальций невелика, купить его можно и под заказ.
Как правильно пишется словосочетание «хлористый кальций»
- Как правильно пишется слово «хлористый»
- Как правильно пишется слово «кальций»
Делаем Карту слов лучше вместе
Привет! Меня зовут Лампобот, я компьютерная программа, которая помогает делать
Карту слов. Я отлично
умею считать, но пока плохо понимаю, как устроен ваш мир. Помоги мне разобраться!
Спасибо! Я стал чуточку лучше понимать мир эмоций.
Вопрос: стяжательство — это что-то нейтральное, положительное или отрицательное?
Ассоциации к слову «кальций»
Синонимы к словосочетанию «хлористый кальций»
Предложения со словосочетанием «хлористый кальций»
- Опрыскивание растений в теплице 0,3% – 0,4%-ным раствором хлористого кальция или подкормка кальциевой селитрой.
- Для этого в 1-2 л горячего молока добавьте б чайных ложек хлористого кальция.
- Для того чтобы приготовить такой творог, нужно заранее приобрести в аптеке хлористый кальций.
- (все предложения)
Цитаты из русской классики со словосочетанием «хлористый кальций»
- А дома всех встретили вонючей хлористой известью, «уксусом четырех разбойников» и такой диетой, которая одна без хлору и холеры могла свести человека в постель.
- Молебствие так же мало помогло от заразы, как хлористая известь; болезнь увеличивалась.
- (все
цитаты из русской классики)
Значение слова «хлористый»
-
ХЛО́РИСТЫЙ, —ая, —ое. Находящийся в соединении с хлором, содержащий хлор. Хлористый натрий (поваренная соль). Хлористый кальций. Хлористое железо. (Малый академический словарь, МАС)
Все значения слова ХЛОРИСТЫЙ
Значение слова «кальций»
-
КА́ЛЬЦИЙ, -я, м. Химический элемент, металл серебристо-белого цвета, входящий в состав известняков, мрамора и др. (Малый академический словарь, МАС)
Все значения слова КАЛЬЦИЙ
Отправить комментарий
Дополнительно
Смотрите также
ХЛО́РИСТЫЙ, —ая, —ое. Находящийся в соединении с хлором, содержащий хлор. Хлористый натрий (поваренная соль). Хлористый кальций. Хлористое железо.
Все значения слова «хлористый»
КА́ЛЬЦИЙ, -я, м. Химический элемент, металл серебристо-белого цвета, входящий в состав известняков, мрамора и др.
Все значения слова «кальций»
-
Опрыскивание растений в теплице 0,3% – 0,4%-ным раствором хлористого кальция или подкормка кальциевой селитрой.
-
Для этого в 1-2 л горячего молока добавьте б чайных ложек хлористого кальция.
-
Для того чтобы приготовить такой творог, нужно заранее приобрести в аптеке хлористый кальций.
- (все предложения)
- хлорид кальция
- глицерофосфат кальция
- сульфат кальция
- препараты кальция
- хлористый натрий
- (ещё синонимы…)
- витамин
- творожок
- кости
- зубы
- элемент
- (ещё ассоциации…)
- хлористый натрий
- хлористый калий
- хлористый кальций
- (полная таблица сочетаемости…)
- хлористый кальций
- кальция хлорид
- соли кальция
- кальций способствует
- усваивать кальций
- (полная таблица сочетаемости…)
- Разбор по составу слова «хлористый»
- Разбор по составу слова «кальций»
- Как правильно пишется слово «хлористый»
- Как правильно пишется слово «кальций»
| Хлорид кальция | |
|---|---|
 |
|
| Общие | |
| Систематическое наименование |
Хлорид кальция |
| Традиционные названия | Хлорид кальция, хлористый кальций |
| Хим. формула | CaCl2 |
| Рац. формула | CaCl2 |
| Физические свойства | |
| Молярная масса | 111,08 г/моль |
| Плотность | 2,15 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 772 °C |
| • кипения | 1935 °C |
| Химические свойства | |
Константа диссоциации кислоты  |
8—9 |
| Растворимость | |
| • в воде | 74,5 г/100 мл |
| Структура | |
| Координационная геометрия | Октаэдральная |
| Классификация | |
| Рег. номер CAS | 10043-52-4 |
| PubChem | 5284359 |
| Рег. номер EINECS | 233-140-8 |
| SMILES |
[Cl-].[Cl-].[Ca+2] |
| InChI |
InChI=1S/Ca.2ClH/h;2*1H/q+2;;/p-2 UXVMQQNJUSDDNG-UHFFFAOYSA-L |
| Кодекс Алиментариус | E509 |
| RTECS | EV9800000 |
| ChEBI | 3312 |
| ChemSpider | 23237 |
| Безопасность | |
| ЛД50 | 1,5-3,6 г/кг (крысы, перорально) |
| Токсичность | ПДК 2 мг/м³ |
| Фразы риска (R) | R36 |
| Фразы безопасности (S) | S22, S24 |
| Краткие характер. опасности (H) |
H319 |
| Меры предостор. (P) |
P280, P264, P305+P351+P338, P337+P313 |
| Пиктограммы СГС |
|
| NFPA 704 |
0 2 1 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Хлори́д ка́льция, CaCl2 — химическое неорганическое вещество; кальциевая соль соляной кислоты. Неядовит, зарегистрирован в качестве пищевой добавки E509.
Белые кристаллы плотностью 2,15 г/см³, температура плавления — 772 °C. Обладает высокими гигроскопическими свойствами. Растворимость (г на 100 г H2O): 74 (20 °C) и 159 (100 °C). Водные растворы хлорида кальция замерзают при низких температурах (20%-й — при -18,57 °C, 30%-й — при -48 °C).
CaCl2 образует гидрат CaCl2·6H2O, устойчивый до 29,8 °C; при более высоких температурах из насыщенного раствора выпадают кристаллогидраты с 4, 2 и 1 молекулами H2O. При смешении CaCl2*6H2O (58,8 %) со снегом или льдом (41,2 %) температура понижается до —55 °C (криогидратная точка).
Производство
Структура полимерного гексагидрата хлорида кальция [Ca(H2O)6]2+.
Природный минерал гексагидрата хлорида кальция, ставший известным как антарктицит[en], был впервые обнаружен на дне солёного озера Дон-Жуан на Земле Виктории в Антарктиде.
Получают как побочный продукт в производстве соды (в процессе рекуперации аммиака):
.
Во многих частях света хлорид кальция получается как побочный продукт из известняка по методу Сольве со следующей реакцией:[1]
- 2 NaCl + CaCO3 → Na2CO3 + CaCl2
Потребление в Северной Америке в 2002 году составляло 1529000 тонн.[2]
Как и в других солях, в хлориде кальция могут встречаться следовые количества других катионов щелочных и редкоземельных металлов групп 1 и 2, а также анионов других галогенов 17 группы таблицы химических элементов.
Применение
В химической лаборатории хлорид кальция применяется в качестве наполнителя для осушающих трубок[en], также называемых хлоркальциевыми, предназначенных для изоляции веществ в сосуде от водяных паров атмосферы и для осушки газов. В первом случае такая трубка прямая или согнута под углом 90 градусов и имеет один шарообразный участок, во втором она согнута в виде буквы U и имеет два шарообразных участка[3].
Хлорид кальция также применяют для получения металлического кальция, для осушки и понижения точки росы технологического и импульсного газа:
- на газораспределительных станциях, компрессорных станциях магистральных газопроводов;
- на автогазонаполнительных компрессорных станциях;
- на объектах газодобычи при подготовке газа к транспортировке.
Кроме того, он применяется в следующих областях:
- в смягчении говядины и баранины (снижение затрат на заморозку, хранение и погрузку);
- в консервировании овощей и фруктов (хранение яблок с пропиткой 8 % раствором)[4]
- как ускоритель схватывания цемента;
- как противогололёдное средство;
- как отвердитель в продуктах питания (загуститель для получения низкокалорийных желе);
- в молочной промышленности при производстве ферментированных молочных продуктов, и играет большую роль в формировании сгустка. Добавление хлористого кальция ведёт к увеличению выхода конечного продукта, а также улучшает его свойства;
- в медицине;
- в регулировании жёсткости воды при производстве слабоалкогольных и безалкогольных напитков;
- в изготовлении хлеба (консервант);
- при транспортировке замороженных грузов морем — для избежания замерзания воды в дренажной системе;
- для приготовления жидкости глушения при проведении ремонта на нефтяных и газовых скважинах.
- замораживание грунтов хлористым кальцием [5]
Обеспыливание грунтовых дорог

Разбрызгивание раствора хлорида кальция препятствует испарению влаги и образованию пыли.
Второе по массовости применение хлорида кальция использует гигроскопичность (стремление захватывать влагу) этого соединения, в результате чего образуется липкий гидрат. Концентрированный раствор делает поверхность грунтовой дороги немного влажной и предотвращает образование пыли. Удержанные в гидрате мелкие частички образуют липкий слой. Если бы этого не происходило, частички бы разлетались, приводя к смещению более крупных частиц и постепенному разрушению дороги. Использование хлорида кальция снижает необходимость в разравнивании дороги на 50% и на 80% снижает образование ям, которые необходимо заделывать.[6]
Возможная опасность
В малых количествах и при этом насыщенный влагой хлорид кальция не является токсичным материалом. Однако сухой хлорид кальция крайне гигроскопичен, что может являться источником опасности, поскольку при попадании на кожу интенсивно сушит и раздражает её. При растворении твёрдого хлорида кальция выделяется энергия, поэтому при употреблении внутрь этот экзотермический процесс может приводить к ожогам полости рта и внутренних органов. Употребление внутрь концентрированного раствора приводит к нарушению пищеварения и поражению внутренних органов.[7]
Употребление хлорида кальция может привести к гиперкальциемии.[8]
Примечания
- ↑ Robert Kemp, Suzanne E. Keegan «Calcium Chloride» in Ullmann’s Encyclopedia of Industrial Chemistry 2000, Wiley-VCH, Weinheim. doi:10.1002/14356007.a04_547
- ↑ Calcium Chloride SIDS Initial Assessment Profile, UNEP Publications, SIAM 15, Boston, 22–25 October 2002, страница 11.
- ↑ И. Э. Нифантьев, П. В. Ивченко «Практикум по органической химии» — см. с. 14—15.
- ↑ Химлайн : Пищевая добавка Е509 (Е-509) хлорид кальция : П : Реализация промышленной химии : Продукция и услуги. Дата обращения: 2 июня 2013. Архивировано из оригинала 16 ноября 2013 года.
- ↑ Замораживание грунтов
- ↑ Dust: Don’t Eat It! Control It! Road Management & Engineering Journal. US Roads (TranSafety Inc.) (1 июня 1998). Дата обращения: 9 августа 2006. Архивировано 29 октября 2007 года.
- ↑ Product Safety Assessment (PSA): Calcium Chloride. Dow Chemical Company (2 мая 2006). Дата обращения: 22 июля 2008. Архивировано 17 сентября 2009 года.
- ↑ Calcium Chloride Possible Side Affects.
Эта страница в последний раз была отредактирована 1 марта 2023 в 00:27.
Как только страница обновилась в Википедии она обновляется в Вики 2.
Обычно почти сразу, изредка в течении часа.







