Карбоксильная группа (карбоксил) -СООН — функциональная одновалентная группировка, входящая в состав карбоновых кислот и определяющая их кислотные свойства.
Строение карбоксильной группы
Карбоксильная группа
Карбоксильная группа сочетает в себе две функциональные группы — карбонил =CO и гидроксил -OH, взаимно влияющие друг на друга.
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду и вызванной этим дополнительной (по сравнению со спиртами) поляризации связи О-Н.
В водном растворе карбоновые кислоты диссоциируют на ионы:
R-COOH = R-COO− + H+
Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей.
С увеличением молекулярной массы растворимость кислот в воде уменьшается.
Карбоновые кислоты — это соединения, содержащие одну или несколько карбоксильных групп −COOH.
Строение карбоксильной группы
Карбоксильная группа образована двумя функциональными группами: карбонилом
−C|=O
и гидроксилом
−O−H
.
Между атомами углерода и кислорода карбонильной группы две связи: одна
σ
-связь и одна
π
-связь. Следовательно, атом углерода карбоксильной группы находится в состоянии
sp2
-гибридизации, углы между связями равны (120°).
Электроотрицательность кислорода выше по сравнению с углеродом и водородом, поэтому карбоксильная группа поляризована, и на атомах имеются частичные заряды.
Такое строение оказывает существенное влияние на физические и химические свойства карбоновых кислот.
В общем виде формулу карбоновых кислот можно записать следующим образом:
R−(COOH)n
.
В зависимости от числа функциональных групп кислоты делятся на одноосновные, двухосновные, трёхосновные и т. д.
По строению углеводородного радикала кислоты бывают предельные, непредельные, циклические, ароматические.
Общая формула одноосновных карбоновых кислот:
R−COOH
. Эта формула не подходит для самой простой кислоты — муравьиной (метановой), в которой функциональная группа соединена с атомом водорода:
H−COOH
.
Примеры разных кислот приведены в таблице.
|
Формула кислоты |
Название |
Группа |
| CH3−CH2−COOH | пропановая (пропионовая) кислота | предельная одноосновная |
| C17H35−COOH | стеариновая кислота | предельная одноосновная |
| CH2=CH−COOH | пропеновая (акриловая) кислота | непредельная одноосновная |
| C17H33−COOH | олеиновая кислота | непредельная одноосновная |
| C17H31−COOH | линолевая кислота | непредельная одноосновная |
| HOOC−COOH | щавелевая кислота | предельная двухосновная |
| HOOC−(CH2)4−COOH | адипиновая кислота | предельная двухосновная |
| C6H5−COOH | бензойная кислота | ароматическая одноосновная |
| HOOC−C6H4−COOH | терефталевая кислота | ароматическая двухосновная |
Источники:
Рисунок. Автор: De.Nobelium — собственная работа, Общественное достояние, https://commons.wikimedia.org/w/index.php?curid=1623926. 20.01.2022.
Строение карбоксильной группы -COOH
Карбоксильная группа –COOH, характер её химических связей, строение углеводородного радикала R и их взаимное влияние определяют свойства карбоновых кислот R–COOH.
Группа –COOHСтруктурная формула
карбоксильной группы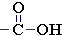
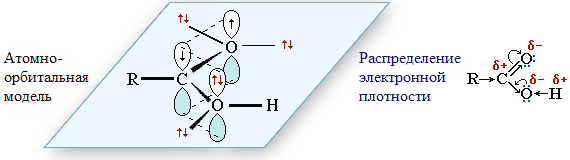
Для атомов углерода и кислорода группы >C=O характерно состояние sp2-гибридизации.
Атом кислорода ОН-группы, связанный в составе карбоксильной группы с sp2-атомом углерода, также имеет sp2-гибридизацию (часть I. sp2-Гибридизация).
Поэтому все три атома О(sp2)–С(sp2)–О(sp2) лежат в одной плоскости, а их негибридизованные p-орбитали расположены перпендикулярно этой плоскости. При перекрывании p-орбиталей образуется система сопряжения с делокализованными связями O…C…O, по которой передаётся взаимное влияние групп ОН и С=О.
Взаимное влияние атомов в молекулах карбоновых кислот характеризуется электронными эффектами атомных групп.
| Группа | Электронный эффект |
| >С=О | –I и –M |
| –ОН | +M и более слабый –I |
| –СООН | –I и –M* |
I — индуктивный эффект,
M — мезомерный эффект
* Для группы СООН при sp2 или sp-атоме радикала R.
В целом группа СООН по отношению к углеводородному радикалу R является электроноакцепторным заместителем.
Электронное строение карбоксильной группы придаёт карбоновым кислотам характерные свойства.
- Карбоксильная группа содержит три полярные ковалентные связи: С=О, С–О и О–Н, способные к гетеролитическому разрыву. Поэтому реакции с их участием идут в основном по ионному механизму.
- Смещение электронной плотности к карбонильному атому кислорода вызывает дополнительную, по сравнению со спиртами и фенолами, поляризацию связи О–Н, что определяет бо́льшую подвижность водородного атома, то есть более сильные кислотные свойства.
- Пониженная электронная плотность (δ+) на атоме углерода в СООН-группе способствует взаимодействию карбоновых кислот с нуклеофильными реагентамиНуклеофильные реагенты, или нуклеофилы — это частицы (анионы или молекулы), имеющие неподеленную пару электронов на внешнем электронном уровне и способные передать эти электроны на образование связи по донорно-акцепторному механизму.. При этом +М-эффект ОН-группы уменьшает частичный положительный заряд атома углерода в группе С=О. В отличие от альдегидов и кетонов, вступающих с нуклеофилами в реакцию нуклеофильного присоединения, для карбоновых кислот характерно нуклеофильное замещение группы –ОН.
- Атом кислорода в группе С=О, имея неподелённую пару электронов, способен присоединять протон Н+ (при действии сильной кислоты). Это играет важную роль в кислотном катализе реакций нуклеофильного замещения.
- Группа –СООН за счёт положительного заряда на атоме углерода снижает электронную плотность на связанном с ней углеводородном радикале R, то есть является по отношению к нему электроноакцепторным заместителем. В случае предельных кислот карбоксильная группа проявляет –I-эффект, а в непредельных (например, CH2=CH–COOH) и ароматических (С6Н5–СООН) — как –I, так и –М-эффект. Выступая в качестве заместителя, карбоксильная группа влияет на направление реакций, идущих по углеводородному радикалу.
- Атом водорода в полярной группе Оδ––Нδ+ одной молекулы кислоты и атом кислорода группы Сδ+=Оδ– другой молекулы способны к образованию межмолекулярной водородной связи –O–H…O=C, что во многом определяет физические свойства карбоновых кислот.
Что мы делаем. Каждая страница проходит через несколько сотен совершенствующих техник. Совершенно та же Википедия. Только лучше.
Карбоксильная группа
Из Википедии — свободной энциклопедии
Карбоксильная группа (карбоксил) -СООН — функциональная одновалентная группа, входящая в состав карбоновых кислот и за счет характера химических связей карбоксильной группы, строения углеводородного радикала R, а также их влияния друг на друга определяющая их кислотные свойства.
Строение карбоксильной группы

Карбоксильная группа
Атомы углерода и кислорода карбонильной группы находятся в состоянии sp2-гибридизации. Атом кислорода из гидроксильной группы связан в карбоксильной группе с sp2-атомом углерода, поэтому он тоже находится в состоянии sp2-гибридизации. По этой причине атомы
О(sp2)-С(sp2)-О(sp2) расположены в одной плоскости, в то время, как принадлежащие им негибридизированные р-орбитали размещаются перпендикулярно этой плоскости. Взаимное влияние карбонильной и гидроксильной групп передается системе сопряжения, которая образовалась при перекрывании р-орбиталей.
В карбоксильной группе есть три полярных ковалентных связи (С=О, С-О, О-Н), которые готовы к гетеролитическому разрыву. По этой причине реакции с участием этих групп атомов чаще всего проходят по ионному механизму.
Свойства водорода в карбоксиле
Карбоксильная группа сочетает в себе две функциональные группы — карбонил (>C=O) и гидроксил (-OH), взаимно влияющие друг на друга.
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду и вызванной этим дополнительной (по сравнению со спиртами) поляризации связи О-Н. Из-за этого атом водорода более подвижен, а значит кислотные свойства выражены сильнее.
Диссоциация
В водном растворе карбоновые кислоты диссоциируют на ионы:
R-COOH = R-COO− + H+
Растворимость
Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей.
С увеличением молекулярной массы растворимость кислот в воде уменьшается.
Взаимодействие с металлами
Замещение водорода карбоксила кислоты металлом происходит при взаимодействии с некоторыми достаточно активными металлами (реакция со щелочными металлами обычно происходит бурно), окислами некоторых металлов и щелочами (нейтрализация) с образованием солей[1].
Электролиз
Свойства гидроксила в карбоксиле
Взаимодействие с галогенами
Замещение гидроксила остатком кислоты
Замещение гидроксила остатком спирта
Замещение гидроксила остатком аммиака-аминогруппой
Замещение гидроксила остатком гидразина
Свойства карбонила в карбоксиле
Примечания
- ↑ Степаненко Б.Н. Курс органической химии. — С. 167-177. — 600 с.
Эта страница в последний раз была отредактирована 3 февраля 2022 в 10:22.
Как только страница обновилась в Википедии она обновляется в Вики 2.
Обычно почти сразу, изредка в течении часа.
Карбоксильная группа, карбоксил, карбоксигруппа –COOH – это одновалентная функциональная группа [1], входящая в состав карбоновых кислот [2], определяющая их кислотные свойства.
- Строение карбоксильной группы
- Примечания
Строение карбоксильной группы

Карбоксильная группа объединяет в себе две функциональные группы – карбонильную = CO [3] и гидроксильную –OH [4], оказывающие друг на друга взаимное влияние. Карбоксильная группа представляет собой сопряженную систему, в которой неразделенная пара электронов атома кислорода гидроксильной группы вступает в сопряжение с `0,-электронами карбонильной группы (р, R03,R03,п-сопряжение). Электронная плотность в сопряженной системе смещена в сторону атома кислорода карбонильной группы, неразделенные пары электронов которого не участвуют в процессе.
Вследствие смещения электронной плотности, связь О-Н оказывается сильно поляризованной, что приводит к появлению у карбоксильной группы ОН-кислотного центра. В то же время, за счет группы ОН, в молекулах карбоновых кислот частично положительный заряд на атоме углерода карбонильной группы несколько уменьшается, по сравнению с альдегидами [5] и кетонами [6]. Кроме того, в результате –І-эффекта карбоксильной группы в молекуле карбоновой кислоты происходит смещение электронной плотности углеводородного остатка, что приводит к появлению С-Н-кислотного центра при ^5,-карбоновом атоме.
Исходя из указанного строения карбоновых кислот, их основные реакции можно условно разделить на четыре группы:
- с участием связи О-Н (кислотные свойства),
- реакции нуклеофильного замещения с участием атома углерода карбонильной группы,
- замещения атомов водорода при ^5,-карбоновом атоме,
- окисления и восстановления.
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду, и, вызванной тем самым, дополнительной (по сравнению со спиртами) поляризацией связи О-Н.
В водном растворе карбоновые кислоты диссоциируют на ионы: R-COOH = R-COOW22, + H+
Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей.
С увеличением молекулярной массы растворимость кислот в воде уменьшается.
Наиболее известным фактом о карбоксильных группах является то, что они входят в состав аминокислот (одновременно с аминогруппами [7]).
Примечания
Примечания и пояснения к статье «Карбоксильная группа (карбоксигруппа)».
При написании статьи о карбоксильных группах (карбоксигруппах) в качестве источников использовались материалы информационных и справочных интернет-порталов, сайтов новостей Britannica.com, MedicineNet.com, Organic-Chemistry.org, Chemistry.Stanford.edu, ScienceDaily.com, SGU.ru, ULSU.ru, Википедия, а также следующие печатные издания:
- Ешкайт Х., Якубке Х.-Д. «Аминокислоты. Пептиды. Белки». Издательство «Мир», 1985 год, Москва,
- Кочетков Н. А., Членов М. А. (редакторы) «Общая органическая химия. Том 10». Издательство «Химия», 1986 год, Москва,
- Опейда Й., Швайка О. «Глоссарий терминов по химии». Издательство «Вебер» (донецкое отделение), 2008 год, Донецк.

Загрузка…
Как правильно пишется словосочетание «карбоксильная группа»
- Как правильно пишется слово «карбоксильный»
- Как правильно пишется слово «группа»
Делаем Карту слов лучше вместе
Привет! Меня зовут Лампобот, я компьютерная программа, которая помогает делать
Карту слов. Я отлично
умею считать, но пока плохо понимаю, как устроен ваш мир. Помоги мне разобраться!
Спасибо! Я стал чуточку лучше понимать мир эмоций.
Вопрос: хороводящий — это что-то нейтральное, положительное или отрицательное?
Ассоциации к слову «группа»
Синонимы к словосочетанию «карбоксильная группа»
Предложения со словосочетанием «карбоксильная группа»
- Присоединение происходит путём образования ковалентной связи между карбоксильной группой аминокислоты и гидроксильной группой третьего углеродного атома рибозы – 3′-OH.
- На одном конце пептида находится свободная аминогруппа, на другом – свободная карбоксильная группа.
- Когда аминокислота попадает в водный раствор, её карбоксильная группа обычно теряет протон, зато аминогруппа в тот же самый момент протон приобретает.
- (все предложения)
Цитаты из русской классики со словосочетанием «карбоксильная группа»
- В одно время здесь собралась группа молодежи. Тут был, во — первых, сын капитана, молодой артиллерийский офицер. Мы помнили его еще кадетом, потом юнкером артиллерийского училища. Года два он не приезжал, а потом явился новоиспеченным поручиком, в свежем с иголочки мундире, в блестящих эполетах и сам весь свежий, радостно сияющий новизной своего положения, какими-то обещаниями и ожиданиями на пороге новой жизни.
- Парни медленно, тесной группой подошли к Софье и жали ей руку молча, неуклюже ласковые. В каждом ясно было видно скрытое довольство, благодарное и дружеское, и это чувство, должно быть, смущало их своей новизной. Улыбаясь сухими от бессонной ночи глазами, они молча смотрели в лицо Софьи и переминались с ноги на ногу.
- Группа высланных выехала из России в сентябре 1922 года.
- (все
цитаты из русской классики)
Сочетаемость слова «группа»
- небольшие группы
съёмочная группа
оперативная группа - группа людей
группа армий
группа захвата - члены группы
состав группы
командир группы - группа остановилась
группа распалась
группа разделилась - присоединиться к группе
создать группу
увидеть группу - (полная таблица сочетаемости)
Значение словосочетания «карбоксильная группа»
-
Карбоксильная группа (карбоксил) -СООН — функциональная одновалентная группа, входящая в состав карбоновых кислот и определяющая их кислотные свойства (Википедия)
Все значения словосочетания КАРБОКСИЛЬНАЯ ГРУППА
Афоризмы русских писателей со словом «группа»
- Литератор должен понять, что он не только пишет пером, но — рисует словами и рисует не как мастер живописи, изображающий человека неподвижным, а пытается изобразить людей в непрерывном движении, в действии, в бесконечных столкновениях между собою, в борьбе классов, групп, единиц.
- Расизм — это спекулятивная подделка под борьбу за народные интересы. На самом деле расизм — это инструмент для манипулирования народом в карьеристских целях узкой реакционной группы.
- (все афоризмы русских писателей)
Отправить комментарий
Дополнительно
Карбоксильная группа -СООН — функциональная одновалентная группа, входящая в состав карбоновых кислот и определяющая их кислотные свойства.
Строение карбоксильной группы
Карбоксильная группа сочетает в себе две функциональные группы — карбонил (>C=O) и гидроксил (-OH), взаимно влияющие друг на друга.
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду и вызванной этим дополнительной (по сравнению со спиртами) поляризации связи О-Н.
В водном растворе карбоновые кислоты диссоциируют на ионы:
R-COOH = R-COO− + H+
Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей.
С увеличением молекулярной массы растворимость кислот в воде уменьшается.