Содержание
- Структурная формула
- Русское название
- Английское название
- Латинское название вещества Периндоприл
- Химическое название
- Брутто формула
- Фармакологическая группа вещества Периндоприл
- Нозологическая классификация
- Код CAS
- Фармакологическое действие
- Характеристика
- Фармакология
- Применение вещества Периндоприл
- Противопоказания
- Применение при беременности и кормлении грудью
- Побочные действия вещества Периндоприл
- Взаимодействие
- Передозировка
- Способ применения и дозы
- Меры предосторожности
- Источники информации
- Торговые названия с действующим веществом Периндоприл
Структурная формула
Русское название
Периндоприл
Английское название
Perindopril
Латинское название вещества Периндоприл
Perindoprilum (род. Perindoprili)
Химическое название
[2S-[1[R*(R*)],2альфа,3а бета,7а бета]]-1-[2-[[1-(Этоксикарбонил)бутил]амино]-1-оксопропил]-октагидро-1H-индол -2-карбоновая кислота (в виде трет-бутиламиновой и аргининовой соли)
Брутто формула
C19H32N2O5
Фармакологическая группа вещества Периндоприл
Фармакологическое действие
—
вазодилатирующее, гипотензивное, кардиопротективное, натрийуретическое, ингибирующее АПФ.
Характеристика
Ингибитор АПФ. Периндоприла эрбумин (трет-бутиламин) — белый кристаллический порошок. Легко растворим в воде (60 вес.%), спирте и хлороформе. Молекулярная масса 368,47 (свободная кислота); 441,61 (терт-бутиламиновая соль).
Периндоприл в форме свободной кислоты периндоприла эрбумина является пролекарством и метаболизируется in vivo путем гидролиза сложноэфирной группы с образованием периндоприлата, биологически активного метаболита.
Фармакология
Механизм действия
Периндоприла эрбумин — пролекарство, превращается в периндоприлат, который ингибирует АПФ у человека и животных. Механизм, посредством которого периндоприлат снижает АД, как полагают, заключается в основном в ингибировании активности АПФ. АПФ — пептидилдипептидаза, которая катализирует превращение неактивного декапептида, ангиотензина I, в вазоконстриктор, ангиотензин II. Ангиотензин II является сильным периферическим вазоконстриктором, который стимулирует секрецию альдостерона корой надпочечников и обеспечивает отрицательную обратную связь в отношении секреции ренина. Ингибирование АПФ приводит к снижению уровня ангиотензина II в плазме, что ведет к снижению вазоконстрикции, повышению активности ренина в плазме и снижению секреции альдостерона. Последнее приводит к диурезу и натрийурезу и может быть ассоциировано с небольшим увеличением сывороточного калия.
АПФ идентичен ферменту кининаза II, разрушающему брадикинин. Еще предстоит выяснить, играет ли повышенный уровень брадикинина, сильного вазодепрессорного пептида, роль в терапевтических эффектах периндоприла эрбумина.
В то время как основной механизм периндоприла в снижении АД, как полагают, осуществляется через РААС, ингибиторы АПФ оказывают некоторый эффект даже при очевидной гипертензии при низком содержании ренина. Периндоприл изучали у относительно небольшого количества пациентов негроидной расы, обычно имеющих низкое содержание ренина, и средний ответ дАД на периндоприл составлял примерно половину ответа, наблюдаемого у пациентов других рас, что согласуется с предыдущим опытом применения других ингибиторов АПФ.
Фармакодинамика
После приема периндоприла ингибирование АПФ зависит от дозы и концентрации в крови, при этом максимальное ингибирование 80–90% достигается при дозе 8 мг и сохраняется в течение 10–12 ч, через 24 ч ингибирование АПФ составляет около 60%. Степень ингибирования АПФ, достигаемая при данной дозе, со временем уменьшается (ID50 увеличивается). Прессорный ответ на инфузию ангиотензина I снижается периндоприлом, но этот эффект не такой стойкий, как эффект на АПФ; через 24 ч после применения дозы 12 мг наблюдается ингибирование примерно на 35%.
Фармакокинетика
Абсорбция
При пероральном приеме периндоприла эрбумина Cmax в плазме достигается примерно через 1 ч. Абсолютная биодоступность периндоприла при приеме внутрь — около 75%. После абсорбции примерно от 30 до 50% системно доступного периндоприла гидролизуется до его активного метаболита периндоприлата, средняя биодоступность которого составляет примерно 25%. Cmax периндоприлата в плазме достигаются через 3–7 ч после приема периндоприла. Прием периндоприла эрбумина с пищей существенно не снижает скорость или степень абсорбции периндоприла по сравнению с состоянием натощак. Однако степень биотрансформации периндоприла в активный метаболит периндоприлат снижается примерно на 43%, что приводит к снижению кривой ингибирования АПФ в плазме примерно на 20%, что, вероятно, клинически несущественно. В клинических испытаниях периндоприл обычно применяли не натощак.
При дозах периндоприла эрбумина 4, 8 и 16 мг Cmax и AUC периндоприла и периндоприлата увеличиваются пропорционально дозе как после однократного перорального приема, так и в равновесном состоянии при режиме многократного приема 1 раз в день.
Распределение
Примерно 60% циркулирующего периндоприла связывается с белками плазмы, и только 10–20% периндоприлата находится в связанном состоянии. Следовательно, взаимодействие с другими ЛС, опосредованное связыванием с белками, не ожидается.
Метаболизм и выведение
Фармакокинетика периндоприла после приема внутрь соответствует многокамерной модели, включая глубокий тканевый компартмент (места связывания АПФ). Средний Т1/2 периндоприла, ассоциированный с большей частью его выведения, составляет примерно от 0,8 до 1 ч.
Периндоприл экстенсивно метаболизируется после приема внутрь, и только от 4 до 12% дозы выводится в неизмененном виде с мочой. Было идентифицировано 6 метаболитов, образующихся в результате гидролиза, глюкуронизации и циклизации посредством дегидратации. К ним относятся активный ингибитор АПФ, периндоприлат (гидролизованный периндоприл), глюкурониды периндоприла и периндоприлата, дегидратированный периндоприл и диастереоизомеры дегидратированного периндоприлата. У человека печеночная эстераза, по-видимому, отвечает за гидролиз периндоприла.
Фармакокинетика активного метаболита периндоприлата также соответствует многокамерной модели после перорального приема периндоприла эрбумина. Образование периндоприлата происходит постепенно, Cmax в плазме достигается между 3 и 7 ч. Последующее снижение концентрации в плазме показывает кажущийся средний Т1/2 от 3 до 10 ч для большей части элиминации с пролонгированным конечным Т1/2 от 30 до 120 ч в результате медленной диссоциации периндоприлата из мест связывания АПФ плазма/ткань. При повторном пероральном приеме периндоприла 1 раз в день периндоприлат кумулирует, концентрация увеличивается примерно в 1,5–2 раза и достигает равновесного уровня в плазме через 3–6 дней. Клиренс периндоприлата и его метаболитов почти исключительно почечный.
Пожилой возраст
Концентрации периндоприла и периндоприлата в плазме крови у пожилых пациентов (старше 70 лет) примерно вдвое выше, чем у молодых пациентов, что отражает как повышенное превращение периндоприла в периндоприлат, так и снижение почечной экскреции периндоприлата.
Сердечная недостаточность
Клиренс периндоприлата снижается у пациентов с застойной сердечной недостаточностью, что приводит к увеличению AUC на 40% в интервале дозирования.
Нарушение функции почек
При дозах периндоприла от 2 до 4 мг AUC периндоприлата увеличивается при снижении функции почек. При Cl креатинина от 30 до 80 мл/мин AUC примерно вдвое больше, чем при 100 мл/мин. Когда Cl креатинина падает ниже 30 мл/мин, AUC увеличивается более заметно.
У ограниченного числа иcследованных пациентов клиренс периндоприла при диализе составлял примерно от 40 до 80 мл/мин. Клиренс периндоприлата при диализе варьировал от 40 до 90 мл/мин.
Нарушение функции печени
Биодоступность периндоприлата повышается у пациентов с нарушением функции печени. Концентрации периндоприлата в плазме у пациентов с нарушением функции печени были примерно на 50% выше, чем у здоровых субъектов или пациентов с гипертензией и нормальной функцией печени.
Доклиническая токсикология
Канцерогенность, мутагенность, влияние на фертильность
Канцерогенность. Каких-либо доказательств канцерогенного действия не наблюдалось в исследованиях у крыс и мышей при применении периндоприла в дозах, до 20 раз (мг/кг) или от 2 до 4 раз (мг/м2) превышающих максимальные предлагаемые клинические дозы (16 мг/сут), в течение 104 нед.
Мутагенность. Генотоксический потенциал периндоприла эрбумина, периндоприлата и других метаболитов не был обнаружен в различных исследованиях in vitro и in vivo, включая тест Эймса, тест на Saccharomyces cerevisiae D4, тест на культуре лимфоцитов человека, тест TK ± на клетках лимфомы мыши, микроядерные тесты на клетках костного мозга мыши, крысы и китайского хомячка.
Нарушение фертильности. Не наблюдалось значимого влияния на репродуктивную функцию или фертильность у крыс, получавших дозы, до 30 раз (мг/кг) или в 6 раз (мг/м2) превышающие предлагаемую максимальную клиническую дозу периндоприла эрбумина, в течение периода сперматогенеза у самцов или оогенеза и беременности у самок.
Клинические исследования
Гипертензия
В плацебо-контролируемых исследованиях при монотерапии периндоприлом (от 2 мг до 16 мг 1 раз в сутки) у пациентов со средним АД около 150/100 мм рт. ст. 2 мг оказали незначительный эффект, но дозы от 4 до 16 мг снижали АД. Дозы 8 мг и 16 мг были неотличимы, и обе имели больший эффект, чем доза 4 мг. В этих исследованиях дозы 8 мг и 16 мг в день приводили к снижению АД в положении лежа на спине на 9–15/5–6 мм рт. ст. При сравнении режимов дозирования 1 раз в день и 2 раза в день режим дозирования 2 раза в день в целом был немного лучше, но не более чем примерно на 0,5–1 мм рт. ст. После приема доз периндоприла от 2 до 16 мг минимальные средние эффекты на сАД и дАД составляли от 75 до 100% от пиковых эффектов.
Эффекты периндоприла на АД были схожими при приеме отдельно или на фоне 25 мг гидрохлоротиазида. В целом эффект периндоприла развивался быстро, с незначительным увеличением эффекта в течение нескольких недель.
Официальные исследования взаимодействия периндоприла эрбумина с другими гипотензивными средствами, кроме тиазидов, не проводили. Ограниченный опыт контролируемых и неконтролируемых исследований, в которых периндоприла эрбумин применяли в сочетании с БКК, петлевым диуретиком или в тройной терапии (бета-адреноблокатор, вазодилататор и диуретик), не свидетельствует о каком-либо неожиданном взаимодействии. В целом ингибиторы АПФ обладают меньшим, чем аддитивный, эффектом при применении вместе с бета-адреноблокаторами, предположительно потому, что последние частично действуют через РААС.
В неконтролируемых исследованиях у пациентов с инсулинозависимым диабетом периндоприл не влиял на гликемический контроль. При длительном применении у этих пациентов не наблюдалось влияния на экскрецию белка с мочой.
Эффективность периндоприла эрбумина не зависела от пола, он был менее эффективен у пациентов негроидной расы, чем у пациентов других рас. У пожилых пациентов (≥60 лет) влияние на среднее АД было несколько меньше, чем у более молодых пациентов, хотя разница не была значимой.
Стабильная ИБС
The EURopean trial On reduction of cardiac events with Perindopril in stable coronary Artery disease (EUROPA) — многоцентровое рандомизированное двойное слепое и плацебо-контролируемое исследование с участием 12218 пациентов со стабильной ИБС без клинических симптомов ХСН. У пациентов имелись доказательства ИБС, подтвержденные предшествующим инфарктом миокарда более чем за 3 мес до скрининга, коронарной реваскуляризацией более чем за 6 мес до скрининга, ангиографическими доказательствами стеноза (по крайней мере 70% сужение одной или нескольких крупных коронарных артерий) или положительным стресс-тестом у мужчин с болью в груди в анамнезе. После вводного периода продолжительностью 4 нед, в течение которого все пациенты получали периндоприл от 2 до 8 мг, пациенты были рандомизированы для получения периндоприла в дозе 8 мг 1 раз в день (n=6110) или плацебо (n=6108). Средний срок наблюдения составил 4,2 года. В исследовании изучалось долгосрочное влияние периндоприла на время до первого случая сердечно-сосудистой смертности, нефатального инфаркта миокарда или остановки сердца у пациентов со стабильной ИБС.
Средний возраст пациентов составлял 60 лет; 85% были мужского пола, 92% принимали ингибиторы агрегации тромбоцитов, 63% — бета-адреноблокаторы и у 56% проводилась гиполипидемическая терапия. Исследование EUROPA показало, что периндоприл значительно снижает относительный риск событий в первичной конечной точке (таблица 1). Этот положительный эффект во многом объясняется снижением риска нефатального инфаркта миокарда. Этот положительный эффект периндоприла на первичный результат был очевиден примерно через 1 год лечения. Результат был схожим для всех заранее отобранных подгрупп по возрасту, основному заболеванию или сопутствующему лечению.
Таблица 1
Первичная конечная точка и снижение относительного риска
| Периндоприл (n=6110) | Плацебо (n=6108) | Снижение относительного риска (95% ДИ) | Р | |
| Комбинированная конечная точка | ||||
| Смертность от сердечно-сосудистых заболеваний, нефатальный инфаркт миокарда или остановка сердца | 488 (8%) | 603 (9,9%) | 20% (от 9 до 29) | 0,0003 |
| Компонент конечной точки | ||||
| Смертность от сердечно-сосудистых заболеваний | 215 (3,5%) | 249 (4,1%) | 14% (от −3 до 28) | 0,107 |
| Нефатальный инфаркт миокарда | 295 (4,8%) | 378 (6,2%) | 22% (от10 до 33) | 0,001 |
| Остановка сердца | 6 (0,1%) | 11 (0,2%) | 46% (от −47 до 80) | 0,22 |
Применение вещества Периндоприл
Гипертензия
Лечение пациентов с эссенциальной гипертензией. Можно применять отдельно или вместе с другими классами гипотензивных средств, в особенности с тиазидными диуретиками.
Стабильная ИБС
Лечение пациентов со стабильной ИБС для снижения риска сердечно-сосудистой смертности или нефатального инфаркта миокарда. Можно применять со стандартным лечением ИБС, таким как антиагрегантная, гипотензивная или гиполипидемическая терапия.
Противопоказания
Гиперчувствительность (включая ангионевротический отек), в т.ч. к любому другому ингибитору АПФ, у пациентов с наследственным или идиопатическим ангионевротическим отеком, одновременное применение с алискиреном у пациентов с сахарным диабетом (см. «Взаимодействие»), в сочетании с ингибитором неприлизина (например, сакубитрил). Не следует применять периндоприла эрбумин в течение 36 ч после перехода на прием комбинации валсартан + сакубитрил (см. «Меры предосторожности»).
Применение при беременности и кормлении грудью
Беременность
Категория действия на плод по FDA — D.
Применение ЛС, влияющих на РААС, во II и III триместрах беременности снижает функцию почек плода и увеличивает заболеваемость и смертность плода и новорожденного. Возникающее в результате маловодие может быть ассоциировано с гипоплазией легких плода и деформациями скелета. Возможные побочные эффекты у новорожденных включают гипоплазию черепа, анурию, гипотензию, почечную недостаточность и смерть. Эти неблагоприятные исходы обычно связаны с применением этих ЛС во II и III триместрах беременности. При установлении беременности необходимо как можно скорее прекратить прием периндоприла эрбумина. В большинстве эпидемиологических исследований, посвященных изучению аномалий плода после экспозиции антигипертензивных средств в I триместре, не обнаружено отличий эффектов ЛС, влияющих на РААС, и других антигипертензивных средств.
Надлежащее управление материнской гипертензией во время беременности важно для оптимизации исходов как для матери, так и для плода.
В случае отсутствия подходящей альтернативы терапии ЛС, влияющими на РААС, у конкретной пациентки, женщина должна быть предупреждена о потенциальном риске для плода. Необходимо выполнять серийные УЗИ для оценки внутриамниотической среды. При возникновении маловодия следует прекратить прием периндоприла эрбумина, если эта терапия не является спасением жизни матери. В зависимости от срока беременности, может потребоваться тестирование плода. Однако следует иметь в виду, что маловодие может появиться только после того, как плод получит необратимое повреждение. Необходимо тщательное наблюдение за состоянием младенцев, которые in utero подверглись экспозиции периндоприла эрбумина, на предмет развития гипертензии, олигурии и гиперкалиемии (см. «Меры предосторожности»).
Радиоактивность была обнаружена у плодов после введения 14С-периндоприла беременным крысам.
Грудное вскармливание
Молоко лактирующих крыс содержало радиоактивность после введения 14C-периндоприла. Неизвестно, секретируется ли периндоприл в грудное молоко. Поскольку многие ЛС секретируются в грудное молоко, следует соблюдать осторожность при применении периндоприла эрбумина кормящими женщинами.
Побочные действия вещества Периндоприл
Поскольку клинические испытания проводятся с различным набором условий, частота встречаемости побочных реакций, наблюдаемых в этих испытаниях, не может непосредственно сравниваться с частотой в других клинических испытаниях и прогнозировать возникновение побочных эффектов в клинической практике.
Опыт клинических испытаний
Следующие побочные реакции обсуждаются в другом разделе:
— анафилактоидные реакции, включая ангионевротический отек (см. «Меры предосторожности»);
— гипотензия (см. «Меры предосторожности»);
— нейтропения и агранулоцитоз (см. «Меры предосторожности»);
— нарушение функции почек (см. «Меры предосторожности»);
— гиперкалиемия (см. «Меры предосторожности»);
— кашель (см. «Меры предосторожности»).
Гипертензия
Безопасность периндоприла эрбумина была оценена примерно у 3400 пациентов с гипертензией в клинических исследованиях в США и за рубежом. Представленные здесь данные основаны на результатах 1417 пациентов, получавших периндоприла эрбумин, которые участвовали в клинических испытаниях в США. Более 220 из этих пациентов получали периндоприла эрбумин в течение как минимум 1 года.
В плацебо-контролируемых клинических испытаниях в США частота преждевременного прекращения терапии из-за возникновения побочных эффектов составила 6,5% у пациентов, получавших периндоприла эрбумин, и 6,7% у пациентов, получавших плацебо. Наиболее частыми причинами были кашель, головная боль, астения и головокружение.
Среди 1012 пациентов в плацебо-контролируемых исследованиях в США общая частота отмеченных нежелательных явлений была сходной у пациентов, получавших периндоприла эрбумин, и у пациентов, получавших плацебо (примерно 75% в каждой группе). Единственными нежелательными явлениями, частота которых при приеме периндоприла эрбумина была по крайней мере на 2% выше, чем при приеме плацебо, были кашель (12% против 4,5%) и боль в спине (5,8% против 3,1%).
О головокружении в группе периндоприла (8,2%) сообщалось не чаще, чем в группе плацебо (8,5%), но его вероятность возрастала с увеличением дозы, что свидетельствует о причинной связи с приемом периндоприла.
Стабильная ИБС
Безопасность периндоприла оценивали в двойном слепом плацебо-контролируемом исследовании EUROPA с участием 12218 пациентов со стабильной ИБС. Общий показатель прекращения приема ЛС и плацебо составил около 22%. Наиболее частыми медицинскими причинами прекращения приема периндоприла, которые возникали чаще, чем в группе плацебо, были кашель, лекарственная непереносимость и гипотензия.
Постмаркетинговый опыт
Добровольные сообщения о побочных эффектах у пациентов, принимающих периндоприла эрбумин, которые были получены с момента его появления на фармацевтическом рынке и их причинно-следственная связь с приемом периндоприла эрбумина не установлена, включают следующие: остановка сердца, эозинофильный пневмонит, нейтропения/агранулоцитоз, панцитопения, анемия (включая гемолитическую и апластическую), тромбоцитопения, острая почечная недостаточность, нефрит, печеночная недостаточность, желтуха (гепатоцеллюлярная или холестатическая), симптоматическая гипонатриемия, буллезный пемфигоид, пузырчатка, острый панкреатит, падения, псориаз, эксфолиативный дерматит и синдром, который может включать артралгию/артрит, васкулит, серозит, лихорадку, сыпь или другие дерматологические проявления, положительный титр антинуклеарных антител, лейкоцитоз, эозинофилия или повышение СОЭ.
Результаты клинических лабораторных исследований
Гематология
Небольшое снижение Hb и гематокрита часто наблюдается у пациентов с гипертензией, принимающих периндоприла эрбумин, но редко имеет клиническое значение. В контролируемых клинических исследованиях ни один пациент не прекратил терапию из-за развития анемии. Лейкопения (включая нейтропению) наблюдалась у 0,1% пациентов в клинических испытаниях в США (см. «Меры предосторожности»).
Функциональные тесты печени
Повышение уровня АЛТ (1,6% периндоприла эрбумин против 0,9% плацебо) и АСТ (0,5% периндоприла эрбумин против 0,4% плацебо) наблюдалось в плацебо-контролируемых клинических испытаниях. Повышение обычно было умеренным и преходящим и исчезало после прекращения терапии.
Взаимодействие
Диуретики
У пациентов, принимающих диуретики, особенно недавно начавших лечение, может иногда наблюдаться чрезмерное снижение АД после начала терапии периндоприла эрбумином. Возможность гипотензивных эффектов можно свести к минимуму, уменьшив дозу или отменив диуретик, или увеличив потребление соли до начала лечения периндоприлом. Если диуретическую терапию нельзя изменить, необходимо обеспечить тщательный медицинский контроль при приеме первой дозы периндоприла эрбумина в течение как минимум 2 ч и до стабилизации АД в течение еще 1 ч (см. «Меры предосторожности»).
Сопутствующие диуретики не влияют на скорость и степень абсорбции и выведения периндоприла. Однако биодоступность периндоприлата снижалась диуретиками, что было ассоциировано со снижением ингибирования АПФ в плазме.
Калиевые добавки и калийсберегающие диуретики
Периндоприла эрбумин может повышать уровень калия в сыворотке крови из-за его способности снижать выработку альдостерона. Применение калийсберегающих диуретиков (в т.ч. спиронолактон, амилорид, триамтерен), калиевых добавок или других ЛС, способных повышать уровень калия в сыворотке (в т.ч. индометацин, гепарин, циклоспорин), может увеличить риск гиперкалиемии. Поэтому, если показано одновременное применение таких средств, необходим частый мониторинг уровня калия в сыворотке крови.
Литий
Сообщалось об увеличении содержания лития в сыворотке крови и симптомах литиевой токсичности у пациентов, получавших одновременно терапию литием и ингибиторами АПФ. Рекомендуется частый мониторинг концентрации лития в сыворотке крови. Применение диуретика может еще больше увеличить риск литиевой токсичности.
Препараты золота
Нитритоидные реакции (симптомы включают покраснение лица, тошноту, рвоту и гипотензию) редко наблюдались у пациентов, получавших инъекционно препарат золота (натрия ауротиомалат) и сопутствующую терапию ингибиторами АПФ, включая периндоприла эрбумин.
Дигоксин
Контролируемое фармакокинетическое исследование не показало влияния на концентрацию дигоксина в плазме при одновременном применении с периндоприла эрбумином, но не исключено влияние дигоксина на концентрацию периндоприла/периндоприлата в плазме.
Гентамицин
Данные у животных предполагают возможность взаимодействия периндоприла и гентамицина. Однако это не было изучено в исследованиях у людей.
НПВС, включая селективные ингибиторы ЦОГ-2
У пожилых людей, пациентов с недостаточным ОЦК (в т.ч. получающих терапию диуретиками) или с нарушенной функцией почек совместное применение НПВС, включая селективные ингибиторы ЦОГ-2, с ингибиторами АПФ, включая периндоприл, может приводить к ухудшению функции почек, включая возможную острую почечную недостаточность. Эти эффекты обычно обратимы. Необходим периодический мониторинг функции почек у пациентов, получающих периндоприл и НПВС.
Антигипертензивный эффект ингибиторов АПФ, включая периндоприл, может быть ослаблен НПВС, включая селективные ингибиторы ЦОГ-2.
Двойная блокада РААС
Двойная блокада РААС АРА II, ингибиторами АПФ или алискиреном ассоциирована с повышенным риском развития гипотензии, гиперкалиемии и изменений функции почек (включая острую почечную недостаточность) по сравнению с монотерапией. У большинства пациентов применение комбинации двух ингибиторов РААС не дает каких-либо дополнительных преимуществ по сравнению с монотерапией. В целом следует избегать сочетанного применения ингибиторов РААС. Необходим тщательный мониторинг АД, функции почек и электролитов у пациентов, принимающих периндоприла эрбумин и другие ЛС, влияющие на РААС.
Не следует принимать алискирен одновременно с периндоприла эрбумином пациентам с сахарным диабетом. Необходимо избегать применения алискирена с периндоприла эрбумином у пациентов с почечной недостаточностью (СКФ <60 мл/мин).
Ингибиторы mTOR
У пациентов, принимающих сопутствующую терапию ингибиторами mTOR (mammalian target of rapamycin — мишень рапамицина в клетках млекопитающих), может быть повышен риск развития ангионевротического отека (см. «Меры предосторожности»).
Ингибитор неприлизина
Пациенты, принимающие одновременно ингибиторы неприлизина, могут иметь повышенный риск развития ангионевротического отека (см. «Меры предосторожности»).
Передозировка
Дозы периндоприла до 2500 мг/кг у мышей, 3000 мг/кг у крыс и 1600 мг/кг у собак были нелетальными. Имеющийся опыт был ограниченным, но предполагал, что передозировка других ингибиторов АПФ также довольно хорошо переносится людьми. Наиболее вероятное проявление — гипотензия, лечение должно быть симптоматическим и поддерживающим. Терапию ингибитором АПФ следует прекратить и наблюдать за состоянием пациента. Обезвоживание, нарушение электролитного баланса и гипотензию следует лечить в соответствии с установленными процедурами.
Среди зарегистрированных случаев передозировки периндоприла пациенты, о которых известно, что они приняли дозу от 80 до 120 мг, нуждались во вспомогательной ИВЛ и поддержке кровообращения. Еще у одного пациента развилась гипотермия, остановка кровообращения, и он умер после проглатывания до 180 мг периндоприла. Вмешательство при передозировке периндоприла может потребовать интенсивной поддержки.
Лабораторные определения уровней периндоприла и его метаболитов в сыворотке крови не являются широко доступными, и такие определения, в любом случае, не играют главную роль в лечении передозировки периндоприла.
Нет данных, позволяющих предположить физиологические шаги (например, для изменения pH мочи), которые могли бы ускорить выведение периндоприла и его метаболитов. Периндоприл может быть удален путем гемодиализа с клиренсом 52 мл/ мин для периндоприла и 67 мл/мин для периндоприлата.
Ангиотензин II, предположительно, мог бы служить специфическим антагонистом-антидотом в лечении передозировки периндоприла, но ангиотензин II по существу недоступен за пределами исследовательских центров. Поскольку гипотензивный эффект периндоприла достигается за счет расширения сосудов и гиповолемии, передозировку периндоприла целесообразно лечить инфузией физиологического раствора.
Способ применения и дозы
Внутрь. Режим дозирования зависит от показаний, возраста, состояния пациента, сопутствующей терапии.
Меры предосторожности
Анафилактоидные и возможные связанные реакции
Возможно, поскольку ингибиторы АПФ влияют на метаболизм эйкозаноидов и полипептидов, включая эндогенный брадикинин, у пациентов, получающих ингибиторы АПФ (включая периндоприла эрбумин), может возникать целый ряд побочных эффектов, некоторые из которых являются серьезными. У пациентов негроидной расы, получающих ингибиторы АПФ, частота возникновения ангионевротического отека выше, чем у пациентов других рас.
Ангионевротический отек головы и шеи. Сообщалось о случаях ангионевротического отека лица, конечностей, губ, языка, голосовых складок или гортани у пациентов, получавших ингибиторы АПФ, включая периндоприла эрбумин (0,1% пациентов, получавших периндоприла эрбумин в клинических испытаниях в США). Ангионевротический отек, ассоциированный с поражением языка, голосовых складок или гортани, может быть фатальным. В таких случаях необходимо немедленно прекратить лечение периндоприла эрбумином и наблюдать за состоянием пациента до тех пор, пока отек не исчезнет. В тех случаях, когда отек локализуется в области языка, голосовых складок или гортани и может вызвать обструкцию дыхательных путей, следует немедленно назначить соответствующее лечение, например п/к введение раствора эпинефрина 1: 1000 (0,3–0,5 мл).
Отек слизистой оболочки ЖКТ. Сообщалось об отеке слизистой оболочки ЖКТ у пациентов, получавших ингибиторы АПФ. Эти пациенты жаловались на боль в животе (с тошнотой или рвотой или без них); в некоторых случаях у пациентов не было ангионевротического отека лица в анамнезе, и уровни С1-эстеразы были нормальными. Ангионевротический отек был диагностирован с помощью различных процедур, включая КТ брюшной полости или УЗИ, или во время операции, и симптомы исчезали после прекращения приема ингибитора АПФ. Ангионевротический отек кишечника следует включать в дифференциальный диагноз у пациентов, принимающих ингибиторы АПФ, при наличии боли в животе.
Гипотензия
Периндоприла эрбумин может вызывать симптоматическую гипотензию. Прием периндоприла эрбумина был ассоциирован с гипотензией у 0,3% пациентов с неосложненной гипертензией в плацебо-контролируемых исследованиях в США. Симптомы, связанные с ортостатической гипотонией, были зарегистрированы еще у 0,8% пациентов.
Симптоматическая гипотензия чаще всего возникает у пациентов со сниженным ОЦК или гипонатриемией в результате длительной терапии диуретиками, ограничения приема поваренной соли, у пациентов, находящихся на диализе, пациентов с диареей или рвотой.
Ингибиторы АПФ могут вызывать чрезмерную гипотензию и быть ассоциированы с олигурией или азотемией, а в редких случаях — с острой почечной недостаточностью и смертью. У пациентов с ИБС или цереброваскулярным заболеванием чрезмерное снижение АД может привести к инфаркту миокарда или нарушению мозгового кровообращения.
У пациентов с риском чрезмерной гипотензии терапию периндоприла эрбумином следует начинать при очень тщательном медицинском наблюдении. За состоянием пациентов следует внимательно наблюдать в течение первых двух недель лечения и всякий раз при увеличении дозы периндоприла эрбумина и/или диуретика.
При возникновении чрезмерной гипотензии пациенту следует немедленно придать положение лежа на спине и при необходимости провести в/в инфузию физиологического раствора. Лечение периндоприла эрбумином обычно можно продолжить после восстановления ОЦК и АД.
Нейтропения/агранулоцитоз
Прием ингибиторов АПФ ассоциирован с агранулоцитозом и угнетением костного мозга, чаще всего у пациентов с почечной недостаточностью, особенно у пациентов с коллагеновыми сосудистыми заболеваниями, такими как СКВ или склеродермия.
Фетальная токсичность — см. «Применение при беременности и кормлении грудью».
Нарушение функции почек
Вследствие ингибирования РААС можно ожидать изменения функции почек у чувствительных людей. Следует периодически контролировать функцию почек у пациентов, применяющих периндоприла эрбумин (см. «Взаимодействие»).
У пациентов с тяжелой застойной сердечной недостаточностью, у которых функция почек может зависеть от активности РААС, лечение ингибиторами АПФ, включая периндоприла эрбумин, может быть ассоциировано с олигурией, прогрессирующей азотемией и в редких случаях — с острой почечной недостаточностью и смертью.
У пациентов с гипертензией с односторонним или двусторонним стенозом почечной артерии может наблюдаться повышение азота мочевины крови и креатинина сыворотки; обычно эти явления обратимы после прекращения приема ингибитора АПФ. У таких пациентов следует контролировать функцию почек в течение первых нескольких недель терапии.
У некоторых пациентов, получавших периндоприла эрбумин, наблюдалось незначительное и транзиторное повышение уровня азота мочевины крови и креатинина сыворотки, особенно у тех, кто одновременно принимал диуретики.
Гиперкалиемия
Повышение уровня калия в сыворотке наблюдалось у некоторых пациентов, принимавших ингибиторы АПФ, включая периндоприла эрбумин. В большинстве случаев это были единичные однократные значения, которые не являлись клинически значимыми и редко являлись причиной отмены. Факторы риска развития гиперкалиемии включают почечную недостаточность, сахарный диабет и одновременный прием таких ЛС, как калийсберегающие диуретики, добавки калия и/или калийсодержащие заменители соли (см. «Взаимодействие»).
У пациентов, применяющих периндоприла эрбумин, следует периодически контролировать уровень калия в сыворотке крови.
Кашель
При применении всех ингибиторов АПФ сообщалось о возникновении постоянного непродуктивного кашля (предположительно, из-за ингибирования распада эндогенного брадикинина), который обычно прекращается после отмены терапии. При дифференциальной диагностике кашля следует учитывать кашель, связанный с применением ингибиторов АПФ.
Печеночная недостаточность
В редких случаях применение ингибиторов АПФ было ассоциировано с синдромом, который начинается с холестатической желтухи и прогрессирует до фульминантного некроза печени, а иногда и смерти. Механизм развития этого синдрома не выяснен. Пациенты, получающие ингибиторы АПФ, у которых развивается желтуха или заметное повышение уровня печеночных ферментов, должны прекратить прием ингибитора АПФ с последующим диспансерным наблюдением.
Хирургические вмешательства/общая анестезия
У пациентов во время хирургических вмешательств или проведения анестезии с применением ЛС, вызывающих гипотензию, периндоприла эрбумин может блокировать образование ангиотензина II, вызываемое компенсаторным высвобождением ренина. Гипотензия, связанная с этим механизмом, может быть скорректирована увеличением ОЦК.
Применение в педиатрии
Новорожденные с экспозицией периндоприла эрбумина in utero в анамнезе. При возникновении олигурии или гипотензии необходимо обратить внимание на поддержание АД и почечной перфузии. Могут потребоваться обменное переливание крови или диализ как средства устранения гипотензии и/или замещения нарушенной функции почек. Периндоприл, проникающий через плаценту, теоретически может быть удален из кровотока новорожденных с помощью этих способов, но ограниченный опыт не показал, что такое удаление является главным для лечения этих младенцев.
Безопасность и эффективность периндоприла эрбумина у педиатрических пациентов не установлены.
Применение в гериатрии
Среднее влияние периндоприла на АД было несколько меньше у пациентов старше 60 лет, чем у более молодых пациентов, хотя разница не была значимой. Концентрации периндоприла и периндоприлата в плазме были увеличены у пожилых пациентов по сравнению с концентрациями у более молодых пациентов. У пожилых пациентов не наблюдалось явного усиления побочных эффектов, за исключением головокружения и, возможно, сыпи.
Рекомендуется начинать прием с низкой дозы и постепенно увеличивать ее по мере необходимости. Необходимо контролировать головокружение из-за возможности падения.
Опыт применения периндоприла эрбумина у пожилых пациентов в суточных дозах, превышающих 8 мг, ограничен.
Почечная недостаточность
У пациентов с почечной недостаточностью может потребоваться корректировка дозы.
Печеночная недостаточность
Биодоступность периндоприлата увеличивается у пациентов с нарушением функции печени.
Источники информации
www.rxlist.com, 2021.
Торговые названия с действующим веществом Периндоприл
| Торговое название | Цена за упаковку, руб. |
|---|---|
| ПЕРИНДОПРИЛ АВЕКСИМА |
255.00 |
| ПЕРИНДОПРИЛ-АЛИУМ |
187.00 |
| Парнавел |
224.90 |
| Периндоприл |
от 116.00 до 496.00 |
| Периндоприл-ВЕРТЕКС |
от 226.00 до 226.00 |
| Периндоприл-СЗ |
от 153.00 до 405.00 |
| Периндоприл-Тева |
от 250.10 до 288.00 |
| Перинева® |
от 172.00 до 607.00 |
| Престариум® А |
от 211.00 до 526.00 |
From Wikipedia, the free encyclopedia
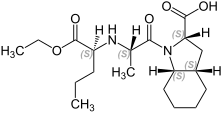 |
|
| Clinical data | |
|---|---|
| Trade names | Coversyl, Coversum, Aceon |
| AHFS/Drugs.com | Monograph |
| Routes of administration |
By mouth |
| ATC code |
|
| Legal status | |
| Legal status |
|
| Pharmacokinetic data | |
| Bioavailability | 24% |
| Protein binding | 20% |
| Metabolism | Kidney |
| Elimination half-life | 1–17 hours for perindoprilat (active metabolite) |
| Identifiers | |
|
IUPAC name
|
|
| CAS Number |
|
| PubChem CID |
|
| IUPHAR/BPS |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| ChEBI |
|
| ChEMBL |
|
| CompTox Dashboard (EPA) |
|
| ECHA InfoCard | 100.120.843 |
| Chemical and physical data | |
| Formula | C19H32N2O5 |
| Molar mass | 368.474 g·mol−1 |
| 3D model (JSmol) |
|
|
SMILES
|
|
|
InChI
|
|
| |
Perindopril is a medication used to treat high blood pressure, heart failure, or stable coronary artery disease.[2]
As a long-acting ACE inhibitor, it works by relaxing blood vessels and decreasing blood volume. As a prodrug, perindopril is hydrolyzed in the liver to its active metabolite, perindoprilat. It was patented in 1980 and approved for medical use in 1988.[3]
Perindopril is taken in the form of perindopril arginine (trade names include Coversyl, Coversum) or perindopril erbumine (Aceon). Both forms are therapeutically equivalent and interchangeable,[4] but the dose prescribed to achieve the same effect differs between the two forms. It is also often combined with another medication, sometimes in the same tablet (see #Combinations below).
Medical uses[edit]
Perindopril shares the indications of ACE inhibitors as a class, including essential hypertension, stable coronary artery disease (reduction of risk of cardiac events in patients with a history of myocardial infarction and/or revascularization), treatment of symptomatic coronary artery disease or heart failure, and diabetic nephropathy.[5]
Combination therapy[edit]
With indapamide[edit]
In combination with indapamide, perindopril has been shown to significantly reduce the progression of chronic kidney disease and renal complications in patients with type 2 diabetes.[6][7] In addition, the Perindopril pROtection aGainst REcurrent Stroke Study (PROGRESS) found that whilst perindopril monotherapy demonstrated no significant benefit in reducing recurrent strokes when compared to placebo, the addition of low dose indapamide to perindopril therapy was associated with larger reductions in both blood pressure lowering and recurrent stroke risk in patients with pre-existing cerebrovascular disease, irrespective of their blood pressure.[8] [9] There is evidence to support the use of perindopril and indapamide combination over perindopril monotherapy to prevent strokes and improve mortality in patients with a history of stroke, transient ischaemic attack or other cardiovascular disease.[8][10]
With amlodipine[edit]
The Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BLA) was a 2005 landmark trial that compared the effects of the established therapy of the combination of atenolol and bendroflumethiazide to the new drug combination of amlodipine and perindopril (trade names Viacoram, AceryCal etc.).[11] The study of more than 19 000 patients world-wide was terminated earlier than anticipated because it clearly demonstrated a statistically significant improvement in mortality and cardiovascular outcomes with the newer treatment. The combination of amlodipine and perindopril remains in the current treatment guidelines for hypertension and the outcomes of the ASCOT-BLA trial paved the way for further research into combination therapy and newer agents.[12]
Contraindications[edit]
- Children
- Pregnancy
- Lactation
- Situations where a patient has a history of hypersensitivity
- Kidney failure
Precautions[edit]
- Assess kidney function before and during treatment where appropriate.
- Renovascular hypertension
- Surgery/anesthesia
- An analysis on the PROGRESS trial showed that perindopril has key benefits in reducing cardiovascular events by 30% in patients with chronic kidney disease defined as a CrCl <60ml/min.[13] A 2016 and 2017 meta-analysis review looking at ACE inhibitors demonstrated a reduction in cardiovascular events but also slowed the decline of renal failure by 39% when compared to placebo.[14][15] These studies included patients with moderate to severe kidney disease and those on dialysis.
- Its renoprotective benefits of decreasing blood pressure and removing filtration pressure is highlighted in a 2016 review.[14] ACE inhibitor can result in an initial increase of serum creatinine, but mostly returns to baseline in a few weeks in majority of patients.[16] It has been suggested that increased monitoring, especially in advanced kidney failure, will minimise any related risk and improve long-term benefits.[17]
- Use cautiously in patients with sodium or volume depletion due to potential excessive hypotensive effects of renin-angiotensin blockade causing symptomatic hypotension.[5] Careful monitoring or short-term dose reduction of diuretics prior to commencing perindopril is recommended to prevent this potential effect.[5] A diuretic may later be given in combination if necessary; potassium-sparing diuretics are not recommended in combination with perindopril due to the risk of hyperkalaemia.[5]
- Combination with neuroleptics or imipramine-type drugs may increase the blood pressure lowering effect. Serum lithium concentrations may rise during lithium therapy.
Side effects[edit]
Side effects are mild, usually at the start of treatment; they include:
- Cough
- Fatigue
- Weakness/Asthenia
- Headache
- Disturbances of mood and/or sleep
Less often
- Taste impairment
- Epigastric discomfort
- Nausea
- Abdominal pain
- Rash
Reversible increases in blood urea and creatinine may be observed. Proteinuria has occurred in some patients. Rarely, angioneurotic edema and decreases in hemoglobin, red cells, and platelets have been reported.
Composition[edit]
Each tablet contains 2, 4, or 8 mg of the tert-butylamine salt of perindopril. Perindopril is also available under the trade name Coversyl Plus, containing 4 mg of perindopril combined with 1.25 mg indapamide, a thiazide-like diuretic.
In Australia, each tablet contains 2.5, 5, or 10 mg of perindopril arginine. Perindopril is also available under the trade name Coversyl Plus, containing 5 mg of perindopril arginine combined with 1.25 mg indapamide and Coversyl Plus LD, containing 2.5 mg of perindopril arginine combined with 0.625 mg indapamide.
The efficacy and tolerability of a fixed-dose combination of 4 mg perindopril and 5 mg amlodipine, a calcium channel antagonist, has been confirmed in a prospective, observational multicenter trial of 1,250 hypertensive patients.[18] A preparation of the two drugs is available commercially as Coveram.
Society and culture[edit]
Trade names[edit]
Perindopril is available under the following brand names among others:
- Acertil
- Actiprex
- Armix
- Idaprex
- Coverene
- Coverex
- Coversum
- Coversyl
- Covinace
- Indapril
- Perindo
- Perineva
- Prenessa
- Prestarium
- Preterax
- Prexanil
- Prexum
- Procaptan
- Provinace
- Pericard
- Percarnil
- Perindal
- Repres
- Relika
Marketing[edit]
On 9 July 2014, the European Commission imposed fines of €427,700,000 on Laboratoires Servier and 5 companies which produce generics due to Servier’s abuse of their dominant market position, in breach of European Union Competition law. Servier’s strategy had included acquiring the principal source of generic production of Perindopril and entering into several pay-for-delay agreements with potential generic competitors.[19]
References[edit]
- ^ «Search Page — Drug and Health Product Register». 23 October 2014.
- ^ «Consumer Medicine Information, GenRx Perindopril» (PDF). Clinical Resources, Medicine information for health professionals. Royal Australian College of General Practitioners. Archived from the original (PDF) on 2007-09-01.
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 467. ISBN 9783527607495.
- ^ «PBS For Health Professionals». Pharmaceutical Benefits Scheme. Australian Government Department of Health and Ageing. 2008. Archived from the original on 2008-10-30. Retrieved 2008-09-04.
- ^ a b c d «Australian Medicines Handbook». amhonline.amh.net.au. Retrieved 2020-05-10.
- ^ on behalf of the NIKA Study Group; Netchessova, T. A.; Shepelkevich, A. P.; Gorbat, T. V. (March 2014). «Efficacy of Single-Pill Perindopril/Indapamide in Patients with Hypertension and Type 2 Diabetes». High Blood Pressure & Cardiovascular Prevention. 21 (1): 63–69. doi:10.1007/s40292-013-0036-x. ISSN 1120-9879. PMID 24357222. S2CID 20819715.
- ^ Patel, Anushka (September 2007). «Effects of a fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomised controlled trial». The Lancet. 370 (9590): 829–840. doi:10.1016/s0140-6736(07)61303-8. ISSN 0140-6736. PMID 17765963. S2CID 21153924.
- ^ a b PROGRESS Collaborative Group (September 2001). «Randomised trial of a perindopril-based blood-pressure-lowering regimen among 6,105 individuals with previous stroke or transient ischaemic attack». Lancet. 2001 Sep 29. 358 (9287): 1033–41. doi:10.1016/s0140-6736(01)06178-5. PMID 11589932. S2CID 10053225.
- ^ PATS Collaborating Group (September 1995). «Post-stroke antihypertensive treatment study. A preliminary result». Chinese Medical Journal. 108 (9): 710–717. ISSN 0366-6999. PMID 8575241.
- ^ Beckett, NS; Peters, R; Fletcher, AE; et al. (May 2008). «HYVET Trial» (PDF). N. Engl. J. Med. 358 (18): 1887–98. doi:10.1056/NEJMoa0801369. PMID 18378519.
- ^ Dahlöf, Björn; Sever, Peter S; Poulter, Neil R; Wedel, Hans; Beevers, D Gareth; Caulfield, Mark; Collins, Rory; Kjeldsen, Sverre E; Kristinsson, Arni; McInnes, Gordon T; Mehlsen, Jesper (September 2005). «Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA): a multicentre randomised controlled trial». The Lancet. 366 (9489): 895–906. doi:10.1016/S0140-6736(05)67185-1. PMID 16154016. S2CID 26084146.
- ^ «Home | The Heart Foundation». www.heartfoundation.org.au. Retrieved 2020-05-10.
- ^ Perkovic, Vlado; Ninomiya, Toshiharu; Arima, Hisatomi; Gallagher, Martin; Jardine, Meg; Cass, Alan; Neal, Bruce; MacMahon, Stephen; Chalmers, John (October 2007). «Chronic Kidney Disease, Cardiovascular Events, and the Effects of Perindopril-Based Blood Pressure Lowering: Data from the PROGRESS Study». Journal of the American Society of Nephrology. 18 (10): 2766–2772. doi:10.1681/ASN.2007020256. ISSN 1046-6673. PMID 17804673.
- ^ a b Xie, Xinfang; Liu, Youxia; Perkovic, Vlado; Li, Xiangling; Ninomiya, Toshiharu; Hou, Wanyin; Zhao, Na; Liu, Lijun; Lv, Jicheng; Zhang, Hong; Wang, Haiyan (2016-05-01). «Renin-Angiotensin System Inhibitors and Kidney and Cardiovascular Outcomes in Patients With CKD: A Bayesian Network Meta-analysis of Randomized Clinical Trials». American Journal of Kidney Diseases. 67 (5): 728–741. doi:10.1053/j.ajkd.2015.10.011. ISSN 0272-6386. PMID 26597926.
- ^ Liu, Youxia; Ma, Xinxin; Zheng, Jie; Jia, Junya; Yan, Tiekun (2017-06-30). «Effects of angiotensin-converting enzyme inhibitors and angiotensin receptor blockers on cardiovascular events and residual renal function in dialysis patients: a meta-analysis of randomised controlled trials». BMC Nephrology. 18 (1): 206. doi:10.1186/s12882-017-0605-7. ISSN 1471-2369. PMC 5493067. PMID 28666408.
- ^ Garlo, Katherine G.; Bates, David W.; Seger, Diane L.; Fiskio, Julie M.; Charytan, David M. (2018-11-02). «Association of Changes in Creatinine and Potassium Levels After Initiation of Renin Angiotensin Aldosterone System Inhibitors With Emergency Department Visits, Hospitalizations, and Mortality in Individuals With Chronic Kidney Disease». JAMA Network Open. 1 (7): e183874. doi:10.1001/jamanetworkopen.2018.3874. ISSN 2574-3805. PMC 6324397. PMID 30646338.
- ^ Ohkuma, Toshiaki; Jun, Min; Rodgers, Anthony; Cooper, Mark E.; Glasziou, Paul; Hamet, Pavel; Harrap, Stephen; Mancia, Giuseppe; Marre, Michel; Neal, Bruce; Perkovic, Vlado (January 2019). «Acute Increases in Serum Creatinine After Starting Angiotensin-Converting Enzyme Inhibitor-Based Therapy and Effects of its Continuation on Major Clinical Outcomes in Type 2 Diabetes Mellitus: The ADVANCE Trial». Hypertension. 73 (1): 84–91. doi:10.1161/HYPERTENSIONAHA.118.12060. hdl:10044/1/66141. ISSN 0194-911X. PMID 30571562. S2CID 58547523.
- ^ Bahl VK, Jadhav UM, Thacker HP. Management of Hypertension with the Fixed Combination of Perindopril and Amlodipine in Daily Clinical Practice: Results from the STRONG Prospective, Observational, Multicenter Study. American Journal of Cardiovascular Drugs May 22, 2009; 9 (3): 135-42 Link text Archived 2011-07-07 at the Wayback Machine
- ^ «Antitrust: Commission fines Servier and five generic companies for curbing entry of cheaper versions of cardiovascular medicine». European Commission. 9 July 2014.
Further reading[edit]
- Wang JG, Pimenta E, Chwallek F (2014). «Comparative review of the blood pressure-lowering and cardiovascular benefits of telmisartan and perindopril». Vascular Health and Risk Management. 10: 189–200. doi:10.2147/VHRM.S59429. PMC 3983078. PMID 24741317.
- Shirley M, McCormack PL (October 2015). «Perindopril/amlodipine (Prestalia(®)): a review in hypertension». American Journal of Cardiovascular Drugs. 15 (5): 363–70. doi:10.1007/s40256-015-0144-1. PMID 26341621. S2CID 40807688.
- Bertrand ME, Vlachopoulos C, Mourad JJ (August 2016). «Triple Combination Therapy for Global Cardiovascular Risk: Atorvastatin, Perindopril, and Amlodipine». American Journal of Cardiovascular Drugs. 16 (4): 241–253. doi:10.1007/s40256-016-0175-2. PMID 27256435. S2CID 13318472.
- Ancion A, Tridetti J, Nguyen Trung ML, Oury C, Lancellotti P (December 2019). «A Review of the Role of Bradykinin and Nitric Oxide in the Cardioprotective Action of Angiotensin-Converting Enzyme Inhibitors: Focus on Perindopril». Cardiology and Therapy. 8 (2): 179–191. doi:10.1007/s40119-019-00150-w. PMC 6828891. PMID 31578675.
External links[edit]
- Official website
Media related to Perindopril at Wikimedia Commons
From Wikipedia, the free encyclopedia
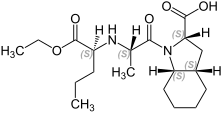 |
|
| Clinical data | |
|---|---|
| Trade names | Coversyl, Coversum, Aceon |
| AHFS/Drugs.com | Monograph |
| Routes of administration |
By mouth |
| ATC code |
|
| Legal status | |
| Legal status |
|
| Pharmacokinetic data | |
| Bioavailability | 24% |
| Protein binding | 20% |
| Metabolism | Kidney |
| Elimination half-life | 1–17 hours for perindoprilat (active metabolite) |
| Identifiers | |
|
IUPAC name
|
|
| CAS Number |
|
| PubChem CID |
|
| IUPHAR/BPS |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| ChEBI |
|
| ChEMBL |
|
| CompTox Dashboard (EPA) |
|
| ECHA InfoCard | 100.120.843 |
| Chemical and physical data | |
| Formula | C19H32N2O5 |
| Molar mass | 368.474 g·mol−1 |
| 3D model (JSmol) |
|
|
SMILES
|
|
|
InChI
|
|
| |
Perindopril is a medication used to treat high blood pressure, heart failure, or stable coronary artery disease.[2]
As a long-acting ACE inhibitor, it works by relaxing blood vessels and decreasing blood volume. As a prodrug, perindopril is hydrolyzed in the liver to its active metabolite, perindoprilat. It was patented in 1980 and approved for medical use in 1988.[3]
Perindopril is taken in the form of perindopril arginine (trade names include Coversyl, Coversum) or perindopril erbumine (Aceon). Both forms are therapeutically equivalent and interchangeable,[4] but the dose prescribed to achieve the same effect differs between the two forms. It is also often combined with another medication, sometimes in the same tablet (see #Combinations below).
Medical uses[edit]
Perindopril shares the indications of ACE inhibitors as a class, including essential hypertension, stable coronary artery disease (reduction of risk of cardiac events in patients with a history of myocardial infarction and/or revascularization), treatment of symptomatic coronary artery disease or heart failure, and diabetic nephropathy.[5]
Combination therapy[edit]
With indapamide[edit]
In combination with indapamide, perindopril has been shown to significantly reduce the progression of chronic kidney disease and renal complications in patients with type 2 diabetes.[6][7] In addition, the Perindopril pROtection aGainst REcurrent Stroke Study (PROGRESS) found that whilst perindopril monotherapy demonstrated no significant benefit in reducing recurrent strokes when compared to placebo, the addition of low dose indapamide to perindopril therapy was associated with larger reductions in both blood pressure lowering and recurrent stroke risk in patients with pre-existing cerebrovascular disease, irrespective of their blood pressure.[8] [9] There is evidence to support the use of perindopril and indapamide combination over perindopril monotherapy to prevent strokes and improve mortality in patients with a history of stroke, transient ischaemic attack or other cardiovascular disease.[8][10]
With amlodipine[edit]
The Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BLA) was a 2005 landmark trial that compared the effects of the established therapy of the combination of atenolol and bendroflumethiazide to the new drug combination of amlodipine and perindopril (trade names Viacoram, AceryCal etc.).[11] The study of more than 19 000 patients world-wide was terminated earlier than anticipated because it clearly demonstrated a statistically significant improvement in mortality and cardiovascular outcomes with the newer treatment. The combination of amlodipine and perindopril remains in the current treatment guidelines for hypertension and the outcomes of the ASCOT-BLA trial paved the way for further research into combination therapy and newer agents.[12]
Contraindications[edit]
- Children
- Pregnancy
- Lactation
- Situations where a patient has a history of hypersensitivity
- Kidney failure
Precautions[edit]
- Assess kidney function before and during treatment where appropriate.
- Renovascular hypertension
- Surgery/anesthesia
- An analysis on the PROGRESS trial showed that perindopril has key benefits in reducing cardiovascular events by 30% in patients with chronic kidney disease defined as a CrCl <60ml/min.[13] A 2016 and 2017 meta-analysis review looking at ACE inhibitors demonstrated a reduction in cardiovascular events but also slowed the decline of renal failure by 39% when compared to placebo.[14][15] These studies included patients with moderate to severe kidney disease and those on dialysis.
- Its renoprotective benefits of decreasing blood pressure and removing filtration pressure is highlighted in a 2016 review.[14] ACE inhibitor can result in an initial increase of serum creatinine, but mostly returns to baseline in a few weeks in majority of patients.[16] It has been suggested that increased monitoring, especially in advanced kidney failure, will minimise any related risk and improve long-term benefits.[17]
- Use cautiously in patients with sodium or volume depletion due to potential excessive hypotensive effects of renin-angiotensin blockade causing symptomatic hypotension.[5] Careful monitoring or short-term dose reduction of diuretics prior to commencing perindopril is recommended to prevent this potential effect.[5] A diuretic may later be given in combination if necessary; potassium-sparing diuretics are not recommended in combination with perindopril due to the risk of hyperkalaemia.[5]
- Combination with neuroleptics or imipramine-type drugs may increase the blood pressure lowering effect. Serum lithium concentrations may rise during lithium therapy.
Side effects[edit]
Side effects are mild, usually at the start of treatment; they include:
- Cough
- Fatigue
- Weakness/Asthenia
- Headache
- Disturbances of mood and/or sleep
Less often
- Taste impairment
- Epigastric discomfort
- Nausea
- Abdominal pain
- Rash
Reversible increases in blood urea and creatinine may be observed. Proteinuria has occurred in some patients. Rarely, angioneurotic edema and decreases in hemoglobin, red cells, and platelets have been reported.
Composition[edit]
Each tablet contains 2, 4, or 8 mg of the tert-butylamine salt of perindopril. Perindopril is also available under the trade name Coversyl Plus, containing 4 mg of perindopril combined with 1.25 mg indapamide, a thiazide-like diuretic.
In Australia, each tablet contains 2.5, 5, or 10 mg of perindopril arginine. Perindopril is also available under the trade name Coversyl Plus, containing 5 mg of perindopril arginine combined with 1.25 mg indapamide and Coversyl Plus LD, containing 2.5 mg of perindopril arginine combined with 0.625 mg indapamide.
The efficacy and tolerability of a fixed-dose combination of 4 mg perindopril and 5 mg amlodipine, a calcium channel antagonist, has been confirmed in a prospective, observational multicenter trial of 1,250 hypertensive patients.[18] A preparation of the two drugs is available commercially as Coveram.
Society and culture[edit]
Trade names[edit]
Perindopril is available under the following brand names among others:
- Acertil
- Actiprex
- Armix
- Idaprex
- Coverene
- Coverex
- Coversum
- Coversyl
- Covinace
- Indapril
- Perindo
- Perineva
- Prenessa
- Prestarium
- Preterax
- Prexanil
- Prexum
- Procaptan
- Provinace
- Pericard
- Percarnil
- Perindal
- Repres
- Relika
Marketing[edit]
On 9 July 2014, the European Commission imposed fines of €427,700,000 on Laboratoires Servier and 5 companies which produce generics due to Servier’s abuse of their dominant market position, in breach of European Union Competition law. Servier’s strategy had included acquiring the principal source of generic production of Perindopril and entering into several pay-for-delay agreements with potential generic competitors.[19]
References[edit]
- ^ «Search Page — Drug and Health Product Register». 23 October 2014.
- ^ «Consumer Medicine Information, GenRx Perindopril» (PDF). Clinical Resources, Medicine information for health professionals. Royal Australian College of General Practitioners. Archived from the original (PDF) on 2007-09-01.
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 467. ISBN 9783527607495.
- ^ «PBS For Health Professionals». Pharmaceutical Benefits Scheme. Australian Government Department of Health and Ageing. 2008. Archived from the original on 2008-10-30. Retrieved 2008-09-04.
- ^ a b c d «Australian Medicines Handbook». amhonline.amh.net.au. Retrieved 2020-05-10.
- ^ on behalf of the NIKA Study Group; Netchessova, T. A.; Shepelkevich, A. P.; Gorbat, T. V. (March 2014). «Efficacy of Single-Pill Perindopril/Indapamide in Patients with Hypertension and Type 2 Diabetes». High Blood Pressure & Cardiovascular Prevention. 21 (1): 63–69. doi:10.1007/s40292-013-0036-x. ISSN 1120-9879. PMID 24357222. S2CID 20819715.
- ^ Patel, Anushka (September 2007). «Effects of a fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomised controlled trial». The Lancet. 370 (9590): 829–840. doi:10.1016/s0140-6736(07)61303-8. ISSN 0140-6736. PMID 17765963. S2CID 21153924.
- ^ a b PROGRESS Collaborative Group (September 2001). «Randomised trial of a perindopril-based blood-pressure-lowering regimen among 6,105 individuals with previous stroke or transient ischaemic attack». Lancet. 2001 Sep 29. 358 (9287): 1033–41. doi:10.1016/s0140-6736(01)06178-5. PMID 11589932. S2CID 10053225.
- ^ PATS Collaborating Group (September 1995). «Post-stroke antihypertensive treatment study. A preliminary result». Chinese Medical Journal. 108 (9): 710–717. ISSN 0366-6999. PMID 8575241.
- ^ Beckett, NS; Peters, R; Fletcher, AE; et al. (May 2008). «HYVET Trial» (PDF). N. Engl. J. Med. 358 (18): 1887–98. doi:10.1056/NEJMoa0801369. PMID 18378519.
- ^ Dahlöf, Björn; Sever, Peter S; Poulter, Neil R; Wedel, Hans; Beevers, D Gareth; Caulfield, Mark; Collins, Rory; Kjeldsen, Sverre E; Kristinsson, Arni; McInnes, Gordon T; Mehlsen, Jesper (September 2005). «Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA): a multicentre randomised controlled trial». The Lancet. 366 (9489): 895–906. doi:10.1016/S0140-6736(05)67185-1. PMID 16154016. S2CID 26084146.
- ^ «Home | The Heart Foundation». www.heartfoundation.org.au. Retrieved 2020-05-10.
- ^ Perkovic, Vlado; Ninomiya, Toshiharu; Arima, Hisatomi; Gallagher, Martin; Jardine, Meg; Cass, Alan; Neal, Bruce; MacMahon, Stephen; Chalmers, John (October 2007). «Chronic Kidney Disease, Cardiovascular Events, and the Effects of Perindopril-Based Blood Pressure Lowering: Data from the PROGRESS Study». Journal of the American Society of Nephrology. 18 (10): 2766–2772. doi:10.1681/ASN.2007020256. ISSN 1046-6673. PMID 17804673.
- ^ a b Xie, Xinfang; Liu, Youxia; Perkovic, Vlado; Li, Xiangling; Ninomiya, Toshiharu; Hou, Wanyin; Zhao, Na; Liu, Lijun; Lv, Jicheng; Zhang, Hong; Wang, Haiyan (2016-05-01). «Renin-Angiotensin System Inhibitors and Kidney and Cardiovascular Outcomes in Patients With CKD: A Bayesian Network Meta-analysis of Randomized Clinical Trials». American Journal of Kidney Diseases. 67 (5): 728–741. doi:10.1053/j.ajkd.2015.10.011. ISSN 0272-6386. PMID 26597926.
- ^ Liu, Youxia; Ma, Xinxin; Zheng, Jie; Jia, Junya; Yan, Tiekun (2017-06-30). «Effects of angiotensin-converting enzyme inhibitors and angiotensin receptor blockers on cardiovascular events and residual renal function in dialysis patients: a meta-analysis of randomised controlled trials». BMC Nephrology. 18 (1): 206. doi:10.1186/s12882-017-0605-7. ISSN 1471-2369. PMC 5493067. PMID 28666408.
- ^ Garlo, Katherine G.; Bates, David W.; Seger, Diane L.; Fiskio, Julie M.; Charytan, David M. (2018-11-02). «Association of Changes in Creatinine and Potassium Levels After Initiation of Renin Angiotensin Aldosterone System Inhibitors With Emergency Department Visits, Hospitalizations, and Mortality in Individuals With Chronic Kidney Disease». JAMA Network Open. 1 (7): e183874. doi:10.1001/jamanetworkopen.2018.3874. ISSN 2574-3805. PMC 6324397. PMID 30646338.
- ^ Ohkuma, Toshiaki; Jun, Min; Rodgers, Anthony; Cooper, Mark E.; Glasziou, Paul; Hamet, Pavel; Harrap, Stephen; Mancia, Giuseppe; Marre, Michel; Neal, Bruce; Perkovic, Vlado (January 2019). «Acute Increases in Serum Creatinine After Starting Angiotensin-Converting Enzyme Inhibitor-Based Therapy and Effects of its Continuation on Major Clinical Outcomes in Type 2 Diabetes Mellitus: The ADVANCE Trial». Hypertension. 73 (1): 84–91. doi:10.1161/HYPERTENSIONAHA.118.12060. hdl:10044/1/66141. ISSN 0194-911X. PMID 30571562. S2CID 58547523.
- ^ Bahl VK, Jadhav UM, Thacker HP. Management of Hypertension with the Fixed Combination of Perindopril and Amlodipine in Daily Clinical Practice: Results from the STRONG Prospective, Observational, Multicenter Study. American Journal of Cardiovascular Drugs May 22, 2009; 9 (3): 135-42 Link text Archived 2011-07-07 at the Wayback Machine
- ^ «Antitrust: Commission fines Servier and five generic companies for curbing entry of cheaper versions of cardiovascular medicine». European Commission. 9 July 2014.
Further reading[edit]
- Wang JG, Pimenta E, Chwallek F (2014). «Comparative review of the blood pressure-lowering and cardiovascular benefits of telmisartan and perindopril». Vascular Health and Risk Management. 10: 189–200. doi:10.2147/VHRM.S59429. PMC 3983078. PMID 24741317.
- Shirley M, McCormack PL (October 2015). «Perindopril/amlodipine (Prestalia(®)): a review in hypertension». American Journal of Cardiovascular Drugs. 15 (5): 363–70. doi:10.1007/s40256-015-0144-1. PMID 26341621. S2CID 40807688.
- Bertrand ME, Vlachopoulos C, Mourad JJ (August 2016). «Triple Combination Therapy for Global Cardiovascular Risk: Atorvastatin, Perindopril, and Amlodipine». American Journal of Cardiovascular Drugs. 16 (4): 241–253. doi:10.1007/s40256-016-0175-2. PMID 27256435. S2CID 13318472.
- Ancion A, Tridetti J, Nguyen Trung ML, Oury C, Lancellotti P (December 2019). «A Review of the Role of Bradykinin and Nitric Oxide in the Cardioprotective Action of Angiotensin-Converting Enzyme Inhibitors: Focus on Perindopril». Cardiology and Therapy. 8 (2): 179–191. doi:10.1007/s40119-019-00150-w. PMC 6828891. PMID 31578675.
External links[edit]
- Official website
Media related to Perindopril at Wikimedia Commons
Периндоприл (Perindopril)
💊 Состав препарата Периндоприл
✅ Применение препарата Периндоприл
Описание активных компонентов препарата
Периндоприл
(Perindopril)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.05.12
Владелец регистрационного удостоверения:
Код ATX:
C09AA04
(Периндоприл)
Лекарственная форма
| Периндоприл |
Таб. 4 мг: 10, 20 или 30 шт. рег. №: ЛП-001215 |
Форма выпуска, упаковка и состав
препарата Периндоприл
Таблетки белого или белого с желтоватым или кремоватым оттенком цвета, плоскоцилиндрической формы с фаской; допускается легкая мраморность.
10 шт. — упаковки ячейковые контурные (алюминий/ПВХ) (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные (алюминий/ПВХ) (2) — пачки картонные.
10 шт. — упаковки ячейковые контурные (алюминий/ПВХ) (3) — пачки картонные.
20 шт. — банки полимерные с кольцом первого вскрытия (1) — пачки картонные.
30 шт. — банки полимерные с кольцом первого вскрытия (1) — пачки картонные.
20 шт. — банки (1) светозащитного стекла — пачки картонные.
30 шт. — банки (1) светозащитного стекла — пачки картонные.
Фармакологическое действие
Ингибитор АПФ. Является пролекарством, из которого в организме образуется активный метаболит периндоприлат. Полагают, что механизм антигипертензивного действия связан с конкурентным ингибированием активности АПФ, которое приводит к снижению скорости превращения ангиотензина I в ангиотензин II, являющийся мощным сосудосуживающим веществом. В результате уменьшения концентрации ангиотензина II происходит вторичное увеличение активности ренина плазмы за счет устранения отрицательной обратной связи при высвобождении ренина и прямое снижение секреции альдостерона. Благодаря сосудорасширяющему действию, уменьшает ОПСС (постнагрузку), давление заклинивания в легочных капиллярах (преднагрузку) и сопротивление в легочных сосудах; повышает минутный объем сердца и толерантность к нагрузке.
Гипотензивный эффект развивается в течение первого часа после приема периндоприла, достигает максимума через 4-8 ч и продолжается в течение 24 ч.
В клинических исследованиях при применении периндоприла (монотерапия или в комбинации с диуретиком) показано значительное снижение риска возникновения повторного инсульта (как ишемического, так и геморрагического), а также риска фатальных или приводящих к инвалидности инсультов; основных сердечно-сосудистых осложнений, включая инфаркт миокарда, в т.ч. с летальным исходом; деменции, связанной с инсультом; серьезных ухудшений когнитивных функций. Данные терапевтические преимущества были отмечены как у пациентов с артериальной гипертензией, так и при нормальном АД, независимо от возраста, пола, наличия или отсутствия сахарного диабета и типа инсульта.
Показано, что на фоне применения периндоприла третбутиламина в дозе 8 мг/сут (эквивалентно 10 мг периндоприла аргинина) у пациентов со стабильной ИБС, отмечается существенное снижение абсолютного риска осложнений, предусмотренных основным критерием эффективности (смертность от сердечно-сосудистых заболеваний, частота нефатального инфаркта миокарда и/или остановки сердца с последующей успешной реанимацией) на 1.9%. У пациентов, ранее перенесших инфаркт миокарда или процедуру коронарной реваскуляризации, снижение абсолютного риска составило 2.2% по сравнению с группой плацебо.
Периндоприл применяется как в виде монотерапии, так и в виде фиксированных комбинаций с индапамидом, с амлодипином.
Фармакокинетика
После приема внутрь периндоприл быстро абсорбируется из ЖКТ. Cmax достигается через 1 ч. Биодоступность составляет 65-70%.
В процессе метаболизма периндоприл биотрансформируется с образованием активного метаболита — периндоприлата (около 20%) и 5 неактивных соединений. Cmax периндоприлата в плазме достигается между 3 и 5 ч после приема. Связывание периндоприлата с белками плазмы крови незначительное (менее 30%) и зависит от концентрации активного вещества. Vd свободного периндоприлата близок к 0.2 л/кг.
Не кумулирует. Повторный прием не приводит к кумуляции и T1/2 соответствует периоду его активности.
При приеме во время еды метаболизм периндоприла замедляется.
T1/2 периндоприла составляет 1 ч.
Периндоприлат выводится из организма почками; T1/2 его свободной фракции составляет 3-5 ч.
У пожилых пациентов, а также при почечной и сердечной недостаточности выведение периндоприлата замедляется.
Показания активных веществ препарата
Периндоприл
Артериальная гипертензия.
Хроническая сердечная недостаточность.
Профилактика повторного инсульта (комбинированная терапия с индапамидом) у пациентов, перенесших инсульт или транзиторное нарушение мозгового кровообращения по ишемическому типу.
Стабильная ИБС: снижение риска сердечно-сосудистых осложнений у больных со стабильной ИБС.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Начальная доза — 1-2 мг/сут в 1 прием. Поддерживающие дозы — 2-4 мг/сут при застойной сердечной недостаточности, 4 мг (реже — 8 мг) — при артериальной гипертензии в 1 прием.
При нарушениях функции почек требуется коррекция режима дозирования в зависимости от значений КК.
Побочное действие
Со стороны системы кроветворения: эозинофилия, снижение гемоглобина и гематокрита, тромбоцитопения, лейкопения/нейтропения, агранулоцитоз, панцитопения, гемолитическая анемия у пациентов с врожденным дефицитом глюкозо-6-фосфатдегидрогеназы.
Со стороны обмена веществ: гипогликемия, гиперкалиемия, обратимая после отмены препарата, гипонатриемия.
Со стороны нервной системы: парестезия, головная боль, головокружение, вертиго, нарушения сна, лабильность настроения, сонливость, обморок, спутанность сознания.
Со стороны органов чувств: нарушения зрения, шум в ушах.
Со стороны сердечно-сосудистой системы: чрезмерное снижение АД и связанные с этим симптомы, васкулит, тахикардия, ощущение сердцебиения, нарушения сердечного ритма, стенокардия, инфаркт миокарда и инсульт, возможно, вследствие чрезмерного снижения АД у пациентов из группы высокого риска.
Со стороны дыхательной системы: кашель, одышка, бронхоспазм, эозинофильная пневмония, ринит.
Со стороны пищеварительной системы: запор, тошнота, рвота, боль в животе, нарушение вкуса, диспепсия, диарея, сухость слизистой оболочки полости рта, панкреатит, гепатит (холестатический или цитолитический).
Со стороны кожных покровов и подкожно-жировой клетчатки: кожный зуд, сыпь, фотосенсибилизация, пузырчатка, повышенное потоотделение.
Аллергические реакции: ангионевротический отек, крапивница, многоформная эритема.
Со стороны костно-мышечной системы: спазмы мышц, артралгия, миалгия.
Со стороны мочевыделительной системы: почечная недостаточность, острая почечная недостаточность.
Со стороны репродуктивной системы: эректильная дисфункция.
Общие реакции: астения, боль в грудной клетке, периферические отеки, слабость, лихорадка, падения.
Со стороны лабораторных показателей: повышение активности печеночных трансаминаз и билирубина в сыворотке крови, повышение концентрации мочевины и креатинина в плазме крови.
Противопоказания к применению
Ангионевротический отек в анамнезе, одновременное применение с алискиреном и алискиренсодержащими препаратами у пациентов с сахарным диабетом или нарушениями функции почек (СКФ <60 мл/мин/1.73 м2), беременность, лактация, детский и подростковый возраст до 18 лет, повышенная чувствительность к периндоприлу, повышенная чувствительность к другим ингибиторам АПФ.
Применение при беременности и кормлении грудью
Периндоприл противопоказан к применению при беременности и в период лактации (грудного вскармливания).
Применение при нарушениях функции почек
При нарушениях функции почек требуется коррекция режима дозирования в зависимости от значений КК.
Применение у детей
Противопоказан в детском возрасте.
Особые указания
С осторожностью следует применять периндоприл при двустороннем стенозе почечных артерий или стенозе почечной артерии единственной почки; почечной недостаточности; системных заболеваниях соединительной ткани; терапии иммуносупрессорами, аллопуринолом, прокаинамидом (риск развития нейтропении, агранулоцитоза); сниженном ОЦК (прием диуретиков, диета с ограничением соли, рвота, диарея); стенокардии; цереброваскулярных заболеваниях; реноваскулярной гипертензии; сахарном диабете; хронической сердечной недостаточности IV функционального класса по классификации NYHA; одновременно с калийсберегающими диуретиками, препаратами калия, калийсодержащими заменителями пищевой соли, с препаратами лития; при гиперкалиемии; хирургическом вмешательстве/общей анестезии; гемодиализе с использованием высокопроточных мембран; десенсибилизирующей терапии; аферезе ЛПНП; состоянии после трансплантации почки; аортальном стенозе/митральном стенозе/гипертрофической обструктивной кардиомиопатии; у пациентов негроидной расы.
Сообщалось о случаях артериальной гипотензии, обмороке, инсульте, гиперкалиемии и нарушениях функции почек (включая острую почечную недостаточность) у предрасположенных пациентов, особенно при одновременном применении с лекарственными препаратами, которые влияют на РААС. Поэтому двойная блокада РААС в результате сочетания ингибитора АПФ с антагонистом рецепторов ангиотензина II или алискиреном не рекомендуется.
Перед началом лечения периндоприлом всем больным рекомендуется исследование функции почек.
Во время лечения периндоприлом следует регулярно контролировать функцию почек, активность печеночных ферментов в крови, проводить анализы периферической крови (особенно у больных с диффузными заболеваниями соединительной ткани, у больных, которые получают иммунодепрессивные средства, аллопуринол). Пациентам с дефицитом натрия и жидкости перед началом лечения необходимо провести коррекцию водно-электролитных нарушений.
Лекарственное взаимодействие
Риск развития гиперкалиемии повышается при одновременном применении периндоприла с другими препаратами, которые способны вызывать гиперкалиемию: алискирен и алискиренсодержащие препараты, соли калия, калийсберегающие диуретики, ингибиторы АПФ, антагонисты рецепторов ангиотензина II, НПВС, гепарин, иммунодепрессанты, такие как циклоспорин или такролимус, триметоприм.
При одновременном применении с алискиреном у пациентов с сахарным диабетом или нарушениями функции почек (СКФ <60 мл/мин) возрастает риск гиперкалиемии, ухудшения функции почек и повышения частоты сердечно-сосудистой заболеваемости и смертности (у пациентов этих групп данная комбинация противопоказана).
Не рекомендуется одновременное применение с алискиреном у пациентов, не имеющих сахарного диабета или нарушений функции почек, т.к. возможно повышение риска гиперкалиемии, ухудшения функции почек и повышения частоты сердечно-сосудистой заболеваемости и смертности.
В литературе сообщалось, что у пациентов с установленным атеросклеротическим заболеванием, сердечной недостаточностью или сахарным диабетом с поражением органов-мишеней, одновременная терапия ингибитором АПФ и антагонистом рецепторов ангиотензина II связана с более высокой частотой развития гипотензии, обморока, гиперкалиемии и ухудшения функции почек (включая острую почечную недостаточность) по сравнению с применением только одного препарата, влияющего на РААС. Двойная блокада (например, при сочетании ингибитора АПФ с антагониста рецепторов ангиотензина II) должна быть ограничена отдельными случаями с тщательным мониторингом функции почек, содержания калия и АД.
Одновременное применение с эстрамустином может привести к повышению риска побочных эффектов, таких как ангионевротический отек.
При одновременном применении препаратов лития и периндоприла возможно обратимое увеличение концентрации лития в сыворотке крови и связанные с этим токсические эффекты (данная комбинация не рекомендуется).
Одновременное применение с гипогликемическими препаратами (инсулин, гипогликемические средства для приема внутрь) требует особой осторожности, т.к. ингибиторы АПФ, в т.ч. периндоприл, могут усиливать гипогликемический эффект этих препаратов вплоть до развития гипогликемии. Как правило, это наблюдается в первые недели проведения одновременной терапии и у пациентов с нарушением функции почек.
Баклофен усиливает антигипертензивный эффект периндоприла, при одновременном применении может потребоваться коррекция дозы последнего.
У пациентов, получающих диуретики, особенно выводящие жидкость и/или соли, в начале терапии периндоприлом может наблюдаться чрезмерное снижение АД, риск развития которого можно уменьшить путем отмены диуретического средства, восполнением потери жидкости или солей перед началом терапии периндоприлом, а также применением периндоприла в низкой начальной дозе с дальнейшим постепенным ее увеличением.
При хронической сердечной недостаточности в случае применения диуретиков периндоприл следует применять в низкой дозе, возможно после уменьшения дозы применяемого одновременно калийнесберегающего диуретика. Во всех случаях функцию почек (концентрация креатинина) следует контролировать в первые недели применения ингибиторов АПФ.
Применение эплеренона или спиронолактона в дозах от 12.5 мг до 50 мг/сут и ингибиторов АПФ (в т.ч. периндоприла) в низких дозах: при терапии сердечной недостаточности II-IV функционального класса по классификации NYHA с фракцией выброса левого желудочка <40% и ранее применявшимися ингибиторами АПФ и «петлевыми» диуретиками, существует риск развития гиперкалиемии (с возможным летальным исходом), особенно в случае несоблюдения рекомендаций относительно этой комбинации. Перед применением данной комбинации необходимо убедиться в отсутствии гиперкалиемии и нарушений функции почек. Рекомендуется регулярно контролировать концентрацию креатинина и калия в крови — еженедельно в первый месяц лечения и ежемесячно в последующем.
Одновременное применение периндоприла с НПВС (ацетилсалициловая кислота в дозе, оказывающей противовоспалительное действие, ингибиторы ЦОГ-2 и неселективные НПВС) может привести к снижению антигипертензивного действия ингибиторов АПФ. Одновременное применение ингибиторов АПФ и НПВС может приводить к ухудшению функции почек, включая развитие острой почечной недостаточности, и увеличению содержания калия в сыворотке крови, особенно у пациентов со сниженной функцией почек. С осторожностью применять данную комбинацию у пациентов пожилого возраста. Пациенты должны получать адекватное количество жидкости; рекомендуется тщательно контролировать функцию почек, как в начале, так и в процессе лечения.
Гипотензивный эффект периндоприла может усиливаться при одновременном применении с другими антигипертензивными препаратами, сосудорасширяющими средствами, включая нитраты короткого и пролонгированного действия.
Одновременное применение глиптинов (линаглиптин, саксаглиптин, ситаглиптин, вилдаглиптин) с ингибиторами АПФ (в т.ч. с периндоприлом) может повышать риск развития ангионевротического отека вследствие подавления активности дипептидилпептидазы IV глиптином.
Одновременное применение периндоприла с трициклическими антидепрессантами, антипсихотическими препаратами и средствами для общей анестезии может приводить к усилению антигипертензивного действия.
Симпатомиметики могут ослаблять антигипертензивный эффект периндоприла.
При применении ингибиторов АПФ, в т.ч. периндоприла, у пациентов, получающих в/в препарат золота (натрия ауротиомалат), был описан симптомокомплекс, при котором наблюдались гиперемия кожи лица, тошнота, рвота, артериальная гипотензия.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
Арентопрес
(TORRENT PHARMACEUTICALS, Индия)
Парнавел
(АТОЛЛ, Россия)
Периндоприл
(PFIZER, США)
Периндоприл
(ПРАНАФАРМ, Россия)
Периндоприл
(TAD PHARMA, Германия)
Периндоприл
(ИЗВАРИНО ФАРМА, Россия)
Периндоприл
(ОЗОН, Россия)
Периндоприл
(БИОХИМИК, Россия)
Периндоприл Авексима
(ИРБИТСКИЙ ХФЗ, Россия)
Периндоприл-Алиум
(АЛИУМ, Россия)
Все аналоги
Поиск лекарств и товаров в аптеках Москвы
Введите название
Регион
Москва
Местоположение
Стабильная ИБС
При развитии эпизода нестабильной стенокардии (значительного или нет) в течение первого месяца терапии
препаратом Периндоприл необходимо оценить соотношение польза/риск при терапии данным препаратом.
Артериальная гипотензия
Ингибиторы АПФ могут вызвать резкое снижение АД. У пациентов с неосложненной артериальной гипертензией симптоматическая артериальная гипотензия развивается редко.
Риск чрезмерного снижения АД повышен у пациентов со сниженным объемом циркулирующей крови (ОЦК), что может отмечаться на фоне терапии диуретиками, при соблюдении строгой бессолевой диеты, гемодиализа, а также при диарее или рвоте, или с тяжелой ренин-зависимой артериальной гипертензией (см. разделы
«Взаимодействие с другими лекарственными средствами», «Побочное действие»).
Симптоматическая артериальная гипотензия может наблюдаться у пациентов с клиническими
проявлениями сердечной недостаточности, как при наличии сопутствующей почечной недостаточности, так и при её отсутствии.
Наиболее часто выраженная артериальная гипотензия может развиться у пациентов с более тяжелой ХСН, принимающих «петлевые» диуретики в высоких дозах, а также на фоне гипонатриемии или почечной недостаточности. Этим пациентам рекомендуется тщательное медицинское наблюдение в начале терапии и при титровании доз препарата Периндоприл. Подобный подход применяется и у пациентов со стенокардией и
цереброваскулярными заболеваниями, у которых выраженная артеральная гипотензия может привести к инфаркту миокарда или нарушению мозгового кровообращения.
В случае развития артериальной гипотензии необходимо придать пациенту горизонтальное положение с приподнятыми ногами, и при необходимости ввести внутривенно 0,9% раствор натрия хлорида для увеличения ОЦК.
Транзиторная артериальная гипотензия не является противопоказанием для дальнейшей терапии. После восстановления ОЦК и АД лечение может быть продолжено при условии тщательного подбора дозы препарата. У некоторых пациентов с ХСН и нормальным или низким АД во время терапии препаратом Периндоприл может произойти дополнительное снижение АД. Этот эффект ожидаем и обычно не является основанием для отмены препарата. Если артериальная гипотензия сопровождается клиническими проявлениями, может потребоваться уменьшение дозы или отмена препарата Периндоприл.
Митральный стеноз/аортальный стеноз/гипертрофическая обструктивная кардиомиопатия
Периндоприл, как и другие ингибиторы АПФ, должен с осторожностью назначаться пациентам с обструкцией выходного тракта левого желудочка (аортальный стеноз, гипертрофическая обструктивная кардиомиопатия), а
также пациентам с митральным стенозом.
Нарушение функции почек
У пациентов с почечной недостаточностью (КК менее 60 мл/мин) начальная доза препарата Периндоприл должна быть подобрана в соответствии с КК (см. раздел «Способ применения и дозы») и затем — в зависимости от
терапевтического ответа. Для таких пациентов необходим регулярный контроль содержания калия и
концентрации креатинина в сыворотке крови (см. раздел «Побочное действие»).
У пациентов с симптоматической сердечной недостаточностью артериальная гипотензия, развивающаяся в начальном периоде терапии ингибиторами АПФ, может привести к ухудшению функции почек.
У таких пациентов иногда отмечались случаи развития острой почечной недостаточности, обычно обратимой.
У некоторых пациентов с двусторонним стенозом почечных артерий или стенозом почечной артерии единственной почки (особенно при наличии почечной недостаточности) на фоне терапии ингибиторами АПФ отмечалось повышение сывороточной концентрации мочевины и креатинина, обратимое после отмены терапии. У пациентов с реноваскулярной гипертензией на фоне терапии ингибиторами АПФ существует повышенный риск развития тяжелой артериальной гипотензии и почечной недостаточности. Лечение таких пациентов должно начинаться под
тщательным медицинским наблюдением, с малых доз препарата и при дальнейшем адекватном
подборе дозы. В течение первых недель терапии препаратом Периндоприл необходимо отменить диуретические средства и регулярно контролировать функцию почек. У некоторых пациентов с артериальной гипертензией, при
наличии ранее не выявленной почечной недостаточности, особенно при сопутствующей терапии
диуретиками, отмечалось незначительное и временное повышение концентрации мочевины и креатинина в сыворотке крови. В этом случае рекомендуется уменьшение дозы препарата Периндоприл и/или отмена
диуретического средства.
Гемодиализ
У пациентов, находящихся на диализе с использованием высокопроточных мембран (например, AN69H), и принимающих одновременно ингибиторы АПФ, было отмечено несколько случаев развития стойких, угрожающих жизни анафилактических реакций. При необходимости проведения гемодиализа необходимо использовать другой тип мембран. Трансплантация почки Опыт применения препарата Периндоприл у пациентов с недавно перенесенной трансплантацией почки отсутствует.
Повышенная чувствительность, ангионевротический отек При приеме ингибиторов АПФ, в том числе и периндоприла, в редких случаях может наблюдаться развитие ангионевротического отека лица, конечностей, губ, слизистых оболочек, языка, голосовых складок и/или гортани (см. раздел «Побочное действие»).
Это состояние может развиться в любой момент лечения. При развитии ангионевротического отека лечение должно немедленно быть прекращено, пациент должен находиться под медицинским наблюдением до полного
исчезновения симптомов. Если отек затрагивает только лицо и губы, то его проявления обычно проходят
самостоятельно, хотя для лечения симптомов могут применяться антигистаминные средства. Отек
языка, голосовых складок или гортани может привести к обструкции дыхательных путей.
Ангионевротический отек, сопровождающийся отеком гортани, может привести к летальному исходу.
При развитии ангионевротического отека необходимо немедленно подкожно ввести эпинефрин
(адреналин) и обеспечить проходимость дыхательных путей. Пациент должен находиться под медицинским наблюдением до полного и стойкого исчезновения симптомов.
У пациентов с отеком Квинке в анамнезе, не связанным с приемом ингибиторов АПФ, может быть
повышен риск его развития при приеме препаратов этой группы (см. раздел «Противопоказания»).
В редких случаях на фоне терапии ингибиторами АПФ развивается ангионевротический отек кишечника. При этом у пациентов отмечается боль в животе как изолированный симптом или в сочетании с тошнотой и рвотой, в некоторых случаях, без предшествующего ангионевротического отека лица и при нормальном уровне С1-эстеразы. Диагноз устанавливается с помощью компьютерной томографии брюшной области, ультразвукового исследования или в момент хирургического вмешательства. Симптомы исчезают после прекращения приема ингибиторов АПФ. Поэтому у пациентов с болью в области живота, получающих ингибиторы АПФ, при проведении дифференциальной диагностики необходимо учитывать возможность развития ангионевротического отека кишечника (см. раздел «Побочное действие»).
Совместное применение с ингибиторами mTOR (mammalian Target of Rapamycin — мишень рапамицина в клетках млекопитающих), например, темсиролимусом, сиролимусом, эверолимусом, рацекадотрилом (ингибитор энкефалиназы, применяемый для лечения острой диареи), эстрамустином.
У пациентов, одновременно получающих терапию ингибиторами mTOR, рацекадотрилом, эстрамустином, может повышаться риск развития ангионевротического отека (например, отек дыхательных путей или языка с нарушением функции дыхания или без него) (см. раздел «Взаимодействие с другими лекарственными средствами»). Анафилактоидные реакции во время проведения процедуры афереза липопротеинов низкой плотности (ЛПНП-афереза)
В редких случаях у пациентов, получающих ингибиторы АПФ, при проведении процедуры афереза ЛПНП с использованием декстран сульфата могут развиваться угрожающие жизни анафилактоидные реакции. Для предотвращения анафилактоидной реакции следует временно прекратить терапию ингибитором АПФ перед каждой процедурой афереза.
Анафилактические реакции при проведении десенсибилизации Имеются отдельные сообщения о развитии длительных, угрожающих жизни анафилактоидных реакций у пациентов, получающих ингибиторы АПФ во время десенсибилизирующей терапии, например, ядом перепончатокрылых насекомых. Ингибиторы АПФ необходимо применять с осторожностью у пациентов, предрасположенных к аллергическим реакциям, проходящих процедуры десенсибилизации. Следует избегать применения ингибиторов АПФ у пациентов, получающих иммунотерапию пчелиным ядом. Тем не менее, данной реакции можно избежать путем временной отмены ингибитора АПФ до начала процедуры десенсибилизации.
Нарушение функции печени
В редких случаях на фоне приема ингибиторов АПФ возникает холестатическая желтуха. При прогрессировании этого синдрома развивается фульминантный некроз печени, иногда с летальным исходом.
Механизм развития этого синдроманеясен.
Если во время приема ингибитора АПФ появляется желтуха или наблюдается повышение активности
«печеночных» ферментов, ингибитор АПФ следует немедленно отменить, а пациент должен находиться под
тщательным наблюдением. Также необходимо провести соответствующее обследование (см.
раздел «Побочное действие»).Нейтропения, агранулоцитоз, тромбоцитопения, анемия
У пациентов на фоне терапии ингибиторами АПФ были отмечены случаи развития нейтропении,
агранулоцитоза, тромбоцитопении и анемии. При нормальной функции почек в отсутствие других
осложнений нейтропения развивается редко. Препарат Периндоприл необходимо с очень большой осторожностью применять у пациентов с системными заболеваниями соединительной ткани (например, СКВ, склеродермия), одновременно получающих иммунодепрессивную терапию, аллопуринол или прокаинамид, а также при комбинировании всех перечисленных факторов, особенно при существующем нарушении функции почек. У таких пациентов возможно развитие тяжелых инфекций, устойчивых к интенсивной антибиотикотерапии. При проведении терапии препаратом Периндоприл у пациентов с вышеперечисленными факторами рекомендуется периодически контролировать количество лейкоцитов в крови и предупреждать пациента о необходимости информировать врача о появлении любых симптомов инфекции, например, боль в горле, лихорадка. Этнические различия Следует учитывать, что у пациентов негроидной расы риск развития ангионевротического отека более высок. Как и другие ингибиторы АПФ, Периндоприл менее эффективен в отношении снижения АД у пациентов негроидной расы. Данный эффект возможно связан с выраженным преобладанием низкоренинового статуса у пациентов негроидной расы с артериальной гипертензией.
Кашель
На фоне терапии ингибиторами АПФ может развиться сухой кашель, который прекращается после отмены препарата. Это следует учитывать при дифференциальной диагностике кашля.
Хирургическое вмешательство и общая анестезия
У пациентов, состояние которых требует обширного хирургического вмешательства или проведения общей анестезии препаратами, вызывающими артериальную гипотензию, ингибиторы АПФ, включая периндоприл, могут блокировать образование ангиотензина II при компенсаторном высвобождении ренина. За сутки до хирургического вмешательства терапию ингибиторами АПФ необходимо отменить. Если ингибитор АПФ отменить невозможно, то артериальная гипотензия, развивающаяся по описанному механизму, может быть скорректирована увеличением ОЦК. Необходимо предупредить хирурга/анестезиолога о том, что пациент принимает ингибиторы АПФ.
Гиперкалиемия
На фоне терапии ингибиторами АПФ, включая периндоприл, у некоторых пациентов может повышаться содержание калия в крови. Факторами риска гиперкалиемии являются почечная недостаточность, возраст старше 70 лет, сахарный диабет, некоторые сопутствующие состояния (дегидратация, острая сердечная недостаточность, метаболический ацидоз), одновременный прием калийсберегающих диуретиков (таких как спиронолактон и его производное эплеренон, триамтерен, амилорид), а также препаратов калия или калийсодержащих заменителей пищевой соли, а также применение других препаратов, способствующих повышению содержания калия в плазме крови (например, гепарин). Применение препаратов калия, калийсберегающих диуретиков, калийсодержащих заменителей пищевой соли может привести к значительному повышению содержания калия в крови, особенно у пациентов со сниженной функцией почек. Г иперкалиемия может привести к серьезным, иногда фатальным нарушениям сердечного ритма. Если необходим одновременный прием периндоприла и указанных выше препаратов, лечение должно проводиться с осторожностью на фоне регулярного контроля содержания калия в сыворотке крови (см. раздел «Взаимодействие с другими лекарственными средствами»). Сахарный диабет
У пациентов с сахарным диабетом, принимающих гипогликемические средства для приема внутрь или
инсулин, в течение первого месяца терапии ингибиторами АПФ необходимо регулярно
контролировать концентрацию глюкозы в крови (см. раздел «Взаимодействие с другими лекарственными средствами»).
Препараты лития Одновременное применение препарата Периндоприл и препаратов
лития не рекомендуется (см. раздел «Взаимодействие с другими лекарственными средствами»).
Калийсберегающие диуретики, препараты калия, калийсодержащие заменители пищевой соли и пищевые добавки
Не рекомендуется одновременное применение препарата Периндоприл и калийсберегаюгцих диуретиков, а
также препаратов калия и калийсодержащих заменителей пищевой соли (см. раздел «Взаимодействие с другими лекарственными средствами»). Двойная блокада РААС Есть данные, свидетельствующие о том, что совместное применение ингибиторов АПФ, АРА II или алискирена (ингибитора ренина) повышает риск развития
артериальной гипотензии, гиперкалиемии и нарушения функции почек (включая острую почечную недостаточность). Таким образом, двойная блокада РААС путем совместного применения ингибиторов АПФ, АРА II или алискирена не рекомендована (см. раздел «Взаимодействие с другими лекарственными средствами»). Если
терапия с помощью двойной блокады является абсолютно необходимой, ее следует проводить только под
строгим медицинским контролем и при регулярном контроле функции почек, содержания электролитов в
крови и АД.
Алискирен и алискиренсодержащие препараты
Противопоказано одновременное применение препарата Периндоприл у пациентов с сахарным диабетом
и/или умеренными или тяжелыми нарушениями функции почек (СКФ менее 60 мл/мин/1,73 м2 площади поверхности тела) и не рекомендуется у других пациентов: возрастает риск гиперкалиемии, ухудшения функции почек и повышения частоты сердечно- сосудистой заболеваемости и смертности.
Противопоказано применение ингибиторов АПФ с АРА II у пациентов с диабетической нефропатией и не рекомендуется у других пациентов (см. раздел «Противопоказания»). Дефицит глюкозо-6- фосфатдегидрогеназы
У пациентов с врожденным дефицитом глюкозо-6- фосфатдегидрогеназы отмечены
единичные случаи развития гемолитической анемии (см. раздел «Побочное действие»).
Влияние на способность управлять транспортными средствами, механизмами
Препарат Периндоприл следует с осторожностью применять пациентам, управляющим автотранспортом и занимающимся видами деятельности, требующими повышенной концентрации внимания
и быстрой реакции, в связи с опасностью развития артериальной гипотензии и головокружения.
