Содержание
- Структурная формула
- Русское название
- Английское название
- Латинское название вещества Калия перманганат
- Химическое название
- Брутто формула
- Фармакологическая группа вещества Калия перманганат
- Нозологическая классификация
- Код CAS
- Фармакологическое действие
- Характеристика
- Фармакология
- Применение вещества Калия перманганат
- Противопоказания
- Побочные действия вещества Калия перманганат
- Взаимодействие
- Передозировка
- Способ применения и дозы
- Торговые названия с действующим веществом Калия перманганат
Структурная формула
Русское название
Калия перманганат
Английское название
Potassium permanganate
Латинское название вещества Калия перманганат
Kalii permanganas (род. Kalii permanganatis)
Химическое название
Калий марганцевокислый
Фармакологическая группа вещества Калия перманганат
Нозологическая классификация
Список кодов МКБ-10
- L89 Декубитальная язва
- T57.1 Токсическое действие фосфора и его соединений
- T40.2 Другими опиоидами
- T50.9.0* Отравление алкалоидами
- T14.1 Открытая рана неуточненной области тела
- T65.6 Красок и красящих веществ, не классифицированных в других рубриках
- L98.4 Хроническая язва кожи, не классифицированная в других рубриках
- T30 Термические и химические ожоги неуточненной локализации
- W57 Укус или ужаливание неядовитым насекомым и другими неядовитыми членистоногими
- T65.0 Цианидов
- J39.9 Болезнь верхних дыхательных путей неуточненная
- N39.9 Расстройство мочевыделительной системы неуточненное
- T65.2 Табака и никотина
- K13.7 Другие и неуточненные поражения слизистой оболочки полости рта
Фармакологическое действие
—
антисептическое, дезодорирующее.
Характеристика
Темно- или красно-фиолетовые кристаллы или мелкий порошок с металлическим блеском. Растворим в воде в соотношении 1:18, слабые растворы имеют розовую окраску, концентрированные — темно-фиолетовую.
Фармакология
При соприкосновении с органическими веществами выделяет атомарный кислород, образует окись марганца, денатурирует белки. Эффективен при лечении ожогов и язв, поскольку обладает сильными дубящими свойствами. При попадании внутрь всасывается, оказывая гематотоксическое действие (метгемоглобинемия).
Применение вещества Калия перманганат
В качестве антисептического средства — промывание ран, смазывание язвенных и ожоговых поверхностей, полоскание рта и горла, а также спринцевание и промывание в гинекологической и урологической практике. Для промываний — желудка при отравлениях, вызванных приемом внутрь алкалоидов, морфина, никотина, синильной кислоты, хинина, фосфора; кожи — при попадании на нее анилина; глаз — при поражении их ядовитыми насекомыми.
Противопоказания
Гиперчувствительность.
Побочные действия вещества Калия перманганат
Аллергические реакции, при использовании концентрированных растворов — ожог и раздражение.
Взаимодействие
Химически несовместим с некоторыми органическими веществами (уголь, сахар, танин) и легко окисляющимися веществами — может произойти взрыв.
Передозировка
При попадании внутрь возникает резкая боль в полости рта, по ходу пищевода, в животе, рвота, диарея; слизистая оболочка полости рта и глотки — отечная, темно-коричневого, фиолетового цвета, возможен отек гортани и развитие механической асфиксии, ожогового шока, двигательного возбуждения, судорог. Часто возникает тяжелая пневмония, геморрагический колит, нефропатия, гепатопатия, явления паркинсонизма. При пониженной кислотности желудочного сока возможно развитие метгемоглобинемии с выраженным цианозом и одышкой. Смертельная доза для детей — около 3 г, для взрослых — 0,3–0,5 г/кг.
В качестве противоядия используют Метиленовый синий (50 мл 1% раствора), аскорбиновую кислоту (в/в — 30 мл 5% раствора), витамин B12 — до 1000 мкг, B6 (3 мл 5% раствора в/м).
Способ применения и дозы
Наружно (в водных растворах): для промывания ран — 0,1–0,5%, для полоскания рта и горла — 0,01–0,1%, для смазывания язвенных и ожоговых поверхностей — 2–5%, для спринцеваний и промываний — 0,02–0,1%.
Торговые названия с действующим веществом Калия перманганат
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Калия перманганат |
от 29.80 до 167.00 |
| Перманганат калия | |
 |
|
 |
|
| Общие | |
|---|---|
| Систематическое наименование | Перманганат калия |
| Химическая формула | KMnO4 |
| Отн. молек. масса | 158,03 а. е. м. |
| Молярная масса | 158,03 г/моль |
| Физические свойства | |
| Плотность вещества | 2.703 г/см³ |
| Состояние (ст. усл.) | бесцветная жикость |
| Термические свойства | |
| Температура разложения | 240 °C |
| Молярная теплоёмкость (ст. усл.) | 119,2 Дж/(моль·К) |
| Энтальпия (ст. усл.) | -813.4 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 6.38 (20 °C) г/100 мл |
| Классификация | |
| номер CAS | [7722-64-7 |
Калия перманганат (лат. Kalii permanganas) — марганцовокислый калий, калиевая соль марганцевой кислоты KMnO4.
- Распространённое название в быту — марганцовка
Содержание
- 1 Физические свойства
- 1.1 Термодинамические свойства
- 2 Химические свойства
- 3 Применение
- 3.1 Медицинское применение
- 3.1.1 Фармакологическое действие
- 3.1.2 Показания
- 3.1.3 Противопоказания
- 3.1.4 Побочные действия
- 3.1.5 Способ применения и дозы
- 3.1.6 Взаимодействие
- 3.2 Другие сферы применения
- 3.1 Медицинское применение
- 4 Получение
- 5 Литература
- 6 См. также
Физические свойства
Внешний вид: тёмно-фиолетовые кристаллы с металлическим блеском. Показатель преломления σ 1,59 (при 20°C).
Растворяется в воде (см. таблицу), жидком аммиаке, ацетоне (2:100), метаноле, пиридине.
| Температура, °C | 10 | 20 | 25 | 30 | 40 | 50 | 65 |
| Растворимость, г/100 г воды | 4,22 | 6,36 | 7,63 | 9 | 12,5 | 16,8 | 25 |
Термодинамические свойства
| Стандартная энтальпия образования ΔH | −813,4 кДж/моль (т) (при 298 К) |
| Стандартная энергия Гиббса образования G | −713,8 кДж/моль (т) (при 298 К) |
| Стандартная энтропия S | 171,71 Дж/моль·K (т) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 119,2 Дж/моль·K (т) (при 298 К) |
Химические свойства
Сильный окислитель. Стандартные окислительно-восстановительные потенциалы приведены в таблице.
| Окисленная форма | Восстановленная форма | Среда | E0, В |
|---|---|---|---|
| MnO4— | MnO42- | OH— | +0,56 |
| MnO4— | H2MnO4 | H+ | +1,22 |
| MnO4— | MnO2 | H+ | +1,69 |
| MnO4— | MnO2 | OH— | +0,60 |
| MnO4— | Mn2+ | H+ | +1,51 |
В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия:
в кислой среде: 2KMnO4 + 5K2SO3 + 3H2SO4 → 6K2SO4 + 2MnSO4 + 3H2O
в нейтральной среде: 2KMnO4 + 3K2SO3 + H2O → 3K2SO4 + 2MnO2 + 2KOH
в щелочной среде: 2KMnO4 + K2SO3 + 2KOH → K2SO4 + 2K2MnO4 + H2O, KMnO4 + K2SO3 + KOH → K2SO4 + K3MnO4 + H2O (на холоду)
Однако надо отметить, что в последняя реакция (в щелочной среде) идёт по указаной схеме только при недостатке восстановителя и высокой концентрации щёлочи, которая обеспечивает замедление гидролиза манганата калия.
При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII):
2KMnO4 + 2H2SO4 → 2KHSO4 + Mn2O7 + H2O,
при этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца MnO3HSO4. По реакции с фторидом йода(V) можно получить аналогичный оксофторид:
KMnO4 + IF5 → KF + IOF3 + MnO3F
При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением:
2KMnO4 →(t) K2MnO4 + MnO2+ O2↑
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением:
5KMnO4 →(t) K2MnO4 +K3MnO4 + 3MnO2+ 3O2↑
Реагирует с солями двухвалентного марганца, например:
2KMnO4 + 3MnSO4 + 2H2O → 5MnO2 + K2SO4 + 2H2SO4
Эта реакция коммутации в принципе обратна дисмутации (диспропорционирование) K2MnO4 на MnO2 и KMnO4.
- Водные растворы перманганата калия термодинамически нестабильны, но кинетически довольно устойчивы. Их сохранность резко повышается при хранении в темноте.
Применение
Применение этой соли чаще всего основано на высокой окисляющей способности перманганат-иона, обеспечивающей антисептическое действие.
|
Перманганат калия (Kalii permanganas) |
||
| Химическое соединение | ||
| ИЮПАК | Перманганат калия | |
| Брутто- формула |
KMnO4 | |
| CAS | 7722-64-7 | |
| Классификация | ||
| Фарм. группа |
Антисептики и дезинфицирующие средства; Гомеопатические средства | |
| АТХ | D08AX06 | |
| МКБ-10 | AB.C | |
| Лекарственные формы | ||
| порошок для приготовления раствора | ||
Медицинское применение
Разбавленные растворы (около 0,1%) перманганата калия нашли широчайшее применение в медицине как антисептическое средство, для полоскания горла, промывания ран, обработки ожогов. В качестве рвотного средства для приёма внутрь при некоторых отравлениях используют разбавленный раствор.
Фармакологическое действие
Антисептическое средство. При соприкосновении с органическими веществами выделяет атомарный кислород. Образующийся при восстановлении препарата оксид образует с белками комплексные соединения — альбуминаты (за счет этого калия перманганат в малых концентрациях оказывает вяжущее, а в концентрированных растворах — раздражающее, прижигающее и дубящее действие). Обладает также дезодорирующим эффектом. Эффективен при лечении ожогов и язв. Способность калия перманганата обезвреживать некоторые яды лежит в основе использования его растворов для промывания желудка при отравлениях неизвестным ядом и пищевых токсикоинфекциях. При попадании внутрь всасывается, оказывая гематотоксическое действие (приводит к развитию метгемоглобинемии). Используется так же в гомеопатии.
Показания
Смазывание язвенных и ожоговых поверхностей — инфицированные раны, язвы и ожоги кожи. Полоскание полости рта и ротоглотки — при инфекционно-воспалительных заболеваниях слизистой оболочки полости рта и ротоглотки (в т.ч. при ангинах). Для промывания и спринцеваний при гинекологических и урологических заболеваниях — кольпиты и уретриты. Для промываний — желудка при отравлениях, вызванных приемом внутрь алкалоидов (морфин, аконитин, никотин), синильной кислотой, фосфором, хинином; кожи — при попадании на нее анилина; глаз — при поражении их ядовитыми насекомыми.
Противопоказания
Гиперчувствительность.
Побочные действия
Аллергические реакции, при использовании концентрированных растворов — ожоги и раздражение. Передозировка. Симптомы: резкая боль в полости рта, по ходу пищевода, в животе, рвота, диарея; слизистая оболочка полости рта и глотки — отечная, темно-коричневого, фиолетового цвета, возможен отек гортани, развитие механической асфиксии, ожогового шока, двигательного возбуждения, судорог, явлений паркинсонизма, геморрагического колита, нефропатии, гепатопатии. При пониженной кислотности желудочного сока возможно развитие метгемоглобинемии с выраженным цианозом и одышкой. Смертельная доза для детей — около 3 г, для взрослых — 0.3-0.5 г/кг. Лечение: метиленовый синий (50 мл 1% раствора), аскорбиновая кислота (в/в — 30 мл 5% раствора), цианокобаламин — до 1 мг, пиридоксин (в/м — 3 мл 5% раствора).
Способ применения и дозы
Наружно, в водных растворах для промывания ран (0.1-0.5%), для полоскания рта и горла (0.01-0.1%), для смазывания язвенных и ожоговых поверхностей (2-5%), для спринцевания (0.02-0.1%) в гинекологической и урологической практике, а также промывания желудка при отравлениях.
Взаимодействие
Химически несовместим с некоторыми органическими веществами (уголь, сахар, танин) и легкоокисляющимися веществами может произойти взрыв.
Другие сферы применения
- Щелочной раствор перманганата калия хорошо отмывает лабораторную посуду от жиров и других органических веществ.
- Растворы (концентрации примерно 3 г/л) широко применяются при тонировании фотографий.
- В пиротехнике применяют в качестве сильного окислителя.
Получение
Химическое или электрохимическое окисление соединений марганца, диспропорционирование манганата калия. Например:
2MnO2 +3 Cl2 + 8KOH → 2KMnO4 + 6KCl + 4H2O
2K2MnO4 + Cl2 → 2KMnO4 + 2KCl
3K2MnO4+2H2O → 2KMnO4+ MnO2 + 4KOH
2K2MnO4 + 2H2O → 2KMnO4 +H2↑ + 2KOH
Последняя реакция происходит при электролизе концентрированного раствора манганата калия и эндотермична, она является основным промышленным способом получения перманганата калия.
Литература
- Вульфсон Н.С. — Препаративная органическая химия с.656,657
- Казанский Б.А. (ред.) — Синтезы органических препаратов (Сборник 3) с.145
- Реми Г. — Курс неорганической химии (Том 1) с.817
См. также
- Марганец;
- Марганцевая кислота;
- Перманганаты.
Wikimedia Foundation.
2010.
From Wikipedia, the free encyclopedia
|
|

|
|

|
|
| Names | |
|---|---|
| IUPAC name
Potassium manganate(VII) |
|
| Other names
Potassium permanganate |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChEMBL |
|
| ChemSpider |
|
| DrugBank |
|
| ECHA InfoCard | 100.028.874 |
| EC Number |
|
| KEGG |
|
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
| UN number | 1490 |
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
KMnO4 |
| Molar mass | 158.034 g/mol |
| Appearance | Purplish-bronze-gray needles purple in solution[1] |
| Odor | odorless |
| Density | 2.7 g/cm3[2]: 4.83 |
| Melting point | 240 °C (464 °F; 513 K) (decomposes) |
|
Solubility in water |
76 g/L (25 °C)[2] 250 g/L (65 °C) |
| Solubility | decomposes in alcohol and organic solvents |
|
Magnetic susceptibility (χ) |
+20.0·10−6 cm3/mol[2]: 4.134 |
|
Refractive index (nD) |
1.59 |
| Structure[3] | |
|
Crystal structure |
Orthorhombic, oP24 |
|
Space group |
Pnma, No. 62 |
|
Lattice constant |
a = 0.909 nm, b = 0.572 nm, c = 0.741 nm |
|
Formula units (Z) |
4 |
| Thermochemistry | |
|
Heat capacity (C) |
119.2 J/mol K |
|
Std molar |
171.7 J K−1 mol−1 |
|
Std enthalpy of |
−813.4 kJ/mol |
|
Gibbs free energy (ΔfG⦵) |
-713.8 kJ/mol |
| Pharmacology | |
|
ATC code |
D08AX06 (WHO) V03AB18 (WHO) |
| Hazards | |
| GHS labelling: | |
|
Pictograms |
  
|
| NFPA 704 (fire diamond) |
2 0 1 OX |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
1090 mg/kg (oral, rat)[4] |
| Related compounds | |
|
Other anions |
Potassium pertechnetate Potassium perrhenate |
|
Other cations |
Sodium permanganate Ammonium permanganate Calcium permanganate Silver permanganate |
|
Related manganates |
Potassium hypomanganate Potassium manganate |
|
Related compounds |
Manganese heptoxide |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
| Clinical data | |
|---|---|
| License data |
|
| Identifiers | |
| CompTox Dashboard (EPA) |
|
| ECHA InfoCard | 100.028.874 |
Potassium permanganate in a vial
Potassium permanganate is an inorganic compound with the chemical formula KMnO4. It is a purplish-black crystalline salt, that dissolves in water as K+ and MnO−
4, an intensely pink to purple solution.
Potassium permanganate is widely used in the chemical industry and laboratories as a strong oxidizing agent, and also as a medication for dermatitis, for cleaning wounds, and general disinfection. It is on the World Health Organization’s List of Essential Medicines.[5] In 2000, worldwide production was estimated at 30,000 tons.[5]
Properties[edit]
Potassium permanganate is the potassium salt of the tetrahedral transition metal oxo complex permanganate, in which four O2− ligands are bound to a manganese(VII) center.
Structure[edit]
KMnO4 forms orthorhombic crystals with constants: a = 910.5 pm, b = 572.0 pm, c = 742.5 pm. The overall motif is similar to that for barium sulfate, with which it forms solid solutions.[6] In the solid (as in solution), each MnO−4 centre is tetrahedral. The Mn–O distances are 1.62 Å.[7]
Color[edit]
The purplish-black color of solid potassium permanganate, and the intensely pink to purple color of its solutions, is caused by its permanganate anion, which gets its color from a strong charge-transfer absorption band caused by excitation of electrons from oxo ligand orbitals to empty orbitals of the manganese(VII) center.[8]
Uses[edit]
Almost all applications of potassium permanganate exploit its oxidizing properties.[9] As a strong oxidant that does not generate toxic byproducts, KMnO4 has many niche uses.
Medical uses[edit]
Potassium permanganate is used for a number of skin conditions.[10] This includes fungal infections of the foot, impetigo, pemphigus, superficial wounds, dermatitis, and tropical ulcers.[11][10] It is on the World Health Organization’s List of Essential Medicines.[5]
Water treatment[edit]
Potassium permanganate is used extensively in the water treatment industry. It is used as a regeneration chemical to remove iron and hydrogen sulfide (rotten egg smell) from well water via a «manganese greensand» filter. «Pot-Perm» is also obtainable at pool supply stores and is used additionally to treat wastewater. Historically it was used to disinfect drinking water[12][13] and can turn the water pink.[14] It currently finds application in the control of nuisance organisms such as zebra mussels in fresh water collection and treatment systems.[15]
Synthesis of organic compounds[edit]
A major application of KMnO4 is as a reagent for the synthesis of organic compounds.[16] Significant amounts are required for the synthesis of ascorbic acid, chloramphenicol, saccharin, isonicotinic acid, and pyrazinoic acid.[9]
KMnO4 is used in qualitative organic analysis to test for the presence of unsaturation. It is sometimes referred to as Baeyer’s reagent after the German organic chemist Adolf von Baeyer . The reagent is an alkaline solution of potassium permanganate. Reaction with double or triple bonds (-C=C- or -C≡C-) causes the color to fade from purplish-pink to brown. Aldehydes and formic acid (and formates) also give a positive test.[17] The test is antiquated.
KMnO4 solution is a common thin layer chromatography stain for the detection of oxidizable functional groups, such as alcohols, aldehydes, alkenes, and ketones. Such compounds result in a white to orange spot on TLC plates.[18][19][20]
Analytical use[edit]
Potassium permanganate can be used to quantitatively determine the total oxidizable organic material in an aqueous sample. The value determined is known as the permanganate value. In analytical chemistry, a standardized aqueous solution of KMnO4 is sometimes used as an oxidizing titrant for redox titrations (permanganometry). As potassium permanganate is titrated, the solution becomes a light shade of purple, which darkens as excess of the titrant is added to the solution. In a related way, it is used as a reagent to determine the Kappa number of wood pulp. For the standardization of KMnO4 solutions, reduction by oxalic acid is often used.[21] In agricultural chemistry, it is used for estimation of active carbon in soil.[22]
Aqueous, acidic solutions of KMnO4 are used to collect gaseous mercury in flue gas during stationary source emissions testing.[23]
In histology, potassium permanganate was used as a bleaching agent.[24][25]
Fruit preservation[edit]
Ethylene absorbents extend storage time of bananas even at high temperatures. This effect can be exploited by packing bananas in polyethylene together with potassium permanganate. By removing ethylene by oxidation, the permanganate delays the ripening, increasing the fruit’s shelf life up to 4 weeks without the need for refrigeration.[26][27][28]
Survival kits[edit]
Potassium permanganate is sometimes included in survival kits: as a hypergolic fire starter (when mixed with glycerol antifreeze from a car radiator;[29][30][31] as a water sterilizer; and for creating distress signals on snow).[32]
Fire service[edit]
Potassium permanganate is added to «plastic sphere dispensers» to create backfires, burnouts, and controlled burns. Polymer spheres resembling ping-pong balls containing small amounts of permanganate are injected with ethylene glycol and projected towards the area where ignition is desired, where they spontaneously ignite seconds later.[33][34] Both handheld[34] and helicopter-[33] or boat-mounted[34] plastic sphere dispensers are used.
Other uses[edit]
Potassium permanganate is one of the principal chemicals used in the film and television industries to «age» props and set dressings. Its ready conversion to brown MnO2 creates «hundred-year-old» or «ancient» looks on hessian cloth (burlap), ropes, timber, and glass.[35]
Potassium permanganate can be used to oxidize cocaine paste to purify it and increase its stability. This led to the Drug Enforcement Administration launching Operation Purple in 2000, with the goal of monitoring the world supply of potassium permanganate; however, potassium permanganate derivatives and substitutes were soon used thereafter to avoid the operation.[36]
Potassium permangate used as an oxidizing agent in the synthesis of cocaine and methcathinone.[37]
History[edit]
In 1659, Johann Rudolf Glauber fused a mixture of the mineral pyrolusite (manganese dioxide, MnO2) and potassium carbonate to obtain a material that, when dissolved in water, gave a green solution (potassium manganate) which slowly shifted to violet and then finally red.[38] The reaction that produced the color changes that Glauber observed in his solution of potassium permanganate and potassium manganate (K2MnO4) is now known as the «chemical chameleon». This report represents the first description of the production of potassium permanganate.[39] Just under 200 years later, London chemist Henry Bollmann Condy had an interest in disinfectants; he found that fusing pyrolusite with sodium hydroxide (NaOH) and dissolving it in water produced a solution with disinfectant properties. He patented this solution, and marketed it as ‘Condy’s Fluid’. Although effective, the solution was not very stable. This was overcome by using potassium hydroxide (KOH) rather than NaOH. This was more stable, and had the advantage of easy conversion to the equally effective potassium permanganate crystals. This crystalline material was known as ‘Condy’s crystals’ or ‘Condy’s powder’. Potassium permanganate was comparatively easy to manufacture, so Condy was subsequently forced to spend considerable time in litigation to stop competitors from marketing similar products.[40]
Early photographers used it as a component of flash powder. It is now replaced with other oxidizers, due to the instability of permanganate mixtures.
Preparation[edit]
Potassium permanganate is produced industrially from manganese dioxide, which also occurs as the mineral pyrolusite. In 2000, worldwide production was estimated at 30,000 tonnes.[9] The MnO2 is fused with potassium hydroxide and heated in air or with another source of oxygen, like potassium nitrate or potassium chlorate.[9] This process gives potassium manganate:
- 2 MnO2 + 4 KOH + O2 → 2 K2MnO4 + 2 H2O
(With sodium hydroxide, the end product is not sodium manganate but an Mn(V) compound, which is one reason why the potassium permanganate is more commonly used than sodium permanganate. Furthermore, the potassium salt crystallizes better.[9])
The potassium manganate is then converted into permanganate by electrolytic oxidation in alkaline media:
- 2 K2MnO4 + 2 H2O → 2 KMnO4 + 2 KOH + H2
Other methods[edit]
Although of no commercial importance, potassium manganate can be oxidized by chlorine or by disproportionation under acidic conditions.[41] The chlorine oxidation reaction is
- 2 K2MnO4 + Cl2 → 2 KMnO4 + 2 KCl
and the acid-induced disproportionation reaction may be written as
- 3 K2MnO4 + 4 HCl → 2 KMnO4 + MnO2 + 2 H2O + 4 KCl
A weak acid such as carbonic acid is sufficient for this reaction:
- 3 K2MnO4 + 2 CO2 → 2 KMnO4 + 2 K2CO3 + MnO2
Permanganate salts may also be generated by treating a solution of Mn2+ ions with strong oxidants such as lead dioxide (PbO2), sodium bismuthate (NaBiO3), or peroxydisulfate. Tests for the presence of manganese exploit the vivid violet color of permanganate produced by these reagents.
Reactions[edit]
Organic chemistry[edit]
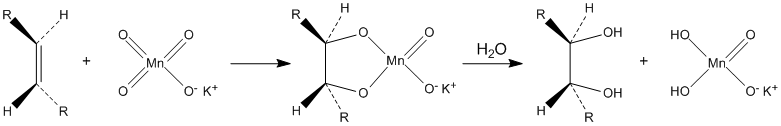
Dilute solutions of KMnO4 convert alkenes into diols. This behaviour is also used as a qualitative test for the presence of double or triple bonds in a molecule, since the reaction decolorizes the initially purple permanganate solution and generates a brown precipitate (MnO2). In this context, it is sometimes called Baeyer’s reagent. However, bromine serves better in measuring unsaturation (double or triple bonds) quantitatively, since KMnO4, being a very strong oxidizing agent, can react with a variety of groups.
Under acidic conditions, the alkene double bond is cleaved to give the appropriate carboxylic acid:[42]
- CH3(CH2)17CH=CH2 + 2 KMnO4 + 3 H2SO4 → CH3(CH2)17COOH + CO2 + 4 H2O + K2SO4 + 2 MnSO4
Potassium permanganate oxidizes aldehydes to carboxylic acids, illustrated by the conversion of n-heptanal to heptanoic acid:[43]
- 5 C6H13CHO + 2 KMnO4 + 3 H2SO4 → 5 C6H13COOH + 3 H2O + K2SO4 + 2 MnSO4
Even an alkyl group (with a benzylic hydrogen) on an aromatic ring is oxidized, e.g. toluene to benzoic acid.[44]
- 5 C6H5CH3 + 6 KMnO4 + 9 H2SO4 → 5 C6H5COOH + 14 H2O + 3 K2SO4 + 6 MnSO4
Glycols and polyols are highly reactive toward KMnO4. For example, addition of potassium permanganate to an aqueous solution of sugar and sodium hydroxide produces the chemical chameleon reaction, which involves dramatic color changes associated with the various oxidation states of manganese. A related vigorous reaction is exploited as a fire starter in survival kits. For example, a mixture of potassium permanganate and glycerol or pulverized glucose ignites readily.[29] Its sterilizing properties are another reason for inclusion of KMnO4 in a survival kit.
Ion exchange[edit]
Treating a mixture of aqueous potassium permanganate with a quaternary ammonium salt results in ion exchange, precipitating the quat salt of permanganate. Solutions of these salts are sometimes soluble in organic solvents:[45]
- KMnO4 + R4NCl → R4NMnO4 + KCl
Similarly, addition of a crown ether also gives a lipophilic salt.[46]
Reaction with acids and bases[edit]
Permanganate reacts with concentrated hydrochloric acid to give chlorine and manganese(II):
- 2 KMnO4 + 16 HCl → 2 Mn2+ + 5 Cl2 + 8 H2O
In neutral solution, permanganate slowly reduces to manganese dioxide (MnO2). This is the material that stains one’s skin when handling KMnO4.
KMnO4 reduces in alkaline solution to give green K2MnO4:[47]
- 4 KMnO4 + 4 KOH → 4 K2MnO4 + O2 + 2 H2O
This reaction illustrates the relatively rare role of hydroxide as a reducing agent.
Addition of concentrated sulfuric acid to potassium permanganate gives Mn2O7.[48] Although no reaction may be apparent, the vapor over the mixture will ignite paper impregnated with alcohol. Potassium permanganate and sulfuric acid react to produce some ozone, which has a high oxidizing power and rapidly oxidizes the alcohol, causing it to combust. As the reaction also produces explosive Mn2O7, this should only be attempted with great caution.[49][50]
Thermal decomposition[edit]
Solid potassium permanganate decomposes when heated:
- 2 KMnO4 → K2MnO4 + MnO2(s) + O2
Safety and handling[edit]
Potassium permanganate poses risks as an oxidizer.[51] Contact with skin will result in a long lasting brown stain.[52]
References[edit]
- ^ Burriel F, Lucena F, Arribas S, Hernández J (1985). Química Analítica Cualitativa [Qualitative Analytical Chemistry] (in Spanish). p. 688. ISBN 84-9732-140-5.
- ^ a b c Haynes WM, ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). CRC Press. ISBN 978-1439855119.
- ^ Hocart R, Mathieu-Sicaud A (1945). «A stabilization factor in the polymorphism of ammonium nitrate». Comptes Rendus Hebdomadaires des Séances de l’Académie des Sciences [Weekly Reports of the Sessions of the Academy of Sciences] (in French). 221: 261–263.
- ^ Chambers M. «Potassium permanganate [USP:JAN] – Similar structures search, synonyms, formulas, resource links, and other chemical information». ChemIDplus: A Toxnet database. U.S. National Library of Medicine. ChemIDplus – CAS: 7722-64-7 InChi: VZJVWSHVAAUDKD-UHFFFAOYSA-N. Archived from the original on 13 August 2014. Retrieved 9 May 2018.
- ^ a b c World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ Brauer E, ed. (1963). Handbook of Preparative Inorganic Chemistry. New York: Academic Press.
- ^ Palenik GJ (1967). «Crystal structure of potassium permanganate». Inorg. Chem. 6 (3): 503–507. doi:10.1021/ic50049a015.
- ^ Miessler GL, Fischer PJ, Tarr DA (2014). Inorganic Chemistry (5th ed.). Pearson. p. 430. ISBN 978-0321811059.
- ^ a b c d e Reidies AH (2002). «Manganese Compounds». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a16_123.
- ^ a b World Health Organization (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). WHO Model Formulary 2008. World Health Organization. pp. 295, 300. hdl:10665/44053. ISBN 9789241547659.
- ^ British Medical Association; Royal Pharmaceutical Society (2015). British national formulary (69 ed.). p. 840. ISBN 9780857111562.
- ^ Assembly of Life Sciences (U.S.). Safe Drinking Water Committee (1977). Drinking water and health, Volume 2. National Academies Press. p. 98. ISBN 978-0-309-02931-5. Retrieved 2016-09-13.
- ^ Downey R, Barrington M (28 February 2005). «Red faces over pink water». The Northern Advocate. Archived from the original on 2011-07-19.
- ^ «Onoway apologizes for ‘alarming’ pink tap water». CBC News. 7 March 2017. Archived from the original on 7 March 2017. Retrieved 8 March 2017.
- ^ «EPA Guidance Manual Alternative Disinfectants and Oxidants». U.S. Environmental Protection Agency. 13 October 2015. Archived from the original on 2016-10-01.
- ^ Fatiadi A (1987). «The Classical Permanganate Ion: Still a Novel Oxidant in Organic Chemistry». Synthesis. 1987 (2): 85–127. doi:10.1055/s-1987-27859.
- ^ Glagovich N (2013). «Baeyer Test». Department of Chemistry and Biochemistry. Central Connecticut State University. Archived from the original on 24 January 2013. Retrieved 9 May 2018.
- ^ Thin Layer Chromatography stains http://www.reachdevices.com/TLC_stains.html
- ^ Jork, H., Funk, W., Fischer, W., Wimmer, H. (1990): Thin-Layer Chromatography: Reagents and Detection Methods, Volume 1a, VCH, Weinheim, ISBN 3-527-278834
- ^ Jork, H., Funk, W., Fischer, W., Wimmer, H. (1994): Thin-Layer Chromatography: Reagents and Detection Methods, Volume 1b, VCH, Weinheim
- ^ Kovacs KA, Grof P, Burai L, Riedel M (2004). «Revising the Mechanism of the Permanganate/Oxalate Reaction». J. Phys. Chem. A. 108 (50): 11026. Bibcode:2004JPCA..10811026K. doi:10.1021/jp047061u.
- ^ «Quick Reference Guide: Potassium Permanganate Test for Active Carbon». Agriculture Victoria—Victorian Resources Online. Victoria, Australia.
- ^ Code of Federal Regulations(7-1-07) Edition, Title 40, Part 60, Appendix A-8, Method 29, Section 7.3.1
- ^ Picken MM (April 2010). «Amyloidosis-where are we now and where are we heading?». Archives of Pathology & Laboratory Medicine. 134 (4): 545–551. doi:10.5858/134.4.545. PMID 20367306.
- ^ Murphy CL, Eulitz M, Hrncic R, Sletten K, Westermark P, Williams T, Macy SD, Wooliver C, Wall J, Weiss DT, Solomon A (July 2001). «Chemical typing of amyloid protein contained in formalin-fixed paraffin-embedded biopsy specimens». American Journal of Clinical Pathology. 116 (1): 135–142. doi:10.1309/TWBM-8L4E-VK22-FRH5. PMID 11447744.
- ^ Scott KJ, McGlasson WB, Roberts EA (1970). «Potassium Permanganate as an Ethylene Absorbent in Polyethylene Bags to Delay the Ripening of Bananas During Storage». Australian Journal of Experimental Agriculture and Animal Husbandry. 10 (43): 237. doi:10.1071/EA9700237.
- ^ Scott KJ, Blake, JR, Stracha, G, Tugwell, BL and McGlasson WB (1971). «Transport of Bananas at Ambient Temperatures using Polyethylene Bags». Tropical Agriculture (Trinidad). 48: 163–165.
- ^ Scott KJ, Gandanegara S (1974). «Effect of Temperature on the Storage Life of bananas Held in Polyethylene Bags with an Ethylene Absorbent». Tropical Agriculture (Trinidad). 51: 23–26.
- ^ a b Gillis B, Labiste D. «Fire by Chemical Reaction». PrimitiveWays. Archived from the original on 2015-09-24.
- ^ «Potassium Permanganate» (PDF). Pole Shift Survival Information. Archived from the original (PDF) on 4 August 2016. Retrieved 9 May 2018.
- ^ «Making Fire with Potassium Permanganate and Glycerin». thesurvivalcache. 3 November 2012. Archived from the original on 13 May 2016. Retrieved 13 September 2016.
- ^ «Distress Signals». Evening Post. CXXI (107): 5. 7 May 1936. Archived from the original on 5 November 2011.
- ^ a b «Aerial Ignition, Plastic Sphere Dispenser Description». Missoula Technology and Development Center. USDA Forest Service. Archived from the original on 26 April 2016. Retrieved 9 May 2018.
- ^ a b c «Wetland Warrior». Dirty Jobs. Season 6. Episode 2.
- ^ Brody E (February 2000). «Victor DeLor contractor profile». PaintPRO. 2 (1). Archived from the original on 2008-07-23. Retrieved 2009-11-12.
One of the techniques DeLor is known for among designers and clients is the special effects he creates with various chemical solutions. When applied to wood surfaces, these chemicals give a weathered appearance to new wood. … To achieve the aesthetic on interior surfaces, DeLor often uses a mixture of water and potassium permanganate, a dry powder chemical.
- ^ Gosmer K, Vammen M (March 10, 2014). «The Terrifying Substances People Put in Cocaine». Vice Media.
- ^ Binder R, Machata G, Stead H (May 2003). «[Analysis of potassium permanganate as addictive drug «precursor»]». Archiv Fur Kriminologie. 211 (5–6): 160–165. PMID 12872685.
- ^ Glauber, Johann Rudolph, Prosperitas Germaniae (The prosperity of Germany), part 3 (Amsterdam, (Netherlands): Johann Jansson, 1659), pp. 93–94. From pp. 93–94: » … donec tandem Magnesiam istam nitro fixo permixtam, in crucibulo forti coctione a nitro reseratam vidi, unde elegans color purpureus provenit, massam hanc effusam in pulvere redegi, aqua calida extraxi, per filtrum liquorem transmisi. Tandem vero elegantissimum purpureum, igneumque liquorem accepi, qui fere singulis horis in frigore tantummodo consistens colorem permutavit, sic ut jam viridis, jam caerulei, jam sanguinei coloris sponte sua factus sit, mox iterum alios elegantissimos colores receperit.» ( … until finally I saw [that] by mixing that magnesia [i.e., magnesia nigra, pyrolusite, the ore containing manganese dioxide ] with fixed niter [i.e., inert niter, potassium carbonate], by cooking [it] in a strong crucible, [the colored compound was] released by the niter, whence a fine purple color arises; this mass [was] poured out, reduced to powder, extracted with hot water, [and] the solution passed through a filter. Then I got a truly most elegant, purple, and fiery solution, which nearly every hour ([while] standing just in the cold) changed color, so that it was spontaneously made now green, now blue, now red in color; soon again it received other most elegant colors.) Glauber JR. «Prosperitatis Germaniae pars …. 3: In qua Salpetrae ex variis ubiq, obviis subiectis facillime atque copiose extrahendi modus traditur. Eiusve utilitates summae declarantur» [Part of the Prosperity of Germany …. 3: In which the method of extracting saltpeter from various everywhere, in the most convenient and abundant manner, is given. His interests are clearly stated] (in Latin). Archived from the original on 2016-12-20 – via Bavarian State Library. Translated in: Glauber JR (1689). The Works of the Highly Experienced and Famous Chymist, John Rudolph Glauber. Translated by Packe C. London, England: Thomas Millbourn. p. 353. Archived from the original on 2012-01-07.
- ^ Weeks ME (1956). Leicester HM (ed.). Discovery of the Elements (6th ed.). Easton, Pennsylvania: Journal of Chemical Education. pp. 172–173.
- ^ «Important Trade Mark Case». Otago Witness. 2 (2420): 53. 2 August 1900. Archived from the original on 4 March 2016.
- ^ Walton HF (1948). Inorganic Preparations. New York: Prentice-Hall. pp. 150–151.
- ^ Lee DG, Lamb SE, Chang VS (1990). «Carboxylic Acids from the Oxidation of Terminal Alkenes by Permanganate: Nonadecanoic Acid». Organic Syntheses.; Collective Volume, vol. 7, p. 397
- ^ Ruhoff JR. «n-Heptanoic acid». Organic Syntheses.; Collective Volume, vol. 2, p. 315
- ^ Gardner KA, Mayer JM (September 1995). «Understanding C-H bond oxidations: H. and H- transfer in the oxidation of toluene by permanganate». Science. 269 (5232): 1849–1851. Bibcode:1995Sci…269.1849G. doi:10.1126/science.7569922. PMID 7569922.
- ^ Herriott AW (1977). «Purple benzene: Solubilization of anions in organic solvents». J. Chem. Educ. 54 (4): 229. Bibcode:1977JChEd..54Q.229H. doi:10.1021/ed054p229.1.
- ^ Doheny Jr AJ, Ganem B (1980). «Purple benzene revisited». J. Chem. Educ. 57 (4): 308. Bibcode:1980JChEd..57..308D. doi:10.1021/ed057p308.1.
- ^ Nyholm RS, Woolliams PR (1968). «Manganates(VI)». Inorganic Syntheses. Inorg. Synth. Inorganic Syntheses. Vol. 11. pp. 56–61. doi:10.1002/9780470132425.ch11. ISBN 978-0-470-13242-5.
- ^ Cotton FA, Wilkinson G, Murillo CA, Bochmann M (1999). Advanced Inorganic Chemistry (6th ed.). Wiley-VCH. ISBN 0-471-19957-5.
- ^ Barthel H, Duvinage B (2000). «Clemens Winkler. His Experiments with Ozone in 1892». Praxis der Naturwissenschaften, Chemie. 49: 18ff.
- ^ Dzhabiev TS, Denisov NN, Moiseev DN, Shilov AE (2005). «Formation of Ozone During the Reduction of Potassium Permanganate in Sulfuric Acid Solutions». Russian Journal of Physical Chemistry. 79: 1755–1760.
- ^ Bretherick L, Urben PG, Pitt MJ (2007). Bretherick’s Handbook of Reactive Chemical Hazards. Vol. 1 (7th ed.). Elsevier Academic Press. pp. 1811–7. ISBN 978-0-12-373945-2.
- ^ Griffin S. «How to Remove Potassium Permanganate». livestrong.com. Archived from the original on 13 April 2018. Retrieved 9 May 2018.
Further reading[edit]
- «Potassium permanganate». Drug Information Portal. U.S. National Library of Medicine.
- «Manganese and compounds Fact Sheet». National Pollutant Inventory. Australia: Department of Climate Change, Energy, the Environment and Water.
- Lazur AM (2009). «The use of potassium permanganate in fish ponds». IFAS Extention. Gainesville, FL: University of Florida. Archived from the original on 2011-06-06.
External links[edit]
- International Chemical Safety Card 0672
From Wikipedia, the free encyclopedia

|
|

|
|

|
|
| Names | |
|---|---|
| IUPAC name
Potassium manganate(VII) |
|
| Other names
Potassium permanganate |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChEMBL |
|
| ChemSpider |
|
| DrugBank |
|
| ECHA InfoCard | 100.028.874 |
| EC Number |
|
| KEGG |
|
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
| UN number | 1490 |
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
KMnO4 |
| Molar mass | 158.034 g/mol |
| Appearance | Purplish-bronze-gray needles purple in solution[1] |
| Odor | odorless |
| Density | 2.7 g/cm3[2]: 4.83 |
| Melting point | 240 °C (464 °F; 513 K) (decomposes) |
|
Solubility in water |
76 g/L (25 °C)[2] 250 g/L (65 °C) |
| Solubility | decomposes in alcohol and organic solvents |
|
Magnetic susceptibility (χ) |
+20.0·10−6 cm3/mol[2]: 4.134 |
|
Refractive index (nD) |
1.59 |
| Structure[3] | |
|
Crystal structure |
Orthorhombic, oP24 |
|
Space group |
Pnma, No. 62 |
|
Lattice constant |
a = 0.909 nm, b = 0.572 nm, c = 0.741 nm |
|
Formula units (Z) |
4 |
| Thermochemistry | |
|
Heat capacity (C) |
119.2 J/mol K |
|
Std molar |
171.7 J K−1 mol−1 |
|
Std enthalpy of |
−813.4 kJ/mol |
|
Gibbs free energy (ΔfG⦵) |
-713.8 kJ/mol |
| Pharmacology | |
|
ATC code |
D08AX06 (WHO) V03AB18 (WHO) |
| Hazards | |
| GHS labelling: | |
|
Pictograms |
  
|
| NFPA 704 (fire diamond) |
2 0 1 OX |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
1090 mg/kg (oral, rat)[4] |
| Related compounds | |
|
Other anions |
Potassium pertechnetate Potassium perrhenate |
|
Other cations |
Sodium permanganate Ammonium permanganate Calcium permanganate Silver permanganate |
|
Related manganates |
Potassium hypomanganate Potassium manganate |
|
Related compounds |
Manganese heptoxide |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
| Clinical data | |
|---|---|
| License data |
|
| Identifiers | |
| CompTox Dashboard (EPA) |
|
| ECHA InfoCard | 100.028.874 |
Potassium permanganate in a vial
Potassium permanganate is an inorganic compound with the chemical formula KMnO4. It is a purplish-black crystalline salt, that dissolves in water as K+ and MnO−
4, an intensely pink to purple solution.
Potassium permanganate is widely used in the chemical industry and laboratories as a strong oxidizing agent, and also as a medication for dermatitis, for cleaning wounds, and general disinfection. It is on the World Health Organization’s List of Essential Medicines.[5] In 2000, worldwide production was estimated at 30,000 tons.[5]
Properties[edit]
Potassium permanganate is the potassium salt of the tetrahedral transition metal oxo complex permanganate, in which four O2− ligands are bound to a manganese(VII) center.
Structure[edit]
KMnO4 forms orthorhombic crystals with constants: a = 910.5 pm, b = 572.0 pm, c = 742.5 pm. The overall motif is similar to that for barium sulfate, with which it forms solid solutions.[6] In the solid (as in solution), each MnO−4 centre is tetrahedral. The Mn–O distances are 1.62 Å.[7]
Color[edit]
The purplish-black color of solid potassium permanganate, and the intensely pink to purple color of its solutions, is caused by its permanganate anion, which gets its color from a strong charge-transfer absorption band caused by excitation of electrons from oxo ligand orbitals to empty orbitals of the manganese(VII) center.[8]
Uses[edit]
Almost all applications of potassium permanganate exploit its oxidizing properties.[9] As a strong oxidant that does not generate toxic byproducts, KMnO4 has many niche uses.
Medical uses[edit]
Potassium permanganate is used for a number of skin conditions.[10] This includes fungal infections of the foot, impetigo, pemphigus, superficial wounds, dermatitis, and tropical ulcers.[11][10] It is on the World Health Organization’s List of Essential Medicines.[5]
Water treatment[edit]
Potassium permanganate is used extensively in the water treatment industry. It is used as a regeneration chemical to remove iron and hydrogen sulfide (rotten egg smell) from well water via a «manganese greensand» filter. «Pot-Perm» is also obtainable at pool supply stores and is used additionally to treat wastewater. Historically it was used to disinfect drinking water[12][13] and can turn the water pink.[14] It currently finds application in the control of nuisance organisms such as zebra mussels in fresh water collection and treatment systems.[15]
Synthesis of organic compounds[edit]
A major application of KMnO4 is as a reagent for the synthesis of organic compounds.[16] Significant amounts are required for the synthesis of ascorbic acid, chloramphenicol, saccharin, isonicotinic acid, and pyrazinoic acid.[9]
KMnO4 is used in qualitative organic analysis to test for the presence of unsaturation. It is sometimes referred to as Baeyer’s reagent after the German organic chemist Adolf von Baeyer . The reagent is an alkaline solution of potassium permanganate. Reaction with double or triple bonds (-C=C- or -C≡C-) causes the color to fade from purplish-pink to brown. Aldehydes and formic acid (and formates) also give a positive test.[17] The test is antiquated.
KMnO4 solution is a common thin layer chromatography stain for the detection of oxidizable functional groups, such as alcohols, aldehydes, alkenes, and ketones. Such compounds result in a white to orange spot on TLC plates.[18][19][20]
Analytical use[edit]
Potassium permanganate can be used to quantitatively determine the total oxidizable organic material in an aqueous sample. The value determined is known as the permanganate value. In analytical chemistry, a standardized aqueous solution of KMnO4 is sometimes used as an oxidizing titrant for redox titrations (permanganometry). As potassium permanganate is titrated, the solution becomes a light shade of purple, which darkens as excess of the titrant is added to the solution. In a related way, it is used as a reagent to determine the Kappa number of wood pulp. For the standardization of KMnO4 solutions, reduction by oxalic acid is often used.[21] In agricultural chemistry, it is used for estimation of active carbon in soil.[22]
Aqueous, acidic solutions of KMnO4 are used to collect gaseous mercury in flue gas during stationary source emissions testing.[23]
In histology, potassium permanganate was used as a bleaching agent.[24][25]
Fruit preservation[edit]
Ethylene absorbents extend storage time of bananas even at high temperatures. This effect can be exploited by packing bananas in polyethylene together with potassium permanganate. By removing ethylene by oxidation, the permanganate delays the ripening, increasing the fruit’s shelf life up to 4 weeks without the need for refrigeration.[26][27][28]
Survival kits[edit]
Potassium permanganate is sometimes included in survival kits: as a hypergolic fire starter (when mixed with glycerol antifreeze from a car radiator;[29][30][31] as a water sterilizer; and for creating distress signals on snow).[32]
Fire service[edit]
Potassium permanganate is added to «plastic sphere dispensers» to create backfires, burnouts, and controlled burns. Polymer spheres resembling ping-pong balls containing small amounts of permanganate are injected with ethylene glycol and projected towards the area where ignition is desired, where they spontaneously ignite seconds later.[33][34] Both handheld[34] and helicopter-[33] or boat-mounted[34] plastic sphere dispensers are used.
Other uses[edit]
Potassium permanganate is one of the principal chemicals used in the film and television industries to «age» props and set dressings. Its ready conversion to brown MnO2 creates «hundred-year-old» or «ancient» looks on hessian cloth (burlap), ropes, timber, and glass.[35]
Potassium permanganate can be used to oxidize cocaine paste to purify it and increase its stability. This led to the Drug Enforcement Administration launching Operation Purple in 2000, with the goal of monitoring the world supply of potassium permanganate; however, potassium permanganate derivatives and substitutes were soon used thereafter to avoid the operation.[36]
Potassium permangate used as an oxidizing agent in the synthesis of cocaine and methcathinone.[37]
History[edit]
In 1659, Johann Rudolf Glauber fused a mixture of the mineral pyrolusite (manganese dioxide, MnO2) and potassium carbonate to obtain a material that, when dissolved in water, gave a green solution (potassium manganate) which slowly shifted to violet and then finally red.[38] The reaction that produced the color changes that Glauber observed in his solution of potassium permanganate and potassium manganate (K2MnO4) is now known as the «chemical chameleon». This report represents the first description of the production of potassium permanganate.[39] Just under 200 years later, London chemist Henry Bollmann Condy had an interest in disinfectants; he found that fusing pyrolusite with sodium hydroxide (NaOH) and dissolving it in water produced a solution with disinfectant properties. He patented this solution, and marketed it as ‘Condy’s Fluid’. Although effective, the solution was not very stable. This was overcome by using potassium hydroxide (KOH) rather than NaOH. This was more stable, and had the advantage of easy conversion to the equally effective potassium permanganate crystals. This crystalline material was known as ‘Condy’s crystals’ or ‘Condy’s powder’. Potassium permanganate was comparatively easy to manufacture, so Condy was subsequently forced to spend considerable time in litigation to stop competitors from marketing similar products.[40]
Early photographers used it as a component of flash powder. It is now replaced with other oxidizers, due to the instability of permanganate mixtures.
Preparation[edit]
Potassium permanganate is produced industrially from manganese dioxide, which also occurs as the mineral pyrolusite. In 2000, worldwide production was estimated at 30,000 tonnes.[9] The MnO2 is fused with potassium hydroxide and heated in air or with another source of oxygen, like potassium nitrate or potassium chlorate.[9] This process gives potassium manganate:
- 2 MnO2 + 4 KOH + O2 → 2 K2MnO4 + 2 H2O
(With sodium hydroxide, the end product is not sodium manganate but an Mn(V) compound, which is one reason why the potassium permanganate is more commonly used than sodium permanganate. Furthermore, the potassium salt crystallizes better.[9])
The potassium manganate is then converted into permanganate by electrolytic oxidation in alkaline media:
- 2 K2MnO4 + 2 H2O → 2 KMnO4 + 2 KOH + H2
Other methods[edit]
Although of no commercial importance, potassium manganate can be oxidized by chlorine or by disproportionation under acidic conditions.[41] The chlorine oxidation reaction is
- 2 K2MnO4 + Cl2 → 2 KMnO4 + 2 KCl
and the acid-induced disproportionation reaction may be written as
- 3 K2MnO4 + 4 HCl → 2 KMnO4 + MnO2 + 2 H2O + 4 KCl
A weak acid such as carbonic acid is sufficient for this reaction:
- 3 K2MnO4 + 2 CO2 → 2 KMnO4 + 2 K2CO3 + MnO2
Permanganate salts may also be generated by treating a solution of Mn2+ ions with strong oxidants such as lead dioxide (PbO2), sodium bismuthate (NaBiO3), or peroxydisulfate. Tests for the presence of manganese exploit the vivid violet color of permanganate produced by these reagents.
Reactions[edit]
Organic chemistry[edit]
Dilute solutions of KMnO4 convert alkenes into diols. This behaviour is also used as a qualitative test for the presence of double or triple bonds in a molecule, since the reaction decolorizes the initially purple permanganate solution and generates a brown precipitate (MnO2). In this context, it is sometimes called Baeyer’s reagent. However, bromine serves better in measuring unsaturation (double or triple bonds) quantitatively, since KMnO4, being a very strong oxidizing agent, can react with a variety of groups.
Under acidic conditions, the alkene double bond is cleaved to give the appropriate carboxylic acid:[42]
- CH3(CH2)17CH=CH2 + 2 KMnO4 + 3 H2SO4 → CH3(CH2)17COOH + CO2 + 4 H2O + K2SO4 + 2 MnSO4
Potassium permanganate oxidizes aldehydes to carboxylic acids, illustrated by the conversion of n-heptanal to heptanoic acid:[43]
- 5 C6H13CHO + 2 KMnO4 + 3 H2SO4 → 5 C6H13COOH + 3 H2O + K2SO4 + 2 MnSO4
Even an alkyl group (with a benzylic hydrogen) on an aromatic ring is oxidized, e.g. toluene to benzoic acid.[44]
- 5 C6H5CH3 + 6 KMnO4 + 9 H2SO4 → 5 C6H5COOH + 14 H2O + 3 K2SO4 + 6 MnSO4
Glycols and polyols are highly reactive toward KMnO4. For example, addition of potassium permanganate to an aqueous solution of sugar and sodium hydroxide produces the chemical chameleon reaction, which involves dramatic color changes associated with the various oxidation states of manganese. A related vigorous reaction is exploited as a fire starter in survival kits. For example, a mixture of potassium permanganate and glycerol or pulverized glucose ignites readily.[29] Its sterilizing properties are another reason for inclusion of KMnO4 in a survival kit.
Ion exchange[edit]
Treating a mixture of aqueous potassium permanganate with a quaternary ammonium salt results in ion exchange, precipitating the quat salt of permanganate. Solutions of these salts are sometimes soluble in organic solvents:[45]
- KMnO4 + R4NCl → R4NMnO4 + KCl
Similarly, addition of a crown ether also gives a lipophilic salt.[46]
Reaction with acids and bases[edit]
Permanganate reacts with concentrated hydrochloric acid to give chlorine and manganese(II):
- 2 KMnO4 + 16 HCl → 2 Mn2+ + 5 Cl2 + 8 H2O
In neutral solution, permanganate slowly reduces to manganese dioxide (MnO2). This is the material that stains one’s skin when handling KMnO4.
KMnO4 reduces in alkaline solution to give green K2MnO4:[47]
- 4 KMnO4 + 4 KOH → 4 K2MnO4 + O2 + 2 H2O
This reaction illustrates the relatively rare role of hydroxide as a reducing agent.
Addition of concentrated sulfuric acid to potassium permanganate gives Mn2O7.[48] Although no reaction may be apparent, the vapor over the mixture will ignite paper impregnated with alcohol. Potassium permanganate and sulfuric acid react to produce some ozone, which has a high oxidizing power and rapidly oxidizes the alcohol, causing it to combust. As the reaction also produces explosive Mn2O7, this should only be attempted with great caution.[49][50]
Thermal decomposition[edit]
Solid potassium permanganate decomposes when heated:
- 2 KMnO4 → K2MnO4 + MnO2(s) + O2
Safety and handling[edit]
Potassium permanganate poses risks as an oxidizer.[51] Contact with skin will result in a long lasting brown stain.[52]
References[edit]
- ^ Burriel F, Lucena F, Arribas S, Hernández J (1985). Química Analítica Cualitativa [Qualitative Analytical Chemistry] (in Spanish). p. 688. ISBN 84-9732-140-5.
- ^ a b c Haynes WM, ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). CRC Press. ISBN 978-1439855119.
- ^ Hocart R, Mathieu-Sicaud A (1945). «A stabilization factor in the polymorphism of ammonium nitrate». Comptes Rendus Hebdomadaires des Séances de l’Académie des Sciences [Weekly Reports of the Sessions of the Academy of Sciences] (in French). 221: 261–263.
- ^ Chambers M. «Potassium permanganate [USP:JAN] – Similar structures search, synonyms, formulas, resource links, and other chemical information». ChemIDplus: A Toxnet database. U.S. National Library of Medicine. ChemIDplus – CAS: 7722-64-7 InChi: VZJVWSHVAAUDKD-UHFFFAOYSA-N. Archived from the original on 13 August 2014. Retrieved 9 May 2018.
- ^ a b c World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ Brauer E, ed. (1963). Handbook of Preparative Inorganic Chemistry. New York: Academic Press.
- ^ Palenik GJ (1967). «Crystal structure of potassium permanganate». Inorg. Chem. 6 (3): 503–507. doi:10.1021/ic50049a015.
- ^ Miessler GL, Fischer PJ, Tarr DA (2014). Inorganic Chemistry (5th ed.). Pearson. p. 430. ISBN 978-0321811059.
- ^ a b c d e Reidies AH (2002). «Manganese Compounds». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a16_123.
- ^ a b World Health Organization (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). WHO Model Formulary 2008. World Health Organization. pp. 295, 300. hdl:10665/44053. ISBN 9789241547659.
- ^ British Medical Association; Royal Pharmaceutical Society (2015). British national formulary (69 ed.). p. 840. ISBN 9780857111562.
- ^ Assembly of Life Sciences (U.S.). Safe Drinking Water Committee (1977). Drinking water and health, Volume 2. National Academies Press. p. 98. ISBN 978-0-309-02931-5. Retrieved 2016-09-13.
- ^ Downey R, Barrington M (28 February 2005). «Red faces over pink water». The Northern Advocate. Archived from the original on 2011-07-19.
- ^ «Onoway apologizes for ‘alarming’ pink tap water». CBC News. 7 March 2017. Archived from the original on 7 March 2017. Retrieved 8 March 2017.
- ^ «EPA Guidance Manual Alternative Disinfectants and Oxidants». U.S. Environmental Protection Agency. 13 October 2015. Archived from the original on 2016-10-01.
- ^ Fatiadi A (1987). «The Classical Permanganate Ion: Still a Novel Oxidant in Organic Chemistry». Synthesis. 1987 (2): 85–127. doi:10.1055/s-1987-27859.
- ^ Glagovich N (2013). «Baeyer Test». Department of Chemistry and Biochemistry. Central Connecticut State University. Archived from the original on 24 January 2013. Retrieved 9 May 2018.
- ^ Thin Layer Chromatography stains http://www.reachdevices.com/TLC_stains.html
- ^ Jork, H., Funk, W., Fischer, W., Wimmer, H. (1990): Thin-Layer Chromatography: Reagents and Detection Methods, Volume 1a, VCH, Weinheim, ISBN 3-527-278834
- ^ Jork, H., Funk, W., Fischer, W., Wimmer, H. (1994): Thin-Layer Chromatography: Reagents and Detection Methods, Volume 1b, VCH, Weinheim
- ^ Kovacs KA, Grof P, Burai L, Riedel M (2004). «Revising the Mechanism of the Permanganate/Oxalate Reaction». J. Phys. Chem. A. 108 (50): 11026. Bibcode:2004JPCA..10811026K. doi:10.1021/jp047061u.
- ^ «Quick Reference Guide: Potassium Permanganate Test for Active Carbon». Agriculture Victoria—Victorian Resources Online. Victoria, Australia.
- ^ Code of Federal Regulations(7-1-07) Edition, Title 40, Part 60, Appendix A-8, Method 29, Section 7.3.1
- ^ Picken MM (April 2010). «Amyloidosis-where are we now and where are we heading?». Archives of Pathology & Laboratory Medicine. 134 (4): 545–551. doi:10.5858/134.4.545. PMID 20367306.
- ^ Murphy CL, Eulitz M, Hrncic R, Sletten K, Westermark P, Williams T, Macy SD, Wooliver C, Wall J, Weiss DT, Solomon A (July 2001). «Chemical typing of amyloid protein contained in formalin-fixed paraffin-embedded biopsy specimens». American Journal of Clinical Pathology. 116 (1): 135–142. doi:10.1309/TWBM-8L4E-VK22-FRH5. PMID 11447744.
- ^ Scott KJ, McGlasson WB, Roberts EA (1970). «Potassium Permanganate as an Ethylene Absorbent in Polyethylene Bags to Delay the Ripening of Bananas During Storage». Australian Journal of Experimental Agriculture and Animal Husbandry. 10 (43): 237. doi:10.1071/EA9700237.
- ^ Scott KJ, Blake, JR, Stracha, G, Tugwell, BL and McGlasson WB (1971). «Transport of Bananas at Ambient Temperatures using Polyethylene Bags». Tropical Agriculture (Trinidad). 48: 163–165.
- ^ Scott KJ, Gandanegara S (1974). «Effect of Temperature on the Storage Life of bananas Held in Polyethylene Bags with an Ethylene Absorbent». Tropical Agriculture (Trinidad). 51: 23–26.
- ^ a b Gillis B, Labiste D. «Fire by Chemical Reaction». PrimitiveWays. Archived from the original on 2015-09-24.
- ^ «Potassium Permanganate» (PDF). Pole Shift Survival Information. Archived from the original (PDF) on 4 August 2016. Retrieved 9 May 2018.
- ^ «Making Fire with Potassium Permanganate and Glycerin». thesurvivalcache. 3 November 2012. Archived from the original on 13 May 2016. Retrieved 13 September 2016.
- ^ «Distress Signals». Evening Post. CXXI (107): 5. 7 May 1936. Archived from the original on 5 November 2011.
- ^ a b «Aerial Ignition, Plastic Sphere Dispenser Description». Missoula Technology and Development Center. USDA Forest Service. Archived from the original on 26 April 2016. Retrieved 9 May 2018.
- ^ a b c «Wetland Warrior». Dirty Jobs. Season 6. Episode 2.
- ^ Brody E (February 2000). «Victor DeLor contractor profile». PaintPRO. 2 (1). Archived from the original on 2008-07-23. Retrieved 2009-11-12.
One of the techniques DeLor is known for among designers and clients is the special effects he creates with various chemical solutions. When applied to wood surfaces, these chemicals give a weathered appearance to new wood. … To achieve the aesthetic on interior surfaces, DeLor often uses a mixture of water and potassium permanganate, a dry powder chemical.
- ^ Gosmer K, Vammen M (March 10, 2014). «The Terrifying Substances People Put in Cocaine». Vice Media.
- ^ Binder R, Machata G, Stead H (May 2003). «[Analysis of potassium permanganate as addictive drug «precursor»]». Archiv Fur Kriminologie. 211 (5–6): 160–165. PMID 12872685.
- ^ Glauber, Johann Rudolph, Prosperitas Germaniae (The prosperity of Germany), part 3 (Amsterdam, (Netherlands): Johann Jansson, 1659), pp. 93–94. From pp. 93–94: » … donec tandem Magnesiam istam nitro fixo permixtam, in crucibulo forti coctione a nitro reseratam vidi, unde elegans color purpureus provenit, massam hanc effusam in pulvere redegi, aqua calida extraxi, per filtrum liquorem transmisi. Tandem vero elegantissimum purpureum, igneumque liquorem accepi, qui fere singulis horis in frigore tantummodo consistens colorem permutavit, sic ut jam viridis, jam caerulei, jam sanguinei coloris sponte sua factus sit, mox iterum alios elegantissimos colores receperit.» ( … until finally I saw [that] by mixing that magnesia [i.e., magnesia nigra, pyrolusite, the ore containing manganese dioxide ] with fixed niter [i.e., inert niter, potassium carbonate], by cooking [it] in a strong crucible, [the colored compound was] released by the niter, whence a fine purple color arises; this mass [was] poured out, reduced to powder, extracted with hot water, [and] the solution passed through a filter. Then I got a truly most elegant, purple, and fiery solution, which nearly every hour ([while] standing just in the cold) changed color, so that it was spontaneously made now green, now blue, now red in color; soon again it received other most elegant colors.) Glauber JR. «Prosperitatis Germaniae pars …. 3: In qua Salpetrae ex variis ubiq, obviis subiectis facillime atque copiose extrahendi modus traditur. Eiusve utilitates summae declarantur» [Part of the Prosperity of Germany …. 3: In which the method of extracting saltpeter from various everywhere, in the most convenient and abundant manner, is given. His interests are clearly stated] (in Latin). Archived from the original on 2016-12-20 – via Bavarian State Library. Translated in: Glauber JR (1689). The Works of the Highly Experienced and Famous Chymist, John Rudolph Glauber. Translated by Packe C. London, England: Thomas Millbourn. p. 353. Archived from the original on 2012-01-07.
- ^ Weeks ME (1956). Leicester HM (ed.). Discovery of the Elements (6th ed.). Easton, Pennsylvania: Journal of Chemical Education. pp. 172–173.
- ^ «Important Trade Mark Case». Otago Witness. 2 (2420): 53. 2 August 1900. Archived from the original on 4 March 2016.
- ^ Walton HF (1948). Inorganic Preparations. New York: Prentice-Hall. pp. 150–151.
- ^ Lee DG, Lamb SE, Chang VS (1990). «Carboxylic Acids from the Oxidation of Terminal Alkenes by Permanganate: Nonadecanoic Acid». Organic Syntheses.; Collective Volume, vol. 7, p. 397
- ^ Ruhoff JR. «n-Heptanoic acid». Organic Syntheses.; Collective Volume, vol. 2, p. 315
- ^ Gardner KA, Mayer JM (September 1995). «Understanding C-H bond oxidations: H. and H- transfer in the oxidation of toluene by permanganate». Science. 269 (5232): 1849–1851. Bibcode:1995Sci…269.1849G. doi:10.1126/science.7569922. PMID 7569922.
- ^ Herriott AW (1977). «Purple benzene: Solubilization of anions in organic solvents». J. Chem. Educ. 54 (4): 229. Bibcode:1977JChEd..54Q.229H. doi:10.1021/ed054p229.1.
- ^ Doheny Jr AJ, Ganem B (1980). «Purple benzene revisited». J. Chem. Educ. 57 (4): 308. Bibcode:1980JChEd..57..308D. doi:10.1021/ed057p308.1.
- ^ Nyholm RS, Woolliams PR (1968). «Manganates(VI)». Inorganic Syntheses. Inorg. Synth. Inorganic Syntheses. Vol. 11. pp. 56–61. doi:10.1002/9780470132425.ch11. ISBN 978-0-470-13242-5.
- ^ Cotton FA, Wilkinson G, Murillo CA, Bochmann M (1999). Advanced Inorganic Chemistry (6th ed.). Wiley-VCH. ISBN 0-471-19957-5.
- ^ Barthel H, Duvinage B (2000). «Clemens Winkler. His Experiments with Ozone in 1892». Praxis der Naturwissenschaften, Chemie. 49: 18ff.
- ^ Dzhabiev TS, Denisov NN, Moiseev DN, Shilov AE (2005). «Formation of Ozone During the Reduction of Potassium Permanganate in Sulfuric Acid Solutions». Russian Journal of Physical Chemistry. 79: 1755–1760.
- ^ Bretherick L, Urben PG, Pitt MJ (2007). Bretherick’s Handbook of Reactive Chemical Hazards. Vol. 1 (7th ed.). Elsevier Academic Press. pp. 1811–7. ISBN 978-0-12-373945-2.
- ^ Griffin S. «How to Remove Potassium Permanganate». livestrong.com. Archived from the original on 13 April 2018. Retrieved 9 May 2018.
Further reading[edit]
- «Potassium permanganate». Drug Information Portal. U.S. National Library of Medicine.
- «Manganese and compounds Fact Sheet». National Pollutant Inventory. Australia: Department of Climate Change, Energy, the Environment and Water.
- Lazur AM (2009). «The use of potassium permanganate in fish ponds». IFAS Extention. Gainesville, FL: University of Florida. Archived from the original on 2011-06-06.
External links[edit]
- International Chemical Safety Card 0672
Состав
Активное вещество в чистом виде.
Форма выпуска
Порошок для приготовления раствора для местного и наружного применения. Расфасовывается в хорошо закупоренную тару (жестянки, банки или — если предназначен для индивидуального пользования — в мелкую упаковку).
Фармакологическое действие
Дезодорирующее, антисептическое.
Фармакодинамика и фармакокинетика
Марганцовокислый Калий — что это?
Марганцовокислый калий или перманганат калия — это марганцовка. Препарат имеет вид мелкого порошка (кристаллов) красно- или темно-фиолетового цвета с металлическим блеском. В воде вещество растворяется в соотношении 1:18, слабый водный раствор розоватый, концентрированный раствор окрашен в темно-фиолетовый цвет.
Фармакодинамика
Антисептик. При соприкосновении перманганата калия (марганцовокислого калия) с органическими веществами образуется атомарный кислород.
Оксид, который образуется при восстановлении препарата, образует комплексные соединения с белками — альбуминаты. За счет чего марганцевокислый калий в малых концентрациях обладает вяжущими свойствами, а в концентрированных растворах проявляет прижигающее, раздражающее и дубящее действие.
Проявляет дезодорирующие свойства. Эффективен при лечении язв и ожогов.
Перманганат калия обладает способностью обезвреживать отдельные яды, и это его свойство нередко используется в ситуациях, когда необходимо сделать промывание желудка при пищевых токсикоинфекциях и отравлении неизвестными веществами.
Фармакокинетика
При попадании внутрь всасывается, может стать причиной развития метгемоглобинемии (гематотоксическое действие).
Показания к применению Марганцовокислого калия: для чего нужна марганцовка?
В качестве антисептика применяются водные растворы с концентрацией около 0,1%.
Средство используют для обработки обожженных участков тела, для промывания язв и инфицированных ран, для полоскания ротоглотки и горла при инфекционно-воспалительных заболеваниях слизистой ротовой полости и ротоглотки (в том числе при ангине), а также для обработки кожи при попадании на нее фениламина (анилина) и глаз в случае их поражения ядовитыми насекомыми.
В качестве рвотного средства перманганат калия принимают внутрь при отравлении алкалоидами (например, аконитином, морфином или никотином), хинином, фосфором, синильной кислотой. Оптимальная концентрация раствора марганцовки при отравлении — 0,02-1%.
С добавлением марганцовокислого калия готовят раствор для купания новорожденного.
Можно ли подмываться раствором Перманганата Калия?
Спринцевание марганцовкой в гинекологии иногда применяют при воспалительных процессах и молочнице.
Мужчинам при молочнице и ряде урологических заболеваний рекомендуют подмывание с марганцовкой.
Спринцевания при молочнице проводят раствором слабо-розового цвета (концентрация не выше 0,1%). Следует помнить, что такое средство как перманганат калия дает краткосрочный противомикробный эффект (патогенная флора уничтожается только на время проведения процедуры), поэтому использовать его следует только как дополнение к основному лечению.
Кристаллы препарата имеют свойство растворяться не сразу. В связи с этим, чтобы не спровоцировать ожог слизистой половых органов, раствор для подмывания/спринцевания готовят следующим образом: вначале в отдельной посуде делают концентрированный (ярко-малинового цвета) раствор, а затем его понемногу вливают в кипяченую воду.
Перманганат Калия при поносе
Водный раствор марганцовокислого калия в народной медицине нередко применяется для лечения поноса. При диарее взрослые обычно принимают средство внутрь, детям же (в том числе младенческого возраста) чаще делают клизму с марганцовкой.
При поносе в стакане воды растворяют несколько кристалликов перманганата калия, а затем вливают полученный раствор в другую емкость с водой. Разовая доза для взрослого — 200 мл, для ребенка — 100 мл. В некоторых случаях для прекращения диареи достаточно выпить 1 разовую дозу лекарства.
Марганцовка — это соль марганцовой кислоты. Ее эффективность при рвоте и поносе обусловлена высокой окисляющей способностью перманганат-иона, которая обеспечивает антисептическое действие средства.
Перманганат Калия при геморрое
При геморрое ванночки, примочки и подмывание с марганцовкой способствуют уменьшению отека, жжения и болезненных ощущений в области прямой кишки, тем самым существенно облегчая состояние пациента.
Для приготовления ванночки при геморрое следует 1,5 ст. ложки сухого порошка перманганата калия развести в 10 л теплой воды. Указанные пропорции относительны.
В первую очередь рекомендуется ориентироваться на цвет готового раствора: жидкость должна быть нежно-розовой, не яркой. Слишком концентрированный раствор может спровоцировать химический ожог и без того воспаленной и чувствительной кожи.
Продолжительность процедуры — 15 минут. Повторять ее для достижения стойкого эффекта нужно 2-3 раза в день. Лечение продолжают до тех пор, пока не станет заметно улучшение.
Если возможности сделать ванночку нет, тот же результат можно получить при помощи примочек (аппликаций) с марганцовкой.
Раствор также может использоваться для регулярной гигиены заднего прохода. Лечение обычно длится около 1 недели.
Противопоказания
Гиперчувствительность.
Побочные действия
Реакции гиперчувствительности. В случае применения слишком концентрированного раствора возможны раздражение и ожоги.
Калия Перманганат: инструкция по применению (Способ и дозировка)
Согласно инструкции по применению, средство применяется наружно, в виде водных растворов различной концентрации:
- 0,02-1%-ный — для промывания желудка при отравлении, спринцеваний и подмывания;
- 0,01-1%-ный — для полоскания горла и ротовой полости;
- 0,1-05%-ный раствор — для обработки ран;
- 2-5%-ный — для смазывания ожоговых и язвенных поверхностей.
Применение концентрированных растворов Марганцовки
Пятипроцентный раствор марганцовокислого калия считается особенно концентрированным, поэтому он не может ни при каких обстоятельствах использоваться для внутреннего потребления и обработки слизистых: средство применяется только в крайних случаях и только наружно.
Некоторые специалисты рекомендуют использовать его для лечения грибковой инфекции кожи и онихомикозов, однако большинство микологов предпочитают назначать специальные противогрибковые препараты, поскольку они, по их мнению, более безопасны и эффективны.
Бытует также мнение что 5%-ный раствор эффективен при укусах ядовитых насекомых (например, тарантулов или скорпионов) и ядовитых змей. В данном случае его используют для промывания пораженного места, однако подобная мера может расцениваться только как первая помощь пострадавшему, и не отменяет необходимости обращения к врачу и немедленной (если это необходимо) госпитализации.
В народной медицине примочки с концентрированным холодным (!) раствором марганцовки иногда используются для лечения термических ожогов. Считается также, что регулярная обработка опасных с точки зрения появления пролежней участков тела крепким раствором марганцовокислого калия, помогает предупредить дистрофическое или язвенно-некротическое изменение тканей.
Безопасность и эффективность такого лечения, однако, следует в обязательном порядке обсуждать с лечащим врачом.
Пятипроцентный раствор используется и для лечения генерализованных поражений кожи, например, пиодермии.
Ванна от прыщей с марганцовокислым калием способствует ускорению подсыхания элементов сыпи и отпадению корочек. Процедуру повторяют ежедневно до исчезновения проявлений заболевания. Продолжительность воздействия — не более 15 минут. После ванной рекомендуется ополоснуть кожу прохладной водой.
Концентрированный раствор можно использовать от прыщей на спине, а также для прижигания мозолей и бородавок. Средство в указанных случаях наносят точечно.
Как развести Марганцовку при ветрянке?
При ветрянке перманганат калия разводят таким образом, чтобы получился не слишком концентрированный раствор. Это значит, что жидкость должна быть светло-розового цвета.
Правила разведения следующие: вначале несколько крупинок марганцовки растворяют примерно в 500 мл теплой воды, а затем полученный раствор переливают в другую емкость и доводят объем воды до нужного.
Сменным в растворе ватным тампоном протирают места высыпаний. Когда высыпания сойдут, для ускорения процесса подсыхания корочек можно принимать ванны с неконцентрированным раствором марганцовокислого калия.
Как сделать 5% раствор Марганцовки?
Для приготовления 5%-ного раствора 5 граммов препарата растворяют в 100 мл воды. Чтобы не ошибиться с дозировкой, необходимо пользоваться кухонными весами.
Если весов нет, в расчетах нужного количества перманганата калия отталкиваются от того, что в 1 ч. ложке его вмещается 6 граммов. Таким образом, для получения 5%-ного раствора, следует добавить это количество марганцовки к 120 мл воды.
Если в аптеке был куплен 3-х граммовый флакон с марганцовкой, для получения раствора нужной концентрации перманганат калия следует соединить с 60 мл воды.
Когда все кристаллы растворятся в воде, готовый раствор процеживают сквозь сложенную в несколько слоев марлю.
Как разводить для купания новорожденного Марганцовку?
Поскольку кожа младенцев очень нежная и чувствительная, для купания должен использоваться светло-розовый, не концентрированный раствор для купания.
Рекомендации относительно того, как сделать слабый раствор марганцовки следующие: в прозрачную стеклянную посуду наливают теплой воды и добавляют небольшое (на кончике ножа) количество перманганата калия.
Убедившись, что все кристаллики растворились, раствор переливают в другую емкость и доливают воду до нужного объема.
Передозировка
Симптомы передозировки проявляются резкой болью в ротовой полости, по ходу пищевода и в животе, диареей, рвотой. Слизистая ротоглотки отекает (возможен отек гортани), изменяет цвет на темно-коричневый или фиолетовый.
Кроме того, у пострадавшего развиваются ожоговый шок и механическая асфиксия; появляются судороги, двигательное возбуждение, явления паркинсонизма, нефропатии, геморрагического колита, гепатопатии.
При пониженной кислотности желудка может развиться метгемоглобинемия с одышкой и выраженным цианозом.
Для ребенка смертельной является доза, равная 3 г. Для взрослого величина смертельной дозы колеблется в пределах от 0,3 до 0,5 г/кг.
Лечение: в/в введение 5% раствора Аскорбиновой кислоты (30 мл), в/м введение Пиридоксина 5% (3 мл) и Цианокобаламина (до 1 г), а также 1% раствора метиленового синего (50 мл).
Взаимодействие
Марганцовокислый калий химически несовместим с рядом органических веществ (включая танин, сахар, уголь).
Взрывается при обработке концентрированной H2SО4 (серной кислотой).
Даже при незначительном (до комнатной температуры) нагреве активно взаимодействует с большинством восстановителей (например, с глицерином) и легкоокисляющимися веществами. Реакция сопровождается саморазогреванием, что в ряде случаев вызывает самовоспламеняющиеся смеси и может привести к взрыву.
Очень опасно растирать кристаллы марганцовокислого калия с порошками активных металлов и неметаллов (алюминием, серой, кальцием, фосфором, магнием и др.), поскольку подобные действия нередко сопровождаются взрывом.
Условия продажи
Перманганат калия в России включен в IV список прекурсоров ПККН, в Украине с 14.06.2013 также признан прекурсором и внесен в список наркотических веществ.
В российских аптеках, согласно утвержденному Приказом Минздавсоцразвития РФ №578 от 13.09.2005 “Перечню ЛС, отпускаемых без рецепта врача”, который действовал до 16.10.2011, средство должно отпускаться без рецепта, но не более 2 упаковок в одни руки.
Рецепт на латинском (образец): Rp: Sol. Kalii permanganatis 5% 10 ml DS. Для обработки краев раны.
Условия хранения
Порошок должен храниться в темном месте в хорошо закупоренной таре.
Срок годности
Не ограничен. Водные растворы рекомендуется хранить не больше 3-4 дней.
Особые указания
Калия перманганат — что это такое?
В Википедии указывается, что калия перманганат, который в быту чаще называют марганцовкой, является калиевой солью марганцовой кислоты — сильной неорганической кислоты, которая имеет формулу HMnO4.
Как выглядит марганцовка, известно всем — каждый хоть раз в жизни видел темно-фиолетовые с металлическим блеском кристаллы.
Свойства и применение Марганцовки в медицине
Марганцовокислый калий является сильным окислителем и, следовательно, обладает выраженным антисептическим (противомикробным) действием.
Эффекты средства объясняются тем, что в водном растворе при наличии легко окисляющихся элементов от марганцовокислого калия начинает активно отщепляться газообразного типа кислород, который проявляет свойства очень мощного антисептика.
В концентрированных растворах марганцовка оказывает выраженное прижигающее и раздражающее действие.
Что можно сделать из Перманганата калия: альтернативные способы применения
Помимо медицины, средство используется:
- для определения перманганатной окисляемости при оценке качества воды по методу Кубеля;
- для мытья лабораторной посуды (щелочной раствор марганцовки хорошо убирает остатки жира и других органических веществ);
- в пиротехнике (в качестве сильного окислителя);
- для тонирования фотографий (растворы с концентрацией перманганата калия 3 г/л);
- в космических жидкостно-ракетных двигателях (в качестве катализатора разложения пероксида водорода);
- для травления дерева;
- для выведения татуировок (однако такой способ не позволяет полностью убрать тату и оставляет шрамы на теле);
- для получения карбоновых кислот из парафинов;
- для отбеливания тканей.
В интернете можно найти видео “Марганцовка и бензин”, в котором перманганат калия рекомендуют добавлять в бензобак автомобиля для обогащения топлива кислородом.
Химические свойства
Формула перманганата калия — KMnO4. Молярная масса — 158,03 г/моль.Вещество имеет вид темно-фиолетовых кристаллов, не образует кристаллогидратов, характеризуется умеренной растворимостью в воде (растворимость повышается при повышении температуры воды), не гидролизуется, в растворах разлагается медленно.
Сильный окислитель при спекании и в растворе. Вступает в реакцию с типичными восстановителями (водородом, этанолом и т.д.). Концентрированные растворы имеют интенсивную фиолетовую окраску, слабые — окрашены в розовый цвет.
Окислительная способность перманганат-иона ослабевает по мере уменьшения кислотности раствора. В щелочной среде под действием восстановителей восстанавливается до манганат-иона; MnO4 в слабощелочной, нейтральной и слабокислой среде переходит в диоксид марганца.
В кислотной среде перманганат-ион трансформируется в аквакатион.
Фактор эквивалентности марганцовокислого калия fэкв(KMnO4) в зависимости от кислотности среды составляет 1/5, ⅓ и 1.
Разбавленный водный раствор марганцовокислого калия неустойчив и разлагается с образованием осадка диоксида марганца (хлопья бурого цвета) и выделение кислорода. Разложение ускоряется под воздействием солнечных лучей.
Особенно быстро портится раствор перманганата калия в присутствии восстановителей.
Подкисленный раствор обесцвечивается под воздействием раствора щавелевой кислоты. Его также используют при проведении титриметрического анализа при определении пероксида водорода, солей железа (II), оксалатов.
Углеводород не обесцвечивает раствор перманганата калия (подкисленный). Бензол не обесцвечивает раствор перманганата калия.К обесцвечиванию ведет пропускание через подкисленный раствор KMnO4 сероводорода.
Этилен обесцвечивает раствор перманганата калия при пропускании через него (по мере окисления этилена в этиленгликоль).
Реакция окисления этилена перманганатом калия выглядит так:
В ходе этой реакции отмечается обесцвечивание фиолетовой окраски водного раствора марганцовокислого калия, поэтому ее используют как качественную реакцию на алкены.
Разбавленный раствор KMnO4 в нейтральной и щелочной среде провоцирует окисление алкенов до диолов (реакция гидроксилирования алкенов или реакция Вагнера).
Окисление ацетилена марганцовокислым калием в слабощелочной среде протекает с образованием оксалата калия. Реакция ацетилена с KMnO4 описывается уравнением: 3C2H2 + 8KMnO4 = 3K2C2O4 +2H2O + 8MnO2 + 2KOH
В кислотной среде ацетилен окисляется до углекислого газа: C2H2 + 2KMnO4 +3H2SO4 =2CO2 + 2MnSO4 + 4H2O + K2SO4
Окисление альдегидов, которые являются сильными восстановителями, протекает при нагревании и описывается формулой: 3CH3CHO + 2KMnO4 = CH3COOH + 2CH3COOK + 2MnO2 + H2O
Окисление этилового спирта перманганатом калия в присутствии концентрированной серной кислоты и при нагревании слабым пламенем начинается с обесцвечивания раствора. В результате этой реакции выпадают хлопья оксида марганца (IV) бурого цвета. При избытке H2SO4 раствор становится бесцветным, ощущается запах уксусного альдегида.
Окисление 3-нитротолуола марганцовокислым калием в щелочной среде позволяет получить о-нитробензойную кислоту.
Разложение перманганата калия при нагревании является одним из способов получения кислорода. Для этого следует насыпать в пробирку с газоотводной трубкой кристаллы KMnO4 и затем нагреть пробирку.
При этом выделяющийся кислород будет по трубке поступать в колбу и постепенно заполнять ее (О2 тяжелее воздуха, поэтому не покидает колбу). Если поместить в колбу тлеющую лучину, она вспыхнет.
Уравнение реакции разложения перманганата калия выглядит так: 2 KMnO4 = K2MnO4 + MnO2 + O2 ↑
Очистка самогона Марганцовкой и содой
У самогонщиков большой популярностью пользуется метод очистки самогона при помощи марганцовки, питьевой соды и щелочи (например, каустической соды). Перманганат калия убирает сивушные масла, питьевая соды нейтрализует уксусную кислоты, щелочь — другие вредные примеси.
При отсутствии щелочи можно ограничиться применением только лишь марганцовки и соды.
Последовательность действий:
- Марганцовку разводят в воде из расчета 1,5 г на 1 л продукта.
- Соду разводят в воде. Для очистки 10 л самогона необходимо приготовить раствор из 100 г соды и 100 мл воды.
- Влить в самогон вначале содовый раствор, перемешать, а затем раствор марганцовки.
- Настаивать в течение получаса.
- Развести каустическую соду (или другую щелочь) водой в равных пропорциях из расчета 2 г на 1 л самогона (щелочь заливают водой, а не высыпают в воду — это важно!).
- Самогон накрывают крышкой и отстаивают в темном месте в течение 12-14 ч, а затем фильтруют через уголь или вату.
Применение Марганцовки в садоводстве
Садоводы и огородники знают о полезных свойствах перманганата калия и поэтому повсеместно используют марганцовку для растений.
Применение на огороде целесообразно, когда необходимо протравить семена перед посадкой: такая обработка позволяет уничтожить зимующих на семенах возбудителей болезней.
Чтобы приготовить раствор нужной концентрации в 100 мл воды растворяют 0,5 г перманганата калия. Семена помещают в полученную жидкость на 20 минут, а затем просушивают.
Обработка картофеля перед посадкой марганцовкой позволяет защитить клубни от болезнетворных грибков и проволочника. Для замачивания клубней используется раствор темно-розового цвета.
Для обработки лука перед посадкой используют розовый раствор. Луковички помещают в него так, чтобы жидкость покрывала их, и оставляют на 8-12 часов.
Для обработки клубники весной хорошо подходит средство с таким составом: 1 стакан золы, 1-2 л кипятка (золу заливают кипящей водой и дают ей остыть), 2 г перманганата калия, 2 г порошка борной кислоты, 1 ст. ложка йода. Смесь процеживают, выливают в ведро и доливают водой, используют для опрыскивания.
Раствор действует и как удобрение, и как средство от вредителей.
Раствором перманганата калия можно проливать грунт для рассады, мыть ящики, горшочки и стаканчики перед посадкой зелени или рассады, обрабатывать парники и теплицы для профилактики болезней растений.
Для обработки почв, для рассады, полива клубники и кустов (крыжовника, малины, смородины) ранней весной используют раствор, приготовленный в пропорциях 3 г перманганата калия на 10 л воды. В особенности хорошо использовать такое средство на песчаных почвах.
Тем не менее, увлекаться марганцовкой для обработки земли и полива цветов все же не стоит — избыточное содержание марганца в почве может неблагоприятно сказаться на развитии растений.
Опрыскивание земляники раствором, приготовленным в пропорциях 2 ч. ложки перманганата калия на 10 л воды спасает землянику от серой гнили. Обработку ягод следует проводить после цветения.
Можно ли поливать рассаду марганцовкой? Раствор перманганата калия обычно используют для дезинфекции почвы в приспособленных под рассаду ящиках и стаканчиках, а также на грядках. Рассаду в стаканчиках нужно поливать теплым розовым раствором раз в десять дней (по желанию чередуя с поливом зольным щелоком).
Перед высадкой в грунт любых семян землю в ящике поливают раствором, для приготовления которого 3-5 г перманганата калия растворяют в 10 л воды.
Многих огородников интересует, можно ли поливать помидоры марганцовкой. Опытные специалисты утверждают, что даже нужно, поскольку такая обработка предотвращает многие заболевания растений.
Можно ли поливать цветы марганцовкой? Можно, но не слишком усердствуя, чтобы не навредить. Польза такого полива раствором перманганата калия огромна.
Во-первых, растение получает дополнительные марганец и калий. Во-вторых, повышается кислотность почвы, что благоприятствует росту некоторых растений. В-третьих, обеззараживается грунт.
Раствор для цветов должен быть бледно-розового цвета. Для его приготовления достаточно капнуть в стакан воды несколько капель концентрированного раствора марганцовки.
Как отмыть с рук Марганцовку?
Чтобы смыть с рук оставленные марганцовкой пятна, можно использовать дольку лимона, спирт или смешанные в равных пропорциях 5-9% уксус и перекись водорода.
Люди, советующие, чем отмыть с кожи марганцовку, также отмечают эффективность универсального моющего средства, которое готовят из 100 г мыла (детского или хозяйственного, натертого на мелкую терку), 100 мл горячей воды, пищевой соды (2-3 ст. ложки) и 2-3 капель эфирного масла.
Марганцовка плюс сахар: развести костер подручными средствами
Чтобы развести огонь без спичек, нужно взять палочку, плоскую дощечку, марганцовку и сахар. Палочкой сильно трут марганцовку с сахаром. В результате химической реакции смесь самовоспламеняется.
Меры предосторожности
Не следует растворять и хранить перманганат калия в металлических емкостях, поскольку марганцовка вступит с ними во взаимодействие и утратит часть лечебных свойств. Оптимально использовать для приготовления водных растворов стеклянную посуду.
Если марганцовка спровоцировала ожог — что делать?
При ожоге ротовой полости, пищевода и желудка концентрированным раствором марганцовокислого калия следует немедленно промыть пострадавшему желудок, дать ему Активированный уголь и слабый раствор перекиси водорода с уксусом (полстакана перекиси и 1 стакан столового уксуса на 2 л воды).
Чем можно заменить марганцовку?
Аналоги перманганата калия: Аммиак+глицерол+этанол, Асептолин, Анмарин, Бактодерм, Витаон, Дерматоло-дегтярный линимент, Диоксизоль, ЗеленКа, Калефлон, Катапол, Катацел, Нафталанная мазь, Спирт этиловый, Протол, Перекись водорода, Тамбуканская грязь, Формидрон, Формагель, Элекасол, Этол 96%, Цинково-салициловая паста, Чага.
При беременности
При беременности допускается только наружное применение марганцовки. Прием раствора перманганата калия внутрь противопоказан.
Определение беременности при помощи Марганцовки
Этот метод определения беременности относится к категории “бабушкиных”, однако многие беременные женщины утверждают, что он является достаточно точным.
В 500 л теплой воды разводят небольшое количество порошка перманганата калия (чтобы жидкость окрасилась в бледно-розовый цвет) и добавляют к полученному раствору немного мочи.
Если жидкость светлеет, беременности нет, если на дно банки выпал осадок в виде хлопьев — есть основания предполагать беременность.
Отзывы
Марганцовка — это проверенный временем антисептик, который, несмотря на обилие других средств, широко используется буквально с рождения. Отзывы о перманганате калия подтверждают его эффективность при кожных заболеваниях, отравлениях, цистите, ангине и еще целом ряде заболеваний.
Некоторые женщины также используют марганцовку от нежелательных волос. Отзывы и фотографии, которыми они сопровождаются, позволяют сделать вывод, что при регулярном применении слабого раствора перманганата калия для удаления волос волоски со временем истончаются и становятся менее заметными.
Однако есть и менее оптимистичные отзывы об удалении волос марганцовкой — в них женщины указывают, что гораздо надежнее прибегнуть к профессиональному удалению волос специальным аппаратом.
Цена Марганцовки. Где взять Перманганат калия?
Приобрести Перманганат калия непросто. В интернете много как сообщений о том, что марганцовка запрещена и найти ее очень проблематично.
На вопрос, почему запретили продажу этого средства, некоторые фармацевты отвечают, что соответствующими приказами марганцовку приравняли к взрывчатым веществам, и продавать ее без лицензии нельзя.
Другие же говорят, что марганцовокислый калий отнесен к наркотическим веществам и, опять-таки, его продажа без соответствующей лицензии невозможна.
В советах относительно того, где купить марганцовку в аптеке Москвы, обычно указывают специализированные аптеки при родильных отделениях и детских поликлиниках, а также ветеринарные аптеки.
Перманганат калия купить в Москве можно также в хозяйственных магазинах и магазинах, которые реализуют товары для садоводства.
Аналогичные рекомендации дают в ответ на вопрос, где можно купить марганцовокислый калий в СПб или Киеве.
Сколько стоит в аптеке Марганцовка? Цена средства варьируется в пределах от 11 до 165 руб. (в зависимости от объема упаковки и формы выпуска).
Перманганат калия ТУ 6-09-03-446-77
Ca(MnO4)2.4H2O
Перманганат калия (лат. Kalii permanganas, распространённое название в быту — марганцовка) — марганцовокислый калий, калиевая соль марганцовой кислоты. Химическая формула — KMnO4. Представляет собой тёмно-фиолетовые, почти чёрные кристаллы, при растворении в воде образующие ярко окрашенный раствор малинового цвета.
| Систематическое наименование |
Перманганат калия |
|---|---|
| Традиционные названия |
Марганцовокислый калий, марганцовка |
| Хим. формула |
KMnO4 |
| Физические свойства | |
| Состояние |
твердое (хрупкие кристаллы) |
| Молярная масса |
158,03 г/моль |
| Плотность |
2,703 г/см³ |
| Термические свойства | |
| Т. разл. |
240 °C |
| Мол. теплоёмк. |
119,2 Дж/(моль·К) |
| Энтальпия образования |
-813,4 кДж/моль |
| Химические свойства | |
| Растворимостьв воде |
6,38 (20 °C) |

Кристаллы перманганата калия под микроскопом

Перманганат калия в виале
Пермангана́т ка́лия (лат. Kalii permanganas, распространённое название в быту — марганцо́вка) — марганцовокислый калий, калиевая соль марганцовой кислоты. Химическая формула — KMnO4. Представляет собой тёмно-фиолетовые, почти чёрные кристаллы, при растворении в воде образующие ярко окрашенный раствор цвета фуксии.
Физические свойства
Внешний вид: тёмно-фиолетовые кристаллы с металлическим блеском. Показатель преломления составляет 1,59 (при 20 °C).
Растворяется в воде (см. таблицу), жидком аммиаке, ацетоне (2:100), метаноле, пиридине.
| Температура, °C | 10 | 20 | 25 | 30 | 40 | 50 | 65 |
|---|---|---|---|---|---|---|---|
| Растворимость, г/100 г воды | 4,22 | 6,36 | 7,63 | 9 | 12,5 | 16,8 | 25 |
Термодинамические свойства
| Стандартная энтальпия образования ΔH | −813,4 кДж/моль (т) (при 298 К) |
|---|---|
| Стандартная энергия Гиббса образования G | −713,8 кДж/моль (т) (при 298 К) |
| Стандартная энтропия S | 171,71 Дж/(моль·K) (т) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 119,2 Дж/(моль·K) (т) (при 298 К) |
Химические свойства
| Окисленная форма | Восстановленная форма | Среда | E0, В |
|---|---|---|---|
| MnO4− | MnO42− | OH− | +0,56 |
| MnO4− | H2MnO4 | H+ | +1,22 |
| MnO4− | MnO2 | H+ | +1,69 |
| MnO4− | MnO2 | OH− | +0,60 |
| MnO4− | Mn2+ | H+ | +1,51 |

Является сильным окислителем. В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия):
- в кислой среде:
;
- в нейтральной среде:
;
- в щелочной среде:
.
Однако последняя реакция (в щелочной среде) идёт по указанной схеме только при недостатке восстановителя и высокой концентрации щёлочи, которая обеспечивает замедление гидролиза манганата калия.
При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII):
.
При этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца 
.
При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением:
.
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением:
.
Реагирует с солями двухвалентного марганца, например:
.
Эта реакция в принципе обратна дисмутации (диспропорционирование) 


Окисляет органические вещества. В частности, разбавленные растворы перманганата калия в щелочной и нейтральной среде окисляют алкены до диолов (реакция Вагнера):
Водные растворы перманганата калия термодинамически нестабильны, но кинетически довольно устойчивы. Их сохранность резко повышается при хранении в темноте.
При смеси с пероксидом водорода протекает следующая реакция:
.
Перманганат калия реагирует с концентрированной соляной, бромоводородной или иодоводородной кислотой. В результате выделяются свободные галогены:
Во время химической реакции хлорид-анион 


Применение
Применение этой соли чаще всего основано на высокой окисляющей способности перманганат-иона, обеспечивающей антисептическое действие.
Медицинское применение
Разбавленные растворы (около 0,1 %) перманганата калия нашли широчайшее применение в медицине как антисептическое средство, для полоскания горла, промывания ран, обработки ожогов. В качестве рвотного средства для приёма внутрь при отравлениях морфином, аконитином и некоторыми другими алкалоидами используют разбавленный (0,02—0,1 %) раствор перманганата калия[1].
Фармакологическое действие
Антисептическое средство. При соприкосновении с органическими веществами выделяет атомарный кислород. Образующийся при восстановлении препарата оксид образует с белками комплексные соединения — альбуминаты (за счёт этого калия перманганат в малых концентрациях оказывает вяжущее, а в концентрированных растворах — раздражающее, прижигающее и дубящее действие). Обладает также дезодорирующим эффектом. Эффективен при лечении ожогов и язв. Способность калия перманганата обезвреживать некоторые яды лежит в основе использования его растворов для промывания желудка при отравлениях неизвестным ядом и пищевых токсикоинфекциях. При попадании внутрь всасывается, оказывая действие (приводит к развитию метгемоглобинемии).
Показания
Смазывание язвенных и ожоговых поверхностей — инфицированные раны, язвы и ожоги кожи. Полоскание полости рта и ротоглотки — при инфекционно-воспалительных заболеваниях слизистой оболочки полости рта и ротоглотки (в том числе при ангинах). Для промывания и спринцеваний при гинекологических и урологических заболеваниях — кольпиты и уретриты. Для промываний — желудка при отравлениях, вызванных приёмом внутрь алкалоидов (морфин, аконитин, никотин), синильной кислотой, фосфором, хинином; кожи — при попадании на неё анилина; глаз — при поражении их ядовитыми насекомыми.
Противопоказания
Гиперчувствительность.
При передозировке: резкая боль в полости рта, по ходу пищевода, в животе, рвота, диарея; слизистая оболочка полости рта и глотки — отёчная, тёмно-коричневого, фиолетового цвета, возможен отёк гортани, развитие механической асфиксии, ожогового шока, двигательного возбуждения, судорог, явлений паркинсонизма, геморрагического колита, нефропатии, гепатопатии. При пониженной кислотности желудочного сока возможно развитие метгемоглобинемии с выраженным цианозом и одышкой. Смертельная доза для детей — около 3 г, для взрослых — 0,3—0,5 г/кг.
Лечение: метиленовый синий (50 мл 1 % раствора), аскорбиновая кислота (внутривенно — 30 мл 5 % раствора), цианокобаламин — до 1 мг, пиридоксин (внутримышечно — 3 мл 5 % раствора).
Способ применения и дозы
Наружно, в водных растворах для промывания ран (0,1—0,5 %), для полоскания рта и горла (0,01—0,1 %), для смазывания язвенных и ожоговых поверхностей (2—5 %), для спринцевания (0,02—0,1 %) в гинекологической и урологической практике, а также промывания желудка при отравлениях.
Предосторожности
Активно взаимодействует при нагреве и даже при комнатной температуре с большинством восстановителей, например, органическими веществами (сахарозой, танинами, глицерином и многими другими), легкоокисляющимися веществами, поэтому при смешивании происходит саморазогревание, что иногда вызывает самовоспламенение смеси (с концентрированным раствором глицерина, или безводным — всегда) и может привести к взрыву.
Очень опасно растирание сухого перманганата калия с органическими веществами и порошками активных металлов и неметаллов (кальцием, алюминием, магнием, фосфором, серой и др.) — весьма вероятен взрыв.
Другие сферы применения
- 1—2%-й раствор используется садоводами для протравливания семян перед посадкой[2]
- Применяется для определения перманганатной окисляемости при оценке качества воды согласно ГОСТ 2761-84 по методу Кубеля[3].
- Щелочной раствор перманганата калия хорошо отмывает лабораторную посуду от жиров и других органических веществ.
- Растворы (концентрации примерно 3 г/л) широко применяются при тонировании фотографий.
- В пиротехнике применяют в качестве сильного окислителя.
- Применяют в качестве катализатора разложения перекиси водорода в космических жидкостно-ракетных двигателях.
- Водный раствор перманганата калия используется для травления дерева, в качестве морилки.
- Водный раствор применяется также для выведения татуировок. Результат достигается посредством химического ожога, при котором отмирают ткани, в которых содержится красящее вещество. Данный метод немногим отличается от простого срезания кожи, обычно он менее эффективен и более неприятен, так как ожоги заживают намного дольше. Татуировка не удаляется полностью, на её месте остаются шрамы.
- Перманганат калия или бихромат натрия используются в качестве окислителя при получении мета- и парафталевых кислот из мета- и параксилолов, соответственно (см. Терефталевая кислота).
- Перманганат калия является прекурсором в синтезе мефедрона и меткатинона (эфедрона)
Получение
Химическое или электрохимическое окисление соединений марганца, диспропорционирование манганата калия. Например:
,
,
,
.
Последняя реакция происходит при электролизе концентрированного раствора манганата калия и эндотермична, она является основным промышленным способом получения перманганата калия.
Ограничение на покупку
Входит в IV список прекурсоров ПККН в России[4] (допускается исключение некоторых мер контроля).
14 июня 2013 года на Украине был признан прекурсором и внесён в список наркотических веществ[5].
Примечания
- ↑ М. Д. Машковский. Лекарственные средства. — М.: ООО «Новая волна», 2002. — Т. 2. — 608 с. — 25 000 экз. — ISBN 5-7864-0129-4.
- ↑ Протравливание семян марганцовкой, приготовление раствора марганцовки. Как правильно развести марганцовку? — Всё о рассаде и теплицах. Дата обращения: 19 февраля 2019. Архивировано 25 февраля 2019 года.
- ↑ 6.2.6. Окисляемость, или химическое потребление кислорода (ХПК). www.anchem.ru. Дата обращения: 11 февраля 2023.
- ↑ Постановление Правительства РФ от 30.06.1998 N 681 «Об утверждении перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации» (с изменениями и дополнениями). Дата обращения: 27 марта 2014. Архивировано 20 апреля 2013 года.
- ↑ На Украине марганцовку признали прекурсором. Газета.Ru (14 июня 2013). Дата обращения: 14 июня 2013. Архивировано 18 июня 2013 года.
Литература
- Вульфсон Н. С. Препаративная органическая химия. — С. 656, 657.
- Казанский Б. А. (ред.). Синтезы органических препаратов (сборник 3). — С. 145.
- Реми Г. Курс неорганической химии (том 1). — С. 817.
Ссылки
- International Chemical Safety Card 0672
Эта страница в последний раз была отредактирована 11 февраля 2023 в 11:59.
Как только страница обновилась в Википедии она обновляется в Вики 2.
Обычно почти сразу, изредка в течении часа.





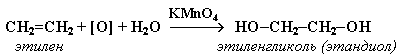





![{displaystyle {ce {2KMnO4->[^{circ }t]K2MnO4 +MnO2 +O2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9118731b5eb0575cae1da3c467a2d760f85453a5)
![{displaystyle {ce {5KMnO4->[^{circ }t]K2MnO4 +K3MnO4 +3MnO2 +3O2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9f9d3b8a183d05ee5073650c26e6bf2bc8ed4e66)