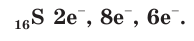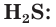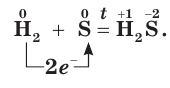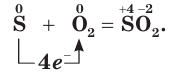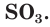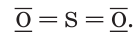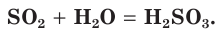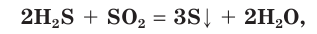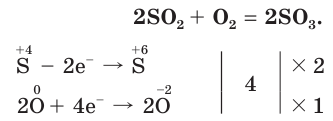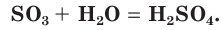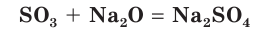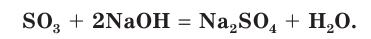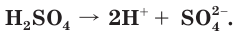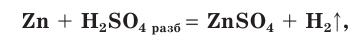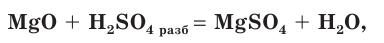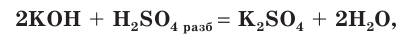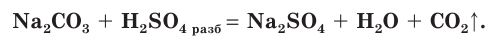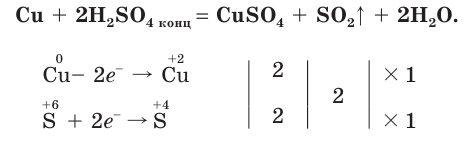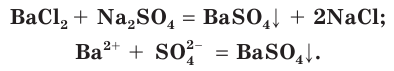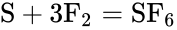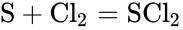Сера — химический элемент № (16). Она расположена в VIА группе третьем периоде Периодической системы.
S16+16)2e)8e)6e
На внешнем слое атома серы содержатся шесть валентных электронов. До завершения внешнего слоя не хватает двух электронов. Поэтому в соединениях с металлами и водородом сера проявляет степень окисления (–2). При взаимодействии с более электроотрицательными элементами (кислородом, галогенами) сера образует соединения, в которых её степень окисления положительная ((+4) или (+6)).
В земной коре сера встречается в самородном виде или в виде минералов и горных пород: (пирит —
FeS2
, цинковая обманка —
ZnS
, свинцовый блеск —
PbS
, гипс —
CaSO4⋅2H2O
, глауберова соль —
Na2SO4⋅10H2O
).
|
|
|
|
Рис. (1). Самородная сера |
Рис. (2). Пирит |
Сера относится к макроэлементам живых организмов. Она содержится в белках. Больше всего серы в белках, которые образуют шерсть, волосы, рога. Входит она также в состав некоторых витаминов и гормонов.
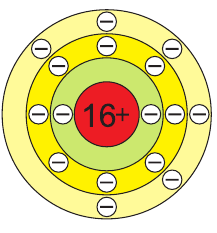
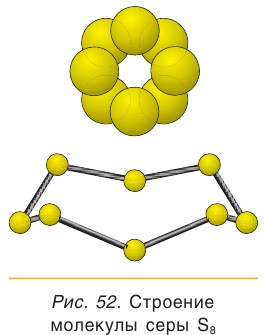
Сера образует несколько аллотропных модификаций. Обычно мы имеем дело с кристаллической серой, которая состоит из восьмиатомных циклических молекул.
Рис. (3). Модель молекулы серы
Молекулы образуют кристаллы разного строения, и поэтому существуют аллотропные видоизменения: ромбическая и моноклинная сера. Обе модификации представляют собой жёлтые легкоплавкие вещества. Температуры плавления их несколько различаются ((+112,8) °С и (+119,3) °С).
Рис. (4). Сера
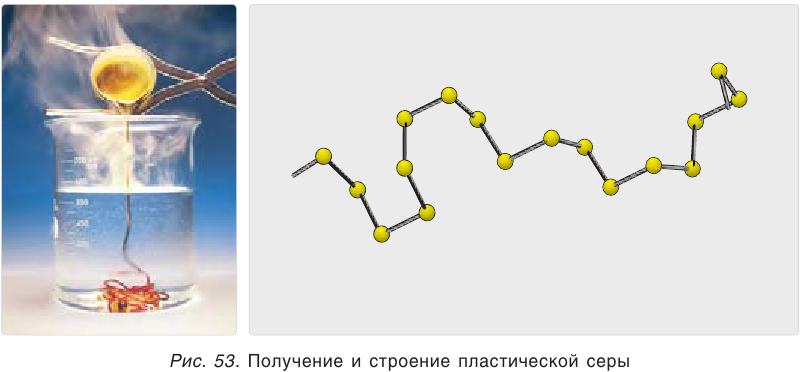
При нагревании сера плавится, превращается в лёгкую жидкость, а затем начинает темнеть и становится вязкой. Образуется пластическая сера, состоящая из длинных линейных молекул.
В воде сера не растворяется и ею не смачивается. Поэтому порошок серы не тонет вводе, несмотря на более высокую плотность ((2,07) г/см³). Такое явление называется флотацией.
Подожжённая сера реагирует с кислородом, и образуется сернистый газ. Сера в этой реакции — восстановитель.
Окислительные свойства сера проявляет в реакциях с металлами и водородом.
С активными металлами и ртутью реагирует при комнатной температуре:
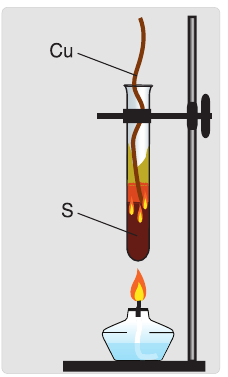
При нагревании сера вступает в реакцию с большинством металлов — железом, алюминием, цинком и другими, кроме золота и платины.
В реакциях с металлами образуются сульфиды.
При повышенной температуре сера реагирует с водородом. Образуется сероводород:
- Используется в химической промышленности для производства серной кислоты;
- находит применение в сельском хозяйстве для обеззараживания помещений;
- входит в состав некоторых мазей;
- используется в производстве спичек и бумаги;
- с её помощью каучук превращают в резину;
- входит в состав взрывчатых веществ.
Источники:
Рис. 1. Самородная сера https://image.shutterstock.com/image-photo/raw-sulphur-sulfur-ore-cutout-600w-1646293537.jpg
Рис. 2. Пирит https://www.shutterstock.com/ru/image-photo/pyrite-mineral-sulfide-group-1734246830
Рис. 3. Модель молекулы серы © ЯКласс
Рис. 4. Сера https://upload.wikimedia.org/wikipedia/commons/thumb/4/44/Sulfur-sample.jpg/1280px-Sulfur-sample.jpg
Содержание:
Сера — химический элемент и простое вещество:
Сера, так же как и кислород, является элементом VIA-группы периодической системы, она находится в третьем периоде. Рассмотрим свойства этого химического элемента и образуемых им простых веществ.
Сера в природе
Массовая доля серы в земной коре составляет около 0,05 %, она является распространенным элементом. В природе сера встречается как в виде самородной серы (рис. 49), так и в составе различных минералов и горных пород (рис. 50): сульфидов
Строение атома серы
В атоме серы 16 электронов (рис. 51), из них 6 электронов — на внешнем электронном слое:
В соединениях с металлами и водородом сера обычно проявляет степень окисления, равную –2, например 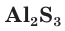
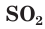
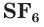
Строение и физические свойства простых веществ
Простое вещество сера существует в виде нескольких аллотропных модификаций, отличающихся составом и строением. Кристаллическая сера — твердое, легкоплавкое вещество желтого цвета. Кристаллическая сера имеет молекулярное строение — состоит из циклических молекул 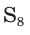
Сера в воде не растворяется и даже не смачивается ею. Если бросить в воду немного порошка серы, то частички серы не осядут на дно, а будут плавать на поверхности воды, образуя желтую пленку (рис. 54).
Химические свойства серы
Сера взаимодействует со многими простыми и сложными веществами, хотя ее реакционная способность ниже, чем у кислорода.
Сера реагирует со многими металлами, кроме золота и платины, проявляя при этом окислительные свойства, например (рис. 55):
Продуктами такого взаимодействия являются сульфиды металлов.
Реакция с серой является основой способа удаления и обезвреживания разлитой ртути, например, из разбитого термометра. Ртуть, которая попала в щели и другие труднодоступные места, засыпают порошком серы. Такой процесс называют демеркуризацией.
Окислительные свойства серы проявляются и в реакциях с некоторыми неметаллами. Сера взаимодействует с водородом при нагревании, образуя летучее соединение — сероводород
Сероводород — бесцветный газ с резким запахом тухлых яиц. Правильнее сказать, что это тухлые яйца пахнут сероводородом, так как этот газ образуется при гниении растительных и животных остатков. Сероводород ядовит. Поэтому его вдыхание может привести к тяжелому отравлению. Однако в небольших количествах сероводород оказывает целебное действие. Он содержится в водах некоторых минеральных источников.
Сера окисляется кислородом, проявляя при этом восстановительные свойства (рис. 56):
Применение серы
Больше половины добытой серы расходуется для получения серной кислоты, одного из самых важных химических продуктов. Нагреванием серы с каучуком получают резину. Как горючее вещество сера входит в состав черного пороха, спичечных головок. Широко применяется сера в сельском хозяйстве для борьбы с вредителями растений. В медицине серу используют для лечения кожных заболеваний.
Сера в соединениях с металлами и менее электроотрицательными элементами проявляет степень окисления –2, а в соединениях с более электроотрицательными элементами — +4 и +6.
Простое вещество сера существует в виде нескольких аллотропных модификаций.
Сера при взаимодействии с металлами, водородом и некоторыми неметаллами ведет себя как окислитель.
В реакции с кислородом сера является восстановителем.
Оксид серы(IV) и оксид серы(VI)
Сера образует с кислородом два оксида: оксид серы(IV), или сернистый газ, 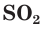
Оксид серы(IV)
Оксид серы(IV) — это бесцветный газ с характерным запахом. Графическая формула его молекулы:
Оксид серы(IV) является кислотным оксидом, проявляя все соответствующие химические свойства: взаимодействует с водой, щелочами и осно Ђвными оксидами.
При растворении оксида серы(IV) в воде образуется слабая двухосновная сернистая кислота:
В этом легко убедиться по изменению окраски лакмуса с фиолетовой на красную в водном растворе оксида серы(IV). Сернистая кислота неустойчива и существует только в растворе. Соли этой кислоты называются сульфитами.
Сернистый газ обладает бактерицидным действием. Поэтому его широко используют для обработки овощехранилищ, плодов и фруктов, чтобы предотвратить их загнивание. Сернистый газ, как и соли сернистой кислоты, применяют для отбеливания соломы, шерсти, бумаги, тканей.
В оксиде серы(IV) сера находится в промежуточной степени окисления +4. Поэтому сернистый газ может проявлять как окислительные свойства, реагируя с восстановителями:
так и восстановительные свойства, взаимодействуя с сильными окислителями:
Реакция взаимодействия сернистого газа с сероводородом — один из важных процессов, протекающих в природе. При извержении вулканов выделяются SO2 и H2S, а при их взаимодействии образуется сера в виде кристаллов. На рисунке вы видите извержение вулкана Килауэа.
Оксид серы(VI)
Оксид серы(VI) SO3 представляет собой бесцветную жидкость, которая при температуре ниже 17 °С превращается в белое твердое вещество. Графическая формула его молекулы представлена на рисунке 58.
Это типичный кислотный оксид. Он реагирует с водой с выделением теплоты, образуя серную кислоту:
Оксид серы(VI) реагирует с основными оксидами:
и щелочами:
Оксид серы(VI) применяется для промышленного получения серной кислоты.
Попадание оксидов серы в атмосферу при сжигании топлива приводит к образованию в облаках кислот и выпадению кислотных дождей. Они губительно действуют на все живое: разрушается почва, изменяется состав почвенных организмов, гибнут ценные виды рыб, исчезает растительность (см. рис.).
Оксид серы(IV) и оксид серы(VI) представляют собой типичные кислотные оксиды.
При взаимодействии с водой оксид серы(IV) и оксид серы(VI) образуют соответственно сернистую и серную кислоты.
Серная кислота
Серная кислота 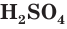
Строение молекулы серной кислоты
Модель молекулы серной кислоты представлена на рисунке 59. В молекуле 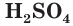
Связи 
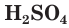
Физические свойства серной кислоты
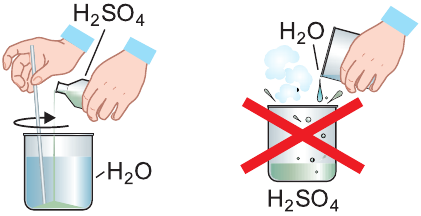
Чистая серная кислота — бесцветная маслянистая нелетучая жидкость без запаха, примерно в 2 раза тяжелее воды. Она смешивается с водой в любых соотношениях. При приготовлении водных растворов серной кислоты выделяется большое количество теплоты, происходит разогревание смеси, которое может сопровождаться ее разбрызгиванием.
Помните!
Кислоту осторожно тонкой струйкой вливают в воду при непрерывном перемешивании раствора.
Обычно водный раствор серной кислоты с массовой долей 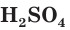
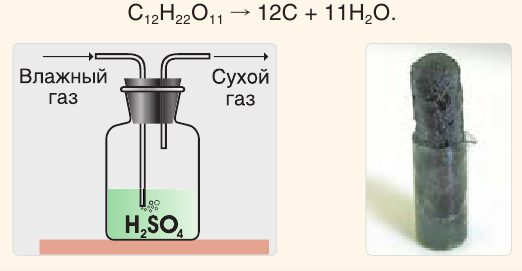
Концентрированная серная кислота используется как водоотнимающий агент, например для осушения газов (см. рис. слева).
Она способна отнимать воду и у сложных веществ, в состав которых входят водород и кислород. Так, под действием концентрированной серной кислоты сахар обугливается и реакционная масса чернеет и вспучивается (см. рис. справа):
Химические свойства серной кислоты
Разбавленная серная кислота, как и соляная, проявляет все характерные для кислот свойства. Она изменяет окраску индикаторов: лакмус и метилоранж в растворе 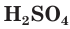
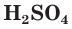
являясь окислителем за счет ионов водорода Н+ .
Разбавленная серная кислота реагирует также с оксидами металлов:
с основаниями:
с солями:
Концентрированная серная кислота по своим свойствам отличается от разбавленной. Она является более сильным окислителем за счет атомов серы, имеющих степень окисления +6. Концентрированная 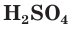
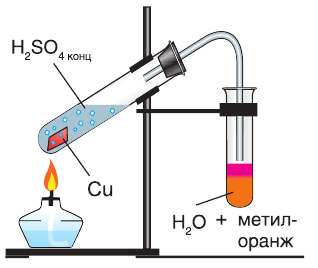
Продемонстрируем действие концентрированной серной кислоты на медь. При приливании концентрированной серной кислоты в пробирку с медью и нагревании смеси раствор окрашивается в серовато-синий цвет и наблюдается выделение газа 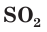
Железо, алюминий и некоторые другие металлы при обычных условиях не реагируют с концентрированной серной кислотой из-за образования защитной пленки на поверхности металла. Поэтому концентрированную серную кислоту можно хранить и перевозить в стальных цистернах (рис. 61).
Концентрированная серная кислота способна взаимодействовать с простыми веществами — неметаллами, а также со многими сложными, в том числе органическими соединениями. Серная кислота обугливает бумагу и древесину, разрушает одежду и кожу — это очень опасное вещество, способное вызывать труднозаживающие химические ожоги.
- Серная кислота — бесцветная, маслянистая жидкость. В водных растворах является сильным электролитом.
- Разбавленная серная кислота проявляет все характерные для кислот свойства: взаимодействует с металлами, стоящими в ряду активности до водорода, с выделением водорода; с оксидами металлов; с основаниями; с солями.
- При взаимодействии концентрированной серной кислоты с медью выделяется оксид серы(IV).
Сульфаты — соли серной кислоты
Серная кислота — один из главных продуктов химической промышленности. Об этом говорят и масштабы мирового производства, достигающие 200 млн т в год.
Соли серной кислоты
Как вы уже знаете из предыдущего параграфа, соли серной кислоты — сульфаты могут образовываться при ее взаимодействии с металлами, оксидами металлов, основаниями и солями.
Большинство сульфатов хорошо растворимы в воде. Растворимые сульфаты, главным образом сульфат магния, содержатся в морской воде и обуславливают ее горький вкус.
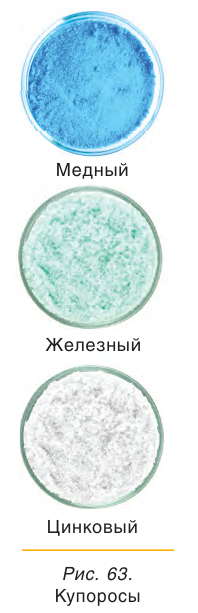
Многие сульфаты способны связывать воду, образуя кристаллогидраты. Кристаллогидраты солей серной кислоты часто называют купоросами, например: 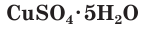
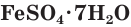

Плохо растворимы сульфаты металлов IIА-группы (кроме сульфатов бериллия и магния), меньше других растворим сульфат бария. При добавлении раствора соли бария, например хлорида бария 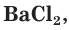
Поэтому для обнаружения серной кислоты и ее солей в водных растворах используют растворимые соли бария.
Применение серной кислоты и сульфатов
Серная кислота — один из важнейших продуктов, широко используемых в различных областях промышленности (рис. 64). Основными ее потребителями являются производства минеральных удобрений, соляной, уксусной и других кислот, моющих средств, взрывчатых веществ, красителей, лекарств. Серная кислота применяется также в металлургии, для очистки нефтепродуктов, в качестве электролита в кислотных аккумуляторах и т. д.
Соли серной кислоты используются в качестве минеральных удобрений, в строительстве, в медицине, для борьбы с вредителями растений, в производстве соды и стекла. Например, кристаллогидраты сульфата меди(II) 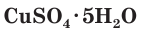
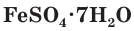
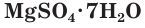
Природный гипс 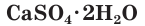
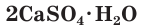
- Серная кислота — один из главных продуктов химической промышленности.
- Большинство сульфатов хорошо растворимы в воде.
- Для обнаружения серной кислоты и ее солей в водных растворах используют растворимые соли бария.
- Азот в химии
- Фосфор в химии
- Углерод в химии
- Кремний в химии
- Основания в химии
- Кислоты в химии
- Соли в химии
- Хлор в химии
|
||||
| Внешний вид простого вещества | ||||
|---|---|---|---|---|
|
|
||||
| Свойства атома | ||||
| Название, символ, номер | Сера / Sulfur (S), 16 | |||
| Атомная масса (молярная масса) |
[32,059; 32,076][комм. 1][1] а. е. м. (г/моль) | |||
| Электронная конфигурация | [Ne] 3s2 3p4 | |||
| Радиус атома | 127 пм | |||
| Химические свойства | ||||
| Ковалентный радиус | 102 пм | |||
| Радиус иона | 30 (+6e) 184 (-2e) пм | |||
| Электроотрицательность | 2,58 (шкала Полинга) | |||
| Электродный потенциал | 0 | |||
| Степени окисления | +6, +4, +2, +1, 0, -1, −2 | |||
| Энергия ионизации (первый электрон) |
999,0 (10,35) кДж/моль (эВ) | |||
| Термодинамические свойства простого вещества | ||||
| Плотность (при н. у.) | 2,070 г/см³ | |||
| Температура плавления | 386 К (112,85 °С) | |||
| Температура кипения | 717,824 К (444,67 °С) | |||
| Уд. теплота плавления | 1,23 кДж/моль | |||
| Уд. теплота испарения | 10,5 кДж/моль | |||
| Молярная теплоёмкость | 22,61[2] Дж/(K·моль) | |||
| Молярный объём | 15,5 см³/моль | |||
| Кристаллическая решётка простого вещества | ||||
| Структура решётки | орторомбическая | |||
| Параметры решётки | a=10,437 b=12,845 c=24,369 Å | |||
| Прочие характеристики | ||||
| Теплопроводность | (300 K) 0,27 Вт/(м·К) | |||
| Номер CAS | 7704-34-9 | |||
| Эмиссионный спектр | ||||
|
|
Се́ра — элемент 16-й группы (по устаревшей классификации — главной подгруппы VI группы), третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 16. Проявляет неметаллические свойства. Обозначается символом S (лат. sulfur). В водородных и кислородных соединениях находится в составе различных ионов, образует многие кислоты и соли. Многие серосодержащие соли малорастворимы в воде.
Содержание
- 1 Изотопы
- 2 История и происхождение названия
- 2.1 Происхождение названия
- 2.2 История открытия
- 3 Сера в природе
- 3.1 Природные минералы серы
- 4 Получение
- 4.1 Производители
- 4.2 Товарные формы
- 5 Применение
- 6 Свойства
- 6.1 Физические свойства
- 6.2 Фазовая диаграмма серы
- 6.3 Химические свойства
- 7 Биологическая роль
- 7.1 Биологической действие
- 8 Пожароопасные свойства серы
- 8.1 Пожары на складах серы
- 9 Юникод
- 10 См. также
- 11 Примечания
- 12 Литература
- 13 Ссылки
Изотопы
Природная Сера состоит из четырёх стабильных изотопов:
32S (95,02 %), 33S (0,75 %), 34S (4,21 %), 36S (0,02 %).
Получены также искусственные радиоактивные изотопы
31S (T½ = 2,4 сек), 35S (T½ = 87,1 сут), 37S (Т½= 5,04 мин) и другие.
История и происхождение названия
Происхождение названия
Слово «сера», известное в древнерусском языке с XV в., заимствовано из старославянского «сѣра» — «сера, смола», вообще «горючее вещество, жир».
Этимология слова не выяснена до настоящих времен, поскольку первоначальное общеславянское название вещества утрачено и слово дошло до современного русского языка в искаженном виде[3].
По предположению Фасмера[4], «сера» восходит к лат. сera — «воск» или лат. serum — «сыворотка».
Латинское sulfur (происходящее из эллинизированного написания этимологического sulpur), предположительно, восходит к индоевропейскому корню *swelp — «гореть»[5].
История открытия
Точное время открытия серы не установлено, но этот элемент использовался до нашей эры.
Сера использовалась жрецами в составе священных курений при религиозных обрядах. Она считалась произведением сверхчеловеческих существ из мира духов или подземных богов.
Очень давно сера стала применяться в составе различных горючих смесей для военных целей. Уже у Гомера описаны «сернистые испарения», смертельное действие выделений горящей серы. Сера, вероятно, входила в состав «греческого огня», наводившего ужас на противников.
Около VIII в. китайцы стали использовать её в пиротехнических смесях, в частности, в смеси типа пороха. Горючесть серы, лёгкость, с которой она соединяется с металлами с образованием сульфидов (например, на поверхности кусков металла), объясняют то, что её считали «принципом горючести» и обязательной составной частью металлических руд.
Пресвитер Теофил (XII в.) описывает способ окислительного обжига сульфидной медной руды, известный, вероятно, ещё в древнем Египте.
В период арабской алхимии возникла ртутно-серная теория состава металлов, согласно которой сера почиталась обязательной составной частью (отцом) всех металлов.
В дальнейшем она стала одним из трёх принципов алхимиков, а позднее «принцип горючести» явился основой теории флогистона. Элементарную природу серы установил Лавуазье в своих опытах по сжиганию.
С введением пороха в Европе началось развитие добычи природной серы, а также разработка способа получения её из пиритов; последний был распространён в древней Руси. Впервые в литературе он описан у Агриколы.
Сера в природе
Большие скопления самородной серы (с содержанием > 25 %) редки, они встречаются в местах вулканической активности, им сопутствуют сернистые фумаролы и сернистые воды[6].
Серная руда разрабатывается в месторождениях самородной серы, добывается из сульфидных руд и промышленных газов[7].
Серные бактерии могут окислять сероводород от гниющих органических остатков до серы и накапливать её[8].
Природные минералы серы
Сера является шестнадцатым по химической распространённости элементом в земной коре. Встречается в свободном (самородном) состоянии и в связанном виде.
Важнейшие природные минералы серы: FeS2 — железный колчедан, или пирит, ZnS — цинковая обманка, или сфалерит (вюрцит), PbS — свинцовый блеск, или галенит, HgS — киноварь, Sb2S3 — антимонит, Cu2S — халькозин, CuS — ковеллин, CuFeS2 — халькопирит. Кроме того, сера присутствует в нефти, природном угле, природных газах и сланцах. Сера — шестой элемент по содержанию в природных водах, встречается в основном в виде сульфат-иона и обусловливает «постоянную» жёсткость пресной воды. Жизненно важный элемент для высших организмов, составная часть многих белков, концентрируется в волосах.
Получение
В древности и в средние века серу добывали, вкапывая в землю большой глиняный горшок, на который ставили другой, с отверстием в дне. Последний заполняли породой, содержащей серу, и затем нагревали. Сера плавилась и стекала в нижний горшок.
В настоящее время серу получают главным образом путём выплавки самородной серы непосредственно в местах её залегания под землёй. Серные руды добывают разными способами — в зависимости от условий залегания. Залежам серы почти всегда сопутствуют скопления ядовитых газов — соединений серы. К тому же нельзя забывать о возможности её самовозгорания.
При добыче руды открытым способом экскаваторами снимают пласты пород, под которыми залегает руда. Взрывами рудный пласт дробят, после чего глыбы руды отправляют на сероплавильный завод, где из концентрата извлекают серу.
В 1890 г. Герман Фраш предложил плавить серу под землёй и через скважины, подобные нефтяным, выкачивать её на поверхность. Сравнительно невысокая (113 °C) температура плавления серы подтверждала реальность идеи Фраша. В 1890 г. начались испытания, приведшие к успеху.
Известно несколько методов получения серы из серных руд: пароводяные, фильтрационные, термические, центрифугальные и экстракционные.
Также сера в больших количествах содержится в природном газе в газообразном состоянии (в виде сероводорода, сернистого ангидрида). При добыче она откладывается на стенках труб и оборудования, выводя их из строя. Поэтому её улавливают из газа как можно быстрее после добычи. Полученная химически чистая мелкодисперсная сера является идеальным сырьём для химической и резиновой промышленности.
Серу из природного сернистого газа получают методом Клауса. Для этого используются так называемые серные ямы, где происходит дегазация серы, на выходе получают модифицированную серу — продукт, широко использующийся в производстве асфальта. Технологические установки для получения серы обычно включают в себя ямы недегазированной серы, ямы дегазации, ямы хранения дегазированной серы, а также налив жидкой серы и склад комовой серы. Стены ямы обычно делают из кирпича, дно заливают бетоном, а сверху закрывают яму алюминиевой крышей. Так как сера — это весьма агрессивная среда, ямы периодически приходится полностью реконструировать.
Крупнейшее месторождение самородной серы вулканического происхождения находится на острове Итуруп с запасами категории A+B+C1 — 4227 тыс. тонн и категории C2 — 895 тыс. тонн, что достаточно для строительства предприятия мощностью 200 тыс. тонн гранулированной серы в год.
Склад серы у химического цеха ММСК (1960-е гг.)
Производители
С 1939 по 1986 гг. крупнейшим производителем серы в СССР был Медногорский медно-серный комбинат (ММСК)[9]: в середине 1950-х гг. он выпускал до 250—280 тысяч тонн в год, что составляло 80 % серы, производившейся в стране.
«…Утром мы были на медносерном заводе. Около 80 процентов серы, выпускаемой в нашей стране, добывается на этом предприятии. „ — До пятидесятого года стране приходилось импортировать много серы из-за границы. Теперь нужда в импорте серы отпала, — говорил директор завода Александр Адольфович Бурба. — Но завод продолжает расширяться. Начали строить цех производства серной кислоты“. С высокой эстакады застывшим потоком повис ярко-жёлтый массив серы. То, что мы видим в небольших количествах в стеклянных баночках в лабораториях, здесь, на заводском дворе, лежало огромными глыбами».
— А. Софронов. В Оренбургских степях (журнал «Огонёк», 1956).
[10]
В начале XXI века основными производителями серы в России являются предприятия ОАО Газпром: ООО Газпром добыча Астрахань и ООО Газпром добыча Оренбург, получающие её как побочный продукт при очистке газа[11].
Товарные формы
В промышленности реализовано получение серы в различных товарных формах[12][стр. 193—196]. Выбор той или иной формы определяется требованиями заказчика.
Комовая сера до начала 1970-х годов была основным видом серы, выпускаемым промышленностью СССР. Её получение технологически просто и осуществляется подачей жидкой серы по обогреваемому трубопроводу на склад, где производится заливка серных блоков. Застывшие блоки высотой 1-3 метра разрушают на более мелкие куски и транспортируют заказчику. Метод, однако, имеет недостатки: невысокое качество серы, потери на пыль и крошку при рыхлении и погрузке, сложность автоматизации.
Жидкую серу хранят в обогреваемых резервуарах и транспортируют в цистернах. Транспорт жидкой серы более выгоден, чем её плавление на месте. Достоинства получения жидкой серы — отсутствие потерь и высокая чистота. Недостатки — опасность возгорания, траты на обогрев цистерн.
Формованная сера бывает чешуйчатая и пластинчатая. Чешуйчатую серу начали производить на НПЗ в 1950-х годах. Для получения используют вращающийся барабан, внутри он охлаждается водой, а снаружи кристаллизуется сера в виде чешуек толщиной 0,5-0,7 мм. В начале 1980-х вместо чешуйчатой стали выпускать пластинчатую серу. На движущуюся ленту подается расплав серы, который охлаждается по мере движения ленты. На выходе образуется застывший лист серы, который ломают с образованием пластинок. Сегодня эта технология считается устаревшей, хотя около 40 % канадской серы экспортируется именно в таком виде ввиду больших капиталовложений в установки для её получения.
Гранулированную серу получают различными методами.
- Водная грануляция (пеллетирование) разработана в 1964 году английской фирмой «Эллиот». Процесс основан на быстром охлаждении капель серы, падающих в воду. Первое внедрение технологии — процесс «Салпел» в 1965 году. Крупнейший завод позже был построен в Саудовской Аравии в 1986 году. На нём каждая из трёх установок может производить до 3500 т гранулированной серы в сутки. Недостаток технологии — ограниченное качество гранул серы, обладающих неправильной формой и повышенной хрупкостью.
- Грануляция в кипящем слое разработана французской компанией «Перломатик». Капли жидкой серы подаются вверх. Они охлаждаются водой и воздухом и смачиваются жидкой серой, которая застывает на образующихся гранулах тонким слоем. Конечный размер гранул 4-7 мм. Более прогрессивным является процесс «Прокор», который широко внедрён в Канаде. В нём применяются барабанные грануляторы. Однако этот процесс очень сложен в управлении.
- Воздушно-башенная грануляция разработана и внедрена в Финляндии в 1962 году. Расплав серы диспергируется с помощью сжатого воздуха в верхней части грануляционной башни. Капли падают и затвердевают, попадая на транспортную ленту.
Молотая сера является продуктом размола комовой серы. Степень измельчения может быть различной. Его проводят сначала в дробилке, потом в мельнице. Таким способом возможно получение очень высокодисперсной серы с размером частиц менее 2 мкм. Грануляцию порошковой серы проводят в прессах. Необходимо использование связующих добавок, в качестве которых используют битумы, стеариновую кислоту, жирные кислоты в виде водной эмульсии с триэтаноламином и другие.
Коллоидная сера — это разновидность молотой серы с размером частиц менее 20 мкм. Её применяют в сельском хозяйстве для борьбы с вредителями и в медицине как противовоспалительные и дезинфицирующие средства. Коллоидную серу получают различными способами.
- Способ получения путём размола широко распространён, поскольку не предъявляет высоких требований к сырью. Одним из лидеров по этой технологии является фирма «Байер».
- Способ получения из расплавленной серы или её паров был внедрён в США в 1925 году. Технология подразумевает смешение с бентонитом, полученная смесь образует устойчивые суспензии с водой. Однако содержание серы в растворе невелико (не более 25 %).
- Экстракционные способы получения основаны на растворении серы в органических растворителях и дальнейшем испарении последних. Однако они не получили широкого распространения.
Высокочистую серу получают используя химические, дистилляционные и кристаллизационные методы. Её применяют в электронной технике, при изготовлении оптических приборов, люминофоров, в производстве фармацевтических и косметических препаратов — лосьонов, мазей, средств против кожных болезней.
Применение
Примерно половина производимой серы используется в производстве серной кислоты.
Серу применяют для вулканизации каучука, как фунгицид в сельском хозяйстве и как сера коллоидная — лекарственный препарат. Также сера в составе серобитумных композиций применяется для получения сероасфальта, а в качестве заместителя портландцемента — для получения серобетона. Сера находит применение для производства пиротехнических составов, ранее использовалась в производстве пороха, применяется для производства спичек.
Свойства
Физические свойства
Природный сросток кристаллов самородной серы
Сера существенно отличается от кислорода способностью образовывать устойчивые цепочки и циклы из атомов. Наиболее стабильны циклические молекулы S8, имеющие форму короны, образующие ромбическую и моноклинную серу. Это кристаллическая сера — хрупкое вещество жёлтого цвета. Кроме того, возможны молекулы с замкнутыми (S4, S6) цепями и открытыми цепями. Такой состав имеет пластическая сера, вещество коричневого цвета, которая получается при резком охлаждении расплава серы (пластическая сера уже через несколько часов становится хрупкой, приобретает жёлтый цвет и постепенно превращается в ромбическую). Формулу серы чаще всего записывают просто S, так как она, хотя и имеет молекулярную структуру, является смесью простых веществ с разными молекулами. В воде сера нерастворима, но хорошо растворяется в органических растворителях, например, в сероуглероде, скипидаре.
Плавление серы сопровождается заметным увеличением объёма (примерно 15 %). Расплавленная сера представляет собой жёлтую легкоподвижную жидкость, которая выше 160 °C превращается в очень вязкую тёмно-коричневую массу. Наибольшую вязкость расплав серы приобретает при температуре 190 °C; дальнейшее повышение температуры сопровождается уменьшением вязкости и выше 300 °C расплавленная сера снова становится подвижной. Это связано с тем, что при нагревании серы она постепенно полимеризуется, увеличивая длину цепочки с повышением температуры. При нагревании серы свыше 190 °C полимерные звенья начинают рушиться.
Сера может служить простейшим примером электрета. При трении сера приобретает сильный отрицательный заряд[13].
Фазовая диаграмма серы
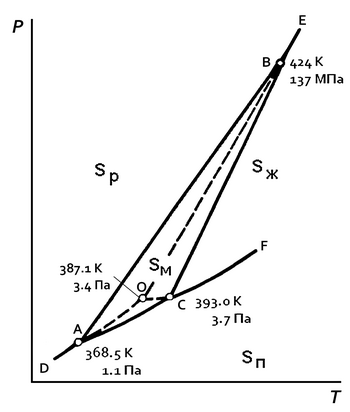
Фазовая диаграмма элементарной серы.
Sp — ромбическая сера; Sм — моноклинная сера; Sж — жидкая сера; Sп — пары серы.
Элементарная кристаллическая сера может существовать в виде двух аллотропных модификаций (энантиотропия серы) — ромбической и моноклинной, — то есть сера диморфна, поэтому для элементарной серы возможно существование четырёх фаз: твёрдой ромбической, твёрдой моноклинной, жидкой и газообразной, а на фазовой диаграмме серы (см. рисунок; для давления использован логарифмический масштаб) имеются два поля твёрдых фаз: область ромбической серы и область существования моноклинной серы (треугольник АВС)[14].
На фазовой диаграмме серы[14]:
- DA — линия возгонки ромбической серы Sp, описывающая зависимость давления насыщенного пара серы Sп от температуры над твёрдой ромбической серой;
- AС — линия возгонки моноклинной серы Sм, описывающая зависимость давления насыщенного пара серы от температуры над твёрдой моноклинной серой;
- СF — линия испарения жидкой серы Sж, описывающая зависимость давления насыщенного пара серы от температуры над расплавом серы;
- AB — линия полиморфного превращения сера ромбическая <—> сера моноклинная, описывающая зависимость температуры фазового перехода между ромбической и моноклинной серой от давления;
- ВЕ — линия плавления ромбической серы, описывающая зависимость температуры плавления ромбической серы от давления;
- ВЕ — линия плавления моноклинной серы, описывающая зависимость температуры плавления моноклинной серы от давления.
Пунктирные линии отражают возможность существования метастабильных фаз, которые наблюдаются при резком изменении температуры:
- AО — линия сублимации перегретой ромбической серы;
- ВО — линия плавления перегретой ромбической серы;
- СО — линия испарения переохлаждённой жидкой серы;
На фазовой диаграмме серы имеются три стабильные тройные точки и одна метастабильная, каждая из которых отвечает условиям термодинамического равновесия трёх фаз[14]:
- точка А (дополнительная): равновесие твёрдой ромбической, твёрдой моноклинной и газообразной серы;
- точка В (дополнительная): равновесие твёрдой ромбической, твёрдой моноклинной и жидкой серы;
- точка С (основная): равновесие твёрдой моноклинной, расплавленной и газообразной серы;
- точка О (метастабильная): метастабильное равновесие между перегретой твёрдой ромбической, переохлаждённой жидкой и газообразной серой.
Как показывает фазовая диаграмма, ромбическая сера не может одновременно находиться в равновесии с расплавом и парами серы[15], поэтому в основной тройной точке (когда равновесные фазы находятся в разных агрегатных состояниях) твёрдая фаза представлена моноклинной серой. Метастабильная тройная точка появляется вследствие низкой скорости превращения одной кристаллической модификации серы в другую[16].
Химические свойства
На воздухе сера горит, образуя сернистый газ — бесцветный газ с резким запахом:
С помощью спектрального анализа установлено, что на самом деле процесс окисления серы в двуокись представляет собой цепную реакцию и происходит с образованием ряда промежуточных продуктов: моноокиси серы S2O2, молекулярной серы S2, свободных атомов серы S и свободных радикалов моноокиси серы SO[17].
Восстановительные свойства серы проявляются в реакциях серы и с другими неметаллами, однако при комнатной температуре сера реагирует только со фтором:
Расплав серы реагирует с хлором, при этом возможно образование двух низших хлоридов (дихлорид серы и дитиодихлорид)[18]:
При избытке серы также образуются разнообразные дихлориды полисеры типа SnCl2.[19]
При нагревании сера также реагирует с фосфором, образуя смесь сульфидов фосфора[20], среди которых — высший сульфид P2S5:
Кроме того, при нагревании сера реагирует с водородом, углеродом, кремнием:
(сероводород)
(сероуглерод)
(сульфид кремния)
При нагревании сера взаимодействует со многими металлами, часто — весьма бурно. Иногда смесь металла с серой загорается при поджигании. При этом взаимодействии образуются сульфиды:
.
Растворы сульфидов щелочных металлов реагируют с серой с образованием полисульфидов:
Из сложных веществ следует отметить прежде всего реакцию серы с расплавленной щёлочью, в которой сера диспропорционирует аналогично хлору:
.
Полученный сплав называется серной печенью.
С концентрированными кислотами-окислителями (HNO3, H2SO4) сера реагирует только при длительном нагревании:
(конц.)
(конц.)
При увеличении температуры в парах серы происходят изменения в количественном молекулярном составе[21]. Число атомов в молекуле уменьшается:
При 800—1400 °C пары состоят в основном из двухатомной серы:
А при 1700 °C сера становится атомарной:
Биологическая роль
Сера — один из биогенных элементов. Сера входит в состав некоторых аминокислот (цистеин, метионин), витаминов (биотин, тиамин), ферментов.
Сера участвует в образовании третичной структуры белка (формирование дисульфидных мостиков).
Также сера участвует в бактериальном фотосинтезе (сера входит в состав бактериохлорофилла, а сероводород является источником водорода). Окислительно-восстановительные реакции серы — источник энергии в хемосинтезе[22].
В человеке содержится примерно 2 г серы на 1 кг веса.
Самородная сера на почтовой марке, 2009
Биологической действие
Чистая сера не ядовита, все же летучие серосодержащие соединения ядовиты (сернистый газ, серный ангидрид, сероводород и др.).
Пожароопасные свойства серы
Тонкоизмельчённая сера склонна к химическому самовозгоранию в присутствии влаги, при контакте с окислителями, а также в смеси с углём, жирами, маслами. Сера образует взрывчатые смеси с нитратами, хлоратами и перхлоратами.
Самовозгорается при контакте с хлорной известью.
Средства тушения: распылённая вода, воздушно-механическая пена[23].
По данным В. Маршалла пыль серы относится к разряду взрывоопасных, но для взрыва необходима достаточно высокая концентрация пыли — порядка 20 г/м³ (20 000 мг/м³), такая концентрация во много раз превышает предельно допустимую концентрацию для человека в воздухе рабочей зоны — 6 мг/м³[24].
Пары образуют с воздухом взрывчатую смесь[25].
Горение серы
Горение серы протекает только в расплавленном состоянии аналогично горению жидкостей. Верхний слой горящей серы кипит, создавая пары, которые образуют слабо светящееся голубое пламя высотой до 5 см[26]. Температура пламени при горении серы составляет 1820 °C[27].
Так как воздух по объёму состоит приблизительно из 21 % кислорода и 79 % азота и при горении серы из одного объёма кислорода получается один объём SO2, то максимальное теоретически возможное содержание SO2 в газовой смеси составляет 21 %. На практике горение происходит с некоторым избытком воздуха, и объёмное содержание SO2 в газовой смеси меньше теоретически возможного, составляя обычно 14-15 %[17].
Обнаружение горения
Обнаружение горения серы пожарной автоматикой является трудной проблемой. Пламя сложно обнаружить человеческим глазом или видеокамерой, спектр голубого пламени лежит в основном в ультрафиолетовом диапазоне. Тепловыделение при пожаре приводит к температуре ниже, чем при пожарах других распространённых пожароопасных веществ. Для обнаружения горения тепловым извещателем необходимо размещать его непосредственно близко к сере. Пламя серы не излучает в инфракрасном диапазоне. Таким образом оно не будет обнаружено распространёнными инфракрасными извещателями. Ими будут обнаруживаться лишь вторичные возгорания. Пламя серы не выделяет паров воды. Таким образом детекторы ультрафиолетовых извещателей пламени, использующие соединения никеля, не будут работать.
Для эффективного обнаружения пламени рекомендуется использовать ультрафиолетовые извещатели с детекторами на основе молибдена. Они имеют спектральный диапазон чувствительности 1850…2650 ангстрем, который подходит для обнаружения горения серы[28].
Пожарная безопасность
Для выполнения требований пожарной безопасности на складах серы необходимо:
- конструкции и технологическое оборудование должны регулярно очищаться от пыли;
- помещение склада должно постоянно проветриваться естественной вентиляцией при открытых дверях;
- дробление комков серы на решётке бункера должно производиться деревянными кувалдами или инструментом из неискрящего материала;
- конвейеры для подачи серы в производственные помещения должны быть снабжены металлоискателями;
- в местах хранения и применения серы необходимо предусматривать устройства (бортики, пороги с пандусом и т. п.), обеспечивающие в аварийной ситуации предотвращение растекания расплава серы за пределы помещения или открытой площадки;
- на складе серы запрещается:
- производство всех видов работ с применением открытого огня;
- складировать и хранить промасленную ветошь и тряпки;
- при ремонте применять инструмент из искродающего материала[29].
Пожары на складах серы
В декабре 1995 года на открытом складе серы предприятия, расположенного в городе Сомерсет-Уэст Западно-Капской провинции Южно-Африканской Республики, произошёл крупный пожар, погибли два человека[30][31].
16 января 2006 г. около пяти вечера на череповецком предприятии «Аммофос» загорелся склад с серой. Общая площадь пожара — около 250 квадратных метров. Полностью ликвидировать его удалось лишь в начале второго ночи. Жертв и пострадавших нет[32].
15 марта 2007 года рано утром на ООО «Балаковский завод волоконных материалов» произошёл пожар на закрытом складе серы. Площадь пожара составила 20 кв.м. На пожаре работало 4 пожарных расчёта с личным составом в 13 человек. Примерно через полчаса пожар был ликвидирован. Никто не пострадал[33].
4 и 9 марта 2008 года произошло возгорание серы в Атырауской области в хранилище серы ТШО на Тенгизском месторождении. В первом случае очаг возгорания удалось потушить быстро, во втором случае сера горела 4 часа. Объём горевших отходов нефтепереработки, к каковым по казахстанским законам отнесена сера, составил более 9 тысяч килограммов[34].
В апреле 2008 недалеко от посёлка Кряж Самарской области загорелся склад, на котором хранилось 70 тонн серы. Пожару была присвоена вторая категория сложности. К месту происшествия выехали 11 пожарных расчётов и спасатели. В тот момент, когда пожарные оказались около склада, горела ещё не вся сера, а только её небольшая часть — около 300 килограммов. Площадь возгорания вместе с участками сухой травы, прилегающими к складу, составила 80 квадратных метров. Пожарным удалось быстро сбить пламя и локализовать пожар: очаги возгорания были засыпаны землёй и залиты водой[35].
В июле 2009 в Днепродзержинске горела сера. Пожар произошёл на одном из коксохимических предприятий в Баглейском районе города. Огонь охватил более восьми тонн серы. Никто из сотрудников комбината не пострадал[36].
В конце июля 2012 под Уфой в поселке Тимашево загорелся склад с серой площадью 3200 квадратных метров. На место выехало 13 единиц техники, в тушении пожара задействован 31 пожарный. Произошло загрязнение атмосферного воздуха продуктами горения. Погибших и пострадавших нет[37].
Юникод
В Юникоде есть алхимический символ серы.
| Графема | Unicode | HTML | ||
|---|---|---|---|---|
| Код | Название | Шестнадцатеричное | Десятичное | Мнемоника |
S, химический элемент VI группы периодической системы Менделеева; атомный номер 16, атомная масса 32,06. Природная С. состоит из четырёх стабильных изотопов: 32S (95,02%), 33S (0,75%), 34S (4,21%), 36S (0,02%). Получены также искусственные радиоактивные изотопы 31S (T1/2 = 2,4 сек), 35S (T1/2 = 87,1 cym), 37S (T1/2 = 5,04 мин).
Историческая справка. С. в самородном состоянии, а также в виде сернистых соединений известна с древнейших времён. Она упоминается в Библии, поэмах Гомера и др. С. входила в состав «священных» курений при религиозных обрядах; считалось, что запах горящей С. отгоняет злых духов. С. давно стала необходимым компонентом зажигательных смесей для военных целей, например «греческого огня» (10 в. н. э.). Около 8 в. в Китае стали использовать С. в пиротехнических целях. Издавна С. и её соединениями лечили кожные заболевания. В период арабской алхимии возникла гипотеза, согласно которой С. (начало горючести) и ртуть (начало металличности) считали составными частями всех металлов. Элементарную природу С. установил А. Л. Лавуазье и включил её в список неметаллических простых тел (1789). В 1822 Э. Мичерлих обнаружил аллотропию С.
Распространение в природе. С. относится к весьма распространённым химическим элементам (кларк 4,7·10-2); встречается в свободном состоянии (Сера самородная) и в виде соединений — сульфидов, полисульфидов, сульфатов (см. Сульфиды природные, Сульфаты природные, Сульфидные руды). Вода морей и океанов содержит сульфаты натрия, магния, кальция. Известно более 200 минералов С., образующихся при эндогенных процессах. В биосфере образуется свыше 150 минералов С. (преимущественно сульфатов); широко распространены процессы окисления сульфидов до сульфатов, которые в свою очередь восстанавливаются до вторичного H2S и сульфидов. Эти реакции происходят при участии микроорганизмов. Многие процессы биосферы приводят к концентрации С. — она накапливается в гумусе почв, углях, нефти, морях и океанах (8,9·10-2%), подземных водах, в озёрах и солончаках. В глинах и сланцах С. в 6 раз больше, чем в земной коре в целом, в гипсе — в 200 раз, в подземных сульфатных водах — в десятки раз. В биосфере происходит круговорот С.: она приносится на материки с атмосферными осадками и возвращается в океан со стоком. Источником С. в геологическом прошлом Земли служили главным образом продукты извержения вулканов, содержащие SO2 и H2S. Хозяйственная деятельность человека ускорила миграцию С.; интенсифицировалось окисление сульфидов.
Физические и химические свойства. С. — твёрдое кристаллическое вещество, устойчивое в виде двух аллотропических модификаций. Ромбическая α-S лимонно-жёлтого цвета, плотность 2,07 г/см3, tпл 112,8 °С, устойчива ниже 95,6°С; моноклинная β-S медово-жёлтого цвета, плотность 1,96 г/см3, tпл 119,3 °С, устойчива между 95,6 °С и температурой плавления. Обе эти формы образованы восьмичленными циклическими молекулами S8 с энергией связи S — S 225,7 кдж/моль.
При плавлении С. превращается в подвижную жёлтую жидкость, которая выше 160 °С буреет, а около 190 °С становится вязкой тёмно-коричневой массой. Выше 190°С вязкость уменьшается, а при 300 °С С. вновь становится жидкотекучей. Это обусловлено изменением строения молекул: при 160 °С кольца S8 начинают разрываться, переходя в открытые цепи; дальнейшее нагревание выше 190 °С уменьшает среднюю длину таких цепей.
Если расплавленную С., нагретую до 250—300 °С, влить тонкой струей в холодную воду, то получается коричнево-жёлтая упругая масса (пластическая С.). Она лишь частично растворяется в сероуглероде, в осадке остаётся рыхлый порошок. Растворимая в CS2 модификация называется λ-S, а нерастворимая — μ-S. При комнатной температуре обе эти модификации превращаются в устойчивую хрупкую α-S. tkип С. 444,6 °С (одна из стандартных точек международной температурной шкалы). В парах при температуре кипения, кроме молекул S8, существуют также S6, S4 и S2. При дальнейшем нагревании крупные молекулы распадаются, и при 900°С остаются лишь S2, которые приблизительно при 1500°С заметно диссоциируют на атомы. При замораживании жидким азотом сильно нагретых паров С. получается устойчивая ниже — 80°С пурпурная модификация, образованная молекулами S2.
С. — плохой проводник тепла и электричества. В воде она практически нерастворима, хорошо растворяется в безводном аммиаке, сероуглероде и в ряде органических растворителей (фенол, бензол, дихлорэтан и др.).
Конфигурация внешних электронов атома S 3s23p 4. В соединениях С. проявляет степени окисления -2, +4, +6.
С. химически активна и особенно легко при нагревании соединяется почти со всеми элементами, за исключением N2, I2, Au, Pt и инертных газов. СO2 на воздухе выше 300 °С образует окислы: SO2 — Сернистый ангидрид и SO3 — Серный ангидрид, из которых получают соответственно сернистую кислоту (См. Сернистая кислота) и серную кислоту (См. Серная кислота), а также их соли Сульфиты и Сульфаты (см. также Тиокислоты и Тиосульфаты). Уже на холоду S энергично соединяется с F2, при нагревании реагирует с Cl2 (см. Серы фториды, Серы хлориды); с бромом С. образует только S2Br2, иодиды серы неустойчивы. При нагревании (150 — 200 °С) наступает обратимая реакция с H2 с получением сернистого водорода (См. Сернистый водород). С. образует также многосернистые водороды общей формулы H2Sx, т. н. сульфаны. Известны многочисленные Сераорганические соединения.
При нагревании С. взаимодействует с металлами, образуя соответствующие сернистые соединения (сульфиды) и многосернистые металлы (полисульфиды). При температуре 800—900 °С пары С. реагируют с углеродом, образуя Сероуглерод CS2. Соединения С. с азотом (N4S4 и N2S5) могут быть получены только косвенным путём.
Получение. Элементарную С. получают из серы самородной, а также окислением сернистого водорода и восстановлением сернистого ангидрида. О способах добычи С. см. Серные руды. Источник сернистого водорода для производства С. — коксовые, природные газы, газы крекинга нефти. Разработаны многочисленные методы переработки H2S; наибольшее значение имеют следующие: 1) H2S извлекают из газов раствором моногидротиоарсената натрия:
Na2HAsS2 + H2S = Na2HAsS3O + H2O.
Затем продувкой воздуха через раствор осаждают С. в свободном виде:
NaHAsS3O + 1/2 O2 = Na2HAsS2O2 + S.
2) H2S выделяют из газов в концентрированном виде. Затем его основная масса окисляется кислородом воздуха до С. и частично до SO2. После охлаждения H2S и образовавшиеся газы (SO2, N2, CO2) поступают в два последовательных конвертора, где в присутствии катализатора (активированный боксит или специально изготовляемый алюмогель) происходит реакция:
2H2S + SO2 = 3S + 2H2O.
В основе получения С. из SO2 лежит реакция восстановления его углём или природными углеводородными газами. Иногда это производство сочетается с переработкой пиритных руд.
В 1972 элементарной С. в мире (без социалистических стран) произведено 32,0 млн. т; основная масса её добывалась из природных самородных руд. В 70-е гг. 20 в. первостепенное значение (в связи с открытием крупных месторождений сероводородсодержащих топливных газов) приобретают методы получения С. из H2S.
Сорта С. Выплавленная непосредственно из серных руд С. называется природной комовой; полученная из H2S и SO2 — газовой комовой. Природная комовая С., очищенная перегонкой, называется рафинированной. Сконденсированная из паров при температуре выше точки плавления в жидком состоянии и затем разлитая в формы — черенковой С. При конденсации С. ниже точки плавления на стенках конденсационных камер образуется мелкий порошок С. — серный цвет. Особо высокодисперсная С. носит название коллоидной.
Применение. С. применяется в первую очередь для получения серной кислоты: в бумажной промышленности (для получения сульфитцеллюлозы); в сельском хозяйстве (для борьбы с болезнями растений, главным образом винограда и хлопчатника); в резиновой промышленности (вулканизующий агент); в производстве красителей и светящихся составов; для получения чёрного (охотничьего) пороха; в производстве спичек.
И. К. Малина.
В медицинской практике применение С. основано на её способности при взаимодействии с органическими веществами организма образовывать сульфиды и пентатионовую кислоту, от присутствия которых зависят кератолитические (растворяющие — от греч. kéras — рог и lytikós — растворяющий), противомикробные и противопаразитарные эффекты. С. входит в состав Вилькинсона мази (См. Вилькинсона мазь) и других препаратов, применяемых для лечения чесотки. Очищенную и осажденную С. употребляют в мазях и присыпках для лечения некоторых кожных заболеваний (себорея, псориаз и др.); в порошке — при глистных инвазиях (энтеробиоз); в растворах — для пиротерапии (См. Пиротерапия) прогрессивного паралича и др.
Сера в организме. В виде органических и неорганических соединений С. постоянно присутствует во всех живых организмах и является важным биогенным элементом (См. Биогенные элементы). Её среднее содержание в расчёте на сухое вещество составляет: в морских растениях около 1,2%, наземных — 0,3%, в морских животных 0,5—2%, наземных — 0,5%. Биологическая роль С. определяется тем, что она входит в состав широко распространённых в живой природе соединений: аминокислот (Метионин, Цистеин), и следовательно белков и пептидов; коферментов (кофермент (См. Коферменты) А, Липоевая кислота), витаминов (Биотин, Тиамин), Глутатиона и другие Сульфгидрильные группы (— SH) остатков цистеина играют важную роль в структуре и каталитическая активности многих ферментов. Образуя дисульфидные связи (— S — S —) внутри отдельных полипептидных цепей и между ними, эти группы участвуют в поддержании пространственной структуры молекул белков. У животных С. обнаружена также в виде органических сульфатов и сульфокислот — хондроитинсерной кислоты (См. Хондроитинсерные кислоты) (в хрящах и костях), таурохолиевой кислоты (в жёлчи), Гепарина, Таурина. В некоторых железосодержащих белках (например, ферродоксинах) С. обнаружена в форме кислотолабильного сульфида. С. способна к образованию богатых энергией связей в макроэргических соединениях (См. Макроэргические соединения).
Неорганические соединения С. в организмах высших животных обнаружены в небольших количествах, главным образом в виде сульфатов (в крови, моче), а также роданидов (в слюне, желудочном соке, молоке, моче). Морские организмы богаче неорганическими соединениями С., чем пресноводные и наземные. Для растений и многих микроорганизмов сульфат (SO42-) наряду с фосфатом и нитратом служит важнейшим источником минерального питания. Перед включением в органические соединения С. претерпевает изменения в валентности и превращается затем в органическую форму в своём наименее окисленном состоянии; т. о. С. широко участвует в окислительно-восстановительных реакциях в клетках. В клетках сульфаты, взаимодействуя с аденозинтрифосфатом (АТФ), превращаются в активную форму — аденилилсульфат:
Катализирующий эту реакцию фермент — сульфурилаза (АТФ: сульфат — адснилилтрансфераза) широко распространён в природе. В такой активированной форме сульфонильная группа подвергается дальнейшим превращениям — переносится на др. акцептор или восстанавливается.
Животные усваивают С. в составе органических соединений. Автотрофные организмы получают всю С., содержащуюся в клетках, из неорганических соединений, главным образом в виде сульфатов. Способностью к автотрофному усвоению С. обладают высшие растения, многие водоросли, грибы и бактерии. (Из культуры бактерий был выделен специальный белок, осуществляющий перенос сульфата через клеточную мембрану из среды в клетку.) Большую роль в круговороте С. в природе играют микроорганизмы — Десульфурирующие бактерии и Серобактерии. Многие разрабатываемые месторождения С. — биогенного происхождения. С. входит в состав антибиотиков (Пенициллины, Цефалоспорины); её соединения используются в качестве радиозащитных средств (См. Радиозащитные средства), средств защиты растений.
Л. И. Беленький.
Лит.: Справочник сернокислотчика, под ред. К. М. Малина, 2 изд., М., 1971; Природная сера, под ред. М. А. Менковского, М., 1972; Некрасов Б. В., Основы обшей химии, 3 изд., т. 1, М., 1973; Реми Г., Курс неорганической химии, пер. с нем., т. 1, М., 1972; Янг Л., Моу Д ж., Метаболизм соединений серы, пер. с англ., М., 1961; Горизонты биохимии, пер. с англ., М., 1964; Биохимия растений, пер. с англ., М., 1968, гл. 19; Торчинский Ю. М., Сульфгидрильные и дисульфидные группы белков, М., 1971; Дегли С., Никольсон Д., Метаболические пути, пер. с англ., М., 1973.
Большая советская энциклопедия. — М.: Советская энциклопедия.
1969—1978.
| Сера / Sulphur (S) | |
|---|---|
| Атомный номер | 16 |
| Внешний вид простого вещества | светло-желтое хрупкое твердое вещество, в чистом виде без запаха |
| Свойства атома | |
| Атомная масса (молярная масса) |
32,066 а. е. м. (г/моль) |
| Радиус атома | 127 пм |
| Энергия ионизации (первый электрон) |
999,0 (10,35) кДж/моль (эВ) |
| Электронная конфигурация | [Ne] 3s2 3p4 |
| Химические свойства | |
| Ковалентный радиус | 102 пм |
| Радиус иона | 30 (+6e) 184 (-2e) пм |
| Электроотрицательность (по Полингу) |
2,58 |
| Электродный потенциал | 0 |
| Степени окисления | 6, 4, 2, -2 |
| Термодинамические свойства простого вещества | |
| Плотность | 2,070 г/см³ |
| Удельная теплоёмкость | 0,732 Дж/(K·моль) |
| Теплопроводность | 0,27 Вт/(м·K) |
| Температура плавления | 386 K |
| Теплота плавления | 1,23 кДж/моль |
| Температура кипения | 717,824 K |
| Теплота испарения | 10,5 кДж/моль |
| Молярный объём | 15,5 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | орторомбическая |
| Период решётки | 10,470 Å |
| Отношение c/a | n/a |
| Температура Дебая | n/a K |
Се́ра (Sulphur — обозн.»S» в таблице Менделеева) — высокоэлектроотрицательный элемент, проявляет неметаллические свойства. В водородных и кислородных соединениях находится в составе различных ионов, образует многие кислоты и соли. Многие серосодержащие соли малорастворимы в воде.
Природные минералы серы
Файл:Electron shell 016 Sulfur.svg Схема атома серы
Сера является шестнадцатым по химической распространенности элементом в земной коре. Встречается в свободном (самородном) состоянии и связанном виде.
Важнейшие природное соединение серы FeS2 — железный колчедан, пирит, ZnS — цинковая обманка, PbS — свинцовый блеск, HgS — киноварь, нефть, природного угля. Сера — шестой элемент по содержанию в природных водах, встречается в основном в виде сульфат-иона и обуславливает «постоянную» жесткость пресной воды. Жизненно важный элемент для высших организмов, составная часть многих белков, концентрируется в волосах.
История открытия и происхождение названия
Сера (англ. Sulfur, франц. Sufre, нем. Schwefel) в самородном состоянии, а также в виде сернистых соединений известна с самых древнейших времен. С запахом горящей серы, удушающим действием сернистого газа и отвратительным запахом сероводорода человек познакомился, вероятно, еще в доисторические времена. Именно из-за этих свойств сера использовалась жрецами в составе священных курений при религиозных обрядах. Сера считалась произведением сверхчеловеческих существ из мира духов или подземных богов. Очень давно сера стала применяться в составе различных горючих смесей для военных целей. Уже у Гомера описаны «сернистые испарения», смертельное действие выделений горящей серы. Сера, вероятно, входила в состав «греческого огня», наводившего ужас на противников. Около VIII в. китайцы стали использовать ее в пиротехнических смесях, в частности, в смеси типа пороха. Горючесть серы, легкость, с которой она соединяется с металлами с образованием сульфидов (например, на поверхности кусков металла), объясняют то, что ее считали «принципом горючести» и обязательной составной частью металлических руд. Пресвитер Теофил (XI в.) описывает способ окислительного обжига сульфидной медной руды, известный, вероятно, еще в древнем Египте. В период арабской алхимии возникла ртутно-серная теория состава металлов, согласно которой сера почиталась обязательной составной частью (отцом) всех металлов. В дальнейшем она стала одним из трех принципов алхимиков, а позднее «принцип горючести» явился основой теории флогистона. Элементарную природу серы установил Лавуазье в своих опытах по сжиганию. С введением пороха в Европе началось развитие добычи природной серы, а также разработка способа получения ее из пиритов; последний был распространен в древней Руси. Впервые в литературе он описан у Агриколы. Таким образом точно происхождение серы не установлено, но как сказано выше этот элемент использовался до Рождества Христова, а значит знаком людям с давних времен.
Происхождение названия
Происхождение латинского sulfur неизвестно. Русское название элемента обычно производят от санскритского «сира» — светло-желтый. Возможно родство «серы» с древнееврейским «серафим»[источник?] — мн. числом от «сераф» — букв. сгорающий, а сера хорошо горит. В древнерусском и старославянском «сера» — вообще горючее вещество, в том числе и жир.
Происхождение серы
Большие скопления самородной серы встречаются не так уж часто. Чаще она присутствует в некоторых рудах. Руда самородной серы — это порода с вкраплениями чистой серы.
Когда образовались эти вкрапления — одновременно с сопутствующими породами или позже? От ответа на этот вопрос зависит направление поисковых и разведочных работ. Но, несмотря на тысячелетия общения с серой, человечество до сих пор не имеет однозначного ответа. Существует несколько теорий, авторы которых придерживаются противоположных взглядов.
Теория сингенеза (т. е. одновременного образования серы и вмещающих пород) предполагает, что образование самородной серы происходило в мелководных бассейнах. Особые бактерии восстанавливали сульфаты, растворенные в воде, до сероводорода, который поднимался вверх, попадал в окислительную зону и здесь химическим путем или при участии других бактерий окислялся до элементарной серы. Сера осаждалась на дно, и впоследствии содержащий серу ил образовал руду.
Теория эпигенеза (вкрапления серы образовались позднее, чем основные породы) имеет несколько вариантов. Самый распространенный из них предполагает, что подземные воды, проникая сквозь толщи пород, обогащаются сульфатами. Если такие воды соприкасаются с месторождениями нефти или природного газа, то ионы сульфатов восстанавливаются углеводородами до сероводорода. Сероводород поднимается к поверхности и, окисляясь, выделяет чистую серу в пустотах и трещинах пород.
В последние десятилетия находит все новые подтверждения одна из разновидностей теории эпигенеза — теория метасоматоза (в переводе с греческого «метасоматоз» означает замещение). Согласно ей в недрах постоянно происходит превращение гипса CaSO4-H2O и ангидрита CaSО4 в серу и кальцит СаСО3. Эта теория создана в 1935 году советскими учеными Л. М. Миропольским и Б. П. Кротовым. В ее пользу говорит, в частности, такой факт.
В 1961 году в Ираке было открыто месторождение Мишрак. Сера здесь заключена в карбонатных породах, которые образуют свод, поддерживаемый уходящими вглубь опорами (в геологии их называют крыльями). Крылья эти состоят в основном из ангидрита и гипса. Такая же картина наблюдалась на отечественном месторождении Шор-Су.
Геологическое своеобразие этих месторождений можно объяснить только с позиций теории метасоматоза: первичные гипсы и ангидриты превратились во вторичные карбонатные руды с вкраплениями самородной серы. Важно не только соседство минералов — среднее содержание серы в руде этих месторождений равно содержанию химически связанной серы в ангидрите. А исследования изотопного состава серы и углерода в руде этих месторождений дали сторонникам теории метасоматоза дополнительные аргументы.
Но есть одно «но»: химизм процесса превращения гипса в серу и кальцит пока не ясен, и потому нет оснований считать теорию метасоматоза единственно правильной. На земле и сейчас существуют озера (в частности, Серное озеро близ Серноводска), где происходит сингенетическое отложение серы и сероносный ил не содержит ни гипса, ни ангидрита.
Все это означает, что разнообразие теорий и гипотез о происхождении самородной серы — результат не только и не столько неполноты наших знаний, сколько сложности явлений, происходящих в недрах. Еще из элементарной школьной математики все мы знаем, что к одному результату могут привести разные пути. Этот закон распространяется и на геохимию.
Получение
Серу получают главным образом выплавкой самородной серы непосредственно в местах её залегания под землей. Серные руды добывают разными способами — в зависимости от условий залегания. Залежам серы почти всегда сопутствуют скопления ядовитых газов — соединений серы. К тому же нельзя забывать о возможности ее самовозгорания.
Добыча руды открытым способом происходит так. Шагающие экскаваторы снимают пласты пород, под которыми залегает руда. Взрывами рудный пласт дробят, после чего глыбы руды отправляют на сероплавильный завод, где из концентрата извлекают серу.
В 1890 г. Герман Фраш, предложил плавить серу под землей и через скважины, подобные нефтяным, выкачивать ее на поверхность. Сравнительно невысокая (меньше 120°C) температура плавления серы подтверждала реальность идеи Фраша. В 1890 г. начались испытания, приведшие к успеху.
Известно несколько методов получения серы из серных руд: пароводяные, фильтрационные, термические, центрифугальные и экстракционные.
Также сера в больших количествах содержится в природном газе в газообразном состоянии (в виде сероводорода, сернистого ангидрида). При добыче она откладывается на стенках труб и оборудования, выводя их из строя. Поэтому её улавливают из газа как можно быстрее после добычи. Полученная химически чистая мелкодисперсная серая является идеальным сырьём для химической и резиновой промышленности.
Крупнейшее месторождение самородной серы вулканического происхождения находится на острове Итуруп с запасами категории A+B+C1 — 4227 тыс. тонн и категории C2 — 895 тыс. тонн, что достаточно для строительства предприятия мощностью 200 тыс. тонн гранулированной серы в год.
Производители
Основными производителями серы в России являются предприятия ОАО Газпром: ООО Газпром добыча Астрахань и ООО Газпром добыча Оренбург, получающие ее как побочный продукт при очистке газа.
Физические свойства
Файл:Sulfur.jpg Природный сросток кристаллов самородной серы
Сера существенно отличается от кислорода способностью образовывать устойчивые гомоцепи. Наиболее стабильны циклические молекулы S8, имеющие форму короны, образующие ромбическую и моноклинную серу. Это кристаллическая сера — хрупкое вещество желтого цвета. Кроме того, возможны молекулы с замкнутыми (S4, S6) цепями и открытыми цепями. Такой состав имеет пластическая сера, вещество коричневого цвета. Формулу пластической серы чаще всего записывают просто S, так как она имеет атомарную структуру, а не молекулярную. В воде сера нерастворима, некоторые её модификации растворяются в органических растворителях, например сероуглероде.
Серу применяют для производства серной кислоты, вулканизации каучука, как фунгицид в сельском хозяйстве и как коллоидная сера — лекарственный препарат. Также сера в составе серобитумных композиций применяется для получения сероасфальта, а в качестве заместителя портландцемента — для получения серобетона.
Химические свойства
Файл:Sera gorit.jpg Горение серы
При комнатной температуре сера реагирует со фтором, хлором и концентрированными кислотами-окислителями (HNO3, H2SO4), проявляя восстановительные свойства:
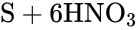
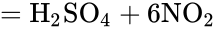
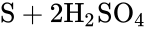
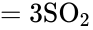
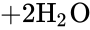
На воздухе сера горит, образуя сернистый ангидрид — бесцветный газ с резким запахом:
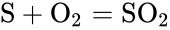
При взаимодействии с металлами образует сульфиды.
2Na+S=Na2S
При нагревании сера реагирует с углеродом, кремнием, фосфором, водородом:
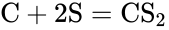
Сера при нагревании растворяется в щелочах — реакция диспропорционирования
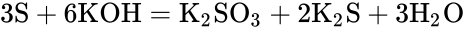
См. также
- Категория:Соединения серы
- Акарициды
Ссылки
| Сера на Викискладе? |
В Викисловаре есть статья «сера»
- Сера на Webelements
- Сера в Популярной библиотеке химических элементов
- Сера самородная на Каталоге Минералов
Эта страница использует содержимое раздела Википедии на русском языке. Оригинальная статья находится по адресу: Сера. Список первоначальных авторов статьи можно посмотреть в истории правок. Эта статья так же, как и статья, размещённая в Википедии, доступна на условиях CC-BY-SA .
Сера — элемент VIa группы 3 периода периодической таблицы Д.И. Менделеева. Относится к
группе халькогенов — элементов VIa группы.
Сера — S — простое вещество имеет светло-желтый цвет. Использовалась еще до нашей эры в составе священных курений при
религиозных обрядах.

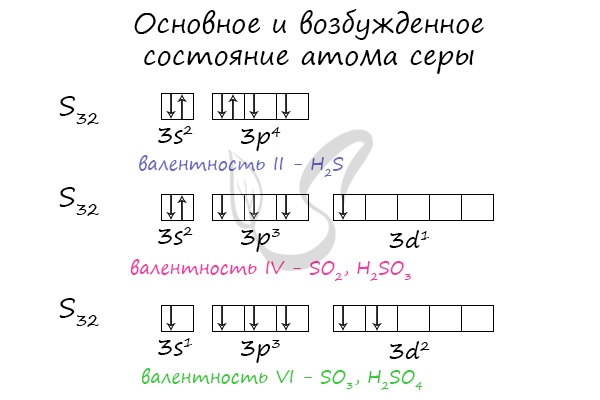
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных
электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
- FeS2 — пирит, колчедан
- ZnS — цинковая обманка
- PbS — свинцовый блеск (галенит), Sb2S3 — сурьмяный блеск, Bi2S3 — висмутовый блеск
- HgS — киноварь
- CuFeS2 — халькопирит
- Cu2S — халькозин
- CuS — ковеллин
- BaSO4 — барит, тяжелый шпат
- CaSO4 — гипс
В местах вулканической активности встречаются залежи самородной серы.

Получение
В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S,
SO2.
H2S + O2 = S + H2O (недостаток кислорода)
SO2 + C = (t) S + CO2
Серу можно получить разложением пирита
FeS2 = (t) FeS + S
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
H2S + H2SO4 = S + H2O (здесь может также выделяться SO2)
Химические свойства
- Реакции с неметаллами
- Реакции с металлами
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
На воздухе сера окисляется, образуя сернистый газ — SO2. Реагирует со многими неметаллами, без нагревания —
только со фтором.
S + O2 = (t) SO2
S + F2 = SF6
S + Cl2 = (t) SCl2
S + C = (t) CS2

При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
K + S = (t) K2S
Al + S = (t) Al2S3
Fe + S = (t) FeS
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
S + H2SO4 = (t) SO2 + H2O
S + HNO3 = (t) H2SO4 + NO2 + H2O
Сера вступает в реакции диспропорционирования с щелочами.
S + KOH = (t) K2S + K2SO3 + H2O
Сера вступает в реакции с солями. Например, в кипящем водном растворе сера может реагировать с сульфитами с образованием тиосульфатов.
Na2SO3 + S → (t) Na2S2O3
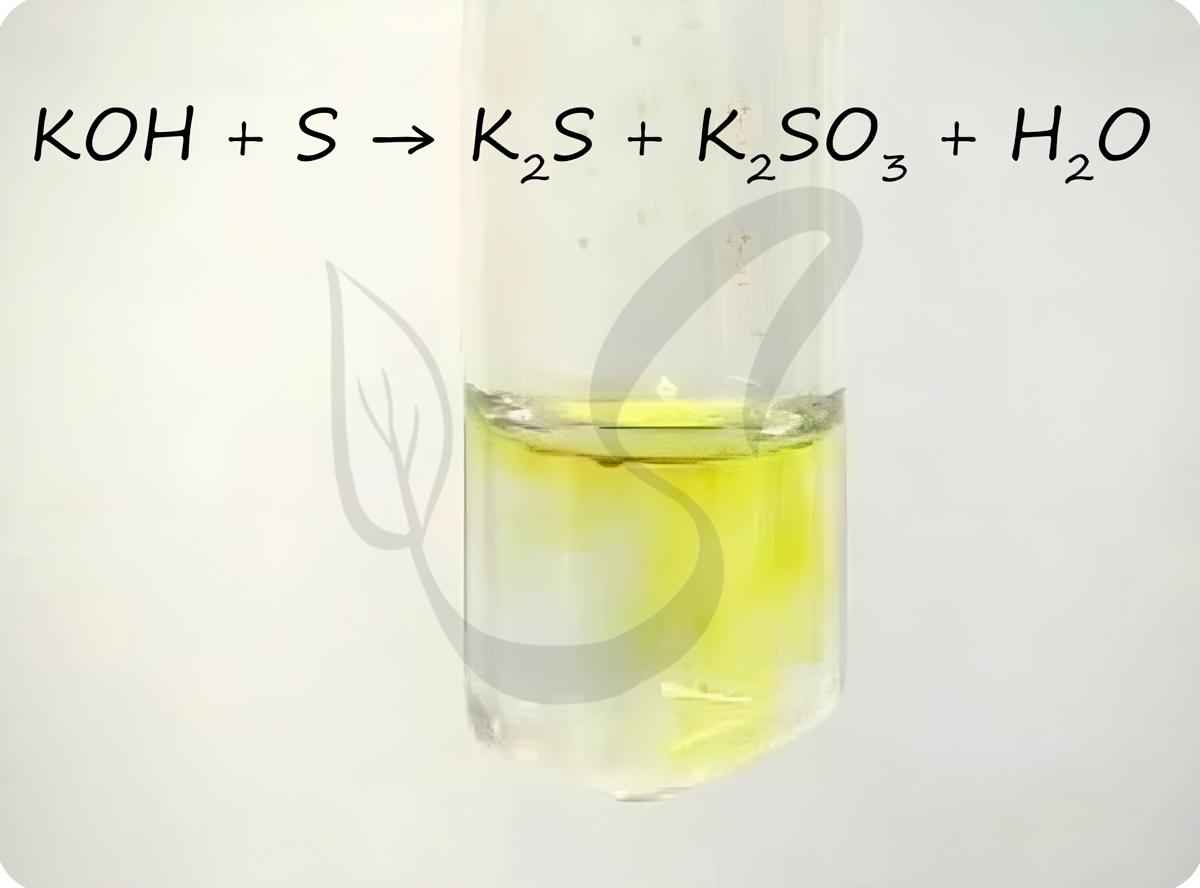
Сероводород — H2S
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные
ванны).

Получение
Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.
Al2S3 + H2O = (t) Al(OH)3↓ + H2S↑
FeS + HCl = FeCl2 + H2S↑

Химические свойства
- Кислотные свойства
- Восстановительные свойства
- Качественная реакция
Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит
от соотношения основания и кислоты).
MgO + H2S = (t) MgS + H2O
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
2KOH + H2S = K2S + 2H2O
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Ca + H2S = (t) CaS + H2
Сероводород — сильный восстановитель (сера в минимальной степени окисления S2-). Горит в кислороде синим пламенем, реагирует с кислотами.
H2S + O2 = H2O + S (недостаток кислорода)
H2S + O2 = H2O + SO2 (избыток кислорода)
H2S + HClO3 = H2SO4 + HCl

Качественной реакцией на сероводород является реакция с солями свинца, в ходе которой образуется сульфид свинца.
H2S + Pb(NO3)2 = PbS↓ + HNO3
Оксид серы — SO2
Сернистый газ — SO2 — при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся
спички).

Получение
В промышленных условиях сернистый газ получают обжигом пирита.
FeS2 + O2 = (t) FeO + SO2
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота,
распадающаяся на сернистый газ и воду.
K2SO3 + H2SO4 = (t) K2SO4 + H2O + SO2↑
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
Cu + H2SO4(конц.) = (t) CuSO4 + SO2 + H2O
- Кислотные свойства
- Восстановительные свойства
- Как окислитель
С основными оксидами, основаниями образует соли сернистой кислоты — сульфиты.
K2O + SO2 = K2SO3
NaOH + SO2 = NaHSO3
2NaOH + SO2 = Na2SO3 + H2O

Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
Fe2(SO4)3 + SO2 + H2O = FeSO4 + H2SO4
SO2 + O2 = (t, кат. — Pt) SO3
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
CO + SO2 = CO2 + S
H2S + SO2 = S + H2O
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Получение
SO2 + H2O ⇄ H2SO3
Химические свойства
- Диссоциация
- Кислотные свойства
- Окислительные свойства
- Восстановительные свойства
Диссоциирует в водном растворе ступенчато.
H2SO3 = H+ + HSO3—
HSO3— = H+ + SO32-
В реакциях с основными оксидами, основаниями образует соли — сульфиты и гидросульфиты.
CaO + H2SO3 = CaSO3 + H2O
H2SO3 + 2KOH = 2H2O + K2SO3 (соотношение кислота — основание, 1:2)
H2SO3 + KOH = H2O + KHSO3 (соотношение кислота — основание, 1:1)
С сильными восстановителями сернистая кислота принимает роль окислителя.
H2SO3 + H2S = S↓ + H 2O
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.
H2SO3 + Br2 = H2SO4 + HBr

Оксид серы VI — SO3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
Получение
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора
(оксид ванадия — Pr, V2O5).
SO2 + O2 = (кат) SO3
В лабораторных условиях разложением солей серной кислоты — сульфатов.
Fe2(SO4)3 = (t) SO3 + Fe2O3
Химические свойства
- Кислотные свойства
- Окислительные свойства
Является кислотным оксидом, соответствует серной кислоте. При реакции с основными оксидами и основаниями образует ее соли — сульфаты и
гидросульфаты. Реагирует с водой с образованием серной кислоты.
SO3 + 2KOH = K2SO4 + 2H2O (основание в избытке — средняя соль)
SO3 + KOH = KHSO4 + H2O (кислотный оксид в избытке — кислая соль)
SO3 + Ca(OH)2 = CaSO4 + H2O

SO3 + Li2O = Li2SO4
SO3 + H2O = H2SO4
SO3 — сильный окислитель. Чаще всего восстанавливается до SO2.
SO3 + P = SO2 + P2O5
SO3 + H2S = SO2 + H2O
SO3 + KI = SO2 + I2 + K2SO4

© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.