Как правильно пишется слово «инфаркт»
инфа́ркт
инфа́ркт, -а
Источник: Орфографический
академический ресурс «Академос» Института русского языка им. В.В. Виноградова РАН (словарная база
2020)
Делаем Карту слов лучше вместе
Привет! Меня зовут Лампобот, я компьютерная программа, которая помогает делать
Карту слов. Я отлично
умею считать, но пока плохо понимаю, как устроен ваш мир. Помоги мне разобраться!
Спасибо! Я стал чуточку лучше понимать мир эмоций.
Вопрос: увал — это что-то нейтральное, положительное или отрицательное?
Ассоциации к слову «инфаркт»
Синонимы к слову «инфаркт»
Предложения со словом «инфаркт»
- Именно в это время у людей случаются инфаркты и инсульты, именно в это время останавливается сердце во сне.
- – Фух… Так можно получить инфаркт! – он в изнеможении опустился на камень.
- – Это не намёк, истинная правда. Вы меня до инфаркта доведёте своими признаниями. С ним тоже приключилась странная история.
- (все предложения)
Каким бывает «инфаркт»
Значение слова «инфаркт»
-
ИНФА́РКТ, -а, м. Очаг омертвения в тканях органов вследствие прекращения тока крови в артериях при их спазме или закупорке. Инфаркт сердечной мышцы. (Малый академический словарь, МАС)
Все значения слова ИНФАРКТ
Отправить комментарий
Дополнительно
Версия: Справочник заболеваний MedElement
Категории МКБ:
Острый инфаркт миокарда неуточненный (I21.9)
Разделы медицины:
Кардиология
Общая информация
Краткое описание
Инфаркт миокарда (ИМ) — это острое заболевание, вызванное развитием очага
ишемическогонекроза
мышцы сердца, возникшего вследствие закупорки коронарной артерии тромбом. В дальнейшем развивается острое несоответствие между потребностью миокарда в кислороде и доставкой его по коронарной артерии (абсолютная или относительная недостаточность коронарного кровотока).
Критерии острого инфаркта миокарда
Термин ИМ используется, когда присутствуют признаки
некроза
миокарда, согласующиеся в клинической картине с ишемией миокарда. При таких условиях диагнозу ИМ соответствует любой из нижеперечисленных критериев:
1. Выявление подъема и/или падения уровня сердечных биохимических маркеров (преимущественно тропонина), а также при наличии признаков ишемии миокарда одновременно с одним из следующих признаков:
— симптомы ишемии;
— визуализация признаков новой потери жизнеспособности миокарда или новой региональной аномалии движения стенки;
— изменения ЭКГ, указывающие на новую ишемию (новые ST-T изменения или новая блокада левой ножки пучка Гиса (БЛНПГ));
— развитие патологических зубцов Q на ЭКГ.
2. Внезапная сердечная смерть (ВСС), включающая остановку сердца. Часто она имеет симптомы, предполагающие ишемию миокарда, и сопровождается, вероятно, новым подъемом ST или вновь возникшей БЛНПГ, и/или со свидетельством наличия свежего тромба на
коронарографии
и/или
аутопсии
. Однако смерть наступает еще до того, как становится возможным получить образцы крови или в то время, когда сердечные биохимические маркеры еще не появились в крови.
3. Для аортокоронарного шунтирования (АКШ) у пациентов с нормальным уровнем тропонина подъем сердечных маркеров служит указателем на перипроцедурный некроз миокарда. Признаками ИМ вследствие АКШ являются:
— подъем уровней биохимических маркеров больше, чем в пять раз по отношению к норме;
— патологические зубцы Q либо БЛНПГ;
— ангиографически задокументированная
окклюзия
венечной артерии или шунта;
— визуализация признаков потери жизнеспособности миокарда.
4. При выполнении чрескожных вмешательств на коронарных артериях (ЧВКА) у больных с исходно нормальным уровнем тропонина, повышение концентрации специфических маркеров повреждения миокарда указывает на развитие
некроза
миокарда в ходе выполнения вмешательства. При увеличении концентрации биомаркеров более чем в 3 раза по сравнению с нормой принято диагностировать ИМ, связанный с выполнением ЧВКА. Выделяют также ИМ, обусловленный подтвержденным тромбозом
стента
.
5. Патоморфологические находки, которые свидетельствуют о наличии острого ИМ.
Критерии для постановки диагноза «первичный инфаркт миокарда»
Любой из приведенных ниже критериев соответствует диагнозу первичного ИМ:
— визуализация свидетельств о регионе потери жизнеспособности миокарда, то есть истончение стенки и утеря способности к сокращению, при отсутствии неишемических причин;
— развитие новых патологических зубцов Q с симптомами или без них;
— наличие вылеченного или лечащегося ИМ.
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Клиническая классификация различных типов инфаркта миокарда
| Тип 1 | Спонтанный инфаркт миокарда, связанный с ишемией вследствие первичного коронарного события, такого как эрозия и/или разрыв, трещина или расслоение бляшки. |
| Тип 2 | Инфаркт миокарда, вторичный по отношению к ишемии, возникшей либо из-за повышения потребности в кислороде, либо из-за снижения его доставки, например, из-за спазма коронарной артерии, коронарной эмболии, анемии, гипертонии или гипотонии. |
| Тип 3 | Внезапная сердечная смерть, включая остановку сердца, часто с симптомами, заставляющими предположить наличие ишемии миокарда, сопровождающимися новыми подъемами сегмента ST, или новой блокады левой ножки пучка Гиса, или признаками свежего тромба в коронарной артерии по данным ангиографии и/или аутопсии. Смерть наступает или до взятия проб крови, или до появления сердечных биомаркеров в крови. |
| Тип 4а | Инфаркт миокарда, связанный (ассоциируемый) с чрескожным коронарным вмешательством (ЧКВ). |
| Тип 4b | Инфаркт миокарда, связанный с тромбозом стента, что документировано ангиографией или аутопсией. |
| Тип 5 | Инфаркт миокарда, связанный с операцией аорто-коронарного шунтирования. |
В зависимости от размеров очагового поражения сердечной мышцы, выделяют два вида инфаркта миокарда:
— мелкоочаговый;
— крупноочаговый.
Около 20% клинических случаев приходится на долю мелкоочаговых инфарктов миокарда, однако часто мелкие очаги некроза в сердечной мышце трансформируются в крупноочаговый инфаркт миокарда (у 30% пациентов).
При мелкоочаговых инфарктах, в отличие от крупноочаговых, не возникают
аневризма
и разрыв сердца. Также течение мелкоочаговых инфарктов реже осложняется сердечной недостаточностью,
тромбоэмболией
,
фибрилляцией желудочков
.
В соответствии с глубиной некротического поражения сердечной мышцы различают следующие виды инфаркта миокарда:
— трансмуральный — с некрозом всей толщи мышечной стенки сердца (чаще крупноочаговый);
— интрамуральный – с некрозом в толще миокарда;
— субэндокардиальный – с некрозом миокарда в зоне прилегания к эндокарду;
— субэпикардиальный — с некрозом миокарда в зоне прилегания к эпикарду.
Согласно изменениям, фиксируемым на ЭКГ, выделяют:
— «Q-инфаркт» — с формированием патологического зубца Q, иногда желудочкового комплекса QS (чаще — крупноочаговый трансмуральный инфаркт миокарда);
— «не Q-инфаркт» – не сопровождается появлением зубца Q, проявляется отрицательными Т-зубцами (чаще — мелкоочаговый инфаркт миокарда).
По топографии и в зависимости от поражения определенных ветвей коронарных артерий, инфаркт миокарда бывает:
— правожелудочковый;
— левожелудочковый: передней, боковой и задней стенок, межжелудочковой перегородки.
По кратности возникновения инфаркт миокарда подразделяется на:
— первичный;
— рецидивирующий (развивается в срок до 8 недель после первичного);
— повторный (развивается спустя 8 недель после предыдущего).
По развитию осложнений инфаркт миокарда может быть:
— осложненный;
— неосложненный.
По наличию и локализации болевого синдрома различают следующие формы инфаркта миокарда:
— типичная – с локализацией боли за грудиной или в
прекордиальной области
;
— атипичная — с атипичными болевыми проявлениями:
а) периферические: леволопаточная, леворучная, гортанно-глоточная, нижнечелюстная, верхнепозвоночная, гастралгическая (абдоминальная);
б) безболевые: коллаптоидная, астматическая, отечная, аритмическая, церебральная;
— малосимптомная (стертая);
— комбинированная.
В соответствии с периодом и динамикой развития инфаркта миокарда выделяют:
— стадию ишемии (острейший период);
— стадию некроза (острый период);
— стадию организации (подострый период);
— стадию рубцевания (постинфарктный период).
Этиология и патогенез
Непосредственной причиной развития инфаркта миокарда (ИМ) является остро наступающее несоответствие коронарного кровообращения запросам миокарда вследствие окклюзии коронарной артерии или резкого уменьшения притока крови по ней с последующей ишемией и некрозом.
Инфаркт миокарда с патологическими зубцами Q (тромботическая окклюзия коронарной артерии) развивается у 80% больных с инфарктом миокарда и приводит к трансмуральному некрозу миокарда и появлению зубца Q на ЭКГ.
Инфаркт миокарда без патологических зубцов Q наиболее часто возникает при спонтанном восстановлении
перфузии
или хорошо развитых
коллатералях
. Размер инфаркта в этом случае меньше, функция левого желудочка страдает меньше, больничная летальность ниже. Однако частота повторных инфарктов миокарда выше, чем при инфаркте миокарда с патологическими зубцами Q, вследствие того, что такие инфаркты миокарда — «незавершенные» (то есть миокард, оставшийся жизнеспособным, снабжается пораженной коронарной артерией); к концу первого года летальность уравнивается. Поэтому при инфаркте миокарда без патологических зубцов Q следует придерживаться более активной лечебно-диагностической тактики.
В основе развития ИМ лежат три патофизиологических механизма:
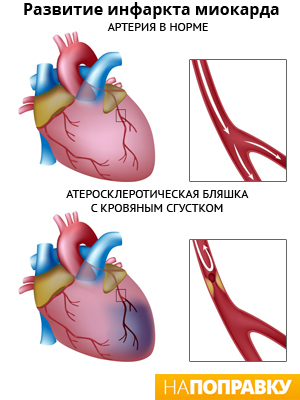
1. Разрыв атеросклеротической бляшки, спровоцированный внезапным повышением активности симпатической нервной системы (резкое повышение артериального давления, частоты и силы сердечных сокращений, усиление венечного кровообращения).
2. Тромбоз на месте разорванной или даже
интактной
бляшки в результате повышения тромбогенной способности крови (за счет усиления
агрегации
тромбоцитов, активации коагулянтной системы и/или ингибирования
фибринолиза
).
3.
Вазоконстрикция
: локальная (участка коронарной артерии, где находится бляшка) или генерализованная (всей коронарной артерии).
Первый этап развития острого инфаркта миокарда (ОИМ), хотя и не всегда обязательный — разрыв атеросклеротической бляшки, который в дальнейшем может иметь различное течение:
1. Благоприятное течение — когда после разрыва бляшки происходит кровоизлияние в бляшку, так называемый «внутреннеинтимальный» тромб, что не вызывает развития инфаркта миокарда, но в дальнейшем может способствовать прогрессированию клинической картины ишемической болезни сердца (ИБС).
2. Неблагоприятное течение — с формированием тромба, который полностью или практически полностью перекрывает просвет венечной артерии.
Выделяют три стадии формирования тромба,
обтурирующего
коронарную артерию:
1. Кровоизлияние в бляшку.
2. Формирование внутрисосудистого неокклюзирующего тромба.
3. Распространение тромба до полной закупорки сосуда.
Внутреннеинтимальный тромб состоит в основном из тромбоцитов. Формирование тромба является ключевым в развитии ОИМ.
Гораздо реже ОИМ возникает не как результат атеротромбоза. Ведущим патогенетическим механизмом в этом случае рассматривается
вазоспазм
.
Инфаркт миокарда как результат
коронароспазма
достаточно часто наблюдается у людей, принимающих наркотики, так называемый «кокаиновый» инфаркт миокарда.
Значительно реже инфаркт миокарда развивается в результате других причин.
Морфологические особенности
Инфаркт — заболевание всегда острое и стадийное. При инфаркте миокарда отмечают, что в первые сутки зона инфаркта внешне никак не отличается от здоровых участков миокарда. Зона инфаркта в это время носит мозаичный характер, то есть среди погибших клеток встречаются также частично или даже полностью работоспособные миоциты. На вторые сутки зона постепенно отграничивается от здоровой ткани и между ними формируется периинфарктная зона.
Часто в периинфарктной зоне различают зону очаговой дистрофии, граничащую с некротической зоной, и зону обратимой ишемии, примыкающую к участкам неповрежденного миокарда.
Все структурные и функциональные изменения в зоне очаговой дистрофии в большинстве случаев подлежат восстановлению (частично или даже полностью).
В зоне обратимой ишемии изменения бывают полностью обратимы. После отграничения зоны инфаркта наступает постепенное размягчение и растворение погибших миоцитов, элементов соединительной ткани, участков сосудов, нервных окончаний.
При крупноочаговом инфаркте миокарда примерно на 10-е сутки на периферии очага некроза уже образуется молодая грануляционная ткань, из которой в дальнейшем формируется соединительная ткань, выполняющая рубец. Заместительные процессы идут от периферии к центру, поэтому в центре очага какое-то время могут еще оставаться очаги размягчения, а это участок, который способен растягиваться, формируя аневризму сердца или даже разрываться при грубом несоблюдении двигательного режима или других нарушениях. В месте некроза плотная рубцовая ткань окончательно формируется не ранее чем через 3-4 месяца.
При мелкоочаговом инфаркте миокарда рубец иногда образуется в более ранние сроки. На скорость рубцевания влияют не только размеры очага некроза, но и состояние коронарного кровообращения в миокарде, в особенности в периинфарктных участках. Помимо этого, имеют значение следующие факторы:
— возраст больного;
— уровень АД;
— двигательный режим;
— состояние обменных процессов;
— обеспеченность пациента полноценными аминокислотами, витаминами;
— адекватность проводимого лечения;
— наличие сопутствующих заболеваний.
Все это определяет интенсивность восстановительных процессов в организме в целом и в миокарде в частности.
Даже относительно небольшая нагрузка в период формирования первичного рубца может привести к развитию аневризмы сердца (выпячиванию стенки желудочка, формированию своеобразного мешка), тогда как уже через месяц такая же нагрузка оказывается полезной и даже необходимой для укрепления сердечной мышцы и формирования более прочного рубца.
Эпидемиология
Признак распространенности: Очень распространено
Сегодня в развитых странах число пациентов с коронарной патологией постоянно растет, причем происходит сдвиг в сторону более молодого возраста, что делает проблему диагностики, лечения и профилактики ишемической болезни социально значимой.
Заболеваемость среди мужчин гораздо выше, чем среди женщин: в среднем 500 на 100 000 мужчин и 100 на 100 000 женщин, в возрасте старше 70 лет эта разница нивелируется.
Возрастной пик заболеваемости инфарктом миокарда — 50-70 лет.
У мужчин пик заболеваемости приходится на зимнее время, у женщин — на осень, снижение заболеваемости у мужчин и женщин происходит одновременно в летний период времени.
Самыми опасным временем суток у мужчин считаются предутренние часы (4-8 часов утра), когда частота развития ИМ достигает 23,9%; у женщин аналогичный показатель составляет 25,9% в утренние часы (8-12 часов). Такая частота развития ИМ в зависимости от сезонности и времени суток совпадает с аналогичными показателями «внезапной смерти».
Внезапная смерть обычно происходит в утренние часы при подъеме больного с постели, что вероятнее всего связано с повышением активности симпатической нервной системы при пробуждении. Это вызывает увеличение вязкости крови и агрегационную активность тромбоцитов с выбросом
вазоактивных
биологических веществ, за чем следует спазм сосудов и тромбообразование, с развитием ишемического инсульта или острого инфаркта миокарда (ОИМ).
Примерно одна треть всех случаев ОИМ (а у более молодых больных еще чаще) завершается летальным исходом на догоспитальном этапе, в большинстве случаев уже через 1 час после появления острых симптомов. Среди пациентов с ОИМ, доживших до поступления в больницу, в результате проведенной современной терапии отмечаются меньшая летальность и более продолжительная выживаемость.
Смерть больных ОИМ в первые 4 часа связана с появлением аритмий и развитием
фибрилляции желудочков
(аритмогенная смерть), а в более поздние сроки — с нарастанием острой сердечной недостаточности (кардиогенный шок).
Факторы и группы риска
Факторы риска развития инфаркта миокарда (ИМ) совпадают с таковыми при ишемической болезни сердца (ИБС).
Немодифицируемые факторы риска:
1. Наследственность. Считается отягощенной по ИБС, если у близких родственников (родители, братья, сестры, дедушки, бабушки) были случаи ИБС по мужской линии до 55 лет, по женской до 65 лет.
2. Возраст. В разных популяциях выявлена прямая зависимость между возрастом человека и частотой возникновения ИБС — чем старше человек, тем выше заболеваемость ИБС.
3. Пол. Мужчины гораздо чаще болеют ИБС. У женщин до 50-55 лет (возраст наступления стойкой менопаузы) ИБС диагностируется крайне редко. Исключение составляют женщины с ранней менопаузой и различными гормональными нарушениями при отягчающих обстоятельствах:
артериальная гипертония
,
гиперлипидемия
, сахарный диабет. После наступления менопаузы частота возникновения ИБС у женщин начинает неуклонно расти, и после 70-75 лет вероятность развития ИБС у мужчин и женщин одинакова.
Модифицируемые факторы риска:
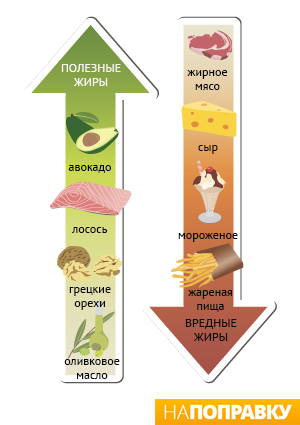
1. Неправильное питание. Употребление пищи, богатой насыщенными жирами животного происхождения, с высоким содержанием поваренной соли и низким содержанием пищевой клетчатки.
2. Артериальная гипертония. Значение повышенного артериального давления, как одного из факторов риска, доказано многочисленными исследованиями во всем мире.
3.
Гиперхолестеринемия
. Повышенное содержание в крови общего холестерина, холестерина липопротеидов низкой плотности. Холестерин липопротеидов высокой плотности рассматривается как фактор антириска — чем выше его уровень, тем меньше риск возникновения ИБС.
4. Слабая физическая активность или отсутствие регулярных физических нагрузок. У людей, ведущих малоподвижный образ жизни, вероятность возникновения ИБС в 1,5-2,4 выше, чем у физически активных.
5. Ожирение. Особенно опасно ожирение по абдоминальному типу, когда жир откладывается в области живота.
6. Табакокурение. Прямая связь курения с развитием и прогрессированием атеросклероза хорошо известна и не нуждается в комментариях.
7. Сахарный диабет. Относительный риск смерти даже у лиц с нарушением толерантности к глюкозе выше на 30%, а у больных сахарным диабетом 2 типа — на 80%.
8. Злоупотребление алкоголем. Однако фактором антириска является употребление до 30 г чистого алкоголя в сутки для мужчин и 20 г — для женщин.
9. Во всем мире сейчас уделяется внимание изучению таких факторов риска, как хронический психоэмоциональный стресс, повышенная частота сердечных сокращений, нарушение системы свертываемости, гомоцистеинемия (повышение уровня в крови
гомоцистеина
).
Ученые также установили зависимость риска развития инфаркта миокарда в зависимости от психо-эмоционального типа человека. Так, холерики имеют в 2 раза больше шансов получить первый инфаркт и в 5 раз больше — повторный, а смертность от инфаркта у них встречается в 6 раз чаще.
Провоцирующими моментами для развития острого инфаркта миокарда (ОИМ) являются интенсивное физическое или психоэмоциональное напряжение. На протяжении часа после значительного физического напряжения риск развития ОИМ возрастает в 6 раз, причем у лиц, ведущих малоподвижный образ жизни, — в 10,7 раза, а у лиц, занимающихся интенсивными физическими упражнениями, — в 2,4 раза. Подобным эффектом обладают и сильные переживания. В течение 2 часов после психоэмоционального перенапряжения риск развития ОИМ возрастает в 2,3 раза.
Частота развития ОИМ возрастает в утренние часы, в течение первого часа после пробуждения. Это касается и частоты развития внезапной смерти, инсульта, транзиторной ишемии миокарда, по данным Холтеровского наблюдения. Повышение риска связывают с увеличением в это время артериального давления и
ЧСС
, усилением
агрегационных
свойств тромбоцитов и снижением
фибринолитической
активности плазмы крови, повышением уровня
катехоламинов
,
АКТГ
,
кортизола
.
Похолодание и изменение атмосферного давления также способствуют повышению риска развития ОИМ. Так, при снижении температуры на 10°С, по сравнению со среднегодовой для данного времени года, риск развития первого ИМ возрастает на 13%, а повторного — на 38%. Изменения атмосферного давления, как в одну, так и в другую сторону, сопровождаются учащением развития ИМ на 11-12%, а повторного — на 30%.
Клиническая картина
Cимптомы, течение
Фазы острого инфаркта миокарда (ОИМ):
1. Продромальный период (длится до 30 суток, может отсутствовать).
2. Острейший период (продолжается до 2 часов от начала
ангинозного статуса
).
3. Острый период (длится до 10 дней от начала инфаркта миокарда).
4. Подострый период (начинается с 10 дня и продолжается до 1-2 месяцев).
5. Период рубцевания (в среднем длится от 2-3 месяцев до полугода, иногда завершается лишь спустя 2-3 года).
В зависимости от стадии болезни ее проявления сильно варьируют.
Продромальный период
В этот период у пациентов развиваются признаки
нестабильной стенокардии
:
— учащаются боли в груди;
— боли появляются при меньших физических нагрузках, а то и вовсе в покое;
— боли хуже снимаются нитратами, требуется большая доза нитратов, чтобы боль прошла.
Острый коронарный синдром (ОКС) объединяет такие заболевания, как нестабильная стенокардия, острый инфаркт миокарда и внезапная сердечная смерть. В основе всех этих состояний, несмотря на разные их проявления, лежит один механизм. Как при инфаркте, так и при
нестабильной стенокардии
нарушается целостность одной из холестериновых бляшек в коронарной артерии. Организм реагирует на образовавшийся дефект, отправляя в очаг тромбоциты и активируя свертывающую систему крови. Как следствие, образуется тромб, перекрывающий ток крови. Кратковременное или неполное перекрытие просвета сосуда вызывает развитие симптомов
нестабильной стенокардии
. Если закупорка усугубляется, происходит инфаркт.
В связи с этим пациентов с нестабильной стенокардией необходимо экстренно госпитализировать.
Острейший период
В этот период наблюдается самая высокая летальность от инфаркта миокарда. В то же время, острейший период – самый благоприятный в плане терапии. Существуют препараты, которые разрушают образовавшийся тромб, тем самым восстанавливая нарушенный ток крови по сосуду. Однако эти лекарства эффективны лишь в течение первых 12 часов с момента развития инфаркта, и чем раньше они применены, тем лучше будет результат.
В острейший период появляется ангинозный статус — очень интенсивная боль, которая локализуется либо за грудиной, либо в левой половине грудной клетки. Пациенты описывают боль как кинжальную, сверлящую или давящую («сердце сжало в тисках»). Зачастую боль накатывает волнами, может отдавать в левое плечо, руку, межлопаточную область, нижнюю челюсть. Иногда она распространяется на правую половину грудной клетки и в верхнюю половину живота.
Боль в целом схожа с таковою во время приступа стенокардии, но интенсивность ее гораздо выше, она не проходит после приема 2-3 таблеток нитроглицерина и обычно длится от 30 минут и дольше.
Помимо боли нередко наблюдается холодный пот, выраженная общая слабость. Артериальное давление чаще снижается в результате уменьшения силы сокращений поврежденного сердца, реже — повышается, поскольку организм в ответ на стресс выбрасывает большое количество адреналина, оказывающего стимулирующее влияние на работу сердечно-сосудистой системы. Почти всегда при инфаркте миокарда пациенты испытывают выраженную тревогу, страх смерти.
Важно знать, что у 20% пациентов острейший период инфаркта протекает малосимптомно (так называемая «безболевая» форма инфаркта миокарда). Такие пациенты отмечают неясную тяжесть в груди («сердечную тоску»), выраженную утомляемость, недомогание, бессонницу, «беспричинную» тревогу.
Еще у части больных инфаркт миокарда может проявлять себя развитием нарушений ритма и проводимости. Такие пациенты ощущают перебои в работе сердца, возможно — резкое учащение, или, напротив, замедление пульса. Могут появляться головокружение, выраженная слабость, эпизоды потери сознания.
Иногда инфаркт миокарда может манифестировать внезапно возникшей одышкой или отеком легких.
Симптоматика клинических вариантов острейшей фазы инфаркта миокарда
|
Болевой (status anginosus) |
Типичное клиническое течение, основным проявлением при котором служит ангинозная боль, не зависящая от позы и положения тела, от движений и дыхания, устойчивая к нитратам. Боль имеет давящий, душащий, жгущий или раздирающий характер с локализацией за грудиной, во всей передней грудной стенке с возможной иррадиацией в плечи, шею, руки, спину, эпигастальную область. Характерно сочетание с гипергидрозом, резкой общей слабостью, бледностью кожных покровов, возбуждением, двигательным беспокойством. |
|
Абдоминальный (status gastralgicus) |
Проявляется сочетанием эпигастральных болей с диспептическими явлениями — тошнотой, не приносящей облегчения рвотой, икотой, отрыжкой, резким вздутием живота. Возможны иррадиация болей в спину, напряжение брюшной стенки и болезненность при пальпации в эпигастрии. |
| Атипичный болевой | Болевой синдром имеет атипичный характер по локализации (например, только в зонах иррадиации — горле и нижней челюсти, плечах, руках и т.д.) и/или по характеру. |
|
Астматический (status astmaticus) |
Единственный признак — приступ одышки, являющийся проявлением острой застойной сердечной недостаточности (сердечная астма или отек легких). |
| Аритмический | Нарушения ритма служат единственным клиническим проявлением или преобладают в клинической картине. |
| Цереброваскулярный | В клинической картине преобладают признаки нарушения мозгового кровообращения (чаще — динамического): обморок, головокружение, тошнота, рвота. Возможна очаговая неврологическая симптоматика. |
| Малосимптомный (бессимптомный) | Наиболее сложный для распознавания вариант, нередко диагностируемый ретроспективно по данным ЭКГ. |
Острый период
В этом периоде острая боль стихает, поскольку процесс разрушения кардиомиоцитов завершен, а некротизированные ткани не чувствительны к боли. Большинство больных могут отмечать сохранение остаточных болей: глухих и постоянных, как правило, локализующихся за грудиной.
На вторые сутки ферменты из поврежденных клеток и разрушенные ткани попадают в кровь, вызывая температурную реакцию: может появляться лихорадка до 39°С, а также недомогание, слабость, потливость.
Действие стрессовых гормонов (адреналина, норадреналина, дофамина) утихает, в результате чего артериальное давление снижается, иногда очень значительно.
В этот период могут появляться тупые боли в груди, усиливающиеся при дыхании, что является признаком развития плевроперикардита. У части больных интенсивные давящие боли в сердце могут возобновиться — в таком случае диагностируется постинфарктная стенокардия либо рецидив инфаркта миокарда.
Поскольку рубец еще не сформирован, а часть мышечных клеток сердца разрушена, в этот период очень важно минимизировать физическую активность, стресс. При несоблюдении этих правил может развиться аневризма сердца или наступить смерть от разрыва сердца.
Подострый период
В этот период болевые ощущения, как правило, отсутствуют. Учитывая тот факт, что сократительная способность сердца снижена, поскольку участок миокарда «выключен» из работы, могут появиться симптомы сердечной недостаточности: одышка, отеки ног. В целом же состояние пациента улучшается: температура нормализуется, артериальное давление стабилизируется, риск развития аритмии уменьшается.
В сердце происходят процессы рубцевания: организм устраняет образовавшийся дефект, замещая разрушенные кардиомиоциты соединительной тканью.
Период рубцевания инфаркта миокарда
В этот период продолжается и завершается образование полноценного рубца из грубоволокнистой соединительной ткани. Самочувствие пациента зависит от величины площади поражения и наличия или отсутствия осложнений инфаркта миокарда.
В целом, состояние нормализуется. Болевых ощущений в сердце нет либо имеется стабильная стенокардия определенного функционального класса. Человек привыкает к новым условиям жизни.
Диагностика
Электрокардиография — важнейший метод диагностики инфаркта миокарда (ИМ), позволяющий:
— выявить ИМ;
— установить локализацию ИМ, его глубину и распространенность;
— диагностировать осложнения ИМ (аритмии, формирование аневризмы сердца)
ЭКГ при ИМ формируется под влиянием трех зон, образующихся в области инфаркта и представленных в таблице ниже (Bayley)
|
Зона некроза — в центре очага поражения |
Трансмуральный ИМ | Патологический зубец Q |
| Нетрансмуральный ИМ | Отсутствие или невыраженность патологического зубца Q | |
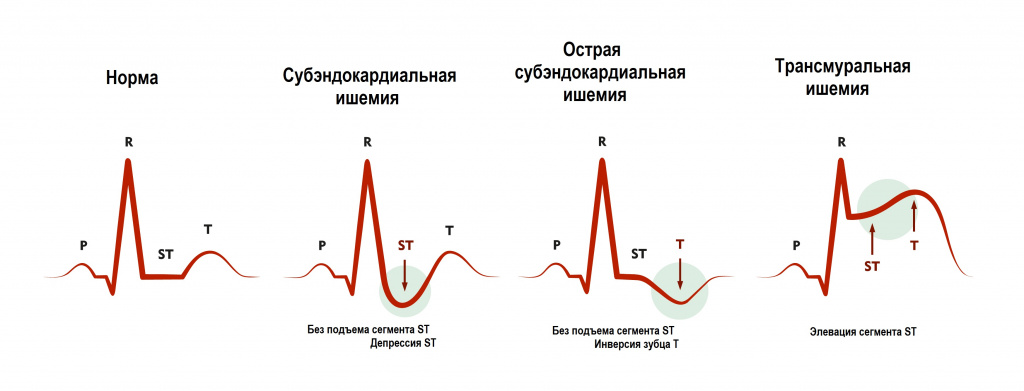
| Зона повреждения — к периферии от зоны некроза, окружает ее | Субэндокардиальный ИМ | Депрессия сегмента ST |
| Субэпикардиальный или трансмуральный ИМ | Элевация сегмента ST | |
| Зона ишемии — кнаружи от зоны повреждения | Субэндокардиальный ИМ | Высокий и широкий зубец Т (высокий коронарный зубец Т) |
| Субэпикардиальный илитрансмуральный ИМ | Отрицательный симметричный зубец Т с заостренной вершиной (отрицательный коронарный зубец Т) |
Диагностика стадии ИМ (в динамике)
Топическая диагностика (локализация) ИМ
В таблице знаком (+) обозначено смещение вверх сегмента RS-Т или положительный зубец Т, знаком (–) — смещение сегмента RS-Т вниз от изолинии или отрицательный зубец Т.
| Локализация ИМ |
Отведения |
Характер изменений ЭКГ |
| Переднеперегородочный |
V1-V3 |
1) Q или QS 2) +(RS-T) 3) -Т |
| Передневерхушечный |
V3,V4 |
1) Q или QS 2) +(RS-T) 1) -Т |
| Переднебоковой |
I, aVL, V5, V6 |
1) Q 2) +(RS-T) 3) -Т |
| Распространенный передний |
I, aVL, V1-V6 |
1) Q или QS 2) +(RS-T) 3) -Т |
|
III, aVF |
Реципрокные изменения: 1) -(RS-T) 2) + Т (высокие) |
|
| Высокий передний (переднебазальный) |
V24-V26, V34- V36 |
1) Q или QS 2) +(RS-T) 3) -Т |
| Заднедиафрагмальный (нижний) |
III, aVF или III, II, aVF |
1) Q или QS 2) + (RS-T) 3) -T |
|
V1-V4 |
Реципрокные изменения: 1) -{RS-T) 2) + Т (высокие) |
|
| Заднебазальный |
V7–V9 (не всегда) |
1) Q или QS 2) +(RS-T) 3) -Т. |
|
V1– V3 |
Реципрокные изменения: 1) -(RS-T), 2) +Т (высокие); 3) Увеличение R. |
|
| Заднебоковой |
V5, V6, Ill, aVF |
1) Q 2) +(RS-T) 3) -Т |
|
V1-V3 |
Реципрокные изменения: 1) увеличение R 2) -(RS-T) 3) + T (высокие). |
|
| Распространенный задний |
III, aVF, III, V5, V6, V7-9 |
1) Q или QS 2) +(RS-T) 3) -Т |
|
V1-V3 |
Реципрокные изменения: 1) увеличение R 2) -(RS-T) 3) +T (высокие). |
Прекардиальное электрокардиографическое картирование сердца
Исследование применяется при остром инфаркте миокарда передней и переднебоковой стенок левого желудочка для косвенного определения размеров зоны некроза и периинфарктной зоны (участок ишемического повреждения). С этой целью после регистрации ЭКГ с 35 точек на поверхности грудной клетки строят картограмму, состоящую из 35 квадратов, каждый из которых соответствует одному из 35 отведений.
Размеры зоны некроза условно оценивают по количеству отведений, в которых выявляются признаки трансмурального некроза – комплекс QS. Это так называемая «площадь трансмурального некроза» (AQS).
Параметры определения величины периинфарктной зоны:
1. Количество отведений (квадратов), в которых регистрируется подъем сегмента RS-Т выше изолинии. Это площадь RS-T (ARS-T).
2. Величина суммарного подъема сегмента RS-Т во всех отведениях (квадратах) картограммы, в которых фиксируется ишемическое повреждение миокарда (ERS-Т).
3. Значение среднего индивидуального подъема сегмента RS-T (NRS-T), который рассчитывается по формуле: NRS – T= ERS – T/ARS–T
Указанные картографические показатели с успехом используются для наблюдения за динамикой зон некроза и периинфарктной зоны в процессе лечения больных острым инфарктом миокарда, а также для оценки прогноза заболевания; чем выше все описанные показатели, тем больше площадь и глубина поражения миокарда и, соответственно, тем хуже прогноз заболевания.
Коронарография
«Золотой стандарт» диагностики ишемической болезни сердца (ИБС). Больные с многососудистым поражением или поражением ствола левой венечной артерии имеют более высокий риск сердечно-сосудистых событий. Роль коронарографии в оценки критичности бляшки и других повреждений исключительно важна, если предполагается последующая
реваскуляризация
.
Сложные стенозы, бифуркационные поражения и извитость стенозированных сосудов служат показателями высокого риска. Самый высокий риск имеется при дефектах наполнения, так как при этом существуют внутрисосудистые тромбы. У 10-15% пациентов с болью в груди нет поражения венечных артерий и у них диагноз ИБС исключается.
Компьютерная томография
В настоящее время данное исследование не может заменить коронарографию при остром коронарном синдроме из-за субоптимальной диагностической точности.
КТ сердца не является оптимальным методом диагностики у больных с острым коронарным синдром из-за высокой вероятности в необходимости выполнения коронарной ангиопластики со стентированием. Это обусловлено тем, что на проведение КТ теряется время, пациент получает контрастный препарат и дозу облучения.
Двухмерная ЭхоКГ
Систолическая функция левого желудочка — важный прогностический показатель для больного с ИБС. Регионарные нарушения сократимости могут наступить сразу после ишемии, задолго до некроза, но они неспецифичны для острых событий и могут быть результатом старого инфаркта миокарда.
Транзиторная локальная акинезия и гипокинезия сегментов левого желудочка могут определяться в ходе ишемии, с восстановлением нормальной кинетики стенки при прохождении ишемии.
Отсутствие нарушений локальной сократимости исключает наличие ИМ.
ЭхоКГ имеет ценность для диагностики других причин болей в груди — расслоение и разрыв аорты, гипертрофическая
кардиомиопатия
,
перикардит
и массивная
ТЭЛА
.
Перфузионная сцинтиграфия
Обычно этот метод исследования недоступен, поэтому у острых больных он используется редко. Нормальная сцинтиграмма миокарда с 99Th в покое достоверно исключает крупноочаговый ИМ. Однако ненормальная сцинтиграмма не указывает на острый ИМ, если только нет данных, что раньше сцинтиграмма была нормальной, до наступления острого состояния, но она указывает на наличие ИБС и необходимость дальнейшего обследования.
Магнитно-резонансная томография
МРТ сердца еще пока не стала рутинной процедурой для визуализации венечных сосудов, но позволяет получить информацию о регионарной сократимости, перфузии и жизнеспособности миокарда. Это позволяет идентифицировать больных с ОКС и острым ИМ. Кроме того, МРТ может исключить или подтвердить другие причины боли в груди — миокардит,
перикардит
, расслаивающую аневризму аорты и
ТЭЛА
Лабораторная диагностика
Лабораторное подтверждение острого инфаркта миокарда (ОИМ) основано на выявлении:
— неспецифических показателей тканевого некроза и воспалительной реакции миокарда;
— гиперферментемии (входит в классическую триаду признаков ОИМ: болевой синдром, типичные изменения ЭКГ, гиперферментемия).
Неспецифические показатели тканевого некроза и воспалительной реакции миокарда:
1. Лейкоцитоз, не превышающий обычно 12-15*109/л (выявляются обычно к концу первых суток от начала заболевания и при неосложненном течении инфаркта сохраняются примерно в течение недели).
2. Анэозинофилия.
3. Небольшой палочкоядерный сдвиг формулы крови влево.
4. Увеличение СОЭ (увеличивается обычно спустя несколько дней от начала заболевания и может оставаться повышенной на протяжении 2-3 недель и дольше даже при отсутствии осложнений ИМ).
Правильная трактовка этих показателей возможна только при сопоставлении с клинической картиной заболевания и данными ЭКГ.
Длительное сохранение (более 1 недели) лейкоцитоза или/и умеренной лихорадки у больных ОИМ свидетельствует о возможном развитии осложнений: (пневмония,
плеврит
, перикардит, тромбоэмболия мелких ветвей легочной артерии и другие).
Гиперферментемия
Основной причиной повышения активности и содержания ферментов в сыворотке крови у больных ОИМ является разрушение кардиомиоцитов и выход высвобождающихся клеточных ферментов в кровь.
Наиболее ценным для диагностики ОИМ является определение активности нескольких ферментов в сыворотке крови:
— креатинфосфокиназы (КФК) и особенно ее МВ-фракции (МВ-КФК);
— лактатдегидрогеназы (ЛДГ) и ее изофермента 1 (ЛДГ1);
— аспартатаминотрансферазы (АСТ);
— тропонина;
— миоглобина.
Повышение активности МВ-фракции КФК, содержащейся преимущественно в миокарде, специфично для повреждения сердечной мышцы, в первую очередь, для ОИМ. МВ-фракция КФК не реагирует на повреждение скелетных мышц, головного мозга и щитовидной железы.
Динамика МВ-КФК при ОИМ:
— через 3-4 часа активность начинает возрастать;
— через 10-12 часов достигает максимума;
— через 48 часов от начала ангинозного приступа возвращается к исходным цифрам.
Степень повышения активности МВ-КФК в крови в целом хорошо коррелирует с размером ИМ — чем больше объем поражения сердечной мышцы, тем выше активность МВ-КФК 1.
Динамика КФК при ОИМ:
— к концу первых суток уровень фермента в 3-20 раз превышает норму;
— через 3-4 суток от начала заболевания возвращается к исходным значениям.
1 Следует помнить, что любые кардиохирургические вмешательства (включая коронароангиографию, катетеризацию полостей сердца и электроимпульсную терапию), как правило, сопровождаются кратковременным подъемом активности МВ-фракции КФК.
В литературе имеются также указания на возможность повышения уровня МВ-КФК при тяжелой пароксизмальной тахиаритмии, миокардитах и длительных приступах стенокардии покоя, расцениваемых как проявление нестабильной стенокардии.
В ряде случаев при обширных инфарктах миокарда вымывание ферментов в общий кровоток замедлено, поэтому абсолютное значение активности МВ-КФК и скорость его достижения могут оказаться меньше, чем при обычном вымывании фермента, хотя и в том, и в другом случае площадь под кривой “концентрация-время” остается одинаковой.
Лактатдегидрогеназа
Активность ЛДГ при ОИМ нарастает медленнее, чем КФК и МВ-КФК, и дольше остается повышенной 2.
Динамика ЛДГ при ОИМ:
— через 2-3 суток от начала инфаркта наступает пик активности;
— к 8-14 суткам происходит возвращение к исходному уровню.
2 Следует помнить, что активность общей ЛДГ повышается также при заболеваниях печени, шоке, застойной недостаточности кровообращения, гемолизе эритроцитов и мегалобластной анемии, ТЭЛА, миокардите, воспалении любой локализации, коронароангиографии, электроимпульсной терапии, тяжелой физической нагрузке и т. д.
Изофермент ЛДГ1 более специфичен для поражений сердца, хотя он также присутствует не только в мышце сердца, но и в других органах и тканях, включая эритроциты.
Аспартатаминотрансфераза
Динамика АСТ при ОИМ:
— через 24-36 часов от начала инфаркта относительно быстро наступает пик повышения активности;
— через 4-7 суток концентрация АСТ возвращается к исходному уровню.
Изменение активности АСТ неспецифично для ОИМ: уровень АСТ вместе с активностью АЛТ повышается при многих патологических состояниях, в том числе при заболеваниях печени 3.
3 При поражениях паренхимы печени в большей степени возрастает активность АЛТ, а при заболеваниях сердца в большей степени возрастает активность АСТ. При ИМ отношение АСТ/АЛТ (коэффициент де Ритиса) больше 1,33, а при заболеваниях печени отношение АСТ/АЛТ меньше 1,33.
Тропонин
Тропонин представляет собой универсальную для поперечно-полосатой мускулатуры структуру белковой природы, локализующуюся на тонких миофиламентах сократительного аппарата миокардиоцита.
Сам тропониновый комплекс состоит из трех компонентов:
— тропонин С — ответственный за связывание кальция;
— тропонин Т — предназначен для связывания тропомиозина;
— тропонина I — предназначен для ингибирования выше указанных двух процессов.
Тропонин Т и I существуют в специфичных для миокарда изоформах, отличающихся от изоформ скелетных мышц, чем и обусловливается их абсолютная кардиоспецифичность 4.
Динамика тропонинов при ОИМ:
— спустя 4-5 часов после гибели кардиомиоцитов вследствие развития необратимых некротических изменений, тропонин поступает в периферический кровоток и определяются в венозной крови;
— в первые 12-24 часа от момента возникновения ОИМ достигается пик концентрации.
Кардиальные изоформы тропонина длительно сохраняют свое присутствие в периферической крови:
— тропонин I определяется на протяжении 5-7 дней;
— тропонин Т определяется до 14 дней.
Присутствие этих изоформ тропонина в крови пациента выявляется при помощи
ИФА
с использованием специфических антител.
4 Следует помнить, что тропонины не являются ранними биомаркерами ОИМ, поэтому у рано обратившихся больных с подозрением на острый коронарный синдром при отрицательном первичном результате необходимо повторное (через 6-12 часов после болевого приступа) определение содержания тропонинов в периферической крови. В этой ситуации даже незначительное повышение уровня тропонинов свидетельствует о дополнительном риске для больного, поскольку доказано существование четкой корреляции между уровнем возрастания тропонина в крови и размером зоны поражения миокарда.
Многочисленными наблюдениями было показано, что повышенный уровень тропонина в крови больных с острым коронарным синдромом может рассматриваться как достоверный показатель наличия у пациента ОИМ. В то же время низкий уровень тропонина у этой категории больных свидетельствует в пользу постановки более мягкого диагноза нестабильной стенокардии.
Миоглобин
Специфичность миоглобина для диагностики ОИМ примерно такая же, как КФК, но ниже, чем МВ-КФК.
Уровень миоглобина может повышаться в 2-3 раза после внутримышечных инъекций, и диагностически значимым обычно считают повышение в 10 и более раз.
Подъем уровня миоглобина в крови начинается даже раньше, чем повышение активности КФК. Диагностически значимый уровень зачастую достигается уже через 4 часа и в подавляющем большинстве случаев наблюдается через 6 часов после болевого приступа.
Высокая концентрация миоглобина в крови наблюдается только в течение нескольких часов, поэтому, если не повторять анализ каждые 2-3 часа, пик концентрации можно пропустить. Измерение концентрации миоглобина может быть применено только в случаях поступления больных в стационар менее чем через 6-8 часов после начала болевого приступа.
Принципы ферментативной диагностики ОИМ
1. У пациентов, поступивших в течение первых 24 часов после ангинозного приступа, производится определение активности КФК в крови — это следует делать даже в тех случаях, когда по клиническим и электрокардиографическим данным диагноз инфаркта миокарда не вызывает сомнения, так как степень повышения активности КФК информирует врача о размерах инфаркта миокарда и прогнозе.
2. Если активность КФК находится в пределах нормы или повышена незначительно (в 2-3 раза), либо у пациента имеются явные признаки поражения скелетной мускулатуры или головного мозга, то для уточнения диагноза показано определение активности МВ-КФК.
3. Нормальные величины активности КФК и МВ-КФК, полученные при однократном заборе крови в момент поступления больного в клинику, недостаточны для исключения диагноза ОИМ. Анализ необходимо повторить хотя бы еще 2 раза через 12 и 24 часа.
4. Если больной поступил более чем через 24 часа после ангинозного приступа, но меньше чем через 2 недели, и уровень КФК и МВ-КФК нормальный, то целесообразно определить активность ЛДГ в крови (предпочтительнее — отношение активности ЛДГ1 и ЛДГ2), АСТ вместе с АЛТ и расчетом коэффициента де Ритиса.
5. Если ангинозные боли повторяются у больного после госпитализации, то рекомендуется измерять КФК и МВ-КФК сразу после приступа и через 12 и 24 часа.
6. Миоглобин в крови целесообразно определять только в первые часы после болевого приступа, повышение его уровня в 10 раз и больше указывает на некроз мышечных клеток, однако нормальный уровень миоглобина отнюдь не исключает инфаркта.
7. Определение ферментов нецелесообразно у бессимптомных больных с нормальной ЭКГ. Диагноз на основании одной только гиперферментемии ставить все равно нельзя — должны быть клинические и (или) ЭКГ-признаки, указывающие на возможность ИМ.
8. Контроль количества лейкоцитов и величины СОЭ необходимо проводить при поступлении пациента и затем не реже 1 раза в неделю, чтобы не пропустить инфекционные или аутоиммунные осложнения ОИМ.
9. Исследование уровня активности КФК и МВ-КФК целесообразно проводить только в течение 1-2 суток от предположительного начала заболевания.
10. Исследование уровня активности АСТ целесообразно проводить только в течение 4-7 суток от предположительного начала заболевания.
11. Повышение активности КФК, МВ-КФК, ЛДГ, ЛДГ1, АСТ не является строго специфичным для ОИМ, хотя при прочих равных условиях активность МВ-КФК отличается более высокой информативностью.
12. Отсутствие гиперферментемии не исключает развития ОИМ.
Дифференциальный диагноз
1. Аллергический и инфекционно-токсический шок.
Симптомы: загрудинная боль, одышка, падение артериального давления.
Анафилактический шок может возникать при любой лекарственной непереносимости. Начало болезни острое, четко приурочено к причинному фактору (инъекция антибиотика, прививка с целью профилактики инфекционного заболевания, введение противостолбнячной сыворотки и др.). В некоторых случаях заболевание начинается через 5-8 дней от момента ятрогенного вмешательства, развивается по типу
феномена Артюса
, в котором сердце выступает в роли шок-органа.
Инфекционно-токсический шок с поражением миокарда может возникнуть при любом тяжелом инфекционном заболевании.
Клинически заболевание очень напоминает инфаркт миокарда (ИМ), отличаясь от него по этиологическим факторам. Дифференциация затрудняется в связи с тем, что при аллергическом и инфекционно-аллергическом шоке могут возникать некоронарогенные некрозы миокарда с грубыми изменениями ЭКГ, лейкоцитозом, увеличением СОЭ, гиперферментемией АСТ, ЛДГ,
ГБД
, КФК, МВ-КФК.
В отличие от типичного ИМ, при данных шоках на ЭКГ не бывает глубокого зубца Q и комплекса QS, дискордантности изменений конечной части.
2. Перикардит (миоперикардит).
Этиологические факторы перикардита: ревматизм, туберкулез, вирусная инфекция (чаще — вирус Коксаки или ECHO), диффузные болезни соединительной ткани; нередко — терминальная ХПН.
При остром перикардите в процесс часто вовлекаются субэпикардиальные слои миокарда.
В типичном варианте при сухом перикардите возникают тупые, давящие (реже — острые) боли в прекордиальной области без иррадиации в спину, под лопатку, в левую руку, свойственные инфаркту миокарда.
Шум трения перикарда регистрируется в те же дни, что и повышение температуры тела, лейкоцитоз, увеличение СОЭ. Шум стойкий, выслушивается в течение нескольких дней или недель.
При ИМ шум трения перикарда кратковременный; предшествует лихорадке и увеличению СОЭ.
Если у больных перикардитом появляется сердечная недостаточность, то она правожелудочковая или бивентрикулярная. Для ИМ характерна левожелудочковая сердечная недостаточность.
Дифференциально-диагностическая ценность энзимологических тестов невелика. Вследствие поражения субэпикардиальных слоев миокарда у больных перикардитом может регистрироваться гиперферментемия АСТ, ЛДГ, ЛДГ1,
ГБД
, КФК и даже изоэнзима МВ-КФК.
В правильной постановке диагноза помогают данные ЭКГ. При перикардите имеются симптомы субэпикардиального повреждения в виде элевации интервала ST во всех 12 общепринятых отведениях (нет дискордантности, свойственной ИМ). Зубец Q при перикардите, в отличие от ИМ, не выявляется. Зубец Т при перикардите может быть отрицательным, он становится положительным через 2-3 недели от начала болезни.
При появлении перикардиального экссудата очень характерной становится рентегнологическая картина.
3. Левосторонняя пневмония.
При пневмонии могут появляться боли в левой половине грудной клетки, иногда интенсивные. Однако в отличие от прекордиальных болей при ИМ, они четко связаны с дыханием и кашлем, не имеют типичной для ИМ иррадиации.
Для пневмонии характерен продуктивный кашель. Начало болезни (озноб, повышение температуры, бои в боку, шум трения плевры) совершенно не типично для ИМ.
Физикальные и рентгенологические изменения в легких помогают диагностировать пневмонию.
ЭКГ при пневмонии может меняться (низкий зубец Т, тахикардия), но никогда не бывает изменений, напоминающих таковые при ИМ.
Как и при ИМ, при пневмонии можно обнаружить лейкоцитоз, увеличение СОЭ, гиперферментемию АСТ, ЛДГ, но только при поражении миокарда повышается активность
ГБД
, ЛДГ1, МВ-КФК.
4. Спонтанный пневмоторакс.
При пневмотораксе возникают сильная боль в боку, одышка, тахикардия. В отличие от ИМ, спонтанный пневмоторакс сопровождается тимпаническим перкуторным тоном на стороне поражения, ослаблением дыхания, рентгенологическими изменениями (газовый пузырь, коллапс легкого, смещение сердца и средостения в здоровую сторону).
Показатели ЭКГ при спонтанном пневмотораксе либо нормальные, либо выявляется преходящее снижение зубца Т.
Лейкоцитоза, увеличения СОЭ при пневмотораксе не бывает. Активность сывороточных ферментов нормальная.
5. Ушиб грудной клетки.
Как и при ИМ возникают сильные боли в груди, возможен шок. Сотрясение и ушиб грудной клетки приводят к повреждению миокарда, что сопровождается элевацией или депрессией интервала ST, негативизацией зубца Т, а в тяжелых случаях — даже появлением патологического зубца Q.
В постановке правильного диагноза решающую роль играет анамнез.
Клиническая оценка ушиба грудной клетки с изменениями ЭКГ должна быть достаточно серьезной, поскольку в основе этих изменений лежат некоронарогенные некрозы миокарда.
6. Остеохондроз грудного отдела позвоночника с компрессией корешка.
При остеохондрозе с корешковым синдромом боли в грудной клетке слева могут быть очень сильными, нестерпимыми. Но, в отличие от болей при ИМ, они исчезают, когда больной принимает неподвижное вынужденное положение, и резко усиливаются при поворотах туловища и дыхании.
Нитроглицерин, нитраты при остеохондрозе совершенно не эффективны.
При грудном «радикулите» определяется четкая локальная болезненность в паравертебральных точках, реже по ходу межреберий.
Количество лейкоцитов, а также значения СОЭ, энзимологических показателей, ЭКГ в пределах нормы.
7. Опоясывающий лишай.
Клиника опоясывающего лишая весьма напоминает описанную выше (см. описание симптомов корешкового синдрома при остеохондрозе позвоночника в грудном отделе).
У некоторых больных может регистрироваться лихорадка в сочетании с умеренным лейкоцитозом, увеличением СОЭ.
ЭКГ, ферментные тесты, как правило, часто помогают исключить диагноз ИМ.
Диагноз «опоясывающий лишай» становится достоверным со 2-4 дня болезни, когда по ходу межреберий появляется характерная пузырьковая (везикулярная) сыпь.
8. Бронхиальная астма.
Астматический вариант ИМ в чистом виде встречается редко, чаще удушье сочетается с болями в предсердечной области, аритмией, симптомами шока.
9. Острая левожелудочковая недостаточность осложняет течение многих болезней сердца, в числе которых кардиомиопатии, клапанные и врожденные пороки сердца, миокардиты и другие.
10. Острый холецистопанкреатит.
При остром холецистопанкреатите, как и при гастралгическом варианте ИМ, возникают сильные боли в эпигастральной области, сопровождающиеся слабостью, потливостью, гипотензией. Однако боли при остром холецистопанкреатите локализуются не только в эпигастрии, но и в правом подреберье, иррадиируют вверх и вправо, в спину, иногда могут быть опоясывающими. Характерно сочетание болей с тошнотой, рвотой, причем в рвотных массах определяется примесь желчи.
Пальпаторно определяется болезненность в точке желчного пузыря, проекции поджелудочной железы, положительные
симптом Кера
,
симптом Ортнера
,
симптом Мюсси
, что не характерно для ИМ.
Вздутие живота, локальное напряжение в правом верхнем квадранте не типично для ИМ.
Лейкоцитоз, увеличение СОЭ, гиперферментемия АСТ, ЛДГ могут появляться при обоих заболеваниях. При холецистопанкреатите отмечается увеличение активности альфа-амилазы сыворотки крови и мочи, ЛДГ 3-5. При ИМ следует ориентироваться на высокие показатели ферментной активности КФК, МВ-КФК,
ГБД
.
ЭКГ при остром холецистопанкреатите: снижение интервала ST в ряде отведений, слабо отрицательный или двухфазный зубец Т.
Крупноочаговое метаболическое повреждение миокарда существенно ухудшает прогноз панкреатита, нередко является ведущим фактором в летальном исходе.
11. Прободная язва желудка.
Как при ИМ, характерны острые боли в эпигастрии. Однако при прободной язве желудка отмечаются нестерпимые, «кинжальные» боли, максимально выраженные в момент прободения и затем уменьшающиеся в интенсивности, при этом эпицентр болей смещается несколько вправо и вниз.
При гастралгическом варианте ИМ боли в эпигастрии могут быть интенсивными, но для них не характерно столь острое, мгновенное начало с последующим спадом.
При прободной язве желудка через 2-4 часа от момента прободения симптоматика меняется. У больных с прободной гастродуоденальной язвой появляются симптомы интоксикации; язык становится сухим, черты лица заостряются; живот становится втянутым, напряженным; отмечаются положительные симптомы раздражения; перкуторно определяется «исчезновение» печеночной тупости; рентгенологически выявляется воздух под правым куполом диафрагмы.
Как при ИМ, так и при прободении язвы температура тела может быть субфебрильной, отмечается умеренный лейкоцитоз в течение первых суток.
Для ИМ типично увеличение активности сывороточных ферментов (ЛДГ, КФК, МВ КФК).
ЭКГ при прободной язве желудка в течение первых суток, как правило, не меняется. На следующий день возможны изменения конечной части за счет электролитных нарушений.
12. Рак кардиального отдела желудка.
При раке кардии нередко возникают интенсивные давящие боли в эпигастрии и под мечевидным отростком, сочетающиеся с транзиторной гипотонией.
В отличие от ИМ при раке кардии эпигастральные боли закономерно повторяются ежедневно, они связаны с приемом пищи.
СОЭ увеличивается при обоих заболеваниях, однако динамика активности ферментов КФК, МВ КФК, ЛДГ,
ГБД
характерна только для ИМ.
Для исключения гастралгического варианта ИМ необходимо ЭКГ-исследование. На ЭКГ выявляются изменения интервала ST (чаще депрессия) и зубца Т (изоэлектричный или слабо отрицательный) в III, avF отведениях, что служит поводом для диагностики мелкоочагового заднего ИМ.
При раке кардии ЭКГ «застывшая», на ней не удается определить характерной для ИМ динамики.
Диагноз рака уточняется при проведении
ФГДС
, рентгенологического исследования желудка в различных положениях тела исследуемого, в том числе и в положении антиортостаза.
13. Пищевая токсикоинфекция.
Как и при ИМ появляются боли в эпигастрии, падает артериальное давление. Однако при пищевой токсикоинфекции боль в эпигастрии сопровождается тошнотой, рвотой, гипотермией. Диарея не всегда встречается при пищевой токсикоинфекции, но ее никогда не бывает при ИМ.
ЭКГ при пищевой токсикоинфекции либо не меняется, либо во время исследования определяются «электролитные нарушения» в виде корытообразного смещения вниз интервала ST, слабоотрицательного или изоэлектрического зубца Т.
Лабораторные исследования при пищевой токсикоинфекции показывают умеренный лейкоцитоз, эритроцитоз (сгущение крови), небольшое повышение активности АЛТ, АСТ, ЛДГ без существенных изменений активности КФК, МВ-КФК,
ГБД
, свойственных ИМ.
14. Острое нарушение мезентерального кровообращения.
Боль в эпигастрии, падение артериального давления возникают при обоих заболеваниях. Дифференциация усложняется тем, что тромбоз мезентеральных сосудов, как и ИМ, поражает, как правило, людей пожилого возраста с различными клиническим проявлениями ИБС, с артериальной гипертонией.
При нарушении кровообращения в системе мезентеральных сосудов боли локализуются не только в эпигастрии, но и по всему животу. Живот умеренно вздут, аускультативно не выявляются звуки перистальтики кишечника, возможно обнаружение симптомов раздражения брюшины.
Для уточнения диагноза проводится обзорная рентгенография брюшной полости и определяется наличие или отсутствие перистальтики кишечника и скопления газа в кишечных петлях.
Нарушение мезентерального кровообращения не сопровождается изменениями ЭКГ и ферментных показателей, характерных для ИМ.
При затруднении в диагностике тромбоза мезентеральных сосудов патогномоничные изменения могут быть обнаружены при лапароскопии и ангиографии.
15. Расслаивающая аневризма абдоминального отдела аорты.
При абдоминальной форме расслаивающей аневризмы аорты в отличие от гастралгического варианта ИМ, характерны следующие признаки:
— начало болезни с болей в груди;
— волнообразный характер болевого синдрома с иррадиацией в поясницу по ходу позвоночника;
— появление опухолевидного образования эластичной консистенции, пульсирующего синхронно с сердцем;
— появление систолического шума над опухолевидным образованием;
— нарастание анемии.
16. Некоронарогенные некрозы миокарда могут возникать при тиреотоксикозе, лейкозах и анемиях, системных васкулитах, гипо- и гипергликемических состояниях.
Клинически на фоне симптоматики основной болезни отмечаются боли в сердце (временами сильные), одышка.
Данные лабораторных исследований бывают малоинформативными в дифференциации некоронарогенных некрозов с ИМ атеросклеротического генеза. Гиперферментемия ЛДГ, ЛДГ1,
ГБД
, КФК, МВ-КФК обусловлены миокардиальными некрозами как таковыми, вне зависимости от их этиологии.
На ЭКГ при некоронарогенных некрозах миокарда выявляются изменения конечной части – депрессия или, реже, элевация интервала ST, негативные зубцы Т, с последующей динамикой, соответствующей нетрансмуральному ИМ.
Точный диагноз устанавливается на основе всей симптоматики заболеваний. Только такой подход дает возможность методически правильно оценить собственно сердечную патологию.
18. Опухоли сердца (первичные и метастатические).
При опухолях сердца могут появляться упорные интенсивные боли в прекордиальной области, резистентные к нитратам, сердечная недостаточность, аритмии.
На ЭКГ отмечаются патологический зубец Q, элевация интервала ST, отрицательный зубец Т. В отличие от ИМ при опухоли сердца не бывает типичной эволюции ЭКГ, она малодинамична.
Сердечная недостаточность, аритмии рефрактерны к лечению. Диагноз уточняется при тщательном анализе клинико-рентгенологических и Эхо-КГ-данных.
19. Посттахикардиальный синдром.
Посттахикардиальным синдромом называется ЭКГ-феномен, выражающийся в преходящей ишемии миокарда (депрессия интервала ST, негативный зубец Т) после купирования тахиаритмии. Данный симптомокомплекс необходимо оценивать очень осторожно.
Во-первых, тахиаритмия может быть началом ИМ и ЭКГ после ее купирования зачастую лишь выявляет инфарктные изменения.
Во-вторых, приступ тахиаритмии в такой степени нарушает гемодинамику и коронарный кровоток, что он может приводить к развитию миокардиальных некрозов, особенно при изначально дефектном коронарном кровообращении у больных со стенозирующим коронарным атеросклерозом. Следовательно, диагноз посттахикардиального синдрома достоверен после тщательного наблюдения за больным с учетом динамики клинических, ЭхоКГ-, лабораторных данных.
20. Синдром преждевременной реполяризации желудочков.
Синдром выражается в элевации интервала ST в вильсоновских отведениях, начинающегося с точки J, расположенной на нисходящем колене зубца R.
Этот синдром регистрируется у здоровых людей, спортсменов, больных с нейроциркуляторной дистонией.
Для постановки правильного диагноза надо знать о существовании ЭКГ-феномена — синдрома преждевременной реполяризации желудочков. При этом синдроме отсутствует клиника ИМ, не бывает свойственной ему динамика ЭКГ.
Примечание
При трактовке симптома «острая боль в эпигастрии» в сочетании с гипотензией при проведении дифференциального диагноза с ИМ надо иметь в виду и более редкие болезни: острую надпочечниковую недостаточность; разрыв печени, селезенки или полого органа при травме; сифилитическую сухотку спинного мозга с табетическими желудочными кризами (анизокория, птоз, рефлекторная неподвижность глазных яблок, атрофия зрительного нерва, атаксия, отсутствие коленных рефлексов); абдоминальные кризы при гипергликемии, кетоацидозе у больных с сахарным диабетом.
Осложнения
Группы осложнений инфаркта миокарда (ИМ):
1. Электрические — нарушения ритма и проводимости:
— брадитахиаритмии;
— экстрасистолии;
— внутрижелудочковые блокады;
— АВ-блокады.
Данные осложнения практически постоянно встречаются при крупноочаговом ИМ. Часто аритмии не являются угрожающими для жизни, но свидетельствуют о серьезных нарушениях (электролитных, продолжающейся ишемии, вагальной гиперактивности и др.), требующих коррекции.
2. Гемодинамические осложнения:
2.1 Вследствие нарушений насосной функции сердца:
— острая левожелудочковая недостаточность;
— острая правожелудочковая недостаточность;
— бивентрикулярная недостаточность;
— кардиогенный шок;
— аневризма желудочка;
— расширение инфаркта.
2.2 Вследствие дисфункции сосочковых мышц.
2.3 Вследствие механических нарушений:
— острая митральная регургитация вследствие разрыва сосочковых мышц;
— разрывы сердца, свободной стенки или межжелудочковой перегородки;
— аневризмы левого желудочка;
— отрывы сосочковых мышц.
2.4 Вследствие электромеханической диссоциации.
3. Реактивные и прочие осложнения:
— эпистенокардический перикардит;
— тромбоэмболии сосудов малого и большого круга кровообращения;
— ранняя постинфарктная стенокардия;
—
синдром Дресслера
.
По времени появления осложнения ИМ классифицируют на:
1. Ранние осложнения, возникающие в первые часы (нередко на этапе транспортировки больного в стационар) или в острейший период (3-4 дня):
— нарушения ритма и проводимости (90%), вплоть до фибрилляции желудочков и полной АВ-блокады (самые частые осложнения и причина летальности на догоспитальном этапе);
— внезапная остановка сердца;
— острая недостаточность насосной функции сердца — острая левожелудочковая недостаточность и кардиогенный шок (до 25%);
— разрывы сердца — наружные, внутренние; медленнотекущие, одномоментные (1-3%);
— острая дисфункция сосочковых мышц (митральная регургитация);
— ранний эпистенокардический перикардит.
2. Поздние осложнения (возникают на 2-3-й неделе, в период активного расширения режима):
— постинфарктный
синдром Дресслера
(3%);
— пристеночный тромбоэндокардит (до 20%);
— хроническая сердечная недостаточность;
— нейротрофические расстройства (плечевой синдром, синдром передней грудной стенки).
Как на ранних, так и на поздних стадиях течения ИМ могут возникать следующие осложнения:
— острая патология желудочно-кишечного тракта (острые язвы, желудочно-кишечный синдром, кровотечения и др.);
— психические изменения (депрессия, истерические реакции, психоз);
— аневризмы сердца (у 3-20% больных);
— тромбоэмболические осложнения: системные (вследствие пристеночного тромбоза) и ТЭЛА (из-за тромбоза глубоких вен голеней).
Тромбоэмболии клинически выявляются у 5-10% больных (на аутопсии — у 45%). Часто они имеют бессимптомное течение и являются причиной смерти у ряда госпитализированных больных с ИМ (до 20%).
У некоторых пожилых мужчин с доброкачественной гипертрофией предстательной железы развивается острая атония мочевого пузыря (снижается его тонус, нет позывов к мочеиспусканию) с увеличением объема пузыря до 2 л, задержкой мочеиспускания на фоне постельного режима и лечения наркотическими препаратами, атропином.
Лечение
Цели неотложной терапии инфаркта миокарда (ИМ):
— купирование болевого синдрома;
— восстановление коронарного кровотока;
— уменьшение работы сердца и потребности миокарда в кислороде;
— ограничение размеров ИМ;
— лечение и профилактика осложнений ИМ.
Купирование болевого приступа
Морфин — препарат выбора для купирования болевого синдрома при ИМ на догоспитальном этапе. Морфин обладает необходимыми эффектами и достаточной для транспортировки длительностью действия.
Препарат вводится внутривенно дробно: 1 мл 1% раствора разводят физиологическим раствором натрия хлорида до 20 мл (1 мл полученного раствора содержит 0,5 мг активного вещества) и вводят 2-5 мг каждые 5-15 минут до полного устранения болевого синдрома либо до появления побочных эффектов (гипотензии, угнетения дыхания, рвоты).
Суммарная доза не должна превышать 10-15 мг (1-1,5 мл 1% раствора) морфина (на догоспитальном этапе не допускается превышение дозы 20 мг).
При невыраженном болевом синдроме, пациентам старческого возраста и ослабленным больным наркотические анальгетики могут вводиться подкожно или внутримышечно. Не рекомендуется вводить подкожно более 60 мг морфина в течение 12 часов.
Для решения вопроса о возможности использования наркотических анальгетиков необходимо:
— убедиться, что типичный или атипичный болевой синдром не является проявлением “острого живота”, и изменения ЭКГ являются специфическим проявлением ИМ, а не неспецифической реакцией на катастрофу в брюшной полости;
— выяснить, имеются ли в анамнезе хронические заболевания системы дыхания (в частности — бронхиальная астма);
— уточнить, когда было последнее обострение бронхообструктивного синдрома;
— установить, имеются ли в настоящее время признаки дыхательной недостаточности, какие, какова степень ее выраженности;
— выяснить, имеется ли у больного в анамнезе судорожный синдром, когда был последний припадок.
Восстановление коронарного кровотока в острейшей фазе ИМ
Поскольку непосредственной причиной развития ИМ является окклюзия коронарной артерии, в основе лечения лежит восстановление коронарного кровотока — коронарная реперфузия путем системного тромболизиса.
Все больные ИМ должны быть безотлагательно обследованы для уточнения показаний и противопоказаний к восстановлению коронарного кровотока.
Показания к проведению тромболизиса:
1. Наличие подъема сегмента ST более чем на 1 mm по крайней мере в двух стандартных отведениях ЭКГ и более чем на 2 mm в двух смежных грудных отведениях.
2. Остро возникшая полная блокада левой ножки пучка Гиса при сроке, прошедшем с начала заболевания, более 30 минут, но не превышающем 12 часов.
Применение тромболитических средств возможно и позже, в случаях когда сохраняются подъем сегмента ST, продолжается боль и/или наблюдается нестабильная гемодинамика.
Абсолютные противопоказания к тромболитической терапии:
— ранее перенесенный геморрагический инсульт или нарушение мозгового кровообращения неизвестной этиологии;
— ишемический инсульт, перенесенный в течение последних 3 месяцев;
— опухоль мозга, первичная и метастазы;
— подозрение на расслоение аорты;
— наличие признаков кровотечения или геморрагического диатеза (за исключением менструации);
— существенные закрытые травмы головы в последние 3 месяца;
— изменение структуры мозговых сосудов, например,
артериовенозная мальформация
, артериальные
аневризмы
.
Относительные противопоказания к тромболитической терапии:
— устойчивая, высокая, плохо контролируемая
артериальная гипертензия
в анамнезе;
— наличие плохо контролируемой артериальной гипертензии (в момент госпитализации САД >180 мм рт.ст., ДАД >110 мм рт.ст.);
—
ишемический инсульт
давностью >3 месяцев;
— деменция или внутричерепная патология, не включенная в абсолютные противопоказания;
— травматичная или длительная (>10 минут), сердечно-легочная реанимация или обширное оперативное вмешательство, перенесенное в течение последних 3 недель;
— недавнее (в течение предыдущих 2-4 недель) внутреннее кровотечение;
— пункция сосуда, не поддающегося прижатию;
— противопоказание для стрептокиназы — введение стрептокиназы, в том числе модифицированной, более 5 суток назад или известная аллергия на нее;
— беременность;
— обострение язвенной болезни;
— прием антикоагулянтов непрямого действия (чем выше
МНО
, тем выше риск кровотечения).
Тромболитические препараты:
— стрептокиназа;
— рекомбинантный тканевой активатор плазминогена (алтеплаза) и его модификация — тенектеплаза;
— модифицированная (рекомбинантная) проурокиназа (пуролаза).
Наиболее часто используется стрептокиназа:
— введение препарата проводится только через периферические вены, попытки катетеризации центральных вен недопустимы;
— перед инфузией возможно внутривенное введение 5-6 мл 25% магния сульфата либо 10 мл кормагнезина-200 в/в струйно, медленно (за 5 минут);
— «нагрузочная» доза аспирина (250-300 мг — разжевать) дается всегда, за исключением случаев, когда аспирин противопоказан;
— 1 500 000 Ед стрептокиназы разводится в 100 мл изотонического раствора хлорида натрия и вводится внутривенно за 30 минут.
Клинические признаки восстановления коронарного кровотока:
— прекращение ангинозных приступов через 30-60 минут после введения тромболитика;
— стабилизация гемодинамики;
— исчезновение признаков левожелудочковой недостаточности;
— быстрая (в течение нескольких часов) динамика ЭКГ с приближением сегмента ST к изолинии и формированием патологического зубца Q, отрицательного зубца Т (возможно внезапное увеличение степени подъема сегмента ST с последующим его быстрым снижением);
— появление реперфузионных аритмий (ускоренного идиовентрикулярного ритма, желудочковой экстрасистолии и др.);
— быстрая динамика МВ-КФК (резкое повышение ее активности на 20-40%).
Показания к проведению антикоагулянтной терапии:
— отсутствие показаний к тромболитической терапии (поздние сроки, мелкоочаговый или не-Q-инфаркт);
— невозможность проведения тромболизиса по организационным причинам;
— отсрочка тромоболизиса до госпитального этапа;
— наличие противопоказаний к тромболизису, не являющихся противопоказанием к назначению гепарина.
При наличии показаний, гепарин вводится на догоспитальном этапе (линейной бригадой) внутривенно болюсно в дозе 10000-15000 МЕ. Если в условиях стационара не проводится тромболитическая терапия, то переходят на длительную внутривенную инфузию гепарина со скоростью 1000 МЕ/час под контролем активированного частичного тромбопластинового времени. Альтернативой может, по-видимому, служить подкожное введение низкомолекулярного гепарина в «лечебной» дозе.
Введение гепарина на догоспитальном этапе не служит препятствием к проведению тромболизиса в условиях стационара.
С первых минут ИМ всем больным, при отсутствии противопоказаний, показано назначение малых доз ацетилсалициловой кислоты (аспирина), антитромбоцитарный эффект которой достигает своего максимума уже через 30 минут и своевременное начало применения которой позволяет существенно снизить летальность.
Наибольший клинический эффект может быть получен при применении ацетилсалициловой кислоты перед проведением тромболизиса.
Доза для первого приема на догоспитальном этапе составляет 160-325 мг (разжевать).
В дальнейшем, на стационарном этапе, препарат назначается 1 раз в сутки по 100-125 мг.
Уменьшение работы сердца и потребности миокарда в кислороде. Показано полноценное обезболивание и применение следующих препаратов:
1. Вазодилататоры-нитраты.
Внутривенное введение нитратов при ОИМ не только помогает купировать болевой синдром, левожелудочковую недостаточность, артериальную гипертензию, но и уменьшает размеры некроза и летальность.
Нитраты вводят капельно под постоянным контролем артериального давления и частоты сердечных сокращений с начальной скоростью 5-10 мкг/мин. с последующим увеличением скорости на 20 мкг/мин. каждые 5 минут до достижения желаемого эффекта или максимальной скорости введения — 400 мкг/мин. Обычно эффект достигается при скорости 50-100 мкг/мин.
При отсутствии дозатора, приготовленный раствор, содержащий в 1 мл 100 мкг нитрата, вводят при тщательном контроле с начальной скоростью 6-8 капель в минуту, которая при условии стабильной гемодинамики и сохранения болевого синдрома может быть постепенно увеличена вплоть до максимальной скорости — 30 капель в минуту.
Продолжительность внутривенного введения нитратов — 24 часа и более; за 2-3 часа до окончания инфузии дается первая доза нитратов перорально.
Передозировка нитратов, вызывающая падение сердечного выброса и снижение систолического артериального давления ниже 80 мм рт. ст., может приводить к ухудшению коронарной перфузии и к увеличению размеров ИМ.
2. Бета-адреноблокаторы.
Внутривенное введение бета-адреноблокаторов, как и применение нитратов, способствует купированию болевого синдрома. Ослабляя симпатические влияния на сердце, они способствуют уменьшению размеров ИМ, подавляют желудочковые аритмии, уменьшают риск разрыва миокарда и повышают таким образом выживаемость пациентов.
При отсутствии противопоказаний бета-адреноблокаторы назначаются всем больным ОИМ.
В первые 2-4 часа заболевания показано дробное внутривенное введение пропранолола (обзидана) по 1 мг в минуту каждые 3-5 минут под контролем артериального давления, частоты сердечных сокращений и ЭКГ до достижения частоты сердечных сокращений 55-60 уд./мин. или до общей дозы 10 мг.
При наличии брадикардии, признаков сердечной недостаточности, АВ-блокакды и снижении систолического артериального давления менее 100 мм рт. ст. пропранолол не назначается; при развитии указанных изменений на фоне применения препарата, его введение прекращается.
Ограничение размеров ИМ
Необходимо адекватное обезболивание, восстановление коронарного кровотока, уменьшение работы сердца и потребности миокарда в кислороде.
Этой же цели служит оксигенотерапия, показанная при ОИМ всем больным в связи с частым развитием
гипоксемии
даже при неосложненном течении заболевания.
Ингаляция увлажненного кислорода, проводящаяся, если это не причиняет чрезмерных неудобств, с помощью маски или через носовой катетер со скоростью 4-6 л/мин., целесообразна в течение первых 24-48 часов заболевания (начинается на догоспитальном этапе и продолжается в стационаре).
Лечение и профилактика осложнений ИМ
Проводятся дифференцированно в зависимости от варианта осложнений (отек легких, кардиогеннй шок, нарушения сердечного ритма и проводимости, а также затянувшийся или рецидивирующий болевой приступ).
Основные хирургические методы лечения ИМ (вопрос о выборе метода всегда решается индивидуально)
1. Аортокоронарное шунтирование (АКШ).
2. Внутрисосудистая операция (баллонная ангиопластика, стентирование).
Коронарная ангиопластика является инвазивным способом лечения ишемической болезни сердца, который направлен на восстановление суженного просвета коронарной артерии различными механическими устройствами, доставляемыми путем чрескожной пункции и катетеризации артериального русла.
Устройства и инструменты для коронарной ангиопластики:
— баллонные катетеры для проведения баллонной ангиопластики;
— атерэктомические катетеры;
— ротаблаторы для проведения мелкодисперсной ротационной абляции;
— лазер-баллоны для лазерной абляции;
— стенты для эндопротезирования коронарных артерий.
Основной метод коронарной ангиопластики — баллонная ангиопластика. Остальные методы имеют ограниченное применение по специальным показаниям.
При баллонной ангиопластике баллонный катетер проводится по артериальной системе к коронарным сосудам. Баллон устанавливается в место сужения коронарной артерии и раздувается под давлением, восстанавливая просвет сосуда.
Абсолютные противопоказания для коронарной ангиопластики:
— локализация стеноза в главном стволе левой коронарной артерии;
— наличие стеноза в коронарной артерии, снабжающей весь оставшийся живой миокард;
— отказ больного от лечения.
Относительные противопоказания:
— тяжелая дисфункция левого желудочка;
— многососудистое окклюзирующее поражение со сложным коллатеральным снабжением миокарда, сопоставимое со стволовым стенозом;
— сложное с точки зрения морфологии поражение коронарной артерии, снабжающей значительный объем миокарда;
— невозможность достичь полной или почти полной
реваскуляризации
;
— нестабильное / неконтролируемое системное или метаболическое нарушение (например, почечная недостаточность, недавний инсульт, желудочно-кишечное кровотечение, лихорадка вследствие инфекции, неконтролируемая гипертензия, тяжелые электролитные нарушения, анафилаксия).
Стентирование, как доминирующая методика эндоваскулярного лечения, является наиболее эффективным и безопасным методом лечения ОИМ. Коронарная ангиопластика со стентированием позволяет воздействовать не только на тромб, но и на атеросклеротическую бляшку, суживающую просвет венечной артерии.
Именно стентирование способно восстанавливать исходную нативную анатомию коронарной артерии, в отличие от консервативной терапии и открытой хирургии.
Показанием к выполнению стентирования у больных с ОИМ является ИМ в ходу с признаками продолжающейся ишемии в области клинико-зависимой артерии при наличии ангиографических критериев возможности выполнения процедуры.
Определяющим фактором сохранения функционального состояния миокарда и снижения летальности у пациентов с ОИМ является время от начала ангинозного приступа до начала процедуры стентирования. Для улучшения непосредственных и отдаленных результатов стентирования необходимо сокращение до минимума временного интервала, с помощью экстренной госпитализации больных с ОИМ в специализированную клинику с наличием рентгеноперационной.
Показания к проведению коронарной ангиопластики постоянно расширяются. Основной стратегический принцип — максимально отсрочить необходимость проведения АКШ.
Поскольку коронарная ангиопластика может осложниться возникновением ситуаций, требующих срочного проведения хирургической операции, то если больной отказывается от АКШ, даже если выявленные сужения дилатируемы, коронарная ангиопластика не проводится.
При ОИМ коронарная ангиопластика (КА) или АКШ проводятся при неэффективности тромболитической терапии. Предпочтение следует отдавать проведению КА. АКШ проводится только при наличии прямых противопоказаний для КА.
При выполнении КА сразу после системного тромболизиса, ее называют немедленной, а через 1-7 суток — поздней.
Проведение немедленной КА сопряжено с высоким риском осложнений. Поэтому, если это возможно, предпочтительно ее выполнение после 4-7-дневной антикоагулянтной и антиагрегантной терапии.
Целью поздней коронарной ангиопластики является устранение остаточного стеноза, профилактика реокклюзии, ускорение восстановления функции левого желудочка. При этом существенно снижается риск формирования аневризмы сердца и летальности больных ОИМ.
Аортокоронарное шунтирование — это кардиохирургическая операция, при которой создается новый путь для кровотока в обход пораженной артерии. Для этого накладывается шунт между аортой и участком артерии после сужения. В качестве шунта применяются: большая подкожная вена, внутренняя грудная артерия, лучевая артерия, синтетический протез.
Доступ к сердцу осуществляется через разрез грудной клетки, чаще — через грудину. Еще один разрез выполняется в месте, где берут шунт. После АКШ требуется достаточно длительный период реабилитации, в течение которого заживают раны и срастается грудина.
Показания к проведению АКШ в остром периоде ИМ:
— неэффективность первичной коронароангиопластики;
— окклюзия сосуда или эндопротеза после эндоваскулярных вмешательств;
— кардиогенный шок;
— наружные и внутренние разрывы сердца.
Прогноз
Около 15-20% больных ИМ погибают на догоспитальном этапе, еще 15% — в больнице.
Общая летальность при ИМ составляет 30-35%.
Большая часть больничной летальности приходится на первые двое суток, поэтому основные лечебные мероприятия проводят именно в этот период.
Контролируемые испытания показали, что восстановление перфузии в течение первых 4-6 часов ИМ способствует ограничению его размеров, улучшению локальной и общей сократимости левого желудочка, снижению частоты больничных осложнений (сердечной недостаточности,
ТЭЛА
, аритмий) и летальности. Восстановление перфузии в течение первых 1-2 часов ИМ особенно благоприятно.
Позднее восстановление перфузии также сопровождается увеличением выживаемости, что связывают с улучшением заживления миокарда и уменьшением частоты аритмий (но не ограничением размеров инфаркта).
Госпитализация
Всем больным показана экстренная госпитализация.
Профилактика
Профилактические мероприятия в острой фазе ИМ
Важнейшее профилактическое значение с первых минут от начала инфаркта имеет антитромбоцитарная и антикоагулянтная терапия. Также целесообразно применение таких препаратов, как β-блокаторы, ингибиторы АПФ, нитраты, блокаторы кальциевых каналов, глюкозо-инсулино-калиевая смесь (ГИК) и др.
Вопрос о необходимости раннего, в том числе внутривенного, назначения бета-блокаторов в острой фазе остается открытым. В настоящее время рекомендуется дождаться стабилизации состояния больного и только после этого назначить бета-блокаторы обычным способом, перорально.
Не обнаружено существенных преимуществ раннего назначения нитратов, поэтому они не рекомендованы для рутинного использования, хотя возможность их применения у отдельных пациентов с продолжающейся ишемией миокарда не исключается.
Не рекомендованы для рутинного использования (без специальных показаний) также блокаторы кальциевых каналов, сульфат магния, ГИК , лидокаин.
Напротив, ингибиторы АПФ, назначаемые с первого дня ИМ, не намного, но достоверно уменьшают раннюю летальность больных. Поэтому в руководстве ESC рекомендуется начать прием ингибиторов АПФ в первые 24 часа от начала инфаркта, если нет противопоказаний.
Вторичная профилактика – общие принципы
Около 8-10% пациентов, выживших после ИМ, в течение года после выписки из стационара переживают повторный инфаркт. Летальность постинфарктных больных гораздо выше, чем смертность в общей популяции. На сегодняшний день известен ряд профилактических мероприятий, оказывающих достоверное благоприятное влияние на прогноз и уровень выживаемости таких пациентов.
1. Всем пациентам, перенесшим инфаркт, настоятельно рекомендуется отказаться от курения. Для медикаментозной поддержки больного, который бросает курить, могут использоваться бупропион и никотинсодержащие препараты, антидепрессанты.
2. Показана достаточная и регулярная физическая активность – аэробная нагрузка умеренной интенсивности как минимум 5 раз в неделю. Для больных высокого риска рекомендованы специальные реабилитационные программы с наблюдением медработников.
3. Если индекс массы тела ≥30 кг/м2 либо окружность талии превышает 102 см у мужчин или 88 см у женщин, необходимо снижение веса. Питание постинфарктных больных должно включать регулярное употребление фруктов, овощей, рыбы, отличаться низким содержанием соли и насыщенных жиров. Целесообразным может быть увеличение потребления омега-3-полиненасыщенных жирных кислот; с этой целью можно включать в рацион жирные сорта рыбы или же принимать рыбий жир. Не следует запрещать пациенту употреблять алкоголь в умеренных количествах.
4. Если у больного имеется сахарный диабет, необходимы соответствующие мероприятия по модификации образа жизни, контролю факторов риска (артериальной гипертензии, ожирения,
дислипидемии
) и сахароснижающая фармакотерапия для поддержания уровня гликозилированного гемоглобина <6,5%.
5. В случае артериальной гипертензии необходимы мероприятия по модификации образа жизни и фармакологическая терапия для поддержания уровня АД <130/80 мм рт. ст. .
Всем пациентам, перенесшим ИМ, при отсутствии противопоказаний как можно раньше следует назначить:
1. Антитромбоцитарную и/или антикоагулянтную терапию:
— АСК 75-100 мг/сут. постоянно;
— клопидогрель 75 мг/сут. в течение 12 месяцев в дополнение к АСК независимо от стратегии лечения (IIa, C) или постоянно вместо АСК, если прием АСК противопоказан;
— если противопоказаны и АСК, и клопидогрель, рекомендованы пероральные антикоагулянты (с удержанием МНО в рамках 2-3);
— пероральные антикоагулянты (с удержанием рекомендованного МНО) специально показаны в ряде клинических ситуаций (наличие мерцательной аритмии, тромба в полости левого желудочка, механических протезов клапанов сердца);
— в случае высокого риска тромбоэмболических событий, пероральные антикоагулянты можно принимать в комбинации с низкими дозами АСК, клопидогрелем или двойной антитромбоцитарной терапией (АСК + клопидогрель).
2. β-блокаторы (независимо от уровня АД или состояния функции левого желудочка).
3. Ингибиторы АПФ (независимо от уровня АД или состояния функции левого желудочка); при непереносимости – блокаторов рецепторов ангиотензина-II.
4. Гиполипидемическую терапию:
— статины рекомендованы у всех пациентов для достижения уровня холестерина липопротеинов низкой плотности (ЛПНП) < 100 мг/дл (2,5 ммоль/л) (I, A), у пациентов высокого риска следует рассмотреть целесообразность снижения этого показателя до еще более низкого целевого уровня – < 80 мг/дл (2,0 ммоль/л);
— если уровень триглицеридов превышает 150 мг/дл (1,7 ммоль/л) и/или содержание холестерина липопротеинов высокой плотности (ЛПВП) < 40 мг/дл (1,0 ммоль/л), рекомендуются соответствующие мероприятия по модификации образа жизни;
— у пациентов, которые не переносят статины, могут использоваться фибраты и препараты омега-3-полиненасыщенных жирных кислот, особенно если уровень триглицеридов > 150 мг/дл (1,7 ммоль/л) и/или содержание холестерина ЛПВП < 40 мг/дл (1,0 ммоль/л).
5. Прививки против гриппа (I, B).
Для уменьшения риска внезапной сердечной смерти у больных с фракцией выброса ≤ 30-40% и СН ≥ II класса по NYHA (или III класса на протяжении по крайней мере 40 суток после ИМ) показана имплантация кардиовертера-дефибриллятора. Следует рассмотреть целесообразность такой тактики и у пациентов с фракцией выброса ≤ 30-35% и СН I класса по NYHA на протяжении, по крайней мере, 40 суток после ИМ.
Информация
Источники и литература
-
ACC/AHA Guideline Update for the Management of Patients With Unstable Angina and Non–ST-Segment Elevation Myocardial Infarction, 2002
-
ACC/AHA Guidelines for the Management of Patients With Unstable Angina /Non–ST-Elevation Myocardial Infarction, 2007
-
ACCF/AHA Guideline for the Management of ST-Elevation Myocardial Infarction, 2013
-
Алперт Дж., Френсис Г. Лечение инфаркта миокарда, М.: Практика, 1994
- стр. 255
-
Бабунашвили А.М., Рабкин И.X., Иванов В.А. Коронарная ангиопластика,М.: АСВ, 1996
- стр. 352
-
Байес де Луна А., Фиол-Сала М., Антман Э.М. ЭКГ при инфаркте миокарда с подъемом ST, СПб: Медицинская литература, 2009
-
Болезни сердца и сосудов. Руководство для врачей в 4 томах, под ред. Чазова Е.И., М.: Медицина, 1992
- «Хирургическое лечение ишемической болезни сердца и инфаркта миокарда» Акчурин Р. С. —
-
Гриффин Б.,Тополь Э. Кардиология (Manual of Cardiovascular Medicine), М.: Практика, 2008
-
Гурвич М.М. Заболевания сердца и сосудов. Лечебное питание, СПб:Эксмо, 2008
-
Кузьменко А.Т., Камышников В.С. Лабораторная диагностика острого инфаркта миокарда, СПб: Адукацыя i выхаванне, 2009
-
Лайбольд Г. Здоровое сердце и сосуды. Лечение и профилактика заболеваний сердечно-сосудистой системы, СПб: АСТ, Астрель, ВКТ, 2008
-
Люсов В.А., Волов Н.А., Гордеев И.Г. Инфаркт миокарда, СПб: Литтерра, 2010
-
Малышева И.С. Инфаркт. Профилактика и лечение, М.:Вектор, 2008
-
Сыркин А.Л. Инфаркт миокарда, СПб: Медицинское информационное агентство, 2006
-
Филатова М. «Жизнь после инфаркта», СПб: АСТ, Сова, 2007
-
Хубутия М.Ш., Газарян Г.А., Захаров И.В. Реперфузионная терапия в остром периоде инфаркта миокарда, СПб: ГЭОТАР-Медиа, 2010
-
Шилов А.М. Инфаркт миокарда, М.:Миклош, 2009
-
Якушин С.С. Инфаркт миокарда. Руководство, СПб: ГЭОТАР-Медиа, 2010
-
«Force on Practice Guidelines (Committee on the Management of Patients with Unstable Angina) 2002», «Journal of the American College of Cardiology» №40, 2002
-
«Myocardial infarction redefined — a consensus document of The Joint European Society of Cardiology/American College of Cardiology committee for the redefinition of myocardial infarction», «Journal of the American College of Cardiology», №36(3), 2000
-
«Дальнейшие шаги в исследовании сердечной недостаточности» Бураковский В.И., Работников В.С., Казаков Э.Н., «Грудная и сердечно-сосудистая хирургия», №7, 1991
-
«Коронарное русло, гемодинамика и сократительная функция миокарда у больных ИБС с постинфарктным кардиосклерозом в аспекте хирургического лечения» Алекян Б.Г.,автореф. дис. канд. мед. наук., М., 1980
-
«Ранние и одногодичные результаты коронарного шунтирования: связь с дислипопротеидемией» Агапов А.А., Власова Э.Е., Акчурин Р.С. и др., журнал «Кардиология», №12, 1996
-
«Факторы риска коронарного шунтирования при нестабильной стенокардии» Агапов А.А., Тарасова Л.В., Ширяев А.А., Акчурин Р.С., журнал «Кардиология», №11, 1996
Информация
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Обзор
Инфаркт миокарда (сердечный приступ) — это тяжелое неотложное состояние, при котором внезапно нарушается кровообращение сердца, обычно из-за кровяного сгустка (тромба). Недостаток притока крови к сердцу может серьезно повредить сердечную мышцу.
Позвоните по телефону скорой помощи — 03 со стационарного телефона, 112 или 911 — с мобильного, если вы подозреваете у себя или кого-либо другого инфаркт миокарда.
До приезда скорой помощи вы можете принять аспирин, если у вас нет на него аллергии. Аспирин разжижает кровь и помогает восстановить поступление крови к сердцу. Чаще аспирин выпускается в таблетках по 500 мг. Примите половину таблетки (250 мг), разжевав ее перед проглатыванием.
Лечение инфаркта миокарда зависит от степени его тяжести. С помощью лекарственных препаратов или хирургической операции можно уничтожить тромб и восстановить кровообращение сердечной мышцы, тем самым сохранить ее жизнеспособность.
Время, требующееся для восстановления после инфаркта, зависит от величины повреждения миокарда. Некоторые люди приступают к работе уже спустя несколько недель после случившегося, другим требуется несколько месяцев.
Инфаркт миокарда — это одна из самых частых причин для вызова скорой помощи. По данным официальной статистики, в России в последние годы острый инфаркт миокарда бывает у немногим более чем 150 тысяч человек в год. Чаще всего инфаркт миокарда случается у людей старше 45 лет. У мужчин вероятность возникновения инфаркта миокарда в два-три раза выше, чем у женщин.
Медицинский прогноз для человека, перенесшего инфаркт миокарда зависит от:
- его возраста — чем вы старше, тем выше вероятность испытать тяжелые осложнения;
- тяжести сердечного приступа — в особенности, какой объем сердечных мышц был поврежден во время инфаркта;
- сколько времени прошло до получения медицинской помощи — чем дольше задержка, тем хуже будет медицинский прогноз.
В целом, в результате инфаркта миокарда умирает примерно треть перенесших его людей. Чаще всего это происходит до попадания в больницу либо же в течение 28 дней после приступа. Если человек выживает в течение 28 дней после инфаркта, медицинский прогноз для него резко улучшается, и большинство таких людей выписываются и живут еще многие годы.
Симптомы инфаркта миокарда
Симптомы включают в себя:
- боль в груди: обычно сосредоточена в центре груди и может ощущаться как сдавление или сжатие грудной клетки;
- боль может распространяться (отдавать ) в другие части тела: в руки (чаще — в левую, реже болят обе руки), нижнюю челюсть, шею, спину и живот;
- одышка;
- тошнота;
- рвота;
- сильное чувство тревоги (похоже на приступ паники);
- головокружение;
- кашель;
- хрипы.
Интенсивность боли значительно различается от человека к человеку. Для многих боль настолько сильна, что они описывают её как «слона, сидящего на моей груди».
Необходимо подчеркнуть, что не все испытывают сильную боль. Часто при инфаркте боль может быть незначительной и даже ошибочно принята за несварение желудка. Именно сочетание перечисленных симптомов говорит о наличии у вас сердечного приступа, а не только сильная боль. У больных диабетом, некоторых женщин и пожилых людей инфаркт может развиваться совсем без боли. Тогда заподозрить его можно по сочетанию остальных значимых симптомов.
Если вы подозреваете у себя или другого человека инфаркт (даже, если не уверены в этом), обязательно вызовите скорую помощь, позвонив — 03 со стационарного телефона, 112 или 911 — с мобильного. Сделать это нужно при первых симптомах, как можно быстрее, не теряя времени на сомнения и раздумья. Лучше врачи исключат инфаркт миокарда и скажут, что вы ошиблись, чем приедут тогда, когда время для спасения жизни будет уже упущено.
Совет для людей со стенокардией
Стенокардия — это заболевание, связанное с нарушением поступления к сердца крови, богатой кислородом. Проявления стенокардии во многом похожи на инфаркт миокарда, но обычно проходят в течение нескольких минут. Тем не менее, иногда у людей со стенокардией может случиться инфаркт миокарда. Важно уметь различать симптомы стенокардии и инфаркта миокарда.
Симптомы стенокардии, как правило, полностью снимает прием лекарственных препаратов. При инфаркте миокарда боль в груди или одышка сохраняются, даже после применения привычных лекарств, которые ранее приносили облегчение.
Если у вас стенокардия, вам могли быть назначены препараты, быстро облегчающие симптомы, например, нитроглицерин. Если первая доза препарата не действует, примите еще одну через пять минут и третью дозу, спустя еще пять минут. Если боль или другие симптомы сохраняется в течение 15 минут, несмотря на три принятые дозы нитроглицерина, вызовите скорую помощь (03 со стационарного телефона, 112 или 911 — с мобильного).
В ожидании бригады скорой помощи
До приезда скорой помощи вы можете принять аспирин, если у вас нет на него аллергии. Аспирин разжижает кровь и помогает восстановить поступление крови к сердцу. Чаще аспирин выпускается в таблетках по 500 мг. Примите половину таблетки (250 мг), разжевав ее перед проглатыванием.
В некоторых случаях инфаркт миокарда может осложниться внезапной остановкой сердца. При остановке сердца человек:
- возможно не дышит;
- не двигается;
- не реагирует на прикосновения или попытки заговорить с ним.
Если вы предполагаете, что у кого-то случилась остановка сердца, вам следует выполнить непрямой массаж сердца, так как он помогает восстановить работу сердца.
Чтобы провести непрямой массаж сердца, положите свою ладонь на центр груди, между сосков. Положите вторую ладонь поверх первой и сцепите пальцы. Используя вес тела (а не только ваших рук), давите прямо вниз (на 4-5 см) на его грудь. Стремитесь делать массаж сердца с частотой 100 надавливаний в минуту.
Эти рекомендации применимы только для взрослых. Прочитайте подробнее о том, как оказать первую помощь ребенку.
Причины инфаркта миокарда
Сердце, как и другие органы нашего тела, нуждается в непрерывном поступлении насыщенной кислородом крови. Если приток крови к сердцу внезапно прерывается, сердечная мышца повреждается и может погибнуть.
Если вовремя не начато лечение, в мышце сердца (миокарде) развиваются необратимые повреждения (некроз — гибель тканей). Если погибла значительная часть миокарда, сердце перестает биться, что приводит к смерти.
Ишемическая болезнь сердца (ИБС)
Ишемическая болезнь сердца (ИБС) — это самая распространенная причина инфаркта миокарда. ИБС — это заболевание, при котором коронарные артерии (крупные кровеносные сосуды, доставляющие кровь к сердцу) забиваются отложениями холестерина. Эти отложения называются атеросклеротическими бляшками.
Во время инфаркта миокарда оболочка одной из бляшек разрывается, что приводит к образованию кровяного сгустка (тромба) в месте разрыва. Тромб может затем перекрыть поступление крови, текущей по коронарной артерии к сердцу, провоцируя инфаркт миокарда. Ниже описаны факторы риска ишемической болезни сердца, многие из которых взаимосвязаны.
Курение. Токсины, содержащиеся в табачном дыму, сужают и повреждают коронарные артерии. Это делает курильщиков более уязвимыми для ИБС. По сравнению с некурящими, у людей, выкуривающих 20 и более сигарет в день, риск развития ИБС и инфаркта миокарда на 60-90% больше. Даже малые дозы табака могут быть опасны. Выкуривая всего лишь одну сигарету в день, вы тем не менее имеете на 30% больше шансов развития ИБС по сравнению с некурящими. Прочитайте подробнее о том, как бросить курить.
Питание. Если вы едите пищу, богатую насыщенными жирами, уровень холестерина в крови будет расти. Это приводит к увеличению риска ИБС и инфаркта миокарда. Некоторые продукты, например, жирная рыба, могут снижать уровень холестерина в крови. Прочитайте подробнее о том, как правильно питаться.
Частое повышение кровяного давления выше нормы (гипертензия), может приводить к ослаблению коронарных артерий, делая их уязвимыми для ИБС. Чем выше кровяное давление, тем больше риск ИБС и инфаркта миокарда.
Сахарный диабет. Повышенный уровень глюкозы в крови, связанный с наличием диабета 1 типа или 2 типа может вызвать повреждение коронарных артерий. Установлено, что люди с сахарным диабетом, заболевают ИБС в 2-5 раз чаще, чем остальные.
Полнота и ожирение не ведут к прямому повышению риска ИБС, но приводят к развитию связанных с ними факторов риска ИБС. В частности, полные и страдающие ожирением люди:
- имеют повышенный риск развития гипертонии;
- предрасположены к наличию повышенного уровня холестерина в крови в результате потребления продуктов, богатых жирами;
- имеют повышенный риск развития сахарного диабета 2 типа.
Недостаток физической активности не связан напрямую с повышенным риском ИБС и инфаркта миокарда. Однако, малоподвижный образ жизни способствует появлению лишнего веса и ожирения, а также — гипертонии.
Избыточное потребление алкоголя способствует повышению кровяного давления (гипертензии) и росту уровня холестерина в крови, повышая риск возникновения ИБС. Также много пьющие люди склонны к нездоровому образу жизни, в том числе — курению, потреблению жирной пищи и недостаточной физической активности.
Возраст и пол. Чем старше вы становитесь, тем выше вероятность развития ИБС. Вероятность инфаркта миокарда у мужчин в два-три раза выше, чем у женщин. Для объяснения этого явления был предложен ряд медицинских обоснований:
- мужчины чаще злоупотребляют алкоголем;
- мужчины чаще страдают избыточным весом (хотя количество людей с ожирением обоих полов примерно одинаково);
- возможно, мужчины менее эффективно справляются со стрессом, чем женщины, и повышенный уровень стресса может воздействовать на их состояние здоровья.
Наследственная предрасположенность. Если у вас имеются родственники первого уровня (родители, братья или сестры) с сердечнососудистыми заболеваниями, такими как стенокардия, инфаркт миокарда или инсульт, то у вас в 2 раза увеличивается вероятность развития таких же заболеваний по сравнению с другими людьми.
Загрязнение воздуха. Недавние исследования обнаружили, что воздействие загрязненного воздуха (в особенностями выхлопных газов), повышает риск развития ИБС и инфаркта миокарда. В исследовании, проведенном в 2011 году, установлено, 1 из 13 случаев инфаркта связан с загрязнением воздуха.
Менее распространенные причины инфаркта
Злоупотребление наркотиками. Такие наркотики как кокаин, амфетамин, крэк и метамфетамин могут вызвать сужение коронарных артерий, ограничение поступления крови к сердцу и инфаркт миокарда. Одна из самых частых причин внезапной смерти молодых людей — инфаркт миокарда, вызванный употреблением кокаина.
Недостаток кислорода в крови (гипоксия). При снижении содержания кислорода в крови, из-за отравления угарным газом или плохой работы легких, к сердцу поступает кровь с пониженным содержанием кислорода. В результате это может привести к повреждению сердечной мышцы — инфаркту миокарда.
Аневризма — это выпячивание стенки кровеносного сосуда. Если стенка кровеносного сосуда истончается до определенной степени, она больше не может выдерживать давление крови, текущей по этому сосуду, и разрывается.
Иногда аневризма может развиться в коронарной артерии, хотя это намного менее распространено, чем другие виды аневризмы. Если разорвется аневризма коронарной артерии, поступление крови к сердцу прекратится, что вызовет инфаркт миокарда.
Диагностика инфаркта миокарда
При подозрении на инфаркт миокарда необходима немедленная госпитализация в больницу, в отделение реанимации и интенсивной терапии, где будет проведена диагностика и начато лечение.
Электрокардиография — это важный метод диагностики инфаркта миокарда. ЭКГ записывает врач или фельдшер скорой помощи, приехавшей к вам по вызову, а затем, в случае госпитализации, повторяют в больнице. ЭКГ измеряет электрическую активность вашего сердца. Каждый раз, когда сердце сокращается, оно вырабатывает слабые электрические импульсы. Аппарат для снятия электрокардиограммы записывает эти импульсы на бумагу, позволяя врачу увидеть, насколько хорошо функционирует ваше сердце.
ЭКГ — безболезненный метод, занимающий не более 5 минут. Во время процедуры электроды (плоские металлические диски) прислоняют к вашим рукам, ногам и грудной клетке. Провода от электродов идут к аппарату ЭКГ, записывающему электрические импульсы. Существует две причины, по которым проведение ЭКГ так важно:
- ЭКГ помогает подтвердить диагноз инфаркт миокарда;
- ЭКГ помогает определить, какой у вас вид инфаркта миокарда, что необходимо для определения дальнейшей тактики лечения.
Диагностика вида инфаркта миокарда
Тип инфаркта миокарда можно определить с помощью такого показателя электрокардиограммы как сегмент ST. Сегмент ST — характеризует состояние сердечной мышцы и уровень её повреждения. Чем выше сегмент ST, тем больше вероятный объем повреждения.
Острый коронарный синдром (ОКС) возникает при нарушении коронарного кровообращения (кровотока в сердечной мышце). Инфаркт миокарда — это один из видов острого коронарного синдрома. Существует три основных вида ОКС:
- инфаркт миокарда с подъемом сегмента ST (ИМП ST);
- инфаркт миокарда без подъема сегмента ST (ИМБП ST);
- нестабильная стенокардия.
Инфаркт миокарда с подъемом сегмента ST (ИМП ST) — это самый серьезный вид инфаркта миокарда. При этом виде инфаркта миокарда продолжительное нарушение поступления крови вследствие полной закупорки коронарной артерии может привести к повреждению обширной области сердца. ИМП ST — это то, о чем в первую очередь подумают люди, когда они услышат об инфаркте миокарда.
Инфаркт миокарда без подъема сегмента ST (ИМБП ST) может быть менее тяжелым по сравнению с ИМП ST, так как поступление крови к сердцу заблокировано лишь частично. В результате, поврежденной оказывается меньшая область сердца.
Нестабильная стенокардия — это вид острого коронарного синдрома, при котором тоже нарушается кровоснабжение сердца, но необратимое повреждение миокарда (некроз) развиться не успевает. Нестабильная стенокардия может в любой момент перейти в инфаркт миокарда, поэтому рассматривается как неотложное медицинское состояние. При нестабильной стенокардии сердечная мышца сохраняет свою функцию.
Другие виды обследования
Для оценки состояния вашего сердца и проверки наличия возможных осложнений могут быть использованы дополнительные виды обследования. Тем не менее, так как инфаркт миокарда — это неотложное состояние, дополнительные виды обследования обычно проводятся тогда, когда первоначальное лечение уже началось и ваше состояние стабилизировалось.
Анализ крови. Повреждение сердца в результате инфаркта вызывает повышение в крови уровня особых белков — ферментов. Ферменты — это специфические белковые соединения, регулирующие химические процессы, происходящие в вашем организме.
При подозрении на инфаркт миокарда у вас возьмут анализ крови и оценят уровень ферментов — кардиомаркеров, которые выделяются в кровь при повреждении миокарда. Уровень белков будут измерять повторно, в течении нескольких дней. Это позволит оценить степень повреждения сердца и проследить за эффектом от лечения.
Рентген грудной клетки может оказаться полезным, если диагноз инфаркт миокарда остается под вопросом, и имеются другие возможные причины ваших симптомов, например, скоплением воздуха между стенкой грудной клетки и легкими (пневмоторакс). Рентген грудной клетки также позволяет провести диагностику осложнений инфаркта миокарда, таких как скопление жидкости в легких (отек легких).
Эхокардиография — вид ультразвукового обследования, использующего звуковые волны для построения изображения тканей и сосудов сердца. Данный метод может использоваться, чтобы точно установить, какие области сердца были повреждены и как эти повреждения повлияли на работу сердца.
Ангиография коронарных артерий помогает найти место закупорки или сужения коронарных артерий, если оно имеется. Во время процедуры в кровяной сосуд предплечья или бедра вводится тонкая трубка, или катетер. Катетер направляется в коронарные артерии под контролем рентгеновских лучей.
Специальная жидкость — контрастное вещество, поступает через катетер. Эта жидкость хорошо различима на рентгеновских снимках. Анализ того, как эта жидкость проходит по сосудам, снабжающим сердце кровью, помогает выявить все закупоренные или суженные участки сосудов. Коронароангиографию часто проводят непосредственно перед хирургической операцией, потому что ее результаты помогают верно спланировать действия хирурга.
Лечение инфаркта миокарда
Инфаркт миокардаявляется неотложным медицинским состоянием. Позвоните по телефону скорой помощи — 03 со стационарного телефона, 112 или 911 — с мобильного, если вы подозреваете, что у вас или кого-то другого инфаркт миокарда.
До приезда скорой помощи вы можете принять аспирин, если у вас нет на него аллергии. Аспирин разжижает кровь и помогает восстановить поступление крови к сердцу. Чаще аспирин выпускается в таблетках по 500 мг. Примите половину таблетки (250 мг), разжевав ее перед проглатыванием.
Лечение инфаркта миокарда зависит от степени его тяжести. Имеется два основных метода лечения самой тяжелой формы инфаркта — инфаркта миокарда с подъемом сегмента ST (ИМП ST):
- использование комбинации лекарственных препаратов для растворения тромба и восстановления кровотока в сердечной мышце (это называется тромболизис);
- хирургическая операция по расширению коронарной артерии, для того чтобы возобновить приток крови к сердцу; обычно для этого проводится коронарная ангиопластика.
Ангиопластика или тромболизис?
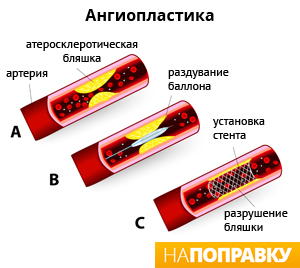
Тем не менее, ангиопластика коронарных артерий — это очень сложный вид хирургического лечения, для проведения которого необходимы квалифицированные специалисты и особое оборудование. Как правило, ангиопластика проводится на базе центров сердечно-сосудистой хирургии (кардиохирургии), которые есть далеко не во всех больницах. Если нет возможности доставить пациента с инфарктом в такую больницу в течение 150 минут, в качестве альтернативы используют тромболизис.
Если результаты ЭКГ показывают, что у вас «менее серьезный» вид инфаркта — инфаркт миокарда без подъема сегмента ST (ИМБП ST) или нестабильная стенокардия, тогда обычно рекомендуются препараты, понижающие свертываемость крови, включая аспирин.
В некоторых случаях, при инфаркте миокарда без подъема сегмента ST или нестабильной стенокардии после первоначального лечения такими препаратами может быть рекомендовано дальнейшее лечение с помощью коронарной ангиопластики или аортокоронарного шунтирования (смотрите ниже).
Коронарная ангиопластика. Во время коронарной ангиопластики в крупную артерию в паху или на руке вводится тонкая трубка, или катетер с раздувающимся баллоном на конце. До места сужения коронарной артерии катетер проводится под контролем рентгеновских лучей. На месте сужения сосуда баллон раздувается, расширяя просвет артерии. Внутрь сосуда обычно устанавливается стент — гибкая металлическая сетка, не дающая артерии сузиться.
Тромболизис — это внутривенное введение лекарственного препарата, называемого тромболитиком. Цель тромболизиса — это разрушение фибрина. Фибрин — плотный белок, который формирует кровяной сгусток, создавая своего рода сетку волокон — основу тромба.
Для лечения инфаркта миокарда используются тромболитики: ретеплазу, альтеплазу и стрептокиназу. Также вам может быть прописана комбинация препаратов, разжижающих кровь, таких как аспирин в низких дозах, гепарин, фондапаринукс, эноксапарин, клопидогрел, прасугрел или тикагрелор, для профилактики повторного образования тромбов.
Если у вас аллергия на аспирин, могут быть использованы такие альтернативы как клопидогрел, прасугрел или тикагрелор. Также вам могут прописать дополнительные препараты — ингибиторы гликопротеина IIb/IIIa, в случае если считается, что имеется повышенный риск повторного инфаркта в ближайшем будущем. Ингибиторы гликопротеина IIb/IIIa не разрушают тромбы,, но предотвращают их рост. Таким образом, они являются методом профилактики повторных сердечных приступов.
Аортокоронарное шунтирование
Иногда техническая возможность проведения коронарной ангиопластики отсутствует из-за особой анатомии ваших артерий. Это может быть в случае, если количество суженых или закупоренных сосудов слишком велико или, если имеется много ответвлений от ваших артерий, которые также закупорены.
Альтернативой ангиопластике в подобной ситуации является проведение аортокоронарного шунтирования (АКШ). Для проведения АКШ выделяют отрезок кровеносного сосуда из другой части тела, обычно из ноги или грудной клетки, для использования в качестве шунта (трансплантанта). Шунты устанавливают вместо закупоренных или суженных артерий. Хирург присоединяет новый кровяной сосуд выше и ниже заменяемого участка артерии.
Осложнения инфаркта миокарда
Потенциальные осложнения, возникающие в результате инфаркта миокарда могут широко варьировать от легких до угрожающих жизни. Многие люди внезапно умирают от осложнений инфаркта миокарда, не успев добраться до больницы.
Мелкоочаговый инфаркт миокарда редко сопровождается осложнениями (однако, также являющийся очень тяжелым состоянием). Крупноочаговый инфаркт миокарда связан с высоким риском осложнений и требует серьезного лечения.
Осложнения инфаркта миокарда могут быть опасными для жизни, это:
- кардиогенный шок — быстро развивающееся состояние, при котором повреждённое сердце не способно полноценно сокращаться и нагнетать кровь в кровеносные сосуды, что сопровождается резким падением давления и нарушением кровообращения в жизненно важных органах;
- разрыв сердца — разрыв сердечных мышц, стенок или клапанов;
- аритмия — нарушение нормального ритма и частоты сердечных сокращений, что в тяжёлых случаях приводит к остановке сердца.
Аритмия — это нарушение ритма сердечных сокращений: учащение (тахикардия), урежение (брадикардия) или неритмичное сердцебиение (например, мерцательная аритмия).
Повреждённые во время инфаркта мышцы сердца неправильно проводят электрические импульсы, которые необходимы для правильной работы сердца, что становится причиной аритмии. Некоторые виды аритмии, например, тахикардия, — относительно безопасны и вызывают такие симптомы как:
- сильное сердцебиение (сердце как будто выскакивает из груди);
- боль в груди;
- головокружение;
- предобморочное состояние;
- слабость (усталость);
- одышка.
Другие виды аритмии могут угрожать вашей жизни:
- полная поперечная блокада, при которой электрические импульсы не способны проходить от одного конца сердца до другого, так что сердце теряет способность нормально перекачивать кровь;
- желудочковая аритмия, при которой сердце начинает работать всё быстрее и быстрее, а затем, сократившись, останавливается.
Опасные для жизни виды аритмии являются одной из основных причин смерти в течение 24 часов после инфаркта. Однако, выживаемость пациентов с аритмией значительно повысилась с изобретением автоматического наружного дефибриллятора (АНД) — переносного электронного устройства, посылающего электрические разряды к сердцу и восстанавливающего нормальный ритм сокращений.
Обычно легкие аритмии проходят под действием лекарственных препаратов, например, бета-блокаторов. При более тяжелых аритмиях, вызывающих повторяющиеся и продолжительные симптомы, может потребоваться имплантация электрокардиостимулятора (пейсмейкера).
Электрокардиостимулятор — это электронный прибор для регуляции сердечного ритма. Его имплантируют в грудную клетку во время хирургической операции.
При сердечной недостаточности сердце неспособно эффективно прокачивать кровь по всему организму. Она может развиться после инфаркта миокарда, если мышцы сердца значительно повреждены. Обычно она затрагивает левую половину сердца (левый желудочек). Основные симптомы сердечной недостаточности:
- одышка;
- слабость;
- отеки рук и ног вследствие застоя крови. Сердечная недостаточность лечится с помощью лекарственных средств, реже применяют хирургическое лечение. Читайте подробнее здесь.
Кардиогенный шок похож на сердечную недостаточность, но является более тяжелым осложнением инфаркта миокарда. Он развивается внезапно, в тех случаях, когда повреждённое сердце не способно эффективно нагнетать кровь в сосуды и снабжать ею жизненно важные органы.
Основные симптомы кардиогенного шока:
- спутанность сознания;
- холодные руки и ноги;
- уменьшение количества мочи или полное отсутствие мочеиспускания;
- учащение сердцебиения и дыхания;
- бледность кожи.
Кардиогенный шок лечат с помощью вазопрессоров. Это тип лекарств, которые сокращают сосуды, что приводит к повышению кровяного давления и улучшению циркуляции крови. Кроме того, могут использоваться препараты, разжижающие кровь и облегчающие её перекачивание по организму.
Когда состояние больного кардиогенным шоком стабилизировано, может понадобиться хирургическая операция для улучшения насосной функции сердца. Один из вариантов — имплантировать маленький аппарат — насос, это называется внутриаортальной баллонной контрпульсацией. Такая операция помогает сердцу нагнетать кровь в сосуды.
Другой вариант лечения — проведение аортокоронарного шунтирования (установка шунта из сосуда, взятого из другой части вашего тела, для обхода закупоренного участка).
Разрыв сердца — это тяжелое и относительно распространенное осложнение инфаркта миокарда, возникающее приблизительно в одном из десяти случаев. Разрыв сердца происходит, когда разрываются мышцы, перегородки или клапаны сердца. Разрыв может произойти, если сердце значительно повреждено во время инфаркта миокарда. Обычно он случается в период от одного до пяти дней после инфаркта миокарда.
Симптомы такие же, как и при кардиогенном шоке. Обычно для устранения полученного повреждения необходима операция на открытом сердце. Медицинский прогноз для пациентов с разрывом сердца неблагоприятен и предположительно половина людей умирает в течение пяти дней после того, как они перенесли разрыв сердца.
Реабилитация после инфаркта
Большинство людей могут вернуться на работу после перенесенного инфаркта миокарда, но сроки реабилитации зависят от индивидуальных особенностей организма, состояния сердца и характера работы, которую вы выполняете. Некоторым требуется всего лишь две недели, чтобы вернуться на работу. Другим людям на восстановление понадобится несколько месяцев. Очень важно не форсировать реабилитацию, а восстанавливать силы постепенно.
Во время реабилитации вам будут оказывать помощь разные медицинские работники, в том числе:
- медицинские сестры;
- физиотерапевты;
- диетологи;
- фармакологи;
- врачи лечебной физкультуры.
Эти специалисты окажут вам лечебную и психологическую поддержку, чтобы обеспечить правильную организацию и безопасность процесса восстановления. Реабилитация начинается уже в больнице, где за вашим состоянием будут внимательно наблюдать и смогут оценить, в чем вы будете нуждаться в дальнейшем. После выписки вы можете продолжить процесс восстановления в домашних условиях. Существует две важные цели реабилитационного процесса:
- Снижение риска нового инфаркта миокарда — за счет сочетания коррекции образа жизни, например, перехода на здоровое питание, и приема лекарств, таких как статины (снижающие уровень холестерина в крови).
- Постепенное восстановление вашей физической формы, чтобы вы могли возобновить нормальную жизнедеятельность (сердечная реабилитация).
Сердечная реабилитация
Программа сердечной реабилитации начинается в больнице. Врач, занимающийся вашей реабилитацией, подробно расскажет вам о:
- состоянии здоровья и ваших возможностях после инфаркта;
- пройденном лечении;
- препаратах, которые вам будет необходимо принимать после выписки;
- возможных причинах вашего инфаркта;
- необходимых изменениях образа жизни, чтобы избежать риска повторного приступа.
При возвращении домой обычно рекомендуют отдыхать и выполнять только легкие упражнения, такие как подъем и спуск по лестнице два-три раза в день или короткая прогулка. В течение нескольких недель, изо дня в день, постепенно увеличивайте уровень своей нагрузки. То, как быстро вы сможете увеличивать уровень нагрузки, будет зависеть от состояния сердца и общего состояния вашего здоровья. Врач может дать вам разъяснения по предлагаемой программе повышения уровня вашей активности.
Лечащий врач в поликлинике может назначить вам курс лечебной физкультуры. Это комплекс специальных физических упражнений, которые регулярно выполняются под контролем врача-физиотерапевта. Лечебная физкультура является важной частью реабилитации и помогает восстановить работу сердца.
Виды упражнений могут быть разными в зависимости от конкретной программы, но они должны быть в основном аэробными. Аэробные упражнения разработаны для усиления сердечных мышц, улучшения кровообращения и уменьшения кровяного давления. Примерами аэробных упражнений являются занятия на велотренажере, ходьба на беговой дорожке, плавание.
Возвращение на работу
Большинство людей могут вернуться к работе после инфаркта миокарда, но как быстро — будет зависеть от состояния здоровья и вашего сердца, а также характера работы, которую вы выполняете. Если работа не связана с тяжелой нагрузкой, например, работа в офисе, вы, возможно, будете способны вернуться на работу всего через две недели.
Однако, если ваша работа требует применения физической силы, или ваше сердце было значительно повреждено, то может пройти несколько месяцев, прежде чем вы вернетесь на работу. Более конкретный трудовой прогноз вам даст лечащий врач.
Секс после инфаркта
Согласно зарубежным исследованиям, занятия сексом не будут представлять угрозы вашему здоровью, как только вы сможете без боли и одышки подниматься на второй этаж по лестнице. Обычно такого состояния можно достичь примерно через 4 недели после инфаркта миокарда. Тогда занятия сексом не повысят риск нового инфаркта. Прочитайте подробнее о сексе после инфаркта миокарда.
Приблизительно у одного из трех мужчин, перенесших инфаркт миокарда, имеется нарушение потенции, которое может создавать трудности для занятий сексом. Чаще всего это является результатом чувства тревоги и эмоционального стресса, связанных с перенесенным инфарктом миокарда. Реже нарушение потенции возникает как побочный эффект приема бета-блокаторов.
Если вы испытываете нарушение потенции, обратитесь к врачу, который порекомендует вам подходящее лечение. Например, вам могут прописать препарат, стимулирующий приток крови к половому члену и облегчающий возникновение эрекции.
Вождение автомобиля после инфаркта
Весьма рекомендуется воздержаться от вождения автомобиля в течение как минимум 4 недель после инфаркта миокарда. После этого вы можете сесть за руль, если только у вас не будет других заболеваний или осложнений, при которых противопоказано вождение автомобиля.
Депрессия после инфаркта
Инфаркт является пугающим и травмирующим событием, после которого часто появляется чувство тревоги. У многих людей перенесенный эмоциональный стресс вызывает подавленное состояние и уныние в первые недели после выписки. Если состояние депрессии не проходит, обратитесь к своему врачу, возможно вам потребуется дополнительное лечение, чтобы избавиться от нервного напряжения. Депрессия ухудшает процесс восстановления после инфаркта.
Снижение риска повторного инфаркта миокарда
Снижение риска повторного инфаркта миокарда включает в себя коррекцию образа жизни и долгосрочное лечение различными препаратами.
Рекомендуется съедать от двух до четырех порций жирной рыбы в неделю. Жирная рыба содержит жирную кислоту омега-3. Омега-3 способствует снижению уровня холестерина в крови. Источники омега-3 кислот:
- сельдь;
- сардины;
- скумбрия;
- лосось;
- форель;
- тунец.
Вместо рыбы врач может порекомендовать вам пищевые добавки или лекарственные препараты, содержащие омега-3 кислоты. Никогда не принимайте пищевые добавки, не проконсультировавшись со своим лечащим врачом. Некоторые добавки, такие как бета-каротин, могут быть потенциально вредными для вашего организма.
Также вам рекомендуется придерживаться средиземноморской диеты: есть больше хлеба, фруктов, овощей, рыбы, и меньше мяса. Замените сливочное масло и сыр на продукты, содержащие в своей основе растительное масло, например, оливковое масло.
Если вы курите, вам строго рекомендуется бросить курить как можно скорее.
Если вы принимаете алкоголь, не превышайте рекомендованных дневных норм потребления. Мужчинам рекомендуется не употреблять более 2-4 порций алкоголя в день регулярно, а женщинам — более 2-3. Под регулярным употреблением понимается каждый день или большую часть дней недели. 1 порция алкоголя примерно соответствует рюмке водки, половине бокала вина или половине кружки пива.
Регулярное превышение рекомендованных норм потребления алкоголя приведет к повышению у вас кровяного давления и уровня холестерина, следовательно и риска повторного инфаркта миокарда. Избегайте пьянства (потребления более трех порций алкоголя в течение одного-двух часов). Это вызывает резкое и значительное повышение кровяного давления, что может оказаться опасным.
В исследованиях доказано, что люди, злоупотребляющие алкоголем после инфаркта в 2 раза чаще умирают от повторного инфаркта или инсульта. Если человек, перенёсший инфаркт бросил пить, риск смерти снижается.
Людям с лишним весом или ожирением рекомендуется похудеть и поддерживать вес в норме с помощью низкокалорийной диеты и физических упражнений.
Как только вы полностью восстановитесь после инфаркта (смотрите выше в разделе о сердечной реабилитации, сколько времени это обычно занимает), вам будут необходимы регулярные физические нагрузки. Взрослым следует тратить на аэробную нагрузку умеренной интенсивности (например, катание на велосипеде или быструю ходьбу) не менее 150 минут (2,5 часа) каждую неделю.
Уровень нагрузки должен быть таковым, чтобы вы слегка запыхались. Если вам трудно довести уровень своей нагрузки до 150 минут в неделю, начните с комфортного для вас уровня нагрузки (например, 5-10 минут легких упражнений в день). По мере улучшения физической формы вы сможете повысить интенсивность своих занятий до должного уровня.
Лекарственная профилактика инфаркта миокарда
В настоящее время для сокращения риска инфаркта миокарда широко применяются четыре вида лекарственных средств:
- ингибиторы ангиотензин-превращающего фермента (иАПФ);
- антиагреганты;
- бета-блокаторы;
- статины.
Ингибиторы АПФ часто используются для снижения кровяного давления. Ингибиторы АПФ уменьшают активность гормона, влияющего на давление. В результате происходит расширение сосудов, уменьшается количество жидкости в организме и снижается давление.
Ингибиторы АПФ противопоказаны людям с некоторыми заболеваниями почек, поэтому врач может назначить вам анализы крови и мочи, чтобы убедиться в отсутствии противопоказаний. При длительном приёме иАПФ, анализы крови и мочи нужно повторять ежегодно. Возможные побочные эффекты ингибиторов АПФ:
- головокружение;
- слабость или усталость;
- головные боли;
- устойчивый, сухой кашель.
Наиболее стойким эффектом является кашель, остальные нежелательные реакции обычно проходят за считанные дни. При приеме ингибиторов АПФ совместно с другими лекарственными препаратами, включая безрецептурные препараты, могут возникнуть непредсказуемые побочные эффекты.
Таким образом, не принимайте никаких препаратов в комбинации с назначенными ингибиторами ИПФ, не проконсультировавшись с врачом. Обычно рекомендуется начать прием ингибиторов АПФ сразу же после инфаркта и, в большинстве случаев, продолжать прием этих препаратов всю жизнь. В случае индивидуальной непереносимости ингибиторов АПФ, может быть предписан альтернативный вид препаратов — блокаторы ангиотензиновых рецепторов.
Антиагреганты и антикоагулянты — это группы препаратов, предназначенные для предупреждения тромбообразования. Они действуют, снижая «липкость» тромбоцитов и разрушая основу тромба из нитей фибрина (белка крови). Тромбоциты — это очень маленькие клеточные образования в крови, которые способствуют образованию в ней тромбов.
Чаще всего, перенёсшим инфаркт людям, для разжижения крови назначается аспирин (который часто используется в качестве болеутоляющего при других заболеваниях). Вам могут также прописать прием дополнительных антиагрегантов, таких как клопидогрел или тикагрелор. Эти препараты также используются при аллергии на аспирин.
Возможные побочные эффекты:
- понос;
- кровоподтеки или кровотечение;
- одышка;
- боль в животе;
- несварение желудка;
- изжога.
Аналогично ингибиторам АПФ, лечение антиагрегантами начинается сразу после инфаркта миокарда. Срок, на который назначаются антиагреганты, варьирует от 4 недель до 12 месяцев, и зависит от вида перенесенного вами инфаркта миокарда и остального лечения, которое вы получаете.
Обычно рекомендуется применять аспирин пожизненно. Если вы испытываете причиняющие вам беспокойство побочные эффекты аспирина, проконсультируйтесь со своим врачом, но не прекращайте прием аспирина, так как резкая отмена препарата повышает риск развития повторного инфаркта миокарда.
Иногда вам также могут прописать прием варфарина. Обычно его выписывают в случае нерегулярного сердечного ритма (мерцательной аритмии) или тяжелого повреждения сердца.
Обширные кровотечения — это самый опасный побочный эффект от приема варфарина. Немедленно обратитесь к врачу и срочно сдайте анализ крови, если вы испытываете какие-либо из следующих побочных эффектов:
- появление крови в моче или кале;
- фекалии черного цвета;
- сильные кровоподтеки;
- длительные кровотечения из носа (дольше 10 минут);
- наличие крови в вашей рвоте;
- появление крови при кашле;
- необычные головные боли;
- у женщин, тяжелые или обильные менструации или любое другое вагинальное кровотечение.
Если вы принимаете препараты от тромбообразования, вызовите скорую помощь, если:
- произошла серьезная травма (несчастный случай);
- вы испытали сильный удар по голове;
- не можете остановить возникшее кровотечение.
Бета-блокаторы — это вид препаратов, применяемых для защиты сердца от дальнейшего повреждения после инфаркта миокарда. Они способствуют расслаблению сердечных мышц, в результате чего сердце бьется медленнее и снижается кровяное давление, что приводит к снижению нагрузки на сердце.
Обычно рекомендуется начать применение бета-блокаторов после стабилизации вашего состояния и продолжать прием бессрочно. Довольно распространенные побочные эффекты бета-блокаторов включают:
- усталость;
- снижение температуры кистей рук и стоп;
- медленное сердцебиение;
- понос;
- тошнота.
Менее распространенные побочные эффекты включают:
- нарушение сна;
- ночные кошмары;
- неспособность достигать или поддерживать эрекцию (нарушение потенции или «импотенция»).
Бета-блокаторы могут также взаимодействовать с другими лекарствами, вызывая негативные побочные эффекты. Поэтому проконсультируйтесь с врачом или фармацевтов перед приемом других препаратов, включая безрецептурные препараты, одновременно с бета-блокаторами.
Статины — это группа препаратов, которые снижают уровень холестерина в крови. Статины назначают, чтобы предупредить закупорку артерий холестериновыми бляшками и снизить риск повторного инфаркта.
Статины блокируют действие в печени фермента, называемого ГМГ-КоА-редуктаза, который задействован в выработке холестерина. Статины иногда имеют незначительные побочные эффекты, в том числе:
- запор;
- понос;
- головные боли;
- боль в животе.
Иногда статины могут вызвать мышечные боли, слабость и повышенную чувствительность. Обратитесь к врачу, если вы испытываете такие симптомы, возможно, вам требуется коррекция дозы препаратов. Как правило, статины рекомендуется принимать бессрочно.
Профилактика инфаркта миокарда
Коррекция образа жизни — это самый эффективный способ предупредить инфаркт миокарда (или возникновение повторного инфаркта миокарда).
Для предупреждения инфаркта миокарда (также как и инсульта) следует соблюдать три основных правила:
- придерживаться сбалансированного питания;
- избегать курения;
- следить на уровнем артериального давления.
Потребление нездоровой пищи с высоким содержанием жиров усиливает атеросклероз (уплотнение стенок артерий) и повышает риск инфаркта миокарда. Продолжение потребления жирных продуктов приведет к росту атеросклеротических бляшек на стенках артерий, потому что жирная пища содержит холестерин. Выделяют два основных вида холестерина:
- Липопротеин низкой плотности (ЛПНП) — состоит в основном из жиров, с маленьким количеством белка. Данный вид холестерина может закупоривать артерии, так что его часто называют «плохим холестерином».
- Липопротеин высокой плотности (ЛПВП) — состоит главным образом из белка, с небольшим количеством жиров. Этот вид способен сокращать отложения холестерина в артериях, так что его часто называют «хорошим холестерином».
Имеется также два вида жиров, насыщенные и ненасыщенные. Избегайте продуктов, содержащих много насыщенных жиров, поскольку они увеличивают уровень плохого холестерина в крови. Продукты, богатые насыщенными жирами:
- мясной пирог;
- колбаса и жирное мясо;
- сливочное масло;
- топленое масло (этот вид масла часто используется в индийской кухне);
- сало;
- сливки;
- твердый сыр;
- пирожные и печенье;
- продукты, содержащие кокосовое или пальмовое масло.
Употребление в пищу небольшого количества ненасыщенных жиров повышает уровень хорошего холестерина и уменьшает отложения на стенках артерий. Среди продуктов с высоким содержанием ненасыщенных жиров:
- жирная рыба;
- авокадо;
- орехи и семечки;
- подсолнечное, рапсовое и оливковое масло.
Кроме того, сократите количество соли в вашем рационе и ешьте много фруктов и овощей. Соль повышает артериальное давление. Чем больше соли вы употребляете в пищу, тем выше ваше кровяное давление. Вы должны стремиться съедать менее 6 грамм соли в день, что примерно равно одной чайной ложке.
Доказано, что потреблении пищи с низким содержанием жиров (в том числе пищи с высоким содержанием клетчатки, такой как цельнозерновой рис, хлеб и макароны, а также — фруктов и овощей) способствует снижению кровяного давления. Вам надо стремиться каждый день съедать пять порций фруктов и овощей по 80 грамм.
Регулярное потребление алкоголя выше допустимых норм приведет к повышению кровяного давления. Помимо этого, алкоголь является высококалорийным продуктом, поэтому регулярно употребляя алкоголь, вы наберете лишний вес. Наличие лишнего веса также приводит к повышению уровня кровяного давления.
Физические упражнения и активный образ жизни приводят к снижению кровяного давление за счет поддержания сердца и кровеносных сосудов в хорошем состоянии. Регулярные физические упражнения могут также помочь вам снизить вес, что также поможет снизить кровяное давление.
Рекомендуются упражнения с невысокой нагрузкой, такие как ходьба, плавание или езда на велосипеде или велотренажере. Занятия с более интенсивной нагрузкой, такие как игра в футбол или теннис, могут навредить вашему здоровью. Посоветуйтесь с лечащим врачом, перед тем, как приступить к занятиям любым видом спорта.
К какому врачу обратиться после инфаркта?
С помощью сервиса НаПоправку выберите хорошего кардиолога. Этот врач занимается лечением и реабилитацией больных после инфаркта. Если вам требуется плановая госпитализация, найдите хорошую кардиологическую клинику на нашем сайте.
Возможно, Вам также будет интересно прочитать
Localisation and translation prepared by Napopravku.ru. NHS Choices provided the original content for free. It is available from www.nhs.uk. NHS Choices has not reviewed, and takes no responsibility for, the localisation or translation of its original content
Copyright notice: “Department of Health original content © 2020”
Все материалы сайта были проверены врачами. Однако, даже самая достоверная статья не позволяет учесть все особенности заболевания у конкретного человека. Поэтому информация, размещенная на нашем сайте, не может заменить визита к врачу, а лишь дополняет его. Статьи подготовлены для ознакомительной цели и носят рекомендательный характер.
Напоправку.ру 2020
Инфаркт миокарда: причины появления, симптомы, диагностика и способы лечения.
Определение
Инфаркт миокарда (ИМ) – это омертвление участка сердечной мышцы вследствие недостаточного ее кровоснабжения с развитием характерной клинической картины.
Причины появления инфаркта миокарда
Сердце – полый мышечный орган, имеющий форму конуса. Стенки сердца состоят из трех слоев. Внутренний слой – эндокард – выстилает полости сердца изнутри, и его выросты образуют клапаны сердца. Средний слой – миокард – состоит из сердечной мышечной ткани. Наружный слой – перикард. Сердце человека имеет четыре камеры: два предсердия и два желудочка. В правое предсердие поступает кровь из тканей самого сердца и всех частей тела (по верхней и нижней полым венам). В левое предсердие впадают четыре легочные вены, несущие артериальную кровь из легких. Из правого желудочка выходит легочный ствол, по которому венозная кровь поступает в легкие. Из левого желудочка выходит аорта, несущая артериальную кровь в сосуды большого круга кровообращения. Кислород к миокарду сердца доставляется по коронарным артериям.
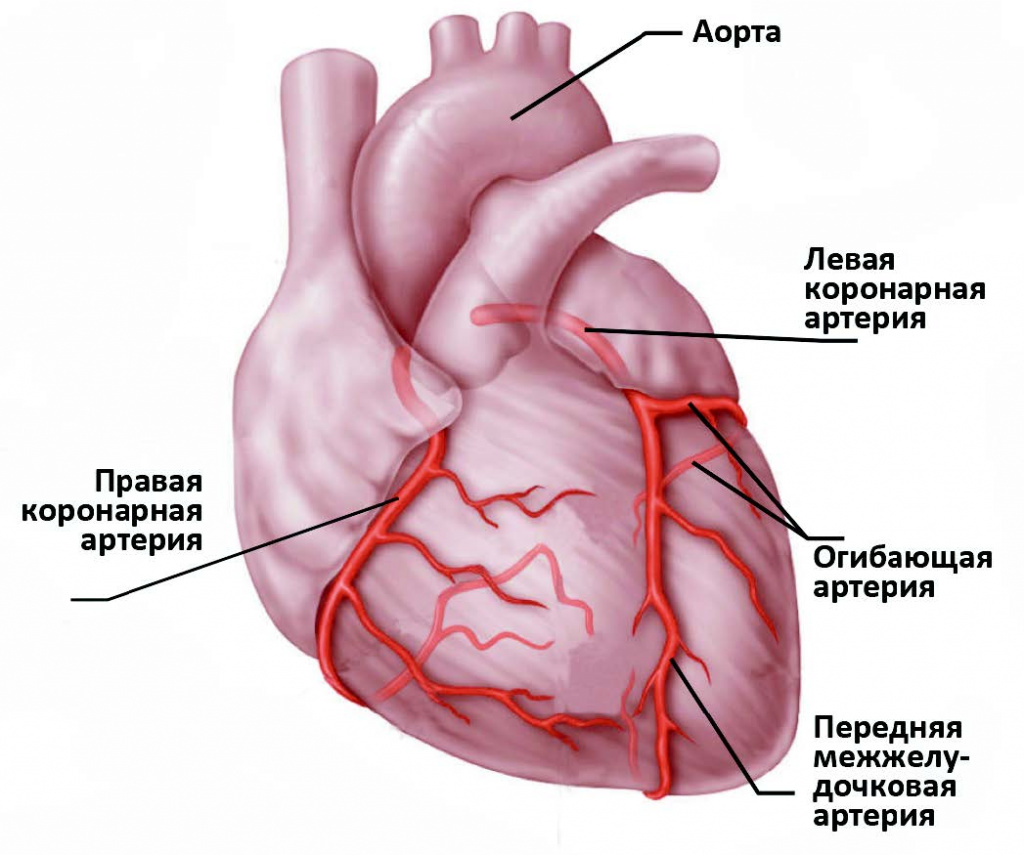
Нарушение кровообращения вследствие атеросклеротического поражения коронарных артерий в 97-98% случаев имеет основное значение в возникновении инфаркта миокарда.
Атеросклерозом может поражаться как одна коронарная артерия, так и все три. Степень и протяженность сужения артерии могут быть различными. При повышении артериального давления склерозированный внутренний слой сосуда (эндотелий) легко повреждается, кровь проникает внутрь бляшки, активируется процесс свертывания крови и формируется тромб, который может частично или полностью закупорить сосуд.
Где может формироваться тромб:
- на месте разрыва уязвимой (нестабильной) атеросклеротической бляшки;
- на дефекте (эрозии) эндотелия коронарной артерии, не обязательно локализованном на поверхности атеросклеротической бляшки;
- в месте гемодинамически незначимого сужения коронарной артерии.
Тромбоз коронарной артерии бывает с полной или неполной пристеночной окклюзией. Тромб, расположенный проксимально (ближе к центру) в коронарной артерии имеет свойство переноситься с током крови более дистально (ближе к стенке сосуда) и приводить к образованию мелких очагов некроза и/или способствовать расширению основного участка некроза.
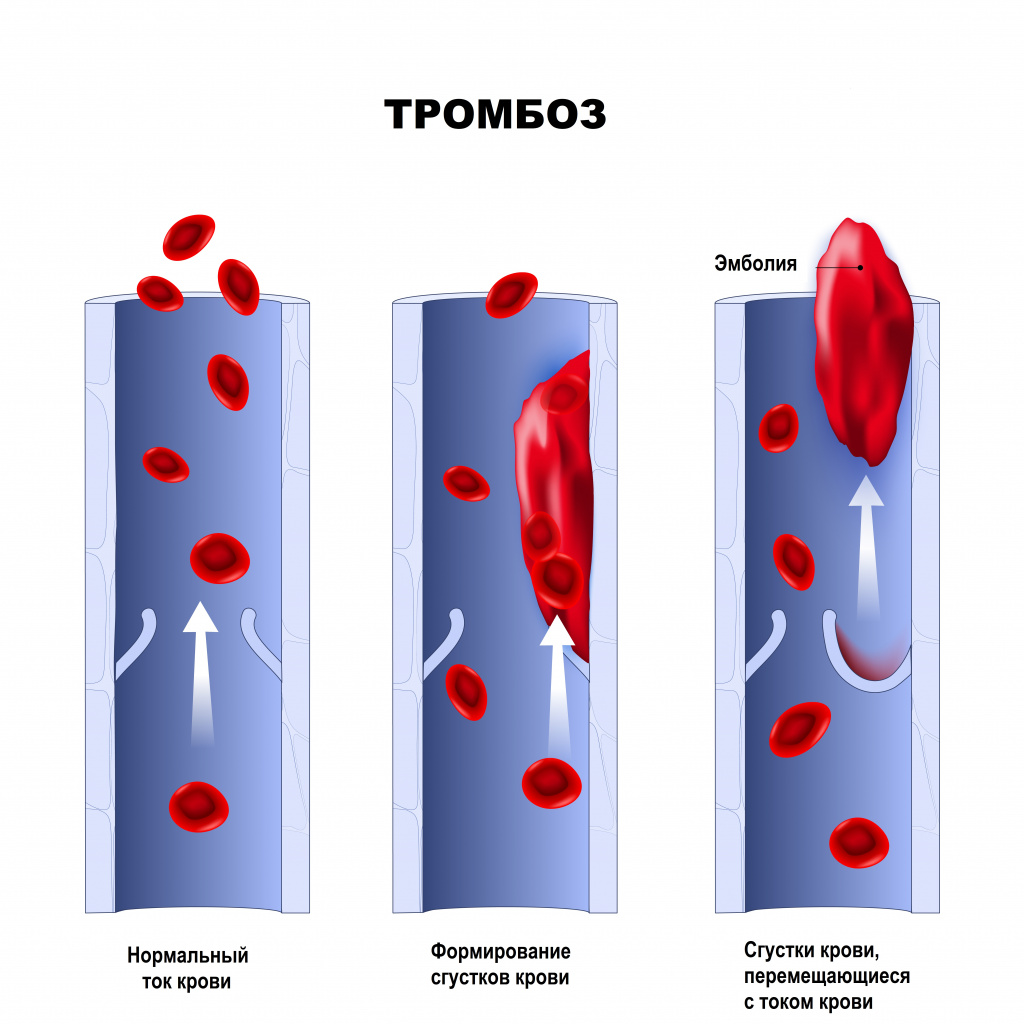
Развивающийся некроз миокарда может быть различных размеров, а некроз, проходящий через все слои сердца (трансмуральный) может стать причиной разрыва миокарда.
Образование очагов некроза в миокарде сопровождается изменением размера, формы и толщины стенки сердца, а сохранившийся миокард испытывает повышенную нагрузку и подвергается гипертрофии с увеличением объема и массы.
Такие сопутствующие состояния как: анемия, воспаление, инфекция, лихорадка, метаболические или эндокринные расстройства (в частности, гипертиреоз) могут спровоцировать или утяжелить ишемию миокарда.
К факторам риска развития инфаркта миокарда относятся:
- гиперлипидемия (нарушение нормального соотношения липидов крови);
- курение,
- сахарный диабет,
- артериальная гипертензия,
- абдоминальное ожирение,
- психосоциальные причины (стресс, депрессия и т.д.),
- низкая физическая активность,
- несбалансированное питание и потребление алкоголя.
Рецидивирующий инфаркт миокарда развивается в течение 28 дней после первоначального инфаркта миокарда. Если ИМ развивается в более поздние сроки, говорят о повторном инфаркте миокарда.
Классификация инфаркта миокарда
I. Острый инфаркт миокарда.
- Острый трансмуральный инфаркт передней стенки миокарда.
- Острый трансмуральный инфаркт нижней стенки миокарда.
- Острый трансмуральный инфаркт миокарда других уточненных локализаций.
- Острый трансмуральный инфаркт миокарда неуточненной локализации.
- Острый инфаркт миокарда неуточненный.
II. Повторный инфаркт миокарда.
- Повторный инфаркт передней стенки миокарда.
- Повторный инфаркт нижней стенки миокарда.
- Повторный инфаркт миокарда другой уточненной локализации.
- Повторный инфаркт миокарда неуточненной локализации.
III. Некоторые текущие осложнения острого инфаркта миокарда.
- Гемоперикард.
- Дефект межпредсердной перегородки.
- Дефект межжелудочковой перегородки.
- Разрыв сердечной стенки без гемоперикарда.
- Разрыв сухожильной хорды.
- Разрыв сосочковой мышцы.
- Тромбоз предсердия, ушка предсердия и желудочка сердца.
- Другие текущие осложнения острого инфаркта миокарда.
IV. Другие формы острой ишемической болезни сердца.
- Коронарный тромбоз, не приводящий к инфаркту миокарда.
- Синдром Дресслера — постинфарктный склероз.
- Другие формы острой ишемической болезни сердца.
- Острая ишемическая болезнь сердца неуточненная.
V. Перенесенный в прошлом инфаркт миокарда.
Симптомы инфаркта миокарда
При инфаркте миокарда в результате нарушения кровообращения в пораженном участке сердца накапливаются продукты обмена, которые раздражают рецепторы миокарда и коронарных сосудов, что проявляется острой болью. Болевой приступ приводит к выбросу адреналина и норадреналина корой надпочечников.
Боль при типичном течении инфаркта миокарда является основным его признаком. Она возникает за грудиной, иногда может отдавать в левую руку, левое плечо, горло, нижнюю челюсть, в подложечную область.
По интенсивности и длительности такая боль в значительной степени превосходит обычный приступ стенокардии. Боль не снимается приемом нитроглицерина. Длительность болевого синдрома может быть различной — от 1 часа до нескольких суток. Иногда инфаркт миокарда сопровождается резкой слабостью, головокружением, головной болью, рвотой, потерей сознания. Больной выглядит бледным, губы синеют, наблюдается потливость.
В первые сутки развития инфаркта миокарда может регистрироваться тахикардия (учащенное сердцебиение), нарушение ритма, повышение температуры до 37-38℃.
В 30% случаев инфаркт миокарда в первые часы своего развития может проявляться нетипично.
Выделяют следующие клинические варианты:
- астматический — протекает как приступ бронхиальной астмы (присутствуют одышка, затрудненное дыхание, чувство нехватки воздуха);
- гастралгический – характеризуется болями в области желудка с распространением в загрудинное пространство, может быть отрыжка, икота, тошнота, многократная рвота, вздутие живота;
- аритмический – возникают нарушения ритма сердца, угрожающие жизни;
- церебральная – характеризуется нарушением мозгового кровообращения (наблюдаются тошнота, головокружение, нарушение сознания с развитием обморока);
- бессимптомный – инфаркт миокарда без типичного болевого приступа. В связи с несоблюдением постельного режима и отсутствием должного лечения протекает неблагоприятно.
Диагностика инфаркта миокарда
Существуют четкие критерии диагностики инфаркта миокарда:
- клиническая картина инфаркта миокарда;
- картина инфаркта миокарда по данным ЭКГ;
- наличие новых участков миокарда со сниженным кровообращением или нарушение сократимости миокарда по данным инструментальных исследований;
- выявление тромбоза коронарных артерий по данным ангиографии.
Для подтверждения диагноза проводят следующие лабораторные исследования:
- определение уровня биохимических маркеров повреждения кардиомиоцитов в крови;
Общий белок (в крови) (Protein total)
Синонимы: Общий белок сыворотки крови; Общий сывороточный белок.
Total Protein; Serum Тotal Protein; Total Serum Protein; TProt; ТР.
Краткая характеристика определяемого вещества Общий бе�…
Альбумин (в крови) (Albumin)
Синонимы: Человеческий сывороточный альбумин; ЧСА; Альбумин плазмы;
Human Serum Albumin; ALB.
Краткая характеристика исследуемого вещества Альбумин
Альбумин – эт…
Креатинин (в крови) (Creatinine)
Синонимы: Анализ крови на креатинин; Сывороточный креатинин; Креатинин сыворотки, оценка СКФ. Сreat; Сre; Blood Creatinine; Serum Creatinine; Serum Creat.
Краткая характеристика определя�…
Мочевина (в крови) (Urea)
Синонимы: Диамид угольной кислоты; Карбамид; Мочевина в крови; Азот мочевины.
Urea nitrogen; Urea; Blood Urea Nitrogen (BUN); Urea; Plasma Urea.
Краткая характеристика аналита Мочевина
Моче�…
Глюкоза (в крови) (Glucose)
Материал для исследования
Сыворотка или плазма крови. Если нет возможности центрифугировать пробу через 30 минут после взятия для отделения сыворотки/плазм…
Триглицериды (Triglycerides)
Синонимы: Липиды крови; нейтральные жиры; ТГ.
Triglycerides; Trig; TG.
Краткая характеристика определяемого вещества Триглицериды
Триглицериды (ТГ) – источник получен…
Калий, натрий, хлор в сыворотке крови (К+, Potassium, Na+, Sodium, Сl-, Chloride, Serum)
Синонимы: Анализ крови на электролиты; Электролиты в сыворотке крови. Electrolyte Panel; Serum electrolyte test; Sodium, Potassium, Chloride; Na/K/Cl.
Краткая характеристика определяемых �…
Магний в сыворотке (Magnesium, Serum; Мg)
Синонимы: Анализ крови на магний; Общий магний; Ионы магния. Serum Magnesium Test; Magnesium test; Magnesium, blood; Serum magnesium.
Краткая характеристика определяемого аналита Магний
…
Инструментальные исследования сердца:
- регистрация 12-канальной электрокардиограммы (ЭКГ) в покое, во время или сразу после приступа боли в грудной клетке для выявления признаков ишемии.
ЭКГ без расшифровки
ЭКГ представляет собой исследование, в основе которого — регистрация биопотенциалов сердца. Применяется для диагностики функциональной активности миокарда.
Рекомендуется зарегистрировать ЭКГ в течение 10 минут на месте первого контакта с медицинским работником (как правило, догоспитально) и безотлагательно интерпретировать ее.
- Трансторакальная эхокардиография (ЭхоКГ) в состоянии покоя № 786 для оценки функции и геометрии левого желудочка, а также для распознавания таких осложнений, как тромбоз полости, разрывы сердца, нарушение функции клапанов, перикардит, расслоение аорты и тромбоэмболия легочной артерии.
- Магнитно-резонансное томографическое (МРТ) исследование сердца для уточнения локализации и объема поражения даже при относительно небольших размерах очага (очагов) некроза. Исследование позволяет дифференцировать ишемическую или воспалительную (миокардиты) природу поражения, а также дать оценку работы клапанного аппарата сердца.
-
Компьютерная томография (КТ) может оказаться полезной для дифференциальной диагностики, если другие методы недостаточно информативны.
- Сцинтиграфия миокарда с 99тТс-пирофосфатом — дополнительный метод диагностики, который показан в тех случаях, когда имеются существенные затруднения в интерпретации изменений ЭКГ.
- Коронароангиография — исследование, выполняемое в условиях операционной путем введения контрастного вещества в устья коронарных артерий под рентгенологическим контролем. Коронароангиогарфия используется для выявления стенозов (сужений) в коронарных артериях, их локализации, протяженности и выраженности, а также для обнаружения участков нестабильности атеросклеротической бляшки. Коронароангиографию проводят для определения показаний к хирургическому лечению.
К каким врачам обращаться
Пациента с острым инфарктом необходимо оперативно доставить в стационар для профилактики осложнений и повышения шансов на выживание.
Система оказания помощи больным инфарктом миокарда включает следующие этапы:
- Догоспитальный этап. Бригада скорой помощи оказывает помощь и транспортирует больного в стационар.
- Госпитальный этап. Помощь оказывается кардиологами в специализированных отделениях.
- Реабилитационный этап. Реабилитация проводится в специальных отделениях больниц или специализированных кардиологических санаториях.
- Диспансерное наблюдение и амбулаторное лечение. Диспансеризация в постинфарктном периоде осуществляется в областных или городских кардиологических центрах или в кардиологических кабинетах поликлиник.
Лечение инфаркта миокарда
На догоспитальном этапе необходимо положить больному под язык таблетку нитроглицерина (или использовать нитросодержащий спрей) и дать аспирин, боль снимается введением обезболивающих препаратов; ликвидируются нарушения ритма сердца.
В острейшем (от 30 мин. до 2 часов) и остром периоде (от 2 часов до 14 суток) необходимо предотвратить увеличение очага омертвения миокарда, устранить боль, восстановить ток крови по сердечным артериям.
При переходе болезни в подострую стадию (до 1 месяца) и в постинфарктном периоде (свыше 1 месяца) необходимо снизить риск рецидива приступа и возможных осложнений.
Для лечения острого инфаркта миокарда используются лекарственные препараты из различных фармакологических групп:
- обезболивающие препараты: анальгетики из группы наркотических обезболивающих в сочетании с анальгином, антигистаминные препараты (димедрол), нейролептанальгезия (комбинация анальгетика с сильным нейролептиком). Для снятия возбуждения могут использоваться транквилизаторы. Для уменьшения гипоксии (снижения уровня кислорода в тканях) используют ингаляции кислорода с помощью носового катетера.
- Тромболитическая терапия необходима для восстановления тока крови по коронарным артериям и растворения тромбов, чтобы омертвение сердечной мышцы не распространялось дальше. Тромболитики вводят внутривенно.
- Антиагреганты препятствуют слипанию тромбоцитов, улучшая кровоток по артериям (ацетилсалициловая кислота). Также используются ингибиторы P2Y12-рецепторов тромбоцитов.
- Внутривенные/подкожные антикоагулянты нужны для профилактики тромбоза глубоких вен и тромбоэмболии легочной артерии.
-
Для ограничения зоны ишемии и некроза миокарда, уменьшения нагрузки на сердце используют нитраты и бета-блокаторы.
Для восстановления коронарного кровотока применяют хирургическое лечение:
- чрескожное коронарное вмешательство (ЧКВ) со стентированием (установкой каркаса в просвет коронарных артерий);
- аорто-коронарное шунтирование (хирургическое вмешательство, в результате которого восстанавливается кровоток в артериях сердца путем создания обхода места сужения коронарного сосуда с помощью отрезка вены с ноги или с внутренней грудной или лучевой артерии).

- Дисфункция сердца как проявление гибели кардиомиоцитов.
- Кардиогенный шок – жизнеугрожающее состояние, вызванное резким снижением сердечного выброса, приводящее к неадекватному кровоснабжению органов и тканей.
- Гемоперикард — кровоизлияние в полость перикарда.
- Отек легких — состояние, обусловленное обильным пропотеванием жидкой части крови в ткань легких, проявляющееся тяжелым удушьем, цианозом и клокочущим дыханием.
- Острая аневризма аорты (расширение участка аорты) и ее разрыв.
- Разрыв стенки левого желудочка (возникает примерно у 1% больных в первую неделю заболевания).
- Разрыв межжелудочковой перегородки.
- Аневризма сердца (участок истонченной рубцовой ткани с выпячиванием стенки желудочка в этой области).
- Острая сердечно-сосудистая недостаточность — состояние, вызванное ослаблением сократительной способности миокарда и застойными явлениями в малом или большом круге кровообращения.
- Тромбоэндокардит — образование пристеночных тромбов в полостях сердца, на клапанах сердца и прилежащем эндокарде при его воспалении.
- Тромбоэмболические нарушения — закупорка сосуда тромбом, оторвавшимся от места своего образования.
- Нарушения сердечного ритма.
- Постинфарктный синдром – это перикардит аутоиммунного генеза, развивающийся спустя несколько недель после острого инфаркта миокарда.
- Постинфарктная недостаточность кровообращения — состояние, при котором сердечно-сосудистая система не обеспечивает полностью потребности организма в кровоснабжении при нормальной жизнедеятельности.
Профилактика инфаркта миокарда
Профилактика инфаркта миокарда подразделяется на первичную и вторичную.
- Первичная профилактика проводится при наличии каких-либо проблем с сердцем до того, как произошел инфаркт, и включает:
- занятия спортом, так как малоподвижный образ жизни отрицательно влияет на сердечно-сосудистую систему;
- отказ от вредных привычек (курения, приема алкоголя);
- правильное питание (включение в рацион свежих овощей, фруктов и зелени, мяса птицы и кролика, рыбы и морепродуктов, ограничение соли; отказ от пряностей при экстрасистолии, так как они провоцируют развитие аритмии);
- отдых и полноценный сон не менее восьми часов в сутки;
- регулярные ежегодные посещения кардиолога для пациентов старше 40 лет с обязательным ЭКГ-исследованием, определением липидного профиля и контролем уровня сахара в крови;
-
контроль артериального давления, повышение которого зачастую провоцирует разрыв атеросклеротической бляшки. При выявленной артериальной гипертензии необходим своевременный и постоянный прием гипотензивных препаратов (снижающих артериальное давление), назначенных кардиологом.
- Вторичная профилактика направлена на предотвращение повторного инфаркта миокарда, проводится пациентам, которые уже перенесли инфаркт миокарда, длится всю жизнь и включает:
- соблюдение всех мер, применяемых для первичной профилактики инфаркта миокарда;
- постоянное применение медикаментозных препаратов, назначенных врачом;
- регулярный контроль состояния, уровня артериального давления, показателей биохимии, изменений на ЭКГ и эхокардиографии.
Источники:
- Клинические рекомендации «Острый инфаркт миокарда с подъемом сегмента ST электрокардиограммы». Минздрав РФ, 2020.
- Кузьмичев Д.Е., Вильцев И.М., Скребов Р.В., Чирков С.В. Инфаркт миокарда в клинике. Проблемы экспертизы в медицине, журнал. 2015. С. 49-51.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы — 19 лет
Поделитесь этой статьей сейчас
Рекомендации
-
2409
05 Марта
-
13067
01 Марта
-
13064
23 Февраля
Похожие статьи
Гангрена
Гангреной называют некроз (омертвение) тканей, который может развиваться в коже, подкожной жировой клетчатке, мышцах, кишечнике, желчном пузыре, легком и т. д.
Постменопауза
Постменопауза: причины появления, симптомы, диагностика и способы лечения.
Сепсис
Сепсис: причины появления, симптомы, диагностика и способы лечения.