- Причины канцероматоза брюшины
- При каких заболеваниях развивается
- Диагностика канцероматоза брюшины
- Стадии канцероматоза брюшной полости
- Симптомы канцероматоза брюшной полости
- Как лечат канцероматоз брюшины
- Какие методики терапии дают лучший результат
- Прогноз при канцероматозном поражении
- Читайте также:
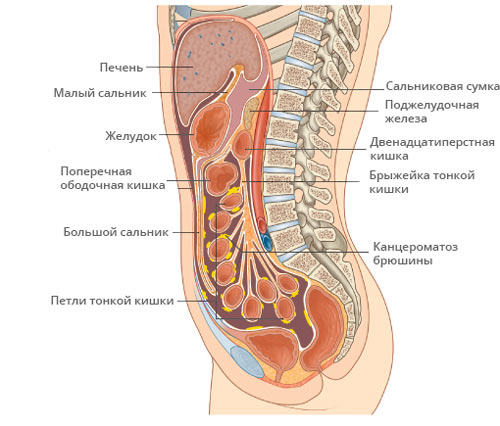
Канцероматоз брюшины — опухолевое поражение листков слизистой оболочки, покрывающей органы и внутреннюю стенку живота. Преимущественно обусловлен разрастанием метастазов рака в брюшной полости, иногда возможно развитие первичного злокачественного процесса — мезотелиомы в самой брюшине.
Метастатическое поражение правильнее называть «карциноматоз», поскольку карцинома — синоним рака. Аналогично метастазы саркомы в брюшину именуют «саркоматоз».
Частое, но не обязательное проявление перитонеального канцероматоза, — выработка асцитической жидкости. С асцитом или без, но поражение брюшины злокачественным процессом всегда угрожает жизни больного и требует очень непростого лечения.
Причины канцероматоза брюшины
Не всякая оторвавшаяся от материнской раковой опухоли клетка способна стать метастазом, в кровеносном русле погибает львиная доля циркулирующих злокачественных клеток. Для обретения способности стать метастазом раковая клетка должна измениться внутренне — научиться вырабатывать вещества, позволяющие самостоятельно жить и внедриться в другом месте, подавляя нормальные клетки.
Оторвавшиеся от узла клетки мигрируют на большие расстояния, раздвигая нормальные клетки, имплантируются в брюшную слизистую, способны даже внедряться внутрь других клеток. После закрепления на местности, начинается размножение и образование целой клеточной колонии.
Кроме переноса метастатических клеток по крови и лимфе, распространение идёт и внутри полости живота — трансцеломически. Не совсем ясно почему злокачественные клетки задерживаются в брюшине, предполагается благотворное действие микроклимата. Большинство метастазов находят в местах с более спокойной обстановкой и слабой перистальтикой органов, или там, где активно всасывается внутрибрюшная жидкость.
Часто клетки «разбрасываются» во время операции и при лапароскопическом вмешательстве вероятность обсеменения вдвое ниже, чем при классической хирургии. Во время операции обязательно проводится профилактика раковой диссеминации путём неоднократной обработки специальными растворами, но самый эффективный способ очищения от диссеминатов — внутриполостная химиотерапия на фоне гипертермии (HIPEC).
При каких заболеваниях развивается
Перитонеальный канцероматоз диагностируют у каждого третьего пациента с новообразованием желудочно-кишечного тракта. Метастазы по брюшине характерны для карцином желудка и поджелудочной железы — поражается до 40% пациентов. При раке кишечника канцероматоз обнаруживают только у десятой части больных. Максимально высокий процент обусловлен злокачественными процессами яичников — на момент выявления болезни две из трёх пациенток уже имеют опухолевые узлы на брюшине.
Вероятность канцероматоза зависит от степени агрессивности раковых клеток и величины первичной опухоли, так при тотальном инфильтративном раке желудка его выявляют чаще, чем при локальном процессе, не разрушившем наружную серозную оболочку органа.
Тем не менее, ни при одном из злокачественных процессов любой локализации, будь то рак молочной железы или простаты, лёгкого или носоглотки, не исключается внутрибрюшинное метастазирование. Посмертно канцероматозные изменения выявляют у каждого третьего, погибшего от прогрессирования заболевания.
Для сарком такая локализация метастазов нетипична, саркоматоз брюшины констатируется едва ли у трёх из сотни больных. В редчайших случаях совершенно доброкачественные по гистологии муцинозные аденома аппендикса и цистаденома яичников тоже способны привести к обсеменению брюшины с выработкой гелеобразного секрета.
У одного из миллиона, и много чаще это будет женщина, выявляют муцинозную аденому аппендикса или муцинозную цистаденому яичников, в последующем часто приводящие к обсеменению брюшины. Распространение аденомуцинозных клеток в полости живота с выработкой гелеобразного секрета именуют уже «псевдомиксома», зачастую при в этой стадии заболевания не удаётся определить первоисточник опухоли.
Диагностика канцероматоза брюшины
Не представляет трудности выявление опухолевого поражения брюшины при асците, в отсутствии выработки патологического секрета диагностика опирается на визуализацию — УЗИ и КТ с контрастированием.
При УЗИ на внутреннем листке, прилежащем к мышцам брюшной стенки, в норме очень тонком и незаметном, можно увидеть напластования толщиной в несколько сантиметров, практически не прослеживаются только мелкие узелки.
КТ с контрастным усилением много информативнее УЗИ, способно выявить сантиметровые образования. Наиболее точный диагностический метод — лапароскопия. Это обследование обязательно при карциноме желудка, при раке яичников предпочтительна операция — диагностика и лечение одновременно.
При лапароскопии или пункции получают асцитическую жидкость для исследования и определения первоисточника злокачественного процесса. Из экссудата выделяют осадок, который изучают под микроскопом и проводят специфические реакции — ПЦР и ИГХ.
ПЭТ на этапе первичной диагностики не всегда информативна, поскольку далеко не все злокачественные клетки легкого, печени, почек способны накапливать изотопы.
Вне всяких сомнений, самый оптимальный метод диагностики — получение кусочка опухолевой ткани для исследования. Биопсия не целесообразна при известном источнике метастазов и после недавнего лечения первичного рака.
Стадии канцероматоза брюшной полости
Стадирование перитонеального канцероматоза нельзя назвать точным, все классификации приблизительны в определении объёма повреждений и не уточняют локализацию узлов. Зачастую, стадирование даёт общее представление о прогнозе эффективности лечебных мероприятий, нежели информирует о настоящем состоянии внутри полости живота.
Разработанная японскими специалистами градация опухолевого распространения по трём степеням, учитывает общий объём поражения, без числа и размеров очагов:
- P1 — ограниченное;
- P2 — разделённые нормальной тканью очаги;
- P3 — множество узлов.
Во время операции хирурги определяют индекс перитонеального канцероматоза (РСI), измеряя узелки в 13 регионах полости, общая сумма баллов влияет на тактику лечения, в первую очередь, на возможность удаления брюшины — перитонэктомию и целесообразность внутриполостной химиотерапии. При некоторых злокачественных процессах прибегают к сложным формулам расчёта РСI.
Наибольшее представление о размерах ракового повреждения даёт стадирование по степеням:
- 0 — в полости чисто,
- I — в одной анатомической зоне узелки до 5 мм,
- II — множественные узелки до 5 мм,
- III — локальное поражение 0.5–2 см,
- IV — 2-х сантиметровые узелки.
Течение канцероматоза определяется не столько размером метастатического узла, сколь клеточной потенцией к прогрессии и выработке асцитической жидкости, общей площадью опухолевой трансформации и клиническими проявлениями.
Симптомы канцероматоза брюшной полости
Перитонеальный канцероматоз небольшой протяжённости может не проявлять себя симптомами, особенно в отсутствии выработки асцитической жидкости. С другой стороны, жидкость может продуцироваться и при отсутствии видимых метастазов. Как правило, симптоматика неспецифична, и в разном наборе могут отмечаться:
- меняющие локализацию болезненные ощущения, а чаще — непонятный дискомфорт в полости живота;
- нарастающая слабость до утраты работоспособности;
- потеря веса при стабильном диетическом режиме;
- прогрессирующее снижение аппетита;
- функциональные нарушения со стороны органов ЖКТ.
Дальнейшее нарастание раковых повреждений сопровождается опухолевой интоксикацией, сдавление желудка опухолевыми узлами осложняется тошнотой и рвотой, кишечника — запорами и поносами с усугублением частичной непроходимости. Распад крупных узлов может вызывать боли и повышение температуры.
Асцит нарушает процесс дыхания и вызывает сердечную недостаточность с постоянными отёками, а частая эвакуация патологической жидкости приводит к белковой недостаточности.
Как лечат канцероматоз брюшины
Ни один из современных методов лечения канцероматоза не гарантирует радикального удаления опухоли, не способен излечить, но может улучшить состояние и существенно продлить жизнь.
Хирургическое лечение канцероматоза технически сложное для оперирующей бригады и трудно переносимое пациентом, поскольку предполагает удаление первичного рака, увеличенных лимфатических узлов, сальниковых сумок и всех видимых опухолевых образований вместе с брюшиной.
Перитонэктомия — многоэтапное вмешательство, включающее удаление нескольких органов и отделов брюшной полости. В результате операции пациент может остаться без селезёнки, желчного пузыря, части кишечника, матки с придатками.
Стандарт терапии канцероматоза — химиотерапия системная и локальная — внутрибрюшинная после удаления асцита или через лапаропорт, установленный во время операции.
Эффективность лекарственной терапии невысокая, за исключением случаев первичного рака яичников. Таргетные и иммуно-онкологические препараты только изучаются в клинических испытаниях.
Какие методики терапии дают лучший результат
Наиболее высокий эффект демонстрирует комбинация трёх методов лечения рака:
- Операция с максимально возможным удалением злокачественных новообразований — циторедукция.
- Локальная внутрибрюшинная гипертермия.
- Внутриполостное введение химиопрепаратов.
Использование во время хирургического вмешательства интраперитонеальной гипертермической химиотерапии (ИГХТ или HIPEC) позволяет максимально долго поддерживать очень высокую концентрацию цитостатика непосредственно в зоне поражения и усилить лекарственное воздействие нагреванием тканей. При весьма скромных исторических результатах хирургического вмешательства устойчивой к цитостатикам псевдомиксомы только HIPEC открывает пациентам перспективу на долгую жизнь.
Технология ИГХТ такова: в течение полутора часов внутрь брюшной полости под давлением подаётся нагретый химиопрепарат в дозе, существенно превышающей максимально разрешённую для внутривенного введения. За счёт локального использования изменяется спектр токсических реакций, исключается опасное для жизни повреждение кроветворения, но возможна боль в животе и временное нарушение функционирования органов ЖКТ.
Интраоперационная фотодинамическая терапия (ФДТ), когда на выявленные с помощью фотосенсибилизатора очаги опухоли воздействуют лазером, уступает HIPEC по результативности, поскольку лазером невозможно проникнуть во все «закоулки» брюшной полости. Тем не менее, целесообразно использование фотодинамической терапии при крупных и немногочисленных раковых узлах.
Прогноз при канцероматозном поражении
На течение процесса влияет объём поражения на момент начала терапии, степень злокачественности опухоли, в свою очередь определяющая чувствительность к химиотерапии. Основополагающее влияние оказывает талант и опыт хирурга, и несомненно, правильность выбора лечебной тактики.
Однозначно революционные результаты в клинических испытаниях показала только HIPEC. После интраоперационной гипертермической ХТ пятилетняя выживаемость при канцероматозе рака желудка выросла максимально до 20%, все прочие методы исключали столь долгое дожитие. При раке толстой кишки с метастазами по брюшине каждый третий пациент прожил более 5 лет, при карциноме слепой кишки и аппендикса — шестеро из десяти вступили во вторую пятилетку жизни.
Список литературы
- Давыдов М.И., Тер-Ованесов М.Д., Буйденок Ю.В. с соавторами/ Гипертермическая интраоперационная интраперитонеальная химиотерапия при раке желудка: существует ли реальная возможность изменить прогноз? // Вестник РОНЦ им. Н. Н. Блохина РАМН; 2010 Т. 21; № 1
- Степанов И.В., Падеров Ю.М., Афанасьев С.Г./ Перитонеальный канцероматоз// Сибирский онкологический журнал; 2014; № 5
- Akiyama H., Yamaoka H., Tanaka K., et al./ Continuous hyperthermic peritoneal perfusion for peritoneal dissemination of gastric cancer // Hepatogastroenterology; 1998.
- Bozzetti F., Bonfanti G., Morabito A., et al/ A multifactorial approach for the prognosis of patients with carcinoma of the stomach after curative resection // Surg. Gynecol. Obstet.; 1986.
- Cotte E., Passot G., Gilly F.N., Glehen O. /Selection of patients and staging of peritoneal surface malignancies // World J. Gastrointest. Oncol.; 2010; Vol. 2.
- Chua T.C., Moran B.J., Sugarbaker P.H., et al. /Early- and longterm outcome data of patients with pseudomyxoma peritonei from appendiceal origin treated by a strategy of cytoreductive surgery and hyperthermic intraperitoneal chemotherapy// J. Clin Oncol 2012.
- Deraco M., Santoro N., Carraro O., Inglese M.G., et al./ Peritoneal carcinomatosis: feature of dissemination. A review // Tumori; 1999.
- Lansom J., Alzahrani N., Liauw W., Morris D.L. /Cytoreductive Surgery and Hyperthermic Intraperitoneal Chemotherapy for Pseudomyxoma Peritonei and Appendix Tumours // Indian J Surg Oncol. 2016 Jun.
- Sugarbaker P.H./ Overview of peritoneal carcinomatosis // Cancerologia; 2008.
.png)
Канцероматоз брюшины – это метастазы, или дополнительные раковые опухоли, развивающиеся в тонкой пленке, которая выстилает стенки брюшной полости и покрывает расположенные в ней органы.
Как развивается канцероматоз, или вторичный рак брюшины?
Рак – это опасное для жизни новообразование, которое бесконтрольно увеличивается, разрушает окружающие ткани и поражает различные органы.
Он развивается после появления в организме всего лишь одной мутировавшей – измененной клетки, отличающейся от нормальных. Она возникает из-за влияния различных заболеваний, наследственных особенностей, воздействия химических веществ, радиации или случайных сбоев, растет и создает множество своих копий.
Большинство из них выявляет и уничтожает иммунная система, но некоторым удается противостоять ей или скрываться от ее внимания. Они выживают, размножаются и формируют опухоль, прорастающую в расположенные рядом с ней ткани.
На этом их опасные свойства не заканчиваются. Здоровые клетки рождаются и работают в строго определенном месте, после чего умирают. Онкологические же ведут себя не так. Во-первых, у них не работает апоптоз – механизм «запрограммированной» смерти, благодаря чему они живут очень долго и не погибают в положенные сроки. Во-вторых, они умеют перемещаться по сосудам лимфатическойЛимфатическая система дополняет сердечно-сосудистую. Циркулирующая в ней лимфа – межклеточная жидкость – омывает все клетки организма и доставляет в них необходимые вещества и забирает отходы. В лимфатических узлах, выполняющих роль «фильтров», опасные вещества обезвреживаются и выводятся из организма. и кровеносной систем, закрепляться в различных тканях и создавать в них метастазы – дополнительные опухоли в областях, расположенных далеко от основного, первичного очага.
Именно таким образом на последней стадии заболевания развивается канцероматоз, или вторичный рак брюшины.
Сначала новообразование возникает в одном из внутренних органов: яичниках, поджелудочной железе, фаллопиевых трубах, по которым яйцеклетка выходит в матку, тонком или толстом кишечнике, мочевом пузыре, желудке, прямой кишке или аппендиксе.
Затем оно прорастает или распространяет свои клетки в брюшину – тонкую пленку из соединительной ткани, состоящую из двух слоев:
- Висцеральный – обволакивает внутренние органы, такие как кишечник, желудок, печень, поджелудочная железа, мочевой пузырь, яичники, матка и селезенка.
- Париетальный – покрывает внутреннюю поверхность стенки брюшной полости.
Между ними есть небольшое количество жидкости, которая работает как смазка и позволяет внутренним органам плавно скользить при смене положения тела. Она постоянно производится и всасывается, из-за чего попавшие в нее неправильные клетки распространяются по тканям с большой скоростью.
Вторичные опухоли, или метастазы, состоят не из измененных тканей брюшины, а из клеток того органа, в котором они впервые возникли.
Такие новообразования возникают как у женщин, так и у мужчин, и развиваются чаще, чем первичный рак. По оценкам научного сообщества, это происходит с 15-20% больных колоректальным раком, поражающим толстую или прямую кишку, и 10-15% пациентов с онкологией желудка.

Симптомы и признаки канцероматоза брюшины
Канцероматоз, или метастазирование брюшины, происходит только на последней стадии онкологии. К этому моменту, как правило, человек уже сталкивается с заметными проблемами со здоровьем или ощущает ухудшение самочувствия. Обычно сначала у него появляются симптомы, связанные с поражением органа, в котором возникла первичная опухоль, а со временем развиваются и признаки вторичного рака, такие как:
- вздутие или боль в области живота;
- тошнота или рвота;
- изменение привычек кишечника и работы мочевыделительной системы;
- потеря аппетита;
- боли в спине или пояснице;
- увеличение размеров живота;
- нарушение работы пищеварительной системы – постоянные сбои и дискомфорт;
- ощущение сытости даже после приема небольшого количества пищи;
- потеря или набор веса из-за скопления жидкости;
- вздутие живота;
- выделения из влагалища;
- постоянная усталость;
- тяжесть или ощущение сдавливания в области живота или таза.
Со временем у человека может возникнуть асцит – скопление в брюшной полости водянистой жидкости, вызывающий одышку – ощущение нехватки воздуха из-за уменьшения пространства, необходимого легким для полного раскрытия на вдохе.
Кроме того, при разрастании опухолей до крупных размеров, пациенты нередко сталкиваются с полной непроходимостью кишечника или блокировкой мочевыделительной системы, а также невозможностью принятия пищи или питья.
Диагностика канцероматоза брюшины
Для выявления поражений брюшины используется несколько методов:
- Компьютерная томография, КТ. При ее проведении специальный аппарат получает множество рентгеновских снимков, объединяемых в одно, очень четкое изображение. Данное исследование позволяет обнаруживать даже небольшие очаги заболевания и подозрительные области.
- Магнитно-резонансная томография, МРТ. В ходе процедуры магниты и радиоволны создают очень детализированную картинку, отражающую состояние внутренних органов.
- УЗИ – быстрый и безопасный метод, использующийся для выявления новообразований брюшной полости. С помощью ультразвука специалист может обнаружить измененные ткани, отличающиеся от нормальных.
- Позитронно-эмиссионная томография, ПЭТ. Метод применяется для выявления метастазов – дополнительных раковых опухолей. До его проведения пациент получает небольшую дозу радиоактивного сахара, который накапливается в измененных клетках. Затем проводится сканирование, показывающее любое, даже самое небольшое их скопление в любых частях тела.
- Лапароскопия– исследование тканей брюшной полости без выполнения крупных разрезов. Эта малоинвазивная методика позволяет получать данные о состоянии внутренних органов, повреждая при этом минимальное количество тканей. Врач делает небольшой прокол в коже и вводит в него лапароскоп – небольшую трубку с источником света и видеокамерой на конце. Устройство передает на экран монитора четкое и подробное, увеличенное в 4-10 раз изображение.
- Биопсия– забор небольшого количества тканей или жидкости из пораженной области и передача их в лабораторию для тщательного изучения клеток.
- Анализ крови на онкомаркеры СА125, СА 19-9, СЕА или НЕ4 – белки, выделяемые некоторыми видами раковых новообразований. Данный метод не используется как единственный способ диагностики, поскольку повышение их уровня не всегда говорит о наличии в организме опухоли.
- Циторедуктивные операции – хирургическое удаление максимального количества пораженных тканей и измененных клеток.
- Внутрибрюшинная гипертермическая химиоперфузия, или HIPEC – введение разогретого до более чем 40 градусов химиотерапевтического средства непосредственно в брюшину. Для ее проведения требуется дорогое высокотехнологичное оборудование, хорошо оснащенная операционная и целая команда докторов различных специальностей. По мнению множества исследователей, сочетание циторедуктивных вмешательств и HIPEC произвело настоящую революцию в лечении канцероматоза. Метод имеет целый ряд противопоказаний, ограничивающих его применение:
- Наличие метастазов – дополнительных раковых опухолей, расположенных за пределами брюшины.
- Плохое общее состояние здоровья пациента.
- Негативная реакция на химиотерапию – рост новообразования или ухудшение самочувствия.
- Большое количество очагов поражения висцеральной брюшины – листка, обволакивающего внутренние органы.
- Перитонеумэктомия – полное или частичное изъятие париетальной брюшины, покрывающей внутреннюю поверхность стенки брюшной полости.
- Удаление поврежденных онкологией внутренних органов – например, матки, ее труб, яичников или пострадавших отделов кишечника.
- Таргетная терапия – введение специальных препаратов, которые воздействуют только на определенные изменения в раковых клетках, и практически не наносят вреда нормальным тканям. Для части пациентов с канцероматозом брюшины могут подойти:
- Моноклональные антитела: доставляют в опухолевую клетку убивающие ее молекулы.
- Ингибиторы ангиогенеза: предотвращают рост новых сосудов, необходимых новообразованию для питания и дальнейшего развития.
- Ингибиторы PARP: вещества, блокирующие восстановление ДНК измененных клеток – молекулы, в которой зашифрована вся информация об организме.
- Боль.
- Вздутие живота – асцит.
- Отеки – скопление жидкости в тканях.
- Депрессию и тревогу.
- Изменение веса.
- Тошноту и рвоту.
- Запоры.
- Потерю аппетита.
- Усталость и слабость.
Лечение канцероматоза брюшины
Борьба с распространившимся по организму раком – очень непростая задача.
Еще совсем недавно единственным методом воздействия на него была химиотерапия – прием или введение в вену специальных препаратов, которые уничтожают быстро делящиеся клетки, в том числе опухолевые. К сожалению, большая часть онкологических новообразований брюшины лишь немного уменьшается в размерах или совсем не реагирует на подобное лечение.
Сегодня врачи используют следующие тактики:
Все подобные вмешательства проводятся только опытными врачами в специализированной клинике.
Любое лечение канцероматоза брюшины можно пройти у нас, в онкологическом центре «Лапино-2».
Наши врачи – кандидаты и доктора медицинских наук с огромным опытом в области борьбы с опасными для жизни опухолями и большим стажем работы в крупнейших федеральных учреждениях.
Мы быстро проводим полную диагностику, берем анализы и в максимально сжатые сроки получаем их результаты из собственной лаборатории.
В нашем центре выполняются все необходимые процедуры на самом современном оборудовании с применением только оригинальных препаратов, дающих предсказуемый результат.

Паллиативное лечение канцероматоза брюшины
К сожалению, даже самые современные достижения медицины не способны победить некоторые запущенные формы рака. В таких случаях пациенту может быть назначено паллиативное, или поддерживающее лечение, задача которого заключается не в полном удалении очагов онкологии из организма, а в улучшении самочувствия и облегчении симптомов болезни. С ее помощью можно контролировать:
Отеки, лимфедема, асцит
Отеки – распространенная проблема, с которой нередко сталкиваются онкологические больные. Они могут быть вызваны задержкой в организме соли и воды из-за приема некоторых лекарств, повреждений сердца, печени или почек, инфекции, неправильного питания, роста опухоли или других причин.
При поражении раком или удалении лимфатических узлов, которые выполняют роль «фильтров», задерживающих и обезвреживающих опасные вещества, у пациентов может возникнуть лимфедема – серьезный отек конечности. Она развивается из-за нарушения циркуляции лимфы, которая омывает все клетки тела, доставляет в них необходимые вещества и забирает отходы.
Облегчить эти симптомы можно с помощью приема диуретиков – мочегонных средств, помогающих почкам выводить натрий и воду, а также ограничения употребления соли.
Асцит – избыточное скопление жидкости в брюшной полости, вызванное повреждением тканей и расположенных в них лимфоузлов. Он приводит к увеличению размеров живота, тошноте, рвоте, повышенной утомляемости и затруднению дыхания. Для улучшения самочувствия его обладателей врачи могут назначить хирургические вмешательства или химиотерапию. В большинстве случаев проводится парацентез – слив лишней жидкости, который дает временное облегчение на несколько недель или дней.
Затруднение дыхания
Одышка, или нехватка воздуха – один из самых распространенных симптомов запущенного рака. Она может быть вызвана как самим заболеванием, так и его лечением. Нередко ее причиной становится асцит, приводящий к ограничению движения диафрагмы – тонкой, похожей на купол мышцы, отделяющей грудную клетку от брюшной полости. В норме при дыхании она движется вверх и вниз, позволяя легким увеличиваться и уменьшаться в объеме, но скопившаяся жидкость давит на нее и не позволяет человеку получать достаточное количество кислорода. Это крайне неприятное ощущение серьезно влияет на качество жизни, ограничивает возможности и усугубляет усталость, беспокойство и депрессию.
Методы лечения и облегчения данного состояния зависят от вызвавшей их причины.
С легкой одышкой можно справиться самостоятельно – достаточно сесть или лечь, подняв верхнюю часть тела под углом 45° с помощью подушек, глубоко вдохнуть через нос и медленно выдохнуть через сжатые губы. Некоторым пациентам помогают различные техники расслабления, отвлечение на музыку, чтение и телевизор.
При появлении серьезных затруднений дыхания, бледности или посинении кожи, слизистых рта и ногтевого ложа, болях, стеснении и тяжести в грудной клетке, проблемах с речью, головокружениях или слабости необходимо срочно обращаться за медицинской помощью.
Непроходимость кишечника
Расположенные в брюшной полости опухоли нередко блокируют кишечник и препятствуют прохождению стула. Это приводит к сильным спазмам, болям в животе и рвоте. Данная ситуация требует срочного вмешательств, поскольку скопившееся в пищеварительном тракте содержимое способно повредить его стенки. Оно может выйти через образовавшее отверстие в брюшную полость и вызвать тяжелую инфекцию.
В таких случаях проводится операция по установке стента – небольшой жесткой трубки, не позволяющей просвету сужаться, или колостомия – выведение здоровой части толстой кишки через отверстие на коже живота.
Если хирургическое лечение невозможно, врачи удаляют содержимое желудка с помощью специальной трубки, введенной через нос.
Непроходимость мочевыводящих путей
Некоторые опухоли брюшной полости блокируют мочеточники, по которым моча выходит в мочевой пузырь. Такая закупорка приводит к скоплению жидкости в почках и нарушению их работы.
В подобных ситуациях специалисты выполняют установку стентов или нефростомию – вводят в почку гибкую трубку, позволяющую ее содержимому перетекать в специальный контейнер – расположенный на теле резервуар.
Прогнозы и выживаемость при канцероматозе брюшины
Согласно данным научных исследований, средняя продолжительность жизни для вторичного рака брюшины составляет 6 месяцев.
Перспективы в немалой степени зависят от расположения первичной опухоли, ее стадии и типа проводимого лечения. Наихудшие прогнозы – примерно 2,9 месяца – у пациентов с поражением поджелудочной железы, около 6,5 месяцев – желудка, и 6,9 месяца – толстой или прямой кишки. Еще сильнее сокращают эти сроки наличие асцита – скопления жидкости в брюшной полости, а также метастазов – дополнительных онкологических новообразований в печени.
Некоторые научные работы показывают, что сочетание циторедуктивных операций и внутрибрюшинной гипертермической химиоперфузии, или HIPEC, заметно повышает выживаемость. Она увеличивается до 62,7 месяцев с 23,9 по сравнению с людьми, которые получают обычную химиотерапию.
Канцероматоз (canceromatosis; карцинома (основа cancinomat-) + -о) — множественные метастазы в серозных оболочках или паренхиме органов, вызванные наличием в организме больного злокачественного новообразования. Перитонеальный канцероматоз — распространение опухолевых клеток по брюшной полости посредством кровотока и лимфотока.
Иногда используют неправильный термин — канцероматоз[источник не указан 747 дней].
Примеры употребления термина
- Карциноматоз брюшины
- Карциноматоз плевры
- Лептоменингеальный канцероматоз
Клиническая картина
Карциноматоз серозных оболочек как правило сопровождается обильным выпотом в соответствующую серозную полость.
Интраоперационно выглядит как просовидные включения в серозной оболочке, которые могут сливаться и образовывать более крупные опухоли.
- Формирование карциноматоза брюшной полости характерно для многих видов рака пищеварительной системы (рак желудка, рак толстой и прямой кишки), однако наиболее характерно — для рака яичников.
- Формирование карциноматоза плевральной полости наиболее характерно для мезотелиомы плевры, рака лёгких, рака молочной железы. Однако данное состояние может быть обусловлено любой опухолью способной метастазировать в лёгкие и плевру.
Лечение
Лечение проводится как хирургическим методом, так и химиотерапией.
Эта страница в последний раз была отредактирована 3 февраля 2023 в 22:02.
Как только страница обновилась в Википедии она обновляется в Вики 2.
Обычно почти сразу, изредка в течении часа.
Канцероматоз – активное метастазирование онкологического процесса в организме, где образуются многочисленные опухолевые узлы. Они указывают на заключительную стадию заболевания и требуют принятия экстренных мер для сохранения жизни и здоровья пациента с учетом тяжелой онкологической патологии. Чаще симптомы канцероматоза сопровождают рак желудка, толстой кишки, яичников и других органов брюшной полости. Нередко заболевание развивается после оперативного вмешательства, не позволяя дать пациенту благоприятный прогноз лечения.
Согласно статистике канцероматоз развивается приблизительно в трети случаев. Причины столь высокого риска до настоящего времени не изучены. При этом вероятность развития осложнения выше при онкологии молочных желез или легких, а при раке головного мозга риск составляет всего 10% от общего числа диагностированных случаев.
Симптомы заболевания
В числе основных признаков, указывающих на развитие канцероматоза, выделяют:
- заметная опухлость пораженного органа, заметная даже при поверхностном осмотре;
- спазмирование пораженной части тела;
- скопление жидкости возле онкологического образования;
- повышение температуры.
Если онкологический процесс сосредоточен в брюшной полости, пациент жалуется на быстрое увеличение объема живота из-за скопления жидкости, колики, тошноту и рвоту. При поражении легких отмечается аритмия, одышка и сильная боль в груди. Подтвердить или опровергнуть диагноз удается после детального инструментального исследования.
Причины появления канцероматоза
Основная причина канцероматоза – онкологическое заболевание, для которого характерно ускоренное деление злокачественных клеток. Мигрируя внутри организма, они распространяют болезнь по телу, вызывая резкое ухудшение состояния больного и снижая шансы на его выздоровление. В большинстве случаев признаки канцероматоза развиваются на фоне следующих онкологических патологий:
- рак желудка;
- поражение желчевыводящих путей;
- онкология яичников;
- патология поджелудочной железы;
- онкология тонкого кишечника;
- рак печени.
Прикрепление к здоровому органу позволяет злокачественным клеткам быстро делиться, поглощая здоровые ткани. Опухоль быстро разрастается, в ней скапливается значительное количество жидкости, что становится причиной отечности. Чем раньше начато лечение, тем выше шансы остановить этот процесс и сохранить функционирование жизненно важного органа.
Стадии развития
В зависимости от распространения различают следующие стадии канцероматоза:
- На первом этапе клетки только начинают свое распространение по организму. Процесс может ускорить недавно проведенное оперативное вмешательство или травма.
- На втором этапе клетки закрепляются на органе и начинают активно размножаться, что приводит к «поглощению» тканей и нарушению функционирования пораженной системы.
При инструментальном исследовании можно выделить три стадии канцероматоза:
- Контур опухоли имеет один пораженный фрагмент.
- Орган поражен в разных частях, но у него еще заметны здоровые ткани.
- Поврежден значительный участок органа.
Диагностика заболевания
Точно поставить диагноз и наметить оптимальный курс лечения канцероматоза позволяют:
- Визуальный осмотр тела пациента в местах предполагаемого развития опухоли.
- Рентгенография.
- Ультразвуковое исследование внутренних органов.
- Компьютерная или магнитно-резонансная томография.
- Биопсия тканей узловых образований.
- Лапароскопические процедуры.
Также в обязательном порядке проводятся лабораторные исследования крови и мочи, благодаря результатам которых можно уточнить работоспособность систем и органов пациента.
Лечение патологии
Сегодня для лечения канцероматоза успешно применяют следующие методики:
- Технология внутрибрюшной перфузионной термохимиотерапии. Предусматривает введение в новообразование подогретого до 420С раствора противоопухолевых препаратов. Он обладает способностью воздействовать на метастатические узлы, способствуя их уменьшению и уничтожению. Этот метод является основой лечебного курса при раке желудка.
- Циторедуктивная операция. Подразумевает удаление первичной опухоли с метастазами и отсевами для замедления распространения заболевания.
- Системная химиотерапия, которую обычно назначают на заключительной стадии лечения для снижения риска рецидива.
Предлагаемые методы лечения позволяют рассчитывать на устранение симптомов заболевания и замедление его распространения по организму.
Прогноз по заболеванию
Говорить о выживаемости пациента с канцероматозом онкологам приходится очень осторожно. На лечение могут негативно повлиять угнетенная иммунная система, имеющиеся хронические заболевания, возраст и характер злокачественной патологии. Благодаря современным методам лечения шансы на исцеление для пациентов гораздо выше, а прогнозы при канцероматозе благоприятнее, чем еще несколько лет назад.
Профилактика
Меры профилактики канцероматоза не предусмотрены из-за вторичного характера заболевания на фоне основного онкологического процесса.
Реабилитация пациентов с канцероматозом
Реабилитационный период для пациентов с канцероматозом длится продолжительное время. Обязательными мероприятиями являются наблюдение онколога, отслеживание симптомов рецидива, а также курсы системной химиотерапии для уничтожения первичных признаков повторного развития заболевания.
Диагностика и лечение канцероматоза в Институте ядерной медицины
Институт ядерной медицины приглашает пациентов с онкологическими заболеваниями на обследование, консультирование и лечение. Оснащение высокоточным оборудованием позволяет пройти комплекс диагностических и терапевтических процедур с гарантией их эффективности и безопасности. Благодаря персональному сопровождению каждого пациента можно рассчитывать на получение всех необходимых услуг, тем более что они построены с учетом действующих международных стандартов и нацелены на оказание всесторонней медицинской помощи.
Вопросы и ответы
Сколько живут с канцероматозом?
Дать конкретный прогноз по пятилетней выживаемости пациента с канцероматозом может только лечащий онколог на основании состояния организма, особенностей течения болезни и прочих факторов. Даже при условно благоприятном прогнозе специалисты готовы сделать все возможное, чтобы устранить нежелательные симптомы и замедлить развитие патологии.
Как проявляется канцероматоз?
Канцероматоз представляет собой обширное метастазирование злокачественных опухолей, которые быстро распространяются по организму и образуют на поверхности органов многочисленные опухолевые узлы. Эту стадию могут сопровождать опухлость пораженной части тела, повышение температуры, нарушения процесса пищеварения, болевые ощущения и т.д. Набор симптомов зависит от типа заболевания и места его локализации.
Лечится ли канцероматоз?
Сегодня пациентам с канцероматозом предлагается сразу несколько способов лечения, позволяющих не только остановить распространение заболевания, но и исключить его рецидив в обозримом будущем. В числе перспективных методов — термохимиотерапия, которая уничтожает злокачественные клетки опухолевых узлов и исключает появление новых образований. Ее могут дополнять другие методы воздействия на онкологический процесс, которые стабилизируют состояние больного.
Литература:
- Солодкий В.А., Фомин Д.К., Гончаров С.В., Кукушкина С.А. Современные подходы к лечению перитонеального канцероматоза при раке желудка (обзор литературы). Сибирский онкологический журнал. 2022;21(1):122-129.
- Хомяков В.М., Рябов А.Б., Колобаев И.В., Болотина Л.В., Уткина А.Б., Соболев Д.Д., Кузнецова О.С., Каприн А.Д. ВНУТРИБРЮШНАЯ АЭРОЗОЛЬНАЯ ХИМИОТЕРАПИЯ ПОД ДАВЛЕНИЕМ В СОЧЕТАНИИ С СИСТЕМНОЙ ХИМИОТЕРАПИЕЙ – НОВЫЙ ПОДХОД В ЛЕЧЕНИИ БОЛЬНЫХ РАКОМ ЖЕЛУДКА С ПЕРИТОНЕАЛЬНЫМ КАРЦИНОМАТОЗОМ. Сибирский онкологический журнал. 2020;19(4):49-58.
Злокачественные опухоли могут метастазировать — распространяться на другие ткани и органы. Если первичная опухоль расположена в брюшной полости, она может распространиться по брюшине — это состояние называется перитонеальным канцероматозом. Такой вариант течения болезни значительно ухудшает прогноз — в среднем, в зависимости от вида опухоли и полученного лечения продолжительность жизни человека составляет от полугода до двух лет. Долгое время пациентам с канцероматозом брюшины могли предложить только паллиативную помощь, но появились и другие методы.
Рассказываем о циторедуктивной операции и гипертермической внутрибрюшинной химиотерапии (HIPEC), которые могут продлить жизнь людям с таким диагнозом.
Этот текст мы написали вместе с Онкоцентром «СМ-Клиника».
Что такое перитонеальный канцероматоз?
Брюшина — оболочка, выстилающая стенки брюшной полости, таза и поверхность внутренних органов — печени, матки, яичников, селезенки, кишечника. Любой патологический процесс, затрагивающий брюшную полость, может распространяться по брюшине за счет движения жидкости и клеток в этом пространстве. Например, эпителиальные опухоли яичников возникают из эпителия маточных труб, который сообщается с брюшиной. Из-за роста опухоли злокачественные клетки «отслаиваются» и могут свободно плавать в перитонеальной жидкости. Как правило, эти клетки имплантируются в область таза и другие части брюшины.
Канцероматоз выглядит как множество опухолевых узлов, покрывающих брюшину. Размер и количество узлов могут быть различными.
При каких опухолях чаще всего развивается канцероматоз брюшины?
Перитонеальный канцероматоз у женщин чаще всего развивается при раке яичников, а у мужчин — при раке толстой кишки и желудка. Например, при раке желудка опухолевые узлы на брюшине возникают у 60% пациентов.
В более редких случаях канцероматоз брюшины может быть самостоятельным заболеванием. Иногда расположение первичной опухоли установить не получается.
Какие симптомы могут указать на перитонеальный канцероматоз?
У этого состояния неспецифические признаки. Среди них:
— увеличение объема живота из-за скопления жидкости в брюшной полости — асцит
— боль в животе
— тошнота, вздутие живота
— запор или диарея
— потеря аппетита
— необъяснимая потеря веса
Злокачественный (то есть вызванный опухолью) асцит, в свою очередь, может вызывать другие симптомы, среди которых:
— одышка
— набор веса
— отеки лодыжек
— усталость
Перитонеальный канцероматоз может вызывать кишечную непроходимость. В этом случае продвижение содержимого желудка и кишечника через ЖКТ затруднено или отсутствует. Злокачественная кишечная непроходимость чаще встречается у пациентов с раком яичников и колоректальным раком.
Как диагностируют канцероматоз брюшины?
Заподозрить перитонеальный канцероматоз можно с помощью УЗИ, КТ и МРТ брюшной полости и малого таза.
В частности, КТ брюшной полости позволяет приблизительно оценить, насколько опухоль распространена. МРТ будет эффективнее для осмотра малого таза и позволит врачу оценить степень поражения находящихся там органов, например матки, мочевого пузыря.
Однако эти методы позволяют обнаружить только крупные очаги — опухолевые узлы до 5 мм редко отчетливо видны во время УЗИ, КТ и МРТ. Наибольшей точностью обладает лапароскопия: через прокол врач вводит в брюшную полость камеру, осматривает брюшину и, если необходимо, проводит биопсию — забирает часть опухоли на исследование.
Почему канцероматоз брюшины сложно лечить?
«Традиционные» методы лечения онкологических заболеваний — лучевая терапия, операция — не эффективны в случае с канцероматозом брюшины. Облучать такую большую область слишком опасно. Не все опухолевые очаги можно удалить хирургическим путем — метастазы могут быть очень маленького размера, незаметными для врача, или располагаться в труднодоступном месте. Оставшиеся опухолевые клетки спровоцируют рецидив заболевания.
Стандарты лечения канцероматоза брюшной полости включают системную химиотерапию, облегчение симптомов. В последние годы в списке методов появились циторедуктивная операция и HIPEC — гипертермическая внутрибрюшинная химиотерапия.
Что такое циторедуктивная операция и HIPEC?
Циторедуктивная операция подразумевает удаление всех видимых опухолевых очагов на брюшине. Гипертермическая внутрибрюшинная химиотерапия (HIPEC) — завершающий этап операции, который нужен, чтобы убить максимальное количество оставшихся микроскопических опухолевых клеток, снизив вероятность рецидива.
Для этого брюшную полость пациента промывают нагретым до 42°C градусов раствором химиопрепаратов. В брюшную полость устанавливают катетеры, через которые в организм пациента попадает раствор. Такой способ введения позволяет охватить все отделы брюшной полости. Для отслеживания температуры в брюшную полость помещают датчики.
Местное, а не системное (внутривенное) применение цитостатиков позволяет увеличить дозу препаратов и при этом избежать побочных явлений. Высокая температура в сочетании высокими дозами химиотерапии усиливают противоопухолевый эффект.
Спустя примерно час–полтора раствор удаляют из брюшной полости, промывают ее физраствором и зашивают. В общей сложности такое вмешательство занимает 8–10 часов.
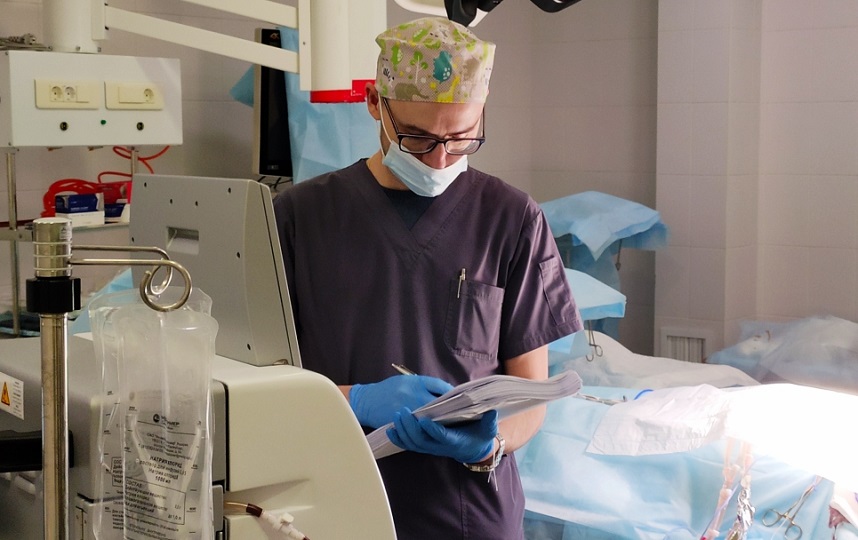
Техник наблюдает за процессом HIPEC-терапии
Кому может подойти такой метод лечения?
Отдельные исследования и мета-анализы демонстрируют эффективность этого метода — циторедуктивная операция в сочетании с гипертермической внутрибрюшинной химиотерапией увеличивает продолжительность жизни пациентов с перитонеальным канцероматозом. Например, в этом исследовании приняли участие пациентки с III стадией эпителиального рака яичников. Авторы приходят к выводу, что добавление гипертермической внутрибрюшинной химиотерапии к циторедуктивной операции увеличивает период без прогрессирования заболевания, общую продолжительность жизни и не повышает количество побочных эффектов по сравнению с циторедуктивной операцией.
Эта лечебная опция считается оптимальным вариантом лечения пациентов с опухолями аппендикса и псевдомиксомами брюшины.
Предполагается также, что профилактическое применение HIPEC может снизить риск развития канцероматоза брюшины в будущем. Не так давно появились данные о положительных результатах профилактического применения HIPEC при раке ободочной кишки, желудка и поджелудочной железы.
Кому циторедуктивная операция и HIPEC не подходят?
Необходимость таких вмешательств определяется исходя из истории болезни, тщательного обследования и общего состояния пациента. Циторедуктивную операцию в сочетании с HIPEC могут не провести, если:
— метастазы вышли за пределы брюшины
— заболевание прогрессирует несмотря на проведенную ранее химиотерапию
— есть кишечная непроходимость, вызванная опухолью
— общее состояние пациента тяжелое
— есть высокая опухолевая нагрузка — опухолевые импланты покрывают значительную часть толстой и тонкой кишки
В целом, исследования, оценивающие эффективность метода, как правило, основаны на результатах нерандомизированных испытаний.
Безопасность процедуры пока изучается. Например, авторы этого исследования пришли к выводу, что циторедуктивная операция в сочетании с HIPEC безопасна и чаще даже безопаснее в сравнении с другими широко распространенными онкологическими процедурами, в частности, операцией Уиппла (способ лечения рака поджелудочной железы — прим. ред.). Однако и сами авторы, и их коллеги отмечают, что у исследования есть недостатки, прежде всего, касающиеся выбора пациентов. У людей с раком поджелудочной железы в большинстве случаев нет других альтернатив, кроме операции Уиппла, а пациенту с перитонеальным канцероматозом можно предложить несколько вариантов: паллиативную терапию, циторедуктивную операцию без HIPEC, — чтобы выбрать оптимальный в конкретном случае способ лечения.
Кроме того, не существует единых протоколов, регламентирующих такое лечение: во время HIPEC могут использоваться различные химиопрепараты, температура, время промывания брюшной полости.
Таким образом, окончательное решение о выборе стратегии лечения пациент и врач должны принять, взвесив все «за» и «против».
Проконсультировать по вопросам назначения циторедуктивной операции в сочетании с HIPEC смогут специалисты Онкоцентра «СМ-Клиника». Врачи Онкоцентра оказывают различные виды помощи пациентам с онкологическими заболеваниями, в том числе проводят циторедуктивные операции с последующей процедурой HIPEC.

Канцероматоз брюшины
Канцероматоз — вариант метастазирования злокачественных опухолей, при котором новые очаги возникают на тех или иных серозных оболочках. Поражению может подвергаться париетальная плевра, оболочки головного мозга, сальник. Однако чаще всего опухоль затрагивает брюшину. Согласно статистике, новообразования желудочно-кишечного тракта на последних стадиях сопровождаются париетальным канцероматозом в 39–40 % случаев. Несколько реже причиной патологии становятся онкологические процессы женской половой системы. Например, карцинома яичников. В редких случаях вторичные очаги образуются на фоне первичной опухоли брюшины.
Развитие канцероматоза одинаково часто происходит у мужчин и женщин. В группу риска входят все больные, страдающие злокачественными новообразованиями, однако наибольшая вероятность этого осложнения присутствует у пациентов с раком желудка, поджелудочной железы, аппендикса, яичников. Вторичное опухолевое поражение брюшины считается неблагоприятным признаком. Оно практически не поддается хирургической коррекции, что в значительной степени ограничивает возможности лечения и требует тщательного подбора консервативной терапевтической схемы.
Причины появления
Образование вторичных опухолей на брюшине происходит по общему принципу формирования метастазов. Сначала клетки на поверхности первичного новообразования теряют связь с ним и меняют свою структуру с эпителиальной на мезенхимальную. После этого происходит их отделение и перемещение с током серозной жидкости к брюшине. Здесь клетки прикрепляются к здоровым тканям и с помощью определенных механизмов передают им информацию о собственных особенностях и структуре. Начинается развитие новой опухоли.
На начальном этапе канцероматоза рост происходит сверху вниз, во многом под влиянием силы тяжести. В дальнейшем его направление меняется и приобретает восходящую направленность. Нужно заметить, что в некоторых случаях причиной обсеменения брюшины опухолевыми клетками становится не их самостоятельное распространение, а манипуляции с первоначальным очагом в ходе хирургического вмешательства. Считается, что при лапароскопических операциях риск составляет 10–15 %, при открытых — 45–60 %.
Классификация
Единого подхода, позволяющего четко классифицировать канцероматоз, не существует. Наиболее распространенным является деление по локализации и объему вторичных очагов, разработанное Японской ассоциацией по лечению рака желудка. В соответствии с ним различают следующие стадии заболевания:
- P1 — брюшина поражена на ограниченном участке;
- P2 — присутствует несколько очагов, однако между ними есть здоровые зоны;
- P3 — брюшина поражена в значительной степени, отмечаются множественные сливающиеся опухоли.
На практике применяется и другой вариант классификации, основанный на количестве и размерах опухолей:
- 0 стадия. Нет видимых новообразований, однако могут присутствовать изменения на клеточном уровне.
- I стадия. Диссеминаты имеют ограниченное распространение и размер не более 5 мм.
- II стадия. Новообразования размером до 5 мм присутствуют на нескольких участках.
- III стадия. Зона поражения ограничена, однако размеры опухолей находятся в пределах 5–20 мм.
- IV стадия. Вторичные опухоли более 5 мм, независимо от их количества и площади распространения.
Симптомы и диагностика
Клиника перитонеального канцероматоза определяется картиной асцита. У пациента обнаруживаются такие симптомы, как:
- быстрое увеличение размеров живота;
- чувство распирания;
- выпячивание пупка;
- притупление перкуторного звука;
- флюктуация при пальпации;
- пальпаторно определяемые опухоли при достижении ими большого размера.
Помимо сказанного, могут присутствовать признаки общетоксического и паранеопластического синдромов: слабость, утомляемость, повышение температуры тела, головокружения, рвота и тошнота, отсутствие аппетита. Диагноз ставится на основании визуализирующих методов исследования: УЗИ органов живота, МРТ или КТ. Наиболее точным способом выявления канцероматоза считают лапароскопию с забором асцитической жидкости и ее последующим анализом в лаборатории для поиска измененных клеток.
Лечение
Лечение канцероматоза брюшины производится путем комбинированного хирургического и терапевтического воздействия. В первую очередь осуществляется удаление первичного рака и резекция брюшины с ликвидацией всех опухолевых очагов или только тех, которые представляется возможным устранить. Во всех случаях показана послеоперационная химиотерапия, позволяющая уничтожить оставшиеся в брюшной полости патологические клетки. Наиболее эффективным считается метод гипертермической интраперитонеальной химиотерапии, который представляет собой промывание пораженных зон подогретым до 39–43 °C раствором цитостатических препаратов. Чаще применяются средства на основе платины. Прогревание усиливает проникновения препарата в ткани за счет снижения интерстициального давления в опухоли, а местное применение дает возможность использовать более высокие дозировки лекарств. Также допускается применение фотодинамической терапии, однако ее эффективность недостаточно высока в связи с тем, что она не останавливает процессы формирования сосудов опухоли.
К числу новых методов, на настоящий момент не входящих в клинические рекомендации РФ, однако активно применяющихся в Европе, относятся:
- АЛФДТ — усовершенствованный вариант фотодинамической терапии, обладающий большей эффективностью за счет более глубокого проникновения луча, активации фотосенсибилизатора и лимфодренажного эффекта;
- микотерапия — воздействие на опухоль компонентами лекарственных грибов;
- гипертермия — прогревание организма для усиления эффективности химиопрепаратов;
- фитотаргетная терапия — лечение с помощью растительных средств;
- активационная терапия — использование биостимуляторов для активации собственных защитных механизмов;
- онкопсихология — важная составляющая лечения, позволяющая пациенту справиться с переживаниями и повысить качество жизни.
Инновационные способы обычно применяются в сочетании с традиционными вариантами терапии, усиливая их действенность и способствуя улучшению прогноза. В качестве самостоятельного лечения они не используются.
Экспертное мнение

Купов Сергей Сергеевич
к.м.н., Врач-онколог
Некоторые новые варианты терапии канцероматоза основаны на давно известных рецептах. Так, токсины грибов применялись для лечения опухолей со времен средневековья, а лекарственные растения тысячелетиями используются в китайской медицине. В чистом виде они не всегда эффективны. Однако средства на их основе, должным образом подготовленные и имеющие необходимую концентрацию, являются в разы более действенными. Сегодня это направление набирает популярность в качестве вспомогательной терапии, однако нельзя исключить, что в дальнейшем получится использовать их и как основном метод борьбы со злокачественными новообразованиями.
Прогноз
Прогноз при канцероматозе брюшины зависит от тяжести течения болезни, количества, размера и локализации очагов. В любом случае это достаточно серьезное проявление онкологии, требующее грамотного подхода к лечению. Продолжительность жизни пациента также зависит от этих факторов, от цитогенетических особенностей и локализации первичной опухоли. На сегодняшний день продолжается поиск более эффективных методик борьбы с рассмотренной проблемой. Предпринимаются попытки таргетного лечения с учетом генетики опухоли, используются новые и совершенствуются старые способы решения проблемы. Пациенту необходимо бороться с болезнью всеми доступными средствами. Шансы на спасение остаются всегда.
Вопросы и ответы
В каких клиниках в Москве можно пройти лечение с помощью гипертермии?
Первой и единственной на сегодняшний день клиникой, применяющей интегративные методики, является медицинский центр Onco.Rehab в Орехово-Зуево. Мы проводим все приведенные в тексте способы лечения, что позволяет добиваться лучших, чем при использовании только традиционной терапии, результатов.
Канцероматоз брюшины — это приговор?
Нет. Но это проблема, которая требует крайне серьезного лечения и длительной борьбы. Использование интегративных методов в сочетании с классическим подходом повышает шансы пациента на жизнь. Однако успех во многом зависит от стадии заболевания.
Можно ли избежать развития перитонеального канцероматоза?
Канцероматоз при онкологических болезнях возникает не сразу. Снизить вероятность его развития можно, если своевременно начать лечение, которое окажется успешным.
Количество показов: 1263
Канцероматоз брюшины
Канцероматоз брюшины – вторичное злокачественное поражение брюшины, являющееся следствием диссеминации эпителиальных опухолей желудочно-кишечного тракта, репродуктивной системы, реже – первичных перитонеальных новообразований. Признаками канцероматоза брюшины являются асцитический синдром, прогрессирующее снижение веса, тошнота, слабость. Диагностика основана на визуализации очагов поражения при проведении МСКТ, УЗИ органов брюшной полости, лапароскопии, цитологическом анализе асцитической жидкости. Лечение включает хирургическое удаление первичного очага с метастазами по брюшине и химиотерапию. Прогноз неблагоприятный.
Общие сведения
Канцероматоз брюшины – наиболее часто встречающийся вариант метастазирования онкологических заболеваний различной локализации. Согласно имплантационной теории развития данной патологии, источником поражения являются опухолевые клетки, которые отделились от первичного очага и попали в брюшную полость с серозной жидкостью. Основным пусковым механизмом данного процесса является утрата клетками опухоли факторов межклеточной адгезии.
Согласно данным статистики, канцероматоз брюшины встречается у 20-35% пациентов с онкопатологией: в 40% случаев данное осложнение формируется при опухолях желудочно-кишечного тракта, в 30% — при раке яичников (причем на момент верификации диагноза рака яичников у подавляющего большинства пациенток уже имеет место поражение брюшины). Канцероматоз брюшины является неблагоприятным прогностическим фактором; данная форма прогрессирующего опухолевого поражения практически не поддается хирургическому лечению, а химиотерапия улучшает состояние лишь на некоторое время.
Канцероматоз брюшины
Причины канцероматоза
Канцероматоз брюшины является вторичным опухолевым поражением, результатом прогрессирования рака различной локализации. Наиболее часто поражением брюшины осложняется рак желудка, тонкого кишечника, поджелудочной железы, злокачественные опухоли яичников, матки, маточных труб, печеночноклеточный рак, реже — первичные опухоли брюшины (перитонеальная мезотелиома). В ряде случаев первичный очаг остается неустановленным.
Развитие канцероматоза брюшины является поэтапным процессом. Первый этап – распространение опухолевых клеток из первичного очага поражения. Это связано с нарушением межклеточного взаимодействия и приобретением клетками опухоли подвижности. При этом эпителиальные клетки меняют фенотип на мезенхимальный, происходит деградация межклеточного матрикса. Распространение опухолевых клеток может происходить в ходе оперативного вмешательства. Их механическое отделение возможно при повреждении лимфатических или кровеносных сосудов. Попавшие в брюшную полость клетки опухоли мигрируют под действием силы тяжести, сокращений внутренних органов, имплантируются в местах повышенной резорбции: большом сальнике, в области слепой кишки, дугласовых карманах.
На втором этапе опухолевые клетки взаимодействуют с мезотелием брюшины. Механизмы адгезии определяются природой клеток, особенностями морфологии брюшины, а также наличием участков ее повреждения. Далее клетки закрепляются в мезотелии, происходит их горизонтальное распространение по поверхности перитонеума, а затем инвазивный рост – прорастание в базальную мембрану, соединительную ткань. Следующим этапом является стимуляция неоангиогенеза – обязательного фактора развития опухоли. Морфопатогенетические механизмы формирования канцероматоза брюшины еще недостаточно изучены, в связи с чем отсутствуют радикальные методы лечения.
Частота развития канцероматоза брюшины зависит не только от первичной локализации опухоли, но и от ее размеров, глубины инвазии, гистотипа, степени дифференцировки (недифференцированный рак желудка осложняется поражением брюшины в 60% случаев, ограниченный – в 15%).
Классификация
Единая классификация данного заболевания отсутствует, поскольку характеристики первичных опухолей, приводящих к поражению брюшины, весьма разнообразны. Наиболее распространена классификация канцероматоза брюшины в зависимости от числа, локализации метастазов, которая предусматривает три степени:
- Р1 – локальное поражение брюшины
- Р2 – несколько областей канцероматоза, разделенных здоровыми участками брюшины
- Р3 – многочисленные очаги поражения
Также используется метод определения индекса канцероматоза брюшины: суммируются баллы измерения максимальных очагов поражения (0-3 балла) в каждой из 13 наиболее вероятных областей поражения брюшины.
Симптомы канцероматоза
Канцероматоз брюшины является вторичным поражением, поэтому его клиническая картина во многом определяется проявлениями первичной опухоли. Характерным признаком является обильный выпот в брюшную полость – формирование асцита. Зачастую асцитический синдром, развивающийся вследствие обструкции лимфатического дренажа, является единственным признаком заболевания, и пациенты могут поступать в отделение гастроэнтерологии или терапии для диагностики причин асцита. Состояние больных тяжелое, характерна значительная потеря веса. Неспецифическими признаками являются тошнота, рвота, выраженная слабость, утомляемость. При наличии крупных метастазов возможно их прощупывание через брюшную стенку.
Диагностика
Канцероматоз брюшины имеет неспецифическую клиническую картину, однако консультация гастроэнтеролога или онколога позволяет предположить данное заболевание на основании симптомов и физикальных данных. Лабораторные анализы не выявляют специфических изменений: определяется лейкоцитоз, ускорение СОЭ. Диагностическая программа обязательно должна включать УЗИ органов брюшной полости и малого таза, позволяющее обнаружить распространенное поражение, а также МСКТ брюшной полости с контрастированием. Обязательно проводится цитологическое исследование асцитической жидкости, полученной при лапароцентезе, которое дает возможность впервые установить или подтвердить диагноз, а также определить гистогенез клеток опухоли.
Информативным методом диагностики канцероматоза брюшины является лапароскопия с осмотром перитонеума, дугласова пространства, диафрагмы, сопровождающаяся биопсией. Высокой специфичностью обладает обратнотранскриптазная полимеразная цепная реакция (ОТ-ПЦР), которая позволяет определить источник диссеминации даже при малом количестве опухолевых клеток.
Сложности диагностики возникают при наличии канцероматоза брюшины без выявленного первичного очага. Данная форма заболевания, встречающаяся в 3-5 % случаев, проявляется клинически только при уже сформировавшемся поражении брюшины. При этом первичный очаг может иметь настолько малые размеры, что его прижизненное обнаружение невозможно.
В качестве дополнительных методов может использоваться определение онкомаркеров (кислой фосфатазы, раково-эмбрионального антигена, альфа-фетопротеина, бета-субъединицы ХГЧ). Такая диагностика не обладает высокой специфичностью, но применяется для оценки прогноза, раннего выявления диссеминации, рецидивов, а также для контроля эффективности лечения.
Лечение канцероматоза брюшины
Хирургическое лечение канцероматоза включает удаление первичной опухоли с регионарными метастазами и отсевами по брюшине. Циторедуктивная операция выполняется в объеме перитонэктомии, может сочетаться с удалением матки и придатков, сигмовидной кишки, желчного пузыря. После проведения операции оценивается индекс полноты циторедукции: СС-0: после проведения хирургического лечения очаги поражения визуально не определяются; СС-1: имеются неудаленные очаги диаметром до 2,5 мм; СС-2: очаги диаметром 2,5 мм – 2,5 см; СС-3: очаги поражения более 2,5 см в диаметре. Однако даже при определении индекса СС-0 нельзя полностью исключить возможность диссеминации, поэтому обязательно проводится химиотерапия.
Системная химиотерапия при канцероматозе брюшины имеет определенные недостатки. На сегодняшний день эффективным методом лечения является интраперитонеальная химиотерапия. При местном введении цитостатических препаратов есть возможность применения высоких дозировок, которые при системной терапии слишком токсичны. Использование гипертермии усиливает поступление активных веществ в опухолевые клетки. Существенным преимуществом является длительное нахождение препарата в брюшной полости. Гипертермическая внутрибрюшная химиотерапия проводится в ходе операции или после ее завершения; химиотерапевтический агент (чаще препараты платины) вводится подогретым до температуры 40-43 градуса. Время циркуляции раствора составляет 30-90 минут.
Альтернативным методом лечения канцероматоза брюшины является фотодинамическая терапия с локальным или системным введением фотосенсибилизатора. Данная методика основана на интраоперационном световом воздействии с применением лазера, которое приводит к прямому повреждению мембран опухолевых клеток. Но такое лечение не устраняет процессы ангиогенеза, поэтому его эффективность недостаточно высока.
Ни один из существующих на сегодняшний день методов лечения канцероматоза брюшины не вызывает полную регрессию опухолевых диссеминантов, а также не предупреждает рецидивирование заболевания, поэтому разработка оптимального лечения продолжается. Исследуется таргетная терапия, целью которой являются молекулярные мишени. Низкая эффективность противоопухолевой терапии обусловлена отсутствием достаточного понимания морфологии и патогенеза заболевания, унифицированной классификации, разнородностью первичных опухолей.
Прогноз и профилактика
Развитие канцероматоза брюшины при злокачественных новообразованиях всегда является неблагоприятным прогностическим признаком. Средняя продолжительность жизни пациентов составляет не более 12 месяцев, а пятилетняя выживаемость – до 10%. Не существует специфической профилактики данной формы поражения брюшины, важную роль играет своевременность выявления и адекватного лечения первичных опухолей. Однако во многих случаях симптомы канцероматоза брюшины возникают уже при значительной диссеминации раковых клеток по брюшной полости.