ПОДПИСЫВАЙТЕСЬ
последние новости Sputnik V
Оставьте свой e-mail для получения новостей
СПУТНИК ЛАЙТ, ПЕРВЫЙ КОМПОНЕНТ СПУТНИК V, ЭТО БЕЗОПАСНАЯ И ЭФФЕКТИВНАЯ ОТДЕЛЬНАЯ ОДНОКОМПОНЕНТНАЯ ВАКЦИНА ПРОТИВ COVID-19, А ТАКЖЕ ИДЕАЛЬНЫЙ БУСТЕР
- Эффективность против заражения более 80%
- Эффективность как отдельной вакцины против заражения штаммом Дельта -70%
- Для возрастной группы до 60 лет эффективность более 75%
- Эффективность вакцины против госпитализации и тяжелых случаев еще выше
Подробнее
ОФИЦИАЛЬНЫЕ ДАННЫЕ ПО РЕЗУЛЬТАТАМ ПРИМЕНЕНИЯ ВАКЦИНЫ «СПУТНИК V» В МИРЕ
В первую годовщину регистрации вакцины «Спутник V» данные о применении препарата в ключевых странах свидетельствуют о его высокой безопасности и эффективности.
Подробнее
НАУЧНЫЕ ИССЛЕДОВАНИЯ ВАКЦИН «СПУТНИК V» И «СПУТНИК ЛАЙТ»
Безопасность и эффективность вакцин «Спутник V» и «Спутник Лайт» были подтверждены многочисленными публикациями в крупнейших международных научных журналах, включая The Lancet и Vaccines.
Подробнее
ПРОВЕРЕННАЯ ТЕХНОЛОГИЯ ИСПОЛЬЗОВАНИЯ ВЕКТОРОВ НА БАЗЕ АДЕНОВИРУСОВ ЧЕЛОВЕКА
Технология использования аденовирусных векторов в качестве векторных вакцин развивается с 80-х годов прошлого века, является безопасной и эффективной, что подтверждается в многочисленных исследованиях.
Подробнее
О ЦЕНТРЕ ИМ. Н.Ф. ГАМАЛЕИ
Национальный исследовательский центр эпидемиологии и микробиологии имени почётного академика Н. Ф. Гамалеи, основанный в 1891 году, является ведущим в своей сфере исследовательским учреждением в мире.
Центр обладает одной из уникальных коллекций вирусов, а также имеет собственную линию по производству вакцин. Центр имени Н.Ф. Гамалеи успешно разработал и зарегистрировал две вакцины против лихорадки Эбола, используя векторы на основе аденовируса.
Подробнее
КЛИНИЧЕСКИЕ ИСПЫТАНИЯ
Вакцина получила свидетельство о регистрации от Минздрава России, и в соответствии с правилами, принятыми во время пандемии, может использоваться для вакцинации населения в России. «Спутник V» — одна из трех вакцин в мире, эффективность которых превышает 90%. Результаты исследования эффективности вакцины «Спутник V» прошли сравнительную международную оценку, полученные данные опубликованы в журнале The Lancet.
Подробнее
ПАРТНЕРСТВА
Россия открыта для международного сотрудничества в борьбе с глобальной угрозой пандемии COVID-19 и других эпидемий в будущем. Мы активно сотрудничаем с более чем 14 странами в рамках производства нашей вакцины за рубежом, включая Индию, Китай, Бразилию, Мексику, Египет, Иран, Италию, Южную Корею, Аргентину, Казахстан, Республику Беларусь, Сербию, Турцию, Вьетнам и другие. Мы будем рады заинтересованным партнерам, которые готовы присоединиться к этой инициативе и помочь нам в спасении человеческих жизней.
Подробнее
КОММЕНТАРИИ ЭКСПЕРТОВ
Мари-Поль Киени
Директор по исследованиям французского Медицинского научно-исследовательского института INSERM
…научные публикации Института имени Гамалеи подтверждают данные Российского фонда прямых инвестиций (РФПИ) об эффективности вакцины «Спутник V» против коронавирусной инфекции.
Хьюго Пицци
Инфекционист, эпидемиолог, магистр общественного здравоохранения и профессор Национального университета Кордобы
Таким образом, наличие двух различных типов вирусных векторов обеспечивает возможность более надежной иммунизации людей. И сейчас в мире пристальное внимание направлено на выяснение возможности комбинировать вторую дозу одной марки с первой дозой другой марки, но, в целом, я убежден в том, что нужно уважать создателей.
Наши данные, полученные во время использования вакцины «Спутник V» в Бахрейне, подтверждают ее высокую эффективность и безопасность. Эта вакцина является одной из разрешенных к использованию, доступных жителям и резидентам Королевства бесплатно.
Мухаммед Ахмед аль-Джабер
Посол ОАЭ в России
Последний этап исследований и клинических испытаний показала, что эффективность вакцины «Спутник V» составляет 91,4%; при этом вакцина предотвращает 100% серьезных случаев течения заболевания.
С первых дней пандемии Россия и ОАЭ подчеркивают важность совместных усилий по борьбе с распространением коронавируса.
Гергей Гульяш
Депутат Национального собрания Венгрии
Результаты всех исследований будут оглашены; однако согласно имеющимся на сегодня данным, по результатам вакцинирования некоторыми вакцинами в объеме более полумиллиона доз, в другом случае – в объеме одного миллиона доз, можно сказать, что «вакцина производства Sinopharm лучше, чем Pfizer, а Спутник – самый лучший».
Петер Альтмайер
Министр экономики
Как Германия, так и Россия, с «Biontech» и «Спутник V», входят в число пионеров разработки вакцин против коронавируса. Разумеется, в Европейском союзе необходимо разрешить «Спутник V».
Альберто Фернандес
Президент Аргентины
Мы рады возможности производить вакцину «Спутник V» в Аргентине. Мы уже используем ее для защиты большой части нашего населения и видим отличные результаты. Производство вакцины у нас станет отличной возможностью добиться новых побед в борьбе с пандемией не только в Аргентине, но в Латинской Америке в целом.
Наор Бар-Зеев
Международный центра доступа к вакцинам Блумбергской Школы общественного здравоохранения Университета Джона Хопкинса
Том Инглесби
Директор Центра безопасности здоровья Блумбергской Школы общественного здравоохранения Университета Джона Хопкинса
Исследования Логунова и его коллег имеют несколько сильных сторон. Во-первых, аденовирусы широко распространены, поэтому люди не могут быть интактными в иммунологическом отношении. Вторая сильная сторона — это порог нейтрализации, который используется в двух исследованиях. Третья сильная сторона заключается в том, что эта вакцина, как и предыдущие, вызвала широкий иммунный ответ. Хотя это не акцентируется, результаты предполагают ответ, взвешенный по T-хелперам 1-го типа, который может быть важен для безопасности вакцины, потенциально снижая риск антителозависимого усиления инфекции. Четвертой сильной стороной стала разработка двух форм вакцины — замороженной и лиофилизированной. Лиофилизированная форма вакцины может обеспечить в рамках существующих температурных возможностей глобальной логистической цепи стабильность, которая необходима для сохранения эффективности вакцины во время ее доставки от завода-изготовителя к получателю. Другим вакцинам только предстоит решить эту задачу. Несмотря на то, что массовое производство будет обходится дороже, стабильность продукта позволит доставить его в удаленные регионы, что необходимо для обеспечения равномерного и равноправного доступа.
Надей Хаким
Вице-президент Британского Красного Креста, вице-президент Международной академии медицинских наук
Результаты клинических испытаний российской вакцины «Спутник V» продемонстрировали впечатляющие результаты, признанные мировым медицинским сообществом. Доказано, что вакцина безопасна и эффективна без выявленных серьезных побочных эффектов, и в ней используется проверенная платформа, основанная на аденовирусных векторах человека, которые в настоящее время являются наиболее безопасным механизмом для введения генетического кода вирусного шипа в организм человека. Этот подход тщательно изучен не только в России, но и за рубежом. Россия имеет длительный и успешный опыт разработки вакцин и остается мировым лидером в этой области. Мы надеемся, что вакцина скоро станет доступной по всему миру, чтобы помочь остановить разрушительную пандемию и позволить людям вернуться к нормальной жизни.
Мухаммад Мунир
Лектор по молекулярной вирусологии Университета Ланкастера
Ряд особенностей делают «Спутник V» очень перспективным. Идея использования двух разных аденовирусов в качестве вектора превосходит многие передовые вакцины. Как правило, иммунная система воспринимает векторные белки как антиген, аналогичный белку S SARS-CoV-2, поэтому она также вызывает иммунный ответ против этих белков. Если люди реиммунизируются (в качестве второй дозы или повторной вакцины), ранее существовавший иммунитет может поставить под угрозу эффективность второй дозы вакцины. Использование вектора другой природы, как в Sputnik V, позволит избежать этой проблемы.
Брендан Врен
Профессор микробного патогенеза Лондонской школы гигиены и тропической медицины
Данные об исследованиях российской вакцины, опубликованные the Lancet, обнадеживают, демонстрируя безопасность и иммуногенность вакцин против COVID-19 на основе аденовируса
Полина Степенски
Заведующая отделением трансплантации костного мозга и иммунотерапии клиники Хадасса, Израиль
Первое, что надо сказать российским ученым и медикам, это «браво!». Эту технологию и научный подход мы прекрасно понимаем и абсолютно одобряем. Вы совершили настоящий прорыв в науке и медицине. Мы благодарны вам за то, что вы сделали замечательную работу.
Замечательно, что вырабатывается устойчивый и гуморальный, и клеточный иммунный ответ. Это обеспечивается за счет использования двух разных векторов, доставляющих препарат и, одновременно, решающих проблему возможного нейтрализующего эффекта при второй инъекции. Доказана очень высокая эффективность двух подобранных аденовирусов. Таким образом, используемая институтом Гамалеи платформа — это правильная платформа.
Проделанная работа вызывает большое уважение, а сам препарат – достоин изучения и применения.
РИА Новости
17.08.2020
Стефан Гайе
Профессор Страсбургского университета
Речь идёт о ценной и эффективной вакцине, которую я лично очень жду. Мне очень интересна работа, проделанная русскими исследователями. Я понял, что используется один из самых продвинутых методов, метод аденовирусного вектора.
Фабио Вилаш-Боаш
Министр здравоохранения штата Баия
Правительство штата Баия, Бразилия, высоко оценивает подписанное соглашение с суверенным фондом Российской Федерации, которое обеспечит доступ к вакцине «Спутник V» для народа Бразилии, как только будет получено одобрение национальных регулирующих органов. Вакцина создана на основе человеческих аденовирусов, что является одной из наиболее безопасных и эффективных платформ в мире. Мы считаем, что третья фаза продолжающихся клинических испытаний подтвердит данные, полученные в рамках фаз 1 и 2
Г.В. Прасад
Со-председатель совета директоров и управляющий директор Dr. Reddy’s
Мы рады сотрудничеству с РФПИ для поставок вакцины в Индию. Результаты фаз 1 и 2 клинических исследований были обнадеживающими, и мы начнем проводить фазу 3 исследований в Индии для выполнения требований регуляторов страны. Вакцина «Спутник V» станет надежным инструментом в борьбе с коронавирусом в Индии.
Шавкат Исмаилов
Председатель правления группы компаний LAXISAM
Важная роль принадлежит сотрудничеству с РФПИ по вакцине «Спутник V», которая создана российскими учеными на базе передовых научных и клинических исследований
Чжун Наньшань
Директор Центра исследований респираторных заболеваний Гуанчжоу, Китай
Высоко оцениваю разработанную Центром Гамалеи вакцину от Covid-19. Поздравляю вашу страну с государственной регистрацией препарата. Российская аденовирусная вакцина является безопасной и должна успешно завершить клинические испытания.
РИА Новости
20.08.2020
Хильдеганд Эртл
Профессор, Центр вакцин и иммунотерапии, Институт Вистар, Филадельфия, США
Из того, что я видела, это, пожалуй, наиболее многообещающая платформа.
C&EN
12.05.2020
Ян Джонс
Профессор вирусологии университета Рединга, Великобритания
Имеется достаточно информации о рекомбинантных вакцинах на основе аденовирусов, чтобы говорить о безопасности самой вакцины при обычной ее дозировке.
BusinessDay
20.08.2020
Ашвани Махаджан
Соучредитель исследовательского центра Свадеши, Индия
Когда решен вопрос с эффективностью, то встает вопрос цены. Считаю, что на оба эти вопроса российская вакцина даст хороший ответ.
Sputnik
20.08.2020
https://ria.ru/20210701/sputnikv-1739169613.html
«Спутник V». Все о первой российской вакцине от коронавируса
Гам-КОВИД-Вак (Спутник V) — что это за вакцина, противопоказания, отзывы привитых
«Спутник V». Все о первой российской вакцине от коронавируса
Гам-КОВИД-Вак», известная также как «Спутник V», — первая зарегистрированная в мире вакцина для профилактики COVID-19. По оценкам разработчиков, препарат… РИА Новости, 02.07.2021
2021-07-01T08:00
2021-07-01T08:00
2021-07-02T18:17
наука
министерство здравоохранения рф (минздрав россии)
федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека (роспотребнадзор)
здоровье
российский фонд прямых инвестиций
биология
вакцины
нии им. гамалеи (национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика н.ф.гамалеи)
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/07e4/0c/1c/1591207795_0:147:3072:1875_1920x0_80_0_0_b1334d2c50f7aef1b5466f0485702743.jpg
МОСКВА, 1 июл — РИА Новости. «Гам-КОВИД-Вак», известная также как «Спутник V», — первая зарегистрированная в мире вакцина для профилактики COVID-19. По оценкам разработчиков, препарат эффективен против всех выявленных штаммов коронавируса SARS-CoV-2, а ее облегченный вариант «Спутник Лайт» идеально подходит для ревакцинации.Что такое «Гам-КОВИД-Вак»»Гам-КОВИД-Вак», или «Спутник V», — первая российская вакцина против ковида, созданная в Центре эпидемиологии и микробиологии имени Н. Ф. Гамалеи. Она относится к классу векторных вакцин. Зарегистрирована 11 августа 2020 года. Состав вакцины «Спутник V»Вакцина состоит из неспособного размножаться аденовируса человека. Этот возбудитель не опасен, он вызывает лишь легкую простуду. В его ДНК встроен ген белка-шипа коронавируса SARS-CoV-2. Белок связывается с рецепторами на поверхности клеток и помогает вирусу проникнуть внутрь. Именно на белок-шип реагирует наш иммунитет. Аденовирусный вектор при этом служит средством доставки.В вакцине используют вектор на основе двух разных штаммов аденовируса человека — 26-го и пятого серотипа (Ad26, Ad5). Выпускают препарат в виде раствора со вспомогательными веществами: например, трис, хлориды натрия и магния, сахароза, полисорбат, магний хлористый гексагидрат, ЭДТА, этанол, вода.Принцип действия и отличия от других вакцинРаствор вводят в мышцу, вскоре в месте укола начинается небольшое воспаление — организм распознает чужеродные вещества и отправляет туда лимфоциты. Аденовирус проникает в них и заставляет вырабатывать коронавирусный белок-шип. В свою очередь иммунитет отвечает целым коктейлем из антител.Антитела — это сигнальные белки, которые дают команды защитной системе организма. Если произойдет встреча с реальным SARS-CoV-2, они помогут его уничтожить. В результате человек не заболеет либо коронавирусная инфекция будет перенесена в легкой форме.В мире есть несколько векторных вакцин от коронавируса. Например, американская компания Johnson & Johnson создала препарат на основе аденовируса человека Ad26, а китайская CanSino Biologics — Ad5. Обе вводят однократно. В отличие от них «Спутник V» делают в два приема. После первой дозы, или, как говорят ученые, праймирующей иммунизации, у привитых формируется первичный, а после второй, бустерной, — вторичный иммунный ответ. Уникальность российской технологии в том, что в первой и второй дозах использованы разные вирусные векторы — сначала Ad26, затем Ad5. При такой схеме общий уровень иммунизации намного выше.Еще одну векторную вакцину разработала англо-шведская компания AstraZeneca. Однако в ней в качестве вектора используют аденовирус шимпанзе.По результатам клинических исследований, которые прошли международную оценку и опубликованы в журнале The Lancet, эффективность вакцины «Спутник V» против COVID-19 составляет 91,6 процента. И в ста процентах случаев она предотвращает развитие тяжелой формы ковида. Анализ данных о заболеваемости коронавирусом среди россиян, привитых обоими компонентами препарата в период с 5 декабря 2020-го по 31 марта 2021-го, показал, что реальная эффективность «Гам-КОВИД-Вак» еще выше — 97,6 процента.Инструкция по применениюПодготовка к вакцинацииНет никаких особенных требований при подготовке в прививке. Роспотребнадзор указывает — перед вакцинацией нет необходимости делать ПЦР-тест, чтобы исключить ковид, или анализ на антитела. Главное, в день вакцинации самочувствие должно быть хорошим.Однако, по мнению ряда экспертов, реакция организма на введение любой вакцины очень индивидуальна. Поэтому людям с серьезными хроническими болезнями нужно предварительно сходить на прием к лечащему врачу и убедиться, что их заболевание в стадии ремиссии и они сейчас не принимают никаких препаратов, которые могут помешать выработке иммунитета.Как делается прививка от коронавируса»Спутник V» предназначен для внутримышечного введения. Укол делают в дельтовидную мышцу плеча. Перед процедурой флакон или ампулу с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания, чтобы не осталось включений льда. Затем протирают снаружи спиртовой салфеткой и осторожно перемешивают содержимое, не допуская встряхивания. Размороженный препарат необходимо использовать в течение двух часов, снова замораживать его нельзя.Для выявления противопоказаний пациента перед вакцинацией должен осмотреть врач. Он опрашивает о самочувствии и контактах с инфицированными, измеряет температуру тела и уровень кислорода в крови. Если температура выше 37 градусов, прививку откладывают.Что нельзя делать после прививкиРекомендуют один день до и два дня после прививки воздержаться от употребления алкоголя, не переутомляться, избегать тяжелых физических нагрузок, снизить уровень стресса, хорошо высыпаться, не злоупотреблять солнечными ваннами, а в сам день вакцинации не посещать бани и бассейны, не купаться в природных водоемах.Ученые советуют есть побольше белковых продуктов — молочных, рыбы, нежирного мяса, поскольку они дают организму необходимый строительный материал для формирования защитных антител, а также богатые пищевыми волокнами пребиотики — овощи, цельнозерновые крупы, бобовые, зелень — и пробиотики — кефир, йогурт, простоквашу, квашеную капусту. Они нужны для поддержания кишечной микрофлоры, которая вносит большой вклад в выработку иммунного ответа на вакцину.Также важно после прививки соблюдать стандартные защитные меры: носить маски в людных местах, тщательно мыть руки, использовать антисептики. Интервал между прививкамиВакцинацию проводят в два этапа с интервалом 21 день: вначале компонентом I в дозе 0,5 миллилитров, затем, через три недели, — компонентом II в дозе 0,5 миллилитров.Когда появятся антитела к коронавирусуПо оценкам ученых, полноценный иммунитет возникает в среднем через 40 дней после первого укола. До истечения этого срока важно не только избежать заражения коронавирусом, но и не подхватить другую ОРВИ, энтеровирус или прочие инфекции. Они могут помешать эффективной выработке иммунитета после вакцинации. Побочные эффекты от вакцины «Спутник V»Клинические исследования показали, что чаще всего после вакцинации возникает гриппоподобный синдром — боль, отек и зуд в месте введения, общее недомогание, озноб, повышение температуры, боль и ломота в мышцах и суставах, головная боль, снижение аппетита. Состояние может длиться от одного до трех дней.Реже проявляются нарушения со стороны дыхательной системы — боль в ротоглотке, заложенность носа, першение в горле. Возможны головокружения, обмороки, тошнота, рвота, диспепсия. В памятке Минздрава указано, что при повышении температуры можно принять нестероидные противовоспалительные препараты, а при покраснении, отечности и болезненности места укола — антигистаминные средства. Никаких серьезных последствий, в том числе тяжелых аллергических реакций, не наблюдалось.Продолжительность действияПока точно не установлено, на какой срок защищает вакцина. Согласно предварительной оценке, антитела класса G у сотрудников Центра Гамалеи, получивших вакцину в порядке эксперимента в марте 2020-го, сохранялись и через девять месяцев. При этом титр антител был выше, чем у переболевших. Противопоказания для вакцинацииПротивопоказания к применению у «Спутника V» примерно такие же, как у всех остальных вакцин: тяжелые формы аллергии, инфекционные и неинфекционные заболевания в острой форме, грудное вскармливание. Прививаться можно всем взрослым старше 18 лет, без верхнего ограничения по возрасту. Детей пока не прививают — из-за отсутствия клинических испытаний, подтверждающих эффективность и безопасность вакцины для людей младше 18. Центр Гамалеи планирует в ближайшее время начать исследование по применению «Спутника V» у детей. Соответствующую заявку ученые подали в Минздрав России.Недавно ведомство разрешило «Спутник V» для беременных женщин с высоким риском тяжелого течения COVID-19. Инструкция рекомендует с осторожностью применять вакцину при хронических заболеваниях печени и почек, тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях центральной нервной системы, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах, а также при некоторых эндокринных заболеваниях, таких как выраженные нарушения функции щитовидной железы и сахарный диабет в стадии декомпенсации.Отмечено, что вакцинация может представлять определенный риск для пациентов со злокачественными новообразованиями и тяжелыми аутоиммунными заболеваниями, так как стимуляция иммунной системы может привести к обострению.А вот пациентам с сердечно-сосудистыми заболеваниями, диабетом, бронхиальной астмой, гепатитом С и онкозаболеваниями в стадии ремиссии, по мнению ученых, вакцинироваться необходимо.РевакцинацияОжидают, что коронавирус станет сезонным и прививаться от него нужно будет ежегодно. А во время обострения эпидемии — раз в шеть месяцев.Специалисты Центра Гамалеи и Минздрава рекомендуют проводить ревакцинацию «Спутником Лайт», которая в ближайшее время поступит в гражданский оборот. Ранее глава РФПИ Кирилл Дмитриев и владелец компании «Р-Фарм» — одного из производителей «Гам-КОВИД-Вак» — заявляли, что ревакцинироваться можно и первым компонентом «Спутника V».Отзывы привитых «Спутником V»»Сегодня привился «Спутником V». Чувствую себя хорошо. Коронавирусом я переболел, есть антитела. Но прививка необходима независимо от уровня титров. Все, кто еще не вакцинировался, — самое время это сделать», — написал врио главы Мордовии Артем Здунов в инстаграме.Врио губернатора Хабаровского края Михаил Дегтярев сделал прививку от ковида повторно. «Первый раз вакциной «Гам-Ковид-Вак» прививался в июле и августе прошлого года. По прошествии 11 месяцев количество антител в крови существенно снизилось, поэтому решил не рисковать ни своим здоровьем, ни здоровьем людей, с которыми работаю и с которыми встречаюсь каждый день», — рассказал он в Telegram-канале.Народные отчеты от вакцинации «Спутником V» публикуются в Telegram-канале @Sputnik_results. Вот несколько отзывов: «М 43, здоров. ГамКовидВакV1 — 16.03 без побочек, V2-07.04 легкая слабость на след день. Антитела на 28.06″.»Ж 22 года V1 28.06.21. В день прививки легкая слабость и сонливость, боль в месте укола».»М 65, системный васкулит (гранулематоз Вегенера) в ремиссии, V2 28.06.21, никаких симптомов, как и после первой дозы».Сертификация вакцины «Спутник V» в других странахВакцина одобрена в 67 странах с общим населением свыше 3,4 миллиарда человек. Так, имея сертификат о прививке «Спутником V», можно въезжать, например, в Грецию, Хорватию, на Кипр, в Турцию, Грузию. Пакет документов о сертификации «Спутника V» также предоставлен ВОЗ. Разработчики ожидают положительное решение в скором времени. В случае одобрения вакцинированные получат цифровые сертификаты, которые облегчат перемещение по странам ЕС.
https://ria.ru/20201225/vaktsina-1590616868.html
https://ria.ru/20210313/kovid-1600996928.html
https://ria.ru/20210413/privivka-1727931944.html
https://ria.ru/20201230/vaktsinatsiya-1591428753.html
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2021
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdnn21.img.ria.ru/images/07e4/0c/1c/1591207795_250:0:2673:1818_1920x0_80_0_0_40065ea61ff99bced84cbf06e94802b1.jpg
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
министерство здравоохранения рф (минздрав россии), федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека (роспотребнадзор), здоровье, российский фонд прямых инвестиций, биология, вакцины, нии им. гамалеи (национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика н.ф.гамалеи), коронавирус covid-19, вакцина «спутник v», вакцинация россиян от covid-19, вакцина «спутник лайт»
Наука, Министерство здравоохранения РФ (Минздрав России), Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор), Здоровье, Российский фонд прямых инвестиций, биология, Вакцины, НИИ им. Гамалеи (Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф.Гамалеи), Коронавирус COVID-19, Вакцина «Спутник V», Вакцинация россиян от COVID-19, Вакцина «Спутник Лайт»
МОСКВА, 1 июл — РИА Новости. «Гам-КОВИД-Вак», известная также как «Спутник V», — первая зарегистрированная в мире вакцина для профилактики COVID-19. По оценкам разработчиков, препарат эффективен против всех выявленных штаммов коронавируса SARS-CoV-2, а ее облегченный вариант «Спутник Лайт» идеально подходит для ревакцинации.
Что такое «Гам-КОВИД-Вак»
«Гам-КОВИД-Вак», или «Спутник V», — первая российская вакцина против ковида, созданная в Центре эпидемиологии и микробиологии имени Н. Ф. Гамалеи. Она относится к классу векторных вакцин. Зарегистрирована 11 августа 2020 года.
Состав вакцины «Спутник V»
Вакцина состоит из неспособного размножаться аденовируса человека. Этот возбудитель не опасен, он вызывает лишь легкую простуду. В его ДНК встроен ген белка-шипа коронавируса SARS-CoV-2. Белок связывается с рецепторами на поверхности клеток и помогает вирусу проникнуть внутрь. Именно на белок-шип реагирует наш иммунитет. Аденовирусный вектор при этом служит средством доставки.
В вакцине используют вектор на основе двух разных штаммов аденовируса человека — 26-го и пятого серотипа (Ad26, Ad5).
Выпускают препарат в виде раствора со вспомогательными веществами: например, трис, хлориды натрия и магния, сахароза, полисорбат, магний хлористый гексагидрат, ЭДТА, этанол, вода.
Принцип действия и отличия от других вакцин
Раствор вводят в мышцу, вскоре в месте укола начинается небольшое воспаление — организм распознает чужеродные вещества и отправляет туда лимфоциты. Аденовирус проникает в них и заставляет вырабатывать коронавирусный белок-шип. В свою очередь иммунитет отвечает целым коктейлем из антител.
Антитела — это сигнальные белки, которые дают команды защитной системе организма. Если произойдет встреча с реальным SARS-CoV-2, они помогут его уничтожить. В результате человек не заболеет либо коронавирусная инфекция будет перенесена в легкой форме.
В мире есть несколько векторных вакцин от коронавируса. Например, американская компания Johnson & Johnson создала препарат на основе аденовируса человека Ad26, а китайская CanSino Biologics — Ad5. Обе вводят однократно.
В отличие от них «Спутник V» делают в два приема. После первой дозы, или, как говорят ученые, праймирующей иммунизации, у привитых формируется первичный, а после второй, бустерной, — вторичный иммунный ответ. Уникальность российской технологии в том, что в первой и второй дозах использованы разные вирусные векторы — сначала Ad26, затем Ad5. При такой схеме общий уровень иммунизации намного выше.
Еще одну векторную вакцину разработала англо-шведская компания AstraZeneca. Однако в ней в качестве вектора используют аденовирус шимпанзе.
По результатам клинических исследований, которые прошли международную оценку и опубликованы в журнале The Lancet, эффективность вакцины «Спутник V» против COVID-19 составляет 91,6 процента. И в ста процентах случаев она предотвращает развитие тяжелой формы ковида.
Анализ данных о заболеваемости коронавирусом среди россиян, привитых обоими компонентами препарата в период с 5 декабря 2020-го по 31 марта 2021-го, показал, что реальная эффективность «Гам-КОВИД-Вак» еще выше — 97,6 процента.
Инструкция по применению
Подготовка к вакцинации
Нет никаких особенных требований при подготовке в прививке. Роспотребнадзор указывает — перед вакцинацией нет необходимости делать ПЦР-тест, чтобы исключить ковид, или анализ на антитела. Главное, в день вакцинации самочувствие должно быть хорошим.
Однако, по мнению ряда экспертов, реакция организма на введение любой вакцины очень индивидуальна. Поэтому людям с серьезными хроническими болезнями нужно предварительно сходить на прием к лечащему врачу и убедиться, что их заболевание в стадии ремиссии и они сейчас не принимают никаких препаратов, которые могут помешать выработке иммунитета.
Как делается прививка от коронавируса
«Спутник V» предназначен для внутримышечного введения. Укол делают в дельтовидную мышцу плеча.
Перед процедурой флакон или ампулу с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания, чтобы не осталось включений льда. Затем протирают снаружи спиртовой салфеткой и осторожно перемешивают содержимое, не допуская встряхивания. Размороженный препарат необходимо использовать в течение двух часов, снова замораживать его нельзя.
Для выявления противопоказаний пациента перед вакцинацией должен осмотреть врач. Он опрашивает о самочувствии и контактах с инфицированными, измеряет температуру тела и уровень кислорода в крови. Если температура выше 37 градусов, прививку откладывают.
Переболеть COVID-19 или привиться? Вся правда о вакцине от коронавируса
Что нельзя делать после прививки
Рекомендуют один день до и два дня после прививки воздержаться от употребления алкоголя, не переутомляться, избегать тяжелых физических нагрузок, снизить уровень стресса, хорошо высыпаться, не злоупотреблять солнечными ваннами, а в сам день вакцинации не посещать бани и бассейны, не купаться в природных водоемах.
Ученые советуют есть побольше белковых продуктов — молочных, рыбы, нежирного мяса, поскольку они дают организму необходимый строительный материал для формирования защитных антител, а также богатые пищевыми волокнами пребиотики — овощи, цельнозерновые крупы, бобовые, зелень — и пробиотики — кефир, йогурт, простоквашу, квашеную капусту. Они нужны для поддержания кишечной микрофлоры, которая вносит большой вклад в выработку иммунного ответа на вакцину.
Также важно после прививки соблюдать стандартные защитные меры: носить маски в людных местах, тщательно мыть руки, использовать антисептики.
Интервал между прививками
Вакцинацию проводят в два этапа с интервалом 21 день: вначале компонентом I в дозе 0,5 миллилитров, затем, через три недели, — компонентом II в дозе 0,5 миллилитров.
Когда появятся антитела к коронавирусу
По оценкам ученых, полноценный иммунитет возникает в среднем через 40 дней после первого укола. До истечения этого срока важно не только избежать заражения коронавирусом, но и не подхватить другую ОРВИ, энтеровирус или прочие инфекции. Они могут помешать эффективной выработке иммунитета после вакцинации.
Ждать нельзя вакцинироваться. Как долго сохраняется иммунитет к ковиду
Побочные эффекты от вакцины «Спутник V»
Клинические исследования показали, что чаще всего после вакцинации возникает гриппоподобный синдром — боль, отек и зуд в месте введения, общее недомогание, озноб, повышение температуры, боль и ломота в мышцах и суставах, головная боль, снижение аппетита. Состояние может длиться от одного до трех дней.
Реже проявляются нарушения со стороны дыхательной системы — боль в ротоглотке, заложенность носа, першение в горле. Возможны головокружения, обмороки, тошнота, рвота, диспепсия.
В памятке Минздрава указано, что при повышении температуры можно принять нестероидные противовоспалительные препараты, а при покраснении, отечности и болезненности места укола — антигистаминные средства. Никаких серьезных последствий, в том числе тяжелых аллергических реакций, не наблюдалось.
Продолжительность действия
Пока точно не установлено, на какой срок защищает вакцина. Согласно предварительной оценке, антитела класса G у сотрудников Центра Гамалеи, получивших вакцину в порядке эксперимента в марте 2020-го, сохранялись и через девять месяцев. При этом титр антител был выше, чем у переболевших.
Противопоказания для вакцинации
Противопоказания к применению у «Спутника V» примерно такие же, как у всех остальных вакцин: тяжелые формы аллергии, инфекционные и неинфекционные заболевания в острой форме, грудное вскармливание. Прививаться можно всем взрослым старше 18 лет, без верхнего ограничения по возрасту.
Без ограничений по возрасту. Доказана эффективность прививок для пожилых
Детей пока не прививают — из-за отсутствия клинических испытаний, подтверждающих эффективность и безопасность вакцины для людей младше 18. Центр Гамалеи планирует в ближайшее время начать исследование по применению «Спутника V» у детей. Соответствующую заявку ученые подали в Минздрав России.
Недавно ведомство разрешило «Спутник V» для беременных женщин с высоким риском тяжелого течения COVID-19.
Инструкция рекомендует с осторожностью применять вакцину при хронических заболеваниях печени и почек, тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях центральной нервной системы, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах, а также при некоторых эндокринных заболеваниях, таких как выраженные нарушения функции щитовидной железы и сахарный диабет в стадии декомпенсации.
Отмечено, что вакцинация может представлять определенный риск для пациентов со злокачественными новообразованиями и тяжелыми аутоиммунными заболеваниями, так как стимуляция иммунной системы может привести к обострению.
А вот пациентам с сердечно-сосудистыми заболеваниями, диабетом, бронхиальной астмой, гепатитом С и онкозаболеваниями в стадии ремиссии, по мнению ученых, вакцинироваться необходимо.
Ревакцинация
Ожидают, что коронавирус станет сезонным и прививаться от него нужно будет ежегодно. А во время обострения эпидемии — раз в шеть месяцев.
Специалисты Центра Гамалеи и Минздрава рекомендуют проводить ревакцинацию «Спутником Лайт», которая в ближайшее время поступит в гражданский оборот. Ранее глава РФПИ Кирилл Дмитриев и владелец компании «Р-Фарм» — одного из производителей «Гам-КОВИД-Вак» — заявляли, что ревакцинироваться можно и первым компонентом «Спутника V».
Отзывы привитых «Спутником V»
«Сегодня привился «Спутником V». Чувствую себя хорошо. Коронавирусом я переболел, есть антитела. Но прививка необходима независимо от уровня титров. Все, кто еще не вакцинировался, — самое время это сделать», — написал врио главы Мордовии Артем Здунов в инстаграме.
Врио губернатора Хабаровского края Михаил Дегтярев сделал прививку от ковида повторно. «Первый раз вакциной «Гам-Ковид-Вак» прививался в июле и августе прошлого года. По прошествии 11 месяцев количество антител в крови существенно снизилось, поэтому решил не рисковать ни своим здоровьем, ни здоровьем людей, с которыми работаю и с которыми встречаюсь каждый день», — рассказал он в Telegram-канале.
Народные отчеты от вакцинации «Спутником V» публикуются в Telegram-канале @Sputnik_results. Вот несколько отзывов:
«М 43, здоров. ГамКовидВакV1 — 16.03 без побочек, V2-07.04 легкая слабость на след день. Антитела на 28.06».
«Ж 22 года V1 28.06.21. В день прививки легкая слабость и сонливость, боль в месте укола».
«М 65, системный васкулит (гранулематоз Вегенера) в ремиссии, V2 28.06.21, никаких симптомов, как и после первой дозы».
«В жар бросало». Привитые от коронавируса честно рассказали обо всем
Сертификация вакцины «Спутник V» в других странах
Вакцина одобрена в 67 странах с общим населением свыше 3,4 миллиарда человек. Так, имея сертификат о прививке «Спутником V», можно въезжать, например, в Грецию, Хорватию, на Кипр, в Турцию, Грузию.
Пакет документов о сертификации «Спутника V» также предоставлен ВОЗ. Разработчики ожидают положительное решение в скором времени. В случае одобрения вакцинированные получат цифровые сертификаты, которые облегчат перемещение по странам ЕС.
Появившаяся одной из первых вакцина российского происхождения с присутствием символа «V» в названии привела многих в недоумение: «Спутник 5» или «Ви»: как нужно произносить это название? Препарат является векторным, доставляющим в организм разные серотипы аденовируса, несущие S-белок шипа SARS-Cov-2. Ad26 и Ad5 лишены способности к размножению, в организме человека они способны вызывать лишь легкие формы ОРВИ, которые быстро проходят.
Подробная информация о «Спутник V» здесь.
История создания вакцины
Прежде чем узнать, «Спутник пять» или «Ви»: как правильно говорить, следует рассмотреть историю создания препарата. Вакцина была разработана в предельно сжатые сроки благодаря наличию у отечественных инфекционистов платформы, которая использовалась при создании лекарственного профилактического средства против лихорадки Эбола. Последняя использовалась для вакцинации более 10 млн человек и доказала свою эффективность.
В 2018 году центр им. Гамалеи создал препарат против респираторного синдрома MERS. Благодаря созданным 2 вакцинам исследователи смогли быстро переключиться на создание нового вида лекарственного средства.
Прививка делается по схеме «прайм-буст», предполагающей двухступенчатую вакцинацию. Первый укол запускает иммунный ответ, второй — делает его более сильным.
Состав вакцины
В качестве действующих веществ выступают 2 серотипа аденовируса (Ad26 и Ad5), использующиеся для доставки S-белка коронавируса к человеческим клеткам. Каждый из них входит в отдельный компонент вакцины. Сам вирус в состав препарата не входит, поэтому вызвать заболевание он не может.
Помимо активных веществ препарат включает дополнительные ингредиенты:
- полисорбат 80;
- ЭДТА динатриевую соль дигидрат;
- пищевую соль (хлорид натрия);
- сахарозу;
- трис;
- магния хлорида гексагидрат;
- воду для инъекций;
- 95 % этанол.
Они способствуют усилению эффективности использования препарата и его сохранности.
Спутник V: как правильно читать
Как правило, вопроса «Спутник Ви»: как пишется» не возникает. Сочетание символов уже неоднократно демонстрировалось как в средствах массовой информации, так и в интернете. В основном непонятно, как произносить последний символ в названии.
По своей сути это то же самое, что и выяснение вопроса, как правильно писать «Спутник V» в русской транслитерации. При создании вакцины ее наименование создавалось таким образом, чтобы олицетворять безусловную победу человека над вирусом. Поэтому в названии заложено имя первого искусственного спутника, созданного в Советском Союзе. Второй символ означает символ победы в латинице или английском языке. Но учитывая, что сегодня международным является последний, он произносится как «Ви».
При этом такое название является торговым. Оно не присутствует на этикетке различных упаковок, поэтому нужно знать, «Спутник Ви» как по-другому называется. Медицинское наименование, присутствующее на картонной пачке, ампулах или флаконах, — «Гам-КОВИД-Вак».
Подготовка к вакцинации
Особых правил по подготовке к проведению медицинской процедуры нет. Как и при любом уколе не рекомендуется:
- посещать спортзал в день прививки;
- злоупотреблять горячительными напитками;
- курить;
- употреблять жареную и жирную пищу.
За 2 недели до вакцинации лучше прекратить любые контакты с болеющими коронавирусом. Перед постановкой прививки нужно обязательно измерить температуру — она не должна превышать 37 °С. Девушкам и женщинам желательно сдать тест на беременность, поскольку она является противопоказанием для вакцинации.
Способ применения
«Спутник V» вводится в дельтовидную мышцу плеча. Выдержанный в течение получаса стеклянный пузырек протирается спиртовой салфеткой, при этом делаются осторожные перемешивающие движения, без резких встряхиваний, после чего он вскрывается и раствор набирается в шприц. 1 доза составляет 0,5 мл.
Постановке прививки предшествует осмотр врачом, который определяет у пациента:
- температуру тела;
- содержание кислорода в крови.
Он опрашивает пациента, выясняя его самочувствие, наличие контактов с людьми, заразившимися COVID-19 за последние 2 недели. Если температура выше 37 °С, пациент приглашается на вакцинацию после ее нормализации.
Ввод компонентов происходит не один за другим, а с периодом ожидания в 21 день. При заражении вирусом населению трудно обеспечить полноценную защиту организма вакциной. Никто не даст гарантию, что пациент не подхватил инфекцию, которая находилась в инкубационном периоде при постановке «Спутника V». Но сделанная прививка облегчает течение заболевания и практически на нет сводит случаи с летальным исходом.
Побочные эффекты
Вакцинация «Спутником V» абсолютным большинством населения переносится хорошо. Отрицательные реакции свидетельствуют о начале формирования иммунитета и протекают с легкой или средней степенью тяжести.
В основном встречаются следующие симптомы:
- характерные для простудных заболеваний;
- зуд, боль и отечность в месте укола;
- ломота;
- повышение температуры;
- озноб;
- головная боль.
Для их ликвидации назначаются НПВП, парацетамол. С целью снятия покраснения и боли в месте инъекции используют антигистаминные препараты. При симптомах простудных заболеваний следует употреблять большое количество жидкости, использовать полоскания горла и назальные спреи.
Возникшие негативные явления, как правило, полностью проходят в течение 2-3 дней после постановки прививки.
Ревакцинация
Этот термин означает постановку повторной прививки, способствующей укреплению ослабшей защиты организма спустя некоторое время. Хороший уровень антител вырабатывается примерно через 40 дней после ввода первого компонента. Но со временем он начинает падать. При этом не учитывается наличие клеточной памяти, которая также должна защищать человеческий организм в течение длительного времени.
Большинство исследователей склоняется к тому, что ревакцинация необходима. Рекомендуется проводить ее не реже 1 раза в полгода в период эпидемий и не реже 1 раза в год при стабильной ситуации с данным вирусом.
Состав вакцины
Состав Гам-КОВИД-Вак указан на одну дозу, которая составляет 0.5 мл.
Компонент 1 содержит:
- активное вещество: рекомбинантные аденовирусные частицы 26 серотипа, в которых содержится ген белка S вируса SARS-CoV-2, по 1 x 1011 частиц с погрешностью 0.5 x 1011 частиц;
- вспомогательные компоненты: магния хлорида гексагидрат (102 мкг), трис(гидроксиметил)аминометан (1.21 мг), сахароза (25 мг), хлорид натрия (2.19 мг), ЭДТА динатриевая соль дигидрат (19 мкг), вода для инъекции (до 0.5 мл), этанол 95% (2.5 мкл), полисорбат 80 (250 мкг).
Компонент 2 содержит:
- активное вещество: аденовирусные рекомбинантные частицы 5 серотипа, которые содержат ген белка S вируса SARS-CoV-2, по 1 x 1011 частиц в дозе с погрешностью 0.5 x 1011 частиц;
- вспомогательные вещества те же, что в первом компоненте.
В составе Гам-КОВИД-Вак-Лио содержится аналогичное количество активного компонента и вспомогательные элементы: магния хлорида гексагидрат (20.4 мкг), трис(гидроксиметил)аминометан (0.24 мг), сахароза (73.5 мг), хлорид натрия (1.4 мг), ЭДТА динатриевая соль дигидрат (3.8 мкг), полисорбат 80 (0.05 мг).
Производители
На данный момент известны следующие производители Гам-КОВИД-Вак:
- ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России;
- АО «Биннофарм»;
- АО «ГЕНЕРИУМ»;
- АО «Р-Фарм»;
- ЗАО «БИОКАД»;
- ЗАО «ЛЕККО»;
- ОАО «Фармстандарт-УфаВИТА».
Владельцем регистрационного удостоверения на производство вакцины Спутник V является ФГБУ «Национальный исследовательский центр микробиологии и эпидемиологии им. почетного академика Н.Ф. Гамалеи» Мин. здравоохранения РФ.
Когда вакцина зарегистрирована?
Вакцина от коронавируса Гам-КОВИД-Вак была зарегистрирована 11 августа 2020 года.
Форма выпуска
Препарат Гам-КОВИД-Вак (Спутник V) выпускают в форме раствора для внутримышечного введения из двух компонентов, по 0.5 мл раствора каждого компонента на 1 дозу.
Замороженный препарат
Оба компонента препарата в виде замороженного раствора — беловатая твердая плотная масса. После разморозки — однородный раствор, бесцветный или слегка желтоватый.
Производство ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи»:
- Препарат во флаконах, закрытых резиновой пробкой, обжатый алюмопластиковым колпаком. По 0.5 мл (1 доза) каждого компонента во флаконе. Флакон каждого компонента вместе с инструкцией помещен в пачку из картона.
Производство АО «Биннофарм»:
- Препарат в прозрачных ампулах с цветной точкой. По 0.5 мл (1 доза) каждого компонента в ампуле. По 5 ампул каждого компонента помещены в ячейковую контурную упаковку из поливинилхлоридной пленки, по 1 ячейковой упаковке вместе с инструкцией в картонной пачке.
Производство АО «ГЕНЕРИУМ» и ЗАО «ЛЕККО»:
- Препарат во флаконах, закрытых резиновой пробкой, обжатый алюмопластиковым колпаком с контролем первого вскрытия. По 3 мл (5 доз) каждого компонента во флаконе. Флакон каждого компонента вместе с инструкцией помещен в пачку из картона.
Производство ЗАО «БИОКАД»:
- Препарат во флаконах, закрытых резиновой пробкой, обжатый алюминиевым колпаком с пластиковой крышкой типа «flip-off». По 3 мл (5 доз) или по 0.5 мл (1 доза) каждого компонента во флаконе. Флакон 6R каждого компонента вместе с инструкцией помещен в пачку из картона. Флакон 2R каждого компонента в контурной ячейковой упаковке из ПВХ пленки вместе с инструкцией помещен в пачку из картона.
Производство ОАО «Фармстандарт-УфаВИТА»:
- Препарат в прозрачных ампулах. По 0.5 мл (1 доза) каждого компонента в ампуле. По 5 ампул каждого компонента помещены в ячейковую контурную упаковку из поливинилхлоридной пленки, по 1 ячейковой упаковке вместе с инструкцией в картонной пачке.
- Препарат во флаконах, закрытых резиновой пробкой, обжатый алюмопластиковым колпаком с контролем первого вскрытия. По 3 мл (5 доз) каждого компонента во флаконе. Флакон каждого компонента вместе с инструкцией помещен в пачку из картона.
Жидкий препарат
Оба компонента препарата в виде однородного раствора, бесцветного или слегка желтоватого оттенка.
Производство ОАО «Фармстандарт-УфаВИТА»:
- Препарат в прозрачных ампулах. По 0.5 мл (1 доза) каждого компонента в ампуле. По 5 ампул каждого компонента помещены в ячейковую контурную упаковку из поливинилхлоридной пленки, по 1 ячейковой упаковке вместе с инструкцией в картонной пачке.
Производство АО «ГЕНЕРИУМ» и ЗАО «ЛЕККО»:
- Препарат во флаконах, закрытых резиновой пробкой, обжатый алюмопластиковым колпаком с контролем первого вскрытия. По 3 мл (5 доз) каждого компонента во флаконе. Флакон каждого компонента в контурной ячейковой упаковке вместе с инструкцией помещен в пачку из картона.
Фармакологическое действие
Комбинированная векторная вакцина Гам-КОВИД-Вак применяется в качестве иммунологического средства.
Фармакодинамика и фармакокинетика
Согласно исследованиям препарата в институте Гамалеи вакцина способствует формированию клеточного и гуморального иммунитета по отношению к вирусной инфекции, ассоциированной SARS-CoV-2. Обладает иммунологической активностью. Безопасность и иммунологические свойства изучались в клинических исследованиях у взрослых пациентов обоих полов. Возраст испытываемых составлял от 18 до 60 лет. При этом 9 человек получали первый компонент и 9 — второй, 20 человек проходили вакцинацию в режиме прайм-буст.
Иммуногенность средства была оценена по уровню спец. антител к белку коронавируса и уровню нейтрализующих вирус антител. У всех пациентов, принимающих участие в исследовании в результате образовывались специфические агенты. Через 42 дня в сыворотке крови всех добровольцев были обнаружены антитела к вирусу.
В центре Гамалеи оценку уровня иммуноглобулинов проводили по сравнению с исходным уровнем до иммунизации. Степень активности клеточного иммунитета была оценена в тесте лимфопролиферации CD8+ и CD4+, по скорости прироста интерферонов гамма в ответ на стимуляцию гликопротеином S.
После проведения вакцинации Спутником V был сформирован напряженный ангитен-специфический клеточный противоинфекционный иммунитет у всех добровольцев. Формировались антиген-специфичные клетки Т-хелперов, Т-киллеров, наблюдалось повышение уровня ИФНγ.
На данный момент испытания вакцины Cпутник V продолжаются, а защитный титр антител достоверно неизвестен. Испытания должны выявить продолжительность защиты организма. Также, пока не проводились клинические исследования по изучению эпидемиологической эффективности средства.
Показания к применению
Применяют для профилактики новой коронавирусной инфекции COVID-19 у взрослых пациентов в возрасте от 18 до 60 лет.
Вакцина Спутник V, противопоказания
Были выявлены следующие противопоказания на Спутник Ви:
- сверхчувствительность к компонентам средства или к вакцинам, содержащим аналогические ингредиенты;
- наличие тяжелых аллергических реакций у пациента ранее;
- неинфекционные и инфекционные острые заболевания;
- обострение хронического заболевания (вакцинацию рекомендуется проводит не ранее, чем через 2-4 недели после полного выздоровления или достижения ремиссии);
- кормление грудью и беременность;
- возраст до 18 и более 60 лет.
Перед тем, как сделать прививку 2 компонентом нужно выяснить у пациента, не возникали ли тяжелые осложнения (аллергические реакции, анафилактический шок, судороги, повышение температуры выше 40 градусов) после инъекции 1 компонента.
Осторожность следует соблюдать:
- при хронических заболеваниях почек и печени;
- пациентам с сахарным диабетом и выраженными нарушениями работы эндокринной системы;
- при тяжелых заболеваниях системы кроветворения;
- больным эпилепсией;
- после инсульта или с другими заболеваниями центральной нервной системы;
- при патологиях сердечно-сосудистой системы, инфаркте в анамнезе, миокардите, перикардите, эндокардите, ишемической болезни;
- пациентам с первичным и вторичным иммунодефицитом;
- при аутоимунных заболеваниях;
- больным астмой, с заболеваниями легких, ХОБЛ;
- при метаболическом синдроме;
- пациентам с атопией, аллергическими реакциями, экземой.
В учреждении, где проводят вакцинацию должны быть в наличии средства противошоковой терапии. В день проведения прививки пациента необходимо осмотреть, измерить температуру. Нельзя делать укол, если у пациента температура выше 37 градусов.
Вакцина Спутник V, побочные эффекты
Побочные эффекты Гам-КОВИД-Вак были выявлены в рамках клинических испытаний и исследований прочих вакцин, разработанных по аналогичной технологии. Реакции бывают легкими или среднетяжелыми. Чаще всего возникают в 1-2 день после прививки и проходят в течение следующих 3 дней. Рекомендуют проводить симптоматические лечение, при необходимости принимать НПВС после вакцинации.
Обычно наблюдаются кратковременные общие и местные реакции:
- гриппоподобный синдром, озноб, рост температуры тела, миалгия, артралгия, общая слабость;
- астения, головные боли, недомогание;
- боли в месте инъекции, отечность и повышение температуры в месте укола.
Реже возникает:
- тошнота, несварение желудка, потеря аппетита;
- увеличение лимфоузлов, аллергические реакции;
- рост уровня ферментов печени, креатинина, трансаминаз, креатинфосфокиназы в крови.
В открытом клиническом исследовании безопасности вакцины не удалось точно определить встречаемость нежелательных реакций, так как выборка участников исследования была ограниченной.
Во время таких исследований выявили следующие побочные эффекты:
- боль, отек, зуд в месте введения вакцины;
- понос, боли в ротоглотке, заложенность носа и першение в горле, ринорея;
- рост уровня Т-лимфоцитов, CD4-лимфоцитов и процентного их содержания;
- снижение числа естественных «киллеров», СD8;
- отклонения в общем анализе мочи, наличие в ней эритроцитов.
Вакцина Гам-КОВИД-Вак (Спутник V), инструкция по применению
Прививка Спутник V от коронавируса проводится внутримышечно. Внутривенное ведение средства строго запрещено. Инъекцию производят в дельтовидную мышцу или в латеральную широкую мышцу бедра.
Лиофилизат необходимо растворить в 1,0 мл воды для инъекций. После чего флакон встряхивают, пока его содержимое полностью не растворится.
Перед введением готового препарата его достают из холодильной камеры и нагревают при комнатной температуре в течение получаса. Раствор перемешивают осторожно покачивая ампулу. Нельзя резко встряхивать средство.
Нельзя использовать препарат, если целостность флакона была нарушена, смазалась маркировка, вещество изменило свои физические свойства, изменился цвет, появились механические включения, истек срок годности.
Лекарственный препарат был зарегистрирован по особой процедуре, и при каждом применении вакцины необходимо уведомлять Федеральную службу по надзору в сфера здравоохранения. Информацию нужно вносить в соответствующий раздел инф. системы ЕГИСЗ.
Вакцинация проводится в 2 этапа. Вначале вводят компонент 1, затем через 3 недели — компонент 2.
Если дальнейшие инъекции были отложены по какой-либо причине, то можно хранить вскрытый флакон по 3 мл не более 2 часов при комнатной температуре.
Передозировка
Нет данных о передозировке Спутник Ви. Вакцина от ковида выпускается для использования в лечебно-профилактических учреждениях, процедура проводится только квалифицированными мед. персоналом и вероятность передозировки крайне мала.
Предполагается, что при случайной передозировке могут возникнуть токсические и токсико-аллергические реакции, указанные в пункте «побочные действия» в более тяжелой форме. Рекомендуется симптоматическая терапия, прием жаропонижающих препаратов и НПВС, кортикостероидов парентерально.
Взаимодействие
Неизвестно вступает ли вакцина от коронавируса Спутник V во взаимодействие с другими препаратами.
Условия продажи
Пока лекарство нельзя приобрести в аптеке самостоятельно.
Условия хранения векторной вакцины Гам-КОВИД-Вак
Раствор для внутримышечного введения хранят в защищенном от света месте при температуре не более 18 °C. Не допустимо хранение размороженного препарата для флаконов по 0,5 мл.
Для флаконов по 3,0 мл — средство можно хранить более 2 часов при комнатной температуре. Держать вакцину дальше от детей.
Срок годности
Срок хранения составляет пол года для всех лек. форм и обоих компонентов средства.
Особые указания
Пациенты, получающие иммуносупрессивную терапию или больные иммунодефицитом могут не получить достаточного иммунного ответа. Поэтому применение средств, угнетающих работу иммунной системы противопоказано за 30 дней до и 30 дней после вакцинации. Пренебрежение правилом может привести к снижению иммуногенности.
Неизвестно, влияет ли инъекция препарата на способность управлять транспортом и опасными механизмами.
Узнать подробности о лекарстве можно на официальном сайте института Гамалеи.
Аналоги
Совпадения по коду АТХ 4-го уровня:
В октябре 2020 года в РФ прошла регистрацию вторая вакцина под названием ЭпиВакКорона. Лекарство было разработано в новосибирском научном центре «Вектор» и представляет собой искусственно синтезированные короткие фрагменты вирусных пептидов, «обучающие» иммунную систему бороться с вирусом. Сейчас препарат также проходит третий этап клинических испытаний.
Также, в феврале 2021 года прошла регистрацию третья вакцина КовиВак исследовательского центра им. Чумакова, в ее состав включен цельный инактивированный вирус.
На данный момент сложно предугадать, какая из вакцин окажется наиболее эффективной.
Детям
Вакцина от ковида Спутник Ви не применяется в возрасте до 18 лет.
При беременности и лактации
Делать прививки нельзя беременным женщинам и во время грудного вскармливания.
Вакцина Спутник V, отзывы
Известно, что в Российской Федерации разработкой лекарства от новой коронавирусной инфекции занялся институт Гамалеи. Вакцина от коронавируса получила уже широко известное название «Спутник V». Перед тем, как проводить иммунизацию массово, лекарству необходимо пройти стадию клинических испытаний. И на данный момент средство проходит этот этап пострегистрационного исследования в Москве. Сделать прививку в тестовом режиме планируется 40 тысячам человек, четверть из них получат плацебо. Параллельно уже началась иммунизация мед. работников и врачей.
Сейчас среди скептически настроенного населения идут горячие споры об эффективности вакцины Спутник V, учитывая тот факт, что некоторые добровольцы, которым делали уколы Гам-КОВИД-Вак, заразились уже на следующий день после прививки. В общем известно около 20 подобных случаев. Это объясняется тем, что большинство заболевавших не успели получить второй укол и иммунитет у них выработаться тоже не успел. Ведь, как известно, устойчивость у вирусу развивается только на 42 день после проведения полного цикла вакцинации. Именно так объяснил данные инциденты директор Института трансляционной медицины и биотехнологии Сеченовского университета Минздрава РФ Вадим Тарасов, который подчеркивает высокую эффектность Спутник V.
Отзывы врачей о препарате в большинстве своем положительные. При этом медики подчеркивают, что вакцина не призвана защитить от болезни на все 100%, она также должна предотвратить развитие тяжелой формы заболевания и летальный исход. Допускается, что после применения лекарства болезнь будет просто протекать в легкой форме и без осложнений.
Интерес также вызывают отзывы привитых добровольцев, которые приняли участие в третьей фазе клинических испытаний. Рандомизированное двойное слепое плацебо-контролируемое клиническое исследование началось 26 августа 2020 года.
Некоторые интересуются, как правильно называть препарат, Спутник Ви или Спутник 5? Правильный ответ — Спутник Ви.
Отзывы добровольцев:
- «… Решила попробовать эту вакцину на себе. На второй день после первой инъекции начала болеть рука, а к вечеру третьего дня поднялась температура 37,5. На пятый день температура спала. После второго укола температура была выше, до 38 Градусов и ощущала я себя, как при гриппе. Через три дня все вроде прошло. Потом сдавала кровь на антитела, уровень IgG составил 11,3, непонятно почему так мало».
- «… Записался на вакцинацию как только узнал, что так можно. Во время прививки покалывало руку, а так не заметил каких-либо побочных реакций. Чувствую себя хорошо пока, вторая прививка тоже прошла нормально. Буду ждать теста на антитела«.
- «… После вакцинации ощущаю себя так, будто переболела гриппом, была высокая температура, головные боли и ломило суставы. Еще болел левый бок. Сбивала температуру 2 недели. К сожалению после болезни антител у меня нет, что странно«.
После прохождения последнего этапа планируется наладить массовое производство вакцины Спутник V и провести иммунизацию достаточного количества населения страны, чтобы сформировать коллективный иммунитет.
Вакцина Спутник V, цена, где купить вакцину Спутник V в Москве
На данный момент указать даже примерную стоимость Спутник Ви сложно. Есть сообщения о том, что предельная стоимость препарата составит не более 1942 рублей за оба компонента. Однако, пока Гам-КОВИД-Вак не появилась в свободной продаже, говорить о точной цене рано.
Все новости о наличии вакцины Спутник М будут в первую очередь публиковаться в наших группах Вконтакте и в Телеграм, добавляйтесь в группы!
Инструкция по применению Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Отпускается по рецепту
Лекарственные формы вакцины Спутник М
раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент II
Международное непатентованное название
Вакцина для профилактики COVID-19
Состав Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Состав на 1 дозу: Компонент I содержит: Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (2,0±1,5) х 10(10) частиц. Вспомогательные вещества: трис (гидроксиметил) аминометан — 1,21 мг, натрия хлорид — 2,19 мг, сахароза — 25,0 мг, полисорбат 80 — 250 мкг, магния хлорида гексагидрат — 102,0 мкг, ЭДТА динатриевая соль дигидрат — 19,0 мкг, этанол (спирт этиловый) 95 % — 2,5 мкл, вода для инъекций — до 0,5 мл.
Группа: Вакцины
Производители: НИЦЭМ им. Н.Ф. Гамалеи (Медгамал)(Россия)
Показания к применению Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Профилактика COVID-19 у подростков в возрасте от 12 до 17 лет (включительно).
Способ применения и дозировка Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу — препарат вводят в латеральную широкую мышцу бедра.
Вакцинацию проводят в два этапа: вначале компонентом I в дозе 0,5 мл, затем, через 3 недели — компонентом II в дозе 0,5 мл. После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Перед иммунизацией флакон с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона! Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту. Не допускается хранение размороженного препарата! Повторное замораживание не допускается!
Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата, путем внесения информации в соответствующий раздел информационной системы ЕГИСЗ.
Противопоказания Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
- Гиперчувствительность к какому-либо компоненту вакцины или вакцине, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания,
- обострение хронических заболеваний — вакцинацию проводят через 2-4 недели после выздоровления или наступления ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ — вакцинацию проводят после нормализации температуры; возраст до 12 лет (в связи с отсутствием данных об эффективности и безопасности).
Противопоказания для введения компонента II:
- тяжелые поствакцинальные осложнения (анафилактический шок, тяжелые генерализованные аллергические реакции, судорожный синдром, температура тела выше 40 °С и т.п.) на введение компонента I вакцины.
Фармакологическое действие
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2. Иммунологические свойства и безопасность вакцины изучали в клиническом исследовании у добровольцев обоего пола в возрасте от 12 до 17 лет включительно. Промежуточный анализ иммуногенности показал, что вакцина формирует иммунный ответ у добровольцев. При исследовании гуморального иммунного ответа сыворотки добровольцев были проанализированы на наличие антител, специфичных к рецептор-связывающему домену гликопротеина S вируса SARS-CoV-2 на 42 день от начала вакцинации: уровень сероконверсии составил 100 %. Иммунизация препаратом Гам-КОВИД-Вак-М формирует антиген-специфический клеточный противоинфекционный иммунитет у 93,2 % обследованных добровольцев (формирование антиген-специфичных клеток обоих популяций Т-лимфоцитов: Т-хелперных (CD4+) и Т-цитотоксических (CD8+) и достоверное повышение секреции ИФНгамма). Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Побочное действие Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Нежелательные явления (НЯ), характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Чаще других могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией; общим недомоганием; утомляемость, головная боль) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции. Реже отмечаются: тошнота, диспепсия, иногда — заложенность носа увеличение регионарных лимфоузлов, паническая атака. У некоторых пациентов возможно развитие аллергических реакций, кратковременное изменение лабораторных показателей крови повышение уровня билирубина, снижение уровня нейтрофилов) в сыворотке крови.
В рамках проведенных клинических исследований безопасности, переносимости и иммуногенности препарата Гам-КОВИД-Вак-М после вакцинации были зарегистрированы следующие НЯ: «Общие нарушения и реакции в месте введения»: гипертермия, боль, отек, зуд в месте вакцинации, астения. Частота развития — очень часто и часто. «Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: заложенность носа. Частота развития — редко. «Нарушения со стороны нервной системы»: головная боль; головокружения — редко. «Желудочно-кишечные нарушения»: тошнота, рвота, диспепсия — редко. «Лабораторные и инструментальные данные»: разнонаправленные отклонения показателей. Все НЯ завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Передозировка
О случаях передозировки не сообщалось. Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок. Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени. Специфических антидотов к препарату не существует. Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (жаропонижающие/НПВС и десенсибилизирующие средства, кортикостероиды — парентерально при выраженном токсико-аллергическом синдроме). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства. Взаимодействие с другими лекарственными средствами Не изучалось. Ввиду отсутствия данных исследований совместимости, вакцину Гам-КОВИД-Вак-М (Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2) нельзя смешивать с другими вакцинами или иными лекарственными средствами в одном шприце.
Взаимодействие Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Не изучалось. Ввиду отсутствия данных исследований совместимости, вакцину Гам-КОВИД-Вак-М (Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2) нельзя смешивать с другими вакцинами или иными лекарственными средствами в одном шприце.
Особые указания
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах. Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов: с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжелых и жизнеугрожающих состояний); со злокачественными новообразованиями. Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Отсутствует опыт клинического применения Гам-КОВИД-Вак-М при беременности.
Согласно результатам изучения репродуктивной токсичности на животных не установлено отрицательного влияния на течение беременности, эмбриофетальное развитие (на самках) и пренатальное развитие потомства. В связи с этим применять препарат Гам-КОВИД-Вак- М при беременности следует только в тех случаях, когда ожидаемая польза для матери превышает потенциальный риск для плода с 22-х недель беременности.
Клинические данные по применению препарата Гам-КОВИД-Вак-М у женщин, кормящих грудью, и младенцев отсутствуют. В настоящий момент нет данных выделяется ли вакцина с молоком. Перед принятием решения о вакцинации кормящей женщины необходимо оценить риски и пользу данной вакцинации. У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности. Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц. Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Условия хранения
Хранить в защищенном от света месте, при температуре не выше минус 18 С. Повторное замораживание не допускается. Хранить в недоступном для детей месте. Условия транспортирования: при температуре не выше минус18 С.

Пример записи о вакцинации I компонентом препарата «Гам-КОВИД-Вак» в сертификате о вакцинации против COVID-19, Москва, 2021 год
«Спу́тник V» ([спу́тник ви]; «V» от англ. victory — «победа»), регистрационное наименование «Гам-КОВИД-Вак» (лат. Gam-COVID-Vac) — комбинированная векторная вакцина для профилактики коронавирусной инфекции COVID-19[6][7][8][9], разработанная Национальным исследовательским центром эпидемиологии и микробиологии имени Н. Ф. Гамалеи[6][7].
В основе вакцины использован аденовирусный вектор со встроенным в него фрагментом генетического материала SARS-CoV-2, имеющим в себе информацию о структуре S-белка шипа вируса. Сам фрагмент генетического материала безопасен для человека, но при этом способен обеспечить формирование устойчивого антительного и клеточного иммунного ответа к вирусу. Ввиду применяемой технологии «гетерологический прайм-буст» (heterologous prime-boost) препарат состоит из двух компонентов, в состав которых входят рекомбинантные аденовирусные векторы на основе двух различающихся сборок аденовируса человека[⇨].
Вакцина была зарегистрирована 11 августа 2020 года Министерством здравоохранения Российской Федерации (регистрационное удостоверение номер ЛП-006395[1]), на основании результатов клинических исследований фазы I/II. Данные результаты исследований были опубликованы позже, 4 сентября 2020 года в журнале «The Lancet»[10]. Безопасность вакцины также была показана промежуточными результатами III фазы испытаний[11], а затем — результатами мониторинга здоровья провакцинированного населения в России и в других странах (от нескольких тысяч до нескольких миллионов человек в каждой), в том числе для лиц старше 60 лет[⇨]. В июле 2021 года начато также исследование безопасности вакцины для подростков[12].
2 февраля 2021 года в журнале «The Lancet» были опубликованы промежуточные результаты исследования фазы III, согласно которым эффективность вакцины «Спутник V» составила 91,6 %, а эффективность вакцины против средней или тяжёлой степени COVID-19 — 100 %[13][14]. После этого вакцина получила разрешение на ввод в гражданский оборот сроком на 5 лет[1]. По предварительным результатам испытаний эффективности вакцины для пожилых было установлено, что она обеспечивает одинаковую защиту для лиц старше 60 лет и даже старше 80 лет[15]. В апреле 2021 года разбработчики вакцины заявили, что по результатам анализа данных 3,8 млн россиян, провакцинированных обоими компонентами «Спутника V», эффективность этой вакцины составила 97,6 %[16]. Данные об эффективности вакцины, в том числе и для лиц старше 60 лет, подтверждаются результатами вакцинации в других странах[⇨]. Кроме того, по данным разработчиков[17][18][19] и независимых исследований[20][21], «Спутник V» эффективен против различных штаммов коронавируса.
Помимо «Спутника V», в оборот выпущена однокомпонентная вакцина «Спутник Лайт», которая представляет собой первый компонент «Спутника V». По данным исследований, эффективность «Спутника Лайт» составляет 79,4 %[⇨].
Для предоставления населению точной и актуальной информации о вакцине был создан официальный сайт вакцины sputnikvaccine.com с информацией на девяти языках. Стратегическим инвестором в разработке и производстве вакцины выступил Российский фонд прямых инвестиций (РФПИ)[22]. По состоянию на июнь 2021 года вакцина «Спутник V» была зарегистрирована в 67 странах[23].
В России, для жителей застрахованных в системе ОМС, вакцинация «Спутником V» бесплатная, как и любая другая включённая в Национальный календарь профилактических прививок. Массовая вакцинация препаратом стартовала в России в декабре 2020 года[24][⇨].
Общее описание
Вакцина Гам-КОВИД-Вак представляет собой вирусную векторную вакцину на основе ДНК- аденовируса человека, который содержит в своём геноме вставку, кодирующую фрагмент S-белка SARS-CoV-2 и вызывающего иммунный ответ[25]. При создании вакцины использовалась клеточная линия HEK 293, полученная из абортированного человеческого эмбриона. По утверждению разработчиков вакцины, в самой вакцине этой линии нет, так как с помощью очистки вирусная частица избавлялась от следов человеческой клетки[26].
Вакцина разработана коллективом лаборатории клеточной микробиологии отдела медицинской микробиологии[27] Национального Центра микробиологии и эпидемиологии им. Н. Ф. Гамалеи Минздрава РФ (руководитель лаборатории — доктор биологических наук, член-корреспондент РАН Д. Ю. Логунов) и вирусологического центра[28][29] 48-го Центрального научно-исследовательского института Минобороны РФ, которые разрабатывали также вакцины против Эболы и БВРС[30][31].
Вакцина получена биотехнологическим путём, при котором не используется патогенный для человека коронавирус SARS-CoV-2. Препарат состоит из двух компонентов: компонент Ⅰ и компонент Ⅱ. В состав компонента Ⅰ входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа (rAd26), несущий ген S-белка вируса SARS-CoV-2; в состав компонента Ⅱ входит вектор на основе аденовируса человека 5 серотипа (rAd5), также несущий ген S-белка вируса SARS-CoV-2. Компоненты вакцины вводятся внутримышечно, в два этапа с интервалом в 3 недели[32]. Использование двух разных серотипов аденовируса предназначено для обхода любого возможного ранее приобретённого аденовирусного иммунитета в популяции[33]. К тому же если бы использовался один и тот же серотип, то после первой дозы к нему выработался бы иммунитет и вектор был бы уничтожен при получении второй дозы, два разных серотипа уменьшают шансы на такой сценарий[34].
В основе препарата «Спутник V» находятся две цепи ДНК-вируса, что отличает её от вакцин Pfizer и Moderna, которые используют более хрупкую цепь РНК. Прочная белковая оболочка обеспечивает лучшую сохранность генетического материала, что позволяет перевозить и хранить вакцину без использования критически низких температур[35].
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|

Картонная пачка и флакон по 3 мл с I компонентом вакцины Гам-КОВИД-Вак производства филиала «Медгамал» НИЦЭМ им. Н. Ф. Гамалеи
После введения вакцины ген-вектор попадает в соматические[какие?] клетки, в результате чего происходит продуцирование ими S-белка SARS-CoV-2, в ответ на что в организме хозяина (привитого) вырабатываются антитела к этому белку[36]. По данным директора НКО «Коллективный иммунитет», биолога Антонины Обласовой, этот процесс происходит в клетках в месте введения вакцины, а не по всему организму[37]. Введение второго компонента вакцины способствует формированию более полноценного иммунитета против инфекции и большего количества B-клеток памяти[38][39]. Два разных серотипа аденовируса использованы во избежание возникновения выраженного иммунного ответа к нему и уничтожения вектора до его внедрения в клетку и начала продукции клеткой S-белка[40][41][42]. Двухвекторный вариант вызывает более сильный иммунный ответ по сравнению с одновекторным; кроме того, аденовирус 26 серотипа стимулирует также клеточный иммунитет (формирование специализированных лимфоцитов, развивающихся в вилочковой железе)[43]. В некоторых случаях при тестировании после вакцинации методом ИФА на антитела, они могут показать отрицательные результаты, так как ряд тестов рассчитан на выявление постинфекционного иммунитета (к N-белкам вируса), а не поствакцинального (в данном случае к S-белкам вируса)[44][45].
![Флаконы по 3 мл с раствором II компонента вакцины Гам-КОВИД-Вак производства АО «Генериум» на вакцинации военных и гражданских специалистов Северного флота в январе 2021 года[46]](https://wiki2.org/wikipedia/commons/thumb/4/46/Gam-COVID-Vac_01.jpg/im244-320px-Gam-COVID-Vac_01.jpg)
Флаконы по 3 мл с раствором II компонента вакцины Гам-КОВИД-Вак производства АО «Генериум» на вакцинации военных и гражданских специалистов Северного флота в январе 2021 года[46]
Полноценный иммунный ответ вырабатывается через 3 недели после V2 (введения второго компонента вакцины), таким образом, на 42-й день от момента начала курса вакцинации при соблюдении его сроков (3 недели между V1 и V2)[47].
Изначально было установлено, что для сохранности свойств вакцины «Спутник V» во всей цепочке холодовой цепи транспортировки и хранения требуется температура не выше минус 18 °С[48][49], что привело к дозакупке соответствующего холодильного (морозильного) оборудования[50][51][52][53][54]. Впоследствии министр здравоохранения России М. Мурашко, заявил, что Минздрав одобрил изменения в регистрационное удостоверение условий хранения и перевозки «Спутник V», разрешив температуру от +2 до +8 градусов, при этом такая вакцина [55].
Создание сухой лиофилизированной формы является длительным и довольно сложным процессом (поэтому себестоимость выше), но она более удобна для хранения и транспортировки, и предназначается для использования в труднодоступных регионах России[42]. По оценкам главы Центра им. Гамалеи Александра Гинцбурга, на вакцинацию бо́льшей части населения России, исходя из доступных мощностей, потребуется 9—12 месяцев[56].
23 октября 2020 года министр здравоохранения России Михаил Мурашко заявил, что вакцинация против коронавирусной инфекции после запуска больших объёмов производства Гам-КОВИД-Вак будет бесплатной для всех граждан России[57]. Минздрав России зарегистрировал предельную отпускную цену производителя на вакцину от коронавируса «Спутник V» на уровне 1942 рубля за два компонента[58]. 25 февраля 2021 года было объявлено о снижении отпускной цены за 2 компонента в 2 раза до 866 рублей 81 копейки, что объясняется отработкой и оптимизацией технологии промышленного производства препарата, а также ростом объёмов производства[59].
С 3 декабря 2020 года вакцины против COVID-19 включены в России в перечень жизненно необходимых и важнейших лекарственных препаратов[60][61][62]. Вакцинация против COVID-19 в России также внесена в национальный календарь профилактических прививок для вакцинации по эпидемическим показаниям[63][64][65].
История
В мае 2020 года Национальный центр эпидемиологических и микробиологических исследований объявил о разработке вакцины, не имеющей серьёзных побочных эффектов[66][67]. К августу 2020 года были закончены два клинических испытания первой и второй фазы с участием по 38 испытуемых в каждом[68]. По данным, предоставленным главой Центра Гамалеи, разработка вакцины «Спутник V» стоила 1,5 млрд рублей[69].
Разработка вакцины, а также доклинические и I / II этапы клинических испытаний велись совместно «НИЦЭМ им. Н. Ф. Гамалеи» Минздрава России и «48 ЦНИИ» Минобороны России, имевших до этого опыт разработки подобных вакцин[70][71][72][73][74] (ГамЭвак и БВРС-ГамВак-Комби[75]). В числе 18 разработчиков вакцины также значатся и руководители этих научных учреждений: А. Л. Гинцбург и С. В. Борисевич[76].
11 августа 2020 года о регистрации в России первой вакцины от коронавируса на совещании с президентом В. В. Путиным доложил[7] министр здравоохранения М. А. Мурашко[77][78]. Вакцина зарегистрирована условно, в соответствии с принятым Правительством Российской Федерации порядком доступа на рынок препаратов, предназначенных для профилактики COVID-19[7][79]. Соответствующее регистрационное удостоверение под номером ЛП-006395[1] было выдано 11 августа Минздравом России[80][81]. 25 августа было выдано удостоверение ЛП-006423 для лиофилизата «Гам-КОВИД-Вак-Лио»[4].
Начало промышленного выпуска вакцины Гам-КОВИД-Вак было запланировано на сентябрь 2020 года[82]. К концу 2020 года собственное производство Гамалеи, согласно интервью латвийскому интернет-изданию Meduza, планировалось вывести к рубежу 2020—2021 года на производственную мощность 3—5 млн доз в месяц[67]. По данным телеканала Вести.ру, к 15 августа произошёл запуск производства; три предприятия могли выпускать порядка миллиона доз в месяц на каждом с потенциальным удвоением мощностей к зиме[83][84].
В начале сентября 2020 года создатели вакцины опубликовали в журнале The Lancet статью с описанием вакцины и результатами её клинических испытаний I и II фазы на людях[42]. 2 февраля 2021 года в журнале были опубликованы промежуточные результаты III фазы клинических испытаний вакцины[85].
21 декабря 2020 года Российский фонд прямых инвестиций (РФПИ), Центр им. Гамалеи, российская фармкомпания «Р-Фарм» с одной стороны и англо-шведская фармацевтическая компания AstraZeneca с другой подписали соглашение о разработке и реализации программы клинических исследований комбинации вакцин от коронавируса. Стороны договорились развивать научные и деловые взаимоотношения, в рамках которых будут изучены возможности совместного использования российской вакцины «Спутник V» и препарата AZD1222, разработанного AstraZeneca и Оксфордским университетом, ради более стойкой и длительной защиты человека от коронавируса[86][87][88][89].
В январе 2021 года начаты испытания вакцины «Спутник Лайт», представляющей собой по существу первый компонент вакцины «Гам-КОВИД-Вак» и предназначенной для ускорения массовой вакцинации путём однократного введения препарата. Длительность защитного эффекта при этом предполагается ниже, чем от полной вакцинации «Спутник V» (со слов А. Гинцбурга, в пределах 4—5 месяцев[90]), при этом при необходимости возможно довакцинирование вторым её компонентом[91][92][93].
4 марта 2021 года Европейское агентство лекарственных средств (EMA) начало проверку вакцины «Спутник V» на соответствие стандартам ЕС по эффективности, безопасности и качеству[94].
Испытания
Доклинические испытания
Доклинические испытания рекомбинантной вакцины на токсичность, безопасность, иммуногенность и защитную эффективность на крупных и мелких животных были проведены на базе 48 ЦНИИ МО РФ. Испытания проводились на двух видах чувствительных млекопитающих: на золотистых сирийских хомячках и двух видах приматов. Достижения сотрудников военного НИИ помогли сократить сроки доклинической оценки безопасности и эффективности вакцины. В частности, использовалась разработанная в НИИ методология количественной оценки возбудителя и лабораторная модель воспроизводства тяжёлого острого респираторного заболевания[95][96].
Клинические испытания
Результаты 1 и 2 фазы испытаний были опубликованы 4 сентября 2020 года в журнале «The Lancet»[97]. В них приняло участие в общей сложности 76 человек (2 группы по 38 человек[98][99]), большинство побочных эффектов было умеренным, серьёзных побочных эффектов не было, смертей не было. Испытания 3 фазы были проведены с 7 сентября по 24 ноября 2020 года уже после регистрации вакцины Министерством здравоохранения РФ[7], и также опубликованы в журнале «The Lancet»[13]. В них получили вакцину 16 427 человек, и 5 435 были в группе плацебо. Эффективность вакцины составила 91—95 %. У получивших вакцину большинство нежелательных явлений было 1-й степени (7 485 явлений). 45 человек из вакцинной группы и 23 из плацебо-группы имели серьёзные побочные явления, но ни одно из них не было признано связанным с вакцинацией. Было зарегистрировано четыре случая смерти (три из вакцинной группы и один из группы плацебо), однако они не были связаны с вакциной[34].
Фаза I / II клинических испытаний «Гам-КОВИД-Вак»
Данная фаза клинических испытаний представляет собой открытое исследование безопасности, переносимости и иммуногенности препарата «Гам-КОВИД-Вак» (англ. Gam-COVID-Vac). 16 июня 2020 года Минздрав РФ выдал разрешение № 241 на проведение данного клинического исследования (КИ)[100].
Испытания жидкой вакцины проводились в Главном военном клиническом госпитале (ГВКГ) имени Н. Н. Бурденко (в филиале № 7 в г. Сергиев Посад-6)[101][102][103][104]. В испытании приняли участие 38 добровольцев. На первом этапе испытания (фаза I) была протестирована безопасность, переносимость и иммуногенность каждого компонента вакцины в отдельности: первой группе из 9 человек был инъецирован компонент I, второй группе из 9 человек был инъецирован компонент II. На втором этапе (фаза II) испытание проводилось по бустерной схеме: 20 человек получили инъекции компонента I, и через 21 день — компонента II. У всех добровольцев выработались высокие титры антител COVID‑19. При этом ни у кого из них не было отмечено серьёзных осложнений иммунизации[105].
Фаза I / II клинических испытаний «Гам-КОВИД-Вак-Лио»
Данная фаза клинических испытаний представляет собой открытое исследование безопасности, переносимости и иммуногенности препарата «Гам-КОВИД-Вак Лио» (англ. Gam-COVID-Vac Lyo). 16 июня 2020 года Минздрав РФ выдал разрешение № 242 на проведение КИ[100].
Испытания лиофильно высушенной вакцины проводились в Сеченовском университете. В испытании приняли участие 38 добровольцев. На первом этапе (фаза I) была протестирована безопасность, переносимость и иммуногенность каждого компонента вакцины в отдельности: первой группе из 9 человек был введён компонент I, второй группе из 9 человек был введён компонент II. На втором этапе (фаза II) испытание проводилось по бустерной схеме: 20 человек получили инъекции компонента I, а через 21 день — компонента II. У всех добровольцев были определены высокие титры антител к COVID‑19, ни у кого из них не было отмечено серьёзных осложнений после иммунизации[98].
Фаза III клинических испытаний (пострегистрационная)
Данная фаза представляет собой рандомизированное двойное слепое плацебо-контролируемое многоцентровое клиническое исследование при параллельном определении эффективности, безопасности и иммуногенности комбинированной векторной вакцины «Гам-КОВИД-Вак» в профилактическом лечении инфекции SARS-CoV-2. Разрешение на проведение данного КИ под номером № 450 было выдано Минздравом РФ 25 августа 2020 года, уже после регистрации вакцины[100][106]. В данном КИ предполагалось принять 40 000 добровольцев в возрасте от 18 лет, разделённых на две группы (3:1) — исследовательская группа из 30 000 добровольцев, получающих комбинированную векторную вакцину Гам-КОВИД-Вак против вируса SARS-CoV-2, и контрольная группа из 10 000 добровольцев, получающих плацебо[107]. В итоге, согласно промежуточным результатам, которые были опубликованы в журнале «The Lancet»[13], непосредственно вакцину получили от 14 964 до 16 427 человек, в группу плацебо вошли от 4902 до 5435[13]. Прививка первой дозой выполнена с 7 сентября по 24 ноября 2020 года[13]. Вакцинация участников третьей фазы испытаний закончилась в декабре 2020 года, а наблюдение за ними должно было длиться 180 дней[37].
Исследование началось 26 августа 2020 на территории Москвы, были задействованы 25 медицинских организаций города[108]. Мониторинг здоровья участников должен был длиться как минимум 6 месяцев, для этого было создано специальное мобильное приложение с дневником самонаблюдения, а некоторые участники получили электронные браслеты для измерения артериального давления и температуры тела[109].
Согласно реестру испытаний, завершение III—IV фаз на основной выборке из 40 000 участников запланировано на 31 декабря 2022[100].
В феврале 2022 года стало известно, что вакцина получила постоянную регистрацию в России[110].
Клинические исследования с участием добровольцев 12—17 лет
5 июля 2021 года в Москве на базе двух больниц начались первая и вторая фаза испытаний вакцины на подростках в возрасте от 12 до 17 лет. Исследование ведётся на 100 добровольцах, ранее не болевших COVID-19 и продлится один год, при этом для подростков предполагается использовать меньшую дозировку препарата. Начало третьей фазы этих испытаний запланирована на конец лета 2021 года[12].
Фаза III, клиническое исследование с участием добровольцев старше 60 лет
Проводится исследование безопасности, переносимости и иммуногенности вакцины «Гам-КОВИД-Вак» против COVID-19 с участием добровольцев в возрастной группе старше 60 лет. Разрешение на проведение было выдано Минздравом РФ 13 октября 2020 года (№ 566); завершение испытаний запланировано на 31 декабря 2021 года[100]. В исследовании принимают участие 110 человек[111] (по данным реестра может принять до 150 человек).
В марте 2021 года глава центра Гамалеи сообщил, что, несмотря на предварительные опасения, вакцина показала одинаковую эффективность для пациентов старше 60 и даже старше 80 лет[15].
Клинические исследования в других странах
Клинические исследования II / III фазы проводились в Беларуси[112], Индии[113], Венесуэле[114], ОАЭ[115].
Фаза IV
Наблюдательные клинические исследования проводятся в Сан-Марино[116], Сербии[117], Бразилии[118], Аргентине[119] и других странах.
Эффективность
11 ноября 2020 года НИЦЭМ им. Н. Ф. Гамалеи совместно с Российским фондом прямых инвестиций опубликовали первый промежуточный анализ данных фазы III клинических исследований вакцины в России. Согласно публикации, эффективность применения вакцины «Спутник V» составила 92 %, расчёт проводился на основе распределения 20 подтверждённых случаев, выявленных в группе плацебо и в группе, получавшей вакцину[120].
2 февраля 2021 года в журнале «The Lancet» были опубликованы более полные промежуточные результаты исследования фазы III[85][121]. В анализ первичных результатов были включены 19 866 человек, получивших вакцину или плацебо. После 21-го дня исследования у 16 из 14 964 участников в группе вакцинированных (0,1 %) и 62 из 4 902 участников в группе плацебо (1,3 %) подтвердился COVID-19. Эпидемиологическая эффективность[122] вакцины составила 91,6 %+3,6%
−5,7% (погрешность указывает 95%-й доверительный интервал, обусловленный вероятностным статистическим разбросом). 97 случаев COVID-19 (63 в группе вакцинированных и 34 в группе плацебо) отмечены ранее, чем через 21 день после введения первой дозы, то есть до начала действия иммунитета, вызванного вакциной, и в анализ не включены. Эпидемиологическая эффективность для участников старше 60 лет равна 91,8 % (в 95%-м доверительном интервале от 67,1 % до 98,3 %) и статистически не отличается от эффективности для всей группы. Случаев умеренного или тяжёлого течения COVID-19 в группе вакцинированных не отмечено, в группе плацебо таких было 20; это означает эффективность против таких форм болезни в 95%-м доверительном интервале от 94,4 % до 100 %. Расхождение между вероятностями заболевания в группах вакцинированных и плацебо на временно́м графике начинается примерно на 18-й день после получения первой дозы[85][121].
| Возраст, лет | Случаев COVID-19 |
Группа вакцины (случаев / из / %) |
Группа плацебо (случаев / из / %) |
Эффективность (в доверит. интервале 95 %) |
|---|---|---|---|---|
| 18—30 | 5 | 1 / 1596 (0,1 %) | 4 / 521 (0,8 %) | 91,9 % (51,2—99,3) |
| 31—40 | 17 | 4 / 3848 (0,1 %) | 13 / 1259 (1,0 %) | 90,0 % (71,1—96,5) |
| 41—50 | 19 | 4 / 4399 (0,1 %) | 15 / 1443 (1,0 %) | 91,3 % (73,7—96,9) |
| 51—60 | 27 | 5 / 3510 (0,1 %) | 22 / 1146 (1,9 %) | 92,7 % (81,1—97,0) |
| > 60 | 10 | 2 / 1611 (0,1 %) | 8 / 533 (1,5 %) | 91,8 % (67,1—98,3) |
| Всего | 78 | 16 / 14964 (0,1 %) | 62 / 4902 (1,3 %) | 91,6 % (85,6—95,2) |
| Эффективность вакцины «Спутник V» в зависимости от времени[85] | ||||
| Начиная со дня 1-й дозы | 175 | 79 / 16427 (0,5 %) | 96 / 5435 (1,8 %) | 73,1 % (63,7—80,1) |
| Начиная с 14 дня после 1-й дозы | 109 | 30 / 14999 (0,2 %) | 79 / 4950 (1,6 %) | 87,6 % (81,1—91,8) |
19 апреля 2021 представители Российского фонда прямых инвестиций в своём пресс-релизе заявили, что эффективность вакцины «Спутник V» по результатам анализа данных 3,8 млн вакцинированных россиян составила 97,6 %. Согласно данным о вакцинации россиян, полностью привитых обоими компонентами в период с 5 декабря 2020 года по 31 марта 2021 года в рамках программы массовой гражданской вакцинации, заболеваемость начиная с 35-го дня с даты первого укола составила всего 0,027 %. При этом заболеваемость среди невакцинированного взрослого населения за сопоставимый период с 35-го дня после запуска массовой гражданской вакцинации составила 1,1 %[16].
16 февраля 2021 года специалисты научного центра вирусологии и биотехнологии «Вектор» заявили о подтверждении эффективности «Спутника V» в отношении британского штамма COVID-19 («Альфа»)[17], а 16 июня 2021 года А. Л. Гинцбург сообщил, что лабораторные исследования показали высокую эффективность вакцины против «индийского» штамма коронавируса («Дельта»)[18].
12 июля 2021 года в ведущем международном журнале «Vaccines» опубликовали данные о том, что «Спутник V» эффективен против новых штаммов коронавируса[19][123]. Согласно данным статьи, снижение уровня вируснейтрализующей активности к ряду штаммов у «Спутника V» значительно меньше по сравнению другими вакцинами.
В сентябре 2021 года аргентинские учёные заявили, что вакцинация двумя компонентами «Спутник V» эффективнее против дельта-штамма, чем после препаратов компаний AstraZeneca и Sinopharm[124].
Независимые исследования эффективности
Россия. НИИ гриппа им. А. А. Смородинцева в сотрудничестве с Институтом междисциплинарных медицинских исследований при Европейском университете в Санкт-Петербурге с 19 февраля 2021 года проводят исследование жителей Санкт-Петербурга, привитых «Спутником V» и давших согласие на измерение уровня антител в крови. Выраженный иммунный ответ уже после первой дозы вакцины отмечался у 83 % участников; на 70-й день (уже после введения второй дозы) антитела IgG не были обнаружены у единственного участника из нескольких сотен. Также у большинства привитых нарастали титры нейтрализующих антител (нейтрализующие антитела на протяжении 70 дней не определялись только у 3 из 57 исследованных)[125]. Методика исследований и предварительные данные были опубликованы в американском журнале «Journal of Medical Virology[en]»[126], а текущие результаты — в журнале «Scientific Reports[en]», издаваемым британской Nature Publishing Group[127]. Один из авторов исследования, эпидемиолог Антон Барчук считает, что исследование подтверждает данные по эффективности, полученные создателями «Спутника V»[37].
В препринте исследования, проведённого этой группой учёных, был сделан вывод о 81 % эффективности вакцины в предотвращении госпитализации и 76 % эффективности в защите от тяжёлых повреждений лёгких[128][129]. Хотя достоверно неизвестно, какой вакциной прививались испытуемые и каким штаммом заражались, подавляющее большинство россиян привито вакциной «Спутник V» и заражено штаммом Дельта.
В публикации научной статьи в журнале Vaccines, авторами которой являются Ольга Матвеева и Александр Ершов описан анализ выборки заболевших москвичей. Выборка была создана летом 2021 года из тех, кто обратился за медицинской помощью в июне и июле 2021 года. В это время в Москве доминировал Дельта вариант коронавируса. В анализе был выявлен тренд на повышение эффективности вакцины «Спутник V» по мере увеличения тяжести заболевания. Эффективность вакцины была выше в отношении смерти или тяжелой формы COVID-19. Кроме того, защитный эффект вакцины был сильнее выражен в более молодых возрастных группах. Для наиболее молодой группы (18—50 лет) эффективность вакцины по предотвращению смерти составляла 95 %, а для старшего поколения (50+) эффективность вакцины была уже ниже и составила 74 %. Защита от тяжелой формы заболевания в группе 18-50 лет в июне-июле была оценена как 81 %, а в группе старше 50 лет — 68 %[130].
Венгрия. В апреле 2021 года власти Венгрии опубликовали результаты исследований эффективности пяти вакцин (используемых в стране «Спутника V», «Moderna», «Pfizer», «Sinopharm» и «AstraZeneca»), проводившихся период с декабря 2020 года по 20 апреля 2021 года и оценивающих процент заболевших и умерших среди вакцинированных двумя компонентами. Согласно их данным, «Спутник V» показал наименьший процент по обоим показателям: на 100 000 населения, привитого этой вакциной, заболело 95 человек (менее 0,1 %), а средняя смертность составила 1 человек (0,001 %)[131][132]. Ряд исследователей обратили внимание, что «Спутник V» начал использоваться в стране позже других вакцин (с 11 февраля), в связи с чем вероятность заболеть после прививки им была меньше, а также что не были опубликованы возрастные группы вакцинированных и методика подсчёта, в связи с чем цифры могут быть неточны. В то же время, сама эффективность «Спутника V» под сомнение ими не ставилась[133].
В ноябре 2021 опубликовано исследование, оценивающее эффективность тех же пяти вакцин на 3,74 млн жителей Венгрии, привитых обеими дозами, в том числе на 0,82 млн, привитых «Спутником V». Согласно опубликованным результатам, относящимся к периоду с 22 января по 10 июля 2021, усреднённая по возрастным когортам эффективность «Спутника V» против заражения составила 85,7 % («Pfizer» — 83,3 %, «Moderna» — 88,7 %, «AstraZeneca» — 71,5 %, «Sinopharm» — 68,7 %). Эффективность вакцин против смерти от COVID-19 составила от 87,8 % («Sinopharm») до 97,5 % («Спутник V»). Частота заражений среди людей, привитых «Спутником V», составила 1,73 случая на 100 000 человеко-дней (среди невакцинированных — 59,03 случая, отношение рисков — 34,1); частота смертей — 0,04 случая на 100 000 человеко-дней (среди невакцинированных — 1,88 случая, отношение рисков — 47)[134].
Аргентина. Министерство здравоохранения провинции Буэнос-Айрес (Аргентина) заявило[135] в начале июня 2021, что согласно проведённому в регионе исследованию среди населения в возрасте 60—79 лет, эффективность первой дозы «Спутника V» составляет 78,9 % против заражения COVID-19, 84,7 % против смерти от коронавирусной болезни и 87,6 % против госпитализации. Группы включали 40 387 однократно вакцинированных с 29 декабря 2020 по 21 марта 2021 и 146 194 невакцинированных; включены только лица, ранее не болевшие COVID-19; учитывались лишь случаи болезни с 21 дня после вакцинации. Этот результат согласуется с опубликованной разработчиками эффективностью от заражения, равной 79,4 % для первой дозы.
Чуть позже, 1 июля 2021 года, министерство здравоохранения Аргентины сообщило, что по предварительным результатам на выборке из 471 682 аргентинцев возрастом старше 60 лет в феврале-июне 2021, эффективность против смерти от COVID-19 составляет 74,9 % для первой дозы «Спутника V» и 93,3 % для полного двухдозового курса вакцинации (для сравнения, в тех же условиях вакцина AstraZeneca показала эффективность 79,5 % и 88,8 %, вакцина Sinopharm — 61,6 % и 84,0 %)[136].
15 июля власти Аргентины опубликовали результаты нового исследования[137], проведённого Национальным научно-техническим исследовательским советом. Согласно данным исследования, более 90 % привитых «Спутником V», помимо выработки антител, получают и долгосрочный клеточный иммунитет[138][139].
Ещё одно исследование, проведённое под руководством американских учёных и опубликованное 26 июля в журнале «Nature Communications»[20], показало эффективность «Спутника V» против различных штаммов коронавируса. Учёные установили, что вакцина хорошо справляется с исходной версией вируса и штаммом «Альфа»; со штаммом «Бета» и вирусами с мутацией E484K — хуже, но при этом всё равно защищает от тяжёлых форм заболевания. Действие против штамма «Дельта» в данной работе не оценивалось[21][140].
В проведённом сотрудниками НИИ Гамалеи исследовании нейтрализующих антител против штамма Омикрон и против штамма B.1.1.1. после вакцинации «Спутник V» был сделан вывод, что уровень нейтрализующих антител против Омикрона в 11,76 раз ниже у вакцинированных и в 7,13 раз ниже у вакцинированных и ревакцинированных, чем уровень нейтрализующих антител против штамма B.1.1.1., причём нейтрализующие антитела к Омикрону были обнаружены у всех ревакцинированных[141].
В журнале EClinicalMedicine от Lancet было опубликовано исследование эффективности однокомпонентной вакцины «Спутник Light» для пожилых людей[142]. Она была проверена в реальных условиях в ходе ретроспективного когортного исследования. Приняли участие около 80000 человек в возрасте от 60 до 79 лет, наблюдение длилось до 82 дней, в среднем 44 дня.
Вакцина оказалась на 78,6 % процента эффективна против инфекции, на 87,6 % против госпитализации и на 84,8 % против смерти. Такая эффективность сопоставима с эффективностью одной дозы других вакцин от COVID-19. Люди, принявшие участие в исследовании, могли не отражать всю популяцию, бессимптомные инфекции и эффективность вакцинации против новых штаммов вируса не были тщательно изучены.
В ещё одном исследовании из Аргентины были изучены антитела после «Спутника V» у 118 медицинских работников младше 65 лет[143]. В течение 6 месяцев изучалось их количество и эффективность против различных штаммов вируса. Титры антител за это время сократились в 3-4 раза. Но нейтрализующая способность этих антител против всех штаммов коронавируса при этом росла. Явление увеличения эффективности антител при снижении их концентрации уже наблюдалось у переболевших людей. Нейтрализующая активность антител была снижена в 2,9, 9,7, 4,2 и 3,4 раза для Альфа, Бета, Гамма и Дельта штаммов по сравнению с оригинальным штаммом через 120 дней после прививки.
В сентябре 2021 года специалисты Института вирусологии факультета медицинских наук Национального университета Кордовы обнародовали результаты исследования ведущих мировых вакцин на способность защищать людей от штамма «Дельта». Самой эффективной в этом вопросе была названа российская «Спутник V», следовали за ней в рейтинге AstraZeneca и Sinopharm. При этом лучше, по версии аргентинских учёных, «Спутник V» от «Дельта»-штамма защищает тех, кто привился его обоими компонентами, но до этого никогда не болел COVID-19[144].
Белоруссия. В ноябре 2021 опубликован препринт специалистов из Белоруссии, где выполнена оценка эффективности «Спутника V». На 1 сентября 2021 (7—8 месяцев с начала вакцинации) среди 1,216 млн полностью вакцинированных «Спутником V» доля заболевших ковидом составляет 0,19 %, тогда как среди непривитого населения — 5,08 % (отношение рисков — 26,7)[145].
Другие страны. 6 июля 2021 года в журнале «Nature» была опубликована статья, обобщающая имеющиеся данные о безопасности и эффективности вакцины[146][147]. Автор статьи сделал вывод, что несмотря на преждевременную регистрацию вакцины в России и критику первых исследований, данные указывают на то, что вакцина безопасна и эффективна и может в скором времени получить одобрение ВОЗ и EMA. По данным статьи, исследования «Спутника V» в ОАЭ, проведённые на 81 тыс. человек с введением обеих доз вакцины, показало эффективность 97,8 % в предотвращении симптоматического COVID-19 и 100 % — от предотвращения тяжёлого течения болезни. Изложены также вышеприведённые оценки эффективности, полученные в Аргентине, и резюмированы исследования безопасности в Аргентине и Сан-Марино (см. Независимые исследования безопасности).
Высокая эффективность российского «Спутника V» доказана и эпидемиологами Сан-Марино и римского Национального института инфекционных заболеваний имени Л. Спалланцани. Их совместное исследование показало, что антитела вырабатываются у 99 % привитых российской вакциной против коронавируса — в большом количестве и высокого качества. Исследование было не только лабораторным, но и жизненным: подавляющее большинство граждан Сан-Марино привиты «Спутником V» — заболеваемость в государстве нулевая, как официально не раз заявляли власти[148].
Безопасность
Технологической платформой, на которой создана вакцина «Спутник V», является вирусный вектор — инструмент, используемый для доставки генетического материала в клетки. Впервые такая технология была использована в 1970-х годах[149]. В «Спутнике V» используется нереплицируемый вирусный вектор — то есть вирус, лишённый механизма размножения, поэтому он не представляет опасности заражения для организма. Вектор используется для транспортировки в клетку вакцинируемого организма генетического материала из другого вируса, против которого делается вакцина.
Конкретно в качестве вектора в вакцине «Спутник V» используется аденовирусный вектор. Аденовирусы, извлекаемые из аденоидов человека и в обычном состоянии вызывающие ОРВИ (аденовирусную инфекцию), уже в 1990-х годах стали использовать для создания векторов[150]. Технология использования аденовирусных векторов в качестве векторных вакцин является безопасной и эффективной, что подтверждается в многочисленных исследованиях[150].
На этой технологической платформе создано 3 вакцины против лихорадки Эбола[151], с помощью которых вакцинировано более 60 000 человек в Африке, Китае и России[152]; одобрено 2 препарата против рака, использованные для терапии более 30 000 человек в Китае[153]; проведено более 250 клинических исследований[150], проведены или ведутся исследования по долгосрочной безопасности, в том числе отсутствие риска канцерогенности и снижения фертильности препарата[154].
По предварительным данным фазы III клинических исследований вакцины «Спутник V», опубликованных[85] её разработчиками в феврале 2021 года в медицинском журнале The Lancet, вакцина является безопасной в применении. Статью разработчиков в журнале прокомментировал профессор Ян Джонсон (Великобритания), признавший эффективность и безопасность этой вакцины[11].
45 участников (0,3 %) из 16 427 в группе вакцинирования и 23 (0,4 %) из 5435 в группе плацебо сообщили о серьёзных побочных эффектах, однако независимый комитет по мониторингу данных подтвердил, что они не связаны с вакцинированием. В ходе исследования умерло четыре испытуемых: 3 из 16 427 вакцинированных и 1 из 5435 в группе плацебо. В группе вакцинированных одна смерть была связана с переломом грудного отдела позвоночника, две — с COVID-19. У умерших от COVID-19 симптомы развились на 4-й и на 5-й день после первой дозы вакцины (таким образом, оба участника были инфицированы до включения в исследование, несмотря на отрицательный результат ПЦР), оба имели сопутствующие заболевания (сердечно-сосудистые и эндокринологические, соответственно). В группе плацебо участник умер от геморрагического инсульта[85][121].
Исследования совместимости
Государственный конгресс Сан-Марино объявил о первых результатах двух начатых исследований вакцины Sputnik V, широко используемой в этой маленькой стране, совместно с Болонским университетом и Римским Национальным институтом инфекционных заболеваний Lazzaro Spallanzani («Спалланцани») в Риме. Первое исследование, проведённое в сотрудничестве с Болонским университетом, было посвящено выявлению побочных реакций на введение препарата, которые на данный момент «можно сказать практически нулевые».
Второе исследование, даже более важное, касается количественной и качественной оценки антител, разработанных российской вакциной: «Исследование все ещё продолжается, но собранные на данный момент данные показывают, что эффективность вакцины выше, чем указано в исследованиях, опубликованных в специализированных журналах, таких как Lancet. Эффективность близка к 100 %». Члены Государственного Конгресса оценили сотрудничество с Российским фондом РФПИ как «отличное» и выбор использования Sputnik V «выигрышным»[155].
Независимые исследования безопасности
Аргентина. Министерство здравоохранения провинции Буэнос-Айрес (Аргентина) опубликовало 24 июня 2021 года результаты мониторинга безопасности вакцин на материале 2,8 млн доз вакцины «Спутник V», использованных в этом регионе с 29 декабря 2020 по 3 июня 2021 (в сравнении с 1,3 млн доз и 0,9 млн доз вакцин «Sinopharm» и «Covishield/AstraZeneca», соответственно). Частота тяжёлых «реакций, предположительно обусловленных иммунизацией» (РПОИ), составляет 0,7; 0,8 и 3,2 случая на миллион доз для перечисленных трёх вакцин, соответственно. Среди лёгких РПОИ, связанных с вакцинацией «Спутником V», отмечаются лихорадка (47 %), головная боль (45 %), боль в мышцах или суставах (39,5 %), а также реакции в месте инъекции: боль (46,5 %) и зуд (7,4 %). Смертей, связанных с иммунизацией, не зафиксировано[156].
Опубликован также более полный отчёт Минздрава Аргентины о безопасности вакцин[119] по результатам применения 6 964 344 доз «Спутника V» (в основном первой инъекции) с 29 декабря 2020 по 2 июня 2021 года включительно. В отчёте утверждается, что количество наблюдавшихся побочных эффектов составляет 40 445 (соответствует частоте 0,58 %), серьёзных (то есть потребовавших госпитализации) побочных эффектов — 194 случая, или 0,00278 % (что чуть меньше, чем у «AstraZeneca», и больше, чем у «Sinopharm»)[157][158][159]. Авторы отчёта предостерегают от прямого сравнения безопасности вакцин по этим данным, поскольку распределение вакцин по половозрастным когортам и по датам вакцинирования различается. Смертей, связанных с вакцинацией «Спутником V», не зарегистрировано. 38 098 случаев побочных эффектов, считающихся связанными с иммунизацией «Спутником V», классифицированы следующим образом:
- головная боль с мышечной болью и/или с болью в суставах и/или астенией: 15 287 случаев (0,219 %);
- повышенная температура с головной болью и/или с мышечной болью и/или болью в суставах и/или с астенией: 14 397 случаев (0,207 %);
- местная реакция с повышением температуры или без него: 3893 случая (0,056 %);
- повышенная температура: 1837 случаев (0,026 %);
- боль в месте инъекции: 1259 случаев (0,018 %);
- желудочно-кишечный синдром с повышением температуры или без него: 678 случаев (0,009 %)
- аллергия: 634 случая (0,009 %);
- лимфаденопатия (увеличение лимфоузлов): 94 случая (0,001 %);
- анафилаксия: 9 случаев (0,0001 %);
- ощущение металлического запаха: 9 случаев (0,0001 %);
- температура выше 40 °C: 6 случаев (<0,0001 %);
Кроме того, для 316 случаев госпитализации (0,0045 %) продолжается анализ их возможной связи с вакцинацией. Для 5 случаев госпитализации после прививки связь с вакцинацией не установлена: 2 случая синдрома Гийена — Барре (острый полирадикулоневрит), 2 случая иммунной тромбоцитопении и 1 случай перикардита.
Белоруссия. В ноябре 2021 опубликован препринт специалистов из Белоруссии[145], где выполнена оценка безопасности «Спутника V» по результатам его применения в этой стране. На 1 сентября 2021 (7-8 месяцев с начала вакцинации) среди 1,487 млн вакцинированных «Спутником V» (в том числе 1,216 млн полностью вакцинированных, то есть в сумме 2,703 млн доз) наблюдалось 80 832 случая побочных реакций (2,99 %), большинство из которых оценены как слабые и умеренные (головная боль, гипертермия, астения). Обнаружены две серьёзные побочные реакции, обе после первой дозы: аллергическая крапивница и анафилактоидная реакция; оба пациента полностью восстановились без каких-либо последствий. За рассматриваемый период среди вакцинированного населения зарегистрирована 281 смерть (независимо от причины), все случаи не связаны с вакцинацией.
Сан-Марино. Исследователи из Италии, Великобритании и Сан-Марино выполнили[160][161] обследование лиц, вакцинированных «Спутником V» в Сан-Марино, которые опрашивались через 7 дней после прививки (2558 человек после введения первой дозы, 1288 человек — после второй дозы). Медианный возраст участников 68 лет, 56 % — женщины. После первой дозы 16,4 % участников сообщили и о местных, и о системных побочных эффектах, 25,8 % — только о системных, 10,2 % — только о местных симптомах. После второй дозы проявления побочных эффектов составляли, соответственно, 31,9 %, 18,5 % и 16,1 %. Главные побочные эффекты вакцинирования: боль в месте укола (24,8 % после первой дозы и 43,8 % после второй), астения (23,8 % и 31,9 %), головная боль (18,5 % и 21,0 %), боль в суставах (16,5 % и 21,9 %). Степень проявления побочных симптомов (оценивалась по 4-балльной системе) после первой дозы 20 участников оценили как значительную (степень 3) и 8 как сильную (степень 4). После второй дозы 3-ю степень указали 17 участников и 4-ю степень — 4 участника. В абсолютном большинстве случаев все проявления побочных эффектов укладывались в двое суток после прививки. Тяжёлых реакций на иммунизацию не выявлено. Исследования продолжены до 3-месячного срока после прививки.
12 июля 2021 года были опубликованы результаты наблюдательного исследования 4 фазы «ROCCA», проведённого на 2558 пациентах старшего возраста (66±14 лет). Исследование продемонстрировало высокий профиль безопасности вакцины для людей старше 60 лет при массовой вакцинации населения. В сравнении с другими вакцинами против COVID-19 «Спутник V» имеет более высокий или равный профиль переносимости. Побочные эффекты у «Спутник V» не превышают таковых у других вакцин, пациенты с хроническими заболеваниями, согласно результатам исследования, переносят «Спутник V» лучше, чем альтернативы[116].
Сербия. 12 июля 2021 года заместитель министра здравоохранения Сербии Мирсад Джерлек заявил, что вакцина «Спутник V» вызвала наименьшее число побочных эффектов по сравнению с другими вакцинами. В Сербии двумя компонентами вакцин привито более 3 млн человек (почти половина населения), из них до 25 % — «Спутником V»[117].
Иран. От 13435 вакцинированных в Иране медицинских работников авторы исследования получили 3236 отчётов о побочных эффектах. Наиболее распространёнными побочными эффектами были боль в месте инъекции (56,9 %), усталость (50,9 %), боль в теле (43,9 %), головная боль (35,7 %), лихорадка (32,9 %), боль в суставах (30,3 %), озноб (29,8 %) и сонливость (20,3 %). Анафилактический шок наблюдался у 0,1 % вакцинированных, о смертельных исходах не сообщалось. Побочные эффекты чаще возникали у молодых людей, чем у старых, чаще у женщин, чем у мужчин, чаще после первой инъекции, чем после второй. Результаты исследования также подтверждают высокую гуморальную иммуногенность против COVID-19 после получения вакцины Спутник V[162].
Статья в журнале «Nature». Данные различных испытаний «Спутника V» в разных странах были обобщены в журнале «Nature» за 6 июля 2021 года. В нём сообщалось[146], что упомянутые выше исследования в Аргентине, основанные на применении 2,8 млн доз «Спутника V», показали отсутствие случаев со смертельным исходом и выявили главным образом лёгкие побочные эффекты. О смертельных случаях, по данным статьи, не сообщали также и власти Сан-Марино (данные приведены выше) и Сербии, где вакцина широко применяется. Исследования в других странах, согласно данным статьи, также показали, что вакцина «Спутник V» не приводит к образованию тромбов[147].
Репродуктивная безопасность. Исследования репродуктивной безопасности «Спутника V» были выполнены в России в Национальном медицинском исследовательском центре акушерства, гинекологии и перинатологии им. В. И. Кулакова группой учёных, независимой от разработчиков вакцины. Исследователи не обнаружили влияния вакцины на репродуктивное здоровье как мужчин[163], так и женщин[164].
Спутник Лайт
6 мая 2021 года Министерство здравоохранения Российской Федерации зарегистрировало однокомпонентную вакцину «Спутник Лайт»[165] (регистрационное удостоверение номер ЛП-006993[166]). Вакцина «Спутник Лайт» (англ. Sputnik Light) — это первый компонент вакцины «Спутник V», он основан на векторе из рекомбинантного аденовируса человека 26-го серотипа (rAd26).
Согласно разработчикам вакцины, эффективность однокомпонентной вакцины «Спутник Лайт» составляет 79,4 % на основании анализа данных с 28 дня после получения иммунизации гражданами РФ в рамках программы массовой вакцинации в период 5 декабря 2020 года — 15 апреля 2021 года[167], а показатель эффективности на уровне около 80 % превышает показатели эффективности многих вакцин, требующих двукратного введения вакцины на курс вакцинации[167].
Согласно разработчикам вакцины, фаза I/II исследования безопасности и иммуногенности «Спутник Лайт» продемонстрировала следующие результаты:[167]
- иммунизация вакциной «Спутник Лайт» позволяет выработать антиген-специфические IgG-антитела у 96,9 % вакцинированных лиц на 28-й день;
- вирус-нейтрализующие антитела вырабатываются на 28-й день после вакцинации у 91,67 %;
- клеточный иммунный ответ к S-белку SARS-CoV-2 формируется у 100 % вакцинированных уже на 10-й день;
- иммунизация вакциной «Спутник Лайт» лиц, у которых есть предсуществующий иммунитет к SARS-CoV-2, позволяет более чем в 40 раз увеличить уровень антиген-специфических IgG антител у 100 % вакцинированных уже на 10-й день;
- серьёзных нежелательных явлений после иммунизации препаратом «Спутник Лайт» не зарегистрировано.
25 июня 2021 года первые серии вакцины «Спутник Лайт» вышли из производства в гражданский оборот[168].
18 ноября 2021 года Минздрав России рекомендовал использовать «Спутник Лайт» для ревакцинации через полгода после первичной в условиях пандемии COVID-19, а также через 6 месяцев после перенесённого заболевания[169].
По состоянию на начало января 2022 года вакцина «Спутник Лайт» была зарегистрирована более чем в 30 странах мира[170].
Гам-КОВИД-Вак-М
24 ноября 2021 года Министерство здравоохранения Российской Федерации зарегистрировало вакцину от коронавируса «Спутник М» (регистрационное наименование — «Гам-КОВИД-Вак-М»[171][172], лат. Gam-COVID-Vac-M[172]) для подростков в возрасте от 12 до 17 лет[173]. Буква «М» означает «для маленьких»[174].
Центр имени Гамалеи заявил, что вакцина сформировала клеточный иммунитет у 93,2 % добровольцев[175].
«Спутник М» представляет собой аналог вакцины «Спутник V», концентрация которой снижена в 5 раз[176][177]. Прививка проводится двумя компонентами.
Подростков в возрасте до 15 лет прививают с согласия родителей, старше 15 лет при наличии их собственного письменного согласия[178].
Предполагалось, что в гражданский оборот вакцина «Спутник М» поступит в конце декабря 2021 года[179]. Однако первые поставки вакцины поступили в регионы лишь в середине января 2022 года[180].
Гам-КОВИД-Вак (назальная форма)
В начале 2021 года стало известно о ведении центром имени Гамалеи работ по созданию назальной формы вакцины Спутник V, которая будет представлять собой второй компонент оригинальной вакцины в виде спрея. По словам главы центра Гамалеи А. Л. Гинцбурга новая форма вакцины позволит сформировать дополнительный иммунитет, благодаря которому вакцинированные не будут распространять инфекцию, хотя и не сможет заменить инъекционную вакцину[181][182].
В феврале 2022 года Гинцбург сообщил, что испытания «Спутника V» в виде спрея проходят успешно, при этом срок испытаний могут сократить, чтобы быстрее ввести препарат в гражданский оборот. По мнению разработчиков вакцины, такая форма даёт меньше побочных эффектов[183].
Производство вакцины
На начало июля 2021 года выпуск «Спутника V» в России осуществлялся на 9 производственных площадках[147].
Кроме того, на конец апреля 2021 года РФПИ были заключены соглашения с 20 производителями вакцин в 10 странах мира[184].
4 июня производство вакцины началось в Сербии, которая стала первой европейской страной, которая начало производство российской вакцины в рамках программы вакцинации населения[185].
22 июля ряд южнокорейских компаний выступил с заявлением, что они получили все необходимые технические инструкции для производства российской вакцины и для начала её производства необходимо лишь получение разрешения на государственном уровне[186].
| Страна производства | Дата начала производства | Производитель | Примечания |
|---|---|---|---|
| С 15 августа 2020 года[84] | «Медгамал» (НИЦЭМ им. Н. Ф. Гамалеи), г. Москва[187] «Генериум» (АО «Фармстандарт»), п. Вольгинский, Владимирская обл.[188] «Биннофарм» (АФК «Система»), г. Москва, г. Зеленоград[189] «Биокад», Санкт-Петербург[190] «Р-Фарм», г. Москва[191] |
||
| С 21 декабря 2020 года[192] | Карагандинский фармацевтический комплекс (КФК), Караганда[192] | ||
| С конца декабря 2020 года[193] | Консорциум из 7 фарм. компаний во главе с «GL Rapha» (Hankook Korus), Чхунчхон[193] | Масштабирование производства с апреля 2021 года[193] | |
| С 15 января 2021 года[194] | «Uniao Quimica» (запланировано на июнь 2021)[195][196] | Серийный выпуск с мая 2021 года. Препарат будет направляться и в другие страны Латинской Америки[197]. | |
| С 26 февраля 2021 года[198] | РУП «Белмедпрепараты»[198] | Серийный выпуск с 25 марта 2021 года[198] | |
| С 20 апреля 2021 года[199] | «Laboratorios Richmond» SACIF[200] | Серийный выпуск с 4 июня 2021 года[200] | |
| С 24 мая 2021 года[201] | «Hetero Biopharma»[202] «Virchow Biotech» (запланировано)[203] «Stelis Biopharma» (запланировано)[204] «Panacea Biotec», г. Бадди[205] «Morepen Laboratories»[206] |
Заключено соглашение о производстве более 300 млн доз вакцины в год[207]. | |
| С 4 июня 2021 года[208] | Институт вирусологии, вакцин и сывороток «Торлак» (Белград)[208] | ||
| С 4 июня 2021 года[209] | «Actoverco»[210] | ||
| С 16 июня 2021 года[211] | «Adienne Pharma & Biotech»[211] | ||
| С 1 июля 2021 года[212] | |||
| С 5 июля 2021 года[213] | «Laboratorios de Biol gicos y Reactivos de Mexico» («BIRMEX»)[213] | ||
| С 21 июля 2021 года[214] | «Vabiotech»[214] | ||
| С 30 июля 2021 года[215] | «Jurabek laboratories», г. Алмалык[215] | Серийный выпуск с 7 октября 2021 года[216]. |
Оценки
Зарубежные специалисты критиковали разработчиков «Гам-КОВИД-Вак» за отсутствие доказательств её эффективности и научных публикаций о проведённых испытаниях на момент презентации препарата[217][218][219][220]. Соответствующая публикация результатов I и II фазы клинических нерандомизированных исследований вакцины была опубликована в медицинском журнале The Lancet 4 сентября 2020 года, спустя менее месяца после презентации[42]. Согласно рецензии Lancet, главным результатом исследований было доказательство безопасности и иммуногенности вакцины[221], однако обнадёживающие итоги исследования ещё не говорят о том, что Гам-КОВИД-Вак готова ко всеобщему использованию[222].
Глава отделения лабораторной медицины Каролинского института Матти Сэльберг отмечает, что малое число участников клинического испытания, в котором были объединены первая и вторая фазы, не позволяет судить об отсутствии побочных эффектов при массовом применении вакцины[68][218], однако, сами разработчики вакцины считают её надёжной, поскольку она была разработана на существующей хорошо испытанной платформе[67]. Также существуют опасения, что побочные эффекты от ранее широко не применявшихся живых вакцин на базе генноинженерных вирусов могут оставаться неизученными[223][224].
21 декабря 2020 года генеральный директор фармацевтической компании AstraZeneca Паскаль Сорио в ходе видеоконференции по случаю подписания соглашения о сотрудничестве с Центром им. Гамалеи, РФПИ и российской фармкомпанией «Р-Фарм» заявил: «Я хотел бы поздравить российских учёных из института Гамалеи, а также РФПИ с разработкой первой в мире вакцины против COVID-19, которая в последнее время продемонстрировала не только иммунный ответ, но и эффективность, защиту против госпитализации. И [регуляторное] одобрение, безусловно, стало важным этапом для этой вакцины»[225][226][227].
После публикации данных промежуточного этапа III фазы испытаний в журнале «Lancet» в западных СМИ начались публикации положительных отзывов о вакцине «Спутник V». Так, агентство Bloomberg назвало вакцину самым серьёзным научным прорывом России со времён Советского Союза[228]. The Wall Street Journal указывает, что «„Спутник V“ представляет собой значительную победу президента России Владимира Путина в глобальной гонке вакцинаций, даёт вотум уверенности в возможностях российской науки и медицины и помогает отразить некоторую критику, с которой Москва столкнулась за быстрое развитие вакцинации и отсутствие опубликованных данных испытаний»[229]. Радио Канада отмечает, что вакцина Спутник V завоевала доверие, а также стала крупной научной и дипломатической победой России[230]. В медицинском журнале The Lancet появилась новая информация о сомнениях в эффективности препарата из-за недостаточности данных, переданных о третьей фазе клинических испытаний российской вакцины от коронавируса «Спутник V». Группа учёных детально проанализировала сведения о препарате и пришла к выводу, что «ограниченный доступ к данным подрывает доверие к исследованиям». Также, в представленных данных о препарате есть несоответствия, а полный протокол исследования так и не был опубликован и предоставлен институтом Гамалеи международному сообществу[231]. В ответе за авторством разработчиков вакцины, опубликованном в The Lancet 12 мая 2021 года, отмечается, что нет никаких научных оснований сомневаться в эффективности вакцины, полученные данные обработаны и проанализированы в соответствии с протоколом исследований, а полученные в ходе реального применения вакцины в Аргентине данные полностью подтверждают её высокую безопасность и эффективность[232].
Австралийский учёный, лауреат Нобелевской премии по физиологии и медицине Дохерти, Питер отметил, что «эффективность вакцины „Спутник V“ в более чем 90 % выглядит великолепно, и к тому же Россия имеет долгую историю разработки хороших вакцин»[233].
Главный иммунолог США Энтони Фаучи заявил: «Если Россия или Китай имеют надёжные вакцины, то они могут обеспечить ими и себя, и некоторые другие страны. Это путь ко всеобщей защите всего человечества»[234].
Инфекционист медицинского центра при Стэнфордском университете Дин Уинслоу считает, что «Спутник V» сыграет важную роль в борьбе с пандемией в мире. Руководитель отделения инфекционных заболеваний при медицинском факультете Гарвадского университета Дэниел Курицкис заявил: «Из того, что я прочитал о вакцине, я понимаю, что её можно хранить при температуре, которую поддерживает обычный холодильник. Это, разумеется, большое преимущество, поскольку позволяет доставить вакцину в те страны, где гораздо меньше возможностей обеспечить хранение при сверхнизкой температуре. Это означает, что в некоторых странах её значительно проще применять». Инфекционист из Университета штата Джорджия в Огасте Роджер Макартур, говоря о том, что вакцина не требует поддержания сверхнизкой температуры при транспортировке, отметил: «Это, конечно, преимущество, в особенности в том, что касается её доставки в места, где вряд ли есть возможность достичь очень низкой температуры, но, думаю, в вакцине важнее всего эффективность и безопасность»[235].
7 июля 2021 года вирусолог, начальник лаборатории особо опасных инфекций ФИЦ Фундаментальной трансляционной медицины, профессор Александр Чепурнов сообщил, что считает «Спутник Лайт» наиболее подходящей вакциной для ревакцинации тех, кто ранее переболел коронавирусом[236].
Международный интерес и поставки

Прибытие первой партии вакцины «Спутник V» в Аргентину 24 декабря 2020 года

Прибытие партии вакцины «Спутник V» в Иран 4 февраля 2021 года
2 декабря 2020 года состоялась презентация «Спутник V» в виртуальном формате для стран — членов ООН. Согласно данным ТАСС, в мероприятии зарегистрировались представители 55 государств, а также представители руководства ООН, ВОЗ, Красного Креста[237]. При этом чуть ранее, в конце ноября, Российский фонд прямых инвестиций (РФПИ) объявил, что стоимость одной дозы вакцины «Спутник V» для международных рынков составит менее 10 $, что делает её гораздо более доступной в сравнении с мРНК-вакцинами других производителей[238].
По заявлениям генерального директора РФПИ Кирилла Дмитриева, на первую неделю декабря фонд получил предварительные заявки на покупку 1,2 млрд доз вакцины из более чем 50 стран[239]. Также была подана заявка на одобрение вакцины в 40 странах[240]. 2 февраля The Wall Street Journal отметил, что уже имеется заказов и предварительных договорённостей на 2,4 млрд доз вакцины «Спутник V»[241].
29 января 2021 года РФПИ подал заявку в Европейское агентство лекарственных средств (EMA) для регистрации российской вакцины в Евросоюзе[242]. 10 февраля EMA сообщило, что они не получали заявку на непрерывный обзор или разрешение на продажу вакцины. Разработчики только выразили заинтересованность в том, чтобы вакцина рассматривалась для непрерывного обзора, но Комитет EMA по лекарственным средствам для человека (CHMP) и Целевая группа по пандемии COVID-19 EMA (COVID-ETF) должны сначала дать своё согласие, прежде чем разработчики смогут представить своё предложение для начала процесса проверки[243].
Согласно СМИ (французское издание Le Monde, Euronews и другие), применение вакцины «Спутник V» в Европе вызвало дискуссию о «глобальной вакцинной дипломатии» и способствовало расколу между лидерами стран, входящих в Евросоюз[244]. В публикациях говорится, что Европейская комиссия пока не вступила в официальные переговоры с Российским фондом прямых инвестиций о поставках российской вакцины, но часть стран Европы, несмотря на это, намерены заказать её, при этом настаивая на скорейшем одобрении «Спутник V» в Евросоюзе, так как в приоритете должна быть забота о здоровье граждан, а не политика[245].
Первой страной, одобрившей использование «Спутника V», не дожидаясь решения Еврокомиссии, стала Венгрия[246]. Лидеры Германии и Австрии также настаивали на одобрении вакцины и были готовы приобретать её, не дожидаясь официальных решений Еврокомиссии. Однако против применения российской вакцины выступил, например, французский министр иностранных дел Жан-Ив Ле Дриан. Член Еврокомиссии по вопросам внутреннего рынка, французский бизнесмен Тьерри Бретон выступил с заявлением о том, что закупка «Спутника V» не является нужной Евросоюзу[247]. Франция также заявила, что призывает не признавать российские и китайские вакцины, и осудила Грецию за то что та допускает российских туристов, привитых в том числе «Спутником V»[248].
30 марта 2021 года стало известно о том, что Австрия приняла решение произвести закупку партии вакцины «Спутник V», несмотря на то, что препарат к тому моменту не успел пройти сертификацию в Европейском агентстве лекарственных средств. О намерении закупить миллион доз российской вакцины заявил австрийский канцлер Себастьян Курц[249]. В ответ на принятое австрийским канцлером решение Еврокомиссия выступила с предупреждением к Австрии о том, что в таком случае вся ответственность за возможные риски ложится на правительство Австрии[250]. Уже 10 апреля австрийский канцлер заявил, что переговоры о закупках «Спутник V» «фактически подошли к концу». «Закупка для нас возможна», — сказал он журналистам на брифинге, его цитирует Kurier. По его словам, речь идёт об 1 млн доз вакцины[251].
27 мая 2021 года руководство Детского фонда ООН (ЮНИСЕФ) и компания Human Vaccine подписали долгосрочное соглашение о поставках российской вакцины «Спутника V» для того, чтобы обеспечить нуждающиеся страны в доступе к вакцине от Covid-19[252].
12 июня 2021 года министр иностранных дел Словакии Иван Корчок заявил об отказе республики закупать новые партии российской вакцины против коронавируса «Спутник V» после получения 1 марта первой партии препарата[253].
21 июля 2021 года Институт общественного здравоохранения Чили одобрил включение российской вакцины «Спутник V» в национальную программу вакцинации. На принятие положительного по интеграции российской вакцины повлияли материалы по вакцинации в Аргентине и Мексике, где «Спутник V» был использован ранее[254].
Директор службы внешней разведки России Сергей Нарышкин считает, что регистрация «Спутника V» в Европейском Союзе тянется «из-за сигналов, которые поступают из высоких кабинетов ЕС»[255].
На начало июля 2021 года, несмотря на отсутствие одобрения ВОЗ, «Спутник V» применялся в 69 странах мира[147]
В сентябре 2021 года стало известно, что специалисты финского Национального института здравоохранения и социального развития считают возможным разрешить въезд в Финляндию людям, привитым российской вакциной[256].
В сентябре 2021 года власти Гонконга признали сертификат о вакцинации «Спутник V»[257]. Теперь россияне смогут лететь в Гонконг напрямую, а не после трёхнедельного пребывания в третьем государстве. Но им предстоит сидеть на карантине 21 день в специализированной гостинице.
Международный союз биатлонистов (IBU) признал вакцину[258]. Полностью вакцинированные освобождаются от любых обязательств по тестированию.
В середине сентября 2021 года ВОЗ приостановила сертификацию российской вакцины от COVID-19 «Спутник V», так как во время инспекции на одной из фабрик, которая составляет часть производства вакцины, было обнаружено, что эта фабрика не соответствует новым правилам наилучшей практики производства[259].
14 декабря 2021 пресс-секретарь Владимира Путина Дмитрий Песков заявил, что российские власти не предоставили Всемирной организации здравоохранения (ВОЗ) всей информации, необходимой для сертификации вакцины из-за разночтений в стандартах, но работа по прохождению процедуры одобрения ВОЗ продолжается[260].
Список стран и территорий, официально зарегистрировавших «Спутник V»
|
5-дозовый флакон (3 мл) с I компонентом вакцины Гам-КОВИД-Вак производства «BIOCAD» в руках аргентинского медработника в больнице Posadas Hospital в Эль-Паломаре[es] провинции Буэнос-Айрес[381] |
Торжественное открытие вакцинации в Иране 12 февраля 2021 года в больнице им. имама Хомейни (перс. بیمارستان امام خمینی), вакцина Гам-КОВИД-Вак производства ЗАО «Лекко»[382][383] |
Флакон с I компонентом вакцины Гам-КОВИД-Вак в руках иранского медработника во время вакцинации в больнице им. шахида Садуги (перс. بیمارستان شهید صدوقی) в Йезде[384] |
Однодозовые ампулы (0,5 мл) с замороженным I компонентом Гам-КОВИД-Вак производства ОАО «Фармстандарт-УфаВИТА» в Аргентине, 2021 |
Страны, признающие российские сертификаты о вакцинации
В сентябре 2021 года в Эстонии заявили, что россияне будут освобождены от тестирования и изоляции в течение одного года после завершения вакцинации, если они полностью вакцинированы и достигли полной иммунной защиты[385]. Привитым россиянам можно посещать общественные места Эстонии без ограничений.
Спортсмены, привитые российской вакциной, пользуются теми же правами на Олимпиаде в Китае, что и другие. По словам посла России в КНР, фактически получается, что страна признала нашу вакцину[386].
События, связанные с вакциной
США: внесение 48-го ЦНИИ МО РФ в санкционный список
26 августа 2020 года 48-й Центральный научно-исследовательский институт Министерства обороны РФ, на базе которого проводились доклинические испытания на токсичность, безопасность, иммуногенность и защитную эффективность вакцины «Спутник V», был внесён в список организаций, деятельность которых противоречит интересам национальной безопасности или внешней политики США. Власти США заявили, что у них есть основания считать 48-й ЦНИИ и его филиалы связанными с программой создания биологического оружия[387].
Критика клинических испытаний
7 сентября 2020 года профессор биологии американского университета Темпл, Энрико Буччи, на сайте Cattivi Scienziati, специализирующемся на борьбе с псевдонаукой, опубликовал открытое письмо[388][389], в котором поставил под сомнение достоверность данных клинических исследований фазы I/II, опубликованных в «The Lancet». Данное письмо было подписано тремя десятками учёных из США, Италии и других стран и было опубликовано во многих ведущих западных СМИ[390][391][392][393]. В тот же день представитель РФПИ от имени Дениса Логунова передал следующее заявление: «НИЦЭМ им. Гамалеи категорически отвергает обвинения в недостоверности статистических данных, опубликованных в журнале The Lancet. Опубликованные данные являются достоверными и точными и прошли экспертизу у пяти рецензентов The Lancet, полноразмерный клинический протокол предоставлялся в редакцию журнала. Мы представили именно те данные, которые получили, а не те, которые должны нравиться итальянским экспертам»[389].
Позже, 18 сентября, в «The Lancet» был опубликован более подробный ответ разработчиков вакцины на критику. В ответе были даны ответы на вопросы учёных, в том числе было указано, что выявленные совпадения, особенно в близких к исходным и начальным значениям, были связаны с дискретностью данных (получаемые значения были не точными, а в виде диапазонов, что значительно увеличивает вероятность совпадений), а также с малым количеством участников в группах[394][395].
22 мая 2021 года профессор Энрико Буччи с коллегами опубликовал в «The Lancet» статью «Расхождения в данных и нестандартная отчётность по промежуточным данным исследования фазы III Спутник V», где раскритиковали авторов III фазы испытаний Спутник V за то, что они не предоставили критикам доступа к полным данным, а также за несоответствия и подозрительные совпадения в данных[396]. Ответ авторов был опубликован в Lancet — они заявили, что ещё 5 ноября 2020 года регулирующим органам и рецензентам Lancet были предоставлены все необходимые данные, и что данных, включённых в статью, достаточно для того, чтобы читатели могли проверить сообщённую эффективность вакцины. Они также заявили, что числовые несоответствия были простыми ошибками или опечатками, которые были легко исправлены[397]. Заслуженный врач РФ, сенатор Владимир Круглый указывал, что попытки дискредитации российской вакцины от коронавируса «Спутник V» — это элемент информационной войны и недобросовестной конкуренции[398][значимость факта?].
Словакия: правительственный кризис
1 марта 2021 года в Словакию была доставлена первая партия вакцины «Спутник V», состоящая из 200 тысяч доз. Всего, согласно договору, было запланировано поставить 2 млн доз[399]. Вакцина была одобрена министром здравоохранения Словакии Мареком Крайчи[400]. Таким образом, Словакия стала второй страной Евросоюза, которая одобрила применение российской вакцины «Спутник V», не дожидаясь решения европейского регулятора EMA.
На следующий день, 2 марта, президент Словакии Зузана Чапутова выразила недовольство решением премьер-министра страны Игора Матовича приобрести для использования в республике российскую вакцину. Она указала, что не будет пропагандировать использование препаратов, не прошедших процесс регистрации в Евросоюзе[401].
Покупка российской вакцины привела к разногласиям в правительстве. Многие члены правительства осудили премьер-министра, который проигнорировал февральское решение правительства, согласно которому в республике должны использоваться только препараты, зарегистрированные в Евросоюзе[402].
12 марта министр здравоохранения Словакии Марек Крайчи ради сохранения правительственной коалиции страны подал в отставку[403]. Позже, 15 марта, в связи с правительственным кризисом, подал в отставку министр труда Милан Крайняк[404]. 17 марта о своей отставке объявил министр экономики Рихард Сулик[405]. 24 марта о своей отставке объявили министр иностранных дел Иван Корчок, министр образования Бронислав Грюлинг и министр юстиции Мария Коликова[406].
30 марта президент Словакии З. Чапутова приняла отставку премьер-министра И. Матовича и поручила сформировать новое правительство[407].
Словакия: дезинформация
6 апреля словацкое издание «Dennik» сообщило, что словацкий Государственный институт по контролю лекарств (ŠÚKL), не выдал разрешение на использование вакцины «Спутник V». В сообщении отмечалось, что для одобрения вакцины не хватает дополнительных данных о доклинических и клинических испытаниях. «Значительная часть данных, примерно 80 %, не была предоставлена даже после повторных запросов». Указывалось также, что поставленная в республику вакцина отличается от образцов, результаты испытаний которых были опубликованы в научном журнале «The Lancet»[408][409].
7 апреля на официальном аккаунте Спутника в твиттер появилось сообщение, что вышеуказанная публикация является вбросом[410]. Было отмечено, что «в нарушение существующего контракта и в акте саботажа Государственный институт по контролю за лекарствами обеспечил тестирование „Спутник V“ в лаборатории, не входящей в сеть официальных сертифицированных лабораторий ЕС по контролю за лекарствами, хотя такие лаборатории были доступны», а также что «все партии „Спутник V“ одинакового качества и проходят строгий контроль качества в Институте Гамалеи». Указывалось, что против российской вакцины ведётся кампания по дезинформации. РФПИ обратился к правительству Словакии с просьбой отправить вакцину в сертифицированную лабораторию ЕС для тестирования. 6 апреля 2021 года РФПИ потребовал вернуть вакцину из-за многочисленных нарушений контракта, чтобы её можно было использовать в других странах[411].
В ответ на это 15 апреля президент Словакии Зузана Чапутова потребовала опубликовать договор о покупке республикой российской вакцины «Спутник V»[412]. Российская сторона отметила, что не против публикации договора о поставке «Спутника V» в Словакию, но в таком случае должен быть опубликован и контракт с Pfizer[413]. 29 апреля Словакия опубликовала договор[414][415].
7 мая специализированная лаборатория в Венгрии подтвердила надёжность российской вакцины «Спутник V», поступившей в Словакию 1 марта[416]. 7 июня в Словакии началось использование российской вакцины[417].
США: давление на Бразилию и другие страны
В начале 2021 года Министерство здравоохранения и социальных служб США опубликовало отчёт о проделанной работе. Как выяснилось из текста доклада, Министерство здравоохранения США вместе с другими правительственными организациями участвовало в кампании давления на бразильские власти с целью убедить отказаться от закупки вакцины «Спутник V» в России под предлогом, что Россия использует поставки вакцины якобы для «усиления своего влияния в регионе в ущерб безопасности США»[418][419].
Бразилия: диффамация вакцины
26 апреля 2021 года Национальное агентство по санитарному надзору Бразилии Anvisa (порт. Agência Nacional de Vigilância Sanitária) не разрешила импорт и использование в стране российской вакцины «Спутник V». Согласно заявлению представителей Anvisa, причиной отказа были отсутствие последовательных и надёжных данных, а также наличие в вакцине аденовируса, способного к репликации[420][421]. Таким образом, 14 штатов Бразилии, ожидавшие разрешения и запланировавшие срочный импорт вакцины для противостояния растущей волне инфекции COVID-19, получили отказ.
28 апреля команда «Спутника V» рассмотрела претензии, заявленные членами правления Anvisa, и продемонстрировала, что эти обвинения не имеют научных оснований и не могут серьёзно рассматриваться в научном сообществе и среди международных регулирующих органов. Представители центра имени Гамалеи заявили, что «ни в одной из производимых серий вакцины „Спутник V“ не было обнаружено воспроизводимых аденовирусов», а существующий контроль гарантирует, что в вакцине нет таких вирусов. В центре отметили, что качество и безопасность вакцины обеспечивается 4-ступенчатой технологией очистки. «В производстве вакцины „Спутник V“ используются только нереплицирующиеся аденовирусные векторы E1 и E3, которые безвредны для человеческого организма», подчеркнули специалисты. Команда Anvisa в Москве имела полный доступ ко всей необходимой документации, а также к исследовательским и производственным площадкам. Также учёные напомнили, что в ходе применения «Спутник V», «в отличие от других вакцин, случаев тромбоза венозного синуса головного мозга не было зарегистрировано»[422][423].
4 июня поздно вечером Anvisa одобрила импорт и ограниченное применение российской вакцины «Спутник V»[424][425].
Подделка вакцины
Фальшивые сайты, продающие фальсифицированные препараты против COVID, и склады с поддельной вакциной были обнаружены в 2020—2021 годах в нескольких странах: Нигерии, Мексике, Китае и других. В марте 2021 года Организация экономического сотрудничества и развития опубликовала отчёт[426], в котором сообщалось, что в 2016 году мировая торговля поддельными лекарствами, по разным оценкам, составляет от 4,4 до 20 миллиардов долларов, что объясняется низкой ответственностью за продажу поддельных препаратов. Фальсифицированную вакцину предполагалось реализовывать под маркой известных препаратов американского, английского, китайского и российского производства[427][428][429][430]. В марте 2021 года в аэропорту мексиканского города Кампече при обыске частного самолёта власти обнаружили и изъяли подготовленную к перевозке в Гондурас партию поддельной вакцины «Спутник V» (1155 флаконов, 5775 доз) в упаковке, имитирующей настоящую[431][432][433].
Примеры афер и способов заработка путём мошенничества с фальсифицированными вакцинами, зафиксированные за рубежом, опубликованы в СМИ[434][435][436][437]. Генеральный секретарь Интерпола Юрген Шток считает, что фальсифицированная вакцина, найденная в Мехико и Южной Африке, лишь «верхушка айсберга» и, вероятно, в обращении находится много партий поддельных вакцин, которые пока не обнаружены[438], так как производство лекарств часто представляет собой глобальную сеть, когда разные этапы производственной цепочки выполняются в разных странах, и затем могут перепаковываться, чтобы снизить таможенные расходы, при этом есть много мест для введения подделок в схемы поставок. В 2021 году вакцины стали «жидким золотом», которое «приносит миллиарды», и рынок поддельных лекарств образует параллельную легальному рынку криминальную сеть с низкими рисками и большими доходами[439].
См. также
- Вакцина против COVID-19
- ГамЭвак-Комби — вакцина против лихорадки Эбола, разработанная НИЦЭМ им. Н. Ф. Гамалеи
- КовиВак — инактивированная вакцина против COVID-19, разработанная ФГБНУ «ФНЦИРИП им. М. П. Чумакова РАН»
- Бетувакс-КоВ-2 — субъединичная вакцина против COVID-19, разработанная в ИСКЧ
- Конвасэл — субъединичная вакцина против COVID-19, разработанная в ФМБА
- ЭпиВакКорона — однокомпонентная пептидная вакцина против COVID-19, разработанная в ГНЦ ВБ «Вектор»
- Ad26.COV2.S — аденовирусная вакцина разработки Johnson & Johnson
- Ad5-nCoV — аденовирусная вакцина, разработанная китайской фармацевтической компанией CanSino Biologics
- AZD1222 — векторная вакцина против COVID-19, разработанная Оксфордским университетом и компанией AstraZeneca
- BNT162b2 — вакцина на базе мРНК против COVID-19, разработанная немецкой биотехнологической компанией BioNTech при сотрудничестве с американской Pfizer
- MRNA-1273 — вакцина против COVID-19, разработанная американской компанией Moderna
Примечания
- ↑ 1 2 3 4 5 6 7 8 Инструкция по медицинскому применению лекарственного препарата Гам-КОВИД-Вак, Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 от 11.08.2020. Архивная копия от 23 января 2021 на Wayback Machine + Изменения № 1 от 01.09.2020. Архивная копия от 22 апреля 2022 на Wayback Machine, *24.09.2020. Архивная копия от 22 апреля 2022 на Wayback Machine, № 3 от 23.10.2020 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, № 5 от 14.12.2020 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, № 6 от 25.12.2020, № 4 и 8 от 30.12.2020 (25.12.2020). Архивная копия от 22 апреля 2022 на Wayback Machine, переоформ. от 30.12.2020. Архивная копия от 22 апреля 2022 на Wayback Machine, № 7 и 9 от 13.01.2021. Архивная копия от 22 апреля 2022 на Wayback Machine. Инструкция от 20.01.2021. Архивная копия от 22 апреля 2022 на Wayback Machine + Изменения № 1 от 18.02.2021 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, *18.03.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 2 от 19.03.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, *21.04.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, *30.04.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 4 от 21.04.2021 (06.05.2021). Архивная копия от 22 апреля 2022 на Wayback Machine, № 5 от 04.06.2021 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, № 8 от 07.06.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, *24.06.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 10 от 25.06.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 11 от 01.07.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 3 и 9 от 14.07.2021 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, *14.07.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 13 от 26.07.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 7 от 17.08.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, *19.08.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, *02.09.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, переоформ. от 08.09.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 14 от 15.09.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, *21.09.2021. Архивная копия от 22 апреля 2022 на Wayback Machine. Инструкция от 15.10.2021 (26.11.2021) + Изменения № 1 от 21.10.2021 (26.11.2021), № 4 от 26.11.2021 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, № 7 от 30.12.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 6 от 11.01.2022 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, № 2 от 25.01.2022. Архивная копия от 22 апреля 2022 на Wayback Machine, № 8 от 31.01.2022. Архивная копия от 22 апреля 2022 на Wayback Machine, № 3 от 15.02.2022 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, № 9 от 24.02.2022. Архивная копия от 22 апреля 2022 на Wayback Machine, *22.03.2022. Архивная копия от 22 апреля 2022 на Wayback Machine // Регистрационные данные и электронные образы документов на сайте «Государственный реестр лекарственных средств».
- ↑ 1 2 3 4 Инструкция по медицинскому применению лекарственного препарата Гам-КОВИД-Вак-М, Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 от 24.11.2021. Архивная копия от 4 апреля 2022 на Wayback Machine + Изменения № 1 от 26.11.2021. Архивная копия от 31 марта 2022 на Wayback Machine, № 2 от 04.04.2022. Архивная копия от 22 апреля 2022 на Wayback Machine // Регистрационные данные и электронный образ документов на сайте «Государственный реестр лекарственных средств».
- ↑ 1 2 3 4 Инструкция по медицинскому применению лекарственного препарата Спутник Лайт, Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 от 06.05.2021. Архивная копия от 22 апреля 2022 на Wayback Machine + Изменения № 2 от 25.06.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 3 от 30.06.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 1 от 09.07.2021 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, № 6 от 05.08.2021 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, *11.08.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 7 от 19.08.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, *31.08.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, № 9 от 26.10.2021. Архивная копия от 16 декабря 2021 на Wayback Machine, № 8 от 06.12.2021 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, *07.12.2021. Архивная копия от 22 апреля 2022 на Wayback Machine, *17.01.2022. Архивная копия от 22 апреля 2022 на Wayback Machine, № 4 от 28.01.2022 с переоформ. Архивная копия от 22 апреля 2022 на Wayback Machine, № 12 от 31.01.2022. Архивная копия от 22 апреля 2022 на Wayback Machine, *05.03.2022. Архивная копия от 22 апреля 2022 на Wayback Machine, № 13 от 22.03.2021. Архивная копия от 22 апреля 2022 на Wayback Machine // Регистрационные данные и электронный образ документов на сайте «Государственный реестр лекарственных средств».
- ↑ 1 2 3 4 5 Инструкция по медицинскому применению лекарственного препарата Гам-КОВИД-Вак-Лио, Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 от 25.08.2020. Архивная копия от 5 апреля 2021 на Wayback Machine + Переоформления от 06.12.2021, от 11.03.2022. Архивная копия от 22 апреля 2022 на Wayback Machine // Регистрационные данные и электронный образ документа на сайте «Государственный реестр лекарственных средств».
- ↑ 1 2 3 4 Инструкция по медицинскому применению лекарственного препарата Гам-КОВИД-Вак (капли назальные), Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 от 31.03.2022. Архивная копия от 22 апреля 2022 на Wayback Machine // Регистрационные данные и электронный образ документов на сайте «Государственный реестр лекарственных средств».
- ↑ 1 2 Минздрав России зарегистрировал первую в мире вакцину от COVID-19. Министерство здравоохранения Российской Федерации (11 августа 2020). Дата обращения: 11 августа 2020. Архивировано 12 августа 2020 года.
- ↑ 1 2 3 4 5 Совещание с членами Правительства. Стенограмма. Kremlin.ru (11 августа 2020). Дата обращения: 18 августа 2020. Архивировано 18 августа 2020 года.
- ↑ Первую в мире зарегистрированную вакцину от коронавируса назвали «Спутник V». ТАСС (11 августа 2020). Дата обращения: 11 августа 2020. Архивировано 11 сентября 2020 года.
- ↑ Глава РФПИ объяснил значение буквы »V» в названии вакцины »Спутник V». ТАСС (24 декабря 2020). Дата обращения: 1 февраля 2021. Архивировано 28 января 2021 года.
- ↑ Logunov D. Y. et al. Safety and immunogenicity of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine in two formulations: two open, non-randomised phase 1/2 studies from Russia (англ.) // The Lancet. — 2020. — Vol. 396, iss. 10255. — P. 887—897. — doi:10.1016/S0140-6736(20)31866-3. — PMID 32896291.
- ↑ 1 2 Анна Урманцева, Мария Недюк. Удачный запуск: «Спутник V» признан самой безопасной вакциной. Известия (3 февраля 2021). Дата обращения: 30 марта 2021. Архивировано 31 марта 2021 года.
- ↑ 1 2 В Москве началось исследование вакцины «Спутник V» для подростков. Архивная копия от 5 июля 2021 на Wayback Machine. Российская газета, 05.07.2021
- ↑ 1 2 3 4 5 Logunov D. Y. et al. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia (англ.) // The Lancet. — 2021. — Vol. 397, iss. 10275. — P. 671—681. — doi:10.1016/s0140-6736(21)00234-8. — PMID 33545094.
- ↑ Lancet опубликовал результаты третьей фазы исследований »Спутника V». РИА «Новости» (2 февраля 2021). Дата обращения: 20 февраля 2021. Архивировано 2 февраля 2021 года.
- ↑ 1 2 Гинцбург: »Спутник V» показал эффективность для пожилых людей. Российская газета (13 марта 2021). Дата обращения: 12 апреля 2021. Архивировано 12 апреля 2021 года.
- ↑ 1 2 Эффективность вакцины «Спутник V» составила 97,6% по результатам анализа данных 3,8 млн вакцинированных россиян, что делает ее наиболее эффективной вакциной от коронавируса в мире. sputnikvaccine.com (19 апреля 2021). Дата обращения: 5 июня 2021. Архивировано 5 июня 2021 года.
- ↑ 1 2 «Вектор» подтвердил эффективность российских вакцин против британского штамма COVID-19. Коммерсантъ (16 февраля 2021). Дата обращения: 16 февраля 2021. Архивировано 16 февраля 2021 года.
- ↑ 1 2 Гинцбург заявил об эффективности «Спутника V» против индийского штамма. Интерфакс (16 июня 2021). Дата обращения: 16 июня 2021. Архивировано 16 июня 2021 года.
- ↑ 1 2 Gushchin, V.A. et al. Neutralizing Activity of Sera from Sputnik V-Vaccinated People against Variants of Concern (VOC: B.1.1.7, B.1.351, P.1, B.1.617.2, B.1.617.3) and Moscow Endemic SARS-CoV-2 Variants (англ.) // Vaccines : журнал. — 2021. — 12 July (no. 9). — doi:10.3390/vaccines9070779. Архивировано 13 июля 2021 года.
- ↑ 1 2 Ikegame, S., Siddiquey, M.N.A., Hung, CT. et al. Neutralizing activity of Sputnik V vaccine sera against SARS-CoV-2 variants (англ.) // Nature Communications. — 2021. — 26 July (no. 4598). — doi:10.1038/s41467-021-24909-9. Архивировано 27 июля 2021 года.
- ↑ 1 2 «Спутник V» по-разному действует на альфа- и бета-варианты коронавируса. Архивная копия от 27 июля 2021 на Wayback Machine. ТАСС, 26.07.2021
- ↑ Российский фонд прямых инвестиций (РФПИ). Sputnikvaccine.com (2 декабря 2020). Дата обращения: 12 мая 2021. Архивировано 23 ноября 2021 года.
- ↑ Бразилия стала 67-й страной, где одобрено применение вакцины «Спутник V». Sputnikvaccine.com (5 июня 2021). Дата обращения: 5 июня 2021. Архивировано 6 июня 2021 года.
- ↑ В Москве стартует вакцинация первоочередников от коронавируса. РИА «Новости» (5 декабря 2020). Дата обращения: 7 февраля 2021. Архивировано 21 января 2021 года.
- ↑ Coronavirus Vaccine Trials Advance in Race for Covid-19 Protection (англ.). Bloomberg. Дата обращения: 10 августа 2020. Архивировано 3 декабря 2020 года.
- ↑ Создатели «Спутника V» ответили на запрос РПЦ о компонентах вакцины. Архивная копия от 11 ноября 2021 на Wayback Machine. Российская газета, 11.02.2021.
- ↑ Кузьмин, Владимир Мишустин: »Спутник V» - одна из самых лучших востребованных вакцин в мире. Российская газета. ФГБУ «Редакция «Российской газеты» (22 мая 2021). — «Появление вакцины от коронавируса «Спутник V» — это заслуга российского доктора наук, заведующего лабораторией клеточной микробиологии Национального исследовательского центра имени Гамалеи Дениса Логунова». Дата обращения: 22 июня 2021. Архивировано 24 июня 2021 года.
- ↑ А. Спиридонова. Мы называем коронавирус «липуч и летуч». Архивная копия от 11 марта 2021 на Wayback Machine // 02.06.2020. «ТВР24»
- ↑ Перечень организаций, на базе которых функционируют специализированные коллекции ПБА I—IV групп. Архивная копия от 11 марта 2021 на Wayback Machine // Приложение 5.6 к СП 1.2.036-95.
- ↑ Russia’s RDIF & Prominent Government Lab Progress COVID-19 Vaccine: Production Facility Readied in the Moscow Region (англ.). trialsitenews.com (10 июня 2020). Дата обращения: 11 августа 2020. Архивировано 8 августа 2020 года.
- ↑ «Вакцина против коронавируса разработана с участием российских военных — 48 Центрального научно-исследовательского института Минобороны РФ». Архивная копия от 11 марта 2021 на Wayback Machine. Интерфакс, 02.06.2020
- ↑ Инструкция по медицинскому применению лекарственного препарата Гам-КОВИД-Вак. Минздрав РФ (11 августа 2020). Дата обращения: 11 августа 2020. Архивировано из оригинала 3 марта 2021 года.
- ↑ Ian Jones, Polly Roy. Sputnik V COVID-19 vaccine candidate appears safe and effective (англ.) // The Lancet. — 2021. — 20 February (vol. 397, iss. 10275). — P. 642–643. — ISSN 1474-547X 0140-6736, 1474-547X. — doi:10.1016/S0140-6736(21)00191-4. — PMID 33545098.
- ↑ 1 2 Chris Baraniuk. Covid-19: What do we know about Sputnik V and other Russian vaccines? (англ.) // BMJ. — 2021. — 19 March (vol. 372). — P. n743. — ISSN 1756-1833. — doi:10.1136/bmj.n743. — PMID 33741559. Архивировано 26 августа 2021 года.
- ↑ Corum, Jonathan. How Gamaleya’s Vaccine Works, The New York Times (7 января 2021). Архивировано 20 апреля 2021 года. Дата обращения: 28 июля 2021.
- ↑ Шмаров М. М., Никонова А. Э., Седова Е. С., Логунов Д. Ю. Рекомбинатные аденовирусы человека как платформа для создания новых эффективных и безопасных вакцин. Архивная копия от 24 июня 2021 на Wayback Machine / Научная статья. DOI: 10.24110/0031-403X-2020-99-6-52-56. НИЦЭМ им. Гамалеи МЗ РФ, ПМГМУ им. Сеченова // Журнал «Педиатрия», 2020. — Том 99, № 6. ISSN 1990—2182. С. 52—56.
- ↑ 1 2 3
Неудобные вопросы о всеобщей вакцинации. Youtube-канал «Редакция», 15.07.2021
- ↑ Е. Краснова. Раскрыт принцип действия вакцины «Спутник V». Газета.ру, 17.12.2020
- ↑ Россиянам описали последствия пропуска второй дозы вакцины. Архивная копия от 21 декабря 2020 на Wayback Machine // 21.12.2020. «Лента.ру».
- ↑ Харченко Е. П. Вакцины против Covid-19: сравнительная оценка рисков аденовирусных векторов. Архивная копия от 13 июля 2021 на Wayback Machine / Научная статья, doi: 10.31631/2073-3046-2020-19-5-4-17, ФГБУН «Институт эволюционной физиологии и биохимии им. И. М. Сеченова» РАН // М.: научный журнал «Эпидемиология и Вакцинопрофилактика», 2020. — Том 19, № 5. ISSN 2073-3046. С. 4-17.
- ↑ И. Ясный. Зачем нужна такая двойная схема, почему недостаточно одной инъекции? Архивная копия от 2 марта 2021 на Wayback Machine. Проект, 07.09.2020
- ↑ 1 2 3 4 Logunov, Denis Y. Safety and immunogenicity of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine in two formulations : two open, non-randomised phase 1/2 studies from Russia : [англ.] : [арх. 4 сентября 2020] / Denis Y. Logunov, Inna V. Dolzhikova, Olga V. Zubkova … [] // Lancet. — 2020. — 4 September. — doi:10.1016/S0140-6736(20)31866-3.
- ↑ Из интервью. Архивная копия от 24 июня 2021 на Wayback Machine с к.б.н., директором Института экономики здравоохранения НИУ ВШЭ Ларисой Попович. iq.hse.ru, 13.11.2020
- ↑ ИФА-тест в поликлиниках Москвы не показывает уровень антител после вакцинации от COVID-19. Архивная копия от 28 января 2021 на Wayback Machine. ТАСС, 22.01.2021
- ↑ До и после прививки. Архивная копия от 16 февраля 2021 на Wayback Machine. Российская газета, 30.01.2021
- ↑ Около 7,6 тыс. военнослужащих и гражданских специалистов Северного флота вакцинированы от коронавирусной инфекции. Архивная копия от 21 января 2021 на Wayback Machine // 15.01.2021. Минобороны РФ. Пресс-служба Северного флота.
- ↑ Е. Манукиян. Иммунитет к COVID-19 после вакцинации «Спутник V» вырабатывается на 42 день. Архивная копия от 20 февраля 2021 на Wayback Machine. Российская газета, 14.12.2020
- ↑ Утверждены условия транспортирования и хранения вакцины «Спутник V». Архивная копия от 1 марта 2021 на Wayback Machine // 08.12.2020. Журнал «Новости GMP».
- ↑ Дело в аденовирусе. Российские вирусологи объяснили, почему «Спутник V» жить не может без крепкого морозца. Архивная копия от 13 февраля 2021 на Wayback Machine // 09.12.2020. Сетевое издание «ДокторПитер».
- ↑ Решение для хранения вакцин от коронавируса позаимствуют у пищепрома. Архивная копия от 14 февраля 2021 на Wayback Machine // 28.12.2020. «Regnum».
- ↑ В. Полякова. Власти Петербурга «в срочном порядке» закупят холодильники для вакцины. Архивная копия от 26 января 2021 на Wayback Machine. РБК, 16.12.2020
- ↑ 90 тысяч доз вакцины от COVID-19 поступит в Приморье. Разъяснение. Архивная копия от 25 февраля 2021 на Wayback Machine // 15.01.2021. Официальный сайт Правительства Приморского края.
- ↑ Три переносных холодильника передали в больницы Красногорска. Архивная копия от 15 апреля 2021 на Wayback Machine // 28.01.2021. Официальный сайт Администрации городского округа Красногорск Московской области.
- ↑ Вакцинация вакциной «ЭпиВакКорона» от центра «Вектор» началась в Новосибирской области. Архивная копия от 4 февраля 2021 на Wayback Machine // 16.12.2020. Официальный сайт Правительства Новосибирской области.
- ↑ Минздрав изменил требования к хранению вакцины «Спутник V». Архивная копия от 8 февраля 2021 на Wayback Machine. РИА Новости, 21.01.2021
- ↑ Центр Гамалеи назвал сроки вакцинации большей части населения России. РБК (4 сентября 2020). Дата обращения: 6 сентября 2020. Архивировано 6 сентября 2020 года.
- ↑ Минздрав пообещал россиянам бесплатную вакцинацию от COVID-19. РБК. Дата обращения: 23 октября 2020. Архивировано 27 октября 2020 года.
- ↑ Минздрав зарегистрировал предельную отпускную цену на вакцину «Спутник V» — РИА Новости, 05.12.2020. Дата обращения: 6 декабря 2020. Архивировано 6 декабря 2020 года.
- ↑ Отпускная цена на «Спутник V» снижена в два раза. Вести.ру. Дата обращения: 26 февраля 2021. Архивировано 26 февраля 2021 года.
- ↑ Правительство включит все вакцины от коронавируса в список жизненно важных лекарств. Архивная копия от 20 апреля 2021 на Wayback Machine. Коммерсантъ, 23.11.2020
- ↑ Вакцины от COVID-19 включены в перечень жизненно важных препаратов. Архивная копия от 24 января 2021 на Wayback Machine // 24.11.2020. «Интерфакс».
- ↑ Распоряжение Правительства РФ от 23.11.2020 № 3073-р «О внесении изменений в распоряжение Правительства РФ от 12.10.2019 г. № 2406-р» / Пункт 2, Приложение 1: пункт 1, подпункт 21 («вакцины в соответствии с национальным календарем профилактических прививок и календарем профилактических прививок по эпидемическим показаниям вакцины для профилактики новой коронавирусной инфекции COVID-19»). Подпункт вступил в силу с 03.12.2020
- ↑ Н. Анисимова. Минздрав внес вакцинацию от COVID в календарь профилактических прививок. Архивная копия от 18 марта 2021 на Wayback Machine. РБК, 16.12.2020
- ↑ Приказ Министерства здравоохранения Российской Федерации от 09.12.2020 № 1307н «О внесении изменений в календарь профилактических прививок по эпидемическим показаниям, утвержденный приказом Министерства здравоохранения Российской Федерации от 21 марта 2014 г. № 125н» / Действующий календарь профилактических прививок по эпидемическим показаниям дополнен вакцинацией «против коронавирусной инфекции вызываемой вирусом SARS-CoV-2». Приказ вступил в юридическую силу с 27.12.2020
- ↑ В будущем вакцинация от COVID-19 будет проходить бесплатно. Российская газета. — «Вакцинацию от COVID-19 будут проводить бесплатно. А в будущем эта прививка войдёт и в Национальный календарь вместе с другими». Дата обращения: 23 октября 2020. Архивировано 26 октября 2020 года.
- ↑ Russia plans to start producing coronavirus vaccine in September (англ.). Daily Sabah (13 июня 2020). Дата обращения: 10 августа 2020. Архивировано 16 июня 2020 года.
- ↑ 1 2 3 Первое большое интервью создатель российской вакцины от коронавируса Денис Логунов дал «Медузе». Meduza (23 июля 2020). Дата обращения: 18 августа 2020. Архивировано 8 августа 2020 года.
- ↑ 1 2 Вакцина от COVID-19 — в словах чиновников и документах разработчика. Фонтанка.ру (11 августа 2020). Дата обращения: 30 января 2022. Архивировано 30 января 2022 года.
- ↑ Глава Центра Гамалеи назвал стоимость разработки вакцины «Спутник V». РБК (21 декабря 2020). Дата обращения: 23 декабря 2020. Архивировано 24 декабря 2020 года.
- ↑ Шойгу рассказал о сроках готовности вакцины от COVID-19, разработанной военными. Архивная копия от 18 октября 2020 на Wayback Machine // 26.05.2020. Газета «Dp.ru».
- ↑ Победа над COVID-19 достигается сообща // 22.06.2020. Газета «Красная звезда». Р. Бирюлин.
- ↑ Тельнова Е. А., Щепин В. О., Загоруйченко А. А. Вакцинация как вызов COVID-19. Архивная копия от 20 июня 2021 на Wayback Machine / Научная статья. DOI: 10.25742/NRIPH.2020.03.010, Национальный научно-исследовательский институт общественного здоровья имени Н. А. Семашко // М.: Бюллетень НИИ общественного здоровья им. Семашко, № 3, 2020 г. ISSN 2415-8410. С. 82-89.
- ↑ Минобороны РФ сообщает о начале клинических испытаний вакцины от коронавируса. Архивная копия от 17 октября 2020 на Wayback Machine // 17.06.2020. «Интерфакс».
- ↑ Военные медики против коронавируса // 02.06.2020. «Союзники. ОДКБ». В. Попов.
- ↑ Коллектив авторов Комбинированная векторная вакцина для профилактики ближневосточного респираторного синдрома индуцирует формирование длительного протективного иммунного ответа к коронавирусу БВРС-КоВ / Научная статья, doi: 10.33029/0206-4952-2020-41-2-135-143. НИЦЭМ им. Н. Ф. Гамалеи, ПМГМУ им. И. М. Сеченова, ФНЦИРИП им. М. П. Чумакова РАН, 48 ЦНИИ Минобороны // М.: журнал «Иммунология», 2020. Том 41, № 2. ISSN 0206-4952. С. 135—143.
- ↑ Коллектив создателей вакцины Спутник V. Архивная копия от 8 февраля 2021 на Wayback Machine // Статья на официальном сайте посвящённой вакцине sputnikvaccine.com.
- ↑ Путин объявил о регистрации в России первой вакцины от коронавируса. РИА Новости (11 августа 2020). Дата обращения: 16 августа 2020. Архивировано 17 августа 2020 года.
- ↑ Коронавирус в России: зарегистрировали вакцину от Covid-19, дочь Путина сделала прививку. Русская служба Би-би-си (11 августа 2020). Дата обращения: 16 августа 2020. Архивировано 13 августа 2020 года.
- ↑ О вакцине для профилактики новой коронавирусной инфекции COVID-19 «Гам-КОВИД-Вак». roszdravnadzor.gov.ru (12 августа 2020). — «в соответствии с постановлением Правительства Российской Федерации от 03.04.2020 № 441. … регистрация лекарственных препаратов «на условиях».». Дата обращения: 18 августа 2020. Архивировано 13 августа 2020 года.
- ↑ Минздрав России зарегистрировал первую в мире вакцину от COVID-19. Министерство здравоохранения РФ (11 августа 2020). Дата обращения: 11 августа 2020. Архивировано 11 августа 2020 года.
- ↑ Путин сообщил о регистрации первой в мире вакцины против коронавируса. РИА Новости (11 августа 2020). Дата обращения: 11 августа 2020. Архивировано 23 августа 2020 года.
- ↑ Голикова назвала сроки выпуска первых партий вакцин НИЦ Гамалеи и «Вектора». Интерфакс (29 июля 2020). Дата обращения: 11 августа 2020. Архивировано 28 марта 2021 года.
- ↑ Антикоронавирусный «Спутник» создали при помощи принципиально новой технологии. Дата обращения: 19 августа 2020. Архивировано 22 августа 2020 года.
- ↑ 1 2 Запущено производство российской антикоронавирусной вакцины. Архивная копия от 11 апреля 2021 на Wayback Machine. «Вести», 15.08.2020
- ↑ 1 2 3 4 5 6 7 Logunov D. Y. et al. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia (англ.) // The Lancet. — 2021. — 2 February. — ISSN 0140-6736. — doi:10.1016/S0140-6736(21)00234-8.
[исправить]
- ↑ AstraZeneca begins programme to assess COVID-19 vaccines combinations / «АстраЗенека» запускает программу клинических исследований комбинации вакцин для профилактики COVID-19. Архивная копия от 31 декабря 2020 на Wayback Machine на сайте https://www.astrazeneca.ru Архивная копия от 30 декабря 2020 на Wayback Machine
- ↑ РФПИ, НИЦЭМ им. Н. Ф. Гамалеи, «АстраЗенека» и «Р-Фарм» договорились о сотрудничестве в области вакцины против коронавируса. Архивная копия от 4 марта 2021 на Wayback Machine на сайте https://rdif.ru Архивная копия от 29 декабря 2020 на Wayback Machine
- ↑ AstraZeneca, РФПИ и Центр им. Гамалеи подписали соглашение о сотрудничестве по вакцинам. Архивная копия от 21 декабря 2020 на Wayback Machine. ТАСС
- ↑ Центр Гамалеи и AstraZeneca подписали меморандум о сотрудничестве. Архивная копия от 31 декабря 2020 на Wayback Machine. Интерфакс
- ↑ Вакцина «Спутник Лайт» будет действовать до пяти месяцев. Коммерсантъ (12 февраля 2021). Дата обращения: 12 февраля 2021. Архивировано 12 февраля 2021 года.
- ↑ An Open Study on the Safety, Tolerability, and Immunogenicity of «Sputnik Light» Vaccine. Архивная копия от 14 февраля 2021 на Wayback Machine // Статья на сайте clinicaltrials.gov.
- ↑ Г. Тадтаев. Минздрав разрешил испытывать на людях препарат от COVID-19 «Спутник Лайт». Архивная копия от 17 февраля 2021 на Wayback Machine. РБК, 11.01.2021
- ↑ И. Невинная. В РФПИ объяснили, зачем нужна вакцина «Спутник Лайт». Архивная копия от 10 февраля 2021 на Wayback Machine. Российская газета, 11.01.2021
- ↑ Евросоюз начал экспертизу вакцины «Спутник V». РИА Новости. Дата обращения: 4 марта 2021. Архивировано 4 марта 2021 года.
- ↑ Прививка от коронавируса будет как обычный укол и даст защиту на год. Комсомольская правда (18 июля 2020). Дата обращения: 18 июля 2020. Архивировано 10 июля 2020 года.
- ↑ Клинические испытания. sputnikvaccine.com (12 декабря 2020). Дата обращения: 12 декабря 2020. Архивировано 4 декабря 2020 года.
- ↑ Denis Y. Logunov, Inna V. Dolzhikova, Olga V. Zubkova, Amir I. Tukhvatulin, Dmitry V. Shcheblyakov. Safety and immunogenicity of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine in two formulations: two open, non-randomised phase 1/2 studies from Russia (англ.) // The Lancet. — 2020-09-26. — Т. 396, вып. 10255. — С. 887–897. — ISSN 1474-547X 0140-6736, 1474-547X. — doi:10.1016/S0140-6736(20)31866-3. Архивировано 17 апреля 2021 года.
- ↑ 1 2 An Open Study of the Safety, Tolerability and Immunogenicity of «Gam-COVID-Vac Lyo» Vaccine Against COVID-19 (англ.) (18 июня 2020). Дата обращения: 5 мая 2021. Архивировано 3 мая 2021 года.
- ↑ Gam-COVID-Vac. Дата обращения: 30 марта 2021. Архивировано 30 апреля 2021 года.
- ↑ 1 2 3 4 5 Реестр разрешений на проведение клинических исследований (РКИ). grls.rosminzdrav.ru. Минздрав РФ (12 декабря 2020). Дата обращения: 12 декабря 2020. Архивировано 1 июля 2021 года.
- ↑ Первая группа участников клинических испытаний вакцины от CoViD-19 выписана из филиала Главного военного клинического госпиталя имени Н. Н. Бурденко. Архивная копия от 2 мая 2021 на Wayback Machine // 15.07.2020. Официальный сайт Минобороны России. Департамент информации и массовых коммуникаций МО РФ.
- ↑ Минобороны отобрало добровольцев для испытания вакцины от COVID-19. Архивная копия от 12 марта 2021 на Wayback Machine // 02.06.2020. РБК. Г. Демурина.
- ↑ Испытания вакцины от коронавируса в филиале Главного военного клинического госпиталя им. Н. Н. Бурденко. Архивная копия от 22 октября 2021 на Wayback Machine // Фоторепортаж от 01.08.2020. РИА-Новости.
- ↑ На ком Минобороны будет испытывать вакцину от коронавируса? Архивная копия от 23 мая 2021 на Wayback Machine // 02.06.2020. АиФ.
- ↑ Study »Gam-COVID-Vac» Vaccine Against COVID-19 (англ.). ClinicalTrials.gov. Health Ministry of the Russian Federation (12 августа 2020). Дата обращения: 12 августа 2020. Архивировано 4 мая 2021 года.
- ↑ Минздрав России выдал Центру Гамалеи разрешение на проведение пострегистрационного клинического исследования вакцины от коронавируса. Минздрав РФ (25 декабря 2020). Дата обращения: 25 декабря 2020. Архивировано 1 ноября 2020 года.
- ↑ Clinical Trial of Efficacy, Safety, and Immunogenicity of Gam-COVID-Vac Vaccine Against COVID-19 (RESIST) (англ.). ClinicalTrials.gov. Health Ministry of the Russian Federation (20 октября 2020). Дата обращения: 20 октября 2020. Архивировано 22 октября 2020 года.
- ↑ Москвичи могут принять участие в пострегистрационных исследованиях вакцины от коронавируса. www.mos.ru. Официальный сайт Мэра Москвы (26 августа 2020). Дата обращения: 26 августа 2020. Архивировано 27 октября 2020 года.
- ↑ Клиническое исследование вакцины. www.mos.ru. Официальный сайт Мэра Москвы (26 августа 2020). Дата обращения: 26 августа 2020. Архивировано 28 августа 2020 года.
- ↑ Минздрав объявил о завершении всех испытаний «Спутника V». РБК. Дата обращения: 14 февраля 2022. Архивировано 14 февраля 2022 года.
- ↑ The Study of »Gam-COVID-Vac» Vaccine Against COVID-19 With the Participation of Volunteers of 60 y.o and Older (англ.). ClinicalTrials.gov. Health Ministry of the Russian Federation (14 октября 2020). Дата обращения: 20 декабря 2020. Архивировано 17 декабря 2020 года.
- ↑ Clinical Trial of Efficacy, Safety, and Immunogenicity of Gam-COVID-Vac Vaccine Against COVID-19 in Belarus (англ.). ClinicalTrials.gov. Health Ministry of the Russian Federation (25 сентября 2020). Дата обращения: 20 декабря 2020. Архивировано 24 декабря 2020 года.
- ↑ Clinical Trial to Assess Safety and Immunogenicity of Gam-COVID-Vac Combined Vector Vaccine for Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Infection (англ.). ClinicalTrials.gov. Health Ministry of the Russian Federation (23 ноября 2020). Дата обращения: 20 декабря 2020. Архивировано 18 декабря 2020 года.
- ↑ Clinical Trial of the Immunogenicity, Safety, and Efficacy of the Gam-COVID-Vac Vaccine Against COVID-19 in Venezuela (англ.). ClinicalTrials.gov. Health Ministry of the Russian Federation (24 ноября 2020). Дата обращения: 20 декабря 2020. Архивировано 17 января 2021 года.
- ↑ A Phase III Clinical Trial of the Immunogenicity and Safety of the Gam-COVID-Vac Vaccine Against COVID-19 in the UAE — Full Text View — ClinicalTrials.gov. Дата обращения: 15 января 2021. Архивировано 21 января 2021 года.
- ↑ 1 2 ROCCA, 2021.
- ↑ 1 2 Минздрав Сербии: «Спутник V» вызвал наименьшее число побочных эффектов : [арх. 12 июля 2021] // Коммерсантъ. — 2021. — 12 июля.
- ↑ Pagotto et al., 2021.
- ↑ 1 2 Campaña Nacional de Vacunación contra la COVID-19: 12º Informe de vigilancia deseguridad en vacunas : 12 o Informe de vigilancia de seguridad en vacunas : [исп.] : [арх. 6 июля 2021]. — Argentina : Ministerio de Salud; Comisión Nacional de Seguridad en Vacuna, 2021. — Junio. — 5 p.
- ↑ Эффективность вакцины «Спутник V» против коронавируса составила 92% в ходе первого промежуточного анализа данных фазы III клинических исследований в РФ. sputnikvaccine.com. НИЦЭМ им. Н. Ф. Гамалеи, РФПИ (11 ноября 2020). Дата обращения: 11 февраля 2021. Архивировано 26 января 2021 года.
- ↑ 1 2 3 Клещенко Е. Предварительные результаты фазы 3 исследований вакцины Гам-КОВИД-Вак. Архивная копия от 28 июня 2021 на Wayback Machine. — Pcr.News. — 2021.02.02.
- ↑ Эпидемиологическая эффективность вакцины определяется по формуле 100% · (α − β)/α, где α — вероятность заболевания в группе плацебо, β — вероятность заболевания в группе вакцинированных.
- ↑ Журнал Vaccines сообщил об эффективности «Спутника V» против новых штаммов коронавируса : [арх. 12 июля 2021] // ТАСС. — 2021. — 12 июля.
- ↑ В Аргентине заявили, что «Спутник V» эффективен против штамма «дельта» - Газета.Ru | Новости. Газета.Ru. Дата обращения: 16 сентября 2021. Архивировано 16 сентября 2021 года.
- ↑ А. А. Барчук; Д. Даниленко. У абсолютного большинства привитых вакциной Sputnik V положительный результат исследования на антитела. Архивная копия от 17 июля 2021 на Wayback Machine (пресс-релиз). Европейский университет в Санкт-Петербурге, 16.06.2021
- ↑ Barchuk, A. et al. Evaluation of the performance of SARS‐CoV‐2 antibody assays for a longitudinal populationbased study of COVID‐19 spread in St. Petersburg, Russia (англ.) // Journal of Medical Virology[en]. — 2021. — doi:10.1002/jmv.27126. Архивировано 17 июля 2021 года.
- ↑ Barchuk, A., Skougarevskiy, D., Titaev, K. et al. Seroprevalence of SARS-CoV-2 antibodies in Saint Petersburg, Russia: a population-based study (англ.) // Scientific Reports[en]. — 2021. — 21 June. — doi:10.1038/s41598-021-92206-y. Архивировано 17 июля 2021 года.
- ↑ Anton Barchuk, Mikhail Cherkashin, Anna Bulina, Natalia Berezina, Tatyana Rakova. Vaccine Effectiveness against Referral to Hospital and Severe Lung Injury Associated with COVID-19: A Population-Based Case-Control Study in St. Petersburg, Russia (англ.) // medRxiv. — 2021-09-03. — P. 2021.08.18.21262065. — doi:10.1101/2021.08.18.21262065. Архивировано 11 сентября 2021 года.
- ↑ Russia’s Sputnik V protects against severe COVID-19 from Delta variant, study shows (англ.). www.science.org. Дата обращения: 3 сентября 2021. Архивировано 4 сентября 2021 года.
- ↑ Olga Matveeva, Alexander Ershov. Retrospective Cohort Study of the Effectiveness of the Sputnik V and EpiVacCorona Vaccines against the SARS-CoV-2 Delta Variant in Moscow (June–July 2021) (англ.) // Vaccines. — 2022-06-21. — Vol. 10, iss. 7. — P. 984. — ISSN 2076-393X. — doi:10.3390/vaccines10070984. Архивировано 21 июля 2022 года.
- ↑ РФПИ опубликовал данные властей Венгрии по безопасности «Спутника V». Архивная копия от 17 июля 2021 на Wayback Machine. РБК, 25.04.2021
- ↑ Венгрия признала «Спутник V» самой безопасной вакциной. Архивная копия от 17 июля 2021 на Wayback Machine. Интерфакс, 25.04.2021
- ↑ Показывают ли венгерские данные о вакцинации, что российская вакцина «Спутник-V» наиболее эффективная? Архивная копия от 17 июля 2021 на Wayback Machine. ИноПресса, 03.05.2021
- ↑ Vokó Z. et al. Nationwide effectiveness of five SARS-CoV-2 vaccines in Hungary - The HUN-VE study (англ.) // Clinical Microbiology and Infection. — 2021. — doi:10.1016/j.cmi.2021.11.011. Архивировано 29 ноября 2021 года. (In Press, Journal Pre-proof.)
- ↑ Sputnik-V tiene una efectividad con una sola dosis de 78,6 % para evitar casos. Архивная копия от 13 июля 2021 на Wayback Machine — Gobierno de la Provincia de Buenos Aires. — 2 de Junio 2021.
- ↑ Ministros de Salud de todo el país consensuaron redoblar esfuerzos para completar los esquemas de vacunación en mayores de 40 años. Архивная копия от 9 июля 2021 на Wayback Machine. — Ministerio de Salud. 01 de julio de 2021.
- ↑ José María Costa. «Sputnik V y Sinopharm generan alta inmunidad celular en más del 80 % de los casos, según el Conicet. Архивная копия от 18 июля 2021 на Wayback Machine» («по данным Conicet, Sputnik V и Sinopharm обеспечивают высокий клеточный иммунитет более чем в 80 % случаев»). La Nación, 15.07.2021
- ↑ В Аргентине выяснили, что более 90 % привитых «Спутником V» получают долгосрочный иммунитет. Архивная копия от 17 июля 2021 на Wayback Machine. ТАСС, 17.07.2021
- ↑ РФПИ: Более 90 % вакцинированных «Спутник V» получают долгосрочный иммунитет. Архивная копия от 17 июля 2021 на Wayback Machine. Российская газета, 17.07.2021
- ↑ Исследование на SARS-CoV-2 показало эффективность антител сывороток крови после «Спутника». Архивная копия от 26 июля 2021 на Wayback Machine. ТАСС, 26.07.2021
- ↑ I. V. Dolzhikova, A. A. Iliukhina, A. V. Kovyrshina, A. V. Kuzina, V. A. Gushchin. Sputnik Light booster after Sputnik V vaccination induces robust neutralizing antibody response to B.1.1.529 (Omicron) SARS-CoV-2 variant (англ.). — 2021-12-21. — P. 2021.12.17.21267976. — doi:10.1101/2021.12.17.21267976v1. Архивировано 2 января 2022 года.
- ↑ Soledad González, Santiago Olszevicki, Martín Salazar, Ana Calabria, Lorena Regairaz. Effectiveness of the first component of Gam-COVID-Vac (Sputnik V) on reduction of SARS-CoV-2 confirmed infections, hospitalisations and mortality in patients aged 60-79: a retrospective cohort study in Argentina (англ.) // EClinicalMedicine. — 2021-10-01. — Т. 40. — ISSN 2589-5370. — doi:10.1016/j.eclinm.2021.101126.
- ↑ María M. Gonzalez Lopez Ledesma, Lautaro Sanchez, Diego S. Ojeda, Santiago Oviedo Rouco, Andres H. Rossi. Temporal Increase in Neutralization Potency of SARS-CoV-2 Antibodies and Reduced Viral Variant Escape after Sputnik V Vaccination (англ.) // medRxiv. — 2021-08-25. — P. 2021.08.22.21262186. — doi:10.1101/2021.08.22.21262186. Архивировано 14 сентября 2021 года.
- ↑ В Аргентине «Спутник V» назвали самым эффективным против дельта-штамма. РБК. Дата обращения: 18 октября 2021. Архивировано 18 октября 2021 года.
- ↑ 1 2 Dashkevich A. M. et al. (November 16, 2021). COVID-19 in the Republic of Belarus: pandemic features and the interim safety and efficacy assessment of the Gam-COVID-Vac vaccine. medRxiv. doi:10.1101/2021.11.15.21265526.
- ↑ 1 2 Nogrady B. Mounting evidence suggests Sputnik COVID vaccine is safe and effective (англ.) // Nature. — 2021. — doi:10.1038/d41586-021-01813-2. Архивировано 29 августа 2021 года.
- ↑ 1 2 3 4 Журнал Nature опубликовал статью о безопасности «Спутника V». Архивная копия от 7 июля 2021 на Wayback Machine. РБК, 07.07.2021
- ↑ В Сан-Марино заявили о почти 100% эффективности «Спутника V». РБК. Дата обращения: 18 октября 2021. Архивировано 18 октября 2021 года.
- ↑ Goff, S. P. Construction of hybrid viruses containing SV40 and λ phage DNA segments and their propagation in cultured monkey cells : [англ.] : [арх. 27 августа 2022] / S. P. Goff, P. Berg // Cell. — 1976. — Vol. 9, no. 4. — P. 695–705. — doi:10.1016/0092-8674(76)90133-1.
- ↑ 1 2 3 Список статей по безопасности векторов аденовируса человека. sputnikvaccine. Дата обращения: 20 февраля 2021. Архивировано 28 января 2021 года.
- ↑ Effects of vaccines in protecting against Ebola virus disease: protocol for a systematic review (англ.). BMJ Open (3 июля 2019). Дата обращения: 20 февраля 2021. Архивировано 6 декабря 2020 года.
- ↑ Johnson & Johnson Receives Positive CHMP Opinion for Janssen’s Investigational Preventive Ebola Vaccine Regimen (англ.). Ritzaus. Дата обращения: 20 февраля 2021. Архивировано 16 января 2021 года.
- ↑ Gendicine. Gendicine showed synergistic therapeutic effects when used in combination with a variety of traditional cancer treatment methods such as radiotherapy, chemotherapy, and hyperthermia. (англ.). ScienceDirect. Дата обращения: 20 февраля 2021. Архивировано 6 декабря 2020 года.
- ↑ The First Approved Gene Therapy Product for Cancer Ad-p53 (Gendicine): 12 Years in the Clinic (англ.). Mary Ann Liebert (1 февраля 2018). Дата обращения: 20 февраля 2021. Архивировано 11 мая 2021 года.
- ↑ San Marino apre al turismo vaccinale dal 17 maggio: sarà somministrato Sputnik (итал.). la Repubblica (12 мая 2021). Дата обращения: 28 июля 2021. Архивировано 28 июля 2021 года.
- ↑ Estudio bonaerense confirma la seguridad de la vacuna Sputnik V. Архивная копия от 25 июня 2021 на Wayback Machine — Gobierno de la Provincia de Buenos Aires. — 24 de Junio 2021.
- ↑ Аргентина отчиталась о побочных эффектах «Спутника». Что стало известно после 7 млн введенных доз? Архивная копия от 7 июля 2021 на Wayback Machine. Телеканал «Дождь», 07.07.2021
- ↑ В Аргентине зарегистрировано меньше 0,003% госпитализаций после вакцинации «Спутником V». Коммерсантъ (8 июля 2021). Дата обращения: 8 июля 2021. Архивировано 8 июля 2021 года.
- ↑ Аргентина раскрыла данные о побочных эффектах у 0.5% привитых «Спутником». РБК (7 июля 2021). Дата обращения: 11 июля 2021. Архивировано 11 июля 2021 года.
- ↑ Montalti M. et al. ROCCA observational study: Early results on safety of Sputnik V vaccine (Gam-COVID-Vac) in the Republic of San Marino using active surveillance (англ.) // EClinicalMedicine. — 2021. — P. 101027. — ISSN 2589-5370. — doi:10.1016/j.eclinm.2021.101027.
[исправить]
- ↑ Montalti M. et al. ROCCA study protocol and interim analysis on safety of Sputnik V vaccine (Gam-COVID-Vac) in the Republic of San Marino: an observational study using active surveillance / medrxiv.org. Архивная копия от 15 марта 2020 на Wayback Machine. May 5, 2021. doi:10.1101/2021.05.03.21256509.
- ↑ Farhang Babamahmoodi, Majid Saeedi, Reza Alizadeh-Navaei, Akbar Hedayatizadeh-Omran, Seyed Abbas Mousavi. Side effects and Immunogenicity following administration of the Sputnik V COVID-19 vaccine in health care workers in Iran (англ.) // Scientific Reports. — 2021-11-02. — Vol. 11, iss. 1. — P. 21464. — ISSN 2045-2322. — doi:10.1038/s41598-021-00963-7. Архивировано 2 января 2022 года.
- ↑ Драпкина Ю.С. и др. Вакцина Гам-КОВИД-Вак (Спутник V) не оказывает негативного влияния на сперматогенез у мужчин // Акушерство и гинекология. — 2021. — Вып. 7. — С. 88—94. — ISSN 2412-5679. — doi:10.18565/aig.2021.7.88-94. [исправить]
- ↑ Долгушина Н.В. и др. Вакцина Гам-КОВИД-Вак (Спутник V) не оказывает негативного влияния на овариальный резерв у женщин репродуктивного возраста // Акушерство и гинекология. — 2021. — Вып. 7. — С. 81—86. — ISSN 2412-5679. — doi:10.18565/aig.2021.7.81-86. [исправить]
- ↑ В России зарегистрировали однокомпонентную вакцину »Спутник Лайт». РИА Новости (6 мая 2021). Дата обращения: 6 мая 2021. Архивировано 6 мая 2021 года.
- ↑ Регистрационное удостоверение номер ЛП-006993. Государственный реестр лекарственных средств (6 мая 2021). Дата обращения: 6 мая 2021. Архивировано 5 июня 2021 года.
- ↑ 1 2 3 Однокомпонентная вакцина «Спутник Лайт» зарегистрирована в России. Спутник V (6 мая 2021). Дата обращения: 5 июня 2021. Архивировано 5 июня 2021 года.
- ↑ Вакцина «Спутник Лайт» поступила в гражданский оборот. Архивная копия от 26 июня 2021 на Wayback Machine. Новая газета, 26 июня 2021
- ↑ В новой методичке Минздрав рекомендует «Спутник Лайт» для ревакцинации. «Коммерсантъ» (18 ноября 2021). Дата обращения: 18 ноября 2021. Архивировано 18 ноября 2021 года.
- ↑ Тунис зарегистрировал «Спутник Лайт» в качестве универсального бустера. Дата обращения: 2 января 2022. Архивировано 2 января 2022 года.
- ↑ Что стало известно о новой вакцине для подростков «Спутник М». Ведомости. Дата обращения: 4 января 2022. Архивировано 4 января 2022 года.
- ↑ 1 2 Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2 — Видаль. Дата обращения: 4 января 2022. Архивировано 4 января 2022 года.
- ↑ Вакцина «Спутник М» для подростков получила регистрацию в России. Газета.ru. Дата обращения: 24 ноября 2021. Архивировано 24 ноября 2021 года.
- ↑ В России зарегистрировали вакцину от COVID-19 для подростков — «Спутник M». «Коммерсантъ» (24 ноября 2021). Дата обращения: 25 ноября 2021. Архивировано 24 ноября 2021 года.
- ↑ Создатели «Спутника М» перечислили побочные эффекты и противопоказания вакцины. «Коммерсантъ» (25 ноября 2021). Дата обращения: 25 ноября 2021. Архивировано 25 ноября 2021 года.
- ↑ Концентрацию «Спутника V» уменьшат в 10 раз для вакцинации детей. Forbes.ru. Дата обращения: 4 января 2022. Архивировано 4 января 2022 года.
- ↑ Концентрация «Спутника V» для детей будет снижена в 10 раз. Коммерсантъ (31 октября 2021). Дата обращения: 4 января 2022. Архивировано 4 января 2022 года.
- ↑ Вакцинация подростков. Что представляет собой »Спутник М»? vesti.ru. Дата обращения: 14 февраля 2022. Архивировано 14 февраля 2022 года.
- ↑ Вакцина «Спутник M»: в правительстве назвали дату начала вакцинации детей от COVID-19. sib.fm. Дата обращения: 14 февраля 2022. Архивировано 14 февраля 2022 года.
- ↑ «Спутник М» появился в регионах: главное о вакцине от коронавируса для детей и подростков. 360tv.ru. Дата обращения: 14 февраля 2022. Архивировано 14 февраля 2022 года.
- ↑ В чем суть назальной вакцины от коронавируса и в чем ее плюсы? Аргументы и факты (15 мая 2021). Дата обращения: 23 ноября 2021. Архивировано 23 ноября 2021 года.
- ↑ Глава Центра имени Гамалеи заявил, что вакцина от ковида в виде спрея поможет привитым не становиться переносчиками болезни. Фонтанка.ру (22 ноября 2021). Дата обращения: 23 ноября 2021. Архивировано 22 ноября 2021 года.
- ↑ Гинцбург рассказал о ходе клинических испытаний «Спутника V» в виде спрея. Lenta.RU. Дата обращения: 17 февраля 2022. Архивировано 17 февраля 2022 года.
- ↑ Производство »Спутник V» на экспорт будет после проведения прививочной кампании в РФ. Интерфакс. Дата обращения: 19 мая 2021. Архивировано 19 мая 2021 года.
- ↑ RTS, Radio televizija Srbije, Radio Television of Serbia. Počela proizvodnja vakcine »sputnjik» na Torlaku. www.rts.rs. Дата обращения: 28 июля 2021. Архивировано 28 июля 2021 года.
- ↑ Jetema joins GL Rapha’s consortium to make Russia’s Sputnik V vaccine (кор.). KBR (22 июля 2021). Дата обращения: 28 июля 2021. Архивировано 28 июля 2021 года.
- ↑ Филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф.Гамалеи» Минздрава России начал маркировку вакцины для профилактики коронавирусной инфекции «Спутник V». Минздрав РФ (9 сентября 2020). Дата обращения: 15 апреля 2021. Архивировано 18 апреля 2021 года.
- ↑ «Генериум» начал отгрузку вакцины «Спутник V» в медицинские учреждения. Ведомости (9 ноября 2020). Дата обращения: 15 апреля 2021. Архивировано 18 апреля 2021 года.
- ↑ Мария Котова. Центр Гамалеи расширяет число партнеров по производству «Спутник V». Ведомости (6 ноября 2020). Дата обращения: 15 апреля 2021. Архивировано 18 апреля 2021 года.
- ↑ Виктория Саитова. Biocad начал поставку «Спутника-V» для масштабной вакцинации. РБК (16 декабря 2020). Дата обращения: 15 апреля 2021. Архивировано 10 августа 2021 года.
- ↑ «Р-Фарм» начала производство вакцины «Спутник V». РИА Новости (11 марта 2021). Дата обращения: 15 апреля 2021. Архивировано 16 апреля 2021 года.
- ↑ 1 2 В Казахстане рассказали о производстве вакцины »Спутник V». РИА Новости (13 апреля 2021). Дата обращения: 15 апреля 2021. Архивировано 13 апреля 2021 года.
- ↑ 1 2 3 Быстрее, больше, безопасней: как в Южной Корее производят «Спутник V». Архивная копия от 21 июля 2021 на Wayback Machine. РИА Новости, 06.05.2021
- ↑ В Бразилии с 15 января начнется производство «Спутника V». Архивная копия от 18 января 2021 на Wayback Machine. ТАСС, 11.01.2021
- ↑ В Бразилии началось производство вакцины »Спутник V». РИА Новости (13 января 2021). Дата обращения: 15 апреля 2021. Архивировано 20 апреля 2021 года.
- ↑ Na “guerra das vacinas”, União Química se prepara para lançar Sputnik V e dispara contra Butantan e Fiocruz. Дата обращения: 5 мая 2021. Архивировано 5 мая 2021 года.
- ↑ В Бразилии произвели первую партию вакцины «Спутник V». Российская газета (20 мая 2021). Дата обращения: 21 мая 2021. Архивировано 20 мая 2021 года.
- ↑ 1 2 3 «Спутник V» в Беларуси: как производят вакцину на «Белмедпрепаратах». Архивная копия от 21 июля 2021 на Wayback Machine. Sputnik.by, 14.05.2021
- ↑ Аргентина начала производить «Спутник V». Архивная копия от 21 июля 2021 на Wayback Machine. Газета.ru, 20.04.2021
- ↑ 1 2 Путин и Фернандес дали старт производству «Спутника V» в Аргентине. РИА Новости (4 июня 2021). Дата обращения: 5 июня 2021. Архивировано 5 июня 2021 года.
- ↑ В Индии началось производство вакцины «Спутник V». Архивная копия от 9 июля 2021 на Wayback Machine. Российская газета, 24.05.2021
- ↑ Индия одобрила первую партию произведенной в стране вакцины «Спутник V». РИА Новости (1 июня 2021). Дата обращения: 5 июня 2021. Архивировано 5 июня 2021 года.
- ↑ РФПИ и Virchow Biotech договорились о партнерстве для производства вакцины «Спутник V» в Индии. Sputnik Vaccine (22 марта 2021). Дата обращения: 15 апреля 2021. Архивировано 18 апреля 2021 года.
- ↑ РФПИ и Stelis Biopharma договорились о партнерстве для производства 200 миллионов доз вакцины «Спутник V». Sputnik Vaccine (19 марта 2021). Дата обращения: 15 апреля 2021. Архивировано 18 апреля 2021 года.
- ↑ РФПИ и Panacea Biotec начали производство вакцины «Спутник V» в Индии. Архивная копия от 24 мая 2021 на Wayback Machine. rdif.ru, 24.05.2021
- ↑ В Индии выпустили тестовую партию вакцины «Спутник V». Архивная копия от 6 июля 2021 на Wayback Machine. РБК, 06.07.2021
- ↑ Россия заключила соглашение с Индией на производство 300 млн доз вакцины «Спутник V». GMPnews (3 сентября 2020). Дата обращения: 11 декабря 2020. Архивировано 13 августа 2021 года.
- ↑ 1 2 Путин и Вучич по видеосвязи дали старт производству «Спутника V» в Сербии. Архивная копия от 13 июля 2021 на Wayback Machine. Коммерсантъ, 04.06.2021
- ↑ В Иране произведены пробные партии «Спутника V». Архивная копия от 21 июля 2021 на Wayback Machine. Интерфакс, 04.06.2021
- ↑ Тестовая партия вакцины «Спутник V» произведена в Иране. Sputnikvaccine (26 июня 2021). Дата обращения: 26 июня 2021. Архивировано 27 июня 2021 года.
- ↑ 1 2 В Италии запустили производство «Спутника V». Lenta.ru (16 июня 2021). Дата обращения: 18 июля 2021. Архивировано 18 июля 2021 года.
- ↑ В Армении началось производство «Спутника V». ТАСС (1 июля 2021). Дата обращения: 7 июля 2021. Архивировано 9 июля 2021 года.
- ↑ 1 2 В Мексике произвели тестовую партию «Спутника V». ТАСС (5 июля 2021). Дата обращения: 22 июля 2021. Архивировано 21 июля 2021 года.
- ↑ 1 2 Во Вьетнаме произвели первую партию вакцины «Спутник V». ТАСС (21 июля 2021). Дата обращения: 22 июля 2021. Архивировано 21 июля 2021 года.
- ↑ 1 2 В Узбекистане произвели первую партию «Спутника V». ТАСС (30 июля 2021). Дата обращения: 27 августа 2021. Архивировано 3 августа 2021 года.
- ↑ Узбекистан начал производить «Спутник V». «Коммерсантъ» (7 октября 2021). Дата обращения: 7 октября 2021. Архивировано 7 октября 2021 года.
- ↑ Cohen J. Russia’s approval of a COVID-19 vaccine is less than meets the press release (англ.) // Science : журн. — 2020. — 11 August. Архивировано 26 августа 2021 года.
- ↑ 1 2 В Швеции прокомментировали регистрацию российской вакцины от COVID-19 : [арх. 13 августа 2020] // РИА Новости. — 2020. — 11 августа.
- ↑ Callaway E. Russia’s fast-track coronavirus vaccine draws outrage over safety : The immunization is the first approved for widespread use but could be dangerous because it hasn’t been tested in large trials, say researchers : [англ.] : [арх. 11 августа 2020] / Ewen Callaway // Nature : журн. — 2020. — 11 August. — doi:10.1038/d41586-020-02386-2. — PMID 32782400.
- ↑ Matthew Chance. Russia says foreign inquiries about its potential fast-track Covid-19 vaccine are pouring in. But questions abound. CNN (30 июля 2020). Дата обращения: 3 марта 2021. Архивировано 13 декабря 2021 года.
- ↑ COVID-19 vaccines: early success and remaining challenges (неопр.). The Lancet (4 сентября 2020). doi:10.1016/S0140-6736(20)31867-5. Дата обращения: 6 сентября 2020. Архивировано 9 сентября 2020 года.
- ↑ Russia’s COVID-19 vaccine: Trial results ’encouraging but small’ (англ.). Euronews (4 сентября 2020). Дата обращения: 6 сентября 2020. Архивировано 14 сентября 2020 года.
- ↑ Office of Infectious Disease and HIV/AIDS Policy (OIDP). Vaccine Types (англ.). HHS.gov (26 апреля 2021). Дата обращения: 30 января 2022. Архивировано 16 июля 2021 года.
- ↑ Akira Sakurai, Takashi Ogawa, Jun Matsumoto, Tetsunari Kihira, Shinji Fukushima. Regulatory aspects of quality and safety for live recombinant viral vaccines against infectious diseases in Japan (англ.) // Vaccine. — 2019-10-08. — Vol. 37, iss. 43. — P. 6573–6579. — ISSN 0264-410X. — doi:10.1016/j.vaccine.2019.08.031. Архивировано 5 февраля 2021 года.
- ↑ Встреча по случаю подписания меморандума между НИЦЭМ имени Гамалеи, компанией «АстраЗенека», РФПИ и «Р-Фарм». Архивная копия от 15 февраля 2021 на Wayback Machine // kremlin.ru
- ↑ В AstraZeneca рассказали о комбинации своей вакцины со «Спутник V». Архивная копия от 31 декабря 2020 на Wayback Machine // РИА
- ↑ Главный исполнительный директор AstraZeneca поздравил Россию с разработкой «Спутника V». Архивная копия от 26 января 2021 на Wayback Machine // rt.com
- ↑ Bloomberg (США): Putin’s Once-Scorned Vaccine Now Favorite in Pandemic Fight. Дата обращения: 8 февраля 2021. Архивировано 8 февраля 2021 года.
- ↑ Russian Covid-19 Vaccine Was Highly Effective in Trial, Boosting Moscow’s Rollout Ambitions. Дата обращения: 8 февраля 2021. Архивировано 7 февраля 2021 года.
- ↑ Spoutnik V est en orbite : un triomphe scientifique et politique pour la Russie. Архивная копия от 17 февраля 2021 на Wayback Machine // Радио Канада
- ↑ [Подозрительный «Спутник V»: ученые объяснили, почему не доверяют российской вакцине https://www.rosbalt.ru/world/2021/05/16/1901662.html], Росбалт (16.05.2021).
- ↑ Denis Y. Logunov, Inna V. Dolzhikova, Dmitry V. Shcheblyakov. Data discrepancies and substandard reporting of interim data of Sputnik V phase 3 trial – Authors’ reply (англ.) // The Lancet. — 2021-05-12. — Т. 0, вып. 0. — ISSN 1474-547X 0140-6736, 1474-547X. — doi:10.1016/S0140-6736(21)00894-1.
- ↑ Лауреат Нобелевской премии прокомментировал данные об эффективности «Спутника V» // ТАСС
- ↑ Главный инфекционист США отреагировал на публикацию данных о «Спутнике V». Архивная копия от 8 февраля 2021 на Wayback Machine // РИА Новости
- ↑ Эксперты в США оценили преимущества вакцины «Спутник V». Архивная копия от 5 февраля 2021 на Wayback Machine // ТАСС
- ↑ Вирусолог назвал лучшую вакцину для переболевших коронавирусом. Архивная копия от 7 июля 2021 на Wayback Machine. Известия, 07.07.2021
- ↑ В презентации российской вакцины «Спутник V» в ООН приняли участие более 50 стран. ТАСС. Дата обращения: 20 апреля 2021. Архивировано 20 апреля 2021 года.
- ↑ Сергей Галаянц. Вакцина Спутник V будет стоить менее $10 за дозу на экспорт. Vademecum (24 ноября 2020). Дата обращения: 11 декабря 2020. Архивировано 28 января 2021 года.
- ↑ В РФПИ отметили изменения в позиции зарубежных стран по «Спутник V». РИА Новости (8 декабря 2020). Дата обращения: 11 декабря 2020. Архивировано 10 декабря 2020 года.
- ↑ РФПИ подал заявки на одобрение вакцины «Спутник V» регуляторам 40 стран. РИА Новости (2 декабря 2020). Дата обращения: 11 декабря 2020. Архивировано 13 декабря 2020 года.
- ↑ Kantchev, Georgi. Russian Covid-19 Vaccine Was Highly Effective in Trial, Boosting Moscow’s Rollout Ambitions (англ.), www.wsj.com, The Wall Street Journal (2 February 2021). Архивировано 3 февраля 2021 года. Дата обращения: 4 февраля 2021.
- ↑ РФПИ подал заявку на регистрацию «Спутника V» в ЕС 29 января. ТАСС (9 февраля 2021). Дата обращения: 9 февраля 2021. Архивировано 9 февраля 2021 года.
- ↑ Clarification on Sputnik V vaccine in the EU approval process. EMA (10 февраля 2021). Дата обращения: 25 февраля 2021. Архивировано 24 февраля 2021 года.
- ↑ Covid-19 : le grand écart des Européens sur le vaccin russe Spoutnik V, Le Monde.fr (30 марта 2021). Архивировано 30 марта 2021 года. Дата обращения: 30 марта 2021.
- ↑ Orlando Crowcroft. Values over vaccines? The story of COVID jab diplomacy in Eastern Europe (англ.). euronews.com. Дата обращения: 2 апреля 2021. Архивировано 1 апреля 2021 года.
- ↑ 1 2 Венгрия первой в Евросоюзе одобрила применение вакцины «Спутник V». Архивная копия от 21 января 2021 на Wayback Machine. РИА Новости, 21.01.2021
- ↑ Le Monde сообщила о расколе в ЕС из-за поставок «Спутника V». РБК. Дата обращения: 30 марта 2021. Архивировано 30 марта 2021 года.
- ↑ Во Франции выразили сожаление, что Греция признает вакцины России и КНР. Газета.Ru. Дата обращения: 11 июля 2021. Архивировано 11 июля 2021 года.
- ↑ Австрия закупит «Спутник V». Газета.Ru. Дата обращения: 30 марта 2021. Архивировано 31 марта 2021 года.
- ↑ Еврокомиссия предупредила Австрию о последствиях закупки «Спутника V». vesti.ru. Дата обращения: 30 марта 2021. Архивировано 30 марта 2021 года.
- ↑ Канцлер Австрии заявил о завершении переговоров по закупке «Спутника V». Архивная копия от 13 июня 2021 на Wayback Machine на сайте https://www.interfax.ru/ Архивная копия от 30 сентября 2007 на Wayback Machine
- ↑ ЮНИСЕФ и Human Vaccine подписали соглашение о поставках вакцины «Спутник V». Новости ООН (27 мая 2021). Дата обращения: 28 июля 2021. Архивировано 28 июля 2021 года.
- ↑ Словакия отказалась закупать новые партии «Спутника V». lenta.ru. Дата обращения: 16 июня 2021. Архивировано 13 июня 2021 года.
- ↑ Chile approves emergency use of Sputnik-V coronavirus vaccine. Reuters (21 июля 2021). Дата обращения: 28 июля 2021. Архивировано 1 августа 2021 года.
- ↑ Нарышкин: Регистрация »Спутника V» в ЕС затягивается специально. Российская газета. Дата обращения: 19 мая 2021. Архивировано 19 мая 2021 года.
- ↑ Финские медики считают возможным разрешить въезд без тестов привитым «Спутником V». ТАСС. Дата обращения: 23 сентября 2021. Архивировано 23 сентября 2021 года.
- ↑ В Гонконге признали российские сертификаты о вакцинации от ковида. Life.ru (28 сентября 2021). Дата обращения: 28 сентября 2021. Архивировано 28 сентября 2021 года.
- ↑ Международный союз биатлонистов признал вакцину «Спутник V». ТАСС. Дата обращения: 19 октября 2021. Архивировано 19 октября 2021 года.
- ↑ Песков объяснил, почему Россия не передала ВОЗ все данные о «Спутнике V». РБК. Дата обращения: 30 января 2022. Архивировано 20 января 2022 года.
- ↑ Песков: Россия пока не предоставила ВОЗ часть данных по »Спутнику V», но процесс идет. ТАСС. Дата обращения: 30 января 2022. Архивировано 27 декабря 2021 года.
- ↑ Первые 70 пунктов вакцинации от COVID-19 начали работать в Москве. Interfax.ru. Дата обращения: 30 января 2022. Архивировано 22 июля 2022 года.
- ↑ «Спутник V» получила первое регистрационное удостоверение за рубежом. Ведомости. Дата обращения: 30 января 2022. Архивировано 12 мая 2022 года.
- ↑ Посол России прокомментировал начало вакцинации от COVID-19 в Белоруссии. РИА Новости (29 декабря 2020). Дата обращения: 29 декабря 2020. Архивировано 30 декабря 2020 года.
- ↑ Власти Аргентины одобрили использование вакцины «Спутник V». РИА Новости (23 декабря 2020). Дата обращения: 23 декабря 2020. Архивировано 23 декабря 2020 года.
- ↑ Аргентина, получив «Спутник V», заявила о старте масштабной вакцинации. Дата обращения: 25 декабря 2020. Архивировано 25 декабря 2020 года.
- ↑ Сербия зарегистрировала российскую вакцину от коронавируса. Lenta.RU. Дата обращения: 30 января 2022. Архивировано 30 января 2022 года.
- ↑ В Сербии 5 января начнется вакцинация российским »Спутником V». Российская газета. Дата обращения: 30 января 2022. Архивировано 23 октября 2021 года.
- ↑ Боливия зарегистрировала вакцину »Спутник V». РИА Новости (20210106T1947). Дата обращения: 30 января 2022. Архивировано 15 апреля 2022 года.
- ↑ В Боливии началась вакцинация препаратом »Спутник V». ТАСС. Дата обращения: 30 января 2022. Архивировано 5 февраля 2021 года.
- ↑ Алжир зарегистрировал вакцину «Спутник V». Interfax.ru. Дата обращения: 30 января 2022. Архивировано 6 февраля 2022 года.
- ↑ В Алжире начали вакцинацию населения «Спутником V». Interfax.ru. Дата обращения: 30 января 2022. Архивировано 31 января 2022 года.
- ↑ Палестина зарегистрировала вакцину «Спутник V». Interfax.ru. Дата обращения: 30 января 2022. Архивировано 17 мая 2021 года.
- ↑ В секторе Газа начали вакцинацию от COVID-19 препаратом «Спутник V». Дата обращения: 16 марта 2021. Архивировано 11 марта 2021 года.
- ↑ Вакцина «Спутник V» зарегистрирована в Венесуэле. Дата обращения: 13 января 2021. Архивировано 13 января 2021 года.
- ↑ Женщина-хирург: первая вакцинированная «Спутником V» в Венесуэле (El Nacional, Венесуэла). inosmi.ru. www.elnacional.com (20 февраля 2021). Дата обращения: 20 февраля 2021. Архивировано 20 февраля 2021 года.
- ↑ Вакцину «Спутник V» зарегистрировали в Парагвае. Дата обращения: 15 января 2021. Архивировано 15 января 2021 года.
- ↑ Twitter — @sputnikvaccine — 22.02.2021. Дата обращения: 22 февраля 2021. Архивировано 22 февраля 2021 года.
- ↑ Turkmenistan has become the first country in Central Asia to register Sputnik V vaccine (англ.). sputnikvaccine.com. Дата обращения: 30 января 2022. Архивировано 28 августа 2021 года.
- ↑ В Ашхабаде началась вакцинация, в Мары рейды по отлову безмасочников. Радио Азатлык. Дата обращения: 6 мая 2021. Архивировано 10 мая 2021 года.
- ↑ Венгрия начала вакцинацию населения «Спутником V». Интерфакс. Дата обращения: 11 февраля 2021. Архивировано 11 февраля 2021 года.
- ↑ Breaking: UAE approves Russia’s Sputnik vaccine for emergency use. wam. Дата обращения: 30 января 2022. Архивировано 23 марта 2022 года.
- ↑ В ОАЭ оценили эффективность »Спутника V». РИА Новости (20210629T1004). Дата обращения: 30 января 2022. Архивировано 23 марта 2022 года.
- ↑ СМИ: правительство Пакистана одобрило экстренное использование вакцины «Спутник V»
- ↑ В Пакистане началась вакцинация «Спутником V». Дата обращения: 5 апреля 2021. Архивировано 5 апреля 2021 года.
- ↑ Вакцина «Спутник V» зарегистрирована в Иране. Дата обращения: 26 января 2021. Архивировано 26 января 2021 года.
- ↑ Иран начал вакцинацию «Спутником V». Дата обращения: 8 февраля 2021. Архивировано 8 февраля 2021 года.
- ↑ «Спутник V» зарегистрировали в Гвинее. Дата обращения: 29 января 2021. Архивировано 29 января 2021 года.
- ↑ Гвинея начала экспериментальную вакцинацию «Спутником V». Дата обращения: 10 июля 2021. Архивировано 10 июля 2021 года.
- ↑ Тунис зарегистрировал российскую вакцину «Спутник V». РИА Новости (30 января 2021). Дата обращения: 30 января 2021. Архивировано 30 января 2021 года.
- ↑ В Тунисе началась вакцинация «Спутником V». Дата обращения: 14 марта 2021. Архивировано 14 марта 2021 года.
- ↑ Армения зарегистрировала российскую вакцину «Спутник V». Дата обращения: 1 февраля 2021. Архивировано 1 февраля 2021 года.
- ↑ В Армении начали вакцинацию медработников препаратом «Спутник V». Архивная копия от 11 марта 2021 на Wayback Machine на сайте https://tass.ru/ Архивная копия от 8 октября 2020 на Wayback Machine
- ↑ Мексиканский регулятор одобрил использование вакцины «Спутник V». Дата обращения: 3 февраля 2021. Архивировано 3 февраля 2021 года.
- ↑ Вакцинация с использованием «Спутника V» началась в Мехико. Дата обращения: 24 февраля 2021. Архивировано 24 февраля 2021 года.
- ↑ «Спутник V» зарегистрировали в Никарагуа. Дата обращения: 3 февраля 2021. Архивировано 3 февраля 2021 года.
- ↑ В Никарагуа начали массовую вакцинацию российским препаратом «Спутник V». Дата обращения: 3 марта 2021. Архивировано 3 марта 2021 года.
- ↑ Минздрав Ливана одобрил экстренное использование вакцины »Спутник V». ТАСС. Дата обращения: 30 января 2022. Архивировано 18 февраля 2021 года.
- ↑ В Ливане началась вакцинация »Спутником V». ТАСС. Дата обращения: 30 января 2022. Архивировано 29 апреля 2021 года.
- ↑ Вакцину «Спутник V» зарегистрировали в Республике Сербской. Дата обращения: 5 февраля 2021. Архивировано 5 февраля 2021 года.
- ↑ В Республике Сербской стартовала вакцинация «Спутником V». Дата обращения: 12 февраля 2021. Архивировано 12 февраля 2021 года.
- ↑ Мьянма зарегистрировала «Спутник V». Дата обращения: 6 февраля 2021. Архивировано 6 февраля 2021 года.
- ↑ Вакцину «Спутник V» зарегистрировали в Монголии. Архивная копия от 9 февраля 2021 на Wayback Machine на сайте https://tass.ru/ Архивная копия от 8 октября 2020 на Wayback Machine
- ↑ Монголия начала вакцинацию населения от коронавируса. Дата обращения: 10 июля 2021. Архивировано 18 декабря 2021 года.
- ↑ Бахрейн зарегистрировал вакцину «Спутник V». «Коммерсантъ» (10 февраля 2021). Дата обращения: 10 февраля 2021. Архивировано 10 февраля 2021 года.
- ↑ Минздрав Бахрейна сообщил о начале вакцинации «Спутником V». Архивная копия от 17 февраля 2021 на Wayback Machine на сайте https://tass.ru/ Архивная копия от 8 октября 2020 на Wayback Machine
- ↑ 1 2 РФПИ подтвердил регистрацию «Спутник V» в Черногории и Сент-Винсенте и Гренадинах. ТАСС. Дата обращения: 12 февраля 2021. Архивировано 12 февраля 2021 года.
- ↑ Черногория начала вакцинацию «Спутником V». Архивная копия от 20 февраля 2021 на Wayback Machine на сайте https://tass.ru/ Архивная копия от 8 октября 2020 на Wayback Machine
- ↑ «Спутник V» зарегистрировали в Казахстане. Архивная копия от 12 февраля 2021 на Wayback Machine на сайте https://tass.ru/ Архивная копия от 8 октября 2020 на Wayback Machine
- ↑ В Казахстане стартовала вакцинация от коронавируса «Спутником V». РИА Новости (1 февраля 2021). Дата обращения: 1 февраля 2021. Архивировано 31 января 2021 года.
- ↑ РФПИ подтвердил регистрацию вакцины «Спутник V» в Узбекистане. Дата обращения: 17 февраля 2021. Архивировано 17 февраля 2021 года.
- ↑ В Ташкенте началась вакцинация «Спутником V». Дата обращения: 29 апреля 2021. Архивировано 29 апреля 2021 года.
- ↑ Вакцину «Спутник V» зарегистрировали в Габоне. Дата обращения: 17 февраля 2021. Архивировано 17 февраля 2021 года.
- ↑ «Спутник V» зарегистрировали в Сан-Марино. Архивная копия от 19 февраля 2021 на Wayback Machine на сайте https://tass.ru/ Архивная копия от 8 октября 2020 на Wayback Machine
- ↑ В Сан-Марино началась вакцинация препаратом «Спутник». Дата обращения: 25 февраля 2021. Архивировано 25 февраля 2021 года.
- ↑ Вакцину «Спутник V» зарегистрировали в Гане. Дата обращения: 20 февраля 2021. Архивировано 20 февраля 2021 года.
- ↑ Сирия зарегистрировала вакцину «Спутник V». Дата обращения: 22 февраля 2021. Архивировано 22 февраля 2021 года.
- ↑ Дамаск ожидает прибытия новой партии «Спутника V» в апреле. Дата обращения: 26 марта 2021. Архивировано 26 марта 2021 года.
- ↑ «Спутник V» прошел процедуру регистрации в Киргизии. Дата обращения: 23 февраля 2021. Архивировано 23 февраля 2021 года.
- ↑ Мамбет Мамакеев: «Как аксакал кыргызской медицины обращаюсь к кыргызскому народу: сделайте прививку от COVID-19». www.med.kg. Дата обращения: 6 мая 2021. Архивировано 7 мая 2021 года.
- ↑ «Спутник V» зарегистрировали в Гайане. Дата обращения: 23 февраля 2021. Архивировано 23 февраля 2021 года.
- ↑ Египет зарегистрировал вакцину «Спутник V». Дата обращения: 24 февраля 2021. Архивировано 24 февраля 2021 года.
- ↑ Гондурас зарегистрировал «Спутник V». Дата обращения: 24 февраля 2021. Архивировано 24 февраля 2021 года.
- ↑ Минздрав Республики Гондурас. Cuarto Informe de Eventos Supuestamente Atribuibles a la Vacunación e Inmunización (ESAVI) con la vacuna contra la COVID-19 primera dosis fabricante Sputnik V (ES) // https://www.salud.gob.hn/. — 2021. — Апрель.
- ↑ Гватемала зарегистрировала вакцину «Спутник V». Архивная копия от 25 февраля 2021 на Wayback Machine на сайте https://interfax.ru/ Архивная копия от 25 февраля 2021 на Wayback Machine
- ↑ РФПИ ответил на претензии Гватемалы по »Спутнику V». РИА Новости (30 июня 2021). Дата обращения: 30 июня 2021. Архивировано 30 июня 2021 года.
- ↑ «Спутник V» зарегистрировали в Молдавии. Дата обращения: 26 февраля 2021. Архивировано 26 февраля 2021 года.
- ↑ С 4 мая в Молдове начинается вакцинация препаратом от ковида «Спутник V». Архивная копия от 4 мая 2021 на Wayback Machine на сайте https://www.kp.md/
- ↑ «Спутник V» зарегистрировали в Словакии. Дата обращения: 1 марта 2021. Архивировано 1 марта 2021 года.
- ↑ В Словакии начинается применение »Спутника V». ТАСС (7 июня 2021). Дата обращения: 7 июня 2021. Архивировано 7 июня 2021 года.
- ↑ 1 2 3 Вакцину «Спутник V» одобрили в Анголе, Джибути и Республике Конго. Дата обращения: 3 марта 2021. Архивировано 3 марта 2021 года.
- ↑ В Республике Конго началась вакцинация от COVID-19 с использованием «Спутника V». Дата обращения: 24 марта 2021. Архивировано 24 марта 2021 года.
- ↑ РФПИ подтвердил регистрацию вакцины «Спутник V» в Шри-Ланке. Дата обращения: 4 марта 2021. Архивировано 4 марта 2021 года.
- ↑ Шри-Ланка получила первую партию вакцины »Спутник V». Российская газета (4 мая 2021). Дата обращения: 18 мая 2021. Архивировано 18 мая 2021 года.
- ↑ «Спутник V» зарегистрировали в Лаосе. Дата обращения: 4 марта 2021. Архивировано 4 марта 2021 года.
- ↑ РФПИ подтвердил регистрацию вакцины «Спутник V» в Ираке. Дата обращения: 4 марта 2021. Архивировано 4 марта 2021 года.
- ↑ «Спутник V» зарегистрировали в Северной Македонии. Дата обращения: 7 марта 2021. Архивировано 7 марта 2021 года.
- ↑ В Северной Македонии началась вакцинация «Спутником V». РИА Новости (10 марта 2021). Дата обращения: 10 марта 2021. Архивировано 10 марта 2021 года.
- ↑ В Зимбабве разрешили использовать «Спутник V» для массовой вакцинации. Дата обращения: 9 марта 2021. Архивировано 9 марта 2021 года.
- ↑ В Зимбабве доставили первую партию вакцины «Спутник V». Дата обращения: 10 июля 2021. Архивировано 10 июля 2021 года.
- ↑ Власти Марокко одобрили применение российской вакцины «Спутник V». Дата обращения: 10 марта 2021. Архивировано 10 марта 2021 года.
- ↑ Вакцину «Спутник V» одобрили к применению в Кении. Дата обращения: 10 марта 2021. Архивировано 10 марта 2021 года.
- ↑ Иордания одобрила экстренное применение вакцины «Спутник V». Дата обращения: 10 марта 2021. Архивировано 10 марта 2021 года.
- ↑ Иордания начала вакцинацию от коронавируса «Спутником V». Дата обращения: 4 апреля 2021. Архивировано 4 апреля 2021 года.
- ↑ Вакцина »Спутник V» получила одобрение в Намибии. ТАСС (11 марта 2021). Дата обращения: 11 марта 2021. Архивировано 11 марта 2021 года.
- ↑ Минздрав Азербайджана утвердил применение «Спутника V». Дата обращения: 12 марта 2021. Архивировано 12 марта 2021 года.
- ↑ В Азербайджане начинается вакцинация от коронавируса «Спутником V». Архивная копия от 18 мая 2021 на Wayback Machine на сайте https://tass.ru/ Архивная копия от 8 октября 2020 на Wayback Machine
- ↑ Филиппины одобрили вакцину «Спутник V» для экстренного применения. Дата обращения: 19 марта 2021. Архивировано 19 марта 2021 года.
- ↑ На Филиппинах началось применение вакцины «Спутник V». Архивная копия от 4 мая 2021 на Wayback Machine на сайте https://tass.ru/ Архивная копия от 8 октября 2020 на Wayback Machine
- ↑ Камерун зарегистрировал вакцину »Спутник V». ТАСС. Дата обращения: 30 января 2022. Архивировано 27 апреля 2021 года.
- ↑ Вакцину «Спутник V» одобрили на Сейшельских Островах. Дата обращения: 19 марта 2021. Архивировано 19 марта 2021 года.
- ↑ На Сейшельских Островах началась вакцинация »Спутником V». ТАСС. Дата обращения: 30 января 2022. Архивировано 21 июля 2022 года.
- ↑ Маврикий стал 55-й страной, одобрившей вакцину «Спутник V». Дата обращения: 22 марта 2021. Архивировано 22 марта 2021 года.
- ↑ Маврикий открыл внешние границы для зарубежных туристов. Дата обращения: 16 июля 2021. Архивировано 16 июля 2021 года.
- ↑ Вьетнам зарегистрировал вакцину «Спутник V». ТАСС (23 марта 2021). Дата обращения: 7 июня 2021. Архивировано 7 июня 2021 года.
- ↑ СМИ: Вьетнам начал применять «Спутник V» для вакцинации населения от COVID-19. Архивная копия от 17 октября 2021 на Wayback Machine на сайте https://tass.ru/ Архивная копия от 8 октября 2020 на Wayback Machine
- ↑ Вакцина «Спутник V» одобрена в Антигуа и Барбуде. Дата обращения: 26 марта 2021. Архивировано 26 марта 2021 года.
- ↑ «Спутник V» одобрили в Мали. Дата обращения: 30 марта 2021. Архивировано 30 марта 2021 года.
- ↑ РФПИ: Панама одобрила применение вакцины «Спутник V». Дата обращения: 1 апреля 2021. Архивировано 1 апреля 2021 года.
- ↑ Премьер Ливии назвал полученную российскую вакцину «первой каплей дождя». Дата обращения: 29 апреля 2021. Архивировано 29 апреля 2021 года.
- ↑ Первую партию вакцины «Спутник V» доставили в Ливию. Дата обращения: 10 июля 2021. Архивировано 10 июля 2021 года.
- ↑ India approves Russia’s Sputnik V COVID-19 vaccine. Дата обращения: 12 апреля 2021. Архивировано 12 апреля 2021 года.
- ↑ В Индии начали применять «Спутник V». РИА Новости (14 мая 2021). Дата обращения: 14 мая 2021. Архивировано 14 мая 2021 года.
- ↑ Непал одобрил использование «Спутника V». Дата обращения: 21 апреля 2021. Архивировано 21 апреля 2021 года.
- ↑ В Бангладеш одобрили экстренное использование вакцины «Спутник V». Дата обращения: 28 апреля 2021. Архивировано 28 апреля 2021 года.
- ↑ Турция стала 63-й страной, в которой зарегистрирована вакцина «Спутник V». Дата обращения: 13 мая 2021. Архивировано 13 мая 2021 года.
- ↑ В Албании одобрили применение «Спутника V». ТАСС (30 апреля 2021). Дата обращения: 7 июня 2021. Архивировано 1 мая 2021 года.
- ↑ Применение вакцины «Спутник V» одобрено в Республике Мальдивы. Дата обращения: 13 мая 2021. Архивировано 13 мая 2021 года.
- ↑ Применение «Спутника V» одобрили в Эквадоре. ТАСС (15 мая 2021). Дата обращения: 15 мая 2021. Архивировано 15 мая 2021 года.
- ↑ Бразильский фармрегулятор одобрил импорт и применение вакцины «Спутник V». ТАСС (5 июня 2021). Дата обращения: 5 июня 2021. Архивировано 5 июня 2021 года.
- ↑ Применение вакцины «Спутник V» одобрено в Нигерии. Sputnikvaccine.com (15 июля 2021). Дата обращения: 15 июля 2021. Архивировано 15 июля 2021 года.
- ↑ В Чили одобрили экстренное применение вакцины »Спутник V». ТАСС (21 июля 2021). Дата обращения: 21 июля 2021. Архивировано 21 июля 2021 года.
- ↑ Indonesia approves Russia’s Sputnik V vaccine for emergency use. Reuters (25 августа 2021). Дата обращения: 25 августа 2021. Архивировано 25 августа 2021 года.
- ↑ «Спутник V» и »Спутник Лайт» одобрили в Камбодже. ТАСС. Дата обращения: 30 января 2022. Архивировано 3 ноября 2021 года.
- ↑ Австралия разрешила въезд привитым «Спутником V». Meduza (17 января 2022). Дата обращения: 7 февраля 2022. Архивировано 7 февраля 2022 года.
- ↑ TGA recognises the Gamaleya Institute vaccine (Sputnik V, Russian Federation) for international travel to Australia. TGA (17 января 2022). Дата обращения: 7 февраля 2022. Архивировано 7 февраля 2022 года.
- ↑ COVID-19 vaccines recognised by Australia. TGA (17 января 2022). Дата обращения: 7 февраля 2022. Архивировано 7 февраля 2022 года.
- ↑ В ДНР началась вакцинация от коронавируса. РИА Новости (1 февраля 2021). Дата обращения: 30 января 2022. Архивировано 25 мая 2021 года.
- ↑ В ЛНР начнется вакцинация от коронавируса «Спутником V». Дата обращения: 1 февраля 2021. Архивировано 1 февраля 2021 года.
- ↑ В Южной Осетии началась вакцинация от коронавируса «Спутником V». РИА Новости (4 мая 2021). Дата обращения: 16 мая 2021. Архивировано 16 мая 2021 года.
- ↑ Вакцинация от коронавирусной инфекции в Абхазии началась. sputnik-abkhazia (12 мая 2021). Дата обращения: 17 мая 2021. Архивировано 13 мая 2021 года.
- ↑ Comenzó la campaña de vacunación contra COVID-19 en Argentina. Архивная копия от 27 января 2021 на Wayback Machine // «Argentina Unida», 29.12.2020
- ↑ آغاز واکسیناسیون سراسری علیه بیماری کووید۱۹. Архивная копия от 15 февраля 2021 на Wayback Machine // Фоторепортаж в «Mehr News Agency».
- ↑ Изображение флакона с вакциной на начале вакцинации в Иране. Архивная копия от 15 февраля 2021 на Wayback Machine // Фоторепортаж в «Mehr News Agency».
- ↑ واکسیناسیون کووید ۱۹ در یزد // Фоторепортаж в «Mehr News Agency».
- ↑ В Эстонии признали российские вакцины, получившие разрешение на продажу - Газета.Ru | Новости. Газета.Ru. Дата обращения: 16 сентября 2021. Архивировано 16 сентября 2021 года.
- ↑ Посол России рассказал о признании российской вакцины на Олимпиаде в Пекине. Lenta.RU. Дата обращения: 25 января 2022. Архивировано 25 января 2022 года.
- ↑ США введут санкции против двух НИИ Минобороны России. РБК (26 августа 2020). Дата обращения: 27 июня 2021. Архивировано 27 августа 2020 года.
- ↑ Cattivi Scienziati, fighting bad and pseudo-science. Архивная копия от 17 сентября 2020 на Wayback Machine, 07.09.2020.
- ↑ 1 2 Учёные попросили объяснить «странности» в статье о российской вакцине от COVID-19. N+1. Дата обращения: 10 сентября 2020. Архивировано 26 сентября 2020 года.
- ↑ Polina Ivanova. Some scientists spot ’unlikely’ patterns in Russia vaccine data: letter (англ.). Reuters (9 сентября 2020). Дата обращения: 9 сентября 2020. Архивировано 9 сентября 2020 года.
- ↑ Holly Ellyatt. Scientists question ‘strange’ data in Russian coronavirus vaccine trial after ‘unlikely’ patterns (англ.). CNBC (10 сентября 2020). Дата обращения: 10 сентября 2020. Архивировано 29 марта 2021 года.
- ↑ Johanna Kuroczik. Der neue Sputnikschock (нем.). FAZ (13 сентября 2020). Дата обращения: 13 сентября 2020. Архивировано 15 сентября 2020 года.
- ↑ Neue Zweifel an russischem Corona-Impfstoff (нем.). Süddeutsche Zeitung (16 сентября 2020). Дата обращения: 16 сентября 2020. Архивировано 17 сентября 2020 года.
- ↑ Denis Y. Logunov, Inna V. Dolzhikova, Amir I. Tukhvatullin, Dmitry V. Shcheblyakov. Safety and efficacy of the Russian COVID-19 vaccine: more information needed – Authors’ reply (англ.) // The Lancet. — 2020-10-03. — Т. 396, вып. 10256. — С. e54–e55. — ISSN 1474-547X 0140-6736, 1474-547X. — doi:10.1016/S0140-6736(20)31970-X.
- ↑ «Данные проверены дважды»: The Lancet опубликовал ответ российских учёных на критику их вакцины от COVID-19. Forbes.ru. Дата обращения: 30 сентября 2020. Архивировано 26 сентября 2020 года.
- ↑ Enrico M. Bucci. Data discrepancies and substandard reporting of interim data of Sputnik V phase 3 trial (англ.). The Lancet (12 мая 2021). Дата обращения: 25 декабря 2021. Архивировано 18 мая 2021 года.
- ↑ Denis Y. Logunov, Inna V. Dolzhikova, Dmitry V. Shcheblyakov. Data discrepancies and substandard reporting of interim data of Sputnik V phase 3 trial – Authors’ reply (англ.) // The Lancet. — 2021-05-22. — Т. 397, вып. 10288. — С. 1883–1884. — ISSN 1474-547X 0140-6736, 1474-547X. — doi:10.1016/S0140-6736(21)00894-1.
- ↑ Врач назвал дискредитацию »Спутника V» элементом информационной войны. РИА Новости (11 декабря 2020). Дата обращения: 11 декабря 2020. Архивировано 11 декабря 2020 года.
- ↑ Вторая страна ЕС одобрила использование российской вакцины «Спутник V». РБК (1 марта 2021). Дата обращения: 1 марта 2021. Архивировано 1 марта 2021 года.
- ↑ Минздрав Словакии разрешил использовать в стране вакцину »Спутник V». ТАСС (2 марта 2021). Дата обращения: 21 июня 2021. Архивировано 24 июня 2021 года.
- ↑ Президент Словакии выразила недовольство приобретением российской вакцины от коронавируса. ТАСС (2 марта 2021). Дата обращения: 21 июня 2021. Архивировано 24 июня 2021 года.
- ↑ СМИ: покупка российской вакцины привела к разногласиям в правительстве Словакии. ТАСС (2 марта 2021). Дата обращения: 21 июня 2021. Архивировано 24 июня 2021 года.
- ↑ СМИ: глава Минздрава Словакии оставил пост ради сохранения правительственной коалиции. ТАСС (12 марта 2021). Дата обращения: 21 июня 2021. Архивировано 24 июня 2021 года.
- ↑ Министр труда Словакии подал в отставку в связи правительственным кризисом. ТАСС (15 марта 2021). Дата обращения: 21 июня 2021. Архивировано 24 июня 2021 года.
- ↑ Министр экономики Словакии объявил об отставке. ТАСС (17 марта 2021). Дата обращения: 21 июня 2021. Архивировано 24 июня 2021 года.
- ↑ СМИ: министры иностранных дел и образования Словакии подали в отставку. ТАСС (24 марта 2021). Дата обращения: 21 июня 2021. Архивировано 15 мая 2021 года.
- ↑ Президент Словакии приняла отставку премьер-министра Игора Матовича. ТАСС (30 марта 2021). Дата обращения: 21 июня 2021. Архивировано 24 июня 2021 года.
- ↑ Veronika Folentová. Sputnik V u nás nie je identický s tým v Lancete. Štátny ústav nemá dosť informácií na to, aby odporučil očkovanie (словацк.). dennikn.sk (6 апреля 2021). Дата обращения: 6 апреля 2021. Архивировано 7 апреля 2021 года.
- ↑ Словакия обвинила Россию в поставках «Спутника», который отличается от описанного в журнале The Lancet. РФПИ потребовал вернуть вакцину. Meduza (8 апреля 2021). Дата обращения: 21 июня 2021. Архивировано 19 июня 2021 года.
- ↑ Sputnik V. Thread (англ.). Twitter (7 апреля 2021). Дата обращения: 20 июня 2021. Архивировано 14 июня 2021 года.
- ↑ Sputnik V. Thread (англ.). Twitter (8 апреля 2021). Дата обращения: 20 июня 2021. Архивировано 22 июня 2021 года.
- ↑ Президент Словакии потребовала обнародовать договор о покупке «Спутника V». ТАСС (15 апреля 2021).
- ↑ Российская сторона не против публикации договора о поставке «Спутника V» в Словакию. ТАСС (24 апреля 2021). Дата обращения: 21 июня 2021. Архивировано 24 апреля 2021 года.
- ↑ Словакия опубликовала договор о покупке вакцины «Спутник V». ТАСС (29 апреля 2021). Дата обращения: 21 июня 2021. Архивировано 30 апреля 2021 года.
- ↑ Supply Agreement Nr.964/2021 (англ.). Central register of contracts. Дата обращения: 21 июня 2021. Архивировано 20 июня 2021 года.
- ↑ Венгерская лаборатория подтвердила надежность «Спутника V», поступившего в Словакию. ТАСС (7 мая 2021). Дата обращения: 21 июня 2021. Архивировано 10 мая 2021 года.
- ↑ В Словакии начинается применение «Спутника V». ТАСС (6 мая 2021). Дата обращения: 7 июня 2021. Архивировано 7 июня 2021 года.
- ↑ США признали попытки принудить Бразилию отказаться от «Спутника V». РБК (16 марта 2021). Дата обращения: 20 июня 2021. Архивировано 27 июня 2021 года.
- ↑ Sputnik V. Tread. Twitter (15 марта 2021). Дата обращения: 27 июня 2021. Архивировано 27 июня 2021 года.
- ↑ Anvisa não aprova importação da vacina Sputnik V (порт.). Ministério da Saúde (26 апреля 2021). Дата обращения: 23 июня 2021. Архивировано 14 июня 2021 года.
- ↑ Бразильский регулятор не разрешил ввоз »Спутника V». ТАСС (27 апреля 2021). Дата обращения: 23 июня 2021. Архивировано 24 июня 2021 года.
- ↑ Центр им. Гамалеи отверг претензии Бразилии к «Спутнику V». Интерфакс (28 апреля 2021). Дата обращения: 20 июня 2021. Архивировано 21 июня 2021 года.
- ↑ Sputnik V Statement on Brazilian health regulator Anvisa’s decision to postpone Sputnik V authorization in Brazil: (англ.). Sputnik V (28 апреля 2021). Дата обращения: 20 июня 2021. Архивировано 19 июня 2021 года.
- ↑ Anvisa aprova, com restrições, importação excepcional de doses da Covaxin e Sputnik V (порт.). Globo.com (4 июня 2021). Дата обращения: 20 июня 2021. Архивировано 18 июня 2021 года.
- ↑ Бразильский фармрегулятор одобрил импорт и применение вакцины »Спутник V». ТАСС (5 июня 2021). Дата обращения: 5 июня 2021. Архивировано 5 июня 2021 года.
- ↑ Coronavirus (COVID-19) and the global trade in fake pharmaceuticals (англ.). OECD.org. Дата обращения: 2 апреля 2021. Архивировано 23 марта 2021 года.
- ↑ Scammers Are Setting Up Fake Covid Vaccine Websites. Wall Street Journal. Дата обращения: 2 апреля 2021. Архивировано 31 марта 2021 года.
- ↑ Nigeria warns of reported fake COVID-19 vaccines (англ.). Anadolu Agency (16 января 2021). Дата обращения: 2 апреля 2021. Архивировано 30 января 2021 года.
- ↑ Fake coronavirus vaccine seizures in several countries are ‘tip of the iceberg,’ Interpol warns (англ.). The Washington Post. Дата обращения: 2 апреля 2021.
- ↑ Мексиканские наркобароны занялись подделкой вакцин. Вести.ру. Дата обращения: 2 апреля 2021.
- ↑ Власти Мексики изъяли партию поддельной вакцины «Спутник V». Архивная копия от 20 марта 2021 на Wayback Machine. РБК, 18.03.2021
- ↑ Aduanas y Ejército Mexicano decomisan vacunas SPUTNIK V en aeronave privada en la Aduana de Campeche. Архивная копия от 18 марта 2021 на Wayback Machine. — Servicio de Administración Tributaria.
- ↑ В Мексике изъяли партию поддельного «Спутника V». Коммерсантъ (18 марта 2021). Дата обращения: 18 марта 2021. Архивировано 18 марта 2021 года.
- ↑ Названы основные способы мошенничества с вакцинацией. Московский комсомолец (13 марта 2021). Дата обращения: 9 апреля 2021. Архивировано 20 марта 2021 года.
- ↑ Ада Горбачева. Как мошенники на Западе предлагают вакцины в Сети. Российская газета (5 января 2021). Дата обращения: 9 апреля 2021. Архивировано 18 января 2021 года.
- ↑ Ада Горбачева. Поддельные справки и поддельные вакцины. Купить в интернете можно все, кроме здоровья и гарантий безопасности. Независимая газета (6 апреля 2021). Дата обращения: 5 мая 2021. Архивировано 17 апреля 2021 года.
- ↑ Sputnik vaccine businessman bought for his employees turns out to be fake (англ.). Mexico News Daily. Дата обращения: 9 апреля 2021. Архивировано 20 апреля 2021 года.
- ↑ Fake Russian vaccines officially hit the scene (англ.). Putman Media. Дата обращения: 9 апреля 2021. Архивировано 21 марта 2021 года.
- ↑ Stone, J. How Counterfeit Covid-19 Vaccines And Vaccination Cards Endanger Us All : [англ.] : [арх. 8 апреля 2021] // Forbes. — 2021. — 31 March.
Литература
- Marco Montalti, Giorgia Soldà, Zeno Di Valerio, Aurelia Salussolia, Jacopo Lenzi. ROCCA observational study: Early results on safety of Sputnik V vaccine (Gam-COVID-Vac) in the Republic of San Marino using active surveillance (англ.) // EClinicalMedicine. — 2021. — August (vol. 38). — P. 101027. — doi:10.1016/j.eclinm.2021.101027.
- Vanina Pagotto, Analia Ferloni, María Mercedes Soriano, Morena Díaz, Nahuel Braguinsky Golde. Active monitoring of early safety of Sputnik V vaccine in Buenos Aires, Argentina // Medicina. — 2021. — Т. 81, вып. 3. — С. 408–414. — ISSN 1669-9106.
- Вакцина «Спутник V» вызывает сероконверсию и приобретение нейтрализующей активности против SARS-CoV-2 после первой дозы. medach.pro. Дата обращения: 30 января 2022.
- Andres H. Rossi, Diego S. Ojeda, Augusto Varese, Lautaro Sanchez, Maria M. Gonzalez Lopez Ledesma. Sputnik V vaccine elicits seroconversion and neutralizing capacity to SARS-CoV-2 after a single dose (англ.) // Cell Reports Medicine. — 2021-08. — Vol. 2, iss. 8. — P. 100359. — doi:10.1016/j.xcrm.2021.100359.
Ссылки
- Действующая (со всеми внесёнными изменениями по состоянию на 28.12.2020) инструкция к вакцине «Гам-КОВИД-Вак» — документ на официальном сайте Росздравнадзора.
- Спутник V. sputnikvaccine.com. Российский фонд прямых инвестиций. — сайт, посвящённый вакцине.
- Наталья Телегина, Елена Виноградова. Эликсир молодости, нановакцины и «Кагоцел»: над чем прежде работали учёные, создавшие для Путина «Спутник V», Открытые Медиа (8 октября 2020).
Неудобные вопросы о всеобщей вакцинации. Интервью Youtube-канала «Редакция» с медиками с ответами на частые вопросы о вакцине «Спутник V», 15.07.2021 (1 час 30 минут).
Эта страница в последний раз была отредактирована 20 февраля 2023 в 18:40.
Как только страница обновилась в Википедии она обновляется в Вики 2.
Обычно почти сразу, изредка в течении часа.

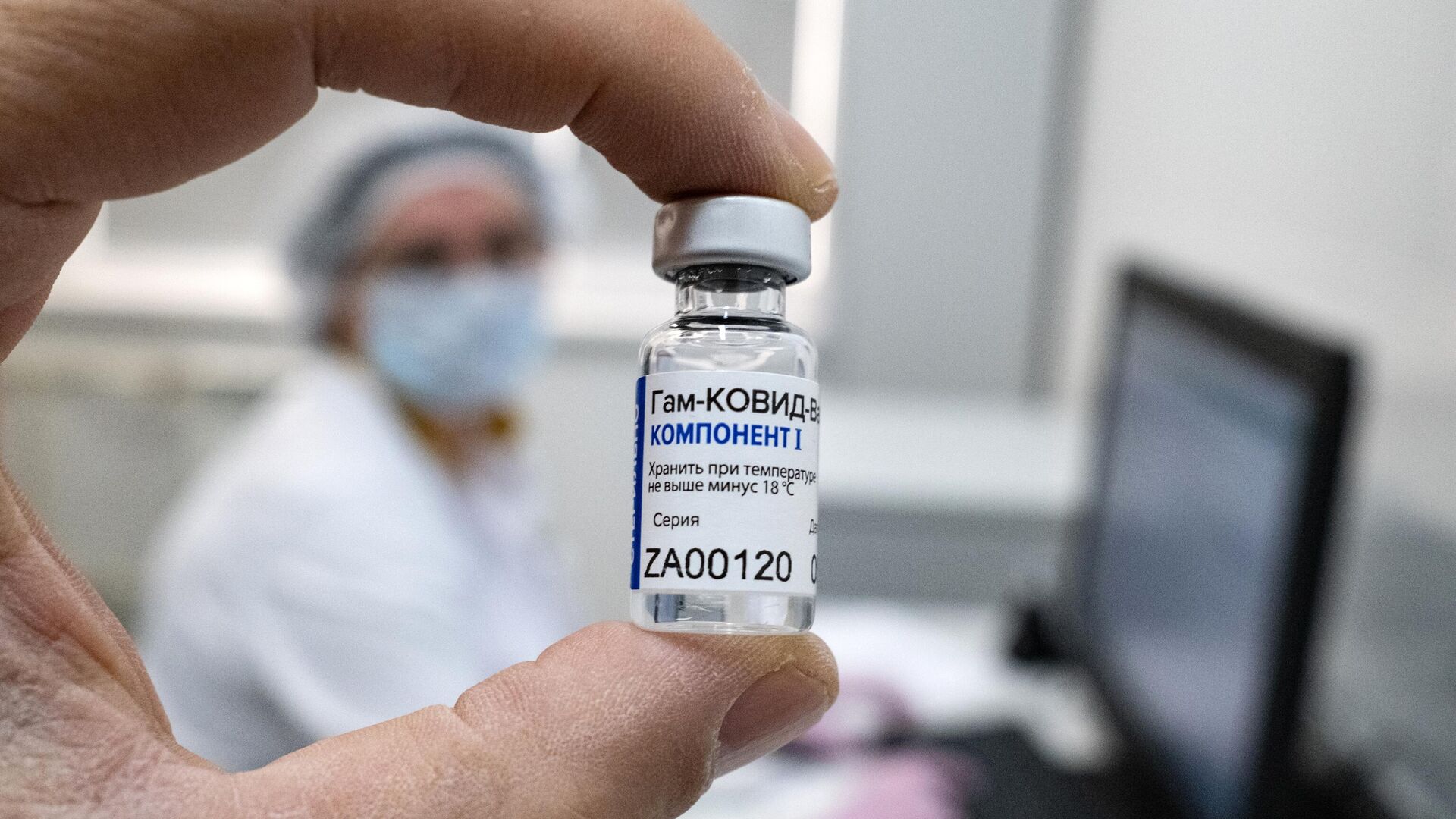
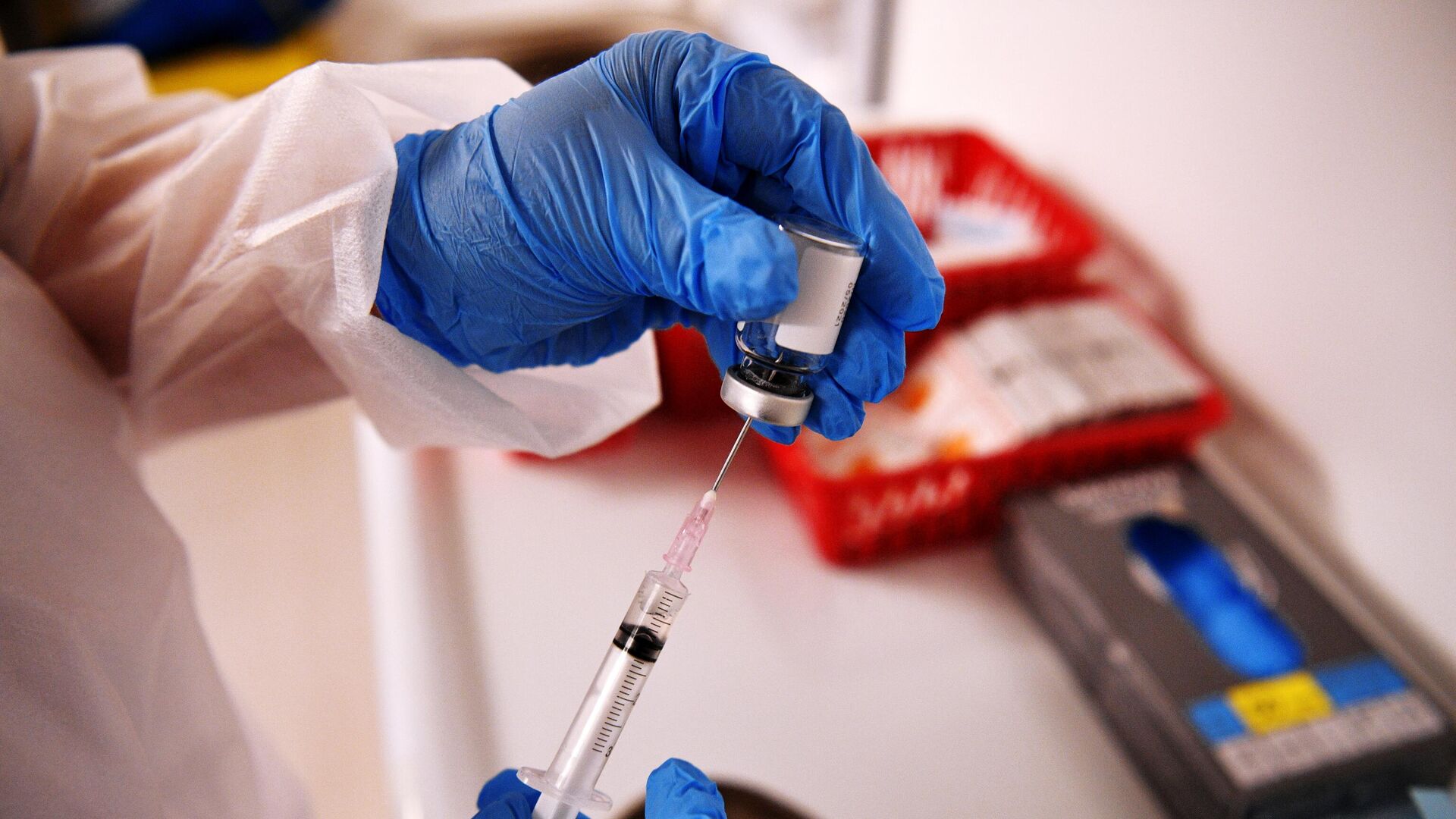
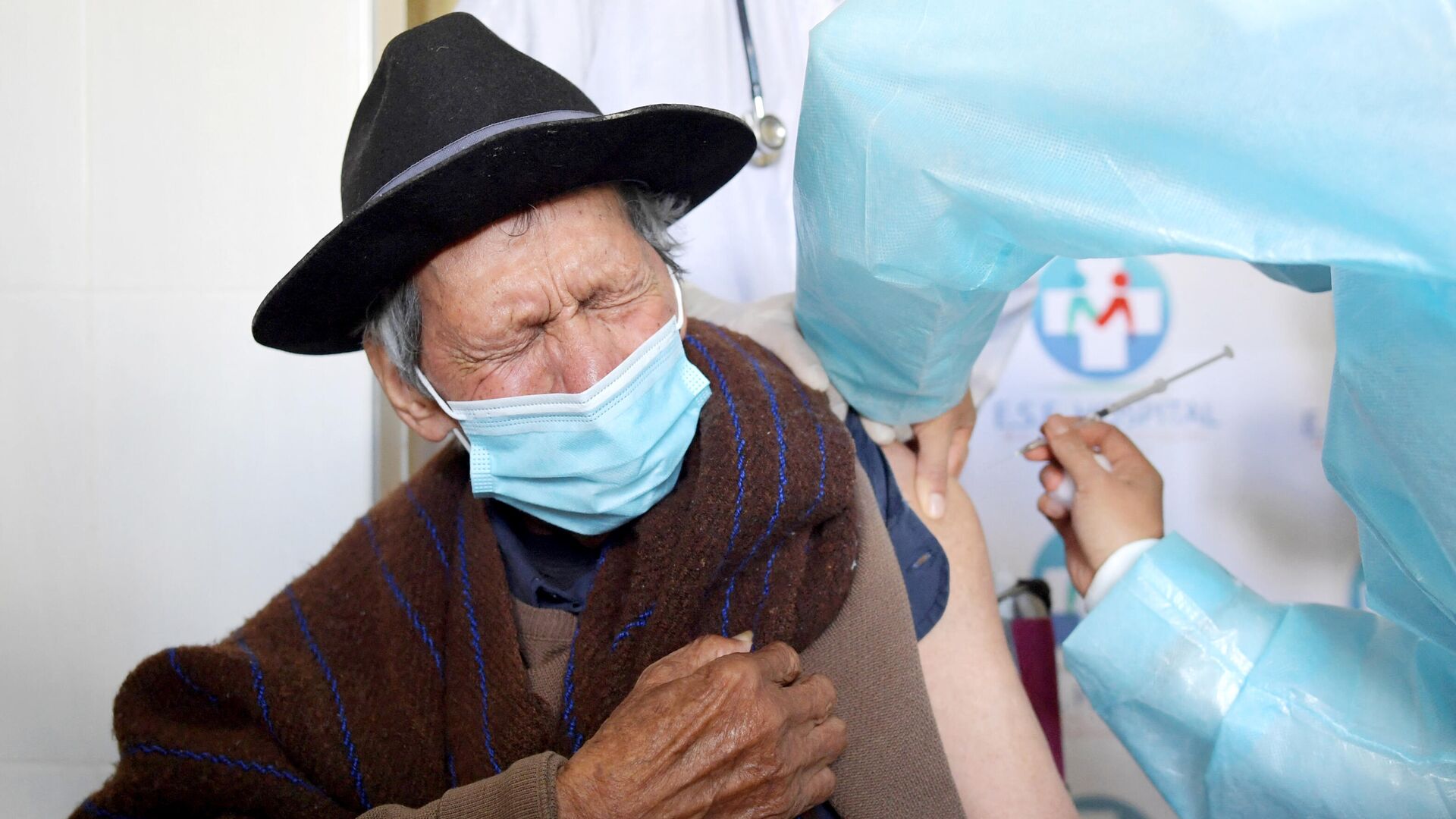
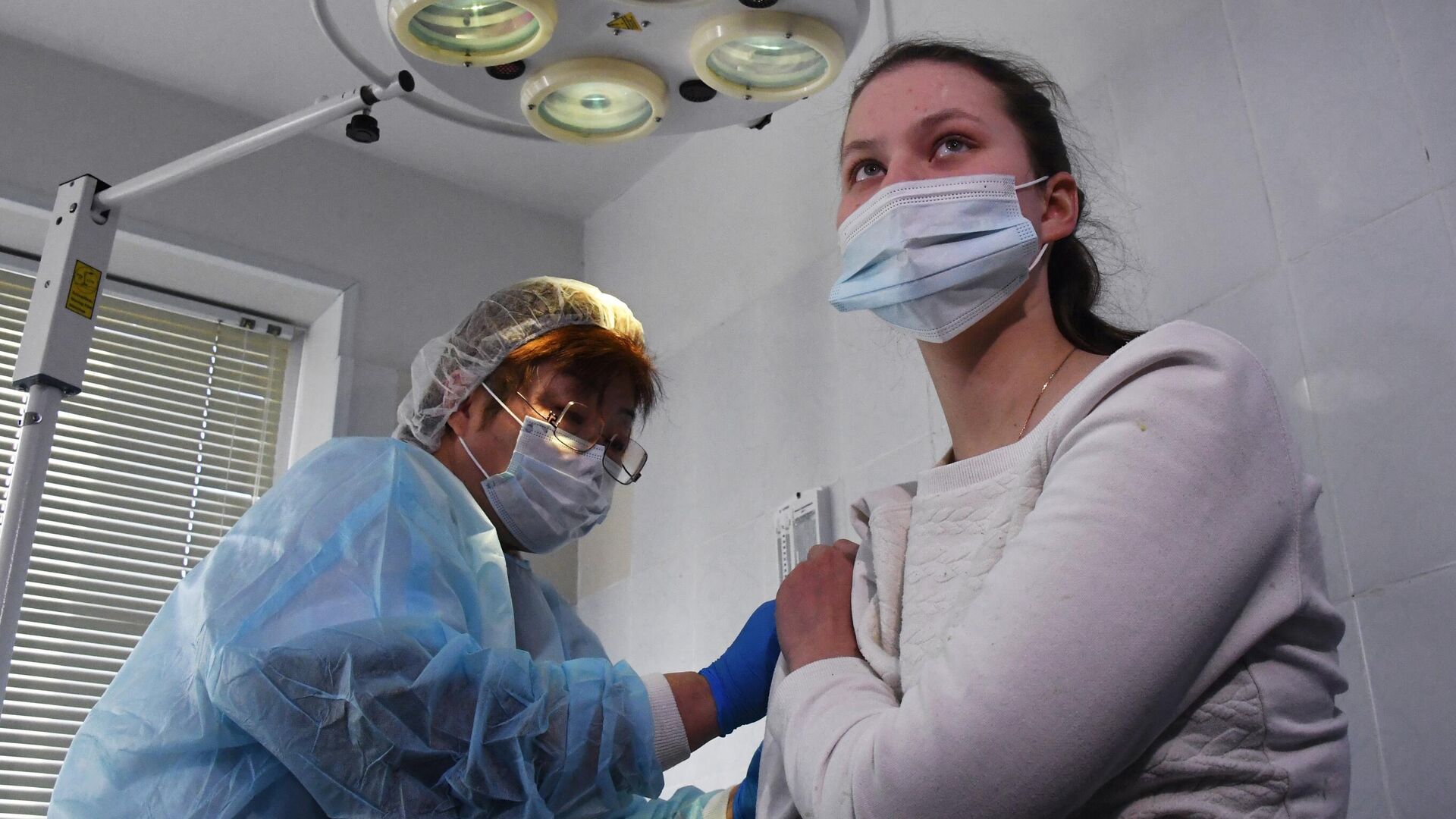
![5-дозовый флакон (3 мл) с I компонентом вакцины Гам-КОВИД-Вак производства «BIOCAD» в руках аргентинского медработника в больнице Posadas Hospital в Эль-Паломаре[es] провинции Буэнос-Айрес[381]](https://wiki2.org/wikipedia/commons/thumb/a/a7/Comenz%C3%B3_la_campa%C3%B1a_de_vacunaci%C3%B3n_contra_COVID-19_en_Argentina.jpg/im244-320px-Comenz%C3%B3_la_campa%C3%B1a_de_vacunaci%C3%B3n_contra_COVID-19_en_Argentina.jpg)
![Торжественное открытие вакцинации в Иране 12 февраля 2021 года в больнице им. имама Хомейни (перс. بیمارستان امام خمینی), вакцина Гам-КОВИД-Вак производства ЗАО «Лекко»[382][383]](https://wiki2.org/wikipedia/commons/thumb/e/e9/3686979_%D8%A2%D8%BA%D8%A7%D8%B2_%D9%88%D8%A7%DA%A9%D8%B3%DB%8C%D9%86%D8%A7%D8%B3%DB%8C%D9%88%D9%86_%D8%B3%D8%B1%D8%A7%D8%B3%D8%B1%DB%8C_%D8%B9%D9%84%DB%8C%D9%87_%D8%A8%DB%8C%D9%85%D8%A7%D8%B1%DB%8C_%DA%A9%D9%88%D9%88%DB%8C%D8%AF%DB%B1%DB%B9.jpg/im244-320px-3686979_%D8%A2%D8%BA%D8%A7%D8%B2_%D9%88%D8%A7%DA%A9%D8%B3%DB%8C%D9%86%D8%A7%D8%B3%DB%8C%D9%88%D9%86_%D8%B3%D8%B1%D8%A7%D8%B3%D8%B1%DB%8C_%D8%B9%D9%84%DB%8C%D9%87_%D8%A8%DB%8C%D9%85%D8%A7%D8%B1%DB%8C_%DA%A9%D9%88%D9%88%DB%8C%D8%AF%DB%B1%DB%B9.jpg)
![Флакон с I компонентом вакцины Гам-КОВИД-Вак в руках иранского медработника во время вакцинации в больнице им. шахида Садуги (перс. بیمارستان شهید صدوقی) в Йезде[384]](https://wiki2.org/wikipedia/commons/thumb/9/9c/3686878_%D9%88%D8%A7%DA%A9%D8%B3%DB%8C%D9%86%D8%A7%D8%B3%DB%8C%D9%88%D9%86_%DA%A9%D9%88%D9%88%DB%8C%D8%AF_%DB%B1%DB%B9_%D8%AF%D8%B1_%DB%8C%D8%B2%D8%AF.jpg/im244-320px-3686878_%D9%88%D8%A7%DA%A9%D8%B3%DB%8C%D9%86%D8%A7%D8%B3%DB%8C%D9%88%D9%86_%DA%A9%D9%88%D9%88%DB%8C%D8%AF_%DB%B1%DB%B9_%D8%AF%D8%B1_%DB%8C%D8%B2%D8%AF.jpg)
