| Кальций | |
|---|---|
| Умеренно твёрдый, серебристо-белый металл | |

Кальций в атмосфере аргона |
|
| Название, символ, номер | Кальций/Calcium (Ca), 20 |
| Атомная масса (молярная масса) |
40,078(4) а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 4s2 |
| Радиус атома | 197 пм |
| Ковалентный радиус | 174 пм |
| Радиус иона | (+2e) 99 пм |
| Электроотрицательность | 1,00 (шкала Полинга) |
| Электродный потенциал | −2,76 В |
| Степени окисления | 2 |
| Энергия ионизации (первый электрон) |
589,4 (6,11) кДж/моль (эВ) |
| Плотность (при н. у.) | 1,55 г/см³ |
| Температура плавления | 1112 К; 838,85 °C |
| Температура кипения | 1757 К; 1483,85 °C |
| Уд. теплота плавления | 9,20 кДж/моль |
| Уд. теплота испарения | 153,6 кДж/моль |
| Молярная теплоёмкость | 25,9 Дж/(K·моль) |
| Молярный объём | 29,9 см³/моль |
| Структура решётки | кубическая гранецентрированная |
| Параметры решётки | 5,580 Å |
| Температура Дебая | 230 K |
| Теплопроводность | (300 K) (201) Вт/(м·К) |
| Номер CAS | 7440-70-2 |
Кальций (Ca от лат. Calcium) — элемент второй группы (по старой классификации — главной подгруппы второй группы), четвёртого периода, с атомным номером 20. Простое вещество кальций — мягкий, химически активный щёлочноземельный металл серебристо-белого цвета. Впервые получен в чистом виде Г. Дэви в 1808 году.
Содержание
- 1 История и происхождение названия
- 2 Нахождение в природе
- 2.1 Изотопы
- 2.2 В горных породах и минералах
- 2.3 Миграция в земной коре
- 2.4 В биосфере
- 3 Получение
- 4 Физические свойства
- 5 Химические свойства
- 6 Применение
- 7 Биологическая роль
История и происхождение названия
Название элемента происходит от лат. calx (в родительном падеже calcis) — «известь», «мягкий камень». Оно было предложено английским химиком Гемфри Дэви, в 1808 г. выделившим металлический кальций электролитическим методом. Дэви подверг электролизу смесь влажной гашёной извести с оксидом ртути HgO на платиновой пластине, которая являлась анодом. Катодом служила платиновая проволока, погруженная в жидкую ртуть. В результате электролиза получалась амальгама кальция. Отогнав из неё ртуть, Дэви получил металл, названный кальцием.
Соединения кальция — известняк, мрамор, гипс (а также известь — продукт обжига известняка) применялись в строительном деле уже несколько тысячелетий назад. Вплоть до конца XVIII века химики считали известь простым телом. В 1789 году А. Лавуазье предположил, что известь, магнезия, барит, глинозём и кремнезём — вещества сложные.
Нахождение в природе
Из-за высокой химической активности кальций в свободном виде в природе не встречается.
На долю кальция приходится 3,38 % массы земной коры (5-е место по распространенности (3-е среди металлов) после кислорода, кремния, алюминия и железа). Содержание элемента в морской воде — 400 мг/л.
Изотопы
Основная статья: Изотопы кальция
Кальций встречается в природе в виде смеси шести изотопов: 40Ca, 42Ca, 43Ca, 44Ca, 46Ca и 48Ca, среди которых наиболее распространённый — 40Ca — составляет 96,97 %. Ядра кальция содержат магическое число протонов: Z = 20. Изотопы 40
20Ca20
и 48
20Ca28
являются двумя из пяти существующих в природе дважды магических ядер.
Из шести природных изотопов кальция пять стабильны. Шестой изотоп 48Ca, самый тяжёлый из шести и весьма редкий (его изотопная распространённость равна всего 0,187 %), испытывает двойной бета-распад с периодом полураспада (4,39 ± 0,58)⋅1019 лет.
В горных породах и минералах
Кальций, энергично мигрирующий в земной коре и накапливающийся в различных геохимических системах, образует 385 минералов (четвёртое место по числу минералов).
Большая часть кальция содержится в составе силикатов и алюмосиликатов различных горных пород (граниты, гнейсы и т. п.), особенно в полевом шпате — анортите Ca[Al2Si2O8].
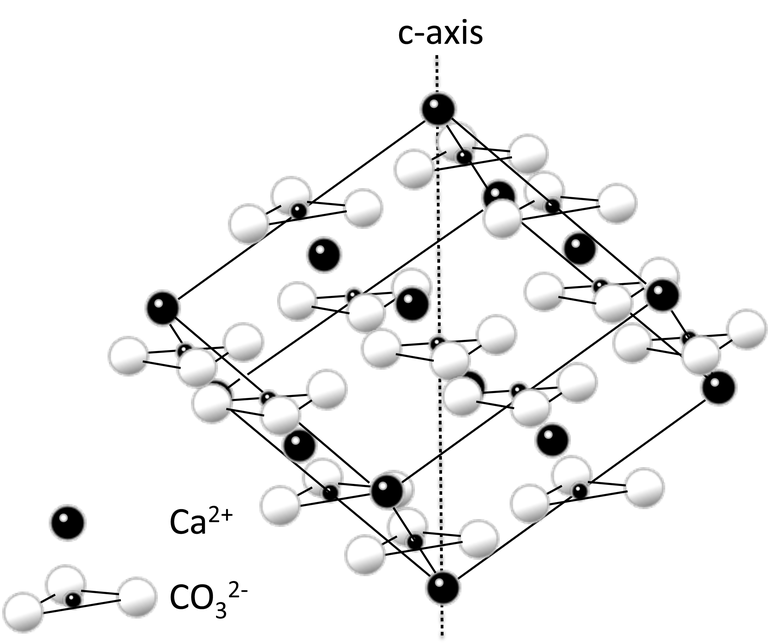
Довольно широко распространены такие минералы кальция, как кальцит CaCO3, ангидрит CaSO4, алебастр CaSO4·0.5H2O и гипс CaSO4·2H2O, флюорит CaF2, апатиты Ca5(PO4)3(F,Cl,OH), доломит MgCO3·CaCO3. Присутствием солей кальция и магния в природной воде определяется её жёсткость.
Осадочная порода, состоящая в основном из скрытокристаллического кальцита — известняк (одна из его разновидностей — мел). Под действием регионального метаморфизма известняк преобразуется в мрамор.
Миграция в земной коре
В естественной миграции кальция существенную роль играет «карбонатное равновесие», связанное с обратимой реакцией взаимодействия карбоната кальция с водой и углекислым газом с образованием растворимого гидрокарбоната:
-
- CaCO3 + H2O + CO2 ⇄ Ca(HCO3)2 ⇄ Ca2+ + 2HCO3−
(равновесие смещается влево или вправо в зависимости от концентрации углекислого газа).
Огромную роль играет биогенная миграция.
В биосфере
Соединения кальция находятся практически во всех животных и растительных тканях (см. ниже). Значительное количество кальция входит в состав живых организмов. Так, гидроксиапатит Ca5(PO4)3OH, или, в другой записи, 3Ca3(PO4)2·Ca(OH)2 — основа костной ткани позвоночных, в том числе и человека; из карбоната кальция CaCO3 состоят раковины и панцири многих беспозвоночных, яичная скорлупа и др. В живых тканях человека и животных 1,4—2 % Ca (по массовой доле); в теле человека массой 70 кг содержание кальция — около 1,7 кг (в основном в составе межклеточного вещества костной ткани).
Получение
Свободный металлический кальций получают электролизом расплава, состоящего из CaCl2 (75—80 %) и KCl или из CaCl2 и CaF2, а также алюминотермическим восстановлением CaO при 1170—1200 °C 4CaO + 2Al → CaAl2O4 + 3Ca
Физические свойства
Металл кальций существует в двух аллотропных модификациях. До 443 °C устойчив α-Ca с кубической гранецентрированной решеткой (параметр а = 0,558 нм), выше устойчив β-Ca с кубической объемно-центрированной решеткой типа α-Fe (параметр a = 0,448 нм). Стандартная энтальпия ΔH0 перехода α → β составляет 0,93 кДж/моль.
При постепенном повышении давления начинает проявлять свойства полупроводника, но не становится полупроводником в полном смысле этого слова (металлом уже тоже не является). При дальнейшем повышении давления возвращается в металлическое состояние и начинает проявлять сверхпроводящие свойства (температура сверхпроводимости в шесть раз выше, чем у ртути, и намного превосходит по проводимости все остальные элементы). Уникальное поведение кальция похоже во многом на стронций (то есть параллели в периодической системе сохраняются).
Химические свойства
Кальций — типичный щёлочноземельный металл. Химическая активность кальция высока, но ниже, чем более тяжёлых щёлочноземельных металлов. Он легко взаимодействует с кислородом, углекислым газом и влагой воздуха, из-за чего поверхность металлического кальция обычно тускло-серая, поэтому в лаборатории кальций обычно хранят, как и другие щёлочноземельные металлы, в плотно закрытой банке под слоем керосина или жидкого парафина.
В ряду стандартных потенциалов кальций расположен слева от водорода. Стандартный электродный потенциал пары Ca2+/Ca0 −2,84 В, так что кальций активно реагирует с водой, но без воспламенения:
-
- Ca + 2H2O → Ca(OH)2 + H2↑
С активными неметаллами (кислородом, хлором, бромом, йодом) кальций реагирует при обычных условиях:
-
- 2Ca + O2 → 2CaO
-
- Ca + Br2 → CaBr2
При нагревании на воздухе или в кислороде кальций воспламеняется и горит красным пламенем с оранжевым оттенком («кирпично-красным»). С менее активными неметаллами (водородом, бором, углеродом, кремнием, азотом, фосфором и другими) кальций вступает во взаимодействие при нагревании, например:
-
- Ca + H2 → CaH2
-
- Ca + 6B → CaB6
-
- 3Ca + N2 → Ca3N2
-
- Ca + 2C → CaC2
-
- 6Ca + P4 → 2Ca3P2
-
- 2Ca + Si → Ca2Si
Кроме получающихся в этих реакциях фосфида кальция Ca3P2 и силицида кальция Ca2Si, известны также фосфиды кальция составов CaP и CaP5 и силициды кальция составов CaSi, Ca3Si4 и CaSi2.
Протекание указанных выше реакций, как правило, сопровождается выделением большого количества теплоты. Во всех соединениях с неметаллами степень окисления кальция +2. Большинство из соединений кальция с неметаллами легко разлагается водой, например:
-
- CaH2 + 2H2O → Ca(OH)2 + 2H2↑
-
- Ca3N2 + 6H2O → 3Ca(OH)2 + 2NH3↑
Ион Ca2+ бесцветен. При внесении в пламя растворимых солей кальция пламя окрашивается в кирпично-красный цвет.
Такие соли кальция, как хлорид CaCl2, бромид CaBr2, йодид CaI2 и нитрат Ca(NO3)2, хорошо растворимы в воде. Нерастворимы в воде фторид CaF2, карбонат CaCO3, сульфат CaSO4, ортофосфат Ca3(PO4)2, оксалат CaC2O4 и некоторые другие.
Важное значение имеет то обстоятельство, что, в отличие от карбоната кальция CaCO3, кислый карбонат кальция (гидрокарбонат) Ca(HCO3)2 в воде растворим. В природе это приводит к следующим процессам. Когда холодная дождевая или речная вода, насыщенная углекислым газом, проникает под землю и попадает на известняки, то наблюдается их растворение, а в тех местах, где вода, насыщенная гидрокарбонатом кальция, выходит на поверхность земли и нагревается солнечными лучами, протекает обратная реакция
-
- CaCO3 + CO2 + H2O ⇄ Ca(HCO3)2
Так в природе происходит перенос больших масс веществ. В результате под землёй могут образоваться огромные карстовые полости и провалы, а в пещерах образуются красивые каменные «сосульки» — сталактиты и сталагмиты.
Наличие в воде растворенного гидрокарбоната кальция во многом определяет вре́менную жёсткость воды. Вре́менной её называют потому, что при кипячении воды гидрокарбонат разлагается, и в осадок выпадает CaCO3. Это явление приводит, например, к тому, что в чайнике со временем образуется накипь.
Применение
Главное применение металлического кальция — это использование его как восстановителя при получении металлов, особенно никеля, меди и нержавеющей стали. Кальций и его гидрид используются также для получения трудно восстанавливаемых металлов, таких, как хром, торий и уран. Сплавы кальция со свинцом применяются в некоторых видах аккумуляторных батарей и при производстве подшипников. Кальциевые гранулы используются также для удаления следов воздуха из электровакуумных приборов. Чистый металлический кальций широко применяется в металлотермии при получении редкоземельных элементов.
Кальций широко применяется в металлургии для раскисления стали наряду с алюминием или в сочетании с ним. Внепечная обработка кальцийсодержащими проволоками занимает ведущее положение в связи с многофакторностью влияния кальция на физико-химическое состояние расплава, макро- и микроструктуры металла, качество и свойства металлопродукции и является неотъемлемой частью технологии производства стали. В современной металлургии для ввода в расплав кальция используется инжекционная проволока, представляющая из себя кальций (иногда силикокальций или алюмокальций) в виде порошка или прессованного металла в стальной оболочке. Наряду с раскислением (удалением растворенного в стали кислорода) использование кальция позволяет получить благоприятные по природе, составу и форме неметаллические включения, не разрушающиеся в ходе дальнейших технологических операций.
Изотоп 48Ca — один из эффективных и употребительных материалов для производства сверхтяжёлых элементов и открытия новых элементов таблицы Менделеева. Это связано с тем, что кальций-48 является дважды магическим ядром, поэтому его устойчивость позволяет ему быть достаточно нейтроноизбыточным для лёгкого ядра; при синтезе сверхтяжёлых ядер необходим избыток нейтронов.
Биологическая роль
Основная статья: Кальций в живых организмах
Кальций — распространённый макроэлемент в организме растений, животных и человека. В организме человека и других позвоночных большая его часть находится в скелете и зубах. В костях кальций содержится в виде гидроксиапатита. Из различных форм карбоната кальция (извести) состоят «скелеты» большинства групп беспозвоночных (губки, коралловые полипы, моллюски и др.). Ионы кальция участвуют в процессах свертывания крови, а также служат одним из универсальных вторичных посредников внутри клеток и регулируют самые разные внутриклеточные процессы — мышечное сокращение, экзоцитоз, в том числе секрецию гормонов и нейромедиаторов. Концентрация кальция в цитоплазме клеток человека составляет около 10−4 ммоль/л, в межклеточных жидкостях около 2,5 ммоль/л.
Потребность в кальции зависит от возраста. Для взрослых в возрасте 19—50 лет и детей 4—8 лет включительно дневная потребность (RDA) составляет 1000 мг, а для детей в возрасте от 9 до 18 лет включительно — 1300 мг в сутки . В подростковом возрасте потребление достаточного количества кальция очень важно из-за интенсивного роста скелета. Однако по данным исследований в США всего 11 % девочек и 31 % мальчиков в возрасте 12—19 лет достигают своих потребностей. В сбалансированной диете большая часть кальция (около 80 %) поступает в организм ребёнка с молочными продуктами. Оставшийся кальций приходится на зерновые (в том числе цельнозерновой хлеб и гречку), бобовые, апельсины, зелень, орехи. Всасывание кальция в кишечнике происходит двумя способами: через клетки кишечника (трансцеллюлярно) и межклеточно (парацелюллярно). Первый механизм опосредован действием активной формы витамина D (кальцитриола) и её кишечными рецепторами. Он играет большую роль при малом и умеренном потреблении кальция. При большем содержании кальция в диете основную роль начинает играть межклеточная абсорбция, которая связана с большим градиентом концентрации кальция. За счёт чрезклеточного механизма кальций всасывается в большей степени в двенадцатиперстной кишке (из-за наибольшей концентрации там рецепторов в кальцитриолу). За счёт межклеточного пассивного переноса абсорбция кальция наиболее активна во всех трёх отделах тонкого кишечника. Всасыванию кальция парацеллюлярно способствует лактоза (молочный сахар).
Усвоению кальция препятствуют некоторые животные жиры (включая жир коровьего молока и говяжий жир, но не сало) и пальмовое масло. Содержащиеся в таких жирах пальмитиновая и стеариновая жирные кислоты отщепляются при переваривании в кишечнике и в свободном виде прочно связывают кальций, образуя пальмитат кальция и стеарат кальция (нерастворимые мыла). В виде этого мыла со стулом теряется как кальций, так и жир. Этот механизм ответственен за снижение всасывания кальция, снижение минерализации костей и снижение косвенных показателей их прочности у младенцев при использовании детских смесей на основе пальмового масла (пальмового олеина). У таких детей образование кальциевых мыл в кишечнике ассоциируется с уплотнением стула, уменьшением его частоты, а также более частым срыгиванием и коликами.
Концентрация кальция в крови из-за её важности для большого числа жизненно важных процессов точно регулируется, и при правильном питании и достаточном потреблении обезжиренных молочных продуктов и витамина D дефицита не возникает. Длительный дефицит кальция и/или витамина D в диете приводит к увеличению риска остеопороза, а в младенчестве вызывает рахит.
Избыточные дозы кальция и витамина D могут вызвать гиперкальцемию. Максимальная безопасная доза для взрослых в возрасте от 19 до 50 лет включительно составляет 2500 мг в сутки (около 340 г сыра Эдам).
|
Периодическая система химических элементов Д. И. Менделеева |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
Электрохимический ряд активности металлов |
|---|
|
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu, |
кальций
- кальций
-
к’альций, -я
Русский орфографический словарь. / Российская академия наук. Ин-т рус. яз. им. В. В. Виноградова. — М.: «Азбуковник».
.
1999.
Синонимы:
Смотреть что такое «кальций» в других словарях:
-
КАЛЬЦИЙ — (Са) желтый блестящий и тягучий металл. Удельный вес 1,6. Словарь иностранных слов, вошедших в состав русского языка. Павленков Ф., 1907. КАЛЬЦИЙ (ново лат. calcium, от лат. calx известь). Серебристого цвета металл. Словарь иностранных слов,… … Словарь иностранных слов русского языка
-
КАЛЬЦИЙ — КАЛЬЦИЙ, Calcium, хим. элемент, симв. Са, блестящий, серебристо белого цвета металл с кристаллич. изломом, относящийся к группе щелочно земельных металлов. Уд. вес 1,53; ат. в. 40,07; точка плавления 808°. Са относится к числу весьма… … Большая медицинская энциклопедия
-
КАЛЬЦИЙ — (Calcium), Ca, химический элемент II группы периодической системы, атомный номер 20, атомная масса 40,08; относится к щелочно земельным металлам; tпл 842шC. Содержится в костной ткани позвоночных, раковинах моллюсков, яичной скорлупе. Кальций… … Современная энциклопедия
-
КАЛЬЦИЙ — металл серебристо белого цвета, вязкий, ковкий, на воздухе быстро окисляющийся. Темп pa плавления 800 810°. В природе встречается в виде различных солей, образующих залежи мела, известняка, мрамора, фосфоритов, апатитов, гипса и др. На жел. дор.… … Технический железнодорожный словарь
-
КАЛЬЦИЙ — (лат. Calcium) Ca, химический элемент II группы периодической системы, атомный номер 20, атомная масса 40,078, относится к щелочноземельным металлам. Название от латинского calx, родительный падеж calcis известь. Серебристо белый металл,… … Большой Энциклопедический словарь
-
КАЛЬЦИЙ — (символ Са), широко распространенный серебристо белый металл из группы ЩЕЛОЧНОЗЕМЕЛЬНЫХ, впервые выделен в 1808 г. Содержится во многих горных породах и минералах, особенно в известняке и гипсе, а также в костях. В организме способствует… … Научно-технический энциклопедический словарь
-
Кальций — Ca (от лат. Calx, род. падеж calcis известь *а. calcium; н. Kalzium; ф. calcium; и. calcio), хим. элемент II группы периодич. системы Mенделеева, ат.н. 20, ат. м. 40,08. Cостоит из шести стабильных изотопов: 40Ca (96,97%), 42Ca (0,64%),… … Геологическая энциклопедия
-
КАЛЬЦИЙ — КАЛЬЦИЙ, кальция, мн. нет, муж. (от лат. calx известь) (хим.). Химический элемент металл серебристо белого цвета, содержащийся в извести. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
-
КАЛЬЦИЙ — КАЛЬЦИЙ, я, муж. Химический элемент, мягкий серебристо белый металл. | прил. кальциевый, ая, ое. Кальциевые соли. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
-
КАЛЬЦИЙ — муж. металл, составляющий химическую основу извести. Кальцинировать что, пережигать металл, соль или камень. Кальцинация жен. действие это, пережиг, перекалка. Толковый словарь Даля. В.И. Даль. 1863 1866 … Толковый словарь Даля
-
КАЛЬЦИЙ — (Calcium), Ca, хим. элемент II группы периодич. системы элементов, ат. номер 20, ат. масса 40,08, относится к щелочноземельным металлам. ПриродныйК. состоит из смеси 6 стабильных изотопов с массовыми числами 40, 42 44, 46 и 48, среди к рых наиб.… … Физическая энциклопедия
100% гарантия натуральности каждого камня — доставка в любую точку мира
Этот химический элемент жизненно важен в буквальном смысле: из него состоят наши кости и зубы. Кальций – это также морские раковины, цветные мелки, сталактиты и сталагмиты в пещерах.
Содержание
- Что представляет собой
- История
- Физико-химические характеристики
- Присутствие в природе
- Технология получения
- Где используется
- Промышленность
- Наука
- Другие сферы
- Биологическое влияние
- Жизненные процессы
- Питание
- Нормы
- Симптомы нехватки/переизбытка
- Цены
Что представляет собой
Кальций – это химический элемент периодической системы Д. И. Менделеева под №20. Мягкий серебристо-белый металл блестит, но затем тускнеет под пленкой-оксидом.
Состоит из шести стабильных изотопов, при этом 97% состава приходится на Ca40.
Относится к щелочноземельным металлам.
Международное обозначение – Calcium (Ca).
История
Применение кальциевых минералов – мрамора, гипса, известняка – исчисляется тысячелетиями.
Чистый металл первым в истории получил британский химик Гемфри Дэви (1808 год). Для этого он применил электролиз к смеси из оксида ртути и мокрой гашеной извести. Получив амальгаму, отделил ртуть.
Он же предложил латинское название элемента: calcis означает мягкий камень, известка.
-50%
Большой выбор украшений из натуральных камней и минералов со скидкой -50%
Физико-химические характеристики
Кальций представлен двумя модификациями кубической решетки: с гране- и объемноцентрированной структурой.
Металл наделен многими достоинствами: пластичен, режется ножом, обрабатывается прессованием, прокаткой.
Химические свойства проявляются при нагревании:
- Взаимодействие с горячей водой приводит к образованию водородного «фонтана». Но реакция проходит без взрывов или горения.
- Взаимодействует с кислотами, неметаллами, образуя соединения.
- Даже при комнатной температуре во влажном микроклимате покрывается пленкой.
Нагреваясь в кислороде либо на воздухе, кальций, его растворимые соли горят. Пламя получается красно-оранжевым. По цвету его легко отличить от других металлов.
Химическая активность вещества зашкаливает. Для устранения этого недостатка металл хранят в керосине, растопленном парафине либо закупоренном сосуде.
| Свойства атома | |
|---|---|
| Название, символ, номер | Ка́льций/Calcium (Ca), 20 |
| Атомная масса (молярная масса) |
40,078(4) а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 4s2 |
| Радиус атома | 197 пм |
| Химические свойства | |
| Ковалентный радиус | 174 пм |
| Радиус иона | (+2e) 99 пм |
| Электроотрицательность | 1,00 (шкала Полинга) |
| Электродный потенциал | −2,76 В |
| Степени окисления | 2 |
| Энергия ионизации (первый электрон) |
589,4 (6,11) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 1,55 г/см³ |
| Температура плавления | 1112 К; 838,85 °C |
| Температура кипения | 1757 К; 1483,85 °C |
| Уд. теплота плавления | 9,20 кДж/моль |
| Уд. теплота испарения | 153,6 кДж/моль |
| Молярная теплоёмкость | 25,9 Дж/(K·моль) |
| Молярный объём | 29,9 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая гранецентрированная |
| Параметры решётки | 5,580 Å |
| Температура Дебая | 230 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) (201) Вт/(м·К) |
| Номер CAS | 7440-70-2 |
Уникальные свойства кальция как металла проявляются при усилении давления.
Под давлением он ведет себя как полупроводник, затем как металл, потом подобно сверхпроводнику. По проводимости в разы превосходит все химические элементы (например, ртуть – вшестеро).
Присутствие в природе
Кальций – третий по распространенности в земной коре среди металлов, пятый среди всех элементов. Четвертый по количеству минералов (385).
Однако высокая химическая активность исключает присутствие элемента в свободном виде:
- Это компонент минералов и соединений. Самые распространенные минералы – гипс, кальцит, алебастр, флюорит, апатит, доломит.
Апатит - Из кальцита состоит известняк. Метаморфизм превращает его в мрамор. Самая известная разновидность известняка – мел.
Горная порода кальцит
Вещество с формулой СаСО3 – обычный мел.
- Щелочноземельный металл обнаружен в каменных метеоритах – как почти ненаходимые на земле сульфиды.
Тонна земной коры содержит 32,7 кг кальция, литр морской воды – 410 мг.
Из морской воды кальций как строительный материал вытаскивают моллюски, кораллы.
Концентрацией кальция в составе определяется степень жесткости воды.
Технология получения
Конечный продукт промышленного производства – металлический кальций.
Получение металла проходит двумя методами:
Более 8000 видов товара из 500 разновидностей натурального камня. Ежедневное обновление!
- Электролиз. Расплавляют CaCl2, задействуя медно-кальциевый анод. Из полученного медно-кальциевого сплава (2:1) отгоняют металл.
- Алюминотермия. Прокаливается смесь CaO и порошковый алюминий. Конденсат из кальциевых паров аккумулируется на охлаждаемой поверхности.
Для обоих способов получения металла требуется вакуум и 960-1900°С.
Единственный производитель кальция в Европе – Чепецкий механический завод. Его открыли в 1949 году для нужд отечественной урановой промышленности. Уже тогда СССР отработал процесс восстановления урана кальцием. Сегодняшний ассортимент шире.
Где используется
Утилитарные характеристики металла обусловили сферы применения.
Промышленность
Львиная доля продукции металлургических комбинатов достается промышленному комплексу.
Здесь миссия кальция многогранна:
- Восстановление редкоземельных, тугоплавких элементов из соединений. Речь о хроме, никеле, меди, тории, уране.
- Удаление серы из бензина, керосина, других нефтепродуктов.
- Раскисление стали и сплавов цветных металлов.
- Получение антифрикционных сплавов.
- Очистка электровакуумных приборов от воздуха, других газов.
- Обезвоживание органических растворителей.
Металл используется при производстве аккумуляторных батарей, подшипников, оболочек кабелей.
Наука
Изотоп Ca-48 – материал с высоким КПД для производства сверхтяжелых элементов.
Кальцием восстанавливают уран.
С его помощью ученые пополняют таблицу Менделеева.
Другие сферы
Кальциевые материалы нашли применение на бытовом уровне:
- Строительный материал (известняк, гипс, мрамор).
- Сырье при производстве гипса, включая медицинский.
- Дезинфектор (хлорка).
- Мелки для рисования.
- Аптечные препараты, БАДы (особенно с витамином D).
Эстетично выглядящие образцы (флюорит, кальцинит, мрамор) попадают в минералогические коллекции.
Биологическое влияние
Кальций – важный для биологических организмов макроэлемент (1,6-2,1% по массе): он есть в растениях, организме животных, человека.
Жизненные процессы
Макроэлемент аккумулируется костями и зубами.
Известь (карбонат кальция) – строительный материал ракушек, кораллов, яичной скорлупы, накипи в чайнике.
Вещество задействовано в следующих процессах:
- Свертывание крови.
- Сокращение мышц.
- Секреция гормонов.
Тело человека массой 60 кг содержит полтора килограмма кальция.
Достаточное количество металла критично для детей и подростков: их скелет растет каждую минуту. У младенцев может проявиться рахитичность.
Питание
Макроэлемент поступает в организм во время еды. В детском возрасте продукт номер один – молоко.
Рацион взрослых разнообразнее. Веществом насыщены продукты всех групп:
- Цельнозерновой хлеб, гречка.
- Морепродукты, рыба (особенно мягкие кости).
- Бобовые.
- Орехи, свежий кунжут.
- Листовой салат, укроп, петрушка, спаржа.
Всасыванию кальция содействует лактоза, препятствуют кофе, углеводы, пальмовое масло, животные жиры (кроме сала).
Нормы
Суточная потребность в макроэлементе определяется возрастом (г):
| Возраст (лет) | Количество кальция (мг) |
| 0-6 | 1490 |
| 7-9 | 750 |
| 10-12 (мальчики) | 910 |
| 10-12 (девочки) | 1250 |
| 13-19 | 1250 |
| 20-49 | 1050 |
| 49+ | 1150-1350 |
Беременным и кормящим матерям требуется повышенная норма вещества.
Симптомы нехватки/переизбытка
Дефицит металла в организме проявляется многопланово:
- судороги, онемение конечностей, суставная боль;
- тахикардия;
- гипертония;
- расслоение, ломкость ногтей.
На ментальном плане это депрессия, нервозность.
Хроническая нехватка макроэлемента ведет к хрупкости костей (остеопорозу).
Об избытке макроэлемента сигнализируют отвращение к еде, неутолимая жажда, расстройство ЖКТ (тошнота, рвота), повышенное мочеотделение, слабость.
Избыток вещества опасен: организм «цементируется».
Максимальная суточная доза кальция для взрослых – 2,5 г.
Цены
На российском рынке представлена промышленная и аптечная продукция.
Цены на промышленный кальций (руб. / кг):
- металлический – 450;
- кусковой (чистота: 99,82%) – 1500;
- хлористый технический – 47;
- хлористый пищевой – 95.
Аптечный сегмент представлен отечественной и зарубежной продукцией. Упаковка глюконата кальция (10 таблеток) российского производства стоит 15-25 руб., препарата «Кальций-Д3 Никомед» – 300 — 700 руб.
100% гарантия натуральности каждого камня — доставка в любую точку мира
Химический элемент кальций находится в главной подгруппе второй группы четвёртого периода таблицы Менделеева, обозначается символом Ca (лат. Calcium).
Кальций один из самых важных элементов в питании человека. Без него работа многих органов и систем может быть либо частично парализована, либо полностью прекращена. Он участвует в регулировке мышечных сокращений, в передаче нервных импульсов, а также регулирует работу кровеносной системы.
Человеческий организм не способен самостоятельно продуцировать кальций для своих потребностей. Поэтому ежедневно этот химический элемент должен поступать с пищей. Суточная норма кальция у взрослого человека составляет 1000 mg. Для тех кому больше 50 лет норма должна быть уже 1200 mg в сутки. Беременным и кормящим женщинам кальция необходимо значительно больше – до 2000 mg.
Продукты, богатые кальцием
Молочные продукты занимают лидирующие места по содержанию кальция. Самым богатым на этот элемент считается молоко и творог. Йогурты и закваски также богаты кальцием. Различные сорта сыров, особенно твердые, богаты кальцием. В плавленных сырках его меньше.
В рыбных консервах содержатся перемолотые кости, а они хорошие источники кальция, который легко усваивается организмом человека. Разваренные кости рекомендуется кушать вместе с рыбой. Большое содержание кальция в консервах сардин – 500 mg на 100 g продукта. Следующими идут консервы из лосося и скумбрии – 210 и 240 mg.
Многие недооценивают значение зелени в питании, а ведь она тоже содержит кальций, причем иногда его содержание может составить конкуренцию даже молочным продуктам. В петрушке содержится 245 mg кальция, в листовой капусте – 210 mg. И даже листья одуванчика содержат кальций – 103 mg на 100 g зеленых листьев.
Кальций присутствует даже во фруктах. Небольшие его количества есть в бананах, яблоках, мандаринах и грейпфрутах (в среднем 10 mg на 100 g).
Различные виды орехов – бразильский орех и миндаль, также богаты кальцием (по 158 и 273 mg на 100 g). Кунжут содержит 1000 mg кальция на 100 g, а в маке – 1500 mg.
Есть кальций в бобах – белой и красной фасоли, а также в бобах сои.
Кальций есть в большинстве пряных трав и специй. Например, в базилике, укропе, тимьяне, душице, корице, розмарине, гвоздике и чесноке.
Ряд экспериментов подтвердили версию ученых о том, что существует около 7 минералов, употребление которых позволяет значительно увеличить продолжительность человеческой жизни. Среди этой «великолепной семерки» – кальций. Его дефицит провоцирует возникновение около полутора сотни самых разных заболеваний, связанных с нарушениями в работе опорно-двигательной, сердечно-сосудистой, эндокринной, пищеварительной систем.
Откуда кальций в продуктах растительного и животного происхождения
Перемещается химический элемент из одного вещества в другое, из почвы в растения, как и многие другие целебные минералы, с помощью водной среды. Животные также являются очередным звеном в природной цепи питания. В неволе они едят древесный уголь, лижут склоны скалистых берегов рек. В фермерских животноводческих хозяйствах, зоопарках животные дополнительно к корму получают куски поваренной соли, золу.
Древние греки вымаливали у своих богов наводнения, чтобы воды Великого Нила насытили истощенные земли и сделали их вновь плодородными. А долгожители высокогорного Тибета, где нет полноводных рек, и редкостью является дождь или снег, используют ледниковую воду для пополнения организма минеральными солями. Современному человеку нужно знать куда больше, чтобы выжить в век высоких технологий и экологических проблем окружающей среды.
В каких веществах высоко содержание кальция:
- в молочных продуктах питания;
- в яичной скорлупе;
- в лекарственных препаратах.
По каждому пункту есть исключительные детали, знания которых поможет избежать ошибок в желании получить недостающий химический элемент.
Ошибка 1
Среди качественных молочных продуктов питания, взрослым организмом хуже всего усваивается молоко. Оно является под запретом во многих оздоровительных программах питания, употребление же кисломолочных, напротив, рекомендуется.
Ошибка 2
В процессе приготовления порошка из яичной скорлупы домашних куриных яиц обязательно удаление тонкой малозаметной пленки и промывание их проточной водой.
Ошибка 3
В состав лекарственных препаратов, распространяющихся через аптечные сети, входят в большом количестве молочный сахар и лактоза, отчего значительно увеличивается доза их употребления, а металла кальция попадает в организм все меньше. Высоким показателем содержания и всасывания в кровь характеризуются коллоидные минералы.
В природе коллоидные минералы образуют растения-труженики, но подкармливают их фермеры самыми необходимыми металлами, от которых зависит урожайность: калием, фосфором, натрием. Кальций растения, как и люди, недополучают. Только выращивая овощи и зелень на личном приусадебном участке можно проследить за внесением добавок, содержащих бесценный кальций, и получить полноценные продукты питания.
По подсчетам ученых медиков, в человеке более 1% кальция, участвующего в жизнедеятельности организма, его количество постоянно должно пополняться. Лишая себя целебного минерала, он ежедневно укорачивает свою жизнь на несколько минут. Ведь прекрасная цель – дожить до ста лет! А систематически употребляя кальций, можно жить долго и качественно.
|
Кальций |
|
|---|---|
| Атомный номер |
20 |
| Внешний вид простого вещества |
|
| Свойства атома | |
|
Атомная масса (молярная масса) |
40,078 а. е. м. (г/моль) |
| Радиус атома |
197 пм |
|
Энергия ионизации (первый электрон) |
589,4 (6,11) кДж/моль (эВ) |
| Электронная конфигурация |
[Ar] 4s2 |
| Химические свойства | |
| Ковалентный радиус |
174 пм |
| Радиус иона |
(+2e) 99 пм |
|
Электроотрицательность (по Полингу) |
1,00 |
| Электродный потенциал |
−2,76 В |
| Степени окисления |
2 |
| Термодинамические свойства простого вещества | |
| Плотность |
1,55 г/см³ |
| Молярная теплоёмкость |
25,9[1] Дж/(K·моль) |
| Теплопроводность |
(201) Вт/(м·K) |
| Температура плавления |
1112 K |
| Теплота плавления |
9,20 кДж/моль |
| Температура кипения |
1757 K |
| Теплота испарения |
153,6 кДж/моль |
| Молярный объём |
29,9 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки |
кубическая гранецентрированная |
| Параметры решётки |
5,580 Å |
| Отношение c/a | — |
| Температура Дебая |
230 K |
| Ca | 20 |
| 40,078 | |
| [Ar]4s2 | |
| Кальций |
Ка́льций —элемент главной подгруппы второй группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 20. Обозначается символом Ca (лат. Calcium). Простое вещество кальций (CAS-номер: 7440-70-2) — мягкий, химически активный щёлочноземельный металл серебристо-белого цвета.
История и происхождение названия
Схема атома кальция
Название элемента происходит от лат. calx (в родительном падеже calcis) — «известь», «мягкий камень». Оно было предложено английским химиком Хэмфри Дэви, в 1808 г. выделившим металлический кальций электролитическим методом. Дэви подверг электролизу смесь влажной гашёной извести с оксидом ртути HgO на платиновой пластине, которая являлась анодом. Катодом служила платиновая проволока, погруженная в жидкую ртуть. В результате электролиза получалась амальгама кальция. Отогнав из неё ртуть, Дэви получил металл, названный кальцием. Соединения кальция — известняк, мрамор, гипс (а также известь — продукт обжига известняка) применялись в строительном деле уже несколько тысячелетий назад. Вплоть до конца XVIII века химики считали известь простым телом. В 1789 году А. Лавуазье предположил, что известь, магнезия, барит, глинозём и кремнезём — вещества сложные.
Нахождение в природе
Из-за высокой химической активности кальций в свободном виде в природе не встречается.
На долю кальция приходится 3,38 % массы земной коры (5-е место по распространенности после кислорода, кремния, алюминия и железа).
Изотопы
Кальций встречается в природе в виде смеси шести изотопов: 40Ca, 42Ca, 43Ca, 44Ca, 46Ca и 48Ca, среди которых наиболее распространённый — 40Ca — составляет 96,97 %.
Из шести природных изотопов кальция пять стабильны. Шестой изотоп 48Ca, самый тяжелый из шести и весьма редкий (его изотопная распространённость равна всего 0,187 %), как было недавно обнаружено, испытывает двойной бета-распад с периодом полураспада 5,3×1019 лет.
В горных породах и минералах
Большая часть кальция содержится в составе силикатов и алюмосиликатов различных горных пород (граниты, гнейсы и т. п.), особенно в полевом шпате — анортите Ca[Al2Si2O8].
В виде осадочных пород соединения кальция представлены мелом и известняками, состоящими в основном из минерала кальцита (CaCO3). Кристаллическая форма кальцита — мрамор — встречается в природе гораздо реже.
Довольно широко распространены такие минералы кальция, как кальцит CaCO3, ангидрит CaSO4, алебастр CaSO4·0.5H2O и гипс CaSO4·2H2O, флюорит CaF2, апатиты Ca5(PO4)3(F,Cl,OH), доломит MgCO3·CaCO3. Присутствием солей кальция и магния в природной воде определяется её жёсткость.
Кальций, энергично мигрирующий в земной коре и накапливающийся в различных геохимических системах, образует 385 минералов (четвёртое место по числу минералов).
Миграция в земной коре
В естественной миграции кальция существенную роль играет «карбонатное равновесие», связанное с обратимой реакцией взаимодействия карбоната кальция с водой и углекислым газом с образованием растворимого гидрокарбоната:
СаСО3 + H2O + CO2 ↔ Са (НСО3)2 ↔ Ca2+ + 2HCO3—
(равновесие смещается влево или вправо в зависимости от концентрации углекислого газа).
Огромную роль играет биогенная миграция.
В биосфере
Соединения кальция находятся практически во всех животных и растительных тканях (см. тж. ниже). Значительное количество кальция входит в состав живых организмов. Так, гидроксиапатит Ca5(PO4)3OH, или, в другой записи, 3Ca3(PO4)2·Са(OH)2 — основа костной ткани позвоночных, в том числе и человека; из карбоната кальция CaCO3 состоят раковины и панцири многих беспозвоночных, яичная скорлупа и др. В живых тканях человека и животных 1,4-2 % Са (по массовой доле); в теле человека массой 70 кг содержание кальция — около 1,7 кг (в основном в составе межклеточного вещества костной ткани).
Получение
Свободный металлический кальций получают электролизом расплава, состоящего из CaCl2 (75-80 %) и KCl или из CaCl2 и CaF2, а также алюминотермическим восстановлением CaO при 1170—1200 °C:
4CaO + 2Al = CaAl2O4 + 3Ca.
Свойства
Физические свойства
Металл кальций существует в двух аллотропных модификациях. До 443 °C устойчив α-Ca с кубической гранецентрированной решеткой (параметр а = 0,558 нм), выше устойчив β-Ca с кубической объемно-центрированной решеткой типа α-Fe (параметр a = 0,448 нм). Стандартная энтальпия ΔH0 перехода α → β составляет 0,93 кДж/моль.
Химические свойства
Кальций — типичный щелочноземельный металл. Химическая активность кальция высока, но ниже, чем всех других щелочноземельных металлов. Он легко взаимодействует с кислородом, углекислым газом и влагой воздуха, из-за чего поверхность металлического кальция обычно тускло серая, поэтому в лаборатории кальций обычно хранят, как и другие щелочноземельные металлы, в плотно закрытой банке под слоем керосина или жидкого парафина.
В ряду стандартных потенциалов кальций расположен слева от водорода. Стандартный электродный потенциал пары Ca2+/Ca0 −2,84 В, так что кальций активно реагирует с водой, но без воспламенения:
Ca + 2Н2О = Ca(ОН)2 + Н2↑ + Q.
С активными неметаллами (кислородом, хлором, бромом) кальций реагирует при обычных условиях:
2Са + О2 = 2СаО, Са + Br2 = CaBr2.
При нагревании на воздухе или в кислороде кальций воспламеняется. С менее активными неметаллами (водородом, бором, углеродом, кремнием, азотом, фосфором и другими) кальций вступает во взаимодействие при нагревании, например:
Са + Н2 = СаН2, Ca + 6B = CaB6,
3Ca + N2 = Ca3N2, Са + 2С = СаС2,
3Са + 2Р = Са3Р2 (фосфид кальция), известны также фосфиды кальция составов СаР и СаР5;
2Ca + Si = Ca2Si (силицид кальция), известны также силициды кальция составов CaSi, Ca3Si4 и CaSi2.
Протекание указанных выше реакций, как правило, сопровождается выделением большого количества теплоты (то есть эти реакции — экзотермические). Во всех соединениях с неметаллами степень окисления кальция +2. Большинство из соединений кальция с неметаллами легко разлагается водой, например:
СаН2 + 2Н2О = Са(ОН)2 + 2Н2↑,
Ca3N2 + 3Н2О = 3Са(ОН)2 + 2NH3↑.
Ион Ca2+ бесцветен. При внесении в пламя растворимых солей кальция пламя окрашивается в кирпично-красный цвет.
Такие соли кальция, как хлорид CaCl2, бромид CaBr2, иодид CaI2 и нитрат Ca(NO3)2, хорошо растворимы в воде. Нерастворимы в воде фторид CaF2, карбонат CaCO3, сульфат CaSO4, ортофосфат Ca3(PO4)2, оксалат СаС2О4 и некоторые другие.
Важное значение имеет то обстоятельство, что, в отличие от карбоната кальция СаСО3, кислый карбонат кальция (гидрокарбонат) Са(НСО3)2 в воде растворим. В природе это приводит к следующим процессам. Когда холодная дождевая или речная вода, насыщенная углекислым газом, проникает под землю и попадает на известняки, то наблюдается их растворение:
СаСО3 + СО2 + Н2О = Са(НСО3)2.
В тех же местах, где вода, насыщенная гидрокарбонатом кальция, выходит на поверхность земли и нагревается солнечными лучами, протекает обратная реакция:
Са(НСО3)2 = СаСО3 + СО2↑ + Н2О.
Так в природе происходит перенос больших масс веществ. В результате под землей могут образоваться огромные провалы, а в пещерах образуются красивые каменные «сосульки» — сталактиты и сталагмиты.
Наличие в воде растворенного гидрокарбоната кальция во многом определяет временную жёсткость воды. Временной её называют потому, что при кипячении воды гидрокарбонат разлагается, и в осадок выпадает СаСО3. Это явление приводит, например, к тому, что в чайнике со временем образуется накипь.
Применение
Применение металлического кальция
Главное применение металлического кальция — это использование его как восстановителя при получении металлов, особенно никеля, меди и нержавеющей стали. Кальций и его гидрид используются также для получения трудновосстанавливаемых металлов, таких, как хром, торий и уран. Сплавы кальция со свинцом находят применение в аккумуляторных батареях и подшипниковых сплавах. Кальциевые гранулы используются также для удаления следов воздуха из электровакуумных приборов.
Металлотермия
Чистый металлический кальций широко применяется в металлотермии при получении редких металлов.
Легирование сплавов
Чистый кальций применяется для легирования свинца, идущего на изготовление аккумуляторных пластин, необслуживаемых стартерных свинцово-кислотных аккумуляторов с малым саморазрядом. Также металлический кальций идет на производство качественных кальциевых баббитов БКА.
Ядерный синтез
Изотоп 48Ca — наиболее эффективный и употребительный материал для производства сверхтяжёлых элементов и открытия новых элементов таблицы Менделеева. Например, в случае использования ионов 48Ca для получения сверхтяжёлых элементов на ускорителях ядра этих элементов образуются в сотни и тысячи раз эффективней, чем при использовании других «снарядов» (ионов).
Применение соединений кальция
Гидрид кальция
Нагреванием кальция в атмосфере водорода получают CaH2 (гидрид кальция), используемый в металлургии (металлотермии) и при получении водорода в полевых условиях.
Оптические и лазерные материалы
Фторид кальция (флюорит) применяется в виде монокристаллов в оптике (астрономические объективы, линзы, призмы) и как лазерный материал. Вольфрамат кальция (шеелит) в виде монокристаллов применяется в лазерной технике, а также как сцинтиллятор.
Карбид кальция
Карбид кальция CaC2 широко применяется для получения ацетилена и для восстановления металлов, а также при получении цианамида кальция (нагреванием карбида кальция в азоте при 1200 °C, реакция идет экзотермически, проводится в цианамидных печах).
Химические источники тока
Кальций, а также его сплавы с алюминием и магнием используются в резервных тепловых электрических батареях в качестве анода(например кальций-хроматный элемент). Хромат кальция используется в таких батареях в качестве катода. Особенность таких батарей — чрезвычайно долгий срок хранения (десятилетия) в пригодном состоянии, возможность эксплуатации в любых условиях (космос, высокие давления), большая удельная энергия по весу и объёму. Недостаток в недолгом сроке действия. Такие батареи используются там, где необходимо на короткий срок создать колоссальную электрическую мощность (баллистические ракеты, некоторые космические аппараты и.др.).
Огнеупорные материалы
Оксид кальция, как в свободном виде, так и в составе керамических смесей, применяется в производстве огнеупорных материалов.
Лекарственные средства
Соединения кальция широко применяются в качестве антигистаминного средства.
Хлорид кальция
Глюконат кальция
Глицерофосфат кальция
Кроме того, соединения кальция вводят в состав препаратов для профилактики остеопороза, в витаминные комплексы для беременных и пожилых.-
Биологическая роль кальция
Кальций — распространенный макроэлемент в организме растений, животных и человека. В организме человека и других позвоночных большая его часть содержится в скелете и зубах в виде фосфатов. Из различных форм карбоната кальция (извести) состоят скелеты большинства групп беспозвоночных (губки, коралловые полипы, моллюски и др.). Ионы кальция участвуют в процессах свертывания крови, а также в обеспечении постоянного осмотического давления крови. Ионы кальция также служат одним из универсальных вторичных посредников и регулируют самые разные внутриклеточные процессы — мышечное сокращение, экзоцитоз, в том числе секрецию гормонов и нейромедиаторов и др. Концентрация кальция в цитоплазме клеток человека составляет около 10−7 моль, в межклеточных жидкостях около 10−3 моль.
Потребность в кальции зависит от возраста. Для взрослых необходимая дневная норма составляет от 800 до 1000 миллиграммов (мг), а для детей от 600 до 900 мг, что для детей очень важно из-за интенсивного роста скелета. Большая часть кальция, поступающего в организм человека с пищей, содержится в молочных продуктах, оставшийся кальций приходится на мясо, рыбу, и некоторые растительные продукты (особенно много содержат бобовые). Всасывание происходит как в толстом, так и тонком кишечнике и облегчается кислой средой, витамином Д и витамином С, лактозой, ненасыщеными жирными кислотами. Немаловажна роль магния в кальциевом обмене, при его недостатке кальций «вымывается» из костей и осаждается в почках (почечные камни) и мышцах.
Усваиванию кальция препятствуют аспирин, щавелевая кислота, производные эстрогенов. Соединияясь с щавелевой кислотой, кальций дает нерастворимые в воде соединения, которые являются компонентами камней в почках.
Содержания кальция в крови из-за большого количества связанных с ним процессов точно регулируется, и при правильном питании дефицита не возникает. Продолжительное отсутствие в рационе может вызвать судороги, боль в суставах, сонливость, дефекты роста, а также запоры. Более глубокий дефицит приводит к постоянным мышечным судорогам и остеопорозу. Злоупотребление кофе и алкоголем могут быть причинами дефицита кальция, так как часть его выводится с мочой.
Избыточные дозы кальция и витамина Д могут вызвать гиперкальцемию, после которой следует интенсивная кальцификация костей и тканей (в основном затрагивает мочевыделительную систему). Продолжительный переизбыток нарушает функционирование мышечных и нервных тканей, увеличивает свертываемость крови и уменьшает усвояемость цинка клетками костной ткани. Максимальная дневная безопасная доза составляет для взрослого от 1500 до 1800 миллиграмм.
Содержание кальция в продуктах питания:
Продукты Кальций, мг/100 г
Мак 1460
Кунжут 783
Крапива 713
Просвирник лесной 505
Подорожник большой 412
Галинсога 372
Сардины в масле 330
Будра плющевидная 289
Шиповник собачий 257
Миндаль 252
Подорожник ланцетолист. 248
Лесной орех 226
Амарант семя 214
Кресс-салат 214
Кале 212
Соя бобы сухие 201
Молоко коровье 120
Малое содержание кальция: рыба (30-90); творог (80); хлеб с отрубями (60); мясо, субпродукты, крупы, свекла (менее 50).
Рекомендуемые Всемирной Организацией Здравоохранения суточные нормы потребления кальция:
- Дети до 3 лет — 600 мг.
- Дети от 4 до 10 лет — 800 мг.
- Дети от 10 до 13 лет — 1000 мг.
- Подростки от 13 до 16 лет — 1200 мг.
- Молодежь от 16 и старше — 1000 мг.
- Взрослые от 25 до 50 лет — от 800 до 1200 мг.
- Беременные и кормящие грудью женщины — от 1500 до 2000 мг.
История кальция
Кальций был открыт в 1808 году Хэмфри Дэви, который путём электролиза гашеной извести и оксида ртути получил амальгаму кальция, в результате процесса выгонки ртути из которой и остался металл, получивший название кальций. На латыни известь звучит как calx, именно это название и было выбрано английским химиком для открытого вещества.
Общая характеристика кальция
Кальций является элементом главной подгруппы II группы IV периода периодической системы химических элементов Д.И. Менделеева, имеет атомный номер 20 и атомную массу 40,08. Принятое обозначение – Ca (от латинского – Calcium).
Физические и химические свойства
Кальций является химически активным мягким щелочным металлом серебристо-белого цвета. Из-за взаимодействия с кислородом и углекислым газом поверхность металла тускнеет, поэтому кальций нуждается в особом режиме хранения – в обязательном порядке плотно закрытая ёмкость, в которой металл заливают слоем жидкого парафина или керосина.
Суточная потребность в кальции
Кальций – наиболее известный из необходимых человеку микроэлементов, суточная потребность в нём составляет от 700 до 1500 мг для здорового взрослого человека, но она увеличивается во время беременности и лактации, это нужно учитывать и получать кальций в виде препаратов.
Нахождение в природе
Кальций имеет очень высокую химическую активность, поэтому в свободном (чистом) виде не встречается в природе. Тем не менее, является пятым по распространённости в земной коре, в виде соединений имеется в осадочных (известняк, мел) и горных породах (гранит), много кальция содержит полевой шпат анорит.
В живых организмах распространён достаточно широко, его наличие обнаружено в растениях, организмах животных и человека, где он присутствует, в основном, в составе зубов и костной ткани.
Продукты питания богатые кальцием
Источники кальция: молочные и кисломолочные продукты (основной источник кальция), брокколи, капуста, шпинат, листья репы, капуста цветная, спаржа. Кальций содержат также яичные желтки, бобы, чечевица, орехи, инжир (calorizator). Ещё хороший источник пищевого кальция – мягкие кости лосося и сардин, любые морепродукты. Чемпионом по содержанию кальция является кунжут, но только в свежем виде.
В организм кальций должен поступать в определенном соотношении с фосфором. Оптимальным соотношением этих элементов принято считать 1 : 1,5 (Са : Р). Поэтому правильно употреблять продукты питания, богатые этими минералами одновременно, например, говяжью печень и печень жирных сортов рыб, зелёный горошек, яблоки и редис.
Усвояемость кальция
Препятствием для нормального усвоения кальция из пищевых продуктов является употребление в пищу углеводов в виде сладостей и щелочей, которые нейтрализуют соляную кислоту желудка, необходимую для растворения кальция. Процесс усвоения кальция достаточно сложен, поэтому иногда недостаточно получать его только с пищей, необходим дополнительный приём микроэлемента.
Взаимодействие с другими
Для улучшения всасывания кальция в кишечнике необходим витамин D, который имеет свойство облегчать процесс усвоения кальция. При приёме кальция (в виде добавок) в процессе еды происходит блокировка всасывания железа, но приём препаратов кальция отдельно от пищи никак не влияет на этот процесс.
Полезные свойства кальция и его влияние на организм
Почти весь кальций организма (от 1 до 1,5 кг) находится в костях и зубах. Кальций участвует в процессах возбудимости нервной ткани, сократимости мышц, процессах свертываемости крови, входит в состав ядра и мембран клеток, клеточных и тканевых жидкостей, обладает антиаллергическим и противовоспалительным действием, предотвращает ацидоз, активирует ряд ферментов и гормонов. Кальций также участвует в регуляции проницаемости клеточных мембран, оказывает действие, противоположное натрию.
Признаки нехватки кальция
Признаками нехватки кальция в организме являются такие, на первый взгляд, не связанные между собой симптомы:
- нервозность, ухудшение настроения;
- учащённое сердцебиение;
- судороги, онемение конечностей;
- замедление роста и детей;
- повышенное артериальное давление;
- расслоение и ломкость ногтей;
- боль в суставах, понижение «болевого порога»;
- обильные менструации.
Причины нехватки кальция
Причинами нехватки кальция могут служить несбалансированные диеты (особенно голодания), низкое содержание кальция в пище, курение и увлечение кофе и кофеинсодержащими напитками, дисбактериоз, болезни почек, щитовидной железы, беременность, периоды лактации и менопаузы.
Признаки избытка кальция
Избыток кальция, который может возникнуть при чрезмерном употреблении молочных продуктов или неконтролируемом приёме препаратов, характеризуется сильной жаждой, тошнотой, рвотой, потерей аппетита, слабостью и усиленным мочеотделением.
Применение кальция в жизни
Кальций нашёл применение в металлотермическом получении урана, в виде природных соединений используется как сырьё для производства гипса и цемент, как средство дезинфекции (всем известная хлорка).
Автор: Виктория Н. (специально для Calorizator.ru)
Копирование данной статьи целиком или частично запрещено.
История открытия
Считается, что кальций был известен человеку еще с древних времён. В Древнем Риме, в Месопотамии и других цивилизациях Востока с использованием гашеной и негашеной извести возводили массивные и долговечные здания и сооружения. Но в чистом виде этот микроэлемент удалось получить лишь в XIX веке. Английский химик Гемфри Дэви в 1808 году проводил опыты и путём электролизации гашеной извести получил оксиды ртути, из которой выплавил новый металл, названный кальцием.
Ученый смог определить молярную формулу, вычислить уравнение и степень валентности этого микроэлемента.
В последующем человек научился получать чистый кальций путем использования различных технологий. Проведенные в последующем исследования показали, что этот микроэлемент содержится в большом количестве в земле, причём по мере приближения к ядру его массовая доля увеличивается. Он находится в различных горных породах, но в чистом виде в природе не встречается.
Нахождение в природе
Считается, что кальций — это один из самых распространённых элементов на Земле. Его общая доля составляет 3,38% всей массы коры. Однако из-за высокой активности его большая часть содержится в составе различных оксидов. Также он встречается в горных породах, в том числе в граните, различных силикатах и алюмосиликатах. В осадочных породах это соединение представлено в виде известняка, мела и различных минералов.
Природными источниками являются:
- доломит;
- флюорит;
- кальцит;
- гипс;
- алебастр;
- апатиты.
Также широко распространены в природе минералы кальция, в том числе ангидрид, известняк, доломит, апатиты и флюорит. Соли этого элемента содержатся в пресной или морской воде, определяя её показатели жесткости.
Экспериментальным путем установлено, что кальций входит в состав различных живых организмов, в том числе в костную ткань позвоночных видов, к которым относится человек. Из карбоната состоят жёсткие панцири и раковины различных беспозвоночных, скорлупа яиц птиц с пресмыкающимися.
Характеристики вещества
В естественных условиях кальций представляет собой металл с характерным серебристо-белым цветом. Он имеет высокую химическую активность, поэтому часто образует множество различных классов и всевозможных соединений с оксидами. Этот элемент представляет большую ценность для промышленного и технического химического синтеза, он необходим для правильной жизнедеятельности большинства живых видов на планете Земля. По своим физическим свойствам кальций относится к категории щелочноземельных, он отлично растворяется в воде, в особенности много этого соединения содержится в морской воде.
Его химические и физические характеристики зависят от особенностей схемы кристаллической решетки этого элемента. Строение атома кальция стандартно и отличается простотой. В зависимости от содержащихся в нем примесей, строение решетки этого микроэлемента может быть объемно-центрическим или кубическо-гранецентрическим. За счёт наличия металлического типа связи в молекуле обеспечивается максимально возможная прочность такого соединения.
Основные свойства:
- способность быстро окисляться на воздухе;
- образует многочисленные оксиды;
- применяется в восстановительных реакциях редкоземельных металлов.
Характеристики и химические свойства кальция могут изменяться в зависимости от наличия примесей и температуры окружающей среды. В обычных условиях этот металл имеет агрегатное твердое состояние. Его температура плавления составляет 842 градусов по Цельсию. Он является отличным тепло и электропроводником. Он реагирует на изменения показателей давления, которое модифицирует конфигурацию и положение его атомной решетки. При нагревании выше температуры плавления металл становится жидким, в последующем теряет свои свойства и переходит в парообразное состояние. Температура кипения составляет 1448 градусов.
Опытным путем установлена крайне интересная способность этого элемента. Под воздействием высокого давления это соединение теряет свою способность электропроводимости и другие характеристики кальция.
Однако в последующем после остывания все параметры восстанавливаются при этом отмечаются признаки сверхпроводника, которые в несколько раз превышают аналогичные показатели других элементов. Подобное делает кальций перспективным материалом при изготовлении микрочипов и изделий точной электроники.
Основные способы получения
Кальций обладает повышенной активностью, поэтому часто входит в различные соединения с другими элементами. Именно по этой причине длительное время не удавалось получить чистый материал без содержания различных примесей. Только лишь в начале XIX века англичанину Гемфри Дэви удалось путем электролиза синтезировать металл без содержания примесей. Ученый смог обнаружить взаимодействие электрического тока и расплавов солей с твердыми минералами.
Даже сегодня по прошествии стольких лет технология электролиза солей является наиболее востребованной, что объясняется её простотой и эффективностью. В металлургии применяется способ алюминотермии, который позволяет получить металл с чистотой порядка 98%. Развитие технологий и методов получения этого металла ограничено тем фактом, что такой процесс является ресурсоемким, требуя большого количества тепловой энергии и электрического тока огромной мощности.
Чистый металл хранят в герметичных емкостях с ограниченным доступом кислорода. Для предупреждения реакции с кислородом и водой кальций заливают слоем специальной жидкости (керосином или жидким парафином), что позволяет осуществлять транспортировку и длительное хранение этого металла, предупреждая его окисление и потерю химической чистоты.
На открытом воздухе кальций быстро начинает взаимодействовать с углекислым газом и кислородом, покрываясь характерным темным налетом.
Применение кальция
В чистом виде металл кальций применяют в качестве восстановителя при химических реакциях изготовления редкоземельных сплавов. Также этот элемент незаменим как раскислитель для бронзы, стали и других различных соединений. В химической промышленности он применяется при производстве бензина, позволяя удалять из топлива лишнюю серу. Из оксидов этого элемента изготавливают оболочки электрических кабелей, также из него выполняют антифрикционные материалы, которые незаменимы в радиоэлектронике и электронной промышленности.
Кальций — это биогенный элемент, необходимый для правильного протекания всех жизненных процессов в организме человека. Он присутствует в жидкостях и тканях растений и животных, поэтому играет важнейшую роль в правильной регенерации клеток. Польза и значение этого элемента для организма была установлена в начале прошлого века, а сегодня выводы ученых подтверждены многочисленными исследованиями. У человека содержание кальция достигает 2%, а у некоторых микроорганизмов — до 38%. Ученым известно лишь несколько видов простейших животных, жизнедеятельность которых может происходить без этого микроэлемента.
Большинство растений насыщаются кальцием из почвы, потребляя чистые микроэлементы с помощью специальных окислителей, выделяемых их клетками. Животные, в том числе человек, получают этот минерал с водой и пищей. Кальций необходим для образования клеточных мембран, также этот микроэлемент требуется для правильного обмена веществ. Его нехватка в организме приводит к развитию различных опасных заболеваний, вплоть до смерти человека.
Отдельные виды беспозвоночных научились запасаться кальцием, который необходим им для построения нового скелета и защитного панциря. К сожалению, у высших животных такой способности нет, поэтому им требуется постоянно получать этот микроэлемент извне, в том числе употребляя в пищу различные овощи и фрукты. Последние исследования показали, что обеспечить правильное всасывание кальция в организме человека можно лишь при наличии большого количества витамина D и других различных ферментов.